Употребление витаминов при лечении рака кажется максимально натуральным и безопасным — мы же получаем эти вещества с едой, значит, большие их дозы навредить не могут, а только укрепят организм.
- Полезны ли витамины в лечении рака?
- Витамин А и рак легкого
- Витамин С и колоректальный рак
- Витамин E
- Витамин D
- Витамин H
- Цинк
- Витамины группы В
- Витамин K
- Тревожные новости
На самом деле люди устроены гораздо сложнее и «больше» в данном случае не значит «лучше». Да и сами витамины не так просты: в организме они участвуют в разных биохимических процессах, и их действие на поведение опухолевых очагов не всегда однозначно.
Интеллектуальная собственность https://www.euroonco.ru
Полезны ли витамины в лечении рака?
И вслед за этим вопросом многие пациенты тут же задают следующий: «Какие лучшие витамины при онкологии?».
Несмотря на то что говорил в свое время химик Лайнус Полинг, а вслед за ним и сторонники ортомолекулярной медицины, нет никаких доказательств того, что витамины могут лечить рак. В некоторых случаях есть лишь данные скромных исследований о пользе витаминов совместно с химиотерапией. Но гораздо больше информации о вреде от приема таких пищевых добавок онкологическими больными. Поэтому в первую очередь пациентам стоило бы задавать врачам другой вопрос: какие витамины не принимать при онкологии?

Витамин А и рак легкого
Ретиноиды (формы витамина A или связанные с ним вещества) не имеют доказательств эффективности при лечении онкологических заболеваний у людей, кроме одного случая — промиелоцитарного лейкоза. Это заболевание обычно лечится с помощью химиотерапии и ретиноевой кислоты (природного метаболита витамина A). Что касается снижения риска развития рака благодаря ретиноидам, то бета-каротин, например, здесь плохой помощник. Если принимать его дополнительно, у курильщиков несколько повышается риск развития рака легкого.
В то же время, одно исследование, проведенное в 2015 году, показало, что витамин A может помочь витамину D в профилактике рака легких у курильщиков.
В целом результаты исследований, посвященных влиянию приема витамина A и ретиноидов на риск развития рака, неоднозначны. В некоторых экспериментах (правда, они были проведены не на людях, а на клеточных линиях и животных) было показано, что эти вещества подавляют развитие рака кожи, молочной железы, полости рта, легких, печени, желудочно-кишечного тракта, предстательной железы и мочевого пузыря. В других исследованиях ученые обнаружили, что антиоксидантные пищевые добавки, включая бета-каротин, не оказывают защитного эффекта и даже могут повысить смертность среди онкологических больных. Кроме того, в высоких дозах витамин A и ретиноиды токсичны.

Витамин С и колоректальный рак
Витамин C очень популярен у сторонников ортомолекулярной медицины. Как и другие витамины, он не доказал свою эффективность при лечении рака, однако, по некоторым данным, может улучшать качество жизни онкологических больных. Внутривенное введение витамина C пациенткам с раком молочной железы и раком яичников улучшало их общее состояние на фоне химиотерапии или лучевой терапии. То же происходило в случаях, когда рак уже не поддавался лечению (в этой ситуации применялись высокие дозы витамина в таблетках).
А вот при лечении миелоидного лейкоза, рефрактерного колоректального рака с метастазами, меланомы с метастазами химиопрепараты в сочетании с витамином C давали серьезные побочные эффекты и ухудшали течение болезни. Также есть серьезные основания полагать, что витамин C в драже и таблетках может взаимодействовать с бортезомибом и снижать его эффективность. Кроме того, высокие дозы витамина C не следует применять людям с болезнями почек: это может привести к мочекаменной болезни или почечной недостаточности.
Вообще, впервые о витамине C как о веществе, способном уничтожать раковые клетки, начали говорить в 70-х годах прошлого столетия. И действительно, результаты первых исследований на эту тему оказались весьма обнадеживающими. Но проведенные впоследствии крупные рандомизированные исследования не показали пользы аскорбиновой кислоты для онкологических больных. В настоящее время нет ни одной серьезной крупной работы, которая бы это подтвердила.
Тем не менее, недавно у ученых вновь проснулся интерес к витамину C как к противоопухолевому средству. Во многом этому способствовала работа исследователей из Университета штата Айова (Iowa State University), опубликованная в начале 2017 года. Авторы указывают, что витамин может атаковать раковые клетки, только если он присутствует в крови в высокой концентрации, которой сложно достичь при его пероральном (то есть путем проглатывания) приеме. Если вводить аскорбиновую кислоту в обход кишечника — внутривенно, — то ее концентрация в крови будет в 100–500 раз выше. Витамин C расщепляется в организме с образованием перекиси водорода, которая повреждает ткани, ДНК. В опухолевых клетках низкая активность фермента каталазы, поэтому они не могут эффективно расщеплять перекись и страдают сильнее, чем нормальные.
Результаты этой работы нельзя воспринимать как призыв срочно принимать витамин C в убойных дозах или вводить его внутривенно. Повторимся: пока нет ни одного реального достоверного доказательства того, что это помогает в профилактике или лечении рака. К тому же, высокие дозы аскорбинки — 2000 мг в день и более — могут привести к таким побочным эффектам, как головные боли, диарея, изжога, тошнота. При длительном приеме у некоторых людей образуются камни в почках.
Витамин E
Подтверждений того, что витамин E помогает бороться с раком, нет. Что касается профилактики развития онкологических заболеваний, то и тут найдено мало пользы от этого вещества — скорее, больше вреда. В нескольких исследованиях было установлено, что прием витамина E в высоких дозах немного снижает риск развития колоректального рака, при этом достоверно повышаются шансы заболеть раком мочевого пузыря, желудка и простаты.
По данным исследований, антиоксиданты (витамины A, C, E, бета-каротин, селен) повышают смертность при некоторых онкологических заболеваниях. Лучевая терапия и параллельный приём витамина E и бета-каротина повышает смертность от рака головы и шеи. Врачи также считают, что антиоксиданты могут взаимодействовать с химиопрепаратами и ухудшать эффект лучевой терапии.
Витамин D
Это единственный витамин, который реально помогает предотвратить развитие некоторых злокачественных опухолей, и это подтверждается научными исследованиями.
Например, в 2018 году были опубликованы результаты исследования с участием 5000 женщин в возрасте 55 лет и старше. Ученые обнаружили, что у участниц с уровнем витамина D в крови 60 нг/мл и более риск развития рака молочной железы был на 80% ниже по сравнению с теми, у кого уровень витамина составил 20 нг/мл и менее. Более ранние работы подтверждают, что низкие уровни витамина D связаны с более высокими рисками развития злокачественных опухолей груди. Также была обнаружена связь между высоким содержанием витамина D в крови и более высокой выживаемостью среди женщин, у которых уже диагностировано онкологическое заболевание.
Но есть и небольшая ложка дегтя. В 2018 году исследователи из Национального онкологического института США (National Cancer Institute) провели исследование с участием 26 тысяч мужчин старше 50 лет и женщин старше 55 лет. Участников поделили на четыре группы: одним регулярно давали витамин D и плацебо, вторым — омега-3 ненасыщенные жирные кислоты, третьим — витамин и ненасыщенные кислоты, четвертым — два плацебо. После периода наблюдения оказалось, что в группах, получавших и не получавших витамин D, примерно одинаковое количество участников заболели раком и умерли от него. Ученые продолжают наблюдение, возможно, со временем разница всё-таки появится.
Известно, что низкие уровни витамина D в крови связаны с повышенным риском и других типов злокачественных опухолей, в частности, рака кишечника, мочевого пузыря.
В небольших исследованиях было установлено, что прием витамина D3 снижает скорость повышения простат-специфического антигена, являющегося признаком развития рака простаты. Однако несмотря на обнадеживающие данные в ранних исследованиях, в крупных не было замечено улучшения работы химиопрепаратов при лечении рака предстательной железы благодаря витамину D3.
Витамин H
У витамина H, или биотина, тоже есть один побочный эффект, который способен навредить онкологиче6ским больным. Исследования показывают, что биотин при онкологии влияет на результаты лабораторных анализов, которые проводятся при раке простаты, молочной железы, щитовидной железы. Таким образом, врач может получить неверные данные и допустить ошибки в диагностике.
Цинк
Еще пациенты нередко спрашивают: можно ли цинк при онкологии? Этот минерал важен для нормального функционирования клеток, передачи нервных импульсов, защиты организма от инфекций. Есть некоторые данные, что прием цинка помогает справиться с некоторыми побочными эффектами лучевой терапии у онкологических пациентов: сохранить ощущение вкуса, уменьшить язвы во рту, воспалительный процесс. Но эта польза неоднозначна. Чтобы ее подтвердить, нужны дополнительные исследования.
Витамины группы В
Теперь поговорим о том, можно ли принимать витамины группы B при онкологии.
Прием витаминов группы B практически не влияет на риск развития рака – об этом, в частности, говорят результаты метаанализа, опубликованные в августе 2016 года. В анализ были включены рандомизированные контролируемые исследования с участием 74 498 пациентов. Ученые обнаружили, что прием биологически активных добавок с витаминами группы B не повлиял ни на заболеваемость раком, ни на показатели смертности от онкологических заболеваний. Единственный эффект, который был обнаружен: прием витаминов группы B снижает риск развития меланомы кожи.
Исследования по отдельным витаминам из этой группы дают противоречивые результаты. Например, считается, что на состояние онкологических больных и течение заболевания негативно влияет дефицит витамина B12 (цианкобаламина), так как он участвует в кроветворении. В то же время, есть научные данные, которые подтверждают, что дополнительный прием витаминов B6 и B12 повышает риск развития рака легкого у мужчин, особенно у курильщиков. А одно исследование, опубликованное в 2012 году, показало, что дефицит витамина B6 повышает риск развития онкопатологий, в то время как высокое его содержание в рационе, напротив, обладает защитным эффектом.
Прием фолиевой кислоты (витамина B9) для лечения рака — тоже пока дело рискованное, так как есть крайне противоречивые данные о пользе этого вещества. Основные исследования были проведены не на людях. В одних было показано, что фолиевая кислота при онкологии помогает справиться с болезнью, в других — что она способствует росту опухоли. В любом случае высокие дозы фолиевой кислоты могут взаимодействовать с метотрексатом и другими подобными химиопрепаратами, поэтому лучше не принимать витамин B9 самовольно.
Витамин K
С витамином K дело обстоит примерно так же, как с фолиевой кислотой: он показал эффективность на клеточных культурах и животных в замедлении роста раковых клеток (особенно в случае рака печени). Однако исследования на людях не дали такого результата.
Тревожные новости
19 декабря 2019 года Журнале клинической онкологии (Journal of Clinical Oncology) были опубликованы результаты небольшого исследования. 1134 пациента с раком молочной железы на ранней стадии с высоким риском рецидива согласились заполнить анкеты, в которых указали, какие витамины и пищевые добавки они принимали во время лечения. В дальнейшем на ними наблюдали, регистрировали случаи рецидива и смерти.
Результаты оказались следующими:
- У пациентов, которые принимали антиоксиданты (в том числе витамины A, C и E) до и после курса химиотерапии, на 41% чаще происходили рецидивы, и они на 40% чаще погибали.
- Прием антиоксидантов только до или только после химиотерапии не влиял на результаты лечения.
- Можно ли при онкологии принимать витамин B12? Пациенты, принимавшие препараты витамина B12 до и вовремя лечения, на 83% чаще имели рецидив и вдвое чаще умирали.
- При приеме препаратов железа до и во время химиотерапии риск рецидива повышался на 91%.
- У людей, принимавших омега-3 жирные кислоты до и во время химиотерапии, рецидивы происходили на 67% чаще.
- При этом прием поливитаминов не влиял на результаты.
Однозначные выводы делать рано, но эти данные заставляют задуматься и требуют дальнейшего изучения вопроса.
Можно ли пить поливитамины при онкологии? Конечно же, с осторожностью нужно относиться и к приему комплексных витаминных препаратов, например, Мильгамме при онкологии. Ведь в их состав входят все те же компоненты, о которых мы говорили выше, со всеми их возможными побочными эффектами.
Хотя витамины и нужны организму человека для нормальной работы, не стоит переоценивать их значение. Это не лекарства, и тем более не панацея. В противном случае они уже давно были бы включены в протоколы противоопухолевой терапии. Эффективно бороться с раком можно только с помощью специальных препаратов, назначенных онкологом. А если вы решили параллельно принимать витамины или другие пищевые добавки — предварительно нужно обязательно проконсультироваться с лечащим врачом, как минимум, поставить его в известность. Доктор расскажет, какие биологически активные препараты и витаминные комплексы можно принимать в конкретном случае, а какие витамины нельзя при онкологии.
| Подробнее о лечении в «Евроонко»: | |
| Консультация онколога в «Евроонко» | от 5 100 руб |
| Скорая помощь для онкологических больных | от 13 050 руб |
Список литературы:
- https://www.ncbi.nlm.nih.gov/
- https://www.ncbi.nlm.nih.gov/
- https://www.ncbi.nlm.nih.gov/
- https://www.cancercouncil.com.au/
- https://www.mayoclinic.org/
- https://www.sciencedaily.com/
- https://www.cancercouncil.com.au/
- https://www.webmd.com/
- https://www.medicalnewstoday.com/
- https://www.cancer.gov/
- https://www.medicalnewstoday.com/
- https://www.breastcancer.org/
- https://journals.lww.com/
- https://theconversation.com/
- https://pubmed.ncbi.nlm.nih.gov/
12.07.2015
Мнения учёных и специалистов
Режим питания и диеты против рака: мнения учёных и специалистов – витамин B17, сырые овощи и фрукты, гречка, зелёный чай и другое
Эта статья также посвящена профилактике и исцелению от тяжёлых заболеваний, в первую очередь – рака и сердечно-сосудистых заболеваний. Мы хотели бы вас коротко познакомить с несколькими интересными авторами, которые сами излечились и помогли в этом другим. Но, пожалуйста, обратите внимание, что мы всё же советуем совмещать лучшие достижения всех видов медицины и не отвергать современную медицину полностью. Первый автор – молодой учёный Давид Серван-Шрейбер, типичный западный человек (по своему менталитету), которому в 30 лет поставили диагноз – большая злокачественная опухоль головного мозга. Рак мозга на такой стадии считается неизлечимым. Но он вылечился и написал две книги: «Излечение» и «Антирак». Он провёл множество исследований и пришёл к выводам, которые могут помочь многим либо в излечении, либо в профилактике рака.
Прежде всего, он обратил внимание на то, что целые народы в 7, а иногда и в 60 раз меньше болеют раком (а сотни лет назад вообще не знали, что такое рак) и, даже заболев, меньше умирают от рака, чем жители западных стран. Наследственность влияет всего на 15%, остальное зависит от образа жизни. И если мы изменим питание, увеличим физическую нагрузку, максимально уменьшим контакт с химией, включая бытовую химию и парфюмерию, внимательней будем относиться к своей духовной жизни, то сможем свести к минимуму возможность заболевания страшными болезнями.
Он пишет, что у всех в организме присутствуют раковые клетки, из которых может развиться опухоль. И именно наш образ жизни питает рак или поддерживает механизмы защиты, препятствующие размножению раковых клеток. И последние научные разработки говорят о том, что болезнь возможно остановить, даже не разрушая раковые клетки, а просто помешать организму подпитывать рост опухоли, например, не давая ей создавать новые кровеносные сосуды. Выводы его исследований и его советы:
Опухоли питаются рафинированным сахаром.
До Второй мировой войны скот и куры питались травой, сегодня – соей и кукурузой. В траве есть кислоты типа омега-3, а в сое и кукурузе – типа омега-6. А баланс между омега-3 и омега-6 отвечает за контроль над воспалительными процессами в нашем организме. Так что, поедая мясо и искусственно выращенную рыбу, мы нарушаем этот баланс.
Очень важно добавлять в пищу, желательно ежедневно, куркуму. Эта специя является самым мощным противовоспалительным природным средством. Кстати, Аюрведа и многие восточные медицинские школы утверждают то же самое. Те, кто употребляют её в пищу, намного реже страдают от рака, болезни Альцгеймера, сердечно-сосудистых заболеваний.
Зелёный чай, по результатам его исследований, естественным путём выводит яды из нашего организма и повышает эффективность лучевой терапии, например, при раке мозга на 60-70%.
Исключить или сильно сократить в рационе питания продукты из белой муки, сахар, картофель, все хрустящие хлопья, картофельные и кукурузные.
Употреблять в пищу злаки, хлеб из муки грубого помола, тёмный рис, гречку, батат (сладкий картофель), молочные продукты натурального происхождения (не прошедшие промышленную обработку), масло оливковое и льняное, оливки, и очень важно пить чистую воду.
Витамин B17 – эффективный разрушитель раковых клеток
Книга второго автора, американского писателя-документалиста Эдуарда Гриффина «Мир без рака» посвящена истории одного открытия, главным героем которого является витамин B17 или лаэтрил, или амигдалин (содержится в семенах горького миндаля, в косточках абрикосов, персиков, слив, вишен и др. растений) – вещество, стремительно уничтожающее раковые клетки.
Автор приводит научные свидетельства того, что профилактика рака очень проста, и недоумевает, почему же ортодоксальная медицина объявила войну лекарству, с помощью которого многие клиники успешно вылечили своих пациентов? Автор находит ответ не в науке, а в политике в области рака – а она скрыта в экономической мотивации тех, кто доминирует в медицинском истеблишменте. Если ежегодно миллиарды долларов уходят на исследования в области рака, а другие миллиарды приходят от продаж химсоединений, то перед нами вырисовывается вполне понятная картина: от рака живут больше людей, чем от него умирают. И если решение может быть найдено в простом витамине, то в одночасье рушится гигантская индустрия, которая, само собой, этому всеми силами противится.
Фармацевтические компании проводят исследования только тех химсоединений, которые они изобретают; таким образом, если лекарство утверждено, у них появляются эксклюзивные права на его продажу. И они никогда не пойдут на то, чтобы провести исследования простой еды, которая не может быть ими запатентована и продаётся в любом супермаркете. Вещество, убивающее рак, было найдено в большинстве фруктовых косточек, в частности абрикосовых. Семя абрикоса было объявлено лекарством от всех известных видов рака 35 лет назад.
Учёные заявили, что, если эти семена входят в ежедневную диету человека, раковые клетки у него никогда не будут развиваться, так же как, например, человек никогда не заболеет цингой, если он съедает в день хотя бы один апельсин. Витамин B17 найден в семенах яблока, персика, вишни, винограда и абрикоса. Он обнаружен в некоторых бобовых и многих травах, а также в горьком миндале. Жёсткое ядро в глубине абрикоса находится там совсем не для того, чтобы его выбрасывать.
Он идентифицировал этот компонент как часть семейства нитрилоцидов, которые в изобилии встречаются в природе в более чем 1200 съедобных растениях. В особенно большом количестве этот компонент содержится в семенах плодов семейства Prunus Rosacea (горький миндаль, абрикос, терновник, вишня, персик и слива), но также он содержится в травах, кукурузе, сорго, просе, кассаве (тапиоке), семени льна, яблочных семенах и многих других пищевых продуктах, которые были удалены из диеты человека современной цивилизацией. Добавим: чтобы любой витамин усваивался, важно держать свой желудочно-кишечный тракт в чистом состоянии и воздерживаться от продуктов, которые нарушают обмен веществ и мешают усвоению – это мясо, белый хлеб, кофе, сахар, спиртное, пиво, генетически модифицированные продукты, различные химические добавки и курение.
Чудотворная гречка
Третий автор – доктор Вульф Ласкин, проработавший в онкологии более 30 лет. Есть множество документальных свидетельств о том, что те люди, которые следовали его советам, полностью излечились от самых сложных видов рака различной стадии. Его методика также была основана, в первую очередь, на изменении диеты. Кстати, эта диета очищает сосуды и предотвращает развитие атеросклероза, инфаркта и инсульта. Также в этой методике подробно раскрывается важность гена P53, флавоноида кварцетина в излечении от рака.
Доктор Ласкин много внимания уделял психологическому настрою пациента. Уже вначале он сформулировал для себя 5 пунктов правильного питания: включать в диету больше сырых продуктов, допускать минимум тепловой обработки пищи, исключить консервированные продукты, включать в рацион пищевые волокна, клетчатку и пить очищенную воду. Позже он пришёл к выводу, что нужно перейти на низкобелковую диету (не больше 35 грамм белка в день для человека весом 65 кг) и свести к минимуму потребление мяса и жирной пищи, жевать пищу 25-30 раз.
Прекратить ослаблять иммунную систему (которая призвана остановить распространение и избавиться от приносящих болезни клеток): стрессом; практически всеми химическими лекарствами, особенно антибиотиками и жаропонижающими; неправильным питанием; вредными привычками, прежде всего курением и алкоголем. Больше заниматься физической активностью и употреблять в пищу продукты, усиливающие иммунную систему и обладающие антиканцерогенным действием: красная морковь, зелёный лук, щавель, абрикосы, рябина, алоэ, шиповник и др.
Но особенно он призывал есть гречку и шиповник, которые содержат флавоноиды (кверцитин, генистеин, анегинин, лютеолин), которые обеспечивают подавление любых разновидностей онкологии на всех этапах развития опухоли за счёт восстановления комплекса, в котором находится ген P53. Он рекомендовал есть гречку на протяжении месяца, сочетая с другими продуктами, содержащими витамины, в первую очередь E и C, а также минералы. Кварцетин был открыт учёными только в конце XX века. Он есть также и в нерафинированном коричневом рисе (а не в рафинированном белом, который в основном продаётся в магазинах и является безполезным и даже вредным продуктом). Об этом писал также известный японский учёный Жорж Озава.
Важнейший практический совет
Известный американский иммунолог Уильям Полл ещё в 70-х годах прошлого века доказал, что пероксидаза хрена при натирании повышает фагоцитоз макрофага к антителам в 4 тысячи раз и уничтожает микробы, вызывающие не только хронические воспаления дыхательных путей, но и раковые клетки. То есть, если вы начнёте дышать 1-2 минуты натёртым хреном, то избавитесь от ОРЗ, гриппа, гайморита, ангины, тонзиллита, хронического воспаления лёгких. Введение клизмы из пероксидазы хрена: через 10-15 процедур на контрольном сканировании метастазы рака не фиксировались или купировались.
Три факта о профилактике рака в нескольких предложениях
1. В докладе Всемирного фонда исследований рака и Американского института по исследованию рака были проанализированы случаи заболевания 12-ю различными видами рака в Соединённых Штатах, Великобритании, Бразилии и Китае. Примерно треть этих заболеваний можно предотвратить благодаря здоровому питанию, физической активности и контролю над весом, считают специалисты. Эта цифра не включает в себя те преимущества, которые даёт в борьбе с раком прекращение курения. Только употребление табака приводит к трети всех случаев развития этой болезни.
2. Генетики заявляют, что им удалось полностью расшифровать генетический код двух самых распространённых онкологических заболеваний – рака кожи и лёгких. По словам представителей фонда Wellcome Trust, это открытие может совершить революцию в профилактике и лечении раковых заболеваний. Учёные обнаружили в ДНК клетки опухоли, развившейся из-за рака кожи – меланомы, более 30 тысяч ошибок генетического кода, причём практически все из них были вызваны чрезмерным воздействием солнечного излучения. (Старайтесь не бывать на открытом солнце с 11:00 до 17:00.) В ДНК рака лёгких генетики насчитали 23 тысячи ошибок, в подавляющем большинстве спровоцированных воздействием табачного дыма.
Из этого учёные сделали вывод, что у среднего курильщика на каждые 15 выкуренных сигарет приходится по одному нарушению генетического кода. При этом, по их словам, люди, бросающие курить, уменьшают вероятность заболеть раком лёгких, так как рано или поздно клетки, содержащие мутировавшие гены, будут заменены.
3. Алкоголь – одна из основных причин заметно участившихся случаев возникновения рака ротовой полости и горла среди сорокалетних мужчин и женщин, говорят учёные. Согласно статистике число случаев заболевания раком губ, языка, десен и горла среди людей возрастной группы от 40 до 50 лет возросло на четверть за последнее десятилетие. Ещё одной причиной заболевания раком такого рода медики считают недостаточное количество овощей и фруктов в рационе человека. «Люди даже не представляют, насколько тесная связь существует между алкоголем и онкологическими заболеваниями. Болезнь печени по-прежнему считается основным результатом злоупотребления алкоголем. Однако всё больше и больше людей начинают страдать онкологией из-за своего пристрастия» (Дон Шенкер).
Онкологические заболевания являются результатом прогресса, к такому выводу пришли исследователи из Манчестерского университета. Раковые опухоли крайне редко возникали во времена, когда природа и воздух ещё не были загрязнены, а сами люди питались правильно. По словам профессора Розали Дэвид, в природе нет ничего такого, что могло бы спровоцировать эпидемию онкологических заболеваний.
Дата публикации: 10.08.2023
Обновлено: 11.08.2023
Прием витаминов и рак
Руководитель Онкоцентра «СМ-Клиника», д.м.н., профессор А.П. Серяков
На приемах пациенты часто задают мне и другим нашим онкологам вопрос «Можно ли принимать витамины при онкологическом заболевании? Не спровоцируют они более активное развитие рака?»
Вообще, витамины – незаменимые соединения органического типа. Они необходимы человеку всегда, поскольку именно витамины дают силы — активируют работу иммунной системы, увеличивают общую выносливость организма, нормализуют обмен веществ. Очень важно, что витамины способствуют дополнительной защите организма от инфекций, которых в период лечения онкозаболевания, безусловно, нужно опасаться.
Я советую своим пациентам придерживаться сбалансированной диеты по белкам, жирам, углеводам, микроэлементам и, естественно, витаминам. Если у человека в целом сбалансированное, достаточное по количеству калорий и объему питание, то необходимости в дополнительном приеме таких активных веществ, как витамины, нет. Другое дело, если в результате лабораторной диагностики выявлен дефицит конкретных витаминов. В этом случае обсуждаемо назначение пациенту витаминов в суточных дозах.
Отдельно хочу остановиться на дефиците витамина D. Проведенное в США в период с 1991 по 2015 гг. среди более чем 94 тысяч женщин в возрасте от 25 до 42 лет исследование показало, что витамин D помогает снизить число случаев колоректального рака примерно на 50% [1]. Также в настоящее время проводится анализ собранных в течение нескольких лет данных, позволяющих предположить, что регулярный прием витаминов C и Е имеет похожий результат.
А вот исследование, выполненное сотрудниками университета Огайо, продемонстрировало, что витамины B6 и B12 могут способствовать развитию рака легкого. Однако таким образом они влияют не на всех – в группе риска оказываются преимущественно курящие мужчины [2]. И все же к приему витаминов B-группы пациентам с онкозаболеваниями следует относиться осторожно – предварительно необходимо посоветоваться с вашим лечащим врачом.
Источники:
- https://www.mdedge.com/hematology-oncology/article/247942/gastrointestinal-cancer/vitamin-d-status-may-play-pivotal-role
- https://theconversation.com/vitamin-b-supplements-linked-to-lung-cancer-heres-why-you-probably-dont-need-to-worry-82806
Вам была полезена эта публикация?2622Поставить оценку
Отзывы о клинике
Тщательность обследования:
Посоветуете ли Вы клинику:
08.03.2023
Я посетил онкологическую клинику, чтобы получить консультацию по поводу своего здоровья. Я был приятно удивлен профессиональным и доброжелательным отношением персонала. Врачи были очень внимательны к моим проблемам и дали мне полезные рекомендации. Клиника была чистой и ухоженной, а оборудование было современным и хорошо обслуживалось. Я чувствовал себя в безопасности и уверенности, что получаю лучшее возможное лечение. Я бы порекомендовал эту клинику всем, кто нуждается в качественном онкологическом лечении.
Вам был полезен этот комментарий? 67 60
Миронова Тома Эдуардовна
Тщательность обследования:
Посоветуете ли Вы клинику:
Вам был полезен этот комментарий? 68 60
Андрей
Тщательность обследования:
Посоветуете ли Вы клинику:
11.03.2020 15:52:00
Понравилось: лечение дало результат
Не понравилось: дорого, не всегда понимал назначения врача, много анализов
Узнал что у меня онкология еще в прошлом году. Стадия не запущенная и была вероятность выздоровления. Стал искать клинику для лечения, мне нужны были самые лучшие. СМ- клинику на Волгоградском проспекте мне порекомендовал знакомый доктор. Сказал что они профилируются на онкологических заболевания и специалисты там толковые, мол можно обращаться. По рекомендации обратился сюда. Пришлось пройти большое количество обследований для уточнения диагноза. Потом мне назначили комплексное лечение. Что у меня вызывало смущения, я не до конца понимал назначения врача. Когда спрашивал что это за лекарство и зачем мне сейчас его назначили, получал довольно уклончивый ответ, что с моим заболеванием это самые проверенные назначения и эти препараты обычно хорошо переносятся пациентами. Мне показалось что врач мне попался очень неразговорчивый и грубый. На обходе буквально несколько минут у меня был, я понимаю что загружены все, но всё же хотелось бы больше внимания. Сейчас я здоров, самое главное что болезнь удалось вылечить, лечение было результативным, сейчас чувствую себя нормально. Ремиссия, надеюсь так будет и дальше.
Вам был полезен этот комментарий? 68 56
Мухамед
Тщательность обследования:
Посоветуете ли Вы клинику:
27.02.2020
Прохожу сейчас тут лечение, у меня проблема с кожей на руке. Пока ничего плохого сказать не могу. Пройду до конца лечение и напишу сюда свое окончательное впечатление.
Вам был полезен этот комментарий? 45 54
Светлана
Тщательность обследования:
Посоветуете ли Вы клинику:
28.01.2020
После того, как я узнала, что у меня есть онкология жизнь немного приняла другую форму и поворот. Проходила лечение и обследование в различных клиниках. Мало где делали качественное обследование. Но вот решила обратиться за лечением в СМ- клинику. Здесь меня приняли без проблем после лечения и наблюдения в других клиниках, в то время когда различные онкологические центры отказывали в помощи. Здесь же пошли на встречу. Провели онкологический скрининг, экспресс и лабораторную диагностику, а так же взяли необходимые лабораторные анализы. В принципе, лечение проходило нормально. Не могу выделить прям особо запоминающихся моментов, все лечение было построено грамотно и нормально. Мне была оказана квалифицированная помощь врачей, специалисты они конечно отличные. Но я до этого была в других клиниках, там обслуживание и отношение к пациентам было лучше. Так сказать, мне есть с чем сравнивать. Еще отмечу цены, конечно здесь они выше, чем в те клиники, куда я обращалась до этого. Можно было бы немного и снизить, так сказать за не очень приветливую обстановку в самой клинике. В целом неплохая клиника, особенно спасибо врачам за квалифицированную помощь, оказанную в лечении онкологии.
Вам был полезен этот комментарий? 34 45
Видео-отзывы о клинике
Клиника
02.04.2020
Вам был полезен этот комментарий? 44 35
Публикации врача
08.08.2023
Механическая желтуха при раке
Термином «механическая желтуха» принято обозначать комплекс симптомов, который внешне проявляется ок…
08.08.2023
Эндоскопические методы диагностики в онкологии
Хорошо известно, что в случае с онкологическими заболеваниями крайне важно поставить диагноз как…
Витамины, как часть натурального природного окружения, стояли у истоков зарождения жизни. На это окружение ориентированы все системы гомеостаза, адаптационных механизмов и возрастного онтогенеза человека [3]. Витамины в химическом смысле – это органические, низкомолекулярные соединения, абсолютно необходимые для жизнедеятельности человека [4,6,36]. Они обладают ферментными и/или гормональными функциями, но не являются источником энергии, пластическим материалом. Они необходимы для всех аспектов жизнедеятельности организма, в том числе и для противоопухолевого иммунитета. Витамины играют важную роль в обмене ксенобиотиков, формировании антиоксидантной защиты организма, и в то же время в ряде случаев витамины либо не синтезируются, либо их синтез, образование активных форм в значительной мере подавлены (особенно у онкологических больных, при дисбиозе, после инфаркта миокарда, при заболеваниях печени и т.д.). Наконец, они могут просто поступать в организм с пищей в недостаточном количестве. Содержание витаминов в пищевых продуктах, как правило, не обеспечивает суточной потребности организма [6]. У ряда больных витамины могут не усваиваться (рак желудка, сокращение площади всасывания при удалении участка тонкого кишечника, дисбактериоз, старение эпителиоцитов, рвота и т.д.). В связи с этим возникает необходимость в дополнительном обеспечении организма витаминами.
Витамины, как часть натурального природного окружения, стояли у истоков зарождения жизни. На это окружение ориентированы все системы гомеостаза, адаптационных механизмов и возрастного онтогенеза человека [3]. Витамины в химическом смысле – это органические, низкомолекулярные соединения, абсолютно необходимые для жизнедеятельности человека [4,6,36]. Они обладают ферментными и/или гормональными функциями, но не являются источником энергии, пластическим материалом. Они необходимы для всех аспектов жизнедеятельности организма, в том числе и для противоопухолевого иммунитета. Витамины играют важную роль в обмене ксенобиотиков, формировании антиоксидантной защиты организма, и в то же время в ряде случаев витамины либо не синтезируются, либо их синтез, образование активных форм в значительной мере подавлены (особенно у онкологических больных, при дисбиозе, после инфаркта миокарда, при заболеваниях печени и т.д.). Наконец, они могут просто поступать в организм с пищей в недостаточном количестве. Содержание витаминов в пищевых продуктах, как правило, не обеспечивает суточной потребности организма [6]. У ряда больных витамины могут не усваиваться (рак желудка, сокращение площади всасывания при удалении участка тонкого кишечника, дисбактериоз, старение эпителиоцитов, рвота и т.д.). В связи с этим возникает необходимость в дополнительном обеспечении организма витаминами.
Витамины поступают с пищей, которая сама по себе может содержать множество потенциальных канцерогенов и мутагенов (микотоксины, нитрозосоединения, пиролизидиновые алкалоиды, гетероциклические амины, фурокумарины, хинолиновые и хиноксалиновые производные, отдельные ароматические углеводороды), быть не сбалансированной по составу жиров, белков, углеводов, витаминов, микроэлементов (МЭ) [1]. Мутагенами и канцерогенами при определенных условиях могут быть пищевые добавки: бромат калия, хлорид олова, сорбиновая кислота, тиобендазол, формальдегид, нитрит натрия, бисульфит натрия, бутилгидрокситолуол (Е321), бутилгидроксианизол (Е320), пищевой зеленый, метаниловый желтый, оранжевый II, флоксин, пунцовый SX, пиколинат хрома и др.; неорганические соединения: двухвалентные катионы металлов (Mo, Hg, Cu, Mn, Cr, Ni, Co и др.), неорганические соединения Co, Cd, Hg, As, Cr3+, Cr6+, различные соединения Ni, двухвалентные соли Pb; ацетат, оксид, сульфид и хлорид цинка; четырехвалентный ванадий, некоторые соединения Se, Mo, Be, Al, Pl, Sb, Cu, Mn, Sn и др.; противопаразитарные, антимикробные, антивирусные и др. лекарственные препараты [1–3,5,22,58]. Общим свойством большинства канцерогенов является их способность к метаболическому превращению в сильные электрофильные реагенты, активно взаимодействующие с нуклеофильными центрами генетического аппарата клетки [1]. Это является решающим в процессе повреждения клетки и ее трансформации, в том числе онкологической.
Интерес к теме «витамины и канцерогенез» возник в фокусе их потенциальной антиканцерогенности. В конце 80–х годов XX века были получены данные об антиканцерогенном действии совокупности всех витаминов в физиологических дозах, а также данные о преимуществах зеленолистной диеты (эффект фолатов, клетчатки, эпигаллокатехинов, эссенциальных элементов селена, кальция, магния и т.д.) для профилактики рака толстой кишки. Выражение «фолиевая противораковая диета» получило широкое распространение [24].
В развитых странах отмечается увеличение длительности жизни и, как следствие, рост опухолей в пожилом и старческом возрасте. В то же время именно у пожилых людей, имеющих максимальный процент эпизодов возникновения онкопатологии, прием витаминов, селена, других биодобавок вырос в десятки раз. Применение микронутриентов проходит период систематизиции и доказательного анализа. Большинство исследователей отмечают слабую антиканцерогенность или нейтралитет в отношении опухолевого роста, характерную для витаминов в физиологических дозах [19,26,35,48,49–57,59,69,77,90,91]. В отдельных исследованиях показана безопасность у онкологических больных приема и более высоких, нежели физиологические, доз витамина С [17,29,89], витамина В1 [60], его жирорастворимого деривата (бенфотиамина) [10], витамина В12 [13,71], никотинамида [39,80] и др. Еще больше всколыхнула общественное сознание конца ХХ века гипотеза дважды лауреата Нобелевской премии Лайнуса Полинга о противораковом действии фармакологических доз – гипердоз (выше физиологических доз в 3–10 раз) и мегадоз (выше физиологических более чем в 10–100 раз) витамина С [30]. Экспериментальные и клинические исследования по витаминам активизировались. Стал изучаться дозозависимый антионкологический порог, естественные или природные изоформы витаминов и синтетические дериваты. Оказалось, что онкозащитное действие физиологических доз витаминов начинает действовать еще внутриутробно: плацебо–контролируемое исследование [70] показало, что употребление беременными витаминных комплексов в течение двух триместров (6 месяцев) уменьшает риск возникновения опухолей мозга у новорожденных (отношение вероятности (OR) = 0,7; 95% доверительный интервал (CI)=0,5, 0,9) с тенденцией снижения риска при длительном употреблении витаминов (тенденция р=0,0007). Наибольшее снижение риска развития опухолей мозга в возрасте до 5 лет наблюдалось в группе детей, родившихся от матерей, принимавших витамины на протяжении всех трех триместров (т.е. 9 месяцев) (OR=0,5; CI=0,3, 0,8). Этот эффект не изменялся в зависимости от гистологии опухоли. Очень важными являются экспериментальные доказательства безопасности использования комплексов витаминов, включая витамины группы В, С, Е, D при кахексии при раке, отсутствие при этом активации метастазирования, улучшение общего состояния [66].
Сегодня онкологическая заболеваемость рассматривается как вариант патологического феноптоза. Перспектива здорового долголетия и профилактики рака показана научной программой «Геном человека». Пропорция значимости «онкологические полиморфизмы генома: онкогены внешней среды» составляет 6–8%:92–94%, т.е. гены, ответственные за развитие онкологии, являются теми мишенями, состояние которых меняют микронутриенты [2,3,5]. Несмотря на то, что со времени открытия первого витамина прошло много лет, вокруг витаминов кипят научные страсти. С одной стороны, витамины – это всего лишь незаменимые, эссенциальные микронутриенты, а с другой – мощные лекарственные средства (витамин С – лечение цинги, витамин В1 – лечение полинейропатии). В норме цианкобаламин и фолаты активируют нормальное деление и дифференцировку клеток. Опухолевые клетки недифференцированы или дифференцированы, делятся неуправляемо и сверхактивно. Как же быть с витаминами, особенно с дополнительным назначением витаминов онкологическим больным? Как быть с обеспечением витаминами стареющего населения, попадающего в полосу риска по злокачественным заболеваниям по возрасту?
Витамин С. Опухолевые клетки синтезируют значительное количество коллагеназ и стромелизина, а также активатора плазминогена, что способствует разрыхлению межклеточного матрикса, нарушению цитоархитектоники клеток и высвобождению их для метастазирования. Уникальная роль витамина С заключается в том, что витамин С принимает участие в синтезе коллагена и совместно с аминокислотой, лизин – в образовании коллагеновых мостиков в соединительной ткани. Это позволяет целенаправленно использовать витамин С в период реабилитации после оперативных вмешательств на опухолях, в методиках замедления метастазирования, стимуляции ранозаживления и преодоления астенизации [31]. Не менее интересны исследования по профилактике возникновения опухолей с использованием витамина С. В жизнедеятельности клеток и организма в процессе возникновения и развития злокачественной опухоли преобладают процессы окисления. Поддержание pH ресурса желудочного сока, крови – еще один вектор антиканцерогенного действия витамина С, биофлавоноидов и продуктов питания их концентрирующих [2,77]. В связи с этим активно развивается антиканцерогенная диетология, обеспечивающая поддержание pH желудочного сока, крови, мочи в диапазоне нормы. Профилактические возможности овощей и фруктов с повышенным содержанием витаминов С, Е, β–каротина в отношении злокачественной трансформации слизистой желудка исследованы Plummer M. с соавт. (2007) у 1980 чел., под контролем гистологических исследований слизистой. Пациенты 3 года получали один из витаминов или плацебо. Витамины–антиоксиданты не влияли на малигнизацию слизистой оболочки желудка [67]. В другом исследовании изучено значение обеспеченности различными витаминами при раковом поражении почки (767 больных, 1534 – контроль). Не получено достоверной связи обеспеченности для ретинола, a–каротина, β–каротина, β–криптоксантина, лютеин–зеаксантина, витамина D, витамина В6, фолата, никотиновой кислоты. Bosetti C. с соавт. (2007) отмечен «выгодный» эффект для больных с раком почки достаточной обеспеченности витаминами С и Е [19]. Сочетание аскорбиновой кислоты и трехокиси мышьяка с дексаметазоном эффективно у больных с множественной миеломой [90].
Низкая обеспеченность витамином С, недостаточное потребление фруктов и овощей, богатых аскорбиновой кислотой и аскорбатами, способствует инфицированию Helicobacter pylori; и то, и другое провоцирует рак желудка. Больным с атрофическим гастритом проводилась эрадикационная терапия амоксициллином и омепразолом в течение 2 недель по поводу наличия в желудке Helicobacter pylori. В дальнейшем в течение 7,3 лет они получали препараты витамина C, E, селена, экстракт чеснока, дистиллированное масло чеснока. Повторные эндоскопии с биопсией показали, что эрадикация Helicobacter pylori способствовала значительному улучшению состояния слизистой оболочки желудка, однако последующая длительная витаминотерапия и препараты чеснока не влияли на частоту развития у больных рака желудка [92]. Если при разбивке по видам рака и применения какого–либо одного витамина удается обнаружить достоверную разницу в плане защиты от опухолей, то при рассмотрении всех опухолей и приема всех витаминов в комплексах достоверных связей не обнаружено. Напротив, при анализе Bjalakovic G. et al. (2007) 385 публикаций, по данным 68 исследований, у 232606 участников в категории пожилых пациентов смертность от рака оказалась незначительно выше среди тех, кто длительно употреблял антиоксиданты (витамин Е, β–каротин, ретинол), а в 47 испытаниях у 180938 участников антиоксиданты показали несколько более высокую достоверность по увеличению смертности. При этом длительный профилактический прием селена и витамина С имеет слабую корреляцию со снижением смертности и риском опухолей [14]. Исследователи вовсе не склонны рассматривать эти данные, как «приговор антиоксидантам». Анализируемые больные – особая часть человеческой популяции. Они имели тяжелые хронические заболевания и низкий статус здоровья. Известно, что именно пожилые люди с хроническими заболеваниями в США, Европе, Китае значительно чаще употребляют биологически активные добавки с антиоксидантами, нежели здоровые. При этом, чем тяжелее состояние больного, тем чаще он прибегает к использованию витаминов. Таким образом, группа «сравнения» в данном анализе – более здоровые люди. Вот почему авторы ни в коей мере не склонны рассматривать прием витаминов и микроэлементов в качестве причины повышенной смертности. Очень важно для врача иметь возможность ознакомиться с такими важными итоговыми исследованиями в виде полнотекстовых статей, а не по резюме или лишь по названию статьи. Врач не может опираться в своих оценках витаминов и микроэлементов на информацию популярных изданий, некоторых сайтов в интернете, которые в погоне за броскими заголовками представляют важнейший материал в несколько видоизмененном виде. Доказательной медицине еще предстоит провести когортный анализ и сопоставить уровень состояния здоровья, смертности и приема витаминов в адекватных группах сравнения. Весь опыт витаминологии и биоэлементологии говорит в пользу взвешенного безопасного профилактического подхода.
Исследовались разные комбинации витаминов и минералов с целью снижения смертности от рака легкого среди 29584 здоровых китайцев (ретинол + цинк; рибофлавин + никотиновая кислота; аскорбиновая кислота + молибден; β–каротин+a–токоферол + Se). На протяжении испытательного срока (1986–1991) и через 10 лет (2001) были отмечены 147 смертных случая от рака легкого. Показано отсутствие различий в показателях смертности от рака легкого для любой из четырех видов витаминно–минеральных добавок [47]. Пятилетнее исследование о влиянии аскорбиновой кислоты (50 мг и 500 мг) на риск ринита проведено в Японии. Витамин С, независимо от дозы, существенно уменьшал частоту возникновения ринита и его появлений, но не оказывал никакого воздействия на продолжительность болезни [73].
Вопрос об онкологической безопасности высокодозированных лекарственных форм витаминов был поднят исследованиями по β–каротину [36,43,62]. В конце прошлого века был установлен так называемый «β–каротиновый парадокс»: физиологические дозы β–каротина оказывали защитный эффект при раке бронхов и легких у курильщиков, высокие дозы каротина приводили к возрастанию встречаемости заболевания [37]. Достаточно убедительно установлено, что физиологическое потребление β–каротина значительно снижает процент первичных опухолей головы, шеи, легких и пищевода [11,35], лейко– и эритроплакий, диспластических и метапластических изменений клеток [85]. Значительное снижение уровня ретинола, b–каротина и, особенно, ликопина обнаружено у детей, больных СПИДом, ассоциированным с угрозой злокачественного перерождения [81]. Многочисленными многоцентровыми плацебо–контролируемыми исследованиями показана роль каротина в подавлении экспрессии рецепторов к эпидермальному фактору роста (ЭФР), что приводит к индукции апоптоза в трансформированных под влиянием канцерогенеза клетках [36]. β–каротин защищает ДНК от повреждения и, кроме того, снижает экспрессию аномальной изоформы Р53 – цитомаркера рака. В эксперименте установлено, что β–каротин повышает экспрессию ключевого белка межклеточных контактов коннексина 43 (С43) мышиными фибробластами и предотвращает нарушение контактного торможения и малигнизацию эпителия. β–каротин подавляет пролиферацию только в основаниях кишечных крипт и не действует на верхушечные отделы энтероцитов, которые чаще подвергаются воздействию различными внешними канцерогенами [36].
Раннее плацебо–контролируемое исследование Hennekens C.H. с соавт. (1996) длительностью 12 лет (22000 человек) свидетельствуют, что длительное назначение физиологических доз b–каротина не оказывает ни благоприятного, ни вредного влияния на частоту возникновения злокачественных новообразований и сердечно–сосудистых заболеваний у мужчин [43]. Однако избыточное потребление b–каротина рассматривается как вероятный риск возникновения рака легких у курильщиков (особенно у злостных курильщиков) [63]. Четырехлетнее плацебо–контролируемое двойное слепое исследование (CARET, 2004) у 18000 человек продемонстрировало, что длительное применение b–каротина в высоких дозах (30 мг/сут.) в сочетании с мегадозами витамина А (ретинол; 25000 МЕ) не только не обеспечивает благоприятный эффект у лиц с повышенным риском рака легких (курильщики с потреблением сигарет от 1 пачки в день на протяжении до 20 лет), но даже несколько увеличивают риск смерти от рака легких и от других причин, связанных с нарушением обмена веществ, особенно у женщин [37]. Доказана связь длительного применения гипердоз b–каротина, витамина Е, ретинола у лиц с полиморфизмом генома, ассоциированного с повышенным риском рака легких, при этом курящих и работающих с асбестом [23]. Причинным канцерогеном в этом случае считают вовсе не b–каротин, как таковой, а образующиеся сложные соединения свободной (избыточной) фракции b–каротина с продуктами сгорания табачного дыма, асбеста [4,6]. Повышенное потребление овощей и фруктов, в том числе содержащих все изоформы каротиноидов, включая b–каротин, наоборот, снижает смертность от рака легких [17]. Очевидно, что для разрешения этих противоречий исследования необходимо дополнить оценкой баланса МЭ (Se, Zn, Mn и др.). Анализ установленных антиканцерогенных эффектов физиологических доз b–каротина предполагает существование иммунофармакологических механизмов кумуляции и микросомальной биотрансформации b–каротина, позволяющих обеспечивать элиминацию канцерогенов через идентичные микросомальные пути утилизации. Вероятно, есть синергизм b–каротина и МЭ в элиминации значительно большего спектра канцерогенов. Индивидуальные отличия в биохимизме, иммунотропном действии b–каротина весьма варьируют [3]. Изучается роль других каротиноидов, экстрагированных из плазмы крови человека (ликопин, лютеин, зеаксантин, пре–b–криптоксантин, b–криптоксантин, a– и g–каротин, полиеновые соединения) [36].
Ретиноиды – это собирательный термин для соединений, входящих в семейство полиизопреноидных липидов; они включают витамин А (ретинол) и его различные естественные и синтетические аналоги. По механизму действия это гормоны, которые активируют специфические рецепторы (RAR–α, β, g). Ретиноиды действуют на разных уровнях: они контролируют рост, дифференцировку, эмбриональное развитие, апоптоз клетки. Каждый ретиноид имеет свой фармакологический профиль, который определяет перспективность его применения в онкологии или дерматологии. Самый важный и изученный эндогенный ретиноид – ретиноевая кислота. Естественные ретиноиды (ретиноевая кислота, ретинол, некоторые метаболиты витамина А и др.) и их синтетические аналоги могут активно воздействовать на дифференцировку, быстрый рост и апоптоз злокачественных клеток, что определяет их роль в онкологии (лечение больных с промиелоцитарным лейкозом) и дерматологии. Исследования V.C. Njar с соавт. (2006) показали, что лечебный эффект ретиноевой кислоты ограничивается ее мультифакторными ингибиторами, например, цитохром P450–зависимыми–4–гидролазными ферментами (особенно CYP26s, ответственный за метаболизм ретиноевой кислоты) [61]. В 2007 году двумя исследовательскими группами (Jing Y. с соавт. [46] и Fenaux P. [30]) заявлено, что при лечении острого промиелоцитарного лейкоза ретиноевой кислотой с препаратами мышьяка можно достичь ремиссии [30]. Cинтезированы очередные аналоги ретинола – тамиберотин (Am80) (высокоэффективен при псориазе, ревматоидном артрите [34]), фенритидин – активатор апоптоза раковых клеток [40]. Недостатком всех синтетических ретиноидов является их токсичность и тератогенность [75]. Изучаются мегадозы витамина А и его аналогов и повышенные дозы пиридоксина для лечения рака мочевого пузыря [22]. Напомним, что витамин А участвует в регуляции транспорта железа и меди из печени к органам–мишеням, а избыточное поступление Fe и Cu промотирует свободнорадикальное окисление и опухоли, особенно у пожилых [4,36].
Xu W.H. с соавт. (2007) было установлено, что для профилактики рака эндометрия имеют значение пищевой ретинол, β–каротин, витамин C, E, пищевые волокна (инулины) [91].
Микронутриенты и их концентрированные формы: ретиноиды, полифенольные антиокислители (эпигаллокатехины, силимарин, изофлавон – генестин, куркумин, ликопен, бета–каротин, витамин E и селен) весьма перспективны и уже используются в лечении рака кожи наряду с нестероидными противовоспалительными средствами, дифлюорометилорнитином, T4 эндонуклеазой V [86]. Ретиноиды и витамин А используются в терапии рака простаты; они действуют антипролиферативно, усиливая дифференцирование клеток, снижая индекс деления и потенцируя апоптоз [64].
Выполнены актуальные исследования по отдельным видам витаминов и группам витаминов (витамины группы В). Для улучшения качества жизни онкологических больных очень важен витамин В1. Митохондрии – главные внутриклеточные органеллы, производящие молекулы АТФ. Тиамин и другие витамины группы В – это прежде всего коферменты важнейших ферментов, обеспечивающих функционирование клетки, особенно митохондрий [27,28], ферментов, восстанавливающих энергетические ресурсы в ЦНС, печени, почках, сердечной мышце [45].
Раковые клетки обладают высоким энергетическим метаболизмом и уровнем гликолиза. Для своего роста они нуждаются в огромных количествах глюкозы, и хорошо известно, что избыток простых углеводов в питании – благоприятная среда для роста опухолей [35]. В настоящее время глобальное расширение глюкозотолерантности населения планеты (Россия находится в зоне особого риска распространения глюкозотолерантности!), особенно в зрелом и пожилом возрасте, рассматривается как дополнительный фактор снижения противоопухолевого иммунитета. Избыток сахаров повышает потребность больного в тиамине и тиаминзависимых ферментах, в первую очередь в транскетолазе. Производство АТФ уменьшается по мере роста рака и ведет к раковой кахексии, энергодефициту, зябкости. Многие экспериментально вызванные раки (например, рак грудной железы у крыс) с положительным результатом лечатся тиамином, а также рибофлавином, никотиновой кислотой, коферментом Q10 в составе комбинированной терапии. При этом тиамин при его недостатке именно улучшает соматическое состояние при раке и никак не промотирует развитие опухоли и ее метастазирование. Терапевтическое значение использования комбинации модулирующих энергию витаминов (В1, В2, РР), коэнзима Q10 имеет большую перспективу при раке молочных желез [66].
Периферическая нейропатия – достаточно частое заболевание в пожилом возрасте; особенно часто она развивается у больных диабетом, алкоголизмом [10]. Полинейропатия полиэтиологична; без метаболической витаминотерапии ее течение прогредиентно и может быть неблагоприятным по прогнозу заболевания и жизни. В лечебной тактике раньше использовали большие дозы тиамина. В последние десятилетия используется более эффективный жирорастворимый и проникающий через липидный бислой клеточных мембран дериват витамина В1 – бенфотиамин. При полиневропатии оправдано также применение других нутриентов: пиридоксина, витамина Е, В12, фолатов, биотина, а также α–липоевой кислоты, глутатиона, омега–3 жирных кислот, препаратов Zn, Mg [42]. С профилактической целью предупреждение гиповитаминоза В1 по–прежнему осуществляется путем обогащения пищи физиологическими дозами тиамина (1,2–2,5 мг/сут., в зависимости от энерготрат) [6]. Участие тиамина и бенфотиамина в метаболизме глюкозы эндотелиальной клетки, предотвращение преобразования глюкозы в сорбитол в конечном итоге ограничивает возможность развития характерных осложнений у больных диабетом, снижает глюкозотолерантность (обязательный спутник опухолей) [12].
Тиамин обладает противоболевым эффектом у геронтологических больных с болевым синдромом различной этиологии, в том числе и онкологической; он дозозависим (нарастает от физиологических к фармакологическим дозам) [41,56]. Однако даже высокие дозы водорастворимого тиамина (250 мг/сут.) были не эффективны и не повлияли на окислительное напряжение крови у больных с возрастной гипергликемией, находящихся на управляемом гемодиализе [53]. В чем же причина? Качество клеточных мембран и их проницаемость для микронутриентов – новая страница клинической фармакологии. При изучении возрастной фармакодинамики и кинетики витаминов очень важную роль играет фактор возрастного изменения пластичности мембран (снижение текучести, импрегнация в мембрану клеток патологических трансгенных жиров, обеднение или трасформация рецепторного сигнального аппарата и т.д.). Жирорастворимые аналоги витамина В1 – аллитиамины (от лат. Allium – чеснок) – Fujiwara М. обнаружил в 1954 году, в известных своими иммуномодулирующими свойствами растениях – чесноке, луке и луке–порее. Оказалось, что полученные жирорастворимые дериваты тиамина многократно лучше проникают через бислой липидов клеточных мембран. Прием жирорастворимых форм увеличивает уровни витамина В1 в крови и тканях намного больше, чем водорастворимые соли тиамина (тиамина бромид, тиамина хлорид) [32,34]. Биодоступность бенфотиамина составляет 600, фурсультиамина около 300, а тиамин–дисульфида менее 40 мг/ч/мл [38]. Бенфотиамин может противодействовать обусловленным диабетом эксайтотоксичным процессам в мозге через механизм, не связанный с тканевыми факторами, и не снижая активности выработки фактора некроза опухолей TNF–a (tumor necrosis factor–a) [90].
Витамины В6, В12 и фолиевая кислота получили статус генозащитных витаминов. Витамин В12 содержит кобальт и цианогруппу, образующие координационный комплекс. Источниками витамина является кишечная микрофлора, а также продукты животного происхождения (дрожжи, молоко, красное мясо, печень, почки, рыба и яичный желток). Фолат и холин, как известно, являются центральными донорами метила, необходимого для синтеза митохондриального белка. Именно эти витамины активно способствуют защите митохондриального генома. Сейчас проводится серьезное изучение роли витаминов группы В в нейтрализации клеточного токсического эффекта ряда ксенобиотиков, ядов, а также молекулярных, клеточных и клинических последствий дефицита этих витаминов [28]. Распространенность дефицита витамина В12 увеличивается в пожилом возрасте из–за развития атрофии слизистой оболочки желудка, опухолей желудка и нарушения соответствующей ферментативной обработки пищи, необходимой для преобразования витамина В12 во всасываемую форму. При сочетанном дефиците витамина В12 и фолиевой кислоты вследствие наличия нарушений метаболизма фолатов (врожденная мальабсорбция фолата, нестабильность метилентетрагидрофолатредуктазы, дефицит формиминотрансферазы) вероятность атеросклероза, венозного тромбоза и злокачественной патологии существенно возрастет [86], а для коррекции этих наследственно обусловленных нарушений иногда требуются более высокие дозы витамина В12, фолиевой кислоты, витамина В6 [26]. При этом дотация витамина В12 у пожилых особенно актуальна. В 2007 году исследовательской группой Morris M.S. с соавт. сделано интересное наблюдение: у больных пожилого возраста часто отмечается пониженный уровень витамина В12 в крови в сочетании с уровнем фолиевой кислоты на верхней границе диапазона нормы [59]. Эффективная и безопасная доза витамина В12, приводящая к полной компенсации признаков дефицита, для пожилых и старых людей составляет от 500 мкг/сут. до 1000 мкг per os [63]. Если диагноз дефицита витамина В12 подтвержден лабораторно, необходимо каждые 2–3 месяца проводить курсы витаминотерапии витамина В12 ежедневно в дозе до 1000 мкг [44]. Head K.A. (2006) и Martin S. (2007) призывают рассматривать высокий уровень гомоцистеина в крови в качестве фактического индикатора дефицита витамина В12 и фолиевой кислоты в организме и нового онкологического маркера [44,58]. Поэтому дефицит витамина В12 должен подозреваться не только у всех лиц с болезнями кишечника (особенно при колоректальной аденоме), необъяснимой анемии, полинейропатии, у лиц со старческим слабоумием, включая болезнь Альцгеймера, но и при гипергомоцистеинемии [64].
Уровень цианкобаламина в крови в норме 180–900 пг/мл; при метастазировании опухолей в печень он может быть повышен. При заболеваниях печени (острый и хронический гепатит, цирроз печени, печеночная кома) уровень витамина В12 может превышать норму в 30–40 раз, что связано с выходом депонированого цианкобаламина из разрушенных гепатоцитов. Этот уровень повышается за счет нарастания концентрации в крови транспортного белка – транскобаламина, в то время как истинные запасы витамина В12 в печени истощаются.
Известно, что метаболизм витамина В12 происходит очень медленно и при этом не образуются мутагенные продукты. По данным мета–анализа, проведенного Bleys J. et al. (2006), многолетнее комплексное применение биологически активных добавок к пище в виде комплексов витаминов группы В (В12, В6 и фолиевой кислоты) безопасно и не повышает риск атеросклероза даже в пожилой группе при длительном употреблении [16].
Также сам по себе, в составе добавок к питанию или в виде препаратов витамин В12 нейтрален по отношению к раку простаты. Исследования у 27111 финнов в возрасте 50–69 лет, из которых в 1270 случаях диагностировался рак простаты, показали, что более высокое пищевое потребление витамина В12 не защищает от возникновения рака простаты [35].
В то же время опубликованы многолетние эпидемиологические исследования, оценивающие роль питания и риск рака простаты. Красное мясо и печень, твердые жиры, гиподинамия достоверно повышают риск заболевания. Красное мясо концентрирует железо, насыщенные жиры, в том числе витамин В12. Детализация значимости ряда составляющих этих продуктов обнаружила «виновных» в промотировании опухолей. Это твердые насыщенные жиры, при агрессивной термической обработке (жарение на растительных маслах, грилевание) – трансжиры, алкоголь и железо в составе красного мяса [35]. Вместе с тем само по себе применение витамина В12 и комплексов витаминов группы В (В6, фолиевая кислота и В12) у больных раком простаты оказалось нейтральным. Назначение больным с раком простаты и имеющим установленный дефицит цианкобаламина в плазме крови витамина В12 улучшает соматическое состояние пациентов с раком простаты и не влияет на ее рост и метастазирование, поэтому взаимоотношение между обеспеченностью витамином В12 и раком простаты требует дальнейшего исследования и в настоящее время исследования продолжаются [85]. Кроме того, для возникновения рака простаты достоверно установлен фактор низкой двигательной активности, воздействия повышенной температуры, алкоголя и курения. Свежие овощи, а также селен (в том числе в составе чеснока, водорослей, черного перца, лука, свежих орехов, семечек, но не в составе жареных орехов, жареных семечек, свиного сала, креветок и сметаны) – важные факторы защиты от рака простаты [2,35]. Исключение из питания красного мяса и твердых жиров, алкоголя, биологически активных добавок, содержащих железо, без лабораторно подтвержденной железодефицитной анемии – важная профилактическая и лечебная рекомендация для мужчин, страдающих аденомой простаты и имеющих высокий риск заболевания (возраст, наследственность, простатит).
Низкий уровень фолатов (недостаточное употребление в пищу свежих зеленолистных растений) ассоциирован с высоким риском рака толстого кишечника и молочной железы. При высоком уровне потребления алкоголя этот риск суммируется. Анализ 195 случаев спорадического рака толстой кишки и 195 добровольцев–ровесников показал, что уровень фолата ниже у больных раком толстой кишки; величины витамина В12 не различались в основной и контрольной группах, т.е. в колоректальном карциногенезе большую роль играет пониженный метаболизм фолиевой кислоты [24]. Адекватное потребление фолиевой кислоты предохраняет и от рака молочной железы. Особенно ярко защитный эффект проявляется в популяции с полиморфизмами генома, ассоциированными с нарушениями обмена фолатов. Выявление этих полиморфизмов в детстве и пожизненная коррекция фолатов (зеленолистная диета, свежий сыр, витаминные комплексы) нивелируют генетический компонент. Это подтверждено девятилетним наблюдением у 62739 женщин в период менопаузы; из них в 1812 случаях развился рак молочной железы [52].
Проведенные к текущему моменту иммунологические и биохимические исследования Schroecksnadel K. с соавт. (2007) показали, что дефицит фолиевой кислоты не только способствует реметелированию гомоцистеина – ранее доказанному фактору риска развития злокачественной опухоли (чем ниже концентрации в крови трех водорастворимых витаминов – фолиевой кислоты, витамина В6 и витамина В12, тем выше уровень гомоцистеина в крови [8,81]), но и свидетельствует о снижении общей Т–клеточной иммунной антионкологической защиты [75]. Повышенное потребление фолиевой кислоты, витаминов В6 и В12 снижает риск развития рака молочной железы. У 475 мексиканских женщин с раком молочной железы выявлено пониженное потребление этих витаминов, в то время как у 1391 женщин в возрасте 18–82 лет контрольной группы уровень потребления был адекватным. Результаты исследования признаны доказательными; они еще раз подтвердили тот факт, что нормальное потребление фолиевой кислоты и витамина В12 уменьшает риск развития рака молочной железы [52].
Bolander F. (2006) в аналитическом обзоре «Витамины: не только для ферментов» показал эволюцию научных взглядов от традиционных и изначальных (трактующих витамины как коферменты, ускоряющие химические реакции) к новым, основанным на изучении биохимического маршрута витаминов с использованием новых технологий молекулярной биологии и физико–химической медицины [18]. Не только витамины A и D обладают дополнительными гормоноподобными свойствами. Это известно более 30 лет. Еще четыре витамина: витамин К2, биотин, никотиновая кислота и пиридоксаль фосфат – выполняют гормональные функции. Витамин K2 вовлечен не только в карбоксилирование факторов коагуляции, но и является фактором транскрипции белков костной ткани. Биотин необходим для дифференцировки эпидермиса. Пиридоксаль фосфат (коферментная форма витамина B6), кроме декарбоксилирования и трансаминирования, может ингибировать ДНК полимеразы и несколько видов стероидных рецепторов. Эти качества витамина В6 используются для потенцирования химиотерапии рака. Никотиновая кислота не только конвертирует NAD+ в NADP+, которые используются как водородно/электронные транспортеры в окислительно–восстановительных реакциях, но и обладает сосудорасширяющим и антиатерогенным действием [18]. В течение десятилетий никотиновая кислота используется при лечении больных с дислипидемией, но молекулярные механизмы расшифрованы не были. Прилив крови (сосудистый эффект никотиновой кислоты, рассматриваемый по ситуации и как лечебный, и как побочный эффект терапии) связан с избыточным выбросом сосудорасширящих простагландинов. Повышение восприимчивости опухолей щитовидной железы к лучевой терапии J131 под действием никотинамида объясняется способностью витамина увеличивать кровоток в щитовидной железе [80].
Никотинамид, коферментная форма амида никотиновой кислоты, является предшественником динуклеотида аденина никотинамида β–кофермента [NAD (+)] и играет существенную роль в повышении выживания клетки. Li F. с соавт. (2006) изучили возможности никотинамида как нового агента, способного модулировать клеточный метаболизм, пластичность, воспалительную функцию клетки и влиять на длительность ее жизненного цикла. Предполагаетcя, что никотинамид можно с успехом использовать у больных пожилого возраста не только при ишемии мозга, болезни Паркинсона и Альцгеймера, но и при раке [54]. Установлено, что никотинамид увеличивает продолжительность жизни нормальных человеческих фибробластов. Клетки, обеспеченные никотинамидом, поддерживали высокий уровень митохондриального мембранного потенциала, но при этом отмечен пониженный уровень дыхания, супероксидного аниона, активных радикалов кислорода [48].
Sundravel S. с соавт. (2006) в эксперименте с привитым раком эндометриальной карциномы показали, что сочетание тамоксифена с никотиновой кислотой, рибофлавином, аскорбиновой кислотой уменьшало повышенную активность гликолитических ферментов в плазме крови и увеличивало – глюконеогенетических, приводя показатели к норме. Было высказано предположение, что никотиновая кислота, рибофлавин и аскорбиновая кислота могут использоваться в терапии при эндометриальной карциноме [78]. И действительно, годом позже (2007) Premkumar V.G. с соавт. показали, что лечение тамоксифеном больных раком легкого с метастазами, дополненное никотиновой кислотой, рибофлавином, коферментом Q10, способствовало уменьшению активности метастазирования опухоли по уровню карциноэмбрионального антигена и онкомаркеров (С15–3) [69]. Дополнение никотинамида способствовало более выраженному накоплениею 5–фторурацила в метастазах колоректального рака [39].
Иммунотропные (и антиопухолевые) эффекты витамина D с гормональными эффектами [6] достаточно четко прослеживаются и в эксперименте, и в клинике [7,9,25,68]. Как и для ретиноидов, для витамина D доказано активное участие в регуляции иммуногенеза и клеточной пролиферации. Моноциты и лимфоциты производят рецепторный белок с молекулярным весом 50 кДа для витамина D3 с идентичной аминокислотной последовательностью, как и у кишечного рецепторного белка. Лимфоцитами также дополнительно синтезируется цитозольный рецепторный белок с ММ 80 кДа. Сигнал с этих рецепторных белков достигает NF–κВ–транскрипционного фактора, регулирующего дифференцировку и рост клеток от костномозговых стволовых предшественников до зрелых моноцитов лимфоцитов [58]. Витамин D3 потенцирует действие цитостатика в опухоль, пролонгирует терапевтический эффект и позволяeт минимизировать нагрузку базовым химиопрепаратом [65].
Активный метаболит витамина D3 – кальцитриол (1–α, 25–дигидроксивитамин D3) – также обладает выраженным противоопухолевым эффектом in vitro и in vivo. Кальцитриол ингибирует рост и развитие раковых образований, используя различные механизмы. Так, ингибирование роста рака простаты витамином D3 осуществляется путем воздействия на белок 3 (IGFBP–3), на ферменты циклогеназу и дегидрогеназу и 15 простагландинов и ряд других факторов. S. Swami в 2007 г. на основании клинического опыта предложил дополнить применение препаратов простагландинов при лечении больных раком простаты комбинацией кальцитриола и генистейна [79]. Оба препарата действуют антипролиферативно. Кальцитриол ингибирует путь простагландина PGE2 (потенциатора канцерогенеза) к раковой клетке тремя способами: уменьшая экспрессию циклооксигеназы 2 (COX–2); стимулируя активность 15–гидроксипростагландиндегидрогеназы (15–PGDH); снижая чувствительность рецепторов PGE2 и PGF–2α. Это приводит к уменьшению уровня биологически активного простагландина PGE2 и, в конечном итоге, к ингибированию роста раковых клеток опухоли простаты. Генистейн, один из главных компонентов сои, – мощный ингибитор деятельности цитохрома CYP24, фермента, который регулирует метаболизм кальцитриола, увеличивая период его полужизни. В результате синергидный эффект с гинестином расширяет спектр применения кальцитриола [51].
Имеется противоопухолевая активность у синтезированного H. Maehr с соавт. (2007) деривата кальцитриола – эпимерика с двумя побочными цепочками в положении С–20–III, на модели рака толстой кишки [55]. Cтимулируемая кальцитриолом антипролиферативная продифференциация защищает и от других видов рака, например, под его влиянием происходит подавление роста культуры клеток человеческой хориокарциномы [9]. Полагают, что в условиях низкого содержания белка при онкологии продукция кальцитриола уменьшена из–за нарушенной активности системы цитохрома CYP27B1 [9].
С исследованиями по витамину D связано открытие фактора сезонности рака легких у жителей Норвегии [68]. Были выявлены содружественные сезонные колебания содержания кальцитриола в крови, снижение уровня витамина D3 в период недостаточной инсоляции и возникновения рака легкого. Максимальный уровень витамина D3 в сыворотке крови отмечается с июля по сентябрь. В соответствующий зимний период уровень витамина D3 снижается на 20–120%. Предполагается прогнозировать зимний рост заболеваемости не только раком легкого, но и раком толстой кишки, простаты, молочной железы, Ходжкинской лимфомы. Результаты химиотерапии, оперативных вмешательств и прогноза жизни у больных с раком легких, толстой кишки, простаты лучше, если лечение осуществлено летом [68]. Становится очевидной необходимость проведения в зимний период профилактических антионкологических программ витаминизации у жителей, проживающих в северных регионах и испытывающих дефицит естественной освещенности. Для восстановления функции макрофагов и лимфоцитов при иммунодефиците, обусловленном D–недостаточностью, достаточно приема 400–450 МЕ витамина D3 в день в течение 2—3 месяцев.
Метаболизм витамина D3 тесно связан с обменом элементов. В частности, Ca–связывающие белки, индуцируемые D3, связывают Cu, Zn, Co, Sr, Ba, Ni, Mn, Cd, Pb, Be. Хроническое недостаточное потребление Ca и витамина D — фактор риска рака толстого кишечника, рака легких, рака простаты, молочной железы, Ходжкинской лимфомы [36].
Опухоль и ее хозяин получают питательные вещества из одного источника; это аксиома. Однако организм хозяина, не получая адекватной нормы витаминов, уже исходно имеет низкий ресурс противоопухолевого иммунитета. Адекватное профилактическое обеспечение витаминного, микроэлементного, пектинового баланса в пище – резерв реабилитации иммунитета человека в целом и противоопухолевого иммунитета в частности. Информация об индивидуальных полиморфизмах генома раскрывает возможность целевого использования высокодозовой нутрициологии. Тактики «агрессивной» витаминотерапии и интенсивной терапии выступают новым, только еще раскрывающим свои возможности резервным инструментом для спасения жизней и долгосрочного выхаживания больных. Для этого необходима генетическая паспортизация человека, желательно при рождении или в молодом возрасте. В этом случае есть большой ресурс времени и биологического здоровья для проведения индивидуально подобранной витаминотерапии, отвечающей принципам клинической фармакологии: высокая эффективность и безопасность.
Комментарий
Таким образом, исходя из данных литературы, следует, что витамины обладают широкими фармакологическими и ограниченными противоопухолевыми свойствами. На сегодняшний день в России зарегистрировано большое количество витаминных и витаминно–минеральных комплексов для обеспечения организма как суточными физиологическими, так и повышенными дозами витаминов. Среди отечественных препаратов следует отметить витаминно–минеральные комплексы «Компливит» и «Селмевит» (ОАО «Фармстандарт–УфаВИТА»). Фармацевтическая пропись «Компливита» учитывает российские нормы потребления витаминов и минералов и обеспечивает безопасное дозирование микронутриентов, что позволяет рекомендовать данный комплекс для длительного профилактического применения. Комплекс «Селмевит» содержит дополнительные антиоксидантные компоненты (селен, метионин) и показан для целевой коррекции дефицита селена, а также для снижения негативного воздействия на организм человека факторов внешней среды, провоцирующих процессы свободнорадикального окисления.
Матрица здоровья состоит из многих составляющих, витамины и минералы – важнейший модифицируемый диетический фактор. Осмысленное и индивидуальное назначение витаминов при их дефиците – доказанная линия метаболической защиты организма, в том числе защиты против атеросклероза, онкологии, а также вирусной и инфекционной патологии.
Литература
1. Дурнев АД., Серединин СБ. Мутагены (скрининг и фармакологическая профилактика воздействий). – М.: Медицина, 1998. – 328 с.
2. Жвиташвили ЮБ. Как победить рак. Выбор диеты. – СПб.: Нева, 2002. – 370 с.
3. Кудрин АВ., Громова OA. Микроэлементы в иммунологии и онкологии, Программы института микроэлементов ЮНЕСКО, М.: «Гэотар–МЕД», 2007. – 970 с.
4. Меньщикова Е.Б., Ланкин В.З., Зенков Н.К, Бондарь И.А., Круговых Н.Ф., Труфакин В.А. Окислительный стресс. Прооксиданты и антиоксиданты /Е.Б. Меньщикова и др. ─– М.: «Слово», 2006. – 553 с.
5. Молчанов ОЕ., Правильное питание при онкологических заболеваниях. – СПб, – 2004; – 78 с.
6. Спиричев В.Б., Шатнюк Л.Н., Позднянский В.М. Обогащение пищевых продуктов витаминами и минеральными веществами. ─ Новосибирск: Сибирское университетское издание, 2004. – 547 с.
7. Alagbala A.A., Johnson C.S., Trump D.L., et al. Antitumor Effects of Two Less–Calcemic Vitamin D Analogs (Paricalcitol and QW–1624F(2)–2) in Squamous Cell Carcinoma Cells. Oncology. – 2007; Jan 18;70(6): – P. 483–492.
8. Araki A. Homocysteine and diabetic microangiopathy. [Article in Japanese]. //Nippon Rinsho. – 2006; 64 (11): – P. 2153–8.
9. Avila E, Diaz L, Barrera D, Arranz C, Halhali A, Larrea F.Metabolism of vitamin D in the human choriocarcinoma cell line JEG–3.J. Steroid. Biochem.//Mol. Biol. – 2007; Jan 23. [MEDLINE in press].
10. Benfotiamine – monograph. Altern. Med. Rev. – 2006; Sept.;11(3): – P. 238–242.
11. Benner S.E., Pajak T.F., Stetz J., Lippman S.M. et al. Toxicity of isotretinoin in a chemoprevention trial to prevent second primary tumors following head and neck cancer. //J Natl Cancer Inst. –1994; Dec 7;86(23): – P.1799–1801.
12. Berrone E., Beltramo E., Solimine C., Ape A.U., Porta M. Regulation of intracellular glucose and polyol pathway by thiamine and benfotiamine in vascular cells cultured in high glucose. //J Biol Chem. – 2006; Apr 7;281(14): – P. 9307–13.
13. Bjelakovic G, Nikolova D, Simonetti RG, Gluud C. Antioxidant supplements for preventing gastrointestinal cancers. Cochrane Database Syst Rev. – 2004; Oct 18;(4):CD004183 // Evid Based Nurs. – 2005; Apr;8(2): – P.48.
14. Bjelakovic G., Nagorni A., Nikolova D. Meta–analysis: antioxidant supplements for primary and secondary prevention of colorectal adenoma //Aliment Pharmacol Ther. – 2006 Jul 15;24(2): – P.281–291.
15. Bjelakovic G, Nikolova D, Gluud LL. et al. Mortality in randomized trials of antioxidant supplements for primary and secondary prevention: systematic review and meta–analysis //JAMA. – 2007; Feb 28;297(8): – P.842–857.
16. Bleys J., Miller E.R. 3rd, Pastor–Barriuso R. et al. Vitamin–mineral supplementation and the progression of atherosclerosis: a meta–analysis of randomized controlled trials //Am J Clin Nutr. – 2006; Oct;84(4): – P.680–681.
17. Block G. Vitamin C status and cancer. Epidemiologic evidence of reduced risk. //Ann N Y Acad Sci. – 1992; Sep 30;669: – P. 280–290; discussion 290–292.
18. Bolander F.F. Vitamins: not just for enzymes. // Curr Opin Investig Drugs. – 2006; Oct;7(10): – P. 912–915.
19. Bosetti C., Scotti L., Maso L.D., Talamini R., Montella M., Negri E., Ramazzotti V., Franceschi S., Vecchia C.L. Micronutrients and the risk of renal cell cancer: A case–control study from Italy. //Int J Cancer. – 2007; Feb 15;120(4): – P. 892–896.
20. Brownlee M. The pathobiology of diabetic complications: a unifying mechanism. Diabetes. – 2005; Jun;54(6): – P.1615–25.
21. Brownlee M. The pathobiology of diabetic complications: a unifying mechanism. Diabetes. – 2005; Jun;54(6): – P.1615–25.
22. Busby J.E., Kamat A.M. Chemoprevention for bladder cancer.//J Urol. – 2006; Nov;176(5): – P. 1914–1920.
23. Caraballoso M., Sacristan M., Serra C., Bonfill X. Drugs for preventing lung cancer in healthy people //Cochrane Database Syst Rev. – 2003; (2):CD002141
24. Chang S.C., Lin P.C., Lin J.K., Yang S.H., Wang H.S., Fen–Yau Li A. Role of MTHFR polymorphisms and folate levels in different phenotypes of sporadic colorectal cancers. // Int J Colorectal Dis. – 2006; Aug 29. [MEDLINE in press]
25. Cordes T., Diesing D., Becker S., Diedrich K., Reichrath J., Friedrich M. Vitamin D–metabolism in the human breast cancer cell line MCF–7. //Anticancer Res. – 2006; Jul–Aug;26(4A): – P. 2749–53.
26. Den Heijer M. Are B. Vitamins a risk factor for VTE? Perhaps.// J Thromb Haemost. – 2006; Feb;4(2): – P. 309–11.
27. Depeint F., Bruce W.R., Shangari N., Mehta R., O’Brien P.J. Mitochondrial function and toxicity: role of B vitamins on the one–carbon transfer pathways. //Chem Biol Interact. – 2006; Oct 27;163(1–2): – P. 113–32.
28. Depeint F., Bruce W.R., Shangari N., Mehta R., O’Brien P.J. Mitochondrial function and toxicity: role of the B vitamin family on mitochondrial energy metabolism. //Chem. Biol. Interact. – 2006; Oct 27;163(1–2): – P. 94–112.
29. Devis M.B., Austin J., Partridge D.A. Vitamins C. Its Chemisrty and Biochemisrty, Royal Society of Chemisrty, Cambridge, 1998, 168 p.
30. Fenaux P., Wang Z.Z., Degos L. Treatment of acute promyelocytic leukemia by retinoids.//Curr Top Microbiol Immunol. – 2007; 313: – P. 101–128.
31. Finaud J., Lac G., Filaire E. Oxidative stress: relationship with exercise and training. //Sports Med. – 2006; 36(4): – P. 327–358.
32. Fujiwara М. Allitiamine: a newly found derivative of vitamin B1// J. Biochem. – 1954; V.2: – P. 273–285.
33. Fukasawa H., Kagechika H., Shudo K. Retinoid therapy for autoimmune diseases. //Nihon Rinsho. – 2006; Jun;29(3): – P. 114–126.
34. Gadau S., Emanueli C., Van Linthout S. et al. Benfotiamine accelerates the healing of ischaemic diabetic limbs in mice through protein kinase B/Akt–mediated potentiation of angiogenesis and inhibition of apoptosis. Diabetologia. – 2006; Feb;49(2): – P. 405–420.
35. Geissler C., Powers H. Human Nutrition, Edinburgh. – 2006; – 763 P.
36. Gerste H. Intermediate cancer biomarkers and their use in beta–carotene studies in humans.// Int J Vitam Nutr Res. – 1996; 66(1): – P. 3–18.
37. Goodman G.E., Thornquist M.D., Balmes J. et al.The Beta–Carotene and Retinol Efficacy Trial: incidence of lung cancer and cardiovascular disease mortality during 6–year follow–up after stopping beta–carotene and retinol supplements.// J Natl Cancer Inst. – 2004; Dec 1;96(23): – P. 1743–1750.
38. Greb A., Bitsch R. Comparative bioavailability of various thiamine derivates after oral administration //Int. J Clin Pharmacol Ther – 1998; 36(4): – P. 216–221
39. Gupta N., Saleem A., Kotz B., Osman S. et al. Carbogen and nicotinamide increase blood flow and 5–fluorouracil delivery but not 5–fluorouracil retention in colorectal cancer metastases in patients. //Clin Cancer Res. – 2006. May 15;12(10): – P. 3115–3123.
40. Hail N.Jr., Kim H.J., Lotan R. Mechanisms of fenretinide–induced apoptosis. //Apoptosis. – P. 2006; Oct;11(10): – P. 1677–1694.
41. Harper C. Thiamine (vitamin B1) deficiency and associated brain damage is still common throughout the world and prevention is simple and safe! //Eur J Neurol. – 2006; Oct;13(10): – P. 1078–1082.
42. Head K.A. Peripheral neuropathy: pathogenic mechanisms and alternative therapies. // Altern Med Rev. – 2006; Dec;11(4): – P. 294–329.
43. Hennekens C.H., Buring J.E., Manson J.E. et al. Lack of effect of long–term supplementation with beta carotene on the incidence of malignant neoplasms and cardiovascular disease.// N Engl J Med. – 1996; May 2;334(18): – P. 1145–1149.
44. Hvas A.M., Nexo E. Diagnosis and treatment of vitamin B12 deficiency–an update. //Haematologica. – 2006; Nov;91(11): – P. 1506–1512.
45. Jiang Y.Y. Effect of B vitamins–fortified foods on primary school children in Beijing. //Asia Pac J Public Health. – 2006; 18(2): – P. 21–25.
46. Jing Y., Waxman S.The design of selective and non–selective combination therapy for acute promyelocytic leukemia.//Curr Top Microbiol Immunol. –2007;313: – P. 245–269.
47. Kamangar F., Qiao Y.L., Yu B. et al. Lung cancer chemoprevention: a randomized, double–blind trial in Linxian, China. Cancer Epidemiol Biomarkers Prev. – 2006; Aug;15(8): – P. 1562–1564.
48. Kang H.T., Lee H.I., Hwang E.S. Nicotinamide extends replicative lifespan of human cells. //Aging Cell. – 2006; Oct;5(5): – P. 423–436.
49. Kirsh V.A., Hayes R.B., Mayne S.T. et al. Supplemental and dietary vitamin E, beta–carotene, and vitamin C intakes and prostate cancer risk. //J Natl Cancer Inst. – 2006; Feb 15;98(4): – P. 245–254.
50. Krishnan A.V., Moreno J., Nonn L. et al. Novel pathways that contribute to the anti–proliferative and chemopreventive activities of calcitriol in prostate cancer.//J Steroid Biochem Mol Biol. – 2007; Jan 15. [PubMed abstract – in press].
51. Lajous M., Romieu I., Sabia S. et al. Folate, vitamin B12 and postmenopausal breast cancer in a prospective study of French women. //Cancer Causes Control. – 2006; Nov;17(9): – P. 1209–1213.
52. Lajous M., Lazcano–Ponce E., Hernandez–Avila M., et al Folate, vitamin B(6), and vitamin B(12) intake and the risk of breast cancer among Mexican women. // Cancer Epidemiol Biomarkers Prev. – 2006; Mar;15(3): – P. 443–448.
53. Lapointe A., Couillard C., Lemieux S. Effects of dietary factors on oxidation of low–density lipoprotein particles. //J Nutr Biochem. – 2006; Oct;17(10): – P. 645–658.
54. Li F., Chong Z.Z., Maiese K. Cell Life versus cell longevity: the mysteries surrounding the NAD+ precursor nicotinamide.// Curr Med Chem. – 2006;13(8): – P. 883–895.
55. Maehr H., Uskokovic M., Adorini L. et al. Calcitriol derivatives with two different side chains at C–20 III. J. Steroid. Biochem Mol. Biol. – 2007; Jan 23. [PubMed abstract – in press].
56. Malecka S.A., Poprawski K., Bilski B. Prophylactic and therapeutic application of thiamine (vitamin B1)–a new point of view. //Wiad Lek. – 2006; 59(5–6): – P. 383–387.
57. Manolagas S.C., Yu X.P., Girasole G., Bellido T. Vitamin D and the hematolymphopoietic tissue: a 1994; update. // Semin Nephrol. – 1994; Mar;14(2): – P. 129–143.
58. Martin S. New agents in clinical oncology. //IDrugs. – 2007 Feb;10(2): – 99–101
59. Morris M.S., Jacques P.F., Rosenberg I.H., Selhub J. Folate and vitamin B–12 status in relation to anemia, macrocytosis, and cognitive impairment in older Americans in the age of folic acid fortification.//Am J Clin Nutr. – 2007; Jan;85(1): – P. 193–200.
60. Nascimento M.M., Suliman M.E., Murayama Y. et al. Effect of high–dose thiamine and pyridoxine on advanced glycation end products and other oxidative stress markers in hemodialysis patients: a randomized placebo–controlled study. //J Ren Nutr. 2006; Apr;16(2):119–124.
61. Njar V.C., Gediya L., Purushottamachar P. et al. Retinoic acid metabolism blocking agents (RAMBAs) for treatment of cancer and dermatological diseases. //Bioorg Med Chem. – 2006; Jul 1;14(13): – P. 4323–4340.
62. Omenn G.S., Goodman G.E., Thornquist M.D. Risk factors for lung cancer and for intervention effects in CARET, the Beta–Carotene and Retinol Efficacy Trial. // J Natl Cancer Inst. – 1996; Nov 6;88(21): – P. 1550–1559.
63. Park S., Johnson M.A. What is an adequate dose of oral vitamin B12 in older people with poor vitamin B12 status? // Nutr Rev. – 2006; Aug;64(8): – P. 373–378.
64. Pasquali D., Rossi V., Bellastella G., Bellastella A., Sinisi A.A. Natural and synthetic retinoids in prostate cancer. // Curr Pharm Des. – 2006;12(15): – P. 1923–1929.
65. Pelczynska M., Switalska M., Maciejewska M., Jaroszewicz I., Kutner A., Opolski A. Antiproliferative activity of vitamin D compounds in combination with cytostatics. Anticancer Res. – 2006; Jul–Aug;26(4A): – P. 2701–2705.
66. Perumal S.S., Shanthi P., Sachdanandam P. Energy–modulating vitamins – a new combinatorial therapy prevents cancer cachexia in rat mammary carcinoma.// Br J Nutr. – 2005; Jun;93(6): – P. 901–909.
67. Plummer M., Vivas J., Lopez G., Bravo J.C. et al. Chemoprevention of precancerous gastric lesions with antioxidant vitamin supplementation: a randomized trial in a high–risk population. // J Natl Cancer Inst. – 2007; Jan 17;99(2): – P. 101–103.
68. Porojnicu A.C., Robsahm T.E., Dahlback A. et al. Seasonal and geographical variations in lung cancer prognosis in Norway Does Vitamin D from the sun play a role? //Lung Cancer. – 2007; Jan 4. [PubMed abstract in press].
69. Premkumar V.G., Yuvaraj S., Vijayasarathy K. et al. Effect of Coenzyme Q(10), Riboflavin and Niacin on Serum CEA and CA 15–3 Levels in Breast Cancer Patients Undergoing Tamoxifen Therapy. // Biol Pharm Bull. – 2007; 30(2): – P. 367–370.
70. Preston–Martin S., Pogoda J.M., Mueller B.A., et al. Prenatal vitamin supplementation and risk of childhood brain tumors. Int J Cancer Suppl. – 1998;11: – P. 17–22.
71. Reynolds E. Vitamin B12, folic acid, and the nervous system.//Lancet Neurol. 2006; Nov;5(11): 949–960.
72. Robertson A.M., Finochietto P., Gamba C.A. et al.. Nicotinamide increases thyroid radiosensitivity by stimulating nitric oxide synthase expression and the generation of organic peroxides. //Horm Metab Res. – 2006; Jan;38(1): – P.12–15.
73. Sasazuki S., Sasaki S., Tsubono Y., Okubo S. et al. Effect of vitamin C on common cold: randomized controlled trial. Eur J Clin Nutr. 2006; Jan;60(1):9–17.
74. Schaffer S., Eckert G.P., Schmitt–Schillig S., Muller W.E. Plant foods and brain aging: a critical appraisal. Forum Nutr. – 2006; 59: . – P.86–115.
75. Schroecksnadel K., Frick B., Fiegl M. et al. Hyperhomocysteinaemia and immune activation in patients with cancer. //Clin Chem Lab Med. – 2007;45(1): . – P.47–53.
76. Stadler R., Kremer A. Therapeutic advances in cutaneous T–cell lymphoma (CTCL): from retinoids to rexinoids. //Semin Oncol. – 2006: Feb;33(1 Suppl 3): . – P.7–10.
77. Stirban A., Negrean М., Stratmann B. et al. Benfotiamine prevents macro– and microvascular endothelial dysfunction and oxidative stress following a meal rich in advanced glycation end products in individuals with type 2 diabetes. //Diabetes Care. . – 2006 Sep;29(9): . – P. 2064–2071.
78. Sundravel S., Shanthi P., Sachdanandam P. Therapeutic potential of riboflavin, niacin and ascorbic acid on carbohydrate metabolizing enzymes in secondary endometrial carcinoma bearing rats. //Mol Cell Biochem. – 2006 Aug;288(1–2): – P.73–78.
79. Swami S., Krishnan A.V., Moreno J. et al. Calcitriol and genistein actions to inhibit the prostaglandin pathway: potential combination therapy to treat prostate cancer. //J Nutr. – 2007 Jan;137(1): – P.205S–210S.
80. Tang Y., Zhou L., Gunnet J.W. et al. Enhancement of arachidonic acid signaling pathway by nicotinic acid receptor HM74A. // Biochem Biophys Res Commun. – 2006 Jun 23;345(1): – P.29–37.
81. Thompson J. Vitamins and minerals 4: overview of folate and the B vitamins. //Community Pract. –2006; Jun;79(6): – P.197–198.
82. Tricoire J., Claeyssens–Donadel S., Robert A. et al. Longitudinal evaluation of lymphocyte subsets and serum immunoglobulins in infants born to HIV seropositive mothers //Pediatrie. – 1993; 48(4): – P.283–286.
83. Tsimberidou A.M., Kantarjian H., Keating M.J., Estey E. Optimizing treatment for elderly patients with acute promyelocytic leukemia: is it time to replace chemotherapy with all–trans retinoic acid and arsenic trioxide? // Leuk Lymphoma. – 2006; Nov;47(11): – P.2282–2288.
84. Voss P., Siems W. Clinical oxidation parameters of aging. // Free Radic Res. –2006; Dec;40(12): – P.1339–1349.
85. Weinstein S.J., Stolzenberg–Solomon R. et al. Dietary factors of one–carbon metabolism and prostate cancer risk. // Am J Clin Nutr. – 2006 Oct;84(4): – P.929–935.
86. Whitehead V.M. Acquired and inherited disorders of cobalamin and folate in children.//Br J Haematol. – P.2006; Jul;134(2): – P.125–136.
87. Wright J.M. Oral precancerous lesions and conditions. // Semin Dermatol. – 1994; Jun;13(2): – P.125–131.
88. Wright T.I., Spencer J.M., Flowers F.P. Chemoprevention of nonmelanoma skin cancer. //J Am Acad Dermatol. – 2006; Jun;54(6): – P. 933–946.
89. Wu K.L., Beksac M., van Droogenbroeck J., Amadori S. et al. Phase II multicenter study of arsenic trioxide, ascorbic acid and dexamethasone in patients with relapsed or refractory multiple myeloma. // Haematologica. – 2006; Dec;91(12): – P.1722–1723.
90. Wu S., Ren J. Benfotiamine alleviates diabetes–induced cerebral oxidative damage independent of advanced glycation end–product, tissue factor and TNF–alpha. // Neurosci Lett. – 2006; Feb 13;394(2): – P.158–162.
91. Xu W.H., Dai Q., Xiang Y.B., Zhao G.M. et al. Nutritional factors in relation to endometrial cancer: A report from a population–based case–control study in Shanghai, China. //Int J Cancer. – 2007; Jan 17; [PubMed – индексированный для MEDLINE in press].
92. You W.C., Brown L.M. Zhang L. et al. Randomized double–blind factorial trial of three treatments to reduce the prevalence of precancerous gastric lesions. //J Natl Cancer Inst. – 2006; Jul 19;98(14): – P.974–983.
Статьи
Опубликовано в журнале:
Российский журнал боли 2 2017
О.А. Громова1, Л.В. Стаховская3, И.Ю. Торшин2, М.В. Филимонова4, Е.А. Ковражкина3
1ФГБОУ ВО Ивановская государственная медицинская академия Минздрава России, Иваново, Россия;
2ФГАОУ ВО «Московский физико-технический институт (государственный университет)» (МФТИ), Москва, Россия;
3НИИ ЦВПиИ РНИМУ им. Н.И. Пирогова, Москва, Россия;
4Национальный медицинский исследовательский радиологический центр МЗ РФ, Москва, Россия
В неврологии витамин В12 используется для лечения болевого синдрома и восстановления миелина. Витамин В12 принципиально необходим для фолатного метаболизма и важен для обезвреживания гомоцистеина, метилирования ДНК, биосинтеза нуклеотидов, профилактики анемических состояний.
Нарушение протекания этих процессов, происходящее на фоне дефицита витамина В12 и других витаминов группы В, способствует канцерогенезу.
Показана перспективность использования препаратов витамина В12 в качестве адъювантной терапии у пациентов с опухолевыми заболеваниями, проходящих химиотерапию.
Ключевые слова:
цианкобаламин, гипергомоцистеинемия, тиамин, пиридоксин, фолаты, противоопухолевое действие.
On the antitumor potential of vitamin B12
O.A. Gromova1, L.V. Stakhovskaya3, I.Yu. Torshin2, M.V. Filimonova4, E.A. Kovrazhkina3
1Ivanovo State Medical Academy of the Ministry of Health of Russia
2”Moscow Institute of Physics and Technology (State University)” (MIPT)
3NII ZVPiI RNIMU him. N.I. Pirogova
4National Medical Research Radiological Center of the Ministry of Health of the Russian Federation
In neurology, vitamin B12 is used to treat pain syndrome and restore myelin sheath of the neurons. Vitamin B12 is essential for folate metabolism and is important for neutralizing homocysteine, DNA methylation, biosynthesis of nucleotides and prevention of anemic conditions. Violation of the course of these processes, taking place against a background of deficiency of vitamin B12 and other B vitamins, contributes to carcinogenesis.
The results of clinical studies show that the relationship between vitamin B12 and the risk of tumor diseases is mediated by such factors as the consumption of red meat, alcohol and deficiencies of B vitamins (primarily folates). The prospects of using vitamin B12 preparations as adjuvant therapy in patients with tumorous diseases undergoing chemotherapy are shown herewith.
Keywords:
cyanocobalamin, hyperhomocysteinemia, thiamine, pyridoxine, folate, antitumor effect.
Введение
Среди используемых в неврологии лекарственных средств витамин В12 (цианкобаламин и др.) и другие витамины группы В занимают особое место. Витамин В12 используется, прежде всего, для лечения болевого синдрома и восстановления миелиновых оболочек нервов. У пациентов с гиповитаминозом В12 отмечаются онемение или покалывание конечностей, атаксия, возможно возникновение стойкого парапареза нижних конечностей. Осмотр невролога часто выявляет нарушение чувствительности (болевой, тактильной, вибрационной), повышение сухожильных рефлексов, симптомы Ромберга и Бабинского, признаки периферической полиневропатии и фуникулярного миелоза. При тяжёлой В12-дефицитной анемии могут развиваться психические нарушения – бессонница, депрессия, психозы, галлюцинации, деменция [1].
Дефицит витамина B12 наиболее часто встречается у пациентов в пожилом и старческом возрасте. Дефицит витамина B12 у пожилых людей является проблемой во всем мире и затрагивает не менее 10–15% людей в возрасте старше 60 лет [2]. Атрофический гастрит, в т.ч. возрастной, является основной причиной дефицита B12 вследствие ухудшения всасывания витамина В12 из пищи [3]. Кроме того, гипохлоргидрия при атрофическом гастрите приводит к избыточному росту патогенных бактерий в желудке и тонком кишечнике, что не только приводит к дальнейшему ухудшению всасывания витамина В12, но и к захвату патогенными бактериями витамина В12 для собственных нужд [4].
Последствия дефицита витамина B12 в пожилом возрасте весьма разноплановы. Во-первых, при дефиците кофермента 5-дезоксиаденозилкобаламина накапливаются токсичные метилмалоновая и пропионовая кислоты, которые повреждают миелиновые оболочки, нейроны и провоцируют болевой синдром. Во-вторых, недостаток метилкобаламина нарушает синтез нуклеиновых кислот и метилирование ДНК, что приводит к расстройству образования и созревания эритроцитов, нарушению функции транспорта кислорода и, следовательно, к развитию анемического синдрома. В-третьих, нарушения фолатного метаболизма, обезвреживания гомоцистеина, метилирования ДНК, биосинтеза нуклеотидов, возникающие на фоне дефицита витамина В12, способствуют канцерогенезу [1].
Роль гиповитаминоза В12 как фактора канцерогенеза зачастую недооценивается. Между тем опухолевые заболевания (в частности, опухоли желудка и кишечника) сопровождаются дефицитом витамина B12. При этом, с одной стороны, было показано, что некоторые виды опухолей являются своего рода «ловушками» витамина В12, захватывая витамин из организма пациента и создавая недостаточность витамина В12 в организме. При распаде клеток таких опухолей у пациентов отмечаются кратковременные периоды повышения концентрации витамина В12 в плазме крови. С другой стороны, результаты многочисленных экспериментальных исследований указали на то, что витамин B12 может ингибировать рост опухолевых клеток. Данных о стимулирующем действии витамина B12 на рост опухолей не имеется [5].
Более того, витамины группы В проявляют противоопухолевые эффекты. Например, витамин B12, тиамин, рибофлавин, фолиевая кислота защищают от возникновения плоскоклеточного рака шейки матки [6]. Другой пример – при сниженных уровнях витамина B12 в сыворотке крови у женщин в постменопаузе риск развития рака молочной железы достоверно повышается [7]. Адъювантная терапия витаминами группы В снижает тяжелые токсические осложнения при проведении химиотерапии у пациентов с немелкоклеточным раком легкого препаратом пеметрексед за счет снижения гипергомоцистеинемии и уровней метилмалоната в крови [8].
В то же время у врачей может отмечаться своего рода «фобия» к использованию препаратов витамина В12 у пожилых пациентов и в особенности у пациентов с уже имеющимся онкологическим диагнозом. Ядром этой «фобии» являются вольные интерпретации повышенного уровня витамина В12 в сыворотке крови. Нельзя забывать, что повышенные уровни витамина В12 (более 650 пмоль/л) могут возникать вследствие многочисленных причин: распад тканей печени при остром и хроническом гепатите, циррозе печени, эритролейкемии, миелолейкозе, опухоли печени, метастазов печени, хронической почечной недостаточности, повышенных уровней белка-транспортера витамина В12 (транскобаламина) и др. [1].
При этом эпизоды повышения уровня витамина В12 в сыворотке крови могут наблюдаться даже при дефиците витамина В12 в тканях организма (в первую очередь в печени). Поэтому однократные измерения уровней витамина В12 в сыворотке малоинформативны, и только оценка динамики уровней витамина В12 позволяет делать гораздо более обоснованные выводы. Игнорирование многообразия возможных причин, приводящих к повышению уровней витамина В12 в сыворотке крови, как раз и порождает необоснованные опасения вроде «препараты витамина В12 стимулируют развитие опухолей».
Анализ взаимосвязей между обеспеченностью организма витамином В12 и риском опухолевых заболеваний не может быть рассмотрен в отрыве от фактов, указывающих на важность витамина В12 и др. витаминов группы В в качестве факторов противоопухолевой защиты организма, без учета результатов фундаментальных исследований взаимосвязи дефицита витамина В12 и риска развития опухолевых заболеваний, а также без анализа факторов, «вмешивающихся» в ассоциацию между витамином В12 и риском возникновения опухолевых заболеваний. Все эти направления рассмотрены далее в настоящей статье. Показана перспективность использования препаратов витамина В12 у пациентов с опухолевыми заболеваниями.
Витамины группы В как факторы противоопухолевой защиты организма
Витамин В12 проявляет свои биологические свойства в контексте других витаминов группы В. Прежде всего, следует отметить, что метаболизм фолатов осуществляется при участии витаминов В2, B6, B12 и необходим не только для эпигенетического метилирования геномной ДНК и обезвреживания гомоцистеина, но также для процессов синтеза и репарации ДНК, в особенности синтеза пуринов и пиримидинов. Следовательно, обеспеченность организма этими витаминами существенно влияет на процессы канцерогенеза [9].
Одним из наиболее явных проявлений дефицита витаминов В12, В6 и фолатов является повышение уровней гомоцистеина, который является доказанным фактором риска цереброваскулярной патологии и, кроме того, повышается при опухолевых заболеваниях. Например, средний уровень общего гомоцистеина у пациентов с ларингеальной карциномой (n=25) составил 2,84±1,62 мг/л, в контрольной группе (n=80) – 0,99±0,24 мг/л (p<0,001) [10].
Восполнение дефицита витаминов группы В у пациентов способствует устранению гипергомоцистеинемии и снижает риск возникновения опухолевых заболеваний. Уровни рибофлавина и витамина B6 в плазме крови обратно пропорциональны риску развития рака груди у женщин 35–5 лет: повышение уровня этих витаминов в плазме крови снижает риск заболевания до 50% [11]. Анализ баз данных медицинской документации за 1993–998 гг. (проанализировано 63 257 мужчин и женщин в возрасте 45–74 лет) показал, что более высокие уровни потребления витамина B6 и холина были связаны со статистически значимым снижением риска развития рака поджелудочной железы (витамин B6: ОР 0,52, 95% ДИ 0,36–0,74, р=0,001, холин: ОР 0,67, 95% ДИ 0,48–0,93, р=0,04) [12].
Фолаты в количестве 224–54 мкг/сут, особенно в сочетании с витамином B12 (2,6–7,5 мкг/сут) достоверно снижают риск развития рака молочной железы у женщин в постменопаузе [13]. У детей 3–14 лет более высокое потребление фолиевой кислоты ассоциировано с уменьшением риска опухолей мозга (0,63, 95% ДИ 0,41–0,97) [14]. В метаанализе 47 когортных исследований более высокое потребление фолатов (ОР 0,88, 95% ДИ 0,81–0,95), витамина D (ОР 0,87, 95% ДИ 0,77–0,99), витамина B6 (ОР 0.88, 95% ДИ 0,79–0,99), витамина В2 (ОР 0,86, 95% ДИ 0,76–0,97), витамин А (0,87, 95% ДИ 0,75–1,03) и витамина С (ОР 0,92 95% ДИ 0,80–1.06) были ассоциированы с более низким риском колоректального рака [15]. В крупномасштабном исследовании значительной когорты участников (n=492 293) повышенный риск плоскоклеточного рака пищевода был ассоциирован с низким потреблением фолатов (ОР 1,91, 95% ДИ 1,17–3,10), тогда как потребление витаминов B6 и витамина B12 не влияло на риск заболевания [16].
Фундаментальные исследования взаимосвязи дефицита витамина В12 и риска развития опухолевых заболеваний
Витамин В12 является принципиально важным кофактором биосинтеза молекул-источников метильных групп (например, S-аденозилметионина) для метилирования ДНК и способствует переработке метилфолата в процессе биосинтеза нуклеотидов. Дефицит витамина В12, как известно, индуцирует гипергомоцистеинемию, нарушает процессы биосинтеза и метилирования ДНК. В12-дефицитная диета способствует развитию анемических состояний, нарушает фолатный гомеостаз, приводит к уменьшению геномного метилирования ДНК и увеличению числа ошибочных включений урацила в последовательность ДНК. Все перечисленные механизмы напрямую способствуют канцерогенезу [1, 5, 17].
Реметилирование гомоцистеина в метионин, катализируемое B12-зависимым ферментом метионин синтазой (МС), играет важную роль в метаболизме метильной группы и метионина. Получающийся из гомоцистеина метионин преобразуется в S-аденозилметионин, который и является молекулой-источником метильной группы для реакций метилирования ДНК, РНК, липидов, белков и других молекул [18] (рис. 1).
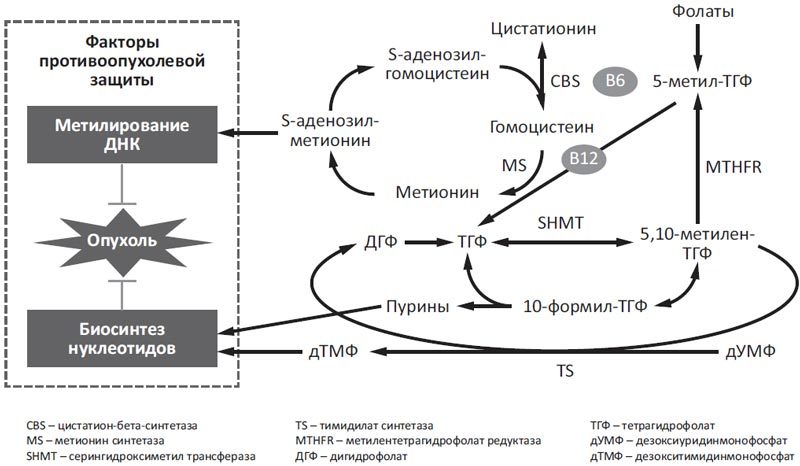
Рисунок 1
Витамин B12 в фолатном обмене веществ.
Дефицит витамина B12, кофактора метионин синтазы, стимулирует дисбаланс метилфолата и последующие изменения в метилировании ДНК и биосинтезе нуклеотидов.
Ферментативно-активные производные витамина В12, метилкобаламин и 5’-деоксиаденозилкобаламин, значительно увеличивают время выживания мышей с внутрибрюшинной имплантацией опухолевых клеток [19]. Витамин B12 в сочетании с тиоловыми антиоксидантами глутатионом и N-ацетилцистеином индуцирует апоптоз клеток лимфоцитарного лейкоза человека. Цитотоксический эффект тормозился ингибиторами каспаз и железо-хелатирующим агентом дефероксамином. Таким образом, апоптоз клеток лимфоцитарного лейкоза человека может быть вызван железо-зависимой дестабилизацией лизосом [20].
Кобаламин потенцирует противоопухолевое действие химиотерапевтического препарата винбластин посредством снижения экспрессии гена MDR-1 в опухолевой линии клеток HepG2. P-гликопротеин, синтезируемый из гена MDR-1 (ген «множественной лекарственной устойчивости-1»), является одним из основных механизмов защиты клеток опухолей от противораковых препаратов. Добавление кобаламина в клетки привело к увеличению активности метионин синтетазы и к значительному снижению экспрессии гена MDR-1. Иными словами, витамин В12 увеличил чувствительность опухолевых клеток к химиотерапии винбластином. Кроме того, кобаламин усиливал чувствительность клеток к винбластину и предотвращал метотрексат-индуцированное повышение экспрессии гена MDR-1 [21]. В результате применения комбинации «винбластин+витамин В12» гибель опухолевых клеток возрастала (рис. 2).
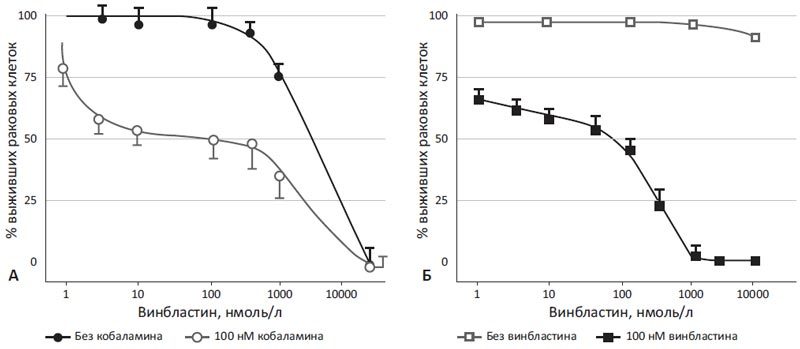
Рисунок 2
Химиочувствительность клеток HepG2:
А – винбластин был добавлен на 48 ч в концентрациях от 1 нМ до 30 мкМ к клеткам, предварительно инкубированным со 100 нМ кобаламина в течение 24 ч (светлые кружки) или без добавления кобаламина (темные кружки);
Б – повышение концентрации кобаламина в отсутствии винбластина (светлые квадраты) или в присутствии 100 нМ дозы винбластина (темные квадраты).
Установлено, что комбинация витаминов В1, В6, В12 (в виде тиамина дисульфида, пиридоксина гидрохлорида и цианкобаламина в составе препарата Нейробион) в дозе 110 мг/кг/сут обладает противоопухолевым эффектом. При субхроническом внутрижелудочном введении животным-опухоленосителям (мыши-гибриды F1) в течение 3 нед наблюдалась устойчивая тенденция к торможению роста карцинома лёгких Льюис (в среднем, на 10…20%), причем препарат Нейробион не влиял на метастазирование опухолей. Таким образом, результаты данного экспериментального исследования указывают на то, что комбинация витаминов В1, В6, В12 проявляет слабо выраженный, но достоверный противоопухолевый эффект (р=0,0062 по тесту Колмогорова-Смирнова) [22].
Витамин В12 и «вмешивающиеся» факторы, влияющие на риск опухолевых заболеваний: результаты клинических исследований
Как было отмечено выше, повышенные уровни сывороточного кобаламина могут быть признаком тяжелой патологии, сопровождающейся массивной гибелью клеток печени или клеток крови. Например, некоторые заболевания печени (острый гепатит, цирроз печени, гепатоцеллюлярная карцинома, метастатические заболевания печени) сопровождаются периодами нарастания концентрации кобаламина в сыворотке крови пациентов. Это явление обусловлено потерями кобаламина при цитолизе гепатоцитов или снижением клиренса кобаламина при дисфункции печени, нарушении желчевыведения, при дисфункции почек. Гематологические расстройства (хронический миелогенный лейкоз, промиелоцитарный лейкоз, полицитемия, гиперэозинофильный синдром) также ассоциированы с повышенными уровнями кобаламина [5].
В частности, скрининговое исследование пациентов многопрофильных стационаров (n=818) показало, что аномально высокие уровни кобаламина в сыворотке достоверно ассоциированы с рядом диагнозов. В исследование вошли пациенты старше 18 лет с низкими (<200 пмоль/л, n=200), нормальными (200–600 пмоль/л, n=202) высокими (601–1000 пмоль/л, n=217) и очень высокими (>1000 пмоль/л, n=199) уровнями кобаламина в крови. Для сахарного диабета 2-го типа установлен небольшой защитный эффект более высоких уровней B12 в сыворотке крови. С очень высокими уровнями B12 в сыворотке крови были ассоциированы алкоголизм (ОР 5,74, 95% ДИ 2,76–11,96), заболевания печени (ОР 8,53, 95% ДИ 3,59–20,23) и опухолевые заболевания (ОР 5,48, 95% ДИ 2,85–10,55) [23] (табл. 1).
Таблица 1
Ассоциации между уровнями витамина В12 в крови, указывающими на степень цитолиза клеток, и различными патологиями. Результаты получены при скрининговом обследовании пациентов многопрофильных стационаров [23].
| Заболевания | 200–600 пмоль/л | 601–1000 пмоль/л | 1000 пмоль/л |
|---|---|---|---|
| Алкоголизм | 1,59 (0,77–3,30) | 3,96 (2,02–7,78) | 5,74 (2,81–11,75) |
| Заболевания печени | 1,66 (0,67–4,11) | 3,63 (1,57–8,41) | 7,76 (3,33–18,08) |
| Раковые заболевания | 1,51 (0,80–2,85) | 1,45 (0,74–2,82) | 6,45 (3,41–12,19) |
| Заболевания почек | 1,19 (0,52–2,72) | 2,20 (1,01–4,77) | 1,30 (0,49–3,47) |
| Аутоиммунные заболевания | 0,78 (0,36–1,72) | 0,95 (0,43–2,09) | 1,23 (0,52–2,92) |
| Бронхолегочные заболевания | 1,34 (0,75–2,38) | 1,67 (0,93–2,98) | 2,49 (1,33–4,66) |
| Сердечно-сосудистые заболевания | 1,06 (0,64–1,78) | 1,07 (0,62–1,82) | 1,68 (0,94–3,01) |
| Психические заболевания | 1,20 (0,76–1,90) | 1,30 (0,81–2,10) | 0,74 (0,40–1,36) |
| Сахарный диабет 2-го типа | 0,72 (0,40–1,31) | 0,49 (0,25–0,98) | 0,81 (0,39–1,66) |
| Неврологические заболевания | 0,76 (0,42–1,37) | 1,28 (0,73–2,25) | 1,69 (0,91–3,13) |
| Заболевания ЖКТ | 0,91 (0,58–1,45) | 1,35 (0,85–2,15) | 0,95 (0,54–1,68) |
Группа пациентов с опухолевыми заболеваниями была подразделена на три подгруппы, соответствующие миелоидным, лимфатическим и солидным (твердым) опухолям. Для этих трех подтипов опухолей была отмечена более частая встречаемость очень высоких уровней витамина B12 (более 1000 пмоль/л), что указывало на активное протекание цитолиза клеток опухолей и высвобождение витамина В12 в кровь [23].
В ряде исследований, проведенных в Дании, было подтверждено наличие повышенных уровней витамина В12 в крови у пациентов с опухолевыми заболеваниями. Например, в когорту, включающую данные медицинских реестров (1998–2014), входила информация о 25 017 пациентах с опухолевыми диагнозами и с уровнями B12, измеренными за 1 год до установления диагноза. Вероятность выживания была ниже среди пациентов с повышенным уровнем B12 (200–600 пмоль/л: 69%, 601–800 пмоль/л: 50%, >800 мкмоль/л: 36%, контроль – 72%) [24]. При метаанализе данных для пациентов из 6 когорт (суммарно, 6 875 случаев рака простаты и 8 104 участника в контрольной группе) было показано, что более высокие концентрации фолатов и витамина B12 в сыворотке крови ассоциированы с небольшим увеличением риска рака простаты: фолаты – на 13% (95% ДИ 2–26%, р=0,018), витамин B12 – на 12% (95% ДИ 1–25%, р=0,017) [25] (рис. 3).
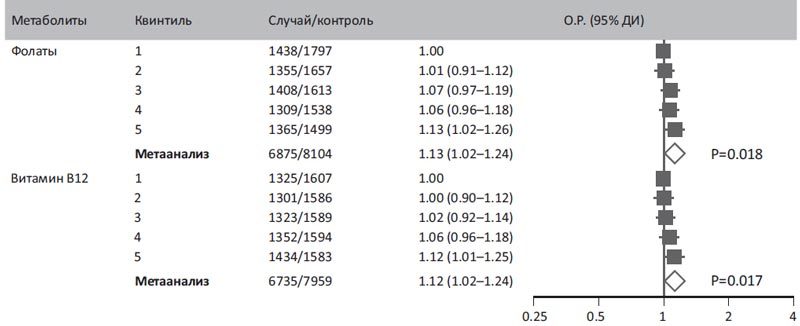
Рисунок 3
Отношение шансов и 95% доверительные интервалы для метаанализа исследований по взаимосвязи рака простаты и уровней фолатов и витамина B12 в сыворотке крови.
Однако само по себе установление статистически достоверной ассоциации между повышенными уровнями витамина В12 в сыворотке/плазме крови и наличием у пациентов опухолевых заболеваний не позволяет сделать никаких практически важных выводов. Это обусловлено тем, что при установлении такого рода «однобоких» ассоциаций исследователи зачастую пренебрегают другими факторами. Например, несмотря на достаточно большой суммарный размер датской когорты (более 14 900 участников) в метаанализе [25], данную работу отличают многочисленные грубые ошибки в анализе данных. Из наиболее вопиющих ошибок следует отметить, во-первых, практически полное отсутствие анализа подгрупп пациентов и, во-вторых, отсутствие адекватного анализа взаимозависимости между другими факторами, имеющимися в наличии у пациентов (в частности, наличие диеты и употребления алкоголя) и риском развития рака.
Важно отметить, что в тексте статьи [25] не встречается даже упоминания о диетических факторах вообще, не говоря о более детальных факторах риска опухолей (таких, как употребление красного мяса и копченостей). В то же время, потребление красного мяса является весьма важным фактором, обеспечивающим взаимосвязь риска опухолевых заболеваний и обеспеченности организма витамином В12.
Как известно, мясо является не только важным источником белка и железа, но и источником витамина B12. С другой стороны, высокий уровень потребления красного и переработанного мяса ассоциирован с повышенным риском развития диабета 2-го типа, опухолей (в частности, ободочной/прямой кишки, простаты и др.) и смертности. Здоровыми альтернативами мясу являются рыба, орехи, овощи и фрукты, бобовые [1, 26].
Поскольку при проведении метаанализа [25] не были проведены адекватный анализ подгрупп и анализ эффектов диетических факторов, то установление ассоциации между риском рака простаты и более высокой концентрацией витамина B12 в плазме крови может иметь весьма тривиальный характер. А именно, более высокое потребление красного мяса (которое, подчеркнём, является доказанным фактором риска опухолей простаты) приводит одновременно и к повышению риска заболевания, и к повышению уровней витамина В12 в крови.
Учет диетарного потребления мяса может приводить к «исчезновению» ассоциации между повышенными уровнями витамина В12 и раковыми заболеваниями. Например, более высокое диетарное потребление фолиевой кислоты и/или витамина B6 ассоциировано с более низким риском рака носоглотки (фолаты ОР 0,66, 95% ДИ 0,48–0,91, р<0,001, витамин B6: ОР 0,72, 95% ДИ 0,52–1,00, р<0,001), в то время как для витамина В12 не было установлено значимых ассоциаций [27]. В данном исследовании диетарное потребление мяса было принято во внимание: по сравнению с контрольной группой пациенты с установленным диагнозом потребляли большее количество мяса (рак носоглотки – 240 г/сут, 95% ДИ 27–802 г/сут, контроль – 216 г/сут, 95% ДИ 14–583, р<0,001) на фоне более низкого потребления свежих овощей и фруктов.
Потребление красного мяса также было учтено в метаанализе 5 наблюдательных исследований, в котором суммарно были проанализированы данные 133 995 пациентов, в т.ч. 2 441 случай рака почки. С поправкой на потребление мяса, сравнение подгруппы пациентов с более высокими уровнями витамина B12 в сыворотке крови с подгруппой с самыми низкими уровнями риск развития рака был ниже на 28% (ОР 0,72, 95% ДИ 0,52–1,00, р=0,048). Заметим, что более высокие уровни в сыворотке витамина B6 (ОР 0,83, 95% ДИ 0,77–0,89, p<0,001) и витамина В2 (увеличение на каждые 5 нмоль/л связано с 6%-ым снижением риска, ОР 0,94, 95% ДИ 0,89–1,00, р=0,045) также способствуют снижению риска рака почки [28].
Помимо потребления красного мяса, существуют и другие факторы, которые также могут «вмешиваться» в ассоциацию между витамином В12 и риском опухолевых заболеваний. Например, сравнение группы пациенток c подтвержденным раком молочной железы (n=2 491) с контрольной группой (n=2 521) показало, что у женщин, потребляющих алкоголь выше среднего уровня, наблюдаются более высокие уровни витамина B12 и больший риск заболевания (ОР 1,26; 95% ДИ 1,00–1,58; р=0,05). Данная ассоциация вполне очевидна: под воздействием алкоголя происходит частичная гибель гепатоцитов (что приводит к повышению уровней витамина В12 в сыворотке) и одновременно повышается риск рака молочной железы (вследствие токсических примесей в составе алкогольных продуктов и канцерогенного действия метаболитов этанола). Ассоциация между уровнями В12 и повышением риска заболевания также отмечена у участниц с пониженными уровнями фолатов в плазме крови (ОР 1,29; 95% ДИ 1,02–1,62, р=0,03) [29].
Различия между дизайном исследований (проспективные или рандомизированные исследования), включенных в метаанализ, могут являться существенным фактором, влияющим на достоверность ассоциаций между уровнями витамина В12 в крови и риском опухолевых заболеваний. Например, метаанализ эпидемиологических исследований показал, что более высокие уровни витамина B12 в сыворотке не были ассоциированы с риском рака молочной железы (ОР 0,73, ДИ 0,44–1,22, р=0,23). В то же время значимое снижение риска при более высоких уровнях витамина B12 в сыворотке было установлено для исследований типа «случай–контроль» (ОР 0,74, 95% ДИ 0,56–0,98, р=0,04), но не для проспективных исследований. Метаанализ также подтвердил, что более высокие уровни пиридоксаль-5’-фосфата (активная форма витамина B6) в сыворотке достоверно ассоциированы со сниженным риском рака молочной железы [30] (рис. 4).
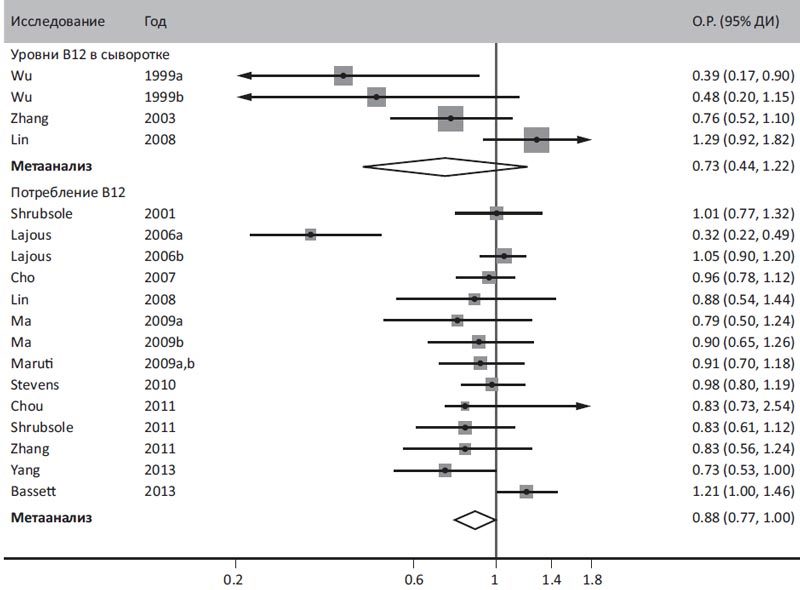
Рисунок 4
Риск рака молочной железы снижается при более высоких уровнях витамина B12 в сыворотке крови и при более высоком потреблении витамина В12.
В целом результаты клинико-эпидемиологических исследований и метаанализов не позволяют сделать вывод об «онкогенности» витамина В12 и других витаминов группы В. Более того, канцерогенез может быть ассоциирован с недостаточной обеспеченностью тканей организма витаминами В6 и В12. Например, метаанализ 17 исследований (n=10 601) указал на дозозависимую ассоциацию между диетарным потреблением витамина B12 и риском развития колоректального рака: прирост ежесуточного потребления витамина B12 каждые 4,5 мкг/сут соответствовал снижению риска заболевания на 4% (ОР 0,96, 95% ДИ 0,93–1,00, р<0,001) [31] (рис. 5, 6).
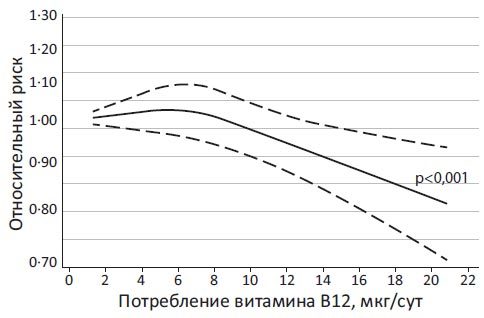
Рисунок 5
Дозозависимая ассоциация между суточным потреблением витамина B12 и риском развития колоректального рака.
Сплошная линия – относительный риск, пунктирная – границ 95% ДИ.
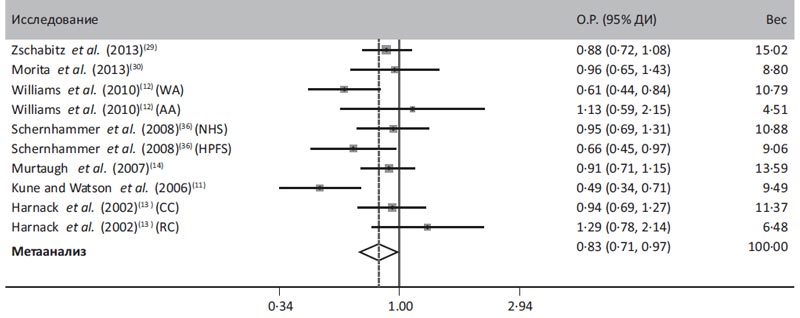
Рисунок 6
Метаанализ относительного риска колоректального рака указал на снижение риска заболевания при более высоком потреблении витамина B12 (>8 мкг/сут). ОР и 95% ДИ представлены черной точкой и горизонтальной линией соответственно; площадь серого квадрата пропорциональна весу исследования в метаанализе.
Об использовании препаратов витамина В12 у пациентов с опухолевыми заболеваниями
Витамин В12 и фолаты применяются для компенсации глубоких дефицитов этих микронутриентов у пациентов с опухолевыми заболеваниями. Например, дефицит витамина B12 и гипергомоцистеинемия характерны для пациентов после хирургического удаления рака желудка. Установлено, что степень резекции желудка является независимым фактором риска дефицита витамина B12. В то время как уровни сывороточного B12 у пациентов были значительно ниже (221±126 пг/мл), чем у здоровых (309±174 пг/мл, р=0,002), уровни гомоцистеина были значительно выше у пациентов с карциномой желудка (14±7 мкмоль/л, контроль – 12,5±6,1 мкмоль/л, р=0,016) [32]. В группе 645 пациентов, перенесших дистальную субтотальную резекцию желудка (ДР, N=469) или тотальную гастроэктомию (ТГ, n=176) дефицит витамина В12 установлен у 100% для ТГ и у 16% для ДР через 4 года после операции (р<0,001). Таким образом, дефицит витамина B12 является неизбежным метаболическим осложнением гастроэктомии.
Глубокий дефицит витамина В12, который присутствует в пациентов после тотальной гастроэктомии в связи с опухолевыми заболеваниями желудка, сопровождается соответствующими неврологическими симптомами. Пациенты с дефицитом витамина В12 (<200 пг/мл, n=30) получали перорально витамин В12 (1500 мкг/сут) в течение 3-х мес. До начала лечения у 29 пациентов отмечены неврологические симптомы, характерные для гиповитаминоза B12. После курсового приема витамином B12, 28 из 29 пациентов испытали облегчение симптомов, а у 16 пациентов симптомы полностью регрессировали [33] (рис. 7).
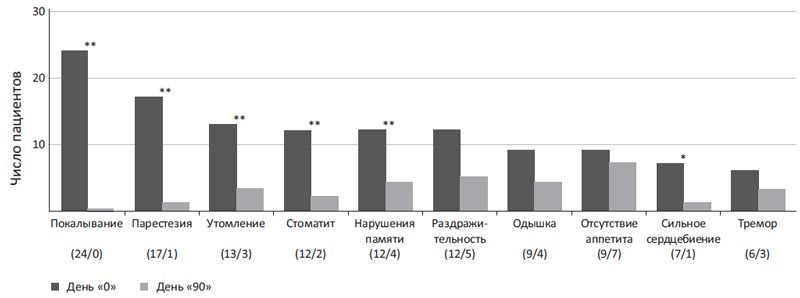
Рисунок 7
Неврологические симптомы до и после перорального приема витамина B12.
Числа в скобках указывают количество пациентов, которые испытали симптом до начала лечения и после прекращения лечения. «*», р<0,05 по тесту МакНамара; «**», р<0,01.
У пациентов, страдающих раком прямой кишки (n=37), проводилось лечение пеметрекседом (500 мг/сут) за 3 нед до операции, что существенно снижало уровни фолатов и В12 в биоптатах опухолевой ткани и в прилегающей слизистой оболочке. Адъювантная терапия фолиевой кислотой и витамином B12 per os не приводила к каким-либо нежелательным эффектам и позволяла компенсировать развивающиеся у пациентов глубокие дефициты витамина В12 и фолатов [34].
Таким образом, препараты витамина В12 могут быть весьма эффективны и безопасны для компенсации дефицита витамина В12, в частности, после резекции желудка. Заметим, что мальабсорбция витамина B12 также происходит после тазового облучения при гинекологических опухолях (как следствие возникающей при этом энтеропатии) [35].
Фолиевая кислота и витамин B12 играют решающую роль в снижении риска тяжелых форм интраэпителиальной неоплазии шейки матки, вызываемой папилломавирусом человека. При исследовании HPV16-положительных женщин (n=315) участницы с более высокими уровнями витамина B12 в плазме крови характеризовались снижением риска рака шейки матки 2-ой, 3-ей, 4-ой стадий заболевания на 60% (р=0,02) [36].
У пациентов с опухолевыми заболеваниями и гиперинсулинемией часто используется метформин. Метаанализ 6 рандомизированных контролируемых исследований показал, что метформин (особенно в дозах свыше 2000 мг/сут) вызывает недостаточность витамина B12 [37] (рис. 8), которая также должна компенсироваться препаратами витамина В12.
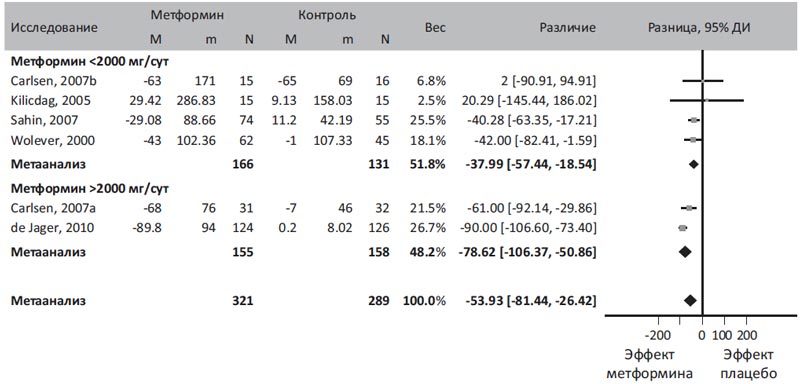
Рисунок 8
Влияние метформина на концентрацию витамина B12.
Заключение
Витамин В12 принципиально необходим для фолатного метаболизма, обезвреживания гомоцистеина, метилирования ДНК, биосинтеза нуклеотидов и профилактики анемических состояний. Нарушение протекания этих процессов, происходящее на фоне дефицита витамина В12 и др. витаминов группы В, способствует канцерогенезу. Результаты клинических исследований показывают, что взаимосвязь между уровнем витамина В12 в организме и риском опухолевых заболеваний опосредуется такими факторами, как потребление красного мяса, алкоголя и дефицитом других витаминов группы В (прежде всего, фолатов). Показана перспективность использования препаратов витамина В12 у пациентов с опухолевыми заболеваниями, проходящими химиотерапию.
Список литературы
- Ребров В.Г., Громова О.А. Витамины, микро- и макроэлементы. М., ГэотарМед, 2008, 956 с.
- Baik H.W., Russell R.M. Vitamin B12 deficiency in the elderly. Annu Rev Nutr. 1999; 19: 357–377.
- King C.E., Leibach J., Toskes P.P. Clinically significant vitamin B12 deficiency secondary to malabsorption of proteinbound vitamin B12. Dig Dis Sci. 1979; 24(5): 397–402.
- Suter P.M., Golner B.B., Goldin B.R., et al. Reversal of protein-bound vitamin B12 malabsorption with antibiotics in atrophic gastritis. Gastroenterology. 1991; 101(4): 1039–1045.
- Volkov I. The master key effect of vitamin B12 in treatment of malignancy – a potential therapy? Med Hypotheses. 2008; 70(2): 324–8 Epub 2007 Jul.
- Hernandez B.Y., McDuffie K., Wilkens LR, et al. Diet and premalignant lesions of the cervix: evidence of a protective role for folate, riboflavin, thiamin, and vitamin B12. Cancer Causes Control. 2003; 14(9): 859–870.
- Wu K., Helzlsouer K.J., Comstock G.W., et al. A prospective study on folate, B12, and pyridoxal 5’-phosphate (B6) and breast cancer. Cancer Epidemiol Biomarkers Prev. 1999; 8(3): 209–217.
- Nakagawa K., Kudoh S., Matsui K., et al. A phase I study of pemetrexed (LY231514) supplemented with folate and vitamin B12 in Japanese patients with solid tumours. Br J Cancer. 2006; 95(6): 677–82 Epub 2006 Au.
- Gruber B.M. B-Group Vitamins: Chemoprevention? Adv Clin Exp Med. 2016; 25(3): 561–8 doi.
- Nacci A., Dallan I., Bruschini L., et al. Plasma homocysteine, folate, and vitamin B12 levels in patients with laryngeal cancer. Arch Otolaryngol Head Neck Surg. 2008; 134(12): 1328–33 doi.
- Agnoli C., Grioni S., Krogh V., et al. Plasma Riboflavin and Vitamin B-6, but Not Homocysteine, Folate, or Vitamin B-12, Are Inversely Associated with Breast Cancer Risk in the European Prospective Investigation into Cancer and Nutrition-Varese Cohort. J Nutr. 2016; 146(6): 1227–34 doi.
- Huang J.Y., Butler L.M., Wang R., et al. Dietary Intake of One-Carbon Metabolism-Related Nutrients and Pancreatic Cancer Risk: The Singapore Chinese Health Study. Cancer Epidemiol Biomarkers Prev. 2016; 25(2): 417–24 doi.
- Lajous M., Lazcano-Ponce E., Hernandez-Avila M., et al. Folate, vitamin B(6), and vitamin B(12) intake and the risk of breast cancer among Mexican women. Cancer Epidemiol Biomarkers Prev. 2006; 15(3): 443–448.
- Greenop K.R., Miller M., Bailey H.D., et al. Childhood folate, B6, B12, and food group intake and the risk of childhood brain tumors: results from an Australian case-control study. Cancer Causes Control. 2015; 26(6): 871–9 doi.
- Liu Y., Yu Q., Zhu Z., et al. Vitamin and multiple-vitamin supplement intake and incidence of colorectal cancer: a metaanalysis of cohort studies. Med Oncol. 2015; 32(1): 434 doi.
- Xiao Q., Freedman N.D., Ren J., et al. Intakes of folate, methionine, vitamin B6, and vitamin B12 with risk of esophageal and gastric cancer in a large cohort study. Br J Cancer. 2014; 110(5): 1328–33 doi.
- Friso S., Choi S.W. The potential cocarcinogenic effect of vitamin B12 deficiency. Clin Chem Lab Med. 2005; 43(10): 1158–1163.
- Choi S.W., Mason J.B. Folate and carcinogenesis: an integrated scheme. J Nutr. 2000; 130(2): 129–132.
- Tsao C.S., Myashita K. Influence of cobalamin on the survival of mice bearing ascites tumor. Pathobiology. 1993; 61(2): 104–108.
- Solovyeva M.E., Faskhutdinova A.A., Solovyev V.V., Akatov V.S. Thiol antioxidants in combination with vitamin B12 induce apoptotic death of human lymphocytic leukemia cells by destabilization of lysosomes with the involvement of iron ions. Bull Exp Biol Med. 2013; 154(4): 449–452.
- Marguerite V., Beri-Dexheimer M., Ortiou S., et al. Cobalamin potentiates vinblastine cytotoxicity through downregulation of mdr-1 gene expression in HepG2 cells. Cell Physiol Biochem. 2007; 20(6): 967–976.
- Громова О.А., Стаховская Л.В., Торшин И.Ю. и др. Противоопухолевые эффекты сочетанного применения витаминов В1, В6 и В12. Неврология, психиатрия, психосоматика, № 2, 2017, 53–58.
- Arendt J.F., Nexo E. Cobalamin related parameters and disease patterns in patients with increased serum cobalamin levels. PLoS One. 2012; 7(9): e45979 doi.
- Arendt J.F., Farkas D.K., Pedersen L., et al. Elevated plasma vitamin B12 levels and cancer prognosis: A populationbased cohort study. Cancer Epidemiol. 2016; 40: 158–65 doi.
- Price A.J., Travis R.C., Appleby P.N., et al. Circulating Folate and Vitamin B12 and Risk of Prostate Cancer: A Collaborative Analysis of Individual Participant Data from Six Cohorts Including 6875 Cases and 8104 Controls. Eur Urol. 2016; 70(6): 941–951 doi.
- Ekmekcioglu C., Wallner P., Kundi M., et al. Red meat, diseases and healthy alternatives: A critical review. Crit Rev Food Sci Nutr. 2016; Crit Rev F:0.
- Zeng F.F., Liu Y.T., Lin X.L., et al. Folate, vitamin B6, vitamin B12 and methionine intakes and risk for nasopharyngeal carcinoma in Chinese adults: a matched case-control study. Br J Nutr. 2016; 115(1): 121–8 doi.
- Mao B., Li Y., Zhang Z., et al. One-Carbon Metabolic Factors and Risk of Renal Cell Cancer: A Meta-Analysis. PLoS One. 2015; 10(10): e0141762 doi.
- Matejcic M., de Batlle J., Ricci C., et al. Biomarkers of folate and vitamin B12 and breast cancer risk: Report from the EPIC cohort. Int J Cancer. 2016; Int J Canc: 101002/ijc30536.
- Wu W., Kang S., Zhang D. Association of vitamin B6, vitamin B12 and methionine with risk of breast cancer: a dose-response meta-analysis. Br J Cancer. 2013; 109(7): 1926–44 doi.
- Sun N.H., Huang X.Z., Wang S.B., et al. A dose-response meta-analysis reveals an association between vitamin B12 and colorectal cancer risk. Public Health Nutr. 2016; 19(8): 1446–56 doi.
- Bilici A., Sonkaya A., Ercan S., et al. The changing of serum vitamin B12 and homocysteine levels after gastrectomy in patients with gastric cancer: do they associate with clinicopathological factors? Tumour Biol. 2015; 36(2): 823–8 doi.
- Kim H.I., Hyung W.J., Song K.J., et al. Oral vitamin B12 replacement: an effective treatment for vitamin B12 deficiency after total gastrectomy in gastric cancer patients. Ann Surg Oncol. 2011; 18(13): 3711–7 doi.
- Stoffregen C.C., Odin E.A., Carlsson G.U., et al. Reduced folate and serum vitamin metabolites in patients with rectal carcinoma: an open-label feasibility study of pemetrexed with folic acid and vitamin B12 supplementation. Anticancer Drugs. 2016; 27(5): 439–46 doi.
- Snijders-Keilholz A., Griffioen G., Davelaar J., et al. Vitamin B12 malabsorption after irradiation for gynaecological tumours. Anticancer Res. 1993; 13(5C): 1877–1881.
- Piyathilake C.J., Macaluso M., Chambers M.M., et al. Folate and vitamin B12 may play a critical role in lowering the HPV 16 methylation-associated risk of developing higher grades of CIN. Cancer Prev Res (Phila). 2014; 7(11): 1128–37 doi.
- Liu Q., Li S., Quan H., Li J. Vitamin B12 status in metformin treated patients: systematic review. PLoS One. 2014; 9(6): e100379 doi.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
