
ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ. ВОЗМОЖНЫ ПОБОЧНЫЕ ЭФФЕКТЫ. НЕОБХОДИМА КОНСУЛЬТАЦИЯ СПЕЦИАЛИСТА.
Автор статьи
Профессия: провизор
Название вуза: Пермская государственная фармацевтическая академия (ПГФА)
Специальность: фармация
Стаж работы: 2 года 8 месяцев
Диплом о фармацевтическом образовании: 105924 3510926 , рег. номер 32018
Места работы: провизор в аптеке, провизор сервиса Мегаптека
Все авторы
Содержание
- РЛС
- Состав
- От чего помогают таблетки
- Побочные действия
- Диувер (Торасемид) или Тригрим: что лучше
- Тригрим или Индапамид: что лучше
- Тригрим или Верошпирон: что лучше
- Краткое содержание
Согласно современным исследованиям, артериальная гипертензия затрагивает 30-45% взрослого населения. При этом значительная часть людей не подозревает о наличии заболевания. Лечением же охвачено менее половины гипертоников.
Человек может не ощущать симптомов повышенного артериального давления до момента развития критических показателей. Обнаружить проблему на начальной стадии можно только путем измерения. Без лечения заболевание прогрессирует, приводя к серьезным последствиям: ишемической болезни сердца, хронической сердечной недостаточности, инсульту или инфаркту.
Провизор расскажет о препарате Тригрим: ознакомит с его составом, показаниями к применению и побочными действиями, а также сравнит с аналогами.
РЛС
Препарат зарегистрирован в Государственном реестре лекарственных средств России (ГРЛС). Официальная лекарственная форма медикамента – таблетки для приема внутрь. В номенклатуре аптеки числятся:
- 2,5 мг;
- 5 мг;
- 10 мг;
- 20 мг.
Международное непатентованное наименование (МНН) – торасемид. С особенностями применения препарата и предосторожностями ознакомит инструкция по применению. Из аптеки лекарство отпускается по рецепту.
Состав
Действующее вещество Тригрим – торасемид. Активное соединение относится к группе диуретических препаратов. Торасемид демонстрирует мочегонное действие, а также уменьшает фиброз миокарда и улучшает функции сердечной мышцы.
В качестве наполнителя таблетки содержат лактозы моногидрат. Присутствие данного компонента ограничивает прием препарата для пациентов с непереносимостью лактозы и другими наследственными заболеваниями, связанными с нарушением всасывания сахаров. Например, синдромом глюкозо-галактозной мальабсорбции.
От чего помогают таблетки
Разберемся с тем, для чего предназначены таблетки. Лекарство назначается в комплексной терапии сердечно-сосудистых заболеваний совместно с антигипертензивными препаратами. В показания Тригрим входят:
- отеки на фоне хронической сердечной недостаточности или заболеваний печени, почек и легких;
- артериальная гипертензия.
Таблетки считают наиболее используемым диуретиком при хронической сердечной недостаточности. Препарат устраняет симптомы задержки жидкости и улучшает качество жизни пациентов. При артериальной гипертензии препарат назначается в качестве альтернативы другим мочегонным препаратам.
Тригрим: пить до еды или после еды?
Мочегонное средство рекомендуется принимать однократно в сутки после еды. Дозировку и продолжительность лечения устанавливает врач. Поможет ознакомиться с особенностями применения препарата взрослым – инструкция по применению «Тригрим: таблетки».
Побочные действия
- повышение холестерина и триглицеридов в крови;
- головная боль;
- головокружение;
- нарушение сердечного ритма;
- покраснение лица;
- носовое кровотечение;
- диарея;
- боль в животе;
- увеличение частоты мочеиспускания;
- жажда;
- и другие.
Диувер (Торасемид) или Тригрим: что лучше
Торасемид, Диувер и Тригрим – прямые аналоги и взаимозаменяемые лекарственные средства при совпадении дозировок. Медикаменты идентичны по составу действующих компонентов и терапевтическим свойствам. Разница между препаратами заключается в производителе и разнообразии доз.
- Тригрим выпускается двумя производителями: АО «Польфарма» и АО «Акрихин». Все стадии производства медикамента совершаются в России. Преимущества Тригрим заключается в широком списке дозировок: от 2,5 мг до 20 мг.
- Торасемид выпускается рядом фармацевтических компаний, преимущественно российских. Например, Торасемид Медисорб (АО «Медисорб», Пермь) и Торасемид-СЗ (НАО «Северная звезда», Кузьмоловский). Таблетки производятся в дозировках 5 мг и 10 мг.
- Диувер – торасемид от хорватской компании «Плива Хрватска д.о.о». Производство, контроль качества и фасовка проходят в двух странах: России и Хорватии. Препарат выпускается в двух дозах: 5 мг и 10 мг.
Нельзя однозначно сказать, что лучше: Тригрим, Торасемид или Диувер. При выборе лекарственного средства в первую очередь рекомендуется учитывать назначение врача.
Тригрим или Индапамид: что лучше
Индапамид входит в перечень жизненно необходимых и важнейших лекарственных препаратов (ЖНВЛП). Медикамент обладает доказанной эффективностью и считается препаратом выбора при артериальной гипертензии.
Согласно стандартам лечения повышенного артериального давления, монотерапия помогает ограниченному числу пациентов. Большинству показана двух— и трехступенчатая схема лечения, одним из звеньев которой является мочегонное средство. Препаратом первой линии в таком случае считается Индапамид из-за благоприятного профиля безопасности и изученности. При его непереносимости или неэффективности назначают другие лекарственные средства. Например, Тригрим.
Какой из препаратов лучше, сказать невозможно. Оба лекарства демонстрируют положительный результат в лечении заболеваний сердечно-сосудистой системы. Полноценную терапию подбирает врач, знакомый с результатами обследования и индивидуальными особенностями пациента.
Тригрим или Верошпирон: что лучше
Верошпирон – мочегонное средство из группы калийсберегающих. Лекарство входит в перечень жизненно необходимых и важнейших лекарственных препаратов (ЖНВЛП). Медикамент входит в стандарты лечения артериальной гипертензии и хронической сердечной недостаточности.
Как правило, Верошпирон добавляют к терапии артериальной гипертензии и хронической сердечной недостаточности при неэффективности предыдущих методов лечения или для усиления действия диуретиков первой линии. Препарат также назначают при снижении уровня калия в крови, вызванном приемом других мочегонных.
Схема лечения сердечно-сосудистых заболеваний подбирается лечащим врачом. Специалист учитывает особенности пациента, предыдущие методы терапии и сопутствующие заболевания. Нельзя самостоятельно заменять мочегонные препараты.
Краткое содержание
- Препарат Тригрим зарегистрирован в Государственном реестре лекарственных средств России (ГРЛС).
- Действующее вещество – торасемид.
- Лекарство назначается в комплексной терапии сердечно-сосудистых заболеваний совместно с антигипертензивными препаратами.
- Имеет побочные действия.
- Торасемид, Диувер и Тригрим – прямые аналоги и взаимозаменяемые лекарственные средства при совпадении дозировок.
- Индапамид считается препаратом выбора при артериальной гипертензии.
- Верошпирон добавляют к терапии артериальной гипертензии и хронической сердечной недостаточности при неэффективности предыдущих методов лечения или для усиления действия диуретиков первой линии.
Задайте вопрос эксперту по теме статьи
Остались вопросы? Задайте их в комментариях ниже – наши эксперты ответят вам. Там же вы можете поделиться своим опытом с другими читателями Мегасоветов.
В статье представлены механизмы развития синдрома задержки жидкости у больных ХСН. Показано преимущество применения петлевого диуретика с антиальдостероновым эффектом — торасемида и антагониста минералокортикоидных рецепторов — эплеренона в комплексной терапии ХСН.
Введение
Несмотря на кардинальные изменения в понимании патогенеза и принципов терапии больных с хронической сердечной недостаточностью (ХСН), направленные на улучшение прогноза, за 16 лет (с 1998 по 2014 г.) увеличилось число пациентов с любым функциональным классом (ФК) ХСН в 2 раза (с 7,18 млн до 14,92 млн), а пациентов с тяжелой ХСН III–IV ФК — в 3,4 раза (с 1,76 млн до 6,0 млн человек). При этом каждый третий пациент с ХСН имеет тяжелый ФК и связанный с этим высокий риск декомпенсации. Профилактика декомпенсации ХСН, которая часто заканчивается гибелью больного, остается важной задачей здравоохранения. Результаты исследования «ЭПОХА-Декомпенсация-ХСН» показали, что основными проявлениями декомпенсации ХСН, потребовавшими госпитализации, были в 58,5% случаев увеличение отеков, появление застойных хрипов в легких, нестабильная гемодинамика; в 21,1% случаев — прогрессирование асцита и анасарки; в 18,5% — развитие острой левожелудочковой недостаточности [1].
Патогенез развития отечного синдрома при ХСН
В основе формирования отечного синдрома при СН лежит снижение сократительной способности миокарда с уменьшением сердечного выброса и увеличением конечно-диастолического объема и давления. При этом повышается давление в левом предсердии и легочных венах с последующим развитием явлений венозного застоя в малом круге кровообращения, отека легких. Увеличение давления в малом круге кровообращения, в свою очередь, приводит к росту постнагрузки на правый желудочек. Это способствует снижению выброса, росту конечного диастолического объема и давления в правом желудочке, в системе верхней и нижней полых вен. Затем происходит перемещение жидкости из сосудистого русла в интерстициальную ткань с развитием периферических отеков. Снижение сердечного выброса автоматически приводит к уменьшению почечного кровотока и активизации ренин-ангиотензин-альдостероновой системы (РААС). Вырабатываемый ангиотензин ІІ вызывает спазм отводящей (эфферентной) артериолы нефрона с увеличением проксимальной реабсорбции и возможным повреждением клубочкового фильтра. Констрикция артериолы проксимального канальца приводит к падению давления в капиллярах и увеличению реабсорбции. В дистальных канальцах нефрона за счет действия альдостерона увеличивается реабсорбция натрия и жидкости, идущей за ним по осмотическому градиенту. В медуллярной части собирательных трубочек происходит увеличение проницаемости эпителия для воды с усилением реабсорбции. Исходя из этого, при ХСН происходит снижение натрийуреза как при концентрировании, так и при разведении мочи. В итоге отмечается избыточная задержка жидкости в сосудистом русле с увеличением объема циркулирующей крови. Повышение гидростатического давления способствует формированию отечного синдрома. Его дополнительный компонент обусловлен снижением онкотического давления в сосудистом русле из-за потери белка «застойной почкой» и феномена разведения. Схема формирования отеков при ХСН представлена на рисунке 1.
Принципы диуретической терапии
Согласно результатам трех эпидемиологических исследований («ЭПОХА-ХСН», «ЭПОХА-Госпиталь-ХСН» и «ЭПОХА-Декомпенсация-ХСН»), назначение рекомендованной терапии ХСН в полном объеме на госпитальном этапе лечения происходит чаще, чем на амбулаторном. После выписки из стационара, где больные находились на лечении по поводу декомпенсации ХСН, более половины пациентов (54,7%) прекращали прием антагонистов минералокортикоидных рецепторов (АМКР). Отсутствие адекватного проведения базисной и диуретической терапии ХСН является одной из причин повторных госпитализаций. Установлено, что с каждой последующей госпитализацией значительно возрастает риск смерти. Прибавка в весе более 2 кг за неделю, появление ортопноэ, кашля, приступов одышки в ночные часы, влажных хрипов в легких, набухания яремных вен, периферических отеков у больных с ХСН являются признаками задержки жидкости в организме и требуют незамедлительной коррекции проводимой терапии. При синдроме задержки жидкости препаратами выбора являются диуретики, которые назначаются всем пациентам при ХСН со сниженной фракцией выброса (ФВ) с отечным синдромом вне зависимости от ФК, обязательно в сочетании с блокаторами РААС для уменьшения симптомов, повышения толерантности к физической нагрузке и сокращения риска госпитализации. Пациентам с ХСН с сохранной ФВ или СН с промежуточной ФВ применение диуретиков рекомендуется только при наличии застойных явлений для уменьшения симптомов [2]. Диуретики восстанавливают нормальное соотношение натрия и воды в моче. Выделяют несколько групп мочегонных препаратов в зависимости от точки приложения воздействия в нефроне. Характеристика основных представителей различных групп мочегонных средств дана в таблице 1 [3, 4].

На начальных стадиях ХСН возможно эффективное назначение тиазидных диуретиков. Однако при более тяжелых стадиях ХСН и значительном снижении скорости клубочковой фильтрации (СКФ), когда тиазидные диуретики перестают работать, целесообразно применение петлевых мочегонных средств. Ведение больных с декомпенсацией ХСН требует обязательного соблюдения основных принципов диуретической терапии. Начинать лечение следует с минимальных доз с постепенным повышением до эффективной под контролем клинического статуса, суточного диуреза, электролитного баланса, СКФ. Дегидратационная терапия включает два этапа. На первом этапе желательно избегать применения ударных доз и быстрой дегидратации, чтобы не спровоцировать гиперактивацию нейрогормонов с развитием синдрома «рикошета» и дизэлектролитемии. Целью активного этапа лечения является достижение положительного диуреза: количество выделенной мочи должно превышать объем выпитой жидкости на 1–2 л с ежедневной потерей массы тела примерно на 1 кг. Как правило, это достигается назначением средних или иногда максимальных доз диуретиков. На втором этапе поддерживающей терапии рекомендуется регулярный, желательно ежедневный, прием мочегонных препаратов в минимально эффективных дозах для поддержания сбалансированного диуреза и стабильной массы тела. Возможно развитие резистентности к диуретической терапии. Основными причинами этого состояния могут быть нарушения электролитного баланса (гипокалиемия <3,5 ммоль/л; гипонатриемия <135 ммоль/л), вторичный гиперальдостеронизм, снижение онкотического давления крови на фоне гипоальбуминемии, значимое снижение СКФ, метаболический алкалоз. Одним из вариантов преодоления резистентности может быть назначение комбинации мочегонных средств с разными точками приложения в нефроне, обязательно в сочетании с ингибиторами РААС и АМКР. По показаниям осуществляются введение альбумина или плазмы, механическое удаление жидкости, в зависимости от уровня артериального давления (АД) следует рассмотреть внутривенное капельное введение эуфиллина или допамина в малых дозах. Алгоритм назначения диуретиков при ХСН представлен в таблице 2 [5].

Особенности применения торасемида
Оптимальным препаратом из группы петлевых диуретиков для лечения больных с ХСН является торасемид, доказавший положительное влияние на процессы ремоделирования миокарда и прогноз у данной категории больных. Препарат показал преимущества клинической эффективности по сравнению с фуросемидом, который многие годы оставался эталонным диуретиком для лечения отечного синдрома при ХСН. Торасемид обратимо связывается с котранспортером натрия/хлора/калия, расположенным в апикальной мембране толстого сегмента восходящей петли Генле, ингибируя реабсорбцию ионов натрия. В результате уменьшаются осмотическое давление внутриклеточной жидкости и реабсорбция воды. В отличие от других петлевых диуретиков торасемид обладает антиальдостероновым действием [6].
Фармакокинетические и фармакодинамические особенности торасемида
Торасемид относится к липофильным препаратам. Имеет стабильную биодоступность — в среднем 80–90%, в то время как у фуросемида наблюдается разброс показателя от 15 до 80%. Абсорбция препарата существенно не зависит от приема пищи (рис. 2) [7].

После приема внутрь максимальная концентрация в плазме крови достигается через 1–2 ч, поэтому препарат начинает работать не сразу, а примерно через 1 ч после приема внутрь, максимальный эффект наблюдается через 2–3 ч. Постепенное накопление активного вещества снижает риск развития толерантности [8]. Кроме этого, плавное диуретическое действие торасемида сопровождается уменьшением количества мочеиспусканий по сравнению с таковым при приеме фуросемида и не ограничивает активность пациентов (рис. 3).
По сравнению с другими петлевыми диуретиками торасемид имеет продолжительный диуретический эффект (до 18 ч) за счет увеличенного периода полувыведения — 3,5–4 ч. Связь с белками плазмы крови — более 99 %. Торасемид в основном (до 80%) метаболизируется в печени с помощью изоферментов системы цитохрома Р450 с образованием трех метаболитов (М1, М3 и М5) [9]. Только 20% препарата выводится почками в неизмененном виде. Поэтому нарушение функции почек не требует коррекции дозы препарата [10, 11]. При нарушении функции печени увеличиваются биодоступность и период полувыведения, однако кумуляция препарата не происходит за счет компенсаторного роста почечного клиренса [12]. У пожилых пациентов общий клиренс и период полувыведения препарата не меняются. Торасемид имеет меньшее сродство по сравнению с фуросемидом к альбумину, поэтому диуретический эффект препарата сохраняется у больных с гипоальбуминемией. Соотношение эквивалентных доз фуросемида и торасемида составляет 4–8:1 для здоровых лиц, 4:1 — для пациентов с СН и 2:1 — при хронической почечной недостаточности [13–15]. Основное действие препарата возрастает линейно в зависимости от увеличения дозы, но экскреция калия при этом значимо не меняется (рис. 4) [7].
Важно, что препарат существенно не влияет на выведение калия и кальция из организма, более того, длительный прием торасемида не оказывает значимого отрицательного действия на углеводный и липидный обмен. Уникальность торасемида (среди петлевых диуретиков) состоит в его влиянии на РААС. Препарат снижает чувствительность рецепторов ангиотензина II 1-го типа и уменьшает восприимчивость гладкомышечных клеток сосудистой стенки к эндогенным вазоконстрикторам за счет активации натрий-кальциевого насоса, обеспечивающего выведение ионов кальция из клетки в обмен на вход ионов натрия, а также подавления входа ионов кальция в клетку [16, 17]. На фоне приема торасемида у больных с умеренно выраженной ХСН уменьшаются уровень адреналина, образование тромбоксана, увеличивается синтез простациклина. Препарат воздействует на альдостероновые рецепторы в почечных канальцах, миокарде, сосудистой стенке и способствует устранению геномных эффектов альдостерона. Его доказанное антифибротическое действие связано с подавлением активности карбокситерминальной протеиназы проколлагена 1-го типа — фермента, который катализирует альдостеронзависимую трансформацию проколлагена 1-го типа в коллаген [18–21]. Регулярный прием торасемида приводит к сокращению объемной фракции коллагена и выраженности фиброза. В экспериментальной работе применение торасемида на модели аутоиммунного миокардита приводило к уменьшению площади миокардиального фиброза, синтеза профиброгенного моноцитарного хемоаттрактантного протеина 1-го типа, коллагена 3-го типа, альдостерон-синтазы в миокарде левого желудочка (ЛЖ). При этом данный эффект у фуросемида и пролонгированной формы торасемида не наблюдается [22–23].
Важно отметить, что диуретическая активность и антифибротические свойства торасемида отмечаются в разные сроки лечения. Так, антигипертензивный и мочегонный эффекты возникают сразу после приема начальной дозы, а реализация антифибротического действия — через 6–9 мес. непрерывной терапии [18].
Торасемид обладает метаболической нейтральностью: не приводит к существенной гипокалиемии, гипомагниемии, гиперурикемии, нарушению липидного и углеводного обмена.
Доказательная база эффективности торасемида при ХСН
В 1999 г. были опубликованы результаты сравнительного рандомизированного исследования PEACH с оценкой клинической эффективности торасемида и фуросемида у больных ХСН II–III ФК. Торасемид в большей степени улучшал качество жизни больных с ХСН. Однако достоверных различий между группами наблюдения по их влиянию на смертность и частоту госпитализаций выявлено не было [23]. Позднее результаты исследования TORIC (Torasemide In Congestive Heart Failure) показали способность торасемида не только улучшать клиническое состояние больных с ХСН, но и положительно влиять на долгосрочный прогноз. В исследовании участвовало 1377 больных с ХСН II–III ФК. Торасемид в дозе 10 мг/сут по сравнению с фуросемидом в дозе 40 мг/сут и другими диуретиками достоверно снижал показатели общей смертности — на 51,5%, сердечно-сосудистой смерти — на 59,7%, внезапной смерти — на 65,8%. В группе торасемида наблюдалось более значимое улучшение клинического состояния больных, сопровождавшееся снижением ФК ХСН. Отмечалась и лучшая переносимость препарата с меньшим развитием побочных эффектов. Так, торасемид достоверно реже приводил к развитию гипокалиемии, чем фуросемид (12,9 и 17,9% соответственно, р=0,013) [24]. Последующие исследования эффективности торасемида у больных с ХСН II–III ФК показали, что 6-месячный прием препарата достоверно снижает уровень натрийуретического пептида в плазме крови, уменьшает конечно-диастолический размер, индекс массы миокарда и улучшает показатели диастолической функции ЛЖ [25].
В российском рандомизированном многоцентровом исследовании «ДУЭЛЬ-ХСН» оценивалось применение торасемида у пациентов с декомпенсацией ХСН. В группе торасемида у больных ХСН II–IV ФК регресс явлений декомпенсации кровообращения происходил на 5 дней раньше, чем в группе фуросемида. Наблюдалось более существенное повышение переносимости физической нагрузки в пробе с 6-минутной ходьбой на фоне приема торасемида по сравнению с таковым при приеме фуросемида (160 и 133 м соответственно, р<0,01). Кроме этого, в группе торасемида достоверно улучшились показатели диастолической функции ЛЖ. В очередной раз подтвердилась лучшая переносимость препарата. В группе торасемида реже развивались гипокалиемия и другие побочные эффекты по сравнению с таковыми в группе фуросемида (0,3 и 4,2% соответственно) [26].
В другом российском открытом многоцентровом рандомизированном исследовании «ТРИОЛЯ» [22] с участием больных с компенсированной ХСН II–III ФК сравнивались эффективность торасемида (Тригрим, «Польфарма», Польша) и эффективность фуросемида. В обеих группах наблюдалось достоверное сопоставимое снижение ФК ХСН. Улучшение качества жизни и повышение толерантности к физической нагрузке по данным теста 6-минутной ходьбы в большей степени отмечались в группе торасемида. Только торасемид способствовал достоверному увеличению ФВ ЛЖ, снижению уровня натрийуретического гормона и уровня альдостерона (на 22,6%, р<0,001), улучшению диастолической функции ЛЖ. А у больных в группе фуросемида отмечалось достоверное повышение маркера синтеза коллагена на 17,8% (р<0,001).
Аналогичные результаты были получены в рандомизированном многоцентровом исследовании «ПОЭТ», в котором торасемид в составе комбинированной терапии пациентов с ХСН II–III ФК по сравнению с фуросемидом приводил к более выраженному уменьшению отечного синдрома, улучшению качества жизни, показателей систолической функции ЛЖ, повышению толерантности к физической нагрузке [27].
Торасемид (Тригрим) является средством, обладающим выраженным диуретическим эффектом и способностью связывать рецепторы альдостерона и уменьшать выраженность фиброза миокарда. В связи с указанными свойствами препарат необходимо применять длительно (пожизненно) для поддержания органопротекции.
Следует отметить, что препарат хорошо переносится, обладает метаболической нейтральностью и может применяться у больных не только с ХСН, но и с артериальной гипертензией (АГ), в т. ч. при резистентной АГ, с сопутствующими заболеваниями: сахарным диабетом, подагрой, гиперлипидемией, хронической болезнью почек (ХБП), у женщин при климактерическом синдроме, циррозе печени [20, 21].
Торасемид в нашей стране длительное время отсутствовал, оригинальные европейские препараты до настоящего времени недоступны. Около 10 лет назад на российском фармацевтическом рынке были зарегистрированы дженерики (под торговыми названиями Диувер и Тригрим), которые хорошо переносятся и отвечают всем требованиям GMP. Тригрим является клинически эффективным, безопасным и более экономичным препаратом. Специальные фармакологические исследования показали, что Тригрим полностью эквивалентен препарату Торем (компания Roche), применяемому в странах Европы. В России Тригрим зарегистрирован как диуретический препарат для лечения ХСН и АГ как в монотерапии, так и в комбинации с другими лекарственными средствами.
Таким образом, торасемид является приоритетным петлевым диуретиком в лечении отечного синдрома при ХСН с доказанным влиянием на прогноз и уникальными фармакологическими свойствами, определяющими продолжительное диуретическое и антиальдостероновое действие с уменьшением явлений фиброза миокарда. Торасемид улучшает клиническое состояние, качество жизни больных ХСН и повышает толерантность к физической нагрузке. Регулярный прием торасемида сокращает частоту и продолжительность госпитализаций по поводу декомпенсации ХСН. Препарат показал отличную переносимость без развития значимых отрицательных метаболических и электролитных нарушений.
Эффективность антагонистов минералокортикоидных рецепторов при ХСН
Одним из принципов успешности лечения отечного синдрома у больных ХСН является совместное применение диуретиков с блокаторами РААС. Установленный феномен «ускользания» блокады синтеза альдостерона на фоне длительного приема ингибиторов ангиотензинпревращающего фермента (иАПФ) и полученные результаты исследования RALES стали основанием для включения АМКР в основную группу препаратов для лечения больных тяжелой ХСН с ФВ ЛЖ < 40%. Блокада минералокортикоидных рецепторов приводит к уменьшению гипергидратации, гипокалиемии, уровня проколлагена 3-го типа, реактивного интерстициального фиброза миокарда, вариабельности ритма сердца, увеличению захвата норадреналина миокардом и барорефлекторной чувствительности. Это, в свою очередь, способствует сокращению массы миокарда, объемов ЛЖ после перенесенного инфаркта миокарда (ИМ); улучшению систолической и диастолической функции ЛЖ, снижению риска развития аритмий, показателей общей смертности, частоты госпитализаций, риска внезапной сердечной смерти у постинфарктных больных ХСН [28]. Добавление спиронолактона в дозе 12,5–50 мг/сут к комплексной терапии больных ХСН III–IV ФК достоверно снижало общую смертность на 30% (р<0,001) в исследовании RALES. В группе спиронолактона были отмечены выраженное улучшение клинического состояния больных и снижение числа госпитализаций из-за прогрессирования ХСН. Однако даже прием минимальных доз препарата приводил к развитию гинекомастии у 10% пациентов, что явилось причиной их исключения из исследования [29]. Это связано со способностью спиронолактона воздействовать не только на минералокортикоидные рецепторы, расположенные в эпителии почечных канальцев, эпителии и гладкомышечных клетках сосудов, сердца, но и на андрогенные и прогестероновые рецепторы. Решение данной проблемы реализовалось при появлении на фармацевтическом рынке селективного АМКР эплеренона.
Эплеренон является селективным блокатором минералокортикоидных рецепторов с минимальной активностью в отношении андрогенных и прогестероновых рецепторов (аффинность к ним в 100 раз меньше, чем у спиронолактона). Препарат хорошо абсорбируется после приема внутрь. При этом прием пищи не оказывает влияния на абсорбцию препарата. Биодоступность составляет 69%. Связывается с белками на 50%. Период полувыведения составляет 4–6 ч. Максимальная концентрация препарата в плазме выявляется через 1,5–2 ч после приема пероральной формы. Метаболизм эплеренона осуществляется с помощью цитохрома Р450 (CYP3A4) с трансформацией до неактивных метаболитов. Выведение препарата в большей степени происходит с мочой — 67%, около 32% — с калом [31]. В неизмененном виде элиминируется менее 5% дозы препарата. У пациентов пожилого возраста коррекции стартовой дозы не требуется, однако рекомендуется тщательный контроль уровня калия. Тяжелые нарушения функции почек и печени являются противопоказаниями для назначения эплеренона.
Проведенные исследования доказали не только положительное влияние эплеренона на прогноз у больных с ХСН, но и способность препарата снижать риск развития ХСН. Так, в исследовании REMINDER с участием 1012 больных с острым инфарктом миокарда (ОИМ) без проявлений СН назначение эплеренона в дозе 25–50 мг/сут приводило к снижению концентрации натрийуретических пептидов (BNP и N-терминальный фрагмент BNP), обладающих высокой отрицательной прогностической ценностью в диагностике ХСН. Через 1 мес. наблюдения концентрация натрийуретических пептидов была повышена у достоверно меньшего количества больных в группе эплеренона (16%) по сравнению с группой контроля (25,9%) (р<0,0002) [32]. Одним из первых проектов с оценкой эффективности эплеренона у больных с клиническими проявлениями ХСН и сниженной ФВ ЛЖ после перенесенного ИМ было рандомизированное плацебо-контролируемое исследование EPHESUS [33]. В исследовании приняли участие 6632 больных с ОИМ сроком от 3 до 14 сут (в среднем 7,3 сут) с ФВ ЛЖ ≤ 40% (средняя ФВ составила 33%) и клиническими проявлениями ХСН I–IV ФК по NYHA. Прогноз улучшался уже на фоне месячного приема препарата — смертность в группе эплеренона была ниже на 31% (р=0,004). К завершению наблюдения в группе эплеренона достоверно снизились сердечно-сосудистая смертность на 17%, (р=0,005); комбинированный показатель смертности от сердечно-сосудистого заболевания (ССЗ) и частоты первой госпитализации по поводу ССЗ — на 13%, (р=0,002); общая смертность и частота любой госпитализации — на 8% (р=0,02); частота первой госпитализации по поводу ХСН — на 15% (р=0,03). В 2010 г. были опубликованы результаты плацебо-контролируемого исследования EMPHASIS-HF, в котором приняли участие 2737 пациентов с ХСН II ФК и систолической дисфункцией ЛЖ (ФВ ЛЖ в среднем составила 26,1%) с предшествующей госпитализацией в течение ближайших 6 мес. по какой-либо сердечно-сосудистой причине или с повышенным уровнем одного из натрийуретических пептидов: BNP ≥ 250 пг/мл или N-терминальный фрагмент pro-BNP ≥ 500 пг/мл у мужчин и ≥ 750 пг/мл у женщин. Эплеренон назначался исходно в дозе 25 мг 1 р./сут с последующим увеличением через 4 нед. до 50 мг 1 р./сут под контролем уровня калия. Средняя доза эплеренона составила 39,1±3,8 мг/сут. Включение эплеренона в состав стандартной терапии ХСН способствовало достоверному снижению риска смерти по сердечно-сосудистой причине и/или госпитализации по поводу ХСН на 37% (p<0,001). По отдельным составляющим комбинированной конечной точки получена сопоставимая положительная динамика: эплеренон уменьшил риск смерти по сердечно-сосудистой причине на 24% (p=0,01), а число госпитализаций из-за прогрессирования ХСН — на 42% (p<0,001) [34].
Эффект эплеренона не зависел от возраста больных, гендерных различий, уровня АД и частоты сердечных сокращений, наличия АГ, сахарного диабета, фибрилляции предсердий, почечной дисфункции, этиологии развития ХСН. Эплеренон в исследовании показал высокий профиль безопасности. Достоверно более частое развитие гиперкалиемии (уровень калия > 5,5 ммоль/л) в группе эплеренона у 158 (11,8%) пациентов по сравнению с таковым при приеме плацебо у 96 больных (7,2%) (p<0,001) требовало коррекции дозы препарата, но не явилось причиной прекращения лечения препаратом. Частота развития таких побочных эффектов, как гинекомастия и ухудшение функции почек, была схожей с таковой в группе плацебо, а эпизоды гипокалиемии (уровень калия < 3,5 ммоль/л) достоверно чаще развивались в контрольной группе (11% против 7,5%, р=0,002). Незначительная частота развития эндокринологических осложнений (в виде гинекомастии и импотенции у мужчин или дисменореи у женщин — 0,7% против 1% в группе плацебо) обусловлена меньшим сродством к рецепторам прогестерона (<1%) и андрогеновым рецепторам (<0,1%).
На основании результатов проведенных исследований АМКР должны применяться у всех пациентов с симптомами ХСН II–IV ФК и ФВ ЛЖ < 40% для снижения риска смерти, повторных госпитализаций и улучшения клинического состояния вместе с иАПФ (блокаторами рецепторов ангиотензина) и β-адреноблокаторами (класс рекомендаций I, уровень доказательности А). Назначение препаратов из этой группы следует рассмотреть у пациентов с сохраненной и промежуточной систолической функцией ЛЖ для снижения количества госпитализаций по поводу ХСН (класс рекомендаций IIа, уровень доказательности B) [2]. Перед назначением диуретической терапии, в т. ч. АМКР, необходимо оценить функцию почек с определением СКФ и уровня электролитов. Поскольку ХБП широко распространена в популяции больных ХСН (от 20 до 60%), выбор препарата и коррекция дозы должны проводиться с учетом СКФ (табл. 3) [35].
Заключение
Оптимизация лечения пациентов с ХСН — трудная и не до конца решенная задача. В клинической практике ежедневно приходится сталкиваться с проблемой выбора оптимального лекарственного средства. В этом случае целесообразно отдавать предпочтение препаратам с доказанной клинической эффективностью, положительным влиянием на прогноз, предсказуемым действием, хорошей переносимостью и экономически более доступным для больного. В нашей стране торасемид и эплеренон с доказанной биоэквивалентностью оригинальным препаратам зарегистрированы под торговыми названиями: Тригрим с дозировками 2,5 мг, 5 мг, 10 мг; Эспиро («Польфарма», Польша) с дозировками 25 мг и 50 мг. Разнообразие дозировок в реальной клинической практике облегчит титрацию препаратов на разных этапах диуретической терапии, а приемлемая цена и количество таблеток в упаковке (Тригрим № 30) повысят приверженность пациента лечению.
Владимир Трофимович Ивашкин, академик РАМН, доктор медицинских наук:
— Мы попросим профессора Арутюнова Григория Павловича рассказать нам об адекватной диуретической терапии хронической сердечной недостаточности. Пожалуйста, Григорий Павлович.
00:13
Арутюнов Григорий Павлович, доктор медицинских наук, профессор:
— Большое спасибо, Владимир Трофимович.
Уважаемые коллеги. Синдром хронической сердечной недостаточности – это очень хорошо известный синдром с древних времен. Меняются времена, но всегда остается большая проблема в описании этого синдрома, в описании симптомов, характерных для этого синдрома.
(Демонстрация слайда).
Современный клинический портрет больного, страдающего недостаточностью кровообращения. Зеленые столбики означают мнение врачей. Красные столбики – так встречается в реальной клинической практике. Как и многие века назад, многие десятилетия на первых позициях по-прежнему чувство нехватки воздуха и четкие выраженные отеки, которые встречаются у этих больных.
Какие бы новые симптомы не появлялись в последние годы (например, утомляемость – великолепно описанный синдром в последние десятилетия XX века), сохраняется особое значение старых симптомов, борьба с которыми, по сути, является клинически значимой в сохранении жизни наших пациентов.
Но слово «отеки» в сознании врача-интерниста, терапевта в первую очередь обязательно ассоциируется со словом «мочегонные препараты».
Как современные рекомендации говорят, когда мочегонные препараты должны появиться в схеме лечения недостаточности кровообращения. Возьмем самых простых больных, самых легких. Недостаточность кровообращения, I-II функциональный класс, еще синусовый ритм.
Старт-терапия всегда начинается с ингибитора АПФ, при непереносимости – это АРА. Только потом, когда титрованы ингибиторы АПФ, при наличии отеков терапевт вправе поставить вопрос о мочегонной терапии.
Если больные с мерцательной аритмией, даже в этой ситуации мочегонные препараты не выходят на первую линию. Это все равно препараты, которые корригируют нейрогормональный профиль больного. Это и гликозиды при мерцательной аритмии. Только тогда, когда титрованными препаратами контролируется ритм, на повестку дня ставится вопрос о мочегонных препаратах.
У более тяжелых больных, III-IV функциональный класс, но все еще сохраняется синусовый ритм, терапевт вправе впервые поставить диуретики, первую линию препаратов.
У больных с мерцательной аритмией III-IV функционального класса стартуют три препарата в лечении. Это ингибиторы АПФ, диуретики (обращаю внимание, диуретики на первой линии) и гликозиды.
02:47
Мы с вами проговорили первое условное место для мочегонных препаратов. Начнем с первого закона назначения мочегонных препаратов для терапевта. Без отеков нет мочегонной терапии. Если нет материального субстрата (нет отеков), терапевт не должен задумываться о мочегонной терапии в лечении ХСН.
Однако сами по себе отеки требуют от терапевта осмысления: что это за отеки. Опишем отеки, которые требуют мочегонные препараты. Вспомним Боткина, его описание отеков. Больные с недостаточностью кровообращения должны подчиняться закону симметрии. Симметричные отеки. Пощупай отеки – они должны быть плотные, холодные. Оцени их цвет – они должны быть синие.
Итак, плотные, холодные, симметричные отеки – это отеки, обусловленные гидростатическими проблемами, недостаточностью кровообращения. Тогда на повестку дня выходят мочегонные препараты.
Когда нарушается закон симметрии, отеки становятся односторонними, для мочегонных препаратов нет места. Это хирургическая проблема, которая требует своего решения, обязательно в экстренном порядке.
Терапевт осмысленно посмотрел на отеки, пощупал, оценил их цвет, температуру и принимает решение о назначении мочегонных препаратов.
Чего мы достигаем, назначая мочегонные препараты. В первую очередь, мы будем влиять на выведение из организма натрия и связанного с натрием хлора. Поскольку объем внеклеточной жидкости регламентируется, главным образом, содержанием натрия и хлора в организме, то мы будем влиять на выход жидкости из организма с первичной, затем вторичной мочой.
04:41
Закон мощности мочегонных препаратов. Чем ближе к нефрону, тем сильнее действие мочегонного препарата. В этом правиле есть исключения. Диакарб не подчиняется этому правилу. Он действует рядом с нефроном. Но это не относится к числу мощных мочегонных препаратов.
Ближе всего уровень петли, будут действовать петлевые диуретики (отсюда их название). Дальше будут действовать тиазидные диуретики. Еще дальше будут действовать калий-сберегающие мочегонные препараты. Итак, мы запомнили первое основное правило. Чем ближе к нефрону, тем мощнее действие мочегонного препарата с единственным исключением для препарата Диакарб.
Посмотрим на второй и третий закон. Они всегда должны быть в оперативной памяти терапевта. Диуретики нельзя назначать дискретно. Назначение мочегонных препаратов 1-2 раза в неделю, по четным или нечетным дням не приносит пользу больному. Напротив, начинают раскачивать нейрогормональный профиль пациента.
Что произойдет с пациентом, когда он будет принимать нерегулярно мочегонные препараты. На какое-то количество времени резко возрастет объем выделяемой мочи. Изменится нейрогормональный профиль. В ответ на выведенную жидкость начнется овер-синтез ангиотензина II, норадреналина. Вы начнете раскачивать нейрогормональный профиль.
Диуретики назначаются в ежедневном режиме в малых дозах, но ни в коем случае не дискретно, что сегодня не должно рассматриваться вообще в схемах лечения недостаточности кровообращения.
Очень интересен вопрос истории развития мочегонных препаратов. На заре медицины мочегонными препаратами являлись сборы трав. Потом совершенно случайно в период лечения сифилиса было обнаружено, что ртуть (ртутная мазь применялась в лечении сифилиса) обладает мочегонным эффектом. Конечно, удивительно токсичный мочегонный препарат оказался.
Эра мочегонных препаратов – это послевоенная эра. После Второй мировой войны, когда были синтезированы первые эффективные мочегонные препараты, которые были не столь токсичны, были клинически высокоэффективны.
Процесс синтеза новых препаратов не завершен. На сегодняшний день в XX веке мы говорим о трех новых классах мочегонных препаратов. Это процесс, который, видимо, будет развиваться все время.
Но мы вспомнили историю синтеза мочегонных препаратов только для того, чтобы подойти к четвертому закону назначения мочегонных препаратов. Диуретики терапевтом назначаются по принципу: от слабейшего к сильнейшему. Это оправданно, потому что чем сильнее мочегонный эффект, чем сильнее мочегонный препарат, тем больше его побочное действие, тем больше его токсическое действие.
07:40
Итак, посмотрим на мочегонный препарат, который гораздо слабее, чем петлевые диуретики.
Это тиазидный диуретик. Он будет, в первую очередь, снижать реабсорбцию хлора. Это его самое главное. Вместе с хлором будет оказывать пассивное воздействие на экскрецию натрия и воды, связанной с натрием.
Очень важно посмотреть, что группа тиазидных диуретиков, о которых мы так легко говорим, очень большая группа. В нее входит хорошо нам известный препарат Индапамид, Гидрохлортиазид, Хлорталидон, более известный в других странах, чем у нас. Тем не менее, это совершенно разные препараты.
Это различие мочегонных препаратов приводит к тому, что терапевт должен помнить про период полувыведения. Это слишком разные периоды полувыведения, чтобы сказать о чем-то едином для этой группы. Период полувыведения мочегонного препарата – важнейший показатель мочегонного препарата. Чем больше период полувыведения, тем больше токсический эффект мочегонного препарата, тем меньше его влияние на нейрогормональный профиль нашего пациента.
(Демонстрация слайда).
Посмотрим на тиазидные диуретики.
Хорошо выделенная белая линия. Один из самых главных побочных эффектов мочегонного тиазидного препарата (две стрелки стоят под уровнем калия) – это высокий вывод калия. Следовательно, высокие дозы тиазидных диуретиков всегда будут чреваты развитием тяжелых нарушений ритма. Натрий выводится существенно меньше, чем калий. Это очень существенный момент.
Наконец, тиазидные диуретики оказывают достаточно токсическое действие на скорость клубочковой фильтрации.
09:20
Побочные эффекты. Сегодня завершилась дискуссия о дозе тиазидных диуретиков. Считается, что 12,5 мг вместе с ингибиторами АПФ безопасно. Дозы ниже, чем 12,5 мг безопасны. Это очень важная для нас находка. Но мы помним, что тиазидные диуретики будут вмешиваться в липидный спектр, влиять на уровень холестерина, оказывать, к сожалению, в высоких дозах негативное влияние на уровень глюкозы крови.
Применение. Здесь терапевт должен запомнить простое правило. Чем хуже функция почки, чем ниже скорость клубочковой фильтрации, тем менее эффективны тиазидные диуретики. При цифре 40 мл/мин. (скорость клубочковой фильтрации, рассчитанная по Кокрофту-Голту или по формуле MDRD) тиазидные диуретики практически неэффективны. Это очень важный момент, когда мы будем строить повседневную схему лечения больных.
Петлевые диуретики намного эффективнее, чем тиазидные диуретики. Точка приложения действия петлевого диуретика – это толстый сегмент восходящей части петли Генле. В этом участке будет реабсорбироваться 25% отфильтровавшегося натрия. Если мы заблокируем вход натрия назад, то вместе с натрием уйдет и вода.
Почему такой высокий эффект у петлевых диуретиков. Вместе с натрием уйдут и другие электролиты. Речь идет о кальции, о магнии. Высокие дозы все равно будут вмешиваться в электролитный баланс и могут быть чреваты нарушениями ритма у пациента.
Петлевой диуретик выводит натрий гораздо больше, чем тиазидный диуретик, но вместе с этим он влияет и на уровень выведения калия. Любой мочегонный препарат, вмешиваясь в электролитный баланс, будет чреват нарушениями ритма.
Не будем забывать, что вместе с выведенным натрием уходит большой объем воды. Следовательно, будет прямое влияние на гематокрит. Если вы лечите лежачего пациента, то создадутся идеальные условия для тромбоза глубоких вен голени. Петлевые диуретики в высоких дозах всегда будут давать высокий уровень выведенной воды из организма. Терапевт всегда должен держать в памяти великую вероятность не только нарушений ритма, но и тромбоза глубоких вен голени с возможным эмболическим синдромом в легочную артерию.
Токсический эффект. Самый главный показатель, от которого во многом зависит продолжительность жизни пациента – это скорость клубочковой фильтрации. Здесь при умеренных дозах нет негативного влияния. Однако появится резкое снижение скорости клубочковой фильтрации при высоких дозах петлевых диуретиков.
12:32
Подойдем к классу петлевых диуретиков.
Они тоже очень разнятся между собой. Это и этакриновая кислота, и Фуросемид и Торасемид. Принципиальный показатель, по которому они разнятся – это период полувыведения. Второй показатель – это метаболизм мочегонного препарата. Чем больше мочегонного препарата выводится через почку, тем более токсичен и негативен его эффект, особенно у больных с изначально измененной функцией почки (как у наших пациентов с недостаточностью кровообращения).
Я хочу привлечь ваше внимание к тем дозам, которые рекомендованы Мировыми рекомендациями для введения, например, Фуросемида. Пероральный, конечно, прием 40 мг, 160 мг – это доза не повседневной практики, однако такая практика существует в мире. Мы должны быть готовы, что дозы петлевых диуретиков не пройдут бесследно.
Где будет негативный эффект высоких доз при повседневном или дискретном приеме? Если мы блокируем всасывание натрия, то мы должны совершенно четко вспомнить, что после прекращения циркуляции препарата в крови произойдет, к сожалению, синдром отскока. Это будет постдиуретическая реабсорбция. Количество натрия, которое будет всасываться с первичной мочи, будет резко возрастать.
Период полувыведения мочегонного препарата становится доминирующим. Мы должны стремиться к большому периоду полувыведения, чтобы срезать синдром повышенной постдиуретической реабсорбции. Это первое. Но если больше натрия всасывается, а клетки к этому не готовы, они будут погибать.
Второй момент. Мы заблокировали всасывание натрия на 25%. Значит, натрий двинулся дальше по канальцам. К сожалению, клетки в дальних отделах не готовы к такому количеству натрия. Это приведет к их прямому токсическому повреждению.
Третий момент, о котором терапевт всегда должен помнить – это скорость клубочковой фильтрации. Чем она ниже, тем выше концентрация при обычных дозах препарата, тем больше прямой токсический эффект мочегонного препарата. Этот прямой токсический эффект мочегонного препарата должен держаться нами в оперативной памяти, потому что он ухудшает состояние пациента, раскачивает его нейрогормональный профиль.
Наконец, запомним, что Фуросемид – основной препарат из этой группы. 65% его выводится почками. Давайте запомним эту цифру. Это очень важная цифра. Она очень высокая, потому что Торасемид будет существенно меньше выводить через почку. Это для терапевта становится существенным при выборе длительной, пожизненной терапии мочегонными препаратами.
15:21
Основные побочные эффекты влияния мочегонных препаратов. Первый и неизменный эффект – это влияние на активность ренин-ангиотензин-альдостероновой системы. Мочегонная терапия всегда приведет к тому, что будет увеличиваться активность ангиотензина II, и последуют каскады, которые будут вызывать высокий уровень ангиотензина II. Будет повышаться общее периферическое сосудистое сопротивление, будет увеличиваться реабсорбция натрия, приводить к гипертрофии миокарда, гипертрофии гладкомышечных элементов.
Второй момент – это нефротоксичный эффект. Любой мочегонный препарат не остается безразличным для почки. Он действует на почку. Наконец, надо помнить, что мы снижаем качество жизни пациента. После назначения мочегонного препарата возрастает количество мочеиспусканий. Это существенно.
Представьте себе реально работающего пациента со вторым функциональным классом, которому вы прописали мочегонный препарат. После приема утром мочегонного препарата на несколько часов возрастает количество мочеиспусканий. В это время он должен двигаться на работу. Мы создаем параметры, которые будут ухудшать его качество жизни.
Очень долго мы знали, что мочегонные препараты не влияют на увеличение продолжительности жизни. Если сказать по мета-анализам, то приводили даже к большей вероятности летальных исходов, к сожалению.
Так было до ключевого исследования, которое было выполнено препаратом Торасемид. Впервые было показано, что мочегонные препараты снижают риски смерти у больных с недостаточностью кровообращения.
17:05
Итак, больной получил петлевой диуретик. Однако вы видите, что наступает некоторая характерность: терапевт не может добиться адекватного выделения мочи. Что должен сделать терапевт у больного с недостаточностью кровообращения. В первую очередь задуматься над pH мочи. Надо закислить мочу.
Хорошо известно, что для этого существует мочегонный препарат из «группы резерва». Речь идет о препарате Диакарб. Назначение Диакарба коротким курсом 5-7 дней меняет pH мочи и повышает эффективность мочегонной терапии петлевыми диуретиками.
Это тоже очень интересная история появления Ацетозоламида. Это был препарат, который вообще появился из антибиотиков. Как антибиотик его сейчас никто и не вспомнит. Но это очень интересный мочегонный препарат, влияющий в первую очередь на pH мочи, помогающий действовать петлевым диуретикам.
Мы подходим к наиболее слабым по мочегонному эффекту препаратам. Это минералкортикоиды. Есть два препарата. Спиронолактон – это оправданно. Эплеренон – это немного условно. Эплеренон – это антагонист рецепторов альдостерона, обладающий мочегонным эффектом.
Они отличаются только одним. Эплеренон отличается от Спиронолактона тем, что у него отрезаны два радикала, которые оказывали половое воздействие. У каждого десятого мужчины, находящегося на Спиронолактоне, развивалась гинекомастия. Эплеренон лишен этого эффекта. Это очень интересное присоединение.
Это препарат, который рассматривается не как самостоятельный мочегонный препарат, а как препарат, присоединяемый к уже существующей мочегонной схеме. В обычных дозах нет какого-либо токсического влияния. Надо запомнить схемы назначения этого препарата.
Когда используются большие дозы. Когда терапевт осознанно идет на применение больших доз. Тогда, когда есть декомпенсация кровообращения и обычная терапия петлевыми диуретиками не позволяет «размочить» больного, добиться стойкого мочегонного эффекта (тогда оправданны большие дозы).
Существуют более часто назначаемые малые дозы (25 – 50 мг). Это дозы, которые прописаны постоянно, пожизненно. Пациенту с III-IV функциональным классом, поскольку там мы достигаем не столько мочегонного эффекта (я очень прошу обратить на это внимание), там мы достигаем эффект блокады D-позиции коллагенов.
Мы впервые говорим о дополнительном действии мочегонного препарата, вообще не относящемся к почке. Мы говорим о блокаде D-позиции коллагена в организме человека, страдающего недостаточностью кровообращения.
19:50
Вернемся к классу мочегонных препаратов. Они все разнятся. В первую очередь, мы обращаем внимание на периоды полувыведения. Это на добровольцах, молодых людях показано, что самый высокий период полувыведения у Торасемида. Чем выше период полувыведения, тем безопасней мочегонный препарат.
Что мы должны помнить из фармакокинетики Торасемида. Самый главный препарат. Там, где неэффективно применение, например, Фуросемида, более эффективен будет Торасемид.
Большой период полувыведения позволяет запомнить две вещи. Его можно применять у больных с изначально измененной функцией почки. У пожилого пациента не надо видоизменять дозировку.
Запомним самую главную вещь. 80% введенного Торасемида метаболизируется в печени. Значит, через почку выделяется всего 20%. Это означает, что можно применять этот препарат у пациентов с изначально измененной функцией почки. Это выделяет Торасемид из всего класса петлевых диуретиков, делая его безопасным и широко применяемым.
Что делает Торасемид ? Посмотрите на слово «альдостерон». Это гормон. Локально в почке из-за того, что у больного недостаточность кровообращения, включилась ренин-ангиотензин-альдостероновая система. Альдостерон, помимо влияния на уровень натрия, будет оказывать влияние на локальный синтез и D-позицию коллагена. Насколько это серьезно. Давайте зададим этот вопрос и посмотрим ответ на него чуть позже.
Концентрация калия и магния не имеет пикообразного снижения. Значит не надо ожидать или, по крайней мере, вероятность тяжелых нарушений ритма не будет очень высокая.
21:41
Еще один момент. Самое главное для пациента. Он знает про уровень калия и натрия, но от твердо видит количество мочеиспусканий, которое возникает после приема мочегонного препарата. Торасемид имеет плавную линию. Это очень важно. Не произойдет резкого ухудшения качества жизни пациента после приема этого мочегонного препарата.
Индекс массы миокарда левого желудочка снижается. Зададим вопрос: почему? Мы второй вопрос задали. Почему уменьшается масса миокарда левого желудочка и зачем надо влиять на уровень коллагена? Достаточно легко объяснить. Действительно улучшается трансмитральный поток крови, потому что вы изменяете объем циркулирующей крови. Это просто объяснить. Но как объяснить индекс массы миокарда левого желудочка?
Еще на одну вещь посмотрим – на гормоны. Изменился объем циркулирующей крови, мозговой натрийуретический пептид уменьшился. Это понятно. Но что произошло с альдостероном. Мочегонный препарат Торасемид оказывает помимо мочегонного эффекта прямое влияние на уровень активности альдостерона.
К чему это приводит? В первую очередь, к уменьшению фиброза. Когда мы с вами родились, то у каждого из нас расстояние между капиллярами и мышечными пучками миокарды было детерминировано генетически. Это расстояние, которое гарантировало равномерное поступление нутриентов и кислорода, было гарантировано количеством коллагена между мышечными пучками.
В молодом возрасте тонкие и нежные нити – это коллаген. У больного с недостаточностью кровообращения прижизненный биоптат. Канаты коллагена, которые депонируются в миокарде, раздвигают пучки, делают миокард толстым и электрически нестабильным. Это, конечно, крайне плохо.
Мочегонный препарат, который может не только уменьшить объем циркулирующей крови, но и повлиять на эту D-позицию коллагена, будет очень важен для нас.
(Демонстрация слайда).
Мощные розовые поля сверху – это на Фуросемиде. Отсутствие розовых полей внизу – это на Торасемиде. Нет коллагена не только в почке, но и в миокарде. Что дает такой эффект применения Торасемида. Мы выбрали Торасемид из целого класса петлевых диуретиков. Достоверно уменьшает госпитализацию. Суммарное количество госпитализации уменьшается. Самое главное – уменьшается просто среднее пребывание пациента на койке.
Почему для нас важны эти цифры? Это не просто механическое уменьшение пребывания пациента в больнице. Это меньше тромбозов глубоких вен, меньшее влияние на нозокомиальные инфекции и меньше эмболий в легочную артерию.
24:29
Больного лечили Фуросемидом, затем перевели на Торасемид. Добьемся ли мы успеха? Да. Применение Торасемида после длительной терапии привело к резкому снижению количества госпитализаций. Это существенная вещь.
Впервые показано, что терапия мочегонным препаратом привела к снижению не только общей смерти, но что существенно важнее, к снижению внезапной смерти. За счет уменьшения D-позиции коллагена, что привело к электрической гомогенизации миокарда. Нет разобщенности, нет электрической нестабильности (по крайней мере, ее намного меньше). Естественно, уменьшение нагрузки, объема. Это очень важные данные для повседневной практики.
Я специально в качестве контраста показываю исследования, которые были выполнены задолго до нашего понимания периода полувыведения мочегонных петлевых диуретиков. До появления Диувера мета-анализ, выполненный на Фуросемиде, плацебо линия выше, чем линия Фуросемида. Это означает, что количество летальных исходов было меньше на терапии без мочегонных препаратов.
Как же тогда помочь больному с недостаточностью кровообращения. Мы все равно встали перед проблемой выбора мочегонного препарата. Когда мы учли период полувыведения, когда мы учли факт того, что Диувер вмешивается в D-позицию коллагена, это привело к снижению смертности и сокращению госпитализации пациентов.
Исследование «TORIC» важно для нас еще и потому, что мы твердо говорили, что мочегонный препарат всегда приводит к увеличенному выведению калия из организма. Значит, ожидаются тяжелые нарушения ритма. Эффект Торасемида мягче по сравнению с Фуросемидом в действии на уровень калия. Нет пикообразного снижения калия.
26:36
Еще один момент. Мы сейчас позволим сами себе сказать, что Диувер обладает продолжительным действием. Это очень важно. Нет пикообразного колебания уровня нейрогормонов. Вопрос второй: нет пикообразного изменения уровня калия, что говорит о том, что навряд ли произойдут тяжелые нарушения ритма.
Для терапевта очень важен факт: внезапная смерть снижается практически на 70%. Мы впервые говорим, что мочегонный препарат может оказать такую мощную антиаритмическую эффективность. Но все-таки в повседневной практике терапевта очень часты ситуации, когда у него рефрактерная почка, когда он не может добиться адекватного количества мочи. Как быть.
Начнем с самой распространенной причины рефрактерности. Это некомплаентность. Пациенты забывают принимать мочегонные либо не пьют его регулярно. Есть сопутствующая терапия, которая требует приема нестероидных противовоспалительных препаратов.
Есть еще один момент. Это, к сожалению, катастрофическое снижение скорости клубочковой фильтрации. Если скорость ниже 40, то первое, что должен сделать терапевт – отказаться от назначения Гидрохлортиазида и подумать о переводе пациента на повседневный прием петлевого диуретика.
Еще один вопрос, на который нужно обратить внимание. Мочегонные препараты никогда не будут эффективны, если вы не контролируете ренин-ангиотензин-альдостероновую систему. Ингибиторы АПФ обязательны у любого пациента, который получает терапию мочегонными препаратами.
Дальше начинается высший пилотаж терапевта – это комбинированная диуретическая терапия. Если вы не достигли эффекта на простой терапии, подумайте о комбинации.
Этапы комбинации. Нет эффекта на простом петлевом диуретике – увеличьте дозу. Нет эффекта – подумайте о способе введения. Возможно, отечный синдром таков, что внутримышечное введение или пероральное не будет эффективно. Тогда надо переходить на внутривенный прием. Если внутривенный прием, терапевт должен знать, что разные скорости окажут разный мочегонный эффект.
Давайте их вспомним. Введение болюсно будет менее эффективно, чем введение капельно на протяжении длительного временного интервала. Если вы не достигли эффекта на петлевом диуретике, комбинируйте его либо с тиазидным (это страшно токсично для почки, но будет эффективно по объему выведенной воды) или комбинируйте со Спиронолактоном. Когда вы добавляете или убираете мочегонный препарат, всегда помните о том, что на Торасемиде наименьшее количество побочных эффектов.
29:21
Но самым главным для нас эффектом будет закон, который звучит так: достигнув эффекта, титруй мочегонный препарат на меньшие дозы. Дольше всех живут больные с ХСН, получающие минимальные дозы мочегонных препаратов. Это крайне важно. Таков срез современного применения мочегонных препаратов в современном лечении ХСН.
Что нас ждет в будущем? Несколько новых классов препаратов. Блокаторы рецепторов аденозина. Они сейчас уже вышли на этап клинических исследований. Это Ролофилин. Это обязательно антагонисты рецепторов вазопрессина (селективные или неселективные). Они уже вышли в повседневную практику. Это пептиды с натрийуретическим эффектом.
Терапия мочегонными препаратами как была, так и остается трудной главой в повседневной практике терапевта, требующей глубоких знаний и высокого пилотажа терапевта в назначении мочегонных препаратов.
Благодарю вас за внимание и честь, которую вы мне оказали.
Владимир Ивашкин: Спасибо большое. Если проанализировать или вспомнить имена всех тех, кто своим вкладом внес в создание этой лестницы эффективности диуретиков, как вы думаете, ученый, который обнаружил мочегонное действие дигиталиса, и вообще нашел дигиталис, получил бы он Нобелевскую премию? Или все-таки был отодвинут другими более современными производителями или создателями мочегонных средств?
Григорий Арутюнов: Нет, я думаю, что ему бы обязательно дали, потому что он повернул вектор клинического мышления. Все-таки интернист, и его осмысление пациента было повернуто раз и навсегда. Стало совершенно другое восприятие пациента, совершенно другое виденье будущего этого пациента. Я думаю, что вклад, который он внес в историю, невозможно переоценить.
Владимир Ивашкин: У него не было химической лаборатории с большим количеством сотрудников. Он просто думал.
Григорий Арутюнов: Он был врач, который смотрел на больного, щупал, слушал, понимал.
Владимир Ивашкин: Спасибо большое.
Сравнительная эффективность и безопасность длительного применения торасемида и фуросемида у больных с компенсированной сердечной недостаточностью. Влияние на маркеры фиброза миокарда
Статьи
Опубликовано в журнале:
«Сердечная Недостаточность» Том 14, № 2, 2013г.
Агеев Ф. Т., Жубрина Е. С., Середенина Е. М, Титов В. Н., Масенко В. П., Коткина Т. И. — НИИ клинической кардиологии им. А. Л. Мясникова ФГБУ «РКНПК» МЗ РФ
Гиляревский С. Р., Голшмид М. В. Синицина И. И. — ГБОУ ДПО «РМАПО» МЗ РФ
Мареев В. Ю. — ФГБОУ ВПО «МГУ им. М. В. Ломоносова»,
Хосева Е. Н. — ГБОУ ВПО «Первый МГМУ имени И.М. Сеченова» МЗ РФ
Деев А. Д., Лукина Ю. В. — ФГБУ «ГНИЦПМ» МЗ РФ
Малишевский М. В., Рогожкина Ю. А. — ГБОУ ВПО «ТюмГМА» МЗ РФ
Сусликов А. В. — ФГБУЗ «БПНЦ РАН»
Резюме
Актуальность. Применение петлевых диуретиков играет важную роль в терапии симптоматической ХСН.
Цель. Сравнительная оценка клинической эффективности торасемида (Тригрим®, Польфарма АО, Польша) и фуросемида (ОАО «Мосхимфармпрепараты им. Н. А. Семашко») у больных ХСН и их влияние на маркеры фиброза миокарда.
Материалы и методы. 108 больных с компенсированной ХСН II–III ФК (по NYHA), находившихся на стандартной терапии СН, были рандомизированы в группы получающих торасемид (n=55, средняя доза 9,8±5,9 мг) или фуросемид (n=53, средняя доза 28,7±14,7 мг). Исходно и спустя 6 месяцев терапии у всех больных проводилась оценка клинического и гемодинамического статуса, качества жизни и функцио нального состояния ЛЖ, а также определялись уровни показателей электролитного обмена, альдостерона, С-терминального пропептида проколлагена I типа (СICP), маркера синтеза коллагена I типа, и С-терминального телопептида коллагена I типа (CITP), маркера деградации коллагена I типа в сыворотке крови.
Результаты. Настоящее исследование показало безопасность и эффективность применения петлевых диуретиков торасемида и фуросемида в плане снижения среднего ФК и тяжести клинического состояния, повышения качества жизни больных умеренной компенсированной ХСН (все р Заключение. Настоящее исследование демонстрирует, что терапия как торасемидом, так и фуросемидом является безопасной и эффективной в плане снижения ФК и повышения качества жизни больных с компенсированной ХСН. Однако клинико-гемо-динамическая эффективность торасемида превосходит фуросемид, что, вероятно, связано с наличием у торасемида дополнительных антиальдостероновых механизмов влияния на функцию сердца, в том числе на процессы синтеза коллагена I типа.
Ключевые слова: NT-proBNP, альдостерон, маркеры фиброза, петлевой диуретик, ХСН
Summary
Background. Te use of loop diuretics plays an important role in therapy for symptomatic CHF.
Aim. Comparative evaluation of clinical efcacy of torasemide (Trigrim®, Polpharma, Poland) and furosemide (N. A. Semashko Moskhimfarmpreparaty) in patients with CHF and effect of these therapies on markers of myocardial fibrosis.
Materials and methods. 108 patients with compensated II–III NYHA FC CHF receiving a standard therapy for HF were randomized to groups receiving torasemide (n=55; mean dose, 9.8±5.9 mg) or furosemide (n=53; mean dose, 28.7±14.7 mg). Clinical and hemodynamic status, quality of life, LV function, and serum levels of electrolytes, aldosterone, procollagen type I C-terminal propeptide (PICP), the marker of type I collagen synthesis, and С-terminal telopeptide of collagen type I (CITP), the marker collagen type I degradation.
Results. Study results demonstrated safety and efficacy of the loop diuretics, torasemide and furosemide, for reducing the average FC and severity of clinical condition and increasing the quality of life in patients with moderately compensated CHF (р Keywords: NT-proBNP, aldosterone, fibrosis markers, loop diuretic, CHF
Петлевые диуретики играют важную роль в терапии больных как острой, так и хронической СН [1, 2]. В условиях венозного застоя уменьшение объема циркулирующей крови на фоне диуретической терапии приводит к снижению диастолического давления в желудочках и к быстрому симптоматическому улучшению. Именно этот механизм долгое время рассматривался как единственный по влиянию данного класса препаратов на выраженность симптомов и качество жизни больных ХСН. При этом априори было принято считать, что более эффективным диуретиком является тот, который оказывает более мощное мочегонное влияние. Своеобразным «эталоном» мочегонного средства для лечения ХСН многие годы оставался петлевой диуретик фуросемид. Однако в 2002 году было завершено большое многоцентровое исследование TORIC, в котором фуросемид сравнивался с новым петлевым диуретиком торасемидом у больных с клинически выраженной СН. В этом исследовании торасемид достоверно превзошел фуросемид не только по способности улучшать клинико-функциональное состояние, но и по влиянию на смертность больных ХСН, хотя это и не было запланированной конечной точкой [3].
Механизмы благоприятного влияния торасемида на течение ХСН еще не до конца определены, но, вероятнее всего, связаны с дополнительными (не диуретическими) свойствами этого препарата. Так, в отличие от фуросемида, торасемид показал способность положительно влиять на активность РААС [4, 5]. В исследованиях in vitro торасемид ингибировал АII индуцированную вазоконстрикцию и стимулировал сосудистые ростовые процессы, а также уменьшал выработку альдостерона и препятствовал его связыванию с соответствующими рецепторами [6–10]. При этом антиальдостероновое действие торасемида представляется особенно важным, поскольку в соответствии с современными представлениями альдостерону отводится ключевая роль не только в развитии электролитных расстройств, но и в прогрессировании фибротических процессов в миокарде и в снижении его податливости, что приводит к появлению и прогрессированию как диастолической, так и систолической дисфункции сердца. Именно этот факт позволяет объяснять превосходство торасемида перед другими диуретиками по влиянию на течение заболевания и, возможно, прогноз больных ХСН.
С клинической же точки зрения такое комбинированное мочегонное и антиальдостероновое действие торасемида может быть наиболее ценно на этапе поддерживающей диуретической терапии, в условиях не столько стационарного, сколько амбулатарно-поликлинического ведения больных ХСН.
Доказано, что неадекватная терапия мочегонными (чаще всего фуросемидом), использование малых доз препарата и режима «выходного дня», когда акцент терапии переносится на субботу–воскресенье, вызванные опасением врачей развития чрезмерной дегидратации и гипокалиемии, является одной из наиболее частых причин декомпенсации СН [11–13]. Уникальные свойства торасемида, включая благоприятный для амбулаторного приема фармакокинетический профиль (бoльшее время полувыведения и продолжительности действия, а также более высокая биодоступность по сравнению с фуросемидом), могут позволить преодолеть эти трудности и опасения поддерживающей диуретической терапии [14, 15].
Целью настоящего исследования было сравнение безо пасности длительной терапии и влияния торасемида (Тригрим®, Польфарма АО, Польша) и фуросемида (ОАО «Мосхимфармпрепараты им. Н. А. Семашко») на течение заболевания и качество жизни, функцию ЛЖ и уровень N-концевого фрагмента предшественника мозгового натрийуретического пептида (NT-proBNP), а также на содержание альдостерона и биохимических маркеров баланса коллагена I типа у пациентов с компенсированной ХСН без очевидных признаков задержки жидкости в организме и не нуждающихся во внутривенном введении петлевых диуретиков.
Материалы и методы
В исследование были включены 108 больных старше 18 лет с признаками умеренной или тяжелой ХСН, несмотря на прием стандартной терапии по поводу ХСН, и при наличии в анамнезе данных о задержке жидкости в организме, потребовавших в свое время госпитализации и / или внутривенного применения диуретиков. При этом получаемая на момент включения в исследование терапия ХСН должна была быть стабильной (по группам используемых препаратов) на протяжении, по меньшей мере, 6 последних месяцев.
В исследование не включались больные с клиническими признаками очевидной задержки жидкости в организме на момент включения: отеками нижних конечностей, гепатомегалией, набуханием шейных вен, влажными хрипами в легких, требующими внутривенного введения петлевых диуретиков. Критериями невключения также были: клинические признаки гиповолемии, гипокалиемии (уровень калия –1; гемодинамически значимые поражения клапанного аппарата сердца; констриктивный перикардит или гемодинамически значимый перикардиальный выпот; легочное сердце или другие заболевания, связанные с изолированной правожелудочковой недостаточностью; ОКС или реваскуляризация миокарда менее чем за 3 месяца до включения больного в исследование; состояния, сопровождающиеся изменением содержания маркеров баланса коллагена (заболевания соединительной ткани, онкологические, ревматологические заболевания, выраженный фиброз печени, легких, клинически выраженный гипо- / гипертиреоз); умеренная / выраженная дисфункция почек (креатинин в сыворотке >130 мкмоль / л).
От каждого больного было получено письменное информированное согласие на добровольное участие в исследовании.
Всем больным проводились клиническое обследование с определением ФК ХСН по NYHA, тяжести клинического состояния с использованием шкалы оценки клинического состояния (ШОКС), оценка качества жизни по данным Миннесотского опросника качества жизни MLHFQ. Всем больным регистрировалась ЭКГ в 12 отведениях, выполнялись трансторакальная ЭхоКГ и допплер–ЭхоКГ в покое, осуществлялся забор лабораторных образцов крови с целью определения уровней NT-proBNP, альдо-стерона и маркеров синтеза (С-терминального пропептида проколлагена I типа, CICP) и распада (С-терминальный телопептид коллагена I типа, CITP) коллагена I типа, показателей электролитного отмена, расчет клиренса креатинина по формуле MDRD.
Эхокардиографическое исследование выполнялось опытными специалистами, находящимися в неведении относительно получаемой больными терапии. Фракция выброса ЛЖ рассчитывалась по стандартной методике Simpson. Состояние диастолической функции ЛЖ оценивалось с помощью импульсного допплеровского исследования трансмитрального кровотока и тканевого допплеровского исследования диастолического подъема основания ЛЖ. При этом определялись следующие показатели: соотношение максимальных скоростей раннего диастолического наполнения и наполнения в систолу предсердий (Е / А) и соотношение скорости Е к максимальной скорости диастолического подъема основания ЛЖ в раннюю диастолу (Е / e’) [16].
Уровень NT-proBNP в плазме определялся методом электрохемилюминисценции. Маркеры фиброза и альдостерона в плазме определялись иммуно-ферментным методом. Переносимость исследуемого препарата оценивалась по частоте возникновения гипокалиемии (В рамках оценки безопасности исследования отслеживались любые нежелательные явления, а также серьезные нежелательные явления (смерть больного; угроза жизни больного; явление, требующее госпитализации или продления текущей госпитализации; приводящее к стойкой и значительной нетрудоспособности и / или инвалидности; приводящее к появлению врожденных аномалий). Нежелательным считался любой негативный признак, симптом или медицинское состояние (заболевание), развивающееся после начала приема исследуемого препарата и не обязательно имеющее причинно-следственную связь с лечением (препаратом).
Дизайн исследования
Все больные, подошедшие по критериям включения / исключения для участия в исследовании, в день скрининга / рандомизации (визит 0) были случайным образом распределены в группу приема торасемида 10-20 мг / сут (n=55) или в группу приема фуросемида 10-80 мг / сут (n=53). Стартовая доза исследуемого препарата выбиралась в зависимости от характера используемой мочегонной терапии на момент включения. Помимо исследуемых препаратов, все больные принимали средства стандартной терапии по поводу ХСН (иАПФ или блокаторы ангиотензиновых рецепторов в оптимальной дозе и β-адреноблокаторы в обязательном порядке; антагонисты альдостерона, сердечные гликозиды по показаниям). Титрование дозы петлевых диуретиков осуществлялось на визите 1. При этом на визитах 1 (7-14 дней) и 2 (3 месяца) проводилось клиническое обследование и осуществлялся забор крови, а на финальном визите 3 (6 месяцев), помимо этого, выполнялась и трансторакальная ЭхоКГ в покое (рис. 1).
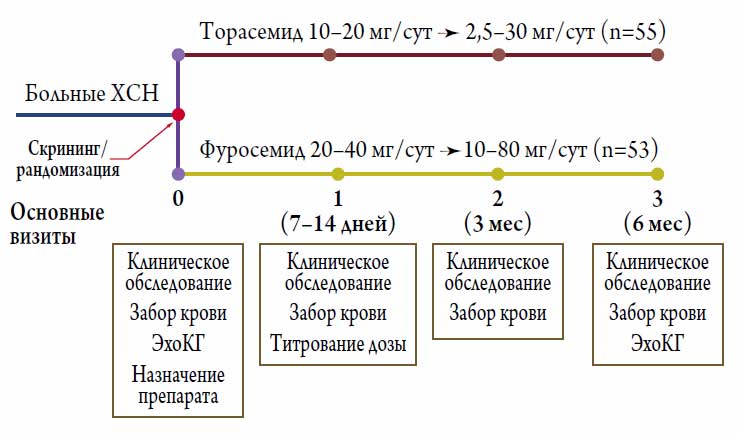
Рисунок 1. Дизайн исследования
Достигнутые средние дозы для обоих препаратов были клинически сопоставимы и составили: 9,8±5,9 мг для торасемида и 28,7±14,7 мг для фуросемида (соотношение средних доз торасемида и фуросемида примерно 1:3).
Статистическая обработка результатов
Статистический анализ полученных результатов проводили с помощью пакета прикладных статистических программ SAS 6.12 (Statistical Analisis System, США). Статистически значимыми считали различия, если вероятность абсолютно случайного их характера не превышала 5 % (p Таблица 1.
Исходная характеристика больных, распределенных в группы торасемида и фуросемида
| Показатель | Торасемид (n=55) |
Фуросемид (n=53) |
р |
|---|---|---|---|
| Клинические данные | |||
| Возраст, лет | 65±8 | 66±7 | н.д. |
| Мужчины / женщины, % | 23 (42 %) / 32 (58 %) |
26 (49 %) / 27 (51 %) |
н.д. |
| Длительность ХСН, лет | 4,8±4,3 | 5,3±3,7 | н.д. |
| Ишемическая / неишемическая этиология СН,% | 26 (47 %) / 29 (53 %) |
23 (43 %) / 30 (57 %) |
н.д. |
| Средний ФК ХСН, баллы | 2,56±0,5 | 2,26±0,68 | н.д. |
| 6-минутный тест ходьбы, м | 298±71 | 289±92 | н.д. |
| Миннесотский вопросник качества жизни, баллы | 48±15 | 47±18 | н.д. |
| Шкала оценки клинического состояния ШОКС, баллы | 4,9±2,9 | 4,2±2,3 | н.д. |
| ЧСС, мин –1 | 76±13 | 75±13 | н.д. |
| САД, мм рт. ст. | 126±14 | 129±12 | н.д. |
| ДАД, мм рт. ст. | 79±9 | 79±8 | н.д. |
| Инструментально-лабораторные данные | |||
| ФВ ЛЖ, % | 47±12 | 46±12 | н.д. |
| Е/Е’ | 16,1±4,7 | 16,6±7,0 | н.д. |
| NT-proBNP, пг / мл | 1598±3474 | 1855±4920 | н.д. |
| Терапия | |||
| Ингибиторы АПФ, % | 41 (74 %) | 44 (83 %) | н.д. |
| БРА,% | 14 (26 %) | 9 (17 %) | н.д. |
| Петлевые диуретики, % | 29 (52 %) | 37 (69 %) | н.д. |
| Тиазидные диуретики, % | 31 (56 %) | 22 (41 %) | н.д. |
| Дигоксин, % | 11 (20 %) | 16 (30 %) | н.д. |
| Спиронолактон, % | 40 (72 %) | 41 (77 %) | н.д. |
| β-блокаторы, % | 49 (89 %) | 49 (92 %) | н.д. |
Данные представлены как среднее значение по группе ± стандартное отклонение среднего.
Результаты
Исходная характеристика больных, распределенных в группы торасемида и фуросемида, представлена в таблице 1. По исходным демографическим, клиническим и ЭхоКГ показателям группы сравнения были сопоставимы друг с другом.
За время исследования выбыли 13 больных, из них по причине неблагоприятных событий – 3, из-за отказа от дальнейшего участия в исследовании – 10.
Бoльшее количество нежелательных событий, в т. ч. прогрессирование ХСН, ассоциировалось с терапией фуросемидом, однако статистической значимости данные различия не достигли (р=0,07) (рис. 2).
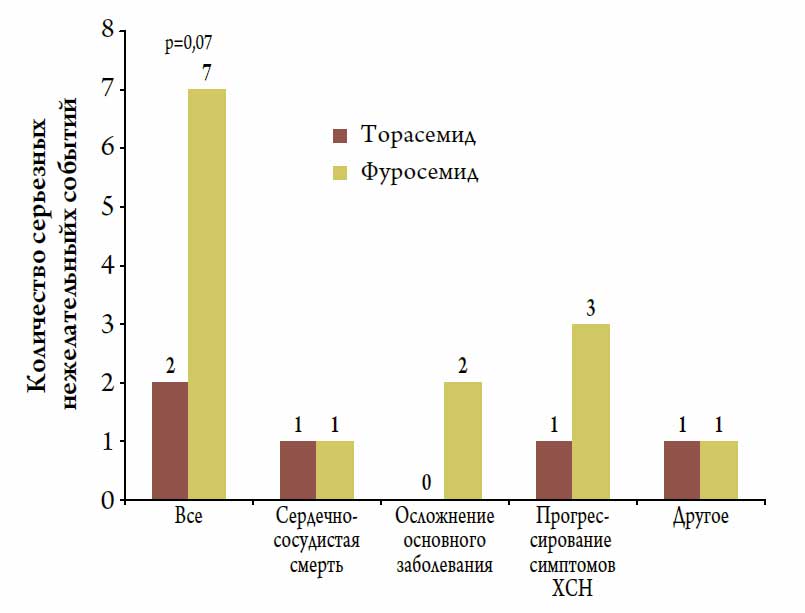
Рисунок 2. Частота развития серьезных нежелательных событий на фоне длительной терапии торасемидом и фуросемидом у пациентов с компенсированной ХСН II-III ФК
Влияние терапии торасемидом и фуросемидом на клинико-функциональный статус и качество жизни больных ХСН (табл. 2)
Терапия исследуемыми препаратами не сопровождалась клинически значимыми колебаниями АД и ЧСС.
За время исследования в обеих группах произошло достоверное снижение среднего ФК NYHA в среднем на 12 % в группе торасемида и на 5 % в группе фуросемида (р
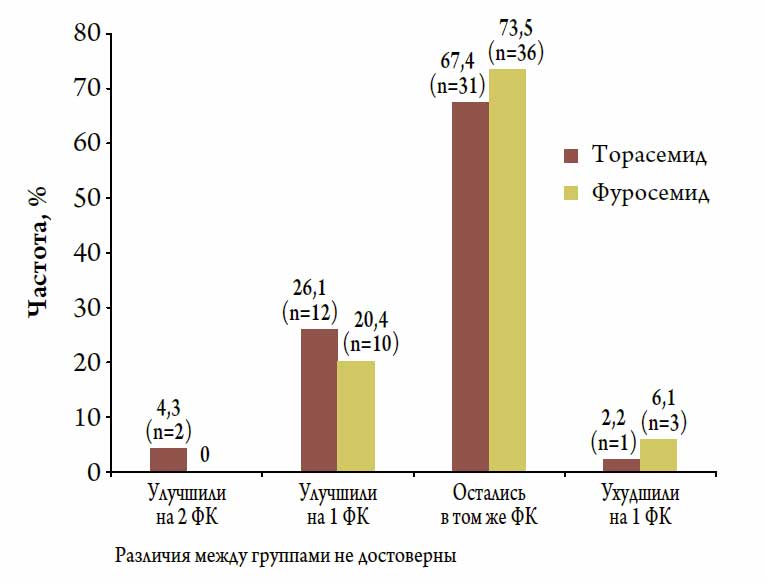
Рисунок 3. Динамика ФК (по NYHA) у пациентов с ХСН, получающих терапию торасемидом и фуросемидом
Кроме того, на фоне терапии как торасемидом, так и фуросемидом отмечалось достоверное (р Таблица 2.
Динамика показателей клинико-функционального статуса, качества жизни, функции ЛЖ и уровня NT-proBNP
| Показатель | Торасемид (n=46) | Фуросемид (n=49) | р групповых динамик |
||||
|---|---|---|---|---|---|---|---|
| Исходно | 6 месяцев | Δ, % | Исходно | 6 месяцев | Δ, % | ||
| Средний ФК NYHA | 2,56±0,50 | 2,26±0,68**** | -11,9±22,3 | 2,51±0,50 | 2,37±0,64** | -5,1±21,8 | н.д. |
| Шкала ШОКС, баллы | 4,95±2,88 | 2,83±2,27**** | -37,0±35,6 | 4,21±2,27 | 2,90±1,71**** | -23,3±29,4 | |
| 6-минутный тест ходьбы, м | 298±71 | 341±95*** | +18,б±41,8 | 289±92 | 310±91 | +25,6±86,7 | н.д. |
| Опросник MLHFQ, баллы | 48±15 | 37±14**** | -9,9±24,4 | 47±17 | 38±14**** | -4,65±18,7 | |
| САД, мм рт. ст. | 126±14 | 125±12 | -0,3±10,4 | 129±12 | 127±12 | -0,7±8,9 | н.д. |
| ДАД, мм рт. ст. | 79±9 | 79±8 | +0,4±11,9 | 79±8 | 76±8 | -2,2±12,9 | н.д. |
| ЧСС, мин -1 | 76±13 | 74±13 | -1,1±14,1 | 75±13 | 75±14 | +1,8±15,9 | н.д. |
| ИМТ, кг / м2 | 31,4±5,4 | 31,5±5,0 | -0,6±3,4 | 30,5±5,9 | 30,3±5,9** | -1,0±3,5 | н.д. |
| ФВ ЛЖ, % | 47,5±12,5 | 50,9±10,5** | +6,2±16,0 | 45,9±12,3 | 48,1±12,5* | +6,7±19,7 | н.д. |
| КДО, мл | 169,8±81,3 | 163,8±88,2 | +0,02±28,8 | 161,5±67,1 | 154,б±69,2 | -3,4±29,3 | н.д. |
| КСО, мл | 96,5±72,8 | 86,4±54,9 | +4,6±41,5 | 92,3±52,2 | 84,7±51,1* | -2,4±36,1 | н.д. |
| Е / А | 1,56±0,90 | 1,42±1,29 | -1,5±28,4 | 1,29±0,64 | 1,41±0,45 | 28,2±18,3 | н.д. |
| Е /е’ | 16,1±4,7 | 14,2±3,5** | -5,8±23,8 | 16,6±7,0 | 16,1±5,9 | +17,2±6,0 | н.д. |
| NT-proBNP, пг / мл | 757 [185; 1379] |
451 [98; 1329]*** |
-22,3 [-55,1; 4,4] |
769 [164; 1263] |
789 [1952; 1522] |
-4,9 [-37,9; 36,3] |
0,08 |
| Калий, ммоль / л | 4,59±0,54 | 4,45±0,55 | -2,4±13,6 | 4,39±0,49 | 4,22±0,45* | -2,9±10,7 | н.д. |
| Креатинин, мкмоль / л | 86,6±26,3 | 85,4±19,3 | +1,8±16,5 | 83,7±19,3 | 82,7±16,3 | +2,7±20,5 | н.д. |
* — р
Влияние терапии торасемидом и фуросемидом на уровни альдостерона и маркеров распада и синтеза коллагена I типа у больных ХСН (табл. 3)
Лишь прием торасемида (но не фуросемида) приводил к достоверному и значительному снижению уровня альдостерона (в среднем на 22,6 %, p Влияние терапии торасемидом и фуросемидом на функциональное состояние ЛЖ и уровень NT-proBNP (табл. 2)
За время исследования на фоне терапии торасемидом отмечалось достоверное повышение ФВ ЛЖ в среднем на 6,2 % (р
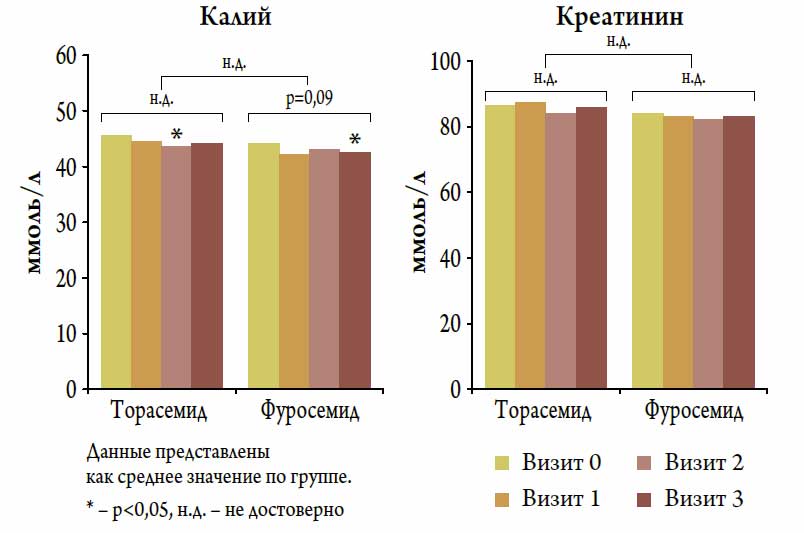
Рисунок 4. Повизитная динамика уровней калия и креатинина на фоне терапии торасемидом и фуросемидом
Влияние терапии торасемидом и фуросемидом на уровни калия и креатинина (табл. 2)
За время исследования в группе торасемида и фуросемида отмечалось незначительное и недостоверное снижение уровня калия плазмы в среднем на 2,4 % и 2,9 % соответственно (рис. 4). При этом частота случаев отклонения уровня калия от нормы (менее 3,5 ммоль / л и более 5,6 ммоль / л) была невелика и достоверно не отличалась между группами: 5 (10,8 %) случаев в группе торасемида и 3 (6,1 %) случая в группе фуросемида, р=0,2. Средний уровень креатинина в обеих группах также практически не менялся (рис. 4 и табл. 2).
Таблица 3.
Динамика уровней альдостерона и маркеров синтеза и распада коллагена I типа на фоне терапии торасемидом и фуросемидом
| Показатель | Торасемид (n=46) | Фуросемид (n=49) | р групповых динамик |
||||
|---|---|---|---|---|---|---|---|
| Исходно | 6 месяцев | Δ, % | Исходно | 6 месяцев | Δ, % | ||
| Альдостерон, пг/мл | 235,4 [121,0; 452,5] |
168,5** [119,4; 360] |
-22,6 [-72,9; 82,6] |
168,0 [84,9; 335,0] |
140,9 [73,9; 300,0] |
+12,5 [-49,9; 138,9] |
0,08 |
| CICP, нг/мл | 88,9 [60,3; 118,8] |
97,3 [82,4; 113,2] |
+13,9 [-13,8; 42,3] |
85,2 [69,1; 103,4] |
96,9** [81,6; 118,2] |
+17,8 [-7,4; 60,5] |
н.д. |
| CITP, нг/мл | 0,29 [0,17; 0,47] |
0,27* [0,10; 0,35] |
-14,9 [-53,5; 25,9] |
0,26 [0,15; 0,40] |
0,23 [0,14; 0,45] |
+7,7 [-29,0; 39,5] |
н.д. |
| CICP/CITP | 317 [211; 489] |
336 [278; 777] |
+7 [-17,4; 117,4] |
323 [200; 514] |
377** [243; 740] |
+26,4 [-17,8; 60,8] |
н.д. |
* – р
С целью более точного описания состояния коллагенового обмена нами были рассчитаны отношения СIСP / CITP для каждой группы больных. Увеличение этого соотношения в динамике свидетельствует в пользу смещения баланса коллагена в сторону его образования и, наоборот, уменьшение – в пользу его распада. На фоне терапии торасемидом не наблюдалось достоверной динамики этого показателя. В то же время применение фуросемида ассоциировалось с достоверным ростом этого соотношения на 26,4 % (р Обсуждение
Сравнительные исследования торасемида с другими диуретиками, главным образом с фуросемидом, при СН выполнялись и ранее, однако, как правило, с участием более тяжелых, декомпенсированных пациентов или в условиях стационара [3, 17, 18]. Так, в исследовании TORIC более 50 % больных имели III или IV (49,4 и 2,4 % соответственно) ФК по классификации NYHA [3].
Российское сравнительное исследование ДУЭЛЬ также проводилось в стационарных условиях у больных ХСН в основном с III ФК NYHA, с признаками застоя, требующих активной диуретической терапии [17]. Настоящее исследование стало одним из первых, целью которого было сравнение петлевых диуретиков у более легких и компенсированных больных (средний ФК составил 2,3–2,6 NYHA), не требующими внутривенного применения диуретиков, в условиях амбулаторной поддерживающей терапии.
Наши данные показали высокую эффективность и безопасность поддерживающего лечения компенсированных больных ХСН как фуросемидом, так и торасемидом, что обеспечивалось не только «мощностью» этих диуретиков, но и тщательным подбором их дозы под контролем клинического состояния, гемодинамики, функции почек и электролитов. Достигнутые средние дозы препаратов составили 9,8±5,9 мг для торасемида и 28,7±14,7 мг для фуросемида, что было несколько меньше, чем в исследовании ДУЭЛЬ (21,7 и 75,6 мг соответственно) и, вероятно, связано с тем, что в наше исследование включались более легкие больные, не нуждавшиеся в активной дегидратации. В исследовании TORIC, в котором тяжесть состояния больных ХСН была несколько выше, чем у нас, стартовая доза препаратов была также больше и составила 10 и 40 мг соответственно.
Тщательная титрация доз препаратов в нашей работе позволила минимизировать риск развития такого опасного осложнения, как клинически значимые гипо- или гиперкалиемия, которые за 6 месяцев терапии наблюдались лишь у 6,1 % больных в группе фуросемида и у 10,8 % больных в группе торасемида. Для сравнения: частота клинически значимых отклонений уровня калия в исследовании TORIC за 9,2 месяцев наблюдения составила 12,9 и 17,9 % на фоне торасемида и фуросемида соответственно. Следует добавить, что в отличие от больных в исследованиях ДУЭЛЬ и TORIC, в нашем исследовании до 75 % больных на старте получали терапию спиронолактоном.
Кроме того, такая стратегия назначения диуретиков позволила избежать другого опасного осложнения диуретической терапии — чрезмерного снижения давления наполнения ЛЖ с развитием синдрома фиксации сердечного выброса (СФСВ). СФСВ развивается вследствие избыточного диуреза и характеризуется снижением сердечного выброса и / или невозможностью его повышения при физической нагрузке. Клинически он проявляется слабостью, тахикардией, ортостатической гипотензией, а при выраженном снижении cердечного выброса — тяжелой гипотонией, повышением уровня креатинина и оли-гурией (преренальная азотемия) [19]. В рамках же нашего исследования прием как фуросемида, так и торасемида не сопровождался клинически значимым снижением АД или повышением ЧСС, а значительного повышения креатинина не было зарегистрировано ни у одного пациента.
Нами было показано, что терапия как торасемидом, так и фуросемидом улучшала клиническое состояние и качество жизни больных с умеренной компенсированной ХСН, что проявлялось примерно равным снижением среднего ФК по NYHA, баллов MLHFQ и ШОКС. Тем не менее детальный анализ выявил, что терапия торасемидом оказывает более выраженное положительное влияние на основные клинические показатели больных ХСН. Так, только при использовании торасемида отмечался достоверный прирост в дистанции 6-мин теста ходьбы, а также достоверное улучшение систолической (увеличение ФВ ЛЖ) и диастолической (отношение Е / е’) функции ЛЖ. Преимущество торасемида перед фуросемидом по влиянию на клиническое и функциональное состояние отмечалось и в ранее опубликованных работах [3, 17, 20-22]. Наше исследование стало одним из первых, в котором было показано, что амбулаторная терапия торасемидом, но не фуросемидом, приводит к достоверному снижению уровня NT-proBNP (-22 %), содержание которого тесно коррелирует с тяжестью клинического состояния и прогнозом у больных ХСН[23-25].
Необходимо отметить, что торасемид и фуросемид в рамках настоящего исследования использовались в эквивалентных по диуретической эффективности дозах в соотношении 1: 3 соответственно. Это позволило сделать вывод, что выявленное нами более благоприятное влияние торасемида на течение ХСН, вероятно, было связано с наличием у этого препарата дополнительных свойств, не связанных с его диуретическим действием.
Обеспечение адекватного прироста сердечного выброса при нагрузке является одной из жизнеобеспечивающих функций сердца и осуществляется в том числе за счет увеличения сократимости миокарда, обеспечиваемой механизмом Франка-Старлинга: увеличением давления наполнения ЛЖ с последующим растяжением кардиомиоцитов, приводящим к росту сократимости и сердечного выброса. Причем именно увеличение давления наполнения ЛЖ, несмотря на свою компенсаторную функцию, при развитии СН носит, как правило,чрезмерный характер, приводя к основным клиническим проявлениям ХСН и ассоциируясь с неблагоприятным прогнозом у данной категории больных [26].
Диуретический эффект петлевых диуретиков позволяет добиться быстрого уменьшения сердечной преднагрузки и давления наполнения ЛЖ. Если при этом удается добиться еще и улучшения механических свойств миокарда, в том числе за счет влияния на баланс миокардиального коллагена, то это приводит к еще большему (дополнительному) снижению давления наполнения ЛЖ. Если при этом удается добиться еще и улучшения механических свойств миокарда, в том числе за счет влияния на баланс миокардиального коллагена, то это приводит к еще большему (дополнительному) снижению давления наполнения ЛЖ. Для петлевых диуретиков такая способность прямо улучшать механические свойства миокарда описана только для торасемида. Исследования Lopez B. с применением метода эндомиокардиальной биопсии показали способность торасемида уменьшать объемную фракцию миокардиального коллагена и уровня С-концевого пептида проколлагена I типа [27]. Механизмы реализации такого положительного действия торасемида на состояние миокарда при ХСН, вероятнее всего, связаны с его самостоятельным модулирующим влиянием на активность нейро-гуморальных систем. В ряде исследований было показано, что в отличие от фуросемида торасемид уменьшает выработку альдостерона, а также препятствует его связыванию с соответствующими рецепторами [7-9], в том числе локально на уровне кардиомиоцитов [10].
Результаты нашего исследования также показали, что торасемид и фуросемид по-разному влияют на баланс коллагена. Так, прием фуросемида ассоциировался с достоверным повышением уровня маркера синтеза коллагена I типа CICP и сдвигом соотношения СICP / CITP в сторону увеличения. Это свидетельствовало о том, что применение фуросемида не сдерживало процессов фиброобразования и смещения баланса коллагена в сторону его синтеза. В то же время на фоне приема торасемида не отмечалось никакой негативной динамики ни одного из этих показателей, что могло свидетельствовать о том, что терапия торасемидом, как минимум, сдерживала негативные тенденции в обмене коллагена, свойственные течению СН.
Тот факт, что терапия торасемидом в нашем исследовании не сопровождалась ожидаемым снижением уровня CICP и соотношения СICP / CITP, возможно, связан с относительно коротким (6 мес) периодом наблюдения, недостаточным для оценки динамики фиброза. Тем не менее 6 месяцев лечения торасемидм оказалось достаточным для того, чтобы добиться отношения E / e’, наиболее тесно связанного с давлением наполнения ЛЖ [11]. Это, в свою очередь, перекликается с результатами ранее проведенных исследований, также продемонстрировавших более выраженное положительное влияние на диастолическую функцию ЛЖ торасемида по сравнению с фуросемидом [20, 28].
СПИСОК ЛИТЕРАТУРЫ
1. McMurray JJ, Adamopoulos S, Anker SD et al. ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure 2012: The Task Force for the Diagnosis and Treatment of Acute and Chronic Heart Failure 2012 of the European Society of Cardiology. Developed in collaboration with the Heart Failure Association(HFA) of the ESC. Eur Heart J. 2012;33 (14):1787-1847.
2. Национальные рекомендации ВНОК и ОССН по диагностике и лечению ХСН (третий пересмотр). Журнал Сердечная Недостаточность. 2010;11 (1):3-62.
3. Cosin J, Diez J. Torasemide in chronic heart failure: Results of the TORIC study. Eur J Heart Fail. 2002;4 (4):507-513.
4. Преображенский Д. В., Некрасова Н. И., Талызина И. В., Патарая С. А. Торасемид — петлевой диуретик нового поколения: особенности фармакологии и клиническая эффективность при сердечной недостаточности. Журнал Сердечная недостаточность. 2010;11 (5):294–300.
5. Friedel H, Buckley MM. Torasemide. A review of its pharmacology and therapeutic potential. Drugs. 1991;41 (1):81–103.
6. Fortuno A, Muniz P, Ravassa S et al. Torasemide inhibits angioten? sin II?induced vasoconstriction and intracellular calcium increase in the aorta of spontaneously hypertensive rats. Hypertension. 1999;34 (1):138–143.
7. Uchida T, Yamanaga K, Nishikawa M et al. Antialdosteronergic efect of torasemide. Eur J Pharmacol. 1991;205 (2):145–150.
8. Uchida T, Yananaga K, Kido H et al. Diuretic and vasodilating actions of torasemide. Cardiology. 1994;84 (Suppl 2):14–17.
9. Goodfriend TL, Ball DL, Oelkers W, Bahr V. Torasemide inhibits aldosterone secretion in vitro. Life Sci. 1998;63 (3):PL45–50.
10. Tsutamoto T, Sakai H, Wada A et al. Torasemide inhibits transcardiac extraction of aldosterone in patients with congestive heart failure. J Am Coll Cardiol. 2004;44 (11):2252–2253.
11. Brater DC. Diuretic therapy. N Engl J Med. 1998;339 (6):387–395.
12. Cody RJ, Kubo SH, Pickworth KK. Diuretic treatment for the sodium retention of congestive heart failure. Arch Intern Med. 1994;154 (17):1905–1914.
13. Беленков Ю. Н., Мареев В. Ю., Агеев Ф. Е. Хроническая сердечная недостаточность. Избранные лекции по кардиологии. – М.: «Гэотар-Медиа», 2006. – 432 с.
14. Brater DC. Benefts and risks of torasemide in congestive heart failure and essential hypertension. Drug Saf. 1996;14 (2):104–120.
15. Kido H, Ohtaki Y. Torasemide (LUPRC): a review of its pharmacological and clinical profle. Nihon Yakurigaku Zasshi. 2001;118 (2):97–105.
16. Nagueh SF, Appleton CP, Gillebert TC et al. Recommendations for the evaluation of lef ventricular diastolic function by echocardio? graphy. J Am Soc Echocardiogr. 2009;22 (2):107–133.
17. Мареев В. Ю., Выгодин В. А., Беленков Ю. Н. Диyретическая терапия Эффективными дозами пероральных диуретиков торасемида (диувера) и фуросемида в лечении больных с обострением Хронической Сердечной Недостаточности (ДУЭЛЬ– ХСН). Журнал Сердечная Недостаточность. 2011;12 (3):3–10.
18. Noe LL, Vreeland MG, Pezzella SM, Troter JP. A pharmacoeconomic assessment of torasemide and furosemide in the treatment of patients with congestive heart failure. Clin Ter. 1999;21 (5):854–866.
19. Opie L, Kaplan N. Diuretics. In: Opie L, Gersh B. (eds): Drugs for the heart (6th ed). Elsevier Saunders 2005; pp. 80–103.
20. Азизова А., Овчинников А., Агеев Ф. Сравнительное влияние торасемида и фуросемида на клинический статус и диастолическую функцию левого желудочка у больных с компенсированной сердечной недостаточностью и высоким давлением наполнения левого желудочка. Журнал Сердечная Недостаточность 2011;12 (6):326–332.
21. Muller K, Gamba G, Jaquet F, Hess B. Torasemide vs. furosemide in primary care patients with chronic heart failure NYHA II to IV – efcacy and quality of life. Eur J Heart Fail. 2003;5 (6):793–801.
22. Stauch M, Stiehl L. Controlled, double?blind clinical trial on the efcacy ans tolerance of torasemide in comparison with furosemide in patients with congestive heart failure – a multicenter study. In: Progress in Pharmacology and Clinical Pharmacology. Ed. By F. M. Eichelbaum et al. vol. 8. № 1. Stutgart New York. 1990. pp. 121–126.
23. Betencourt P. NT-proBNP and BNP: biomarkers for heart failure management. Eur J Heart Fail. 2004;6 (3):359–363.
24. Lee SC, Stevens TL, Sandberg SM et al. Te potential of brain natri-uretric peptide a biomarker for New York Heart Association class during the outpatient treatment of heart failure. J Card Fail. 2002;8 (3):149–154.
25. Koglin J, Pehlivanli S, Schwaiblmair M et al. Role of brain natriuretic peptide in risk stratifcation of patient with congestive heart failure. J Am Coll Cardiol. 2001;38 (7):1934–1941.
26. Meta-Analysis Research Group in Echocardiography (MeRGE) AMI Collaborators. Independent prognostic importance of a restrictive left ventricular flling pattern after myocardial infarction: an individual patient meta-analysis: Meta-Analysis Research Group in Echocardiography acute myocardial infarction. Circulation. 2008;117 (20):2591–2598.
27. Lopez B, Querejrta R, Gonzalez A et al. Effects of loop diuretics on myocardial fibrosis and collagen type I turnover in chronic heart failure. J Am Coll Cardiol. 2004;43 (11):2028–2035.
28. Yamato M, Sasaki T, Honda K. et al. Effects of torasemide on left ventricular function and neurohumoral factors in patients with chronic heart failure. Circ J. 2003;67 (5):384–390.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Частота побочных эффектов, приведенных ниже, определялась соответственно следующему (классификация Всемирной организации здравоохранения): очень часто (более 10 %); часто (более 1 % и менее 10 %); нечасто (более 0,1 % и менее 1 %); редко (более 0,01 % и менее 0,1 %); очень редко (менее 0,01 %), включая отдельные сообщения; частота неизвестна (не может быть оценена при помощи доступных данных).
Со стороны крови и лимфатической системы
Частота неизвестна — тромбоцитопения, лейкопения, агранулоцитоз, апластическая или гемолитическая анемия.
Со стороны обмена веществ и питания
Нечасто — гиперхолестеринемия, гипертриглицеридемия;
Частота неизвестна — снижение толерантности к глюкозе (возможна манифестация латентно протекающего сахарного диабета).
Со стороны нервной системы
Часто — головокружение, головная боль, сонливость;
Нечасто — судороги мышц нижних конечностей;
Частота неизвестна — спутанность сознания, обморок, парестезии в конечностях (ощущение онемения, «ползания мурашек» и покалывания).
Со стороны органа зрения
Частота неизвестна — нарушение зрения.
Со стороны органа слуха и лабиринтные нарушения
Частота неизвестна — нарушение слуха, звон в ушах и потеря слуха (носит, как правило, обратимый характер) обычно у пациентов с почечной недостаточностью или гипопротеинемией (нефротический синдром).
Нарушения со стороны сердечно-сосудистой системы
Нечасто — экстрасистолия, тахикардия, аритмия, усиленное сердцебиение, покраснение лица;
Частота неизвестна — чрезмерная артериальная гипотензия, ортостатическая гипотензия, коллапс, тромбоз глубоких вен, тромбоэмболия, гиповолемия.
Со стороны дыхательной системы
Нечасто — носовые кровотечения.
Со стороны пищеварительной системы
Часто — диарея;
Нечасто — боль в животе, метеоризм;
Частота неизвестна — сухость во рту, тошнота, рвота, потеря аппетита, панкреатит, диспепсические расстройства, внутрипеченочный холестаз.
Нарушения со стороны почек и мочевыводящих путей
Часто — увеличение частоты мочеиспускания, полиурия, никтурия;
Нечасто — учащенные позывы к мочеиспусканию;
Частота неизвестна — олигурия, задержка мочи (например, у пациентов с обструкцией мочевыводящих путей), интерстициальный нефрит, гематурия, повышение концентрации мочевины и креатинина в крови.
Со стороны половых органов
Частота неизвестна — нарушение потенции.
Общие расстройства и нарушения в месте введения
Нечасто — астения (истощение), жажда, слабость, повышенная утомляемость, гиперактивность, нервозность.
Лабораторные показатели
Нечасто — увеличение числа тромбоцитов;
Частота неизвестна — гипергликемия, гиперурикемия, снижение числа эритроцитов, лейкоцитов и тромбоцитов, небольшое повышение активности щелочной фосфатазы в крови, повышение активности некоторых печеночных ферментов (например, гамма- глутамилтрансферазы).
Со стороны кожи и подкожных тканей
Частота неизвестна — кожный зуд, сыпь, крапивница, полиморфная эритема, эксфолиативный дерматит, пурпура, васкулит, фотосенсибилизация.
Со стороны опорно-двигательного аппарата
Частота неизвестна — мышечная слабость.
Со стороны водно-электролитного и кислотно-щелочного баланса
Частота неизвестна — гипонатриемия, гипохлоремия, гипокалиемия, гипомагниемия, гипокальциемия, метаболический алкалоз. Симптомами, указывающими на развитие нарушений электролитного и кислотно-щелочного состояния, могут быть головная боль, спутанность сознания, судороги, тетания, мышечная слабость, нарушения ритма сердца и диспепсические расстройства; гиповолемия и дегидратация (чаще у пациентов пожилого возраста), которые могут привести к гемоконцентрации с тенденцией к развитию тромбоза.
