В статье подробно описана семиотика абдоминальной боли, классификация, дифференциальная диагностика. Обоснована необходимость оценки патогенетического механизма формирования боли у пациента при определении лечебной тактики.
Статья содержит рекомендации по активному использованию в клинической практике препарата Тримедат® для купирования абдоминальной боли после исключения ее острой органической природы.
На основании проведенных исследований авторами статьи сделаны выводы, позволяющие рассматривать Тримедат® как универсальный регулятор моторики. Препарат также купирует боли, восстанавливает флору и функциональную активность кишечника.
В клинической медицине и в гастроэнтерологии в частности такой симптом, как боль в животе, занимает главенствующее место, что обусловлено, во-первых, его распространенностью, а во-вторых, клинической и прогностической значимостью. Абдоминальная боль представляет собой типовой патологический процесс, который лишен нозологической принадлежности. Дать правильную оценку боли и выбрать тактику ведения пациента – далеко не простая задача для врача. От качества оценки боли зависит точность диагноза и своевременное начало лечения. Согласно отчету Всемирной организации гастроэнтерологов и эндоскопистов (OMGE), точность диагностики причин боли в животе к началу XXI века составила лишь 50%, а промежуток времени между появлением боли в животе и верификацией диагноза, включая злокачественные новообразования, составлял от 8 до 37 недель [1]. Международная ассоциация по изучению боли (IASP) определяет симптом боли как:
- неприятное ощущение и эмоциональное переживание, связанное с действительным или возможным повреждением тканей;
- один из видов чувствительности, возникающих вследствие поступления в ЦНС патологических импульсов с периферии без единого универсального раздражителя.
При определении тактики ведения пациента с абдоминальной болью в первую очередь нужно опираться на патогенетический механизм и клиническую классификацию боли, согласно которой боли в животе подразделяют на висцеральные, париетальные (соматические) и отраженные (иррадиирующие) [1, 2].
Классификация абдоминальной боли
Висцеральная боль возникает при раздражении болевых рецепторов органов брюшной полости (ноцицепторов), иннервируемых вегетативной нервной системой. Висцеральная боль:
- может быть схваткообразной или тупой;
- характеризуется отсутствием четкой локализации;
- может отличаться ритмичностью, т.е. быть связанной с приемом пищи, временем суток, актом дефекации;
- может сопровождаться вегетативными реакциями, такими как слабость, бледность, потливость, одышка;
- зоны восприятия боли могут быть размыты или ограничены эпигастральной, мезогастральной, гипогастральной областями;
- при повреждении пищевода, желудка, желчного пузыря, желчевыводящих путей, поджелудочной железы боли проецируются в эпигастральную область;
- при патологии тонкой, слепой кишки боли проецируются в мезогастрии (периумбиликальная область);
- при поражении толстой кишки, органов малого таза боли проецируются в гипогастральную область;
- при вовлечении в патологический процесс парных органов (почки, придатки матки) боль проецируется в боковые отделы живота.
В месте локализации боли отмечается болезненность при пальпации. Висцеральные боли являются следствием нарушения, в первую очередь, моторной функции органов. Поскольку большинство органов пищеварения – это полые органы, механизм формирования боли в значительной степени связан с нарушением тонуса их гладкой мускулатуры с преобладанием гипертонуса. Ведущие механизмы болей – это спазм и растяжение полого органа (спастическая абдоминальная боль и дистензионная боль). Париетальная боль (соматическая):
- возникает при раздражении париетальной брюшины и более четко локализуется в месте раздражения;
- боль, как правило, острая, чаще с внезапным началом, интенсивная, постоянная;
- отсутствует ритмичность;
- свойственна иррадиация;
- лекарственная терапия неэффективна, порой противопоказана.
Большинству больных, как правило, необходимо хирургическое лечение. Париетальные боли возникают при перфорации и пенетрации органов. Отраженные (иррадиирующие) боли:
- локализуются в различных областях, часто удаленных от патологического очага;
- могут быть связаны с заболеваниями органов, расположенных вне брюшной полости, и через афферентные нейроны проецироваться на ту или иную область живота;
- боль передается на участки поверхности тела, которые имеют общую с пораженным органом брюшной полости корешковую иннервацию.
Психогенные боли:
- возникают при отсутствии очага раздражения, которым можно было бы объяснить пусковой механизм боли;
- характер этих болей определяется особенностями личности (наблюдаются у лиц с психоэмоциональными нарушениями);
- боль постоянная, тупая, монотонная, длительная, продолжается месяцами, сочетается с болевым синдромом другой локализации (головная боль, боль во всем теле);
- прекращаются или уменьшаются в условиях психического покоя, отсутствуют во время сна;
- положительный эффект достигается при лечении психотропными средствами.
По продолжительности и течению абдоминальные боли подразделяются на:
- острые, которые развиваются быстро, имеют небольшую продолжительность (от нескольких часов или дней до 1–3 недель);
- хронические, когда имеет место постепенное нарастание, длительное сохранение или рецидивирование на протяжении недель и месяцев.
Хронические боли подразделяются на органические и функциональные. Острая боль несет в себе прогностически неблагоприятную ситуацию, угрожающую развитием тяжелых осложнений, и не исключает необходимости проведения оперативного вмешательства. При острой боли у пациента, как правило, выражены симптомы интоксикации (тошнота, головокружение, сухость языка, гипотония, частый пульс). Больным с острой болью показаны госпитализация и интенсивное наблюдение. При появлении у пациента болей в животе необходимо проводить дифференциальный диагноз с инфарктом миокарда, нижнедолевой пневмонией, тромбозом мезентериальных сосудов, разрывом аневризмы брюшной аорты. Боль в животе может выступать как «маска» таких заболеваний и состояний, как депрессия, заболевания позвоночника, анемия, инфекция мочевых путей.
У пожилых пациентов и лиц, страдающих сахарным диабетом, возможно наличие «стертой» клинической симптоматики, отсутствие отчетливых болевых ощущений. Помимо оценки данных анамнеза и осмотра больного алгоритм лабораторно-инструментального обследования при абдоминальной боли включает рентгенографию, эзофагогастродуоденоскопию (ЭГДС), ультразвуковое исследование (УЗИ) по поисковой методике, биохимический скрининг, общий анализ крови и мочи, исследование кала. На основании полученных результатов можно сделать окончательное заключение о характере патологического процесса и боли (органическая или функциональная).
Наибольшую сложность представляет диагностика хронической функциональной боли в животе, когда при детальном обследовании не удается обнаружить органической патологии и морфологического субстрата, вызвавшего боль, что чревато выбором неправильной тактики ведения больных. Значительную долю гастроэнтерологической патологии составляют функциональные нарушения органов пищеварения. Из числа больных, обращающихся к гастроэнтерологам, 30–50% имеют симптомы различных функциональных расстройств. Проблема функциональных расстройств настолько актуальна, что в 1988, 1999 и 2006 гг. международной экспертной группой были приняты Римские критерии функциональных расстройств желудочно-кишечного тракта, содержащие определение, классификацию, диагностические тесты и методы лечения функциональных расстройств [3, 4, 5].
Классификация функциональных расстройств системы пищеварения
Функциональные гастроинтестинальные расстройства классифицируются следующим образом:
1. Пищеводные расстройства:
- «комок» в горле;
- регургитация;
- функциональная боль за грудиной преимущественно пищеводного генеза;
- функциональное жжение за грудиной;
- функциональная дисфагия;
- неспецифические (неопределенные) пищеводные дисфункции.
2. Гастродуоденальные расстройства:
- функциональная диспепсия (язвенноподобная, дисмоторная, неспецифическая);
- аэрофагия;
- функциональная рвота.
3. Кишечные расстройства:
- синдром раздраженного кишечника;
- функциональное вздутие живота (метеоризм);
- функциональный запор;
- функциональная диарея;
- неспецифические (неопределенные) функциональные расстройства кишечника.
4. Функциональная абдоминальная боль:
- синдром функциональной абдоминальной боли;
- неспецифическая (неопределенная) абдоминальная боль.
5. Билиарные расстройства:
- дисфункция желчного пузыря;
- дисфункция сфинктера Одди.
6. Аноректальные расстройства.
7. Функциональные расстройства у детей.
В соответствии с Римскими критериями выделено несколько общих признаков функциональных расстройств вне зависимости от уровня поражения:
- Продолжительность основных симптомов не менее 3 месяцев на протяжении последнего года.
- Отсутствие органической патологии и видимого морфологического субстрата.
- Множественный характер жалоб со стороны разных органов и систем при общем хорошем состоянии и благоприятном течении заболевания без значимого прогрессирования.
- Существенное нарушение качества жизни пациента.
Функциональная боль является висцеральной болью и сопровождается спазмом и нарушением двигательной функции органов желудочно-кишечного тракта (ЖКТ) неясного генеза. В основе функциональной боли лежит феномен висцеральной гиперчувствительности (гипералгезия – боль, возникающая под воздействием мягких повреждающих стимулов). Хроническая функциональная боль в животе является диагнозом исключения. Признаками, исключающими функциональный характер боли, служат:
- немотивированная потеря массы тела;
- ночные боли;
- возникновение заболевания в возрасте после 40–50 лет;
- лихорадка;
- любые изменения, выявленные при непосредственном обследовании больного (гепатомегалия, спленомегалия, увеличение лимфоузлов и т.д.);
- любые изменения лабораторных показателей крови, мочи, кала (лейкоцитоз, гипербилирубинемия, анемия, увеличение скорости оседания эритроцитов, гематурия, положительная реакция на скрытую кровь в кале и т.д.);
- любые изменения, выявленные с помощью инструментальных методов исследования (камни в билиарной системе, кисты поджелудочной железы, холедохоэктазия и т.д).
Для пациента принципиально важным является избавление от боли. Адекватная симптоматическая терапия, даже если она не имеет этиопатогенетической направленности, но купирует боль, имеет решающее значение для качества жизни пациента. Спазм – это универсальное звено в развитии многих гастроэнтерологических заболеваний, поэтому лечение спазмолитиками в этом случае является патогенетически обоснованным. Не следует допускать ситуаций, когда пациенты терпят боль в животе. Но при этом следует помнить, что при подозрении на острую боль применение анальгетиков противопоказано [1].
Выбор терапевтической тактики
После того как диагностика боли завершена, возникает одна из двух клинических ситуаций:
- Установлен характер органической патологии и вторичность функциональной боли.
- Исключена органическая патология и установлен первичный характер функциональной боли.
Это позволяет определить терапевтическую тактику и выбрать спазмолитик, который может являться этиотропной терапией при функциональной боли или обеспечить проведение симптоматического лечения, если спазм сопровождает основное заболевание, но не играет роли в его патогенезе [6]. Спазмолитические лекарственные препараты служат основным средством для купирования висцеральной абдоминальной боли. Расслабление гладких мышечных клеток сопровождается снижением тонуса стенки полого органа и внутрипросветного давления. Спазмолитики не только купируют боль, но и восстанавливают пассаж содержимого из полого органа, что ведет к улучшению кровоснабжениия его стенки [1, 7, 8]. Назначение спазмолитиков не сопровождается непосредственным вмешательством в механизмы болевой чувствительности, поэтому не «затушевывает» боли и не затрудняет диагностики острой хирургической патологии. Регуляторы моторно-эвакуаторной функции органов ЖКТ представляют собой группу препаратов нескольких фармакологических классов и различаются механизмом и избирательностью действия. Эти препараты подразделяют на:
- Прокинетики: метоклопрамид (Церукал, Реглан), домперидон (Мотилиум), итоприда гидрохлорид (Ганатон).
- Спазмолитики.
- Универсальный модулятор моторики ЖКТ тримебутина малеат (Тримедат®).
Прокинетики усиливают пропульсивную моторику верхних отделов ЖКТ за счет антагонизма с допаминовыми рецепторами. Ганатон помимо этого ингибирует активность ацетилхолинэстеразы, подавляет разрушение ацетилхолина. Спазмолитики подразделяются следующим образом:
1. Миотропные спазмолитики (уменьшают мышечный тонус путем прямого воздействия на гладкомышечные клетки), которые блокируют процесс передачи нервных импульсов в вегетативных ганглиях и нервных окончаниях, стимулирующих гладкомышечные клетки. Это антихолинергические препараты, или М-холиноблокаторы:
- селективные:
– блокаторы кальциевых каналов:
- Спазмомен (отилония бромид);
- Дицетел (пинаверия бромид);
– блокаторы натриевых каналов:
- Мебеверин, Дюспаталин (мебеверина гидрохлорид);
– донаторы окиси азота:
- изосорбида динитрат;
- Нитроглицерин;
- нитропруссид натрия (Нанипрус);
- неселективные:
- ингибиторы фосфодиэстеразы:
- дротаверин (Дротаверина гидрохлорид, Но-шпа);
- Папаверин.
2. Нейротропные спазмолитики (блокаторы холинорецепторов гладкой мышечной клетки):
- природные (атропин, гиосциамин, препараты красавки, платифиллин, скополамин);
- синтетические центральные (адифенин, апрофен, апренал, циклозил);
- полусинтетические периферические (Бускопан).
Механизм действия основных мышечных релаксантов:
- Активация М-холинорецепторов мышечного волокна.
- Активность гладкомышечных клеток находится в прямой пропорциональной зависимости от концентрации Ca++, который обеспечивает сокращение мышечного волокна. Миотропные спазмолитики должны уменьшить концентрацию ионов Ca в миоците.
- Мебеверин способствует деполяризации мембран, блокирует наполнение депо клеток внеклеточным Ca++.
- Высокая активность фосфодиэстеразы необходима для сокращения мышечного волокна. Этот фермент обеспечивает энергией гладкомышечные клетки.
Непростая ситуация сложилась в отношении применения антагониста 5HT3 -рецепторов серотонина – Алосетрона – при диарее и частичного агониста 5HT4 -рецепторов серотонина – тегасерода (Зелмак) – при запорах. И тот и другой препарат подтвердил свою эффективность в контролируемых испытаниях, но только у женщин [3]. Риск серьезных побочных явлений привел к тому, что оба препарата применяются в США с большими ограничениями. В европейских странах они не зарегистрированы. В январе 2012 г. в России зарегистрирован прукалоприд (Резолор) – полный агонист 5HT4-рецепторов серотонина, применяющийся как прокинетик при хронических функциональных запорах. При назначении того или иного релаксанта необходимо учитывать зоны распространения спазмолитического эффекта препарата (табл. 1) [9].
Но-шпа – традиционный спазмолитический препарат (применяется с 1962 г.), входящий в стандарты лечения болезней органов пищеварения. Предпочтительна в случаях, когда боль имеет сочетанную локализацию или склонна к генерализации. Но-шпу применяют чаще короткими курсами: например, для ускорения раскрытия шейки матки в родах, при головных болях напряжения, нефролитиазе, уретролитиазе, спазмах мочевого пузыря. Побочные эффекты отмечаются достаточно редко (в 0,9% случаев), но при длительном применении и в больших дозах могут наблюдаться тошнота, головокружение, тахикардия, гипотензия, запор, бессонница.
Папаверин также обладает спазмолитическим эффектом на многие органы, но его действие на миоциты ЖКТ в 5 раз слабее, чем у Но-шпы. Бускопан применяется с 1958 г., является препаратом безрецептурного отпуска. Это М-холиноблокатор, действующий в месте возникновения спазма. Холинорецепторы в большей степени представлены в ЖКТ, билиарной системе, в меньшей – в органах малого таза. Бускопан не влияет на центральную нервную систему, так как не проникает через гематоэнцефалический барьер. Снимает боль в течение 10–15 минут после применения. Оказывает антисекреторное действие. Назначается коротким курсом «по требованию», в некоторых случаях применяется до 2–3 недель. Основным показанием к применению Бускопана является функциональная и органическая патология верхних отделов ЖКТ. У него имеются атропиноподобные эффекты (сухость во рту и кожных покровов, тахикардия, задержка мочи, парез аккомодации, сонливость). Он противопоказан больным с глаукомой, миастенией.
Мебеверин (дюспаталин) оказывает максимальное спазмолитическое действие на гладкую мускулатуру тонкой и толстой кишки и отчасти воздействует на желчные пути. Путем восстановления градиента давления в кишечнике восстанавливает пассаж желчи. Уменьшая отток калия из клетки, устраняет спазм, не вызывая гипотонии толстой кишки. Препарат известен с 1965 г., применяется для курсового лечения. Представители селективных блокаторов кальциевых каналов клеток в кишечнике – дицетел и спазмомен. У них отсутствуют системное вазодилатирующее и кардиотропное действия, свойственные другим блокаторам Са-каналов. Применяются эти препараты преимущественно при лечении больных с функциональными расстройствами толстой кишки. Эффект дицетела дозозависим. 7–10% введенной дозы попадает в печень и может использоваться при лечении пациентов с билиарными болями, но в этом отношении дицетел преимуществ перед другими спазмолитиками не имеет. В качестве нежелательного эффекта он может вызвать запор. Спазмомен по эффективности незначительно отличается от дицетела. В настоящее время на российском рынке этот препарат отсутствует.
Гимекромон (Одестон) – миотропный спазмолитик, оказывает избирательное спазмолитическое действие на сфинктер Одди и сфинктер Люткенса, снижает давление в билиарной системе, в связи с чем купирует билиарный болевой синдром. Не оказывает влияния на другие гладкие мышцы. Важно, что Одестон не изменяет тонус желчного пузыря.
Тримебутин (Тримедат®) – универсальный регулятор моторики, действует на всем протяжении ЖКТ, включая билиарную систему.
На практике достаточно часто у пациентов встречаются сочетанные разноплановые нарушения моторики с преобладанием того или иного компонента (гипо- или гиперкинетические расстройства). Для определения типа нарушений моторики нередко требуются сложные, инвазивные, дорогостоящие и не всегда доступные в рутинной практике методы исследования: манометрия сфинктера Одди, исследование моторики кишечника с радиоактивным золотом и др. Большинство моторных расстройств имеет сложный генез, поэтому в арсенале врача должны быть лекарственные средства, способные восстанавливать моторику вне зависимости от типа ее нарушения. Таким препаратом является тримебутин, купирующий как спастическую, так и гипомоторную дискинезию кишечника, желчевыводящих путей.
Универсальный модулятор моторики позволяет на ранней стадии начать лечение больных с функциональными расстройствами, сократить количество и стоимость диагностических процедур для уточнения характера моторных расстройств. Тримебутин синтезирован в 1969 г. во Франции и много лет применяется во многих странах под торговым названием Дебридат. В России тримебутин был заявлен российской фирмой «Валента» в 2008 г. под названием Тримедат®. Это препарат из группы опиоидных пептидов, действующий на периферические опиатные рецепторы [10, 11, 12, 13].
Опиатные рецепторы расположены на всем протяжении ЖКТ. Они находятся в нервных сплетениях кишечника – подслизистом Мейснеровском и межмышечном Ауербаховском. Известно 3 подвида опиатных рецепторов: мю-, дельта- и каппа-. Мю- и дельта-рецепторы проводят возбуждающие импульсы, каппа-рецепторы – тормозящие импульсы. Тримедат® связывается с мю-, каппа- и дельта-рецепторами, не обладая специфичностью к какому-либо одному виду. Являясь нормокинетиком, препарат оказывает двойственный регулирующий эффект. Действуя на каппа-рецепторы, он угнетает моторику, действуя на мю- и дельта-рецепторы – стимулирует моторику. Таким образом, Тримедат® оказывает спазмолитическое или прокинетическое действие в зависимости от исходного состояния моторики ЖКТ [8, 14, 15]. Тримедат® оказывает влияние на гуморальную регуляцию ЖКТ: повышает уровень мотилина, снижает уровень гастрина, глюкагона, инсулина, вазоактивного кишечного пептида, панкреатического полипептида, модулируя периферические эффекты:
- ускоряет эвакуацию из желудка;
- модулирует двигательную способность толстой кишки;
- модулирует висцеральную чувствительность.
Показания к применению:
- моторные расстройства при функциональных заболеваниях ЖКТ (неязвенная диспепсия), гастроэзофагеальная рефлюксная болезнь, диспепсические расстройства при гастродуоденальных заболеваниях (язвенная болезнь);
- синдром раздраженного кишечника, проявляющийся болями и коликами в брюшной полости, метеоризмом, диареей и/или запором;
- послеоперационная паралитическая кишечная непроходимость, подготовка к рентгенологическому и эндоскопическому исследованиям ЖКТ;
- для детей: диспепсические расстройства, связанные с нарушением моторики ЖКТ.
Режим дозирования:
- детям 3–5 лет – по 25 мг 3 раза в сутки;
- детям старше 5 лет – по 50 мг 3 раза в сутки;
- детям старше 12 лет и взрослым – по 100–200 мг 3 раза в сутки.
В целом Тримедат® является безопасным препаратом, но при его применении возможны кожные реакции.
Критерии эффективности терапии тримебутином (Тримедатом)
В целом ряде зарубежных рандомизированных исследований, проводимых в разные годы, была доказана эффективность тримебутина при лечении больных синдромом раздраженного кишечника (СРК), при функциональной патологии желчевыводящих путей [8, 11, 14, 16]. Авторы статьи имеют собственный опыт применения Тримедата у больных с СРК. Под наблюдением находились 30 больных с СРК в различных клинических вариантах. СРК с преобладанием запоров констатирован у 17 человек, с преобладанием диареи – у 4 человек, с преобладанием болей и метеоризма – у 9 (у 6 из них отмечался неустойчивый стул: от кашицеобразного до твердой консистенции). Возраст пациентов колебался от 16 до 56 лет (36,8 ± 2,4 года). В обследовании участвовали 23 женщины и 7 мужчин. Больные получали Тримедат® по 200 мг 3 раза в день в течение 28 дней. Критериями эффективности лечения служили:
- Динамика клинических симптомов.
- Динамика метаболитов кишечной флоры (летучих жирных кислот в кале).
- Динамика качества жизни пациентов по опроснику SF-36.
- Регистрация побочных реакций при лечении.
Для верификации диагноза пациентам проводили эндоскопические и/или рентгенологические методы исследования. Пациенты ежедневно заполняли дневник наблюдений. Динамика клинических симптомов представлена в таблице 2. На фоне лечения Тримедатом у 83,3% больных отмечена отчетливая положительная динамика клинических симптомов в основном уже в первые 10–12 дней лечения. Значительная положительная динамика отмечена при оценке опорожнения кишечника. У преобладающего числа больных (24 человека) стул имел мягкую консистенцию в виде мягких комочков или колбасовидной формы. Общая оценка эффективности Тримедата при лечении больных с СРК считалось отличной у 15 человек (50%), хорошей – у 10 человек (33,3%), удовлетворительный эффект отмечен у 4 больных (13,3%), неудовлетворительный – у 1 пациентки (3,4%).
Клинический опыт использования Тримедата подтвердил безопасность этого лекарства. Побочных эффектов в проведенном нами исследовании не отмечено. Для оценки качества жизни пациентов на фоне терапии Тримедатом мы использовали русскоязычную версию опросника SF-36. Все пациенты заполняли опросник до и после 4-недельного лечения Тримедатом. Динамика показателей выявила тенденцию к улучшению качества жизни пациентов с СРК (рис.), но достоверных изменений ни в одном из 8 доменов опросника получено не было. Изучение метаболитов толстокишечной микрофлоры показало положительные сдвиги в экосистеме толстой кишки за счет восстановления среды обитания микрофлоры вследствие нормализации моторно-эвакуаторной функции кишечника.
Выводы
На основании вышеизложенного были сделаны следующие выводы:
- Эффективность Тримедата в лечении больных с СРК составила 83% у больных с разными расстройствами моторики толстой кишки, что позволяет рассматривать Тримедат® как универсальный регулятор моторики.
- Тримедат®, восстанавливая двигательную активность толстой кишки, купирует боли.
- Нормализуя моторно-эвакуаторную функцию кишечника, Тримедат® восстанавливает флору и ее функциональную активность.
Тримедат® следует активно использовать в клинической практике для купирования абдоминальной боли после исключения острой ее органической природы. Задачей врача является выбрать наиболее адекватный препарат, максимально быстро купирующий боль и обладающий минимумом побочных эффектов.
Клиническая эффективность и безопасность схем лечения синдрома раздраженного кишечника
Статьи
(результаты сравнительного исследования)
Опубликовано в Consilium Medicum. 2016; 18 (8): 19–26.
И.В.Маев, А.А.Самсонов, А.В.Яшина, Д.Н.Андреев, В.А.Шестаков, С.А.Караулов
ГБОУ ВПО Московский государственный медико-стоматологический университет им. А.И.Евдокимова Минздрава России. 127473, Россия, Москва, ул. Делегатская, д. 20, стр. 1
Приведены результаты сравнительного неинтервенционного наблюдательного исследования по оценке эффективности и безопасности применения препарата Колофорт в лечении синдрома раздраженного кишечника в сравнении с препаратом тримебутина.
Ключевые слова: синдром раздраженного кишечника, Колофорт, тримебутин.
aleksey.samsonov@gmail.com
Для цитирования: И.В.Маев, Самсонов А.А., Яшина А.В. и др. Клиническая эффективность и безопасность схем лечения синдрома раздраженного кишечника (результаты сравнительного исследования). Consilium Medicum. 2016; 18 (8): 19–26.
Clinical efficacy and safety of treatment regimens for irritable bowel syndrome (a comparative study)
I.V.Maev, A.A.Samsonov, A.V.Yashina, D.N.Andreev, V.A.Shestakov, S.A.Karaulov
A.I.Evdokimov Moscow State University of Medicine and Dentistry of the Ministry of Health of the Russian Federation. 127473, Russian Federation, Moscow, ul. Delegatskaia, d. 20, str. 1
The results of the comparative non-interventional observational study held to evaluate the efficacy and safety of Kolofort in the treatment of irritable bowel syndrome in comparison with trimebutine are given below.Key words: irritable bowel syndrome, Kolofort, trimebutine.
For citation: I.V.Maev, Samsonov A.A., Yashina A.V. et al. Clinical efficacy and safety of treatment regimens for irritable bowel syndrome (a comparative study). Consilium Medicum. 2016; 18 (8): 19–26.
aleksey.samsonov@gmail.com
Синдром раздраженного кишечника (СРК) – наиболее распространенная и изученная патология среди функциональных расстройств желудочно-кишечного тракта (ЖКТ), затрагивающая до 25% популяции [1]. Доля пациентов с СРК, обращающихся за амбулаторной медицинской помощью, составляет 12% и на сегодняшний день является самой большой подгруппой больных в гастроэнтерологических клиниках [2]. Одна из причин пристального внимания к проблеме СРК – несоответствие тяжести состояния пациента и благоприятного прогноза течения заболевания предъявляемым жалобам и субъективной тяжести симптоматики, существенно снижающим качество жизни пациентов и их трудоспособность [3].
Согласно недавно опубликованным Римским критериям IV пересмотра, СРК определяется как функциональное расстройство, при котором периодические боли в животе наблюдаются в среднем по крайней мере 1 день в неделю за последние 3 мес и связаны с 2 или более критериями:
1) дефекацией;
2) изменением частоты стула;
3) изменением формы стула на протяжении последних
3 мес при общей продолжительности жалоб не менее 6 мес.
Римские критерии IV не противоречат Римским критериям III, но исключают термин «дискомфорт» и еще более уточняют временные рамки наличия симптомов [4].
Клинические проявления СРК характеризуются наличием болевого синдрома, что отличает СРК от других функциональных расстройств, и нарушением стула разного характера – запор, диарея и их сочетание.
В зависимости от типа стула выделяют 4 вида (типа) СРК – с преобладанием запоров (СРК-З), с преобладанием диареи (СРК-Д), смешанный (СРК-С) и неспецифический (СРК-Н). Однако в практике часто наблюдается гетерогенность симптомов и «перемещение» одного и того же пациента из одного вида СРК в другой [4].
СРК – всегда диагноз исключения, что означает не только четкое соблюдение Римских критериев IV, но и необходимость тщательного обследования пациента для исключения органической патологии кишечника. В помощь этому существуют так называемые «симптомы тревоги»: дебют симптомов в пожилом возрасте, снижение уровня гемоглобина и железа в крови, лейкоцитоз, повышение СОЭ, гематохезия, ночная симптоматика, потеря массы тела, семейный анамнез органического заболевания кишечника. СРК – полиэтиологичное заболевание. Несмотря на широкую распространенность СРК, его этиопатогенез до конца не расшифрован [5, 6]. В связи с этим отсутствует и единая схема терапии заболевания, обеспечивающая эффективный контроль над ним.
К факторам, вызывающим или провоцирующим развитие симптомов, относят феномен висцеральной гиперчувствительности, перенесенную острую кишечную инфекцию или не связанное с ней нарушение микрофлоры кишечника, наследственную предрасположенность, средовые факторы и стрессовые воздействия [5, 6]. Также к факторам риска СРК относят молодой возраст и женский пол [3]. Данные компоненты этиопатогенеза СРК отдельно или в совокупности ведут к нарушению по оси «мозг–кишечник» – регуляции между центральной нервной системой (ЦНС) и энтеральной нервной системой (ЭНС) [7]. Ключевая задача последней – регуляция основных функций кишечника, в частности ритмической моторной активности тонкой и толстой кишки. В настоящее время большое значение в патогенезе уделяется процессам воспаления в кишечнике, дисбалансу иммунных процессов в кишечнике [8, 9]. В частности, установлена роль мастоцитов, энтероэндокринных клеток в кишечнике и дисбаланса ряда цитокинов, включая фактор некроза опухоли a (ФНО-a), гистамин, серотонин, интерлейкины (ИЛ-1b, 6, 10), что проявляется персистирующим субклиническим воспалением [10]. Медиаторы воспаления, вырабатываемые тучными клетками (гистамин, протеазы и серотонин) и Т-клетками (цитокины), влияют на ЭНС и ЦНС, активность гладкомышечных клеток кишечника, что, в свою очередь, приводит к усугублению изменений кишечного транзита и боли в животе. Также известно, что серотониновые 5-НТ-рецепторы в кишечнике играют важную роль в регуляции моторики и болевой чувствительности. И показанное при СРК увеличение количества серотонинсодержащих энтерохромаффинных клеток – еще один важный фактор формирования клинических симптомов [6].
Терапия пациентов с СРК является трудной задачей, несмотря на обилие лекарственных препаратов. В настоящее время используются спазмолитики, слабительные средства, препараты для купирования диареи, ветрогонные, комбинированные препараты, про- и пребиотики, антибиотики, антидепрессанты и нейролептики [11, 12]. Эффективность препаратов указанных групп показана во множестве клинических исследований с разным уровнем доказательности. Тем не менее до настоящего времени не существует универсальной схемы терапии СРК, которая одинаково хорошо подходила бы ко всем его типам. Гетерогенность клинических проявлений, «перемещение» пациентов из одного типа в другой обусловливают необходимость приема нескольких препаратов, что существенно снижает приверженность пациентов лечению, эффективность терапии и, следовательно, качество жизни [13, 14]. В связи с этим представляются важным поиск и применение препаратов для лечения СРК, не только обладающих симптоматическим действием, но и влияющих на его патогенетические механизмы, что позволило бы обеспечить высокую терапевтическую эффективность вне зависимости от типа СРК.
Недавно в арсенале врача появился новый отечественный комбинированный лекарственный препарат для лечения СРК – Колофорт, созданный на основе антител к мозгоспецифическому белку S-100, ФНО-a и гистамину, прошедших технологическую обработку в процессе производства. В результате в состав Колофорта входят релиз-активные антитела, которые оказывают воздействие на молекулы-мишени – не блокируют, а модифицируют активность белка S-100, рецепторов к гистамину и ФНО-a. Сочетание трех активных компонентов позволяет осуществлять комплексное воздействие на центральные и периферические звенья патогенеза функциональных нарушений кишечника и, в частности, СРК [15].
Полученные в ходе экспериментальных и клинических исследований данные о влиянии Колофорта на функциональное состояние ЖКТ показали, что благодаря нормализующему действию на его моторику, противовоспалительному и успокаивающему эффектам препарат обладает достоверной терапевтической эффективностью при СРК. Колофорт уменьшает боль и висцеральную гиперчувствительность, нормализует паттерн стула, улучшает качество жизни пациентов, положительно влияет на эмоциональные нарушения [16, 17].
Наиболее часто при СРК для купирования болевого синдрома используются спазмолитики. Их применение терапевтически оправдано как в отношении боли в животе, поскольку одна из ее причин – аномальное сокращение гладких мышц в ЖКТ, так и спазма как причины нарушенного кишечного транзита. Широко применяемый спазмолитик при СРК – синтетический холиноблокатор тримебутин (торговое название Тримедат), относящийся к эфирам с третичной аминогруппой и фармакодинамически оказывающий агонистическое действие на энкефалиновую систему кишечника – периферические опиатные рецепторы. Согласно данным официальной инструкции по применению, тримебутин регулирует моторику ЖКТ без влияния на ЦНС, восстанавливая нормальную физиологическую активность мускулатуры кишечника [18]. Нормализуя висцеральную чувствительность, он обеспечивает анальгетический эффект при абдоминальном болевом синдроме. Клинические исследования и лечебная практика демонстрируют успешное применение тримебутина в лечении пациентов с СРК [19].
С учетом изложенного представляется интересным клиническое изучение сравнительной эффективности и безопасности терапии СРК препаратами Колофорт и Тримедат в рутинной практике.
Целью исследования явилась оценка эффективности и безопасности применения препарата Колофорт в терапии СРК в сравнении с Тримедатом.
Неинтервенционное сравнительное клиническое исследование в параллельных группах проводилось с октября 2014 г. по июнь 2016 г. на базе клиники кафедры пропедевтики внутренних болезней и гастроэнтерологии ГБОУ ВПО «МГМСУ им. А.И.Евдокимова».
В исследование включались амбулаторные пациенты обоего пола в возрасте от 18 до 60 лет с установленным диагнозом СРК всех подтипов, который соответствовал Римским критериям III (2006 г.), согласно которым СРК – функциональное расстройство, при котором боль или дискомфорт в животе уменьшается после дефекации, связаны с изменением частоты и консистенции стула, возникают не менее 3 дней в месяц на протяжении последних 3 мес при общей продолжительности жалоб не менее 6 мес [20].
Поскольку исследование носило неинтервенционный характер, до включения в исследование лечащим врачом была назначена терапия препаратом Колофорт или Тримедат. В зависимости от этого пациенты были распределены в одну из двух групп – 1-я группа (основная, группа Колофорта) и 2-я группа (сравнения, группа Тримедата). Колофорт был назначен врачом по схеме: первые 2 нед приема 2 таблетки 3 раза в сутки, начиная с 15-го дня – по 2 таблетки 2 раза в сутки. Тримедат был назначен по 1 таблетке (200 мг) 3 раза в день. Длительность лечения – 12 нед.
Помимо объективного обследования в данном исследовании для оценки клинической динамики симптомов СРК использовались визуальная аналоговая шкала (ВАШ) при СРК, Бристольская шкала формы стула, расчет суммарного индекса висцеральной чувствительности по шкале VSI (Visceral Sensitivity Index) и опросник для оценки качества жизни при СРК (IBS-QoL).
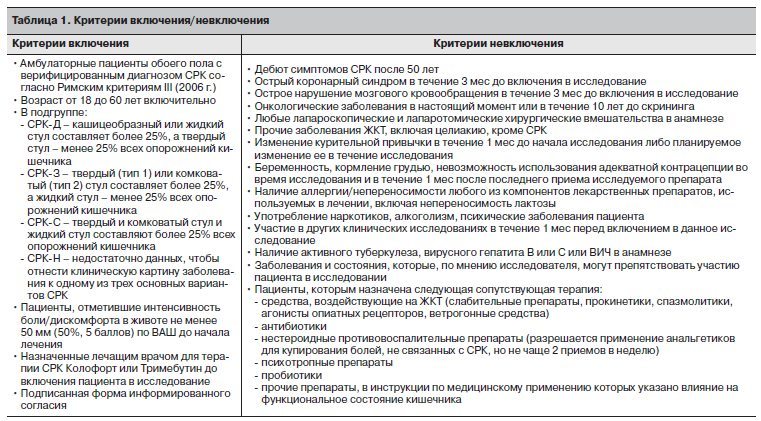
После подписания пациентом информированного согласия на визите 1 подтверждалась возможность его участия в исследовании в соответствии с критериями включения/невключения (табл. 1). В течение последующего периода лечения (12 нед) пациенты совершали еще 4 визита в медицинский центр, в ходе которых проводились объективное обследование, тестирование по указанным опросникам и шкалам, регистрировались сопутствующая терапия (если такая применялась), а также возможные нежелательные явления.
Для оценки эффективности лечения использовались следующие критерии:
• Первичные:
1. Доли пациентов, у которых отмечается снижение выраженности боли/дискомфорта по ВАШ на 30% и более от исходного значения на визитах 3 и 5.
2. Доли пациентов, у которых отмечается снижение выраженности боли/дискомфорта по ВАШ на 90% и более от исходного значения на визитах 3 и 5.
• Вторичные:
1. Доля пациентов в подгруппе СРК-Д с изменением типа стула по Бристольской шкале формы стула до 5 и менее (в среднем за 1 нед).
2. Динамика изменения типа стула по Бристольской шкале.
3. Доля пациентов в подгруппе СРК-З, у которых число актов дефекации увеличилось в среднем на 1 раз в неделю по сравнению с исходным уровнем.
4. Динамика количества актов дефекации у пациентов с СРК-З.
5. Динамика результатов оценки по ВАШ.
6. Динамика значений суммарного балла индекса висцеральной чувствительности по опроснику VSI.
7. Динамика значений суммарного балла опросника качества жизни IBS-QоL.
В процессе исследования выполнялись 5 визитов пациента к врачу: визит 1 (день 0), визит 2 (день 14±3), визит 3 (день 28±3), визит 4 (день 56±3), визит 5 (день 84±3). На каждом визите проводились объективное обследование пациента, включающее измерение массы тела, артериального давления, частоты сердечных сокращений, температуры тела, и оценка безопасности, заполнение опросников ВАШ, VSI, IBS-QoL и определение типа стула по Бристольской шкале. Кроме этого, на визите 1 пациенты подписывали форму информированного согласия, а также проводилась проверка соответствия критериям включения/невключения. Определение критериев безопасности было связано с наличием, характером и продолжительностью нежелательных явлений, их связью с приемом препарата, выраженностью и другими характеристиками, в связи с чем проводилось заполнение соответствующей формы для оповещения отдела клинической безопасности компании-производителя. Для обработки полученных данных использовались стандартные методы описательной статистики, включая дисперсионный анализ, метод Generalized estimating equations (GEE), расчет t-критерия Стъюдента, точного критерия Фишера, критерий χ2, критерий Кохрана–Мантеля–Хенсзеля (модификация критерия χ2 для множественных сравнений), критерий Фаррингтона–Мэннинга.
Результаты исследования
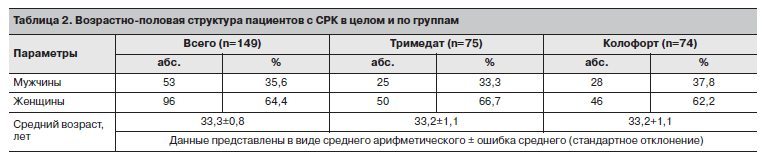
В исследование были включены 149 пациентов обоего пола (53 мужчины – 35,6% и 96 женщин – 64,4%) в возрасте от 18 до 60 лет (средний возраст составил 33,3±0,8 года) с СРК, диагноз которого соответствовал Римским критериям III (2006 г.).
Все рекрутированные пациенты полностью соответствовали критериям включения/невключения в исследование и завершили участие в нем через 12 нед наблюдения. В окончательный анализ эффективности и безопасности включены данные всех 149 пациентов, принимавших участие в исследовании.
В соответствии с назначенной лечащим врачом терапией пациенты были распределены в 2 группы: 74 пациента составили группу Колофорта, 75 – группу Тримедата. Возрастно-половая структура пациентов с СРК в целом и по группам представлена в табл. 2.
Соотношение мужчин и женщин среди пациентов, включенных в исследование, составило примерно 1:2, что согласуется с данными мировой литературы о примерно двукратном преобладании женщин среди лиц, страдающих СРК [3]. Средний возраст по группам был одинаков и составил 33,2±1,1 года.
Согласно классификации СРК по типам в зависимости от преобладающих нарушений стула, пациенты распределились следующим образом: в группе, принимавшей Колофорт, пациенты с СРК-Д составили 39 (53%) человек, СРК-З – 23 (31%), СРК-С и СРК-Н – по 6 (8%) в каждой подгруппе. Аналогичное распределение по субтипам СРК наблюдалось и в группе Тримедата: пациенты с СРК-Д составили 33 (44%) человека, СРК-З – 29 (39%), СРК-С – 5 (6%), СРК-Н – 8 (11%); рис. 1. В целом в сравниваемых группах отмечено доминирование пациентов с СРК-Д и СРК-З. Полученные результаты несколько противоречат эпидемиологическим данным о частоте встречаемости типов СРК с примерно равным распределением по подгруппам СРК-З, СРК-Д, СРК-С, что в данном исследовании, вероятно, связано с переходом одной формы СРК в другую у одного и того же пациента.
Таким образом, по возрастному, половому составу и исходным клиническим характеристикам исследуемые группы были сопоставимы.
Влияние сравниваемой терапии на болевой синдром
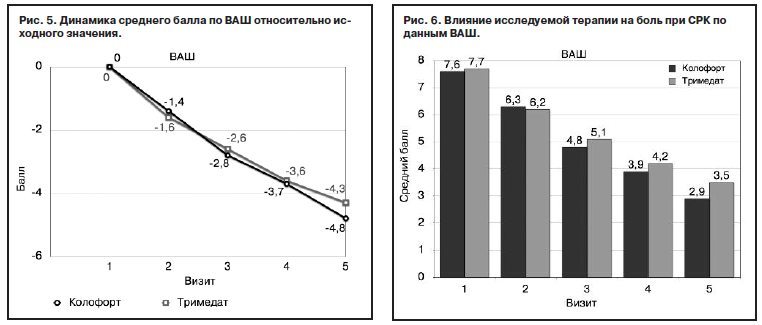
В качестве первичных критериев в данном исследовании оценивалось влияние терапии на болевой синдром, поскольку боль при СРК – один из ключевых симптомов, традиционно рассматриваемый в качестве терапевтической мишени в клинических исследованиях [20]. Также динамика болевого синдрома по ВАШ оценивалась в целом в качестве вторичного критерия.
В соответствии с выбранными первичными критериями эффективности оценивалась доля пациентов со снижением выраженности боли/дискомфорта по ВАШ на 30% и более от исходного значения на визитах 3 и 5. Выбор данного значения был сделан в соответствии с существующими подходами к проведению клинических исследований при СРК – снижение боли в животе на 30% по сравнению с исходным уровнем считается клинически значимым [20].
Через 4 нед терапии, к визиту 3, доля пациентов со снижением боли по ВАШ на 30% и более была сопоставима в обеих группах: 62% пациентов в группе Колофорта и 60% – в группе Тримедата [критерий χ2: χ2=0,07; p=0,7867; критерий Фаррингтона–Мэннинга (nonferiority test): z=1,53; p=0,0633]; рис. 2.
Однако к визиту 5, окончанию курса наблюдения и терапии сравниваемыми препаратами, продемонстрировано статистически значимое превосходство терапии Колофортом по сравнению с Тримедатом: уменьшение выраженности боли на 30% и более отмечено у 95% пациентов основной группы против 84% пациентов в группе сравнения [критерий χ2: χ2=4,4; p=0,0368; критерий Фаррингтона–Мэннинга (nonferiority test): z=3,7; p=0,0001]; рис. 2, 3.
При оценке доли пациентов, у которых отмечено снижение выраженности боли/дискомфорта по ВАШ на 90% и более от исходного значения на визитах 3 и 5, получены сопоставимые данные в сравниваемых группах с тенденцией к лучшим показателям в группе Колофорта, что может говорить о необходимости более длительной терапии СРК (рис. 4).
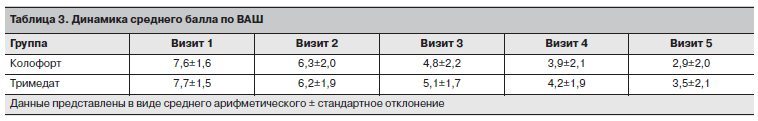
В целом под действием обоих препаратов в течение всего периода наблюдения отмечалась отчетливая сопоставимая положительная динамика в отношении купирования болевого синдрома с тенденцией к несколько большей эффективности в группе Колофорта (дисперсионный анализ: фактор «Группа» F1/145=0,7, p=0,4122; фактор «Визит» F3/435=2,2, p=0,1115; фактор «Группа*Визит» F3/435=3,7, p=0,0229; ковариата «Визит 1» F1/145=100, p=0,0001); рис. 5.Более выраженная тенденция к уменьшению болевого синдрома по ВАШ при приеме Колофорта по сравнению с Тримедатом, несмотря на сопоставимую эффективность проводимой терапии в целом, выявлена уже к визиту 3, через 4 нед терапии (табл. 3; рис. 6).
Выявленная тенденция к большей выраженности купирования боли в животе демонстрировала нарастание до конца исследования.
Таким образом, к окончанию 3-месячного курса Колофорт продемонстрировал более выраженное влияние на уменьшение болевого синдрома.
Влияние сравниваемой терапии на паттерн стула
При анализе динамики изменений типа стула по Бристольской шкале формы кала получены результаты, свидетельствующие о существенном превосходстве терапии Колофортом по сравнению с Тримедатом. У пациентов с СРК-Д уже через 4 нед терапии нормальный стул наблюдался у 90% пациентов, получавших Колофорт, против 58% пациентов, получавших Тримедат (критерий Кохрана– Мантеля–Хенсзеля: χ2=8,4; p=0,0038; для визита 5 точный критерий Фишера: p=0,0024); рис. 7.
Таким образом, Колофорт продемонстрировал достоверно превосходящую Тримедат эффективность во влиянии на нормализацию типа стула по Бристольской шкале у пациентов с СРК-Д. Причем эффективность Колофорта была более выраженной как по срокам, так и по стабильности изменений. Полученные результаты позволяют сделать вывод о более быстром и стабильном действии Колофорта в отношении нормализации типа стула у пациентов с СРК-Д по сравнению с Тримедатом. Различия в динамике влияния исследуемых препаратов на нормализацию типа стула при СРК-Д, вероятно, связаны с особенностями механизма действия препаратов и подтверждают регуляторное, патогенетическое действие Колофорта [13, 21].
Оценка динамики типа стула по Бристольской шкале у пациентов с СРК-З также продемонстрировала статистически значимое преимущество Колофорта по сравнению с Тримедатом (критерий Кохрана–Мантеля–Хенсзеля: χ2=29,1; p=0,0001).
Оба препарата продемонстрировали положительную динамику, но уже через 4 нед терапии доля пациентов с нормальным типом стула в группе Колофорта была более чем в 4 раза больше, чем в группе сравнения. А к концу наблюдения нормальный тип стула отмечен у всех пациентов группы Колофорта, тогда как данный параметр на фоне терапии Тримедатом был на 1/4 меньше и достиг значения лишь в 76% (точный критерий Фишера: визит 3 – p=0,0001, визит 5 – p=0,0135); рис. 8.
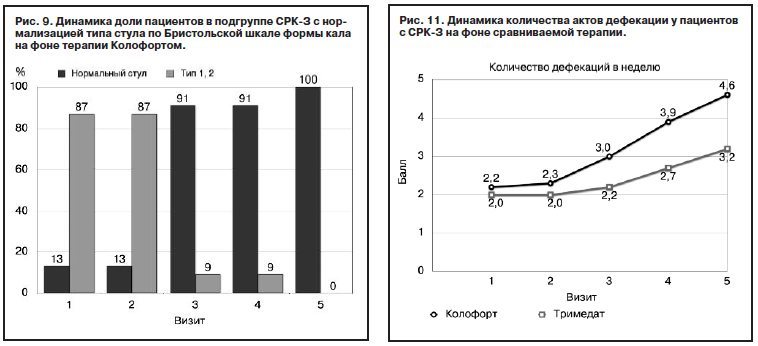
Стоит отметить, что, несмотря на одинаковую долю пациентов с типом стула 1, 2 (87%) на визите 1 и 2 в группе Колофорта, выраженность запора между двумя визитами в течение 2 нед терапии существенно уменьшилась. Так, к визиту 2 по сравнению с визитом 1 доля пациентов с типом стула 2 увеличилась более чем в 2 раза, а доля пациентов с типом стула 1 уменьшилась в 5,5 раза. В дальнейшем к визиту 3 доля пациентов с нормальным типом стула увеличилась в 7 раз, продемонстрировав нормализацию стула у 100% пациентов с СРК-З через 3 мес (рис. 9).
Полученные результаты позволяют сделать вывод о достоверном превосходстве Колофорта по сравнению с Тримедатом в отношении нормализации типа стула у пациентов с СРК-З. Превосходство заключалось в более быстром наступлении эффекта и большей его выраженности. Очевидно, выявленные различия в терапевтической эффективности связаны с особенностями действия Колофорта – его регуляторным влиянием как на центральные, так и на периферические звенья патогенеза заболевания [15–17].
При оценке динамики частоты дефекаций в подгруппе СРК-З определялась доля пациентов, у которых число актов дефекации увеличилось в среднем на 1 раз в неделю по сравнению с исходным уровнем. Было установлено, что результаты, полученные в группе Колофорта, значимо превосходят таковые в группе Тримедата, начиная уже с визита 2, 3-й недели терапии, достигнув максимума к 8-й неделе (метод Generalized estimating equations – GEE): Z=4,8; p=0,0001); рис. 10.
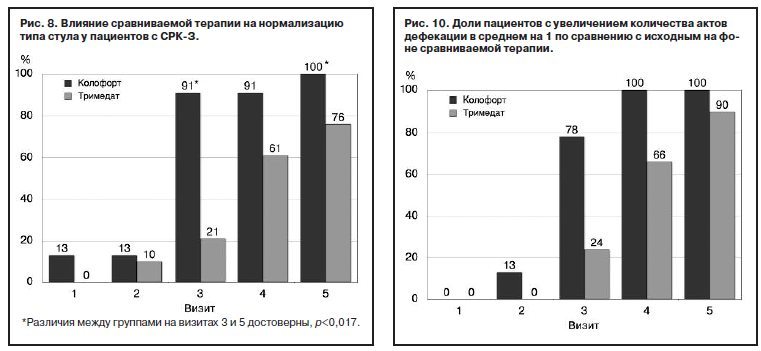
В группе Тримедата увеличение частоты стула происходило значительно медленнее, начавшись только с визита 3, через 4 нед лечения. На визите 4 улучшения по данному критерию достигли на 1/3 меньше пациентов, чем в группе Колофорта, а к окончанию исследования – 90% пациентов, тогда как в группе Колофорта уже на визите 4 отмечалась его нормализация у 100% пациентов.
Средняя динамика количества актов дефекации у пациентов с СРК-З также свидетельствовала в пользу большей эффективности Колофорта, достигнув к окончанию наблюдения в среднем 4,6±0,9 раза в неделю против 3,2±0,6 раза в неделю в группе сравнения. Под действием Колофорта улучшение отмечалось уже с визита 2, тогда как на фоне приема Тримедата первые результаты получены на 4 нед позже, к визиту 3 (рис. 11).
Данные, полученные при оценке влияния сравниваемой терапии на паттерн стула, позволяют сделать вывод о достоверно более быстром наступлении эффекта Колофорта, его большей выраженности и стабильности по сравнению с Тримедатом у пациентов с СРК.
Влияние сравниваемой терапии на висцеральную гиперчувствительность
В ходе данного исследования проводилась оценка влияния проводимой терапии на первичный патофизиологический механизм СРК, который обусловливает возникновение и интенсивность боли, выраженность моторных расстройств – висцеральную гиперчувствительность.
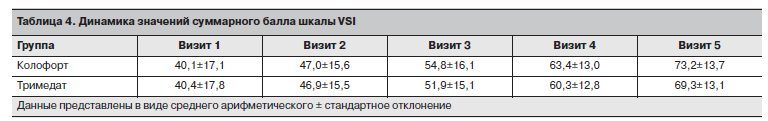
При анализе динамики значений данного критерия эффективности по шкале VSI в ходе исследования установлена статистически значимая тенденция к превосходству терапии Колофортом по сравнению с Тримедатом согласно результатам дисперсионного анализа (фактор «Группа» F1/146=4,3, p=0,0411; фактор «Визит» F3/438=306, p=0,0001; фактор «Группа*Визит» F3/438=2.8, p=0,0725; ковариата «Визит 1» F1/146=263, p=0,0001); табл. 4.
Несмотря на очевидно прослеживаемую в течение всего периода наблюдения тенденцию к преимуществу Колофорта по сравнению с Тримедатом, оценка изменений суммарного балла VSI относительно исходного значения на фоне сравниваемой терапии в целом свидетельствует о сопоставимой эффективности сравниваемых препаратов (дисперсионный анализ: фактор «Группа» F1/147=2,5, p=0,1147; фактор «Визит» F3/441=317, p=0,0001; фактор «Группа*Визит» F3/441=1,9, p=0,1701); рис. 12.
Полученные результаты позволяют сделать вывод о способности как Колофорта, так и Тримедата нормализовывать висцеральную гиперчувствительность, что подтверждают ранее описанные данные о влиянии препаратов на основные клинические проявления СРК. Прослеживаемая на протяжении всего периода наблюдения устойчивая тенденция к несколько большему, хотя и статистически незначимому влиянию Колофорта на изменение висцеральной чувствительности относительно исходного значения, что согласуется с продемонстрированной в данном исследовании его более выраженной терапевтической эффективностью в отношении клинической симптоматики.
Полученные в исследовании положительные результаты по влиянию проводимой терапии на клиническую симптоматику, висцеральную гиперчувствительность нашли свое отражение и в динамике значений суммарного балла опросника качества жизни IBS-QoL. Влияние изучаемой терапии СРК на качество жизни пациентов было сопоставимым в обеих группах при более выраженном его улучшении по сравнению с исходным уровнем в группе пациентов, получавших Колофорт.
В ходе данного исследования какого-либо неблагоприятного влияния на витальные функции и параметры, включая частоту сердечных сокращений, артериальное давление, а также нежелательных явлений в обеих группах зарегистрировано не было.
Исследуемые препараты характеризовались хорошей переносимостью, что наряду с продемонстрированной эффективностью обеспечило высокий уровень приверженности пациентов назначенной им терапии.
Выводы
Проведенное неинтервенционное сравнительное клиническое исследование в параллельных группах для оценки эффективности и безопасности применения препарата Колофорт в терапии СРК в сравнении с Тримедатом продемонстрировало соответствие применяемых препаратов основным клиническим задачам, решаемым при терапии данного заболевания, и в первую очередь – необходимости купирования его ведущих проявлений. При сопоставимой в целом эффективности рассматриваемых препаратов полученные в ходе исследования результаты позволяют сделать следующие выводы:
1. Колофорт более выраженно влияет на уменьшение болевого синдрома – к окончанию исследования установлено статистически значимое превосходство по первичному критерию исследования с уменьшением выраженности боли на 30% и более у 95% пациентов основной группы против 84% пациентов в группе сравнения.
2. Колофорт достоверно более быстро, выраженно и стабильно способствует нормализации паттерна стула при СРК по сравнению с Тримедатом.
3. Колофорт достоверно превосходит Тримедат в эффективности нормализации типа стула по Бристольской шкале у пациентов с СРК, это заключается в более быстром наступлении эффекта и большей его выраженности.
4. Колофорт способствует нормализации висцеральной гиперчувствительности с устойчивой тенденцией на протяжении всего периода наблюдения к несколько большему по сравнению с Тримедатом, хотя и статистически незначимому, влиянию на ее изменение относительно исходного значения.
5. Влияние изучаемой терапии СРК на качество жизни пациентов было сопоставимым в обеих группах при более выраженном его улучшении по сравнению с исходным уровнем в группе пациентов, получавших Колофорт.
6. При сопоставимо высоком уровне безопасности применения сравниваемых препаратов также подтверждена высокая безопасность длительного использования Колофорта в терапии СРК, что иллюстрируют отсутствие зарегистрированных в ходе исследования нежелательных явлений и результаты мониторинга витальных функций пациентов.
Совокупность хорошей переносимости и продемонстрированной эффективности обеспечила высокий уровень приверженности пациентов назначенной терапии.
Таким образом, полученные данные позволяют рекомендовать препарат к широкому применению в терапии СРК вне зависимости от его подтипа и тяжести течения.
Литература
1. Canavan C, West J, Card T. The epidemiology of irritable bowel syndrome. Clin Epidemiol 2014; 6: 71–80.
2. Saha L. Irritable bowel syndrome: Pathogenesis, diagnosis, treatment, and evidence-based medicine. World Journal of Gastroenterology : WJG 2014; 20 (22): 6759–73.
3. Enck P, Aziz Q, Barbara G et al. Irritable bowel syndrome. Nat Rev Dis Primers 2016; 2: 16014.
4. Drossman DA. Functional Gastrointestinal Disorders: History, Pathophysiology, Clinical Features, and Rome IV. Gastroenterology 2016; 150 (6): 1262–79.
5. Lee YJ, Park KS. Irritable bowel syndrome: Emerging paradigm in pathophysiology. World J Gastroenterol 2014; 20 (10): 2456–69.
6. El-Salhy M. Recent developments in the pathophysiology of irritable bowel syndrome. World Journal of Gastroenterology. WJG 2015; 21 (25): 7621–36.
7. Drossman DA, Hasler WL. Rome IV – Functional GI Disorders: Disorders of Gut-Brain Interaction. Gastroenterology 2016; 150 (6): 1257–61.
8. Ohman L, Simrén M. Pathogenesis of IBS: role of inflammation, immunity and neuroimmune interactions. Nat Rev Gastroenterol Hepatol 2010; 7 (3): 163–73.
9. Sinagra E, Pompei G, Tomasello G et al. Inflammation in irritable bowel syndrome: Myth or new treatment target? World J Gastroenterol 2016; 22 (7): 2242–55.
10. Bashashati M, Rezaei N, Shafieyoun A et al. Cytokine imbalance in irritable bowel syndrome: a systematic review and meta-analysis. Neurogastroenterol Motil 2014; 26 (7): 1036–48.
11. Маев И.В., Кучерявый Ю.А., Черемушкин С.В. Эволюция представлений о синдроме раздраженного кишечника. М.: Форте Принт, 2013. / Maev I.V., Kucheria-vyi Iu.A., Cheremushkin S.V. Evoliutsiia predstavlenii o sindrome razdrazhennogo kishechnika. M.: Forte Print, 2013. [in Russian]
12. Malagelada JR, Malagelada C. Mechanism-Oriented Therapy of Irritable Bowel Syndrome. Adv Ther 2016; p. 1–17. URL:link.springer.com/article/10.1007/s12325-016-0336-….
13. Самсонов А.А., Андреев Д.Н., Дичева Д.Т. Синдром раздраженного кишечника с позиций современной гастроэнтерологии. Фарматека. 2014; 18: 7–14. / Samsonov A.A., Andreev D.N., Dicheva D.T. Sindrom razdrazhennogo kishechnika s pozitsii sovremennoi gastroenterologii. Farmateka. 2014; 18: 7–14. [in Russian]
14. Андреев Д.Н., Самсонов А.А., Черемушкин С.В. Синдром раздраженного кишечника: критерии диагностики и подходы к терапии. Фарматека. 2014; 14: 6–11. / Andreev D.N., Samsonov A.A., Cheremushkin S.V. Sindrom razdrazhennogo kishechnika: kriterii diagnostiki i podkhody k terapii. Farmateka. 2014; 14: 6–11. [in Russian]
15. Инструкция по медицинскому применению препарата Колофорт. URL: grls.rosminzdrav.ru/Grls_View_v2.aspx / Instruktsiia po meditsinskomu primeneniiu preparata Kolofort. URL: grls.rosminzdrav.ru/Grls_View_v2.aspx [in Russian]
16. Авалуева Е.Б., Адашева Т.В., Бабаева А.Р. и др. Эффективность и безопасность применения Колофорта при синдроме раздраженного кишечника: итоги многоцентрового двойного слепого плацебо-контролируемого рандомизированного клинического исследования. Гастроэнтерология. 2014; 1: 36–43. / Avalue-va E.B., Adasheva T.V., Babaeva A.R. i dr. Effektivnost’ i bezopasnost’ primeneniia Koloforta pri sindrome razdrazhennogo kishechnika: itogi mnogotsentrovogo dvoinogo slepogo platsebo-kontroliruemogo randomizirovannogo klinicheskogo issledovaniia. Gastroenterologiia. 2014; 1: 36–43. [in Russian]
17. Осадчук М.А., Бурдина В.О. Новые патогенетические подходы к терапии синдрома раздраженного кишечника, основанные на морфофункциональных особенностях данной патологии. Практическая медицина. 2014; 1 (77): 12–20. / Osadchuk M.A., Burdina V.O. Novye patogeneticheskie podkhody k terapii sindroma razdrazhennogo kishechnika, osnovannye na morfofunktsional’nykh osobennostiakh dannoi patologii. Prakticheskaia meditsina. 2014; 1 (77): 12–20. [in Russian]
18. Инструкция по медицинскому применению препарата Тримедат. URL: grls.rosminzdrav.ru/Grls_View_v2.aspx / Instruktsiia po meditsinskomu primeneniiu preparata Trimedat. URL: grls.rosminzdrav.ru/Grls_View_v2.aspx [in Russian]
19. Ивашкин В.Т., Драпкина О.М. Возможности применения тримебутина в лечении больных с синдромом раздраженного кишечника. РЖГГК. 2008; 18 (5): 12–6. / Ivashkin V.T., Drapkina O.M. Vozmozhnosti primeneniia trimebutina v lechenii bol’nykh s sindromom razdrazhennogo kishechnika. RZhGGK. 2008; 18 (5): 12–6. [in Russian]
20. Miller LE. Study design considerations for irritable bowel syndrome clinical trials. Annals of Gastroenterology: Quarterly Publication of the Hellenic Society of Gastroenterology. 2014; 27 (4): 338–45.
21. Казюлин А.Н. Колофорт: механизм действия и возможности патогенетической терапии заболеваний желудочно-кишечного тракта. Гастроэнтерология Санкт-Петербурга. 2016; 1–2: 19–23. / Kaziulin A.N. Kolofort: mekhanizm deistviia i vozmozhnosti patogeneticheskoi terapii zabolevanii zheludochno-kishechnogo trakta. Gastroenterologiia Sankt-Peterburga. 2016; 1–2: 19–23. [in Russian]
22. Ивашкин В.Т., Шелыгин Ю.А., Баранская Е.К. и др. Клинические рекомендации Российской гастроэнтерологической ассоциации, Ассоциации колопроктологов России по диагностике и лечению больных с синдромом раздраженного кишечника. Рос. журн. гастроэнтерологии, гепатологии, колопроктологии. 2014; 2: 92–9. / Ivashkin V.T., Shelygin Iu.A., Baranskaia E.K. i dr. Klinicheskie rekomendatsii Rossiiskoi gastroenterologicheskoi assotsiatsii, Assotsiatsii koloproktologov Rossii po diagnostike i lecheniiu bol’nykh s sindromom razdrazhennogo kishechnika. Ros. zhurn. gastroenterologii, gepatologii, koloproktologii 2014; 2: 92–9. [in Russian]
СВЕДЕНИЯ ОБ АВТОРАХ
Маев Игорь Вениаминович – чл.-кор. РАН, д-р мед. наук, проф., зав. каф. пропедевтики внутренних болезней и гастроэнтерологии ГБОУ ВПО МГМСУ им. А.И.Евдокимова
Самсонов Алексей Андреевич – д-р мед. наук, проф. каф. пропедевтики внутренних болезней и гастроэнтерологии ГБОУ ВПО МГМСУ им. А.И.Евдокимова. E-mail: aleksey.samsonov@gmail.com
Андреев Дмитрий Николаевич – ассистент каф. пропедевтики внутренних болезней и гастроэнтерологии ГБОУ ВПО МГМСУ им. А.И.Евдокимова
Шестаков Вячеслав Александрович – д-р мед. наук, проф. каф. пропедевтики внутренних болезней и гастроэнтерологии ГБОУ ВПО МГМСУ им. А.И.Евдокимова
Яшина Александра Валерьевна – аспирант каф. пропедевтики внутренних болезней и гастроэнтерологии ГБОУ ВПО МГМСУ им. А.И.Евдокимова
Караулов Сергей Алексеевич – канд. мед. наук, ассистент каф. пропедевтики внутренних болезней и гастроэнтерологии ГБОУ ВПО МГМСУ им. А.И.Евдокимова
Портал Consilium Medicum:
con-med.ru/eprint/234435
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
| (cc)]by-nc-sa4.01 ОРИГИНАЛЬНАЯ СТАТЬЯ
Эффективность тримебутина в рамках лечения функциональных заболеваний желудочно-кишечного тракта и желчных путей: наблюдательное многоцентровое исследование
И.В. Маев, Д.Н. Андреевн от имени коллектива исследователей протокола ТМД-06-02-2018
ФГБОУ ВО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова» Минздрава России, Москва, Россия
Аннотация
Цель. Оценка практики применения тримебутина (таблетки с пролонгированным высвобождением, покрытые пленочной оболочкой, 300 мг) для лечения пациентов с функциональными заболеваниями (ФЗ) желудочно-кишечного тракта (ЖКТ) и желчных путей в условиях первичного звена здравоохранения.
Материалы и методы. Проведено проспективное наблюдательное многоцентровое неинтервенционное исследование, в которое включались пациенты обоего пола в возрасте от 18 до 60 лет с верифицированным диагнозом ФЗ ЖКТ и желчных путей (функциональная диспепсия, синдром раздраженного кишечника, дисфункция желчевыводящих путей, дисфункция сфинктера Одди, постхолецистэктомиче-ский синдром). Тримебутин назначался в соответствии с инструкцией по медицинскому применению: внутрь, по 1 таблетке 2 раза в день (с перерывом в 12 ч), длительность — 28 дней. Выраженность клинических симптомов измеряли в баллах по 5-балльной вербальной шкале. Результаты. В исследование включены 4433 пациента, выборку per protocol составил 3831 человек. Доля пациентов с ФЗ ЖКТ, у которых наблюдалось значимое снижение выраженности боли в области живота после лечения, составила 74,73% (95% доверительный интервал -ДИ 73,32-76,11%). После лечения наблюдалось статистически значимое снижение выраженности боли/чувства жжения в эпигастральной области (среднее значение в баллах на 1-м визите составило 1,21 [95% ДИ 1,18-1,25], на 2-м визите — 0,22 [95% ДИ 0,2-0,23]; p<0,001), боли в области живота (1-й визит — 2,01 [95% ДИ 1,98-2,04], 2-й визит — 0,33 [95% ДИ 0,31-0,35]; p<0,001), билиарной боли (1-й визит -1,22 [95% ДИ 1,18-1,26], 2-й визит — 0,2 [95% ДИ 0,19-0,22]; p<0,001), чувства переполнения желудка и раннего насыщения/чувства тяжести (1-й визит — 1,29 [95% ДИ 1,25-1,32], 2-й визит — 0,21 [95% ДИ 0,19-0,22]; p<0,001), выраженности изжоги (1-й визит — 0,92 [95% ДИ 0,88-0,95], 2-й визит — 0,18 [95% ДИ 0,17-0,20]; p<0,001), выраженности отрыжки (1-й визит — 1,13 [95% ДИ 1,09-1,16], 2-й визит — 0,22 [95% ДИ 0,21-0,24]; p<0,001), а также вздутия живота (1-й визит — 1,99 [95% ДИ 1,96-2,03], 2-й визит — 0,43 [95% ДИ 0,41-0,45]; p<0,001). Заключение. Настоящее проспективное наблюдательное многоцентровое неинтервенционное исследование продемонстрировало высокую эффективность тримебутина в рамках лечения пациентов с ФЗ ЖКТ.
Ключевые слова: функциональные заболевания, функциональная диспепсия, синдром раздраженного кишечника, дисфункция желчевыводящих путей, дисфункция сфинктера Одди, постхолецистэктомический синдром
Для цитирования: И.В. Маев, Д.Н. Андреев от имени коллектива исследователей протокола ТМД-06-02-2018. Эффективность тримебутина в рамках лечения функциональных заболеваний желудочно-кишечного тракта и желчных путей: наблюдательное многоцентровое исследование. Терапевтический архив. 2021; 93 (8): 897-903. DOI: 10.26442/00403660.2021.08.200919
_ORIGINAL ARTICLE
Efficacy of trimebutine in the treatment of functional gastrointestinal disorders: an observational multicenter study
Igor V. Maev, Dmitry N. AndreevH on behalf of the team of researchers of the TMD-06-02-2018 protocol
Yevdokimov Moscow State University of Medicine and Dentistry, Moscow, Russia
Abstract
Aim. Evaluation of the practice of using trimebutine (tablets, 300 mg, extended release), for the treatment of patients with functional gastrointestinal disorders (FGID) in primary health care.
Materials and methods. A prospective observational multicenter non-interventional study was carried out, which included patients of both sexes aged 18 to 60 years with a verified diagnosis of functional gastrointestinal disorders (functional dyspepsia, irritable bowel syndrome, biliary tract dysfunction, sphincter of Oddi dysfunction, postcholecystectomy syndrome). Trimebutine was prescribed in accordance with the instructions for medical use: orally, 300 mg twice per day for 28 days. The severity of simptoms was evaluated by five-point rating scale. Results. The study included 4433 patients, the per protocol sample consisted of 3831 people. The proportion of patients with a significant decrease in the severity of abdominal pain after treatment was 74.73% (95% confidence interval — CI 73.32-76.11). At the and of the study a statistically significant decrease in the severity of FGIDV simptoms was observed: epigastric pain/burning (mean score at the 1st visit was 1.21 [95% CI 1.18-1.25], at the 2nd visit — 0.22 [95% CI 0.2-0.23]; p<0.001), abdominal pain (1st visit — 2.01 [95% CI 1.98-2.04), 2nd visit — 0.33 [95% CI 0.31-0.35]; p<0.001), biliary pain (1st visit — 1.22 [95% CI 1.18-1.26], 2nd visit — 0.2 [95% CI 0.19-0.22]; p<0.001), postprandial fullness and early satiation (1st visit — 1.29 [95% CI 1.25-1.32], 2nd visit — 0.21 [95% CI 0.19-0.22]; p<0.001), severity of heartburn (1st visit -0.92 [95% CI 0.88-0.95], 2nd visit — 0.18 [95% CI 0.17-0.20]; p<0.001), belching (1st visit — 1.13 [95% CI 1.09-1.16], 2nd visit — 0.22 [95% CI 0.21-0.24]; p<0.001), as well as abdominal distention (1st visit — 1.99 (95% CI 1, 96, 2.03), 2nd visit — 0.43 [95% CI 0.41-0.45]; p<0.001). Conclusion. The present prospective observational multicenter non-interventional study has demonstrated that trimebutine is an effective approach to treating FGID.
Информация об авторах / Information about the authors
^Андреев Дмитрий Николаевич — канд. мед. наук, доц. каф. ^Dmitry N. Andreev. E-mail: [email protected]; пропедевтики внутренних болезней и гастроэнтерологии. ORCID: 0000-0002-4007-7112 Тел.: +7(495)609-67-00; e-mail: [email protected]; ORCID: 0000-0002-4007-7112
Маев Игорь Вениаминович — акад. РАН, д-р мед. наук, проф., зав. Igor V. Maev. ORCID: 0000-0001-6114-564X каф. пропедевтики внутренних болезней и гастроэнтерологии. ORCID: 0000-0001-6114-564X
Keywords: functional gastrointestinal disorders, functional dyspepsia, irritable bowel syndrome, biliary dysfunction, sphincter of Oddi dysfunction, postcholecystectomy syndrome
For citation: Maev IV, Andreev DN on behalf of the team of researchers of the TMD-06-02-2018 protocol. Efficacy of trimebutine in the treatment of functional gastrointestinal disorders: an observational multicenter study Terapevticheskii Arkhiv (Ter. Arkh). 2021; 93 (8): 897-893. DOI: 10.26442/00403660.2021.08.200919
Введение
Согласно последней дефиниции, предложенной экспертами Римского консенсуса IV пересмотра (2016 г), функциональные заболевания (ФЗ) желудочно-кишечного тракта (ЖКТ) — это группа расстройств, характеризующаяся нарушением взаимодействия между центральной нервной системой (головной мозг) и периферическим звеном нервной системы, обеспечивающим деятельность органов ЖКТ (ось «головной мозг-ЖКТ») [1, 2]. Последние систематические обзоры и метаанализы демонстрируют, что ФЗ ЖКТ являются крайне распространенными в общемировой популяции, достигая 15-25% взрослого и молодого населения развитых стран [3-6]. Преимущественно страдают лица работоспособного возраста, а в гендерной структуре преобладают женщины [2, 3, 6, 7]. Согласно данным недавнего мультинационального исследования A. Sperber и соавт. (2021 г.), полученным при использовании интернет-опроса, среди 73 076 взрослых респондентов диагностическим критериям как минимум одного ФЗ ЖКТ соответствовали 40,3% субъектов (95% доверительный интервал — ДИ 39,940,7) [7]. При этом в субгруппе из Российской Федерации данный показатель составил 44,6% (95% ДИ 42,4-46,8) [7]. Клиническое значение ФЗ ЖКТ определено существенным снижением качества жизни пациентов как за счет показателей физического здоровья, так и эмоционально-психологических составляющих, а также частой коморбидностью с тревожными и депрессивными расстройствами [8-11]. Отдельную проблему представляет собой субоптимальный профиль эффективности большинства средств фармакотерапии ФЗ ЖКТ, что иллюстрируется последними мета-анализами, демонстрирующими высокие показатели NNT (среднее число пациентов, которых необходимо лечить, чтобы достичь определенного благоприятного исхода) при применении традиционных медикаментозных методов лечения [12-16]. Вместе с тем стоит отметить, что компла-ентность пациентов с ФЗ ЖКТ не всегда является очень высокой из-за нередкой полипрагмазии и использования препаратов, требующих высокой кратности приема в течение суток. Так, при одном из наиболее распространенных ФЗ ЖКТ — синдроме раздраженного кишечника (СРК), при котором нередко используются комбинации различных лекарственных средств, частота низкой приверженности фармакотерапии может достигать 38,3-50,9% [17, 18].
Тримебутин (Тримедат®), агонист периферических ц-, 5-, к-опиатных рецепторов, является лекарственным препаратом, регулирующим моторику ЖКТ, действуя на всем его протяжении [19]. При гипермоторике тримебутин способствует снижению тонуса мышечных компонентов ЖКТ, тогда как при преобладании гипотонуса — повышению моторной активности [20, 21]. Такой двойственный механизм действия позволяет препарату увеличивать эвакуаторную функцию желудка, сниженную при функциональной диспепсии (ФД), восстанавливать нарушенную моторику нижних отделов ЖКТ, наблюдающуюся при СРК, а также гармонизировать моторную активность желчного пузыря и желчевыводящих путей [19-21]. Помимо этого тримебутин способствует регрессу висцеральной гиперчувствительности за счет взаимодействия с к-опиатными рецепторами и блокады №+-каналов периферических окончаний чувствительных нейронов, связанных с
висцеральными афферентными С-волокнами [21]. В 2017 г в РФ зарегистрирован тримебутин в лекарственной форме таблетки (300 мг) с пролонгированным высвобождением для приема 2 раза в день (Тримедат® форте).
Цель исследования — оценка практики применения тримебутина (таблетки с пролонгированным высвобождением, покрытые пленочной оболочкой, 300 мг; Тримедат® форте) для лечения пациентов с ФЗ ЖКТ в условиях первичного звена здравоохранения.
Материалы и методы
Дизайн исследования
Проведено проспективное наблюдательное многоцентровое неинтервенционное исследование применения препарата Тримедат® форте в рамках лечения пациентов с ФЗ ЖКТ и желчных путей в условиях первичного звена здравоохранения. Исследуемый препарат назначался в соответствии с инструкцией по медицинскому применению: внутрь, по 1 таблетке 2 раза в день (с перерывом в 12 ч).
В исследование включались пациенты обоего пола в возрасте от 18 до 60 лет с верифицированным диагнозом ФЗ ЖКТ и желчных путей и клиническими проявлениями функциональных расстройств, которым для лечения этого заболевания назначен Тримедат® форте в случае их соответствия критериям включения/невключения. Решение о назначении пациенту препарата Тримедат® форте четко отделено от решения о включении пациента в исследование: оно принималось до включения пациента в исследование в рамках обычной клинической практики и не было связано с проведением данного исследования, т.е. исследуемый препарат не назначался пациенту с целью включения в исследование. Набор пациентов производился 538 исследователями в 60 городах России.
Неинтервенционный дизайн исследования предполагал сбор информации путем простого наблюдения событий в их естественном течении. Наблюдение за пациентом в рамках данного исследования проводилось исключительно в период приема препарата Тримедат® форте. После прекращения приема Тримедат® форте пациент завершал свое участие в исследовании.
Для реализации поставленных целей и задач в рамках исследования предусмотрено две записи:
• 1-я производилась в день включения пациента в исследование (день 0);
• 2-я выполнялась в последний день приема препарата Тримедат® форте.
В соответствии с инструкцией по медицинскому применению Тримедат® форте курс лечения абдоминальной боли, связанной с ФЗ ЖКТ и желчных путей, составляет 28 дней. Таким образом, 2-я запись запланирована на 28-й день исследования, и, следовательно, максимальная продолжительность наблюдения за пациентом в рамках данного исследования составляла 28 дней. Если врач назначал Тримедат® форте на срок менее 28 дней, 2-я запись производилась в последний день приема Тримедат® форте, и дальнейшее наблюдение за пациентом прекращалось.
Критерии включения:
1) пациенты мужского и женского пола в возрасте от 18 до 60 лет включительно;
2) амбулаторные пациенты с верифицированным диагнозом ФЗ ЖКТ и желчных путей и клиническими проявлениями этих функциональных расстройств: боль, спазмы и дискомфорт в области живота, ощущение вздутия (метеоризм) и урчание, моторные расстройства кишечника с изменением частоты стула (диарея или запор), диспепсия, изжога, отрыжка, тошнота, рвота, связанные с ФЗ ЖКТ и желчных путей (ФД, СРК, дисфункция желчевыводящих путей; дисфункция сфинктера Одди, постхолецистэктомический синдром);
3) пациенты, которым врач назначил препарат Тримедат® форте, таблетки с пролонгированным высвобождением, покрытые пленочной оболочкой, 300 мг, АО «Ва-лента Фарм»;
4) информированное согласие в письменной форме на участие в исследовании, предоставленное пациентом или законным представителем.
Критерии невключения:
1) прием препаратов тримебутина в течение 4 нед до подписания формы информированного согласия;
2) злокачественные опухоли в настоящий момент или в течение 10 лет до скрининга;
3) хирургические вмешательства на ЖКТ (за исключением аппендэктомии, холецистэктомии и операции по удалению желчных камней) в анамнезе;
4) прочие заболевания ЖКТ, включая целиакию, кроме ФЗ ЖКТ и желчных путей;
5) беременность, кормление грудью, невозможность использования адекватной контрацепции во время исследования и в течение одного месяца после последнего приема исследуемого препарата;
6) повышенная чувствительность к компонентам, входящим в состав препарата Тримедат® форте;
7) наличие противопоказаний, которые указаны в утвержденных инструкциях по применению лекарственных препаратов, используемых в исследовании;

9) употребление наркотиков, алкоголизм, психические заболевания пациента;
10) наличие активного туберкулеза, вирусного гепатита В или С либо ВИЧ в анамнезе;
11) заболевания и состояния, которые, по мнению исследователя, могут препятствовать участию пациента в исследовании;
12) пациенты, которые получали следующую терапию за 28 дней и менее до начала исследования:
• средства, воздействующие на ЖКТ (слабительные препараты, прокинетики, спазмолитики, агонисты опиатных рецепторов, ветрогонные средства);
• антибиотики;
• нестероидные противовоспалительные препараты (разрешается применение анальгетиков для купирования болей, не связанных с проявлениями ФЗ ЖКТ и желчных путей, но не чаще 2 приемов в неделю);
• психотропные препараты.
Критерии и методы оценки клинических эффектов
исследуемого препарата
Первичный критерий. Доля пациентов, у которых отмечалось снижение выраженности боли в области живота на 2 балла и более от исходного значения на 2-м визите исследования. Выраженность боли измеряли в баллах по 5-балльной вербальной шкале, где 0 — отсутствие проявлений,
1 — слабовыраженные проявления, 2 — проявления средней интенсивности, 3 — сильные проявления и 4 — очень сильные проявления. Значимым снижением в этом исследовании считали снижение на 2 балла и более от исходного значения. При исходно слабовыраженной боли в области живота (1 балл) значимым считалось снижение выраженности боли на 1 балл.
Вторичные критерии:
1. Динамика результатов оценки отдельных симптомов ФЗ ЖКТ и желчных путей по 5-балльной вербальной шкале на фоне лечения.
2. Динамика характера стула на фоне лечения.
3. Оценка пациентом эффективности лечения (выраженное улучшение/улучшение/без изменений/некоторое ухудшение/выраженное ухудшение).
4. Субъективная оценка пациентом отдельных симптомов ФЗ ЖКТ и желчных путей, если применимо для диагностированного заболевания (значительное улучшение/умеренное улучшение/без улучшения).
5. Оценка врачом эффективности лечения (выраженное улучшение/улучшение/без изменений/некоторое ухудшение/выраженное ухудшение).
6. Оценка пациентом удобства применения Тримедат® форте (очень удобно/удобно/неудобно/очень неудобно).
7. Оценка необходимости в приеме дополнительных лекарственных препаратов (помимо Тримедат® форте) для лечения ФЗ ЖКТ и желчных путей (с указанием конкретных препаратов).
8. Оценка среднего времени наступления эффекта Тримедат® форте (снижение выраженности боли в животе) за последнюю неделю исследования после приема утренней дозы Тримедат® форте (менее 1, 1-2, 3-8, 8-24, более 24 ч после приема препарата).
Динамика количества актов дефекации представлена в виде динамики характера стула (диарея, запор, чередование диареи и запора, стул в норме) между 1 и 2-м визитом.
Этика
Исследование, включая архивирование основных документов по исследованию, выполнено в соответствии с правилами надлежащей клинической практики, утвержденными Евразийской экономической комиссией и ICH GCP. Обязательным условием участия в исследовании являлось информированное согласие в письменной форме, предоставленное пациентом или законным представителем.
Статистическая обработка
Статистическая обработка данных осуществлялась с помощью специального программного обеспечения R версии 3.5 в среде RStudio.
Первичный критерий эффективности исследуемого препарата анализировался с помощью параметров:
1) доля пациентов, у которых достигался критерий эффективности (%);
2) биноминальный 95% ДИ.
При оценке значимости динамики использовались методы аналитической статистики: %2 Пирсона, или точный критерий Фишера, или тест МакНемара (категориальные данные), тесты Фридмана или Уилкоксона (количественные данные).
Результаты
Популяция пациентов
В исследование включены 4433 пациента. Число лиц, данные которых пригодны для анализа характеристик
популяции включенных пациентов, составило 3962. С целью обобщения полученных данных диагнозы, указанные врачами согласно кодировке Международной классификации болезней 10-го пересмотра, распределены на несколько групп (по основному диагнозу): ФД, СРК, дискинезия желчевыводящих путей (в том числе дисфункция сфинктера Одди и постхолецистэктомический синдром), неэрозивная форма гастроэзофагеальной рефлюксной болезни (неэрозивная рефлюксная болезнь — НЭРБ). При НЭРБ часто определяется перекрест с ФЗ ЖКТ, тогда как тримебутин, согласно инструкции по медицинскому применению препарата, рекомендован к применению при этих нозологиях. При указании врачом наличия у пациента двух и более диагнозов, относящихся к ФЗ органов ЖКТ и желчных путей, пациент распределен в каждую группу указанных диагнозов. Большая часть пациентов в исследовании имели диагноз СРК («=2246, 56,7%, 2246/3962). Средний возраст участников исследования составил 38,14 года (95% ДИ 37,80-38,49). В гендерном составе преобладали женщины (68,57%).
Сопутствующие заболевания имели 623 пациента. У некоторых зафиксировано несколько сопутствующих заболеваний, поэтому на это число пациентов приходилось 799 случаев сопутствующих заболеваний. Самым часто встречающимся сопутствующим заболеванием стала гипертоническая болезнь (у 80 пациентов, 12,84% от общего числа пациентов с сопутствующими заболеваниями). Медикаментозную терапию сопутствующих заболеваний получали 103 пациента, на это число пациентов приходилось 142 случая назначений лекарственных препаратов. Большую часть препаратов из сопутствующей терапии составили средства для лечения сердечно-сосудистых заболеваний (антигипертензивные препараты), что согласуется с данными о сопутствующих заболеваниях участников исследования.
Клиническая эффективность тримебутина
В анализ клинических эффектов Тримедат® форте включены данные пациентов, которые придерживались рекомендованного режима лечения без существенных отклонений и у которых собран необходимый объем данных (популяция per protocol, «=3831). Из них 99,1% пациентов принимали Тримедат® форте 28 дней. Завершили свое участие в исследовании досрочно 33 пациента. Причинами досрочного завершения исследования служили: купирование болевого синдрома и явлений диспепсии ранее чем через 28 дней («=10), утрата соответствия критериям включения/ невключения («=1), отказ от участия в исследовании («=1), в остальных случаях («=21) причина досрочного завершения исследования не указана.
Из 3831 пациента, включенного в анализ клинических эффектов Тримедат® форте, 1252 (32,68%) больным дополнительно назначены иные помимо Тримедат® форте лекарственные препараты для лечения ФЗ ЖКТ. Наиболее часто в дополнение к Тримедат® форте при лечении ФЗ ЖКТ и желчных путей пациентам назначали ингибиторы протонной помпы (получали 509 пациентов из 1252; 40,65%), панкреатин (получали 339 пациентов из 1252; 27,08%), урсодезоксихолевую кислоту (получали 228 пациентов из 1252; 18,21%). Следовательно, 67,32% пациентов не понадобилось назначение дополнительных лекарственных препаратов для лечения ФЗ ЖКТ и желчных путей во время приема Тримедат® форте.
Доля пациентов, у которых наблюдалось значимое снижение выраженности боли в области живота после
Рис. 1. Распределение пациентов по выраженности боли в области живота в начале и конце исследования в популяции «все участники исследования». Fig.1. Patient distribution by the severity of abdominal pain at the beginning and at the end of the study in the «all study participants» population.
лечения, составила 74,73% (95% ДИ 73,32-76,11). Общее число пациентов, имеющих данные для оценки описываемого параметра, составило 3803 человека. Выявлена статистически значимая разница в распределении пациентов по группам выраженности боли в области живота в начале и конце исследования (p<0,001); рис. 1. В популяции пациентов, которые из желудочно-кишечных средств принимали только Тримедат® форте, доля лиц со значимым снижением выраженности боли в области живота составила 77,35% [95% ДИ 75,64-78,99] (общее число пациентов, имеющих данные для оценки описываемого параметра, составило 2450 человек). Сопоставляя полученные в двух выборках результаты, можно сделать вывод о том, что этот клинический эффект связан с приемом Тримедат® форте.
Динамика выраженности отдельных симптомов. После лечения в общей выборке пациентов наблюдалось статистически значимое снижение выраженности боли/ чувства жжения в эпигастральной области (среднее значение выраженности боли/чувства жжения в эпигастральной области в баллах на 1-м визите составило 1,21 [95% ДИ 1,18-1,25], на 2-м — 0,22 [95% ДИ 0,2-0,23];p<0,001), боли в области живота (среднее значение выраженности боли в области живота в баллах на 1-м визите составило 2,01 [95% ДИ 1,98-2,04], на 2-м — 0,33 [95% ДИ 0,31-0,35]; p<0,001), билиарной боли (среднее значение выраженности билиар-ной боли в баллах на 1-м визите составило 1,22 [95% ДИ 1,18-1,26], на 2-м — 0,2 [95% ДИ 0,19-0,22];p<0,001), чувства переполнения желудка и раннего насыщения/чувства тяжести (среднее значение выраженности чувства переполнения в желудке и раннего насыщения/чувства тяжести в баллах на 1-м визите составило 1,29 [95% ДИ 1,25-1,32], на 2-м — 0,21 [95% ДИ 0,19-0.22]; p<0,001), выраженности изжоги (среднее значение выраженности изжоги в баллах на 1-м визите составило 0,92 [95% ДИ 0,88-0,95], на 2-м —
100 90 80 70 60 50 40 30 20 10 0
42,10
14,07 93,05
21,76 ,1,87
22,07 3,05
¿^2,03
1-й визит (начало исследования)
2-й визит (через 28 дней)
I Диарея ■ Запор ■ Чередование диареи и запора ■ Стул в норме
Рис. 3. Динамика характера стула на фоне лечения. Fig. 3. Dynamics of stool characteristics under treatment.
iНе можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
Рис. 2. Динамика выраженности отдельных симптомов ФЗ ЖКТ и желчных путей по 5-балльной вербальной шкале на фоне лечения в популяции «все участники исследования». Fig. 2. Dynamics of FGID» symptoms severity under treatment according to a five-point rating scale.
0,18 [95% ДИ 0,17-0,20]; /<0,001), выраженности отрыжки (среднее значение выраженности отрыжки в баллах на 1-м визите составило 1,13 [95% ДИ 1,09-1,16], на 2-м — 0,22 [95% ДИ 0,21-0,24]; /<0,001), а также вздутия живота (среднее значение выраженности вздутия живота в баллах на 1-м визите составило 1,99 [95% ДИ 1,96-2,03], на 2-м -0,43 [95% ДИ 0,41-0,45]; /<0,001); рис. 2.
Динамика характера стула на фоне лечения. Общее число пациентов, имеющих данные для оценки описываемого параметра, составило 3801 человека. К концу исследования число пациентов с диареей уменьшилось с 839 до 77, с запором — с 827 до 116, с чередованием диареи и запора — с 535 до 71. Число пациентов с нормальным стулом увеличилось с 1600 до 3537 (рис. 3). Выявлена статистически значимая разница в распределении характера стула между двумя визитами (/<0,001).
Оценка пациентом эффективности лечения. Общее число пациентов, имеющих данные для оценки описываемого параметра, составило 3823 человек; 59,38% пациентов оценили результаты лечения как «выраженное улучшение» (2270/3823; 59,38%; 95% ДИ 57,76-61,02), 38,90% — как «улучшение» (1487/3823; 38,90%; 95% ДИ 37,27-40,53).
Оценка врачом эффективности лечения. Общее число пациентов, имеющих данные для оценки описываемого параметра, составило 3826 человек. У 61,29% пациентов врачи оценили результаты лечения как «выраженное улучшение» (2345/3826; 61,29%; 95% ДИ 59,70-62,92), у 37,56% пациентов — как «улучшение» (1437/3826; 37,56%; 95% ДИ 35,96-39,19).
Оценка пациентом удобства применения Тримедат® форте. Общее число пациентов, имеющих данные для оценки описываемого параметра, составило 3816 человек; 58,81% пациентов оценили удобство применения Тримедат® форте как «очень удобно» (2244/3816; 58,81%; 95% ДИ 57,1860,45), 40,17% — как «удобно» (1533/3816; 40,17%; 95% ДИ 38,55-41,82).
Оценка среднего времени наступления эффекта Тримедат® форте. Общее число пациентов, имеющих данные для оценки описываемого параметра, составило 3803 человека; 41,31% пациентов отметили наступление эффекта в течение 1-2 ч после приема Тримедат® форте (1571/3803; 41,31%; 95% ДИ 39,60-43,06), 31,13% пациен-
тов отметили наступление эффекта в течение менее 1 ч после приема Тримедат® форте (1184/3803; 31,13%; 95% ДИ 29,42-32,88).
Обсуждение
Высокая распространенность ФЗ ЖКТ в общемировой популяции, преимущественное поражение лиц работоспособного возраста, а также значимое снижение качества жизни больных обусловливают медико-социальную значимость этой группы расстройств [1, 2, 7]. Несмотря на гетерогенность паттерна моторных нарушений, общими для большинства ФЗ ЖКТ являются связь симптоматики с тревогой и депрессией, наличие висцеральной гиперчувствительности, нередкий постинфекционный генез заболевания, изменения микробиоты ЖКТ (ассоциация с синдромом избыточного бактериального роста в тонкой кишке), повышение проницаемости слизистой оболочки кишечника и воспаление слизистой оболочки низкой степени активности (от англ. low-grade inflammation) [22-27]. Эффективная фармакотерапия ФЗ ЖКТ остается трудной задачей в условиях рутинной клинической практики, так как у многих пациентов наблюдается субоптимальный комплаенс, что диктует необходимость использования лекарственных форм препаратов с большей дозой действующего вещества или пролонгированным высвобождением [18, 28].
В настоящем исследовании мы решили оценить эффективность тримебутина (таблетки с пролонгированным высвобождением, покрытые пленочной оболочкой, 300 мг) при лечении ФЗ ЖКТ и желчных путей в рамках проспективного наблюдательного многоцентрового исследования. Согласно полученным результатам доля пациентов, у которых наблюдалось значимое снижение выраженности боли в области живота после лечения, составила 74,73%. После лечения в общей выборке пациентов наблюдалось статистически значимое снижение выраженности боли/чувства жжения в эпигастральной области, боли в области живота, билиарной боли, чувства переполнения желудка и раннего насыщения/чувства тяжести, выраженности изжоги, отрыжки, а также вздутия живота. Полученные результаты совпадают с рядом других работ, демонстрирующих высокую эффективность тримебутина в терапии ФЗ ЖКТ. Так, в недавнем рандомизированном плацебо-контролируемом исследовании J. Kountouras и соавт. (2020 г) по применению тримебутина в рамках монотерапии ФД первичная конечная точка (облегчение симптомов) достоверно достигнута в группе, принимавшей тримебутин, ко 2-му визиту пациентов (через 2 нед) и последнему (через 4 нед);
р=0,02) [29]. При этом сцинтиграфическое исследование с применением 99тТс-Тт продемонстрировало, что триме-бутин способствует ускорению эвакуаторной функции желудка достоверно эффективнее, чем плацебо (р=0,036) [29]. Эффективность тримебутина в рамках купирования боли при лечении ФЗ ЖКТ (СРК, ФД и их сочетания) в сравнении с другими спазмолитиками продемонстрирована в исследовании В.Т. Ивашкина и соавт. (2015 г). Данная работа показала, что схемы лечения, в которые включен три-мебутин, продемонстрировали большую эффективность по сравнению со схемами, в которые включали спазмолитики [30]. Важно отметить, что тримебутин влияет на общий патогенетический момент, характерный для ФЗ ЖКТ, -висцеральную гиперчувствительность, что проявляется в регрессии абдоминальной боли, которая существенно влияет на качество жизни пациентов [19-21]. При этом для эффективного достижения этой цели терапия должна длиться не менее 4 нед, о чем свидетельствуют результаты настоящего исследования и других независимых работ, оценивающих эффективность лекарственных препаратов в рамках нивелирования феномена висцеральной гиперчувствительности у пациентов с ФЗ ЖКТ [31-33]. Согласно рекомендациям Российской гастроэнтерологической ассоциации (РГА) и Ассоциации колопроктологов России по диагностике и лечению СРК (2017 г.) тримебутин безопасен при длительном применении, эффективен для лечения сочетанной функциональной патологии (в частности,
Список сокращений
ДИ — доверительный интервал
ЖКТ — желудочно-кишечный тракт
СРК — синдром раздраженного кишечника
при ФД и СРК), а также эффективно уменьшает частоту и выраженность абдоминальной боли [34]. В рекомендациях РГА по диагностике и лечению ФД (2017 г.) также упоминается, что тримебутин ускоряет замедленную эвакуацию содержимого желудка у пациентов с ФД. Поскольку тримебутин также нормализует моторику нижних отделов ЖКТ, его можно применять и при сочетании ФД и СРК [35]. Вместе с тем в рекомендациях РГА по лечению дискинезии желчевыводящих путей (2018 г.) постулируется, что тримебутин эффективен при лечении большинства пациентов с дисфункцией сфинктера Одди III типа и значительной части пациентов с дисфункцией II типа (по Милуокской классификации) [36].
Заключение
Настоящее проспективное наблюдательное многоцентровое неинтервенционное исследование продемонстрировало высокую эффективность применения препарата Тримедат® форте, таблетки с пролонгированным высвобождением, покрытые пленочной оболочкой, 300 мг, для лечения пациентов с ФЗ ЖКТ в условиях первичного звена здравоохранения в РФ.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare no conflict of interest.
ФД — функциональная диспепсия ФЗ — функциональное заболевание
ЛИТЕРАТУРА/REFERENCES
1. Андреев Д.Н., Заборовский А.В., Трухманов А.С., и др. Эволюция представлений о функциональных заболеваниях желудочно-кишечного тракта в свете Римских критериев IV пересмотра (2016 г.). Российский журнал гастроэнтерологии, гепатологии, колопроктоло-гии. 2017;1:4-11. [Andreyev DN, Zaborovsky AV, Trukhmanov AS, et al. Evaluation of the functional gastrointestinal diseases concept from standpoints of Rome IV (2016) diagnostic criteria (review). Russia« Journal of Gastroe«terology, Hepatology, Coloproctology. 2017;27(1):4-11 (in Russian)].D0I:10.22416/1382-4376-2017-27-1-4-11
2. Drossman DA. Functional Gastrointestinal Disorders: History, Pathophysiology, Clinical Features and Rome IV. Gastroe«terology. 2016;S0016-5085(16)00223-7. D0I:10.1053/j.gastro.2016.02.032
3. Oshima T, Miwa H. Epidemiology of Functional Gastrointestinal Disorders in Japan and in the World. J Neurogastroe«terol Motil. 2015;21(3):320-9. D0I:10.5056/jnm14165
4. Lewis ML, Palsson OS, Whitehead WE, van Tilburg MA. Prevalence of functional gastrointestinal disorders in children and adolescents. JPediatr. 2016;177:39-43.e3. pii: S0022-3476(16)30056-7
5. Oka P, Parr H, Barberio B, et al. Global prevalence of irritable bowel syndrome according to Rome III or IV criteria: a systematic review and meta-analysis. La«cet Gastroe«terol Hepatol. 2020;5(10):908-17. D0I:10.1016/S2468-1253(20)30217-X
6. Ford AC, Marwaha A, Sood R, Moayyedi P. Global prevalence of, and risk factors for, uninvestigated dyspepsia: a meta-analysis. Gut. 2015;64(7):1049-57. D0I:10.1136/gutjnl-2014-307843
7. Sperber AD, Bangdiwala SI, Drossman DA, et al. Worldwide Prevalence and Burden of Functional Gastrointestinal Disorders, Results of Rome Foundation Global Study. Gastroe«terology. 2021;160(1):99-114.e3. D0I:10.1053/j.gastro.2020.04.014
8. Chassany O, Marquis P, Scherrer B, et al. Validation of a specific quality of life questionnaire for functional digestive disorders. Gut. 1999;44(4):527-33. D0I:10.1136/gut.44.4.527
9. Aro P, Talley NJ, Agreus L, et al. Functional dyspepsia impairs quality of life in the adult population. Alime«t Pharmacol Ther. 2011;33(11):1215-24. D0I:10.1111/j.1365-2036.2011.04640.x
10. Zamani M, Alizadeh-Tabari S, Zamani V. Systematic review with me-ta-analysis: the prevalence of anxiety and depression in patients with irritable bowel syndrome. Alime«t Pharmacol Ther. 2019;50(2):132-43. D0I:10.1111/apt.15325
11. Lin S, Gao T, Sun C, et al. The association between functional dyspepsia and depression: a meta-analysis of observational studies. Eur J Gastroe«terol Hepatol. 2019;31(8):911-8. D0I:10.1097/MEG.0000000000001451
12. Pinto-Sanchez MI, Yuan Y, Hassan A, et al. Proton pump inhibitors for functional dyspepsia. Cochra«e Database Syst Rev. 2017;11(11):CD011194. D0I:10.1002/14651858.CD011194.pub3
13. Pittayanon R, Yuan Y, Bollegala NP, et al. Prokinetics for Functional Dyspepsia: A Systematic Review and Meta-Analysis of Randomized Control Trials. Am J Gastroe«terol. 2019;114(2):233-43. D0I:10.1038/s41395-018-0258-6
14. Ford AC, Quigley EM, Lacy BE, et al. Efficacy of prebiotics, probiot-ics, and synbiotics in irritable bowel syndrome and chronic idiopathic constipation: systematic review and meta-analysis. Am J Gastroe«terol. 2014;109(10):1547-61. D0I:10.1038/ajg.2014.202
15. Ford AC, Luthra P, Tack J, et al. Efficacy of psychotropic drugs in functional dyspepsia: systematic review and meta-analysis. Gut. 2017;66(3):411-20. D0I:10.1136/gutjnl-2015-310721
16. Ford AC, Lacy BE, Harris LA, et al. Effect of Antidepressants and Psychological Therapies in Irritable Bowel Syndrome: An Updated Systematic Review and Meta-Analysis. Am J Gastroe«terol. 2019;114(1):21-39. D0I:10.1038/s41395-018-0222-5
17. Алексеева О.П., Касимова Л.Н., Горячева Е.Е. Приверженность к терапии у пациентов с патологией желудочно-кишечного тракта. Российский журнал гастроэнтерологии, гепатологии, колопроктологии.
2016;26(1):20-8 [Alekseyeva OP, Kasimova LN, Goryacheva YY. Treatment compliance of patients with gastro-intestinal diseases. Russian Journal of Gastroenterology, Hepatology, Coloproctology. 2016;26(1):20-8 (in Russian)]. D0I:10.22416/1382-4376-2016-26-1-20-28
18. Whitehead WE, Levy RL, Von Korff M, et al. The usual medical care for irritable bowel syndrome. Aliment Pharmacol Ther. 2004;20(11-12):1305-15. D0I:10.1111/j.1365-2036.2004.02256.x
19. Roman FJ, Lanet S, Hamon J, et al. Pharmacological properties of trimebutine and M-monodesmethyltrimebutine. J Pharmacol Exp Ther. 1999;289(3):1391-7. PMID: 10336531
20. Delvaux M, Wingate D. Trimebutine: mechanism of action, effects on gastrointestinal function and clinical results. J Int Med Res. 1997;25(5):225-46. D0I:10.1177/030006059702500501
21. Lee HT, Kim BJ. Trimebutine as a modulator of gastrointestinal motility. ArchPharmRes. 2011;34(6):861-4. D0I:10.1007/s12272-011-0600-7
22. Shah A, Talley NJ, Jones M, et al. Small intestinal bacterial overgrowth in irritable bowel syndrome: a systematic review and meta-analysis of case-control studies. Am J Gastroenterol. 2020;115(2):190-201. D0I:10.14309/ajg.0000000000000504.
23. Кучерявый Ю.А., Андреев Д.Н., Маев И.В. Распространенность синдрома избыточного бактериального роста в тонкой кишке у пациентов с функциональной диспепсией: метаанализ. Терапевтический архив. 2020;92(12):53-8 [Kucheryavyy YA, Andreev DN, Maev IV. Prevalence of small bowel bacterial overgrowth in patients with functional dyspepsia: a meta-analysis. Terapevticheskii Arkhiv (Ter. Arkh). 2020;92(12):53-8 (in Russian)]. D0I:10.26442/00403660.2020.12.200433
24. Андреев Д.Н., Кучерявый Ю.А., Маев И.В. Распространенность и риск нарушений сна у пациентов с функциональной диспепсией: метаанализ. Журнал неврологии и психиатрии им. С.С. Корсакова. 2021;121(1):26-30 [Andreev DN, Kucheryavy YuA, Mayev IV. The prevalence and risk of sleep disorders in patients with functional dyspepsia: a meta-analysis. Korsakov Journal of Neurology and Psychiatry = Zhurnal nevrologii i psikhiatrii imeni S.S. Korsakova. 2021;121(1):26-30 (in Russian)]. D0I:10.17116/jnevro202112101126
25. Андреев Д.Н., Дичева Д.Т. Нарушение проницаемости слизистой оболочки кишечника как фактор этиопатогенеза функциональных заболеваний желудочно-кишечного тракта. Медицинский Совет. 2020;5:87-95 [Andreev DN, Dicheva DT. A breach in the intestinal permeability as a factor of etiopathogenesis of functional gastrointestinal diseases. Meditsinskiy sovet = Medical Council. 2020;5:87-95 (in Russian)]. D0I:10.21518/2079-701X-2020-5-87-95
26. Farre R, Vicario M. Abnormal Barrier Function in Gastrointestinal Disorders. Handb Exp Pharmacol. 2017;239:193-217. D0I:10.1007/164_2016_107
27. Ng QX, Soh AYS, Loke W, et al. The role of inflammation in irritable bowel syndrome (IBS). JInflamm Res. 2018;11:345-9. D0I:10.2147/JIR.S174982
28. Андреев Д.Н., Дичева Д.Т. Оптимизация лечения пациентов с синдромом раздраженного кишечника: фокус на повышение комплаентности. Медицинский Совет. 2019;3:118-24 [Andreev DN, Dicheva DT. 0ptimizing the treatment of patients with irritable bowel syndrome: focus on increased compliance. Meditsinskiy sovet = Medical Council. 2019;3:118-24 (in Russian)]. D0I:10.21518/2079-701X-2019-3-118-124
29. Kountouras J, Gavalas E, Papaefthymiou A, et al. Trimebutine maleate monotherapy for functional dyspepsia: a multicenter, randomized, double-blind placebo controlled prospective trial. Medicina (Kaunas). 2020;56(7):339. D0I:10.3390/medicina56070339
30. Ивашкин В.Т., Полуэктова Е.А., Рейхарт Д.В., и др. Эффективность наиболее часто назначаемых групп препаратов у пациентов с функциональными расстройствами желудочно-кишечного тракта (синдромом функциональной диспепсии и синдромом раздраженного кишечника (Результаты наблюдательного исследования). Российский журнал гастроэнтерологии, гепатологии, колопрок-тологии. 2016;26(4):7-14 [Ivashkin VT, Poluektova YA, Reykhart DV, et al. Efficacy of drugs most commonly prescribed at functional gastrointestinal diseases (functional dyspepsia syndrome and irritable bowel syndrome) observational study results. Russian Journal of Gastroenterology, Hepatology, Coloproctology. 2016;26(4):7-14 (in Russian)].
31. Типикина М.Ю. Оценка роли воспалительных и микробиологических изменений при синдроме раздраженного кишечника у детей. Автореф. дис. … канд. мед. наук. СПб., 2014 [Tipikina MYu. Assessment of the role of inflammatory and microbiological changes in irritable bowel syndrome in children. Abstract of thesis. dis. … Cand. honey. sciences. Saint Petersburg, 2014 (in Russian)].
32. Гриневич В.Б., Сас Е.И., Кравчук Ю.А., и др. Безопасность длительного использования селективных М3-холинолитиков у больных с синдромом раздраженной кишки. РМЖ. 2014;22(15):1103-7 [Grinevich VB, Sas EI, Kravchuk YA, et al. Safety of long-term use of selective M3 anticholinergics in patients with irritable bowel syndrome. Breast cancer. 2014;22(15):1103-7 (in Russian)].
33. Яковенко Э.П., Агафонова Н.А., Яковенко А.В., и др. Агонист опиатных рецепторов тримебутин в терапии функциональных расстройств желчного пузыря и сфинктера Одди. Лечащий врач. 2014;2:56 [Yakovenko EP, Agafonova NA, Yakovenko AV, et al. 0pi-ate receptor agonist trimebutin in the treatment of functional disorders of the gallbladder and the sphincter of 0ddi. Attending doctor. 2014;2:56 (in Russian)].
34. Ивашкин В.Т., Шелыгин Ю.А., Баранская Е.К., и др. Клинические рекомендации Российской гастроэнтерологической ассоциации и Ассоциации колопроктологов России по диагностике и лечению синдрома раздраженного кишечника. Российский журнал гастроэнтерологии, гепатологии и колопроктологии. 2017;27(5):76-93 [Ivashkin VT, Shelygin YuA, Baranskaya YK, et al. Diagnosis and treatment of the irritable bowel syndrome: clinical guidelines of the Russian gastroenterological association and Russian association of col-oproctology. Russian Journal of Gastroenterology, Hepatology, Colo-proctology. 2017;27(5):76-93 (in Russian)].
35. Ивашкин В.Т., Маев И.В., Шептулин А.А., и др. Клинические рекомендации Российской гастроэнтерологической ассоциации по диагностике и лечению функциональной диспепсии. Российский журнал гастроэнтерологии, гепатологии и колопроктологии. 2017;1:50-61 [Ivashkin VT, Mayev IV, Sheptulin AA, et al. Diagnosis and treatment of the functional dyspepsia: clinical guidelines of the Russian Gastroenterological Association. Russian Journal of Gastroenterology, Hepatology, Coloproctology. 2017;27(1):50-61 (in Russian)].
36. Ивашкин В.Т., Маев И.В., Шульпекова Ю.О., и др. Клинические рекомендации Российской гастроэнтерологической ассоциации по диагностике и лечению дискинезии желчевыводящих путей. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2018;28(3):63-80 [Ivashkin VT, Mayev IV, Shulpekova Yu0, et al. Diagnostics and treatment of biliary dyskinesia: clinical guidelines of the Russian gastroenterological Association. Russian Journal of Gas-troenterology, Hepatology, Coloproctology. 2018;28(3):63-80 (in Russian)]. D0I:10.22416/1382-4376-2018-28-3-63-80
Статья поступила в редакцию / The article received: 20.05.2021
omnidoctor.ru
Тримедат: инструкция по применению

Форма выпуска: Таблетки
МНН: Тримебутин
ФТГ: Спазмолитическое средство
Цены в аптеках: Минск
Уточняйте
Содержание
- Что из себя представляет препарат и для чего его применяют
- Противопоказания
- Особые указания и меры предосторожности
- Влияние на способность управлять транспортными средствами или работать с механизмами
- Применение
- Передозировка
- Хранение и срок годности
- Состав
- Внешний вид препарата и содержимое упаковки
Что из себя представляет препарат и для чего его применяют
Фармакотерапевтическая группа: Препараты для лечения функциональных нарушений желудочно-кишечного тракта.
Препарат Тримедат® содержит действующее вещество тримебутин. Тримебутин оказывает влияние на моторную деятельность (перистальтику) желудочно-кишечного тракта.
Препарат Тримедат® применяется у взрослых и детей старше 12 лет при следующих расстройствах:
синдром раздражённого кишечника, функциональные расстройства пищеварительного тракта, сопровождающиеся болями в животе, спазмами, чувством переполнения, метеоризмом, запором или диареей.
Цены в аптеках Минск
Препарат отсутствует в продаже
Аналоги
Необутин, таблетки, 100 мг ×10
Алиум, Россия • Без рецепта
Инструкция
10,37 — 16,20 р.
Где купить
Необутин, таблетки, 200 мг ×30
Алиум, Россия • Без рецепта
Инструкция
21,05 — 34,27 р.
Где купить
Трибукс, таблетки, 100 мг ×30
Биофарм, Польша • Без рецепта
Инструкция
34,40 — 53,79 р.
Где купить
Тримедат форте, таблетки, 300 мг ×20
с пролонгированным высвобождением покрытые пленочной оболочкой, Валента Фарм, Россия • Без рецепта
Инструкция
34,17 — 50,68 р.
Где купить
Тримедат инструкция по применению
Богданова Кристина Дмитриевна
29 октября 2021

ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ. ВОЗМОЖНЫ ПОБОЧНЫЕ ЭФФЕКТЫ. НЕОБХОДИМА КОНСУЛЬТАЦИЯ СПЕЦИАЛИСТА.
Автор статьи
Богданова Кристина Дмитриевна
,
Профессия: врач-педиатр
Название вуза: Уральский государственный медицинский университет (ГБОУ ВПО УГМУ МЗ РФ)
Специальность: педиатрия
Стаж работы: 4 года
Диплом о медицинском образовании: 106624 5087846 рег. номер 1641
Места работы: врач-педиатр в детской поликлинике, врач-консультант в лаборатории, автор статей в Мегаптеке
Все авторы
Содержание
- Показания к применению
- Противопоказания
- Возможные побочные эффекты
- Дозировка
- Тримедат форте
- Что лучше – необутин или тримедат?
- Что лучше – тримедат или дюспаталин?
- Препарат и алкоголь: совместимость
- Задайте вопрос эксперту по теме статьи
Для уменьшения боли и спазма гладкой мускулатуры кишечника врачи назначают тримедат. В одной таблетке лекарственного средства содержится 100 мг, 200 мг, 300 мг тримебутина малеата. Препарат также выпускается в виде порошка для приготовления суспензии для приема внутрь. Лекарственное средство обладает высоким профилем эффективности и минимальным спектром побочных эффектов.
Показания к применению
Гастроэнтерологи проводят симптоматическую терапию кишечных расстройств лекарственным средством тримедат. От чего назначают препарат? Тримедат эффективно уменьшает выраженность дискомфорта, спастической боли в животе, поноса, запора, метеоризма (повышенного газообразования в кишечнике).
Препарат назначают в составе комплексной терапии следующих заболеваний:
- Неэрозивной формы гастроэзофагеальной рефлюксной болезни;
- Желчнокаменной болезни;
- Нарушения функции желчевыводящих путей и сфинктера Одди;
- Синдрома раздражённого кишечника;
- Постхолецистэктомического синдрома;
- Послеоперационной паралитической кишечной непроходимости.
Хотите разбираться в аналогах лекарств, чтобы умело подбирать препараты на свой бюджет? Наша методичка от экспертов-провизоров «Аналоги популярных лекарств» поможет вам в этом! Получить методичку просто: подпишитесь на наши соцсети и напишите в сообщения «аналоги».
Мегаптека в соцсетях: ВКонтакте, Telegram, OK, Viber
Противопоказания
Врачи не назначают лекарственное средство пациентам, у которых повышена чувствительность к основному и вспомогательным ингредиентам препарата, беременным. На время лечения тримедатом женщин, которые кормят младенца грудью, ребёнка переводят на искусственное вскармливание.
Возможные побочные эффекты
Тримедат крайне редко оказывает побочное действие. Иногда у пациентов появляются следующие симптомы:
- Беспокойство;
- Головная боль;
- Головокружение;
- Сонливость;
- Чувство усталости.
У некоторых пациентов возникают неприятные вкусовые ощущения, сухость во рту, тошнота, понос или запор.
Аллергические реакции не выражены и проявляются кожной сыпью. Иногда на фоне приема препарата у женщин нарушается менструальный цикл, молочные железы увеличиваются, становятся болезненными. Эти симптомы проходят при прекращении приема лекарственного средства.
Дозировка
Врачи индивидуально подбирают дозы и кратность приема препарата каждому пациенту в зависимости от показаний, возраста и выраженности клинических проявлений болезни.
Взрослые принимают по 100-200 мг тримедата внутрь трижды в день. Их следует глотать целыми, запивать стаканом очищенной негазированной воды. Раствор для инъекций вводят внутривенно или внутримышечно по одной или две ампулы.
Детям препарат назначают в возрастных дозах согласно возрасту и в соответствующих лекарственных формах. Способ применения тримедата детям следующий:
- 3-5 лет: по 25 мг 3 раза в сутки;
- 5-12 лет: по 50 мг 3 раза в сутки;
- Старше 12 лет – 100-200 мг 3 раза в сутки.
Взрослым пациентам назначают по 100-200 мг 3 раза в сутки. В инструкции отсутствуют рекомендации, принимать тримедат до еды или после еды. Этот вопрос можно согласовать со своим лечащим врачом.
Сколько дней принимать тримедат взрослому для полного курса лечения?
Длительность курса лечения определяет врач. Рекомендуется для профилактики рецидива синдрома раздраженного кишечника в период ремиссии принимать поддерживающую до 300 мг в течение 12 недель.
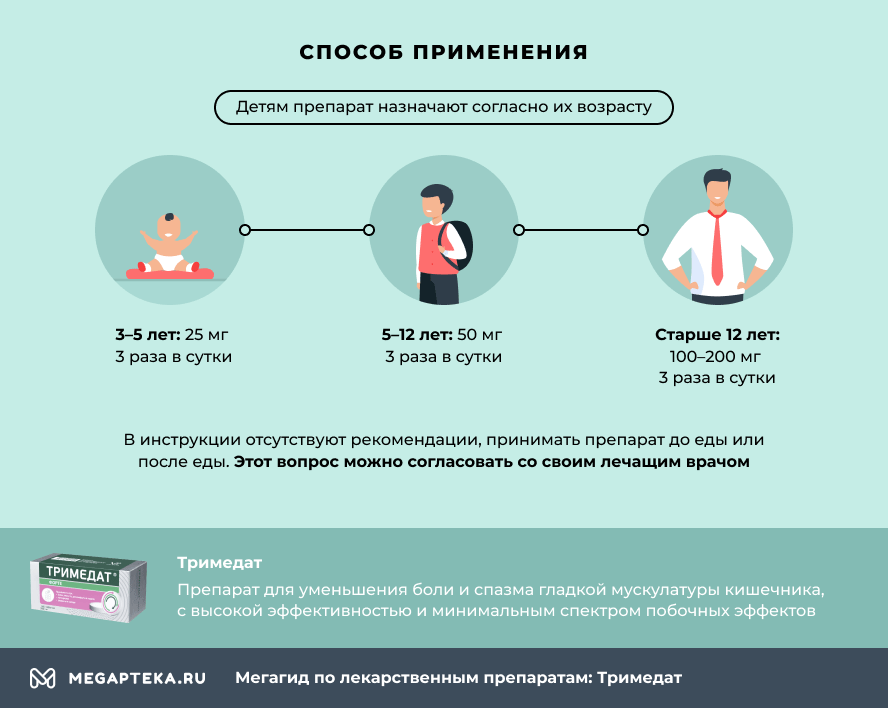
Тримедат форте
Разница между Тримедатом и Тримедатом форте состоит в дозировках, формах выпуска и составе вспомогательных веществ.
Тримедат выпускают в виде обычных таблеток, содержащих 100 и 200 мг тримебутина, а также в форме порошка для приготовления суспензии.
Таблетки и суспензию нужно принимать три раза в сутки, Тримедат форте — только 2 раза. Суспензия разрешена для лечения детей с 3 лет и имеет приятный вкус. К тому же ее легко дозировать в зависимости от возраста ребенка (в комплект входит мерный стаканчик).
Что лучше – необутин или тримедат?
Оба препарата в качестве действующего вещества содержат тримебутин. Кроме того, состав вспомогательных веществ практически идентичен. Врач должен выписывать лекарство по действующему веществу, чтобы пациент мог выбрать в аптеке препарат, подходящий по цене. Оба препарата находятся в одной ценовой категории. Упаковка 200 мг 30 шт. и того, и другого стоит 400-500 рублей. При выборе препараты вы можете смотреть на его доступность в аптеках и цену, которая вас устраивает.
Что лучше – тримедат или дюспаталин?
У Дюспаталина предполагается множественный механизм действия, затрагивающий разные уровни регуляции моторики кишечника. Это повышает эффективность лечения. Тримедат действует на одну систему регуляции работы кишечника, поэтому имеет меньше противопоказаний и побочных эффектов, а также разрешен для применения у детей с 3-х лет.
Препарат и алкоголь: совместимость
При употреблении тримедата с алкоголем усиливается риск развития побочных эффектов препарата (токсического воздействия на печёночные клетки, развитие язвенных дефектов органов пищеварения, желудочно-кишечного кровотечения).
Поэтому врачи не рекомендуют употреблять спиртные напитки не только во время лечения, но и в течение месяца после окончания курса терапии. О развившихся побочных эффектах следует немедленно поставить в известность своего лечащего врача.
При применении тримедата может нарушаться концентрация внимания. Поэтому производитель настоятельно рекомендует пациентам во время лечения осторожно водить транспортные средства, проявлять повышенное внимание во время выполнения работ, требующих быстроты психомоторных реакций.
Задайте вопрос эксперту по теме статьи
Остались вопросы? Задайте их в комментариях ниже – наши эксперты ответят вам. Там же Вы можете поделиться своим опытом с другими читателями Мегасоветов.
