Михаил Гурьевич Полуэктов, доцент, кандидат медицинских наук:
– «Михаил Гурьевич, здравствуйте, как вы относитесь к вальдоксану как к с снотворному? Спасибо». Вальдоксан это агомелатин, антидепрессант, действие которого связывают с влиянием на мелатониновые рецепторы. Считается, что он наиболее эффективен при депрессиях с нарушениями сна, то есть это не снотворное, это антидепрессант, который помогает при определенной форме депрессий.
«Какой препарат эффективен при раннем пробуждении?»
Оксана Михайловна Драпкина, профессор, доктор медицинских наук:
– Давайте скажем, что это Романова Марина Васильевна из Калуги.
Полуэктов М.Г.:
– Да. «Романова Марина Васильевна из Калуги. Какой препарат эффективен при раннем пробуждении?». Лучше при расстройствах сна с ранним пробуждением применять препараты с более длительным периодом полувведения. Если говорить о самых современных препаратах, то это так называемые Z-препараты, зопиклон имеет период полувведения 5-6 часов, как раз его хватает еще и для действия вот на утренние часы. Доксиламин, о котором мы говорили, донормил, также имеет период полувведения 10 часов, то есть он тоже может продлять свое действие до утреннего времени.
«Крюкова Татьяна Ивановна, Липецк. Спасибо за интересную актуальную лекцию, ваши сообщения всегда очень познавательны для широкого круга врачей». Спасибо. Оксана Михайловна, это вам.
Драпкина О.М.:
– «Шавлохова Эмма Акимовна. Здравствуйте». Эмма Акимовна наша участница постоянная из Владикавказа. «Уважаемая Оксана Михайловна, спасибо огромное за outstanding общение в прямом эфире, спасибо большое».
Полуэктов М.Г.:
– Замечательно. Ушакова Ирина Яковлевна, Ростов-на-Дону. Препараты мелатонина относительно новые. Какая у них ниша, когда и кому предпочтительнее?». Препараты мелатонина чем хороши, чем они замечательны? Тем, что они абсолютно безвредны. Ну, абсолютно – нельзя так говорить, имеют исключительно высокий профиль безопасности. Я очень люблю приводить данные исследования, где в течение двух лет пациенты применяли мелатонин в дозе 300 миллиграммов в сутки. 300 миллиграммов это, например, 100 таблеток мелаксена или 150 таблеток другого препарата. Вот поэтому самое главное свойство мелатонина, что он не повредит.
Когда он эффективен? Экзогенный мелатонин эффективен, когда собственный мелатонин перестает вырабатываться. Считается, что после 55 лет у большинства людей фактически уже нет выработки собственного мелатонина. И тогда-то эффект мелатонина как хронобиологического агента начинает быть заметным. Почему его не называют снотворным препаратом? Потому что он действует не через какие-то бодрствующие системы или тормозные системы мозга, он действует через внутренние часы. Он более четко обозначает для мозга время, когда нужно спать, а когда нужно вставать, когда нужно подниматься.
Вот мелатонин как раз обозначает время сна, а яркий солнечный свет обозначает время подъема, вот для чего применяются препараты мелатонина. И действительно, они более эффективны у пожилых людей, у которых часто путается это время ночное и дневное и он дает им сигнал к более правильному соблюдению распорядка. Спасибо.
Драпкина О.М.:
– Спасибо огромное. «Буйкова Светлана Валерьяновна из Чебоксар. Большое спасибо всем, всем, всем за прекрасные лекции». Большое спасибо вам, наши уважаемые коллеги, наша уважаемая дорогая аудитория. Все это мы делаем, и сами учимся, и заряжаемся от вас желанием все дальше и дальше учиться. Татьяна Ивановна Крюкова, Липецк говорит тоже слово спасибо, и модераторам огромное спасибо за прекрасную связь – это я хочу передать нашей технической поддержке, нашему техническому директору со своей командой.
И огромное спасибо вам как всегда за лекции, и так получается, вы часто у нас завершаете интернет-сессию, обычно под занавес всегда выпускают артиста, который может держать аудиторию, который может ее всколыхнуть и вам всегда это удается. Поэтому отдельное вам спасибо за это, Михаил Гурьевич.
Полуэктов М.Г.:
– Настраиваю на сон.
Драпкина О.М.:
– Да, настраиваете на сон. Я хочу сказать. Уважаемые коллеги, у нас сегодня закончилась XXXVI всероссийская интернет-сессия образовательная, следующая такая большая встреча будет 11-12 февраля, нас ждет интернет-конгресс. У нас будет очень много иностранных экспертов. Мы принимаем заявки на те темы, которые вы хотели бы обсудить поподробнее. Пожалуйста, пишите info@internist.ru. И еще раз спасибо за то, что действительно были сегодня с нами, у нас сегодня 12-часовой рабочий день, с 7 до 7 и надеемся, что наше общение было взаимоприятным. Спасибо и до свидания.
Вальдоксан (агомелатин): современный подход к лечению умеренных и тяжелых эндогенных депрессий непсихотического уровня
Статьи
Опубликовано в :
«ОБОЗРЕНИЕ ПСИХИАТРИИ И МЕДИЦИНСКОЙПСИХОЛОГИИ » »» № 3 , 2011
Л.И.Абрамова, Т.Е.Новоженова, С.А.Сорокин
Научный центр психического здоровья РАМН, Москва
Резюме. Проведена оценка терапевтической эффективности и переносимости Вальдоксана (агомелатина) в дозе 25-50 мг в сутки у 26 больных с умеренными и тяжелыми эндогенными депрессиями непсихотического уровня. Продолжительность исследования составила 56 дней. Редукция депрессивной симптоматики отмечена у всех 26 больных. К завершению исследования формирование ремиссии по шкале депрессии HDRS-21 наблюдалось у 76,9% пациентов. Побочные эффекты препарата выявлены лишь в одном случае, имели слабую степень выраженности, быстро редуцировались, не препятствовали проведению терапии. Результаты исследования показали, что Вальдоксан обладает высокой терапевтической антидепрессивной активностью при лечении больных эндогенными депрессивными состояниями непсихотического уровня умеренной и тяжелой степени выраженности.
Ключевые слова: эндогенная депрессия, депрессия непсихотического уровня, Вальдоксан (агомелатин), терапевтическая эффективность, переносимость.
Высокая распространенность депрессивных состояний, трудности их терапевтической коррекции, значимое влияние, которое они оказывают на социальную адаптацию, качество жизни пациентов, обусловливают постоянный интерес к поискам патогенетических механизмов возникновения и развития депрессий, а также оптимизации терапевтического подхода к этому контингенту больных.
В настоящее время существует несколько основных гипотез, на основании которых предпринимаются попытки объяснить патогенез депрессивных нарушений.
Одной из самых ранних гипотез, сформулированных в середине прошлого столетия, является моноаминовая, согласно которой в основе развития депрессии лежит дефицит моноаминов (норадреналина, серотонина) в ключевых областях головного мозга.
Однако депрессию невозможно объяснить только дисфункцией одного из моноаминов [1]. Так, имеющая место генная гипотеза постулирует, что депрессия возникает не столько из-за дефицита моноаминов, сколько из-за изменений в работе генов. Рецепторная гипотеза предполагает, что депрессия развивается не столько из-за уменьшения концентрации нейромедиаторных моноаминов в тканях мозга, сколько из-за нарушения функций рецепторных структур. Продолжаются исследования, направленные на изучение патофизиологических механизмов депрессии и разработку новых препаратов, действующих на гипофизарно-гипоталамо-надпочечниковую систему, нейропептидные рецепторы или промотирующих продукцию факторов роста и/или клеточной пролиферации в гиппокампе. Можно полагать, что все перечисленные механизмы являются звеньями патогенетического процесса, лежащего в основе развития депрессивных нарушений.
Еще одной концепцией развития депрессивных расстройств является хронобиологическая, основывающаяся на том, что депрессивные состояния нередко сопровождаются десинхронизацией биологических ритмов. Исходя из этого возникло предположение реализации антидепрессивного эффекта путем нормализации циркадианных ритмов [2, 3]. Водителем ритма для поддержания циркадианных циклических изменений в организме человека является супрахиазматическое ядро, расположенное в переднем гипоталамусе. Ключевую роль в синхронизации циркадианных ритмов, включая цикл «сон-бодрствование», выполняет хронобиотический гормон мелатонин, который синтезируется в эпифизе [4]. Синтез гормона мелатонина регулируется супрахиазматическим ядром, выработка его приходится на ночную фазу суточного цикла. Мелатонин поступает из эпифиза в супрахиазматическое ядро, где связывается с МТ1— и МТ2-рецепторами и осуществляет регуляцию циркадианных ритмов. Антидепрессивные свойства мелатонина не получили подтверждения в клинических исследованиях, однако послужили основой для создания препаратов, использующих свойства мелатонина.
Французская фармацевтическая компания «Лаборатории Сервье» синтезировала уникальный антидепрессивный препарат Вальдоксан (агомелатин). Терапевтическое действие Вальдоксана реализуется посредством влияния на мелатонинергическую (агонизм к MT1— и МТ2-рецепторам), что предполагает ресинхронизацию циркадианных ритмов, а также серотонинергическую (антагонизм к 5-НТ2С-рецепторам) системы. Антагонизм к 5-НТ2С-рецепторам в силу реципрокных отношений приводит к специфическому и опосредованному высвобождению двух основных нейротрансмиттеров во фронтальной коре, играющих важную роль при депрессии, — норадреналина и дофамина [2, 5, 6]. Благодаря таким свойствам Вальдоксан обнаруживает высокую эффективность при лечении депрессивных состояний, в том числе и сезонного характера [4, 7-9].
В России Вальдоксан используется с 2008 г. К настоящему времени проведен ряд зарубежных и отечественных исследований, в том числе плацебо-контролируемых, а также исследования сравнительного характера [10-13].
Имеются данные о выраженной эффективности Вальдоксана при лечении умеренных и тяжелых депрессивных состояний непсихотического уровня у пациентов в стационарных и амбулаторных условиях [6, 7, 10-15].
Цель исследования — анализ клинической эффективности и переносимости Вальдоксана (агомелатина), используемого в стандартных дозах, при лечении умеренных и тяжелых эндогенных депрессий непсихотического уровня.
Материал и методы исследования
Открытое несравнительное исследование поведено в отделе по изучению эндогенных психических расстройств и аффективных состояний НЦПЗ РАМН в течение 2010 г. Все пациенты дали добровольное письменное согласие на участие в исследовании.
Критерии включения.
В исследование включались больные обоего пола в возрасте от 18 до 65 лет, находившиеся на стационарном, а в ряде случаев в дальнейшем на амбулаторном лечении. Депрессивные состояния больных оценивались в рамках маниакально-депрессивного психоза с моно- или биполярным течением и приступообразной шизофрении. Согласно Международной классификации болезней 10-го пересмотра (МКБ-10) речь шла о единичном депрессивном эпизоде (рубрика F32.1-2; 3 наблюдения), рекуррентном депрессивном расстройстве (рубрика F33.2; 10 наблюдений), депрессивном эпизоде в рамках биполярного аффективного расстройства (F31.3-4; 8 наблюдений), а также о депрессивных состояниях, развивающихся у больных после психотических приступов и отвечающих диагностическим критериям рубрики F20.4 по МКБ-10 «постшизофреническая депрессия» при отсутствии иных продуктивных расстройств (5 наблюдений). Во всех случаях депрессивная симптоматика соответствовала описанию депрессивного эпизода рубрики F32 по МКБ-10, при этом длительность депрессивного состояния составляла не менее 2 недель. Тяжесть депрессивного состояния должна была достигать умеренной или тяжелой степени, составлять не менее 17 баллов по первым 17 пунктам шкалы депрессии Гамильтона (HDRS-21) и не менее 4 баллов по шкале общего клинического впечатления (CGI-S — тяжесть заболевания) на визите 1.
Критерии исключения.
Высокий суицидальный риск (более 2 баллов по пункту 3 шкалы HDRS-21 и/или по клинической оценке исследователя); наличие психотических симптомов (т.е. наличие баллов по пунктам 18-21 шкалы HAMD-21); прием ингибиторов МАО в течение 2 недель до начала исследования; установленная ранее индивидуальная непереносимость Вальдоксана (агомелатина) или неудовлетворительный эффект применения Вальдоксана в анамнезе при назначении препарата в адекватной дозе (не менее 25 мг в сутки) и адекватной длительности (не менее 4 недель); наличие ряда психических расстройств (алкоголизм, наркомания) в анамнезе, тяжелых декомпенсированных заболеваний внутренних органов (почечная и/или печеночная недостаточность, злокачественные новообразования, метаболические заболевания, инсулинозависимый сахарный диабет, тиреотоксикоз); беременность или кормление грудью.
С учетом критериев включения/исключения в исследовании приняли участие 26 больных (23 женщины, 3 мужчин) (преобладание женщин объяснялось, прежде всего, условиями набора материала в женских отделениях) в возрасте: на период настоящего стационирования от 18 до 65 лет (средний возраст 37,3±13,3 года); на период манифестации болезненного процесса — от 6 до 48 лет (в среднем 26,1±13,3 года) (табл. 1). Длительность заболевания от манифестных его проявлений составила от 1 мес до 32 лет (в среднем 11,2±10,4 года). За этот период больные перенесли от 1 до 42 аффективных эпизодов (без учета настоящего) (в среднем 5,4±8,1 аффективных фаз на больного). Длительность исследуемой депрессии составила от 0,5 до 30 мес (в среднем 7,5±9,3 мес).
Таблица 1. Общие характеристики больных, участвующих в исследовании
| Пол | возраст (лет) ± SD | Тяжесть депрессии | Возраст начала заболевания | Длительность заболевания с манифестации (годы) | Длительность депрессии (мес) | Количество перенесенных аффективных фаз | ||
| умеренная | тяжелая | |||||||
| Муж. | 3 | 53±13,1 | 2 | 1 | 15,0±5,0 | 19,2±14,7 | 12,3±15,3 | 15,7±22,9 |
| Жен. | 23 | 34,9±12,1 | 15 | 8 | 25,1±13,8 | 10,1±9,6 | 6,87±8,6 | 4,0±3,2 |
| Все | 26 | 37,3±13,3 | 17 | 9 | 26,1±13,3 | 11,2±10,4 | 7,5±9,3 | 5,4±8,1 |
На период включения в исследование преобладающими в состоянии больных были жалобы на подавленное настроение. У 11 пациентов наряду с этим выявлялось выраженное чувство тревоги, нередко неопределенной, ни чем не мотивированной, сопровождающейся моторным беспокойством. В других 4 наблюдениях ведущим был тоскливый аффект, с локализацией щемящего чувства тоски преимущественно в загрудинной области. В состоянии 3 больных преобладали апато-адинамические, астенические проявления. У 8 пациентов наблюдалось различное сочетание аффективных компонентов, например тревожного аффекта с апато-адинамическими проявлениями, тревоги, перемежающейся с чувством тоски.
В структуре депрессивного состояния наиболее часто встречающимся симптомом было расстройство сна, на период начала исследования лишь 3 больных не предъявляли подобного рода жалоб. Трудности возникали преимущественно с процессом засыпания, этот период был особенно мучителен для больных. Также ухудшалось и качество сна, который был тревожный, с частыми пробуждениями и неприятным характером сновидений, сокращалась общая его продолжительность.
Соматическая патология наблюдалась у 12 (46,2%) больных: наиболее часто — вегетососудистая дистония (8 наблюдений), реже — заболевания желудочно-кишечного тракта в виде язвенной болезни желудка в состоянии ремиссии (2 наблюдения), артериальная гипертония (2 наблюдения), хронический тонзиллит (2 наблюдения), в единичных наблюдениях встречались ишемическая болезнь сердца, эндокринная кардиопатия, опоясывающий лишай; перечисленные заболевания могли встречаться в сочетании у одного больного. К началу терапии Вальдоксаном соматическое состояние всех пациентов было компенсированным, что не исключало применения в ходе исследования сердечно-сосудистых, гипотензивных и других медикаментозных средств в дозах, которые пациенты получали до его начала.
Исследование проводилось с использованием клинического, клинико-психопатологического, психометрического методов с применением оценочных шкал: шкалы для оценки депрессии Гамильтона (Hamilton Depression Rating Scale — HDRS-21); шкалы общего клинического впечатления
— CGI (Clinical Global Impression) c двумя подшкалами: CGI-S
— для оценки тяжести заболевания и CGI-I — для оценки динамики состояния больных в сравнении с исходным уровнем (шкалы использовались для оценки тяжести и динамики депрессивных состояний); UKU (Udvalg for Kliniske Undersogelser Scale) — шкалы для оценки нежелательных явлений (серьезных и несерьезных), возникающих в ходе терапии. Статистическая обработка полученных данных осуществлялась с использованием приложения MS Excel пакета программ MS Office1.
К началу лечения индивидуальный суммарный балл (СБ), отражающий степень тяжести депрессивного состояния, по шкале HDRS-21 составлял от 18 до 39 баллов, в среднем -24,42, 95% ДИ 22,70-26,14, т.е. речь шла о депрессивных состояниях умеренной (17 наблюдений) и тяжелой (9 наблюдений) степени выраженности. По шкале CGI-S тяжесть депрессии к началу лечения была на уровне умеренной — у 17 и тяжелой — у 9 больных (при среднем уровне 4,35).
Курс лечения составил 8 нед (56 дней). Тяжесть депрессивного состояния у больных, его динамика в процессе терапии, возникающие побочные эффекты оценивались c использованием указанных шкал до начала терапии (день 0 -Д0), а затем в ходе исследования в дни 3-й (Д3), 5-й (Д5), 7-й (Д7), 14-й (Д14), 28-й (Д28), 42-й (Д42) и 56-й (Д56) (всего 8 визитов).
Динамика состояния больных по группе в целом в ходе лечения Вальдоксаном (агомелатином) определялась по редукции среднего суммарного балла (ССБ) указанных шкал. Терапевтический эффект оценивался как «значительный» при снижении среднего суммарного балла в сравнении с днем 0 на 50% и более (больные «респондеры»), как «умеренный» — при редукции на 30-49% и как «незначительный» или «отсутствие эффекта» — при уменьшении среднего балла до 29%. При оценке состояния как «ремиссия» средний балл по шкале HDRS-21 у пациента не должен был превышать 6 баллов. Для оценки клинического эффекта использовался также коэффициент редукции R — величина, отражающая редукцию ССБ на любом из визитов по отношению к его исходной величине на визите Д0, выраженная в процентах [16].
До начала (Д0) и в ходе исследования для оценки безопасности применения и переносимости Вальдоксана наряду с клиническими параметрами анализировались показатели соматического состояния больного: масса тела, частота сердечных сокращений, уровень артериального давления, данные электрокардиографии, а также результаты общего и биохимического анализов крови.
Вальдоксан назначался однократно в день, в вечернее время, начиная с 25 мг; 16 больным уже в первые 2 нед при отсутствии явных признаков улучшения психического состояния и при условии хорошей переносимости препарата его доза повышалась до 50 мг, у остальных пациентов до конца исследования сохранялась терапевтически эффективная доза в 25 мг.
При терапии постшизофренических депрессий, с учетом существующих рекомендаций, наряду с применением Вальдоксана была сохранена антипсихотическая терапия. Больные этой группы получали в терапевтических дозах психотропные средства (такие нейролептики, как инвега, зипрекса, абилифай, этаперазин, трифтазин, сероквель), нормотимики в качестве стабилизирующей, поддерживающей терапии. Следует заметить, что используемые дозы в процессе исследования практически не менялись. При стойком расстройстве сна для его регулирования допускалось непродолжительное (не более недели) использование транквилизаторов (лоразепам, седуксен и др.), «мягких» нейролептиков, дозировки которых корригировались в ходе проводимого лечения. Допускался совместный прием Вальдоксана с антидепрессантами иных классов (исключение — ингибиторы МАО), применение которых на этапе, предшествующем настоящему исследованию, не дало ожидаемого терапевтического эффекта, при сохранении их используемой дозы на прежнем уровне.
На каждого пациента исследователи заполняли карту, в которой регистрировались демографические показатели, диагноз, краткий медицинский анамнез, данные клинического состояния пациента, оцениваемого по шкалам, сопутствующие заболевания и их терапия, нежелательные явления, эффективность проводимого лечения.
Таблица 2. Основные статистические показатели для шкал депрессии HDRS-21 и СGI-S при терапии Вальдоксаном
| Дни визитов |
HDRS-21 | CGI-S | ||||||
| Среднее значение ССБ (абс.) | СО* | R** | 95% ДИ*** | Среднее значение (абс.) | СО | R | 95% ДИ | |
| 0 | 24,42 | 4,47 | (22,70–26,14) | 4,35 | 0,49 | (4,16–4,53) | ||
| 3 | 21,42 | 5,99 | 12,28% | (19,12–23,73) | 3,92 | 0,69 | 9,73% | (3,66–4,19) |
| 5 | 19,00 | 6,34 | 22,20% | (16,56–21,44) | 3,69 | 0,68 | 15,04% | (3,43–3,95) |
| 7 | 17,38 | 6,23 | 28,82% | (14,99–19,78) | 3,50 | 0,91 | 19,47% | (3,15–3,85) |
| 14 | 12,08 | 7,19 | 50,55% | (9,31–14,84) | 3,00 | 0,89 | 30,97% | (2,66–3,34) |
| 21 | 9,00 | 6,20 | 63,15% | (6,62–11,38) | 2,54 | 0,90 | 41,59% | (2,19–2,89) |
| 28 | 7,96 | 5,78 | 67,40% | (5,74–10,18) | 2,35 | 1,13 | 46,02% | (1,91–2,78) |
| 42 | 5,58 | 5,01 | 77,17% | (3,65–7,50) | 1,85 | 0,92 | 57,52% | (1,49–2,20) |
| 56 | 3,81 | 3,35 | 84,41% | (2,52–5,09) | 1,46 | 0,81 | 66,37% | (1,15–1,77) |
*СО – стандартное отклонение; **R – коэффициент редукции; ***ДИ – доверительный интервал.
Рис. 1. Динамика коэффициента редукции ССБ по шкалам HDRS-21 и CGI-S при терапии Вальдоксаном.
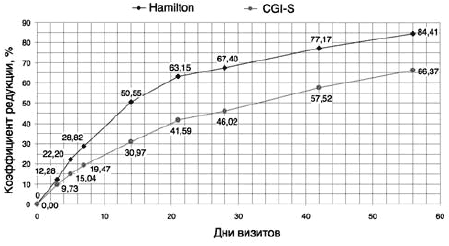
Результаты исследования и их обсуждение
Все 26 больных, включенных в исследование, полностью завершили его, и по конечному результату у всех был отмечен терапевтический эффект. Проведена оценка тяжести депрессивного состояния на период завершения исследования и в динамике по группе в целом с использованием психометрических шкал CGI-S, CGI-I, шкалы депрессии HDRS-21 (табл. 2, рис. 1).
На период завершения исследования клиническое улучшение по шкале CGI-S наблюдалось у всех прошедших исследование больных, при этом у 21 (80,8%) из них улучшение было значительным, пациенты расценены как респондеры; умеренное улучшение отмечалось в 3 (11,5%) наблюдениях и незначительный эффект — в 2 (7,7%) наблюдениях. По шкале депрессии HDRS-21 у всех 26 пациентов редукция ССБ составила 50% и более, что позволяло оценить терапевтический эффект как значительный.
К началу исследования по субшкале CGI-S тяжесть депрессивного состояния у 9 больных оценивалась на уровне 5 — как тяжелая, у 17 больных на уровне 4 — как умеренная. По группе в целом среднее состояние больных соответствовало уровню 4,35, т.е. ближе к градации «умеренная тяжесть заболевания». Уже к 14-му дню терапии отмечался отчетливый клинический эффект, по исследуемой группе в целом уровень тяжести заболевания составлял 3,0 (снизился относительно уровня исходного состояния в 1,5 раза) -«легкий», при коэффициенте редукции R — 30,97% (на этот период лишь у 1 пациента тяжесть состояния оценивалась на уровне 5, уровень 4 наблюдался у 5 пациентов, у 15 больных — уровень 3, у 3 больных — уровень 2 и у 2 пациентов -уровень 1). К 28-му дню тяжесть заболевания приближалась к уровню 2,35 — «пограничное психическое расстройство» (при этом только у 4 пациентов уровень тяжести заболевания составил 4) при R равном 46,02%. К 42-му дню тяжесть заболевания составила 1,85, соответствуя оценке «пограничное психическое расстройство» (уровень 3 тяжести депрессии наблюдался только у 9 больных, у других 17 он был ниже), и к 56-му дню достигла в среднем уровня 1,6, что соответствовало промежуточной оценке тяжести заболевания между «пограничным психическим расстройством» и «не болен» (при этом в 21 наблюдении уровень тяжести заболевания составил 1-2 и только в 5 наблюдениях — 3).
По субшкале CGI-I, служащей для анализа клинического впечатления об изменении состояния пациента в сопоставлении с исходным уровнем, по группе в целом динамика психического состояния больных к 14-му дню оценивалась между «небольшим» и «выраженным» улучшением (уровень 4,62), уже к 28-му дню как «выраженное улучшение» (уровень 5), к завершению терапевтического периода ближе к «очень выраженному улучшению». При этом у 21 (80,8%) пациента из прошедших исследование речь шла об «очень выраженном улучшении» (уровень 6), у остальных 5 (19,2%) -о «выраженном улучшении».
Высокую терапевтическую эффективность Вальдоксана (агомелатина) подтвердил также и анализ динамики ССБ по шкале HDRS-21 (см. табл. 2, рис. 1), согласно которому у всех 26 пациентов редукция ССБ составила 50% и более, что позволяло оценить терапевтический эффект как «значительный». Если к началу терапии тяжесть депрессивного состояния у больных индивидуально оценивалась в диапазоне от 18 до 39 баллов и ССБ по группе в целом был равен 24,42, то к завершению исследования индивидуальный средний балл у больных находился в диапазоне от 0 до 13, а ССБ по группе в целом составил лишь 3,81 при R равном 84,41%. К этому времени только у 6 (23,1%) больных можно было говорить о признаках легкой депрессии (у 3 пациентов — по 7 баллов и в единичных случаях — по 8, 11, и 13 баллов), в остальных же 20 наблюдениях индивидуальный средний балл составлял от 0 до 6, т.е. признаки депрессии отсутствовали, состояние пациентов можно было квалифицировать как ремиссионное.
Клиническое улучшение состояния больных, проявляющееся в улучшении настроения, появлении психофизической активности, снижении интенсивности «грустных» мыслей, в редуцировании конгруэнтных настроению идей самообвинения, малоценности, обвинения сверхценного характера, по группе в целом отчетливо выявлялись уже к 14-му дню лечения, к этому периоду ССБ снизился до 12,08 балла, R — 50,55% (при этом у 5 больных величина среднего балла была уже ниже 7, пациенты находились в состоянии ремиссии). К 21-му дню ССБ составил 9,0 (снизившись сравнительно с начальным уровнем почти втрое — в 2,7 раза при редукции на 63,15%). Отчетливый антидепрессивный эффект сохранялся на дальнейших этапах лечения: к 42-му дню по группе в целом ССБ по шкале HDRS-21 составил 5,58 (R — 77,17%) (средний балл оказался меньше 7 уже у 16 пациентов) и к 56-му дню, к завершению исследования, как уже было отмечено, — 3,81 балла при R — 84,41%.
Рис. 2. Динамика коэффициента редукции ССБ, отражающего собственно тимолептический, стимулирующий, анксиолитический эффекты Вальдоксана
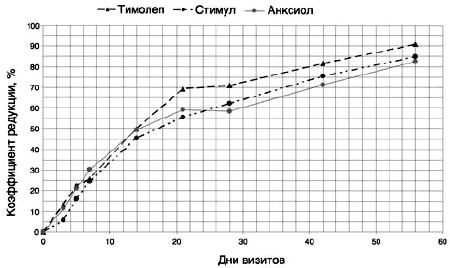
Рис. 3. Динамика коэффициента редукции ССБ признаков 4–6 (нарушения сна) по шкале депрессии HDRS-21.
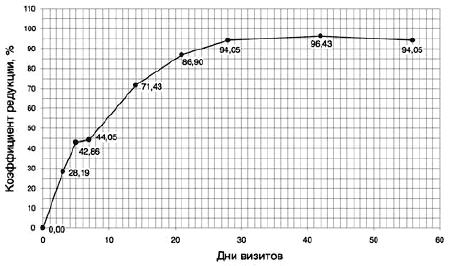
Анализ показал 4 варианта индивидуальной динамики среднего балла по шкале HDRS-21 в исследуемой группе больных. Так, у подавляющего большинства из них (12 наблюдений) эффект развивался быстро, уже к 5-14-му дню терапии было характерно редуцирование среднего балла на 50% и выше, что свидетельствовало о «значительном» улучшении их состояния; в дальнейшем терапевтический эффект продолжал нарастать, но уже более медленными темпами. У 6 пациентов скорость наступления лечебного эффекта также была отчетливо выраженной, но 50% редукция среднего балла выявлялась на 14-21-й день терапии. В 4 наблюдениях кривая нарастания эффекта была пологой, а «значительный» терапевтический эффект развивался после 28 дня лечения. 2-я группа больных занимала как бы промежуточное положение между 1-й и 3-й подгруппами больных. Что касается 4 больных, то их состояние отличалось клинической нестабильностью, проявляющейся чередованием периодов улучшения/снижения глубины депрессии и ухудшения/нарастание глубины депрессии, в то же время в итоге к периоду завершения исследования клинический эффект оказался достаточно высоким и устойчивым. Мы не анализировали особенности разнообразия подобной динамики, для этого требуются больший объем исследуемого материала и иные методические подходы.
Как видно из табл. 2, по шкалам HDRS-21 и CGI-S статистические различия показателей в сопоставлении с Д0 выявляются уже к 5-му дню лечения. Полученные данные по терапевтическому эффекту Вальдоксана совпадают с результатами исследований, проведенных другими авторами.
Проведен анализ трех основных эффектов, свойственных антидепрессантам: собственно тимолептического, стимулирующего, седативного (анксиолитического). Собственно тимолептический эффект Вальдоксана оценивался по динамике ССБ признаков 1-3 (депрессивное настроение, чувство вины, суицидальные намерения) шкалы HDRS-21, отражающих особенности и тяжесть тимического компонента состояния; стимулирующий — по редукции ССБ признаков 7-8 (работоспособность и активность, заторможенность) шкалы HDRS-21, регистрирующих апато-адинамические проявления депрессии; анксиолитический эффект — по редукции ССБ признаков 9-11 (ажитация, психическая тревога, соматическая тревога), отражающих тревожный компонент депрессии. К началу терапии Вальдоксаном ССБ собственно тимического компонента составлял 4,62 балла, апато-адинамического — 4,08 балла, тревожного — 5,46 балла, а к завершению исследования — 0,42 (R -90,63%); 0,62 (R — 84,91%) и 0,96 (R — 82,39%) соответственно, что отражало значительное улучшение состояния больных по данным параметрам (табл. 3). По завершающему результату по редукции признаков собственно тимического компонента «значительное» улучшение наблюдалось у 25 больных, у 1-го пациента речь шла об «умеренном» улучшении (R — 40,0%); схожие результаты отмечены при анализе редукции апато-адинамических проявлений; что касается редукции признаков тревожности, то «значительное» улучшение отмечено у всех 26 больных.
Из рис. 2 видно, что все исследуемые эффекты имели сходную динамику, активно развивались с первых дней терапии, уже к 14-му дню исследования коэффициент редукции ССБ, отражающего выраженность тимических, апато-адинамических, тревожных компонентов состояния больных, составил 50,0%, 49,30% и 45,28% соответственно при сохранении тенденции к нарастанию. К завершению исследования в высокой степени реализовались все три эффекта Вальдоксана, коэффициент редукции признаков, отражающих тимический компонент состояния больных, несколько преобладал и составил 90,83%, коэффициенты редукции признаков апато-адинамического и тревожного компонентов были близкими — 84,91% и 82,39% соответственно. Таким образом, по времени развития эффекта и завершающим результатам общее антидепрессивное действие Вальдоксана можно оценить как сбалансированное.
Согласно существующим данным от 50 до 90% больных с депрессивной симптоматикой жалуются на нарушение сна. Расстройство сна, отражающее изменение суточного циркадианного ритма, биологических часов, регулирующих суточные колебания состояния организма, может проявляться изменением всех его стадий, а именно: увеличением длительности периода засыпания, неспокойным сном, неприятными по содержанию сновидениями, ранним пробуждением с невозможностью вновь заснуть. Установлено, что в сопоставлении с другими антидепрессантами Вальдоксан сокращает время засыпания и улучшает качество сна без сонливости в дневное время [10].
В настоящем исследовании был проведен анализ динамики среднего суммарного балла признаков 4-6 (ранняя бессонница, средняя бессонница, поздняя бессонница) шкалы депрессий HDRS-21 и коэффициента его редукции в ходе лечения Вальдоксаном (рис. 3).
Из рис. 3 видно, что нормализация процесса сна осуществлялась довольно эффективно. Так, если к началу терапии по группе в целом ССБ признаков, характеризующих нарушение сна, составил 3,23, то уже на 5-й день лечения он снизился до 1,85 балла при R — 42,86% (с этого времени выявлялись и статистически значимые различия величины ССБ исследуемого параметра в сопоставлении с его уровнем к началу лечения); к 14-му дню лечения — до 0,92 (уменьшение в 3,5 раза) при R — 71,43%; к 56-му дню — 0,19 при R — 94,05%. При этом к 5-му дню лечения нарушения сна не регистрировались у 8 больных, к 14-му дню — у 13, к 28-му дню — уже у 22 больных, к 56-му дню расстройства сна обнаруживались лишь у 3 пациентов (из них у 2 — на уровне 2 баллов при первоначальном уровне на Д0 равном 6 и 4 баллам соответственно; у 1-го — на уровне 1 балла при изначальном уровне равном 6 баллам). Значительное улучшение на период завершения исследования наблюдалось у всех больных с расстройством сна. Наиболее быстро регулировался процесс засыпания. В наших наблюдениях отсутствовали жалобы на дневную сонливость.
За весь период исследования ни у одного из пациентов не наблюдалось появления новой продуктивной симптоматики.
Побочные эффекты
При оценке клинической эффективности препарата особое внимание уделялось анализу нежелательных явлений, которые возникали в ходе лечения и регистрировались независимо от их причинно-следственной связи с препаратом исследования. Оценка нежелательных (побочных) эффектов проводилась с использованием шкалы UKU с учетом их клинической характеристики, степени тяжести и длительности.
Нежелательные явления были выявлены всего лишь у одного больного. Они характеризовались появлением через неделю от начала лечения изжоги, неприятных ощущений в эпигастрии. По клиническим проявлениям они были отнесены к «автономным побочным эффектам» по шкале UKU. Следует отметить, что пациентка с перечисленными жалобами страдала хроническим гастритом. К терапии был добавлен фестал, мотилиум. Такое состояние продолжалось 4 дня, в дальнейшем описанная симптоматика не повторялась, лечение Вальдоксаном не прекращалось, доза препарата не менялась. Анализ таких параметров, как клинические и биохимические показатели крови, динамика массы тела, показатели электрокардиографии, не обнаружил клинически значимых отклонений в течение всего периода терапии.
Что касается изменений массы тела, то в 12 наблюдениях она была достаточно устойчивой, незначительно повышалась или снижалась до 0,5 кг. Из 10 пациентов с признаками повышения массы тела у 9 она увеличилась не более чем на 1-2 кг, и лишь в единичном случае — на 4 кг (пациентка изначально была с признаками ожирения); еще у 4 пациентов данной подгруппы масса тела до включения в исследование превышала нормальные показатели, что свидетельствовало о нарушении у них жирового обмена. У 6 больных речь шла о компенсации массы тела (увеличение на 1-1,5 кг), потерянной во время предшествующего лечению периода депрессии. Примечательно, что пациенты отмечали преимущественно факт восстановления, но не повышения аппетита.
Заключение
Проведенное 56-дневное исследование клинической эффективности и переносимости Вальдоксана (агомелатина) убедительно показало, что препарат обладает высокой терапевтической антидепрессивной активностью при лечении больных эндогенными депрессивными состояниями непсихотического уровня умеренной и тяжелой степени выраженности.
Особенностью препарата является раннее наступление терапевтического эффекта, который отчетливо проявлялся уже в первые 2 нед лечения, достигая значительной степени выраженности уже к 4-й неделе лечения и не уменьшался на дальнейших этапах его применения. К завершению исследования формирование ремиссии по шкале депрессии HDRS-21 наблюдалось у 76,9% из принявших участие в исследовании больных. Следует отметить, что полученные данные согласуются с результатами ранее проведенных работ.
Несомненное достоинство препарата — сбалансированный характер действия, включающий собственно тимолептический, анксиолитический, стимулирующий эффекты, что позволяет использовать его при депрессиях различной клинической структуры, а именно: с аффектом тоски, тревоги, апато-адинамическими проявлениями, при этом по конечному результату изученные эффекты близки по степени выраженности.
Побочные эффекты применения Вальдоксана имеют невысокую частоту развития, минимальны по степени выраженности и в большинстве случаев транзиторны, не требуют отмены препарата, что, возможно, связано с отсутствием или слабо выраженной его способностью к связыванию с рядом рецепторов, в частности серотониновыми 5-HT1A-, 5-HT2-рецепторами, D1— и D2-допаминовыми рецепторами, α1-, α2-, ß-адренергическими, гистаминовыми H1-рецепторами, холинорецепторами, бензодиазепиновыми и опиоидными рецепторами. Следует отметить, что Вальдоксан может успешно применяться у больных, отягощенных соматическими заболеваниями, так как не вызывает их обострения.
Таким образом, особенности спектра действия Вальдоксана позволяют эффективно использовать его при лечении разных по степени тяжести и клиническим проявлениям эндогенных депрессивных состояний. Быстрота наступления терапевтического эффекта, сохранение его на высоком уровне в ходе дальнейшей терапии, благоприятный профиль нежелательных явлений и их незначительная выраженность, а также непродолжительность существования -несомненные преимущества препарата.
Появление нового мелатонинергического антидепрессанта Вальдоксана (агомелатина), позволяет расширить возможности лечения пациентов с расстройствами депрессивного спектра и нарушениями сна, предотвратить рецидивы заболевания.
Сведения об авторах
Абрамова Лилия Ивановна — д-р мед. наук, вед. науч. сотр. НЦПЗ РАМН
Новоженова Тамара Евгеньевна — врач НЦПЗ РАМН
Сорокин Сергей Александрович — мл. науч. сотр. НЦПЗ РАМН
Список использованной литературы
- Wong ML, Licinio J. From monoamines to genomic targets: a paradigm shift for drug discovery in depression. Nat Rev Drug Discov 2004; 3: 136-51.
- Racagni G, Riva MA, PopoliM. The interaction between the internal clock and antidepressant efficacy. Int Clin Psychopharmacol 2007; (Suppl. 2):9-14
- Turek F, Gillette M. Melatonin, sleep and circadian rhythms: rationale for the development of specific melatonin agonists. Slepp Med 2004; 5: 526-32.
- Srinivasan V, Pandi-Perumal SR, Trakht I et al. Pathophysiology of depression: role of sleep and the melatonergic system. Psychiatry Res 2009; 3: 201-14
- Амон М., Буае П.Т., Моке Е. Перспективы в изучении патогенеза и терапии аффективных расстройств: роль мелатонина и серотонина.Журн. неврол. и психиатр. им. С.СКорсакова. 2007; 11: 77-82.
- Hardeland R, Poeggeler B, Srinivasan Vet al. Melatonergic drugs in clinical practice. Arzneimittelforschung 2008; 58 (1): 1-10.
- Мосолов С.Н. Хронобиологический подход к терапии аффективных состояний. Психиатр. и психофармакотер. Экстравыпуск. 2009; 7-8.
- Eppel AB. Agomelatine adjunctive therapy for acute bipolar depression-preliminary open data. Bipolar Disord 2008; 6: 749-50.
- Lam RW. Addressing circadian rhythm disturbances in depressed patients.JРsychopharmаcol 2008; 7 (Suppl.): 8-13.
- Guilleminault C. Efficacy of the new antidepressant agomelatine versus venlafaxine on subjective sleep of patients with major depressive disorder. EurNeuropsychopharmacol 2005; 15 (Supp. 3)p. 419.
- Kennedy SH, Rizvi S, Fulton Ket al. A double-blind comparison of sexual functioning, antidepressant efficacy and tolerability between agomelatine and venlafaxine XR.J Clin Рsychopharmаcol 2008; 28:329-33.
- Loo H, Hale A D’haenen H. Determination of the dose agomelatine, a melatoninergic agonist and selective 5HT(2C) antagonist, in the treatment of major depressive disorder: a placebo-controlled dose range study. Int ClinPsychopharmcol 2002; 17:239-47
- Montgomery SA Kasper S. Severe depression and antidepressants: focus on a pooled analysis of placebo-controlled studies on agomelatine. Int Clin Psychopharmcol 2007; 22:283-91.
- Иванов СВ. Инновационный подход к терапии депрессии. Психиатр. и психофармакотер. Экстравыпуск. 2009; с. 9-10.
- Злоказова МВ. Опыт применения Вальдоксана при лечении умеренных и тяжелых депрессивных расстройств непсихотического уровня у амбулаторных больных. Психиатр. и психофармакотер.2009; 11 (4): 39-41
- Симонов АН., Абрамова ЛИ. Использование доверительных интервалов для оценки коэффициента редукции среднего суммарного балла шкалы PANNS. Журн. психиатр. 2011; 3.
- Смулевич АБ. Депрессия и циркадианные ритмы (результаты эпидемиологической программы Циркадиан-1). Психиатр. и психофармакотер. Экстравыпуск. 2009; с. 5-7.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Курс сомнологии при кафедре нервных болезней факультета послевузовского профессионального образования Московской медицинской академии им. И.М. Сеченова

Опыт применения агомелатина (вальдоксана) в неврологической практике
Как цитировать:
Левин Я.И. Опыт применения агомелатина (вальдоксана) в неврологической практике. Журнал неврологии и психиатрии им. С.С. Корсакова.
2011;111(11):25‑28.
Levin IaI. . S.S. Korsakov Journal of Neurology and Psychiatry. 2011;111(11):25‑28. (In Russ.)
Взаимосвязь депрессии и инсомнии с неврологическими заболеваниями сложна и недостаточно изучена [4, 5, 9]. Депрессия и инсомния очень часто (до 70%) встречаются в неврологической практике. Они модифицируют клиническую картину неврологической патологии, утяжеляя течение и прогноз, и способствуют хронификации заболеваний. В свою очередь хроническое течение многих неврологических заболеваний становится причиной появления депрессии и инсомнии. Поэтому депрессию и инсомнию нужно лечить специально, не надеясь на то, что они исчезнут параллельно с минимизацией неврологической симптоматики, хотя возможно и такое.
В этой ситуации важно выбирать препараты с двойным — антидепрессивным и нормализующим сон — эффектом, а также с минимальным побочным действием. К таковым относится новый антидепрессант агомелатин (вальдоксан). Он имеет совершенно особый нейрохимический механизм действия, являясь агонистом церебральных мелатониновых рецепторов 1-го и 2-го подтипов (максимально представленных в супрахиазмальном ядре) и антагонистом 5-НТ2С серотониновых рецепторов [4, 10]. Кроме агонизма к мелатониновым рецепторам, вальдоксан специфически повышает содержание норадреналина и дофамина во фронтальной коре. По силе антидепрессивного действия вальдоксан сопоставим с венлафаксином [10].
Уникальность вальдоксана объясняется выраженным антидепрессивным эффектом и нормализующим воздействием на циркадные ритмы. С точки зрения влияния вальдоксана на сон следует отметить следующие особенности [10-12]: отсутствие седативного эффекта при сравнении с бензодиазепинами; достаточно быстрый эффект нормализации сна с преимущественным воздействием на дельта-сон; нормализующее хронобиологическое воздействие — после лечения препаратом максимум дельта-сна возвращается в 1-й цикл сна и в 1-ю половину ночи. Уже на 14-й день приема вальдоксана снижается бодрствование внутри сна, увеличиваются индекс эффективности сна, длительность и представленность дельта-сна; препарат не влияет на фазу быстрого сна (ФБС), включая ее длительность и латентность.
С учетом рецепторного профиля вальдоксана и по результатам ряда исследований можно ожидать минимум негативных эффектов от его применения. Учитывая вышесказанное, использование вальдоксана в неврологической практике представляется перспективным.
Цель настоящей работы — обобщение собственного клинического опыта применения вальдоксана в комплексном лечении больных с ишемическим инсультом, мигренью, фибромиалгией, а также в рамках «лекарственных каникул» при отмене бензодиазепинов.
Материал и методы
Основным показанием к назначению вальдоксана больным было сочетание неврологических заболеваний с депрессией и инсомнией.
Всем пациентам, помимо традиционного клинического осмотра, проводилось психометрическое тестирование выраженности депрессии с помощью госпитальной шкалы тревоги и депрессии (ГШТД), оценивались результаты с показателями 11 баллов и более, что соответствовало клиническим проявлениям депрессии; выраженности нарушений сна с помощью анкеты субъективной балльной оценки сна (АСБОС) [13], оценивались результаты с показателями в 18 и менее баллов, что соответствовало наличию инсомнических расстройств.
Результаты
Ишемический инсульт. Нарушения цикла «сон-бодрствование» в острейшем периоде церебрального инсульта при объективном полисомнографическом исследовании встречаются в 100% случаев [1-3]. Эти нарушения включают инсомнию, расстройства дыхания во сне (синдром апноэ во сне — САС, синдром периодического дыхания, синдром постоянной гиповентиляции), инверсию цикла «сон-бодрствование». Инсульт, как правило, приводит к грубым расстройствам ночного сна, которые проявляются как изменениями его структуры, так и циркадных характеристик. Если в первом случае имеют место качественные изменения в виде серьезных нарушений механизмов генерации и поддержании сна, то во втором — либо сон становится полифазным, либо происходит его инверсия (смещение цикла «бодрствование-сон»). Нарушения сна наиболее выражены у пациентов с инсультами, развившимися во сне [1]. Не менее острой представляется проблема постинсультной депрессии, при этом депрессия нередко возникает с первых клинических проявлений инсульта. Коморбидность депрессии и инсульта подтверждена в исследованиях [8]. Развитие постинсультной депрессии ухудшает качество жизни больных и замедляет процесс восстановления неврологического дефицита. Патогенез постинсультной депрессии варьирует в зависимости от срока после начала заболевания: в 1-й месяц (по некоторым данным — в первые 6 мес) доминирующую роль играет локализация дефекта — большинство исследователей [8] ассоциируют депрессию с очагом в левом полушарии, особенно указывается роль левой лобной доли и базальных ядер (при этом тяжесть нарушения сочетается с близостью очага к переднему полюсу полушария), а также истощение нейротрансмиттерных систем (нарушение обмена дофамина, норадреналина, серотонина), позже — трудности с привыканием к ограниченной активности, к двигательному дефициту. При инсультах в вертебрально-базилярном бассейне депрессии менее частые и выражены слабее, так как согласно некоторым исследователям при этом менее затрагиваются серотонин и норадренергические системы.
Применение вальдоксана у больных с церебральным инсультом базируется также на опыте использования мелатонина [2, 3]. Было проведено изучение действия мелатонина на 15 больных в острейшем периоде ишемического инсульта; их показатели сравнивались с таковыми у 15 здоровых добровольцев (контроль), соответственно подобранных по полу и возрасту. У всех больных регистрировались расстройства сна различной степени выраженности. Исследования показали, что в результате ежевечернего орального приема 3 мг мелатонина в течение 10 дней у больных в острейшем периоде инсульта отмечалось улучшение субъективной оценки качества ночного сна и его объективных характеристик: уменьшение длительности засыпания, уменьшение представленности первой стадии сна, увеличение времени второй стадии. Индекс качества сна (интегративный показатель, чем он ниже, тем лучше структура сна) также снижался. Особенностью мелатонина являлось то, что при инверсии сна он восстанавливал нарушенный биоритм «сон-бодрствование». Отмечалось достоверное снижение уровня депрессии. Личностная и реактивная тревожность оставались без динамики. В неврологической картине динамики не наблюдалось, что, по-видимому, связано с недостаточностью этого срока для выявления положительных сдвигов.
Но не только улучшение цикла «сон-бодрствование» делает мелатонин и мелатониномиметики перспективными для применения у больных с инсультом. Целый ряд экспериментальных и клинических исследований выявляет важнейшие свойства мелатонина для лечения постинсультных пациентов. В исследованиях на животных мелатонин увеличивает церебральную реперфузию у крыс с экспериментальной артериальной окклюзией; уменьшает мозговой отек; повышает нейропластичность в условиях стресса, вызванного инсультом. Из клинических исследований известно, что при врожденной гипоплазии эпифиза повышается риск мозгового инсульта и инфаркта миокарда; изменение иммунного статуса при инсульте, возможно, связано с нарушенной ночной секрецией мелатонина; мелатонин повышает нейропластичность у пожилых. Таким образом, применение мелатониномиметиков в комплексной терапии инсульта имеет достаточное количество предпосылок.
Оценивалось влияние вальдоксана на 10 больных, 5 мужчин и 5 женщин (средний возраст — 67±5,7 года), с ишемическим инсультом, верифицированным на МРТ. У 5 больных препарат назначался с 1-го дня пребывания в стационаре и у 5 — через месяц после развития инсульта. У всех пациентов в неврологическом статусе выявлялся гемипарез разной степени выраженности без речевых нарушений; у 5 пациентов двигательные расстройства регрессировали через 2 нед, у 5 — оставались весь период наблюдения. У всех больных на момент назначения вальдоксана выявлялись нарушения сна по типу инсомнии (показатели по АСБОС у всех были менее 18 баллов, средний балл по группе — 14,0±3,8) и депрессия (показатель депрессии по ГШТД у всех был более 11 баллов, средний балл по группе — 15,0±2,6, средний показатель тревоги — 9,0±3,2). Всем пациентам вальдоксан назначался в дозе 25 мг в 20.00, длительность применения — не менее 28 дней.
Уже через 7-10 дней больные отмечали большее чувство уверенности, более ровное настроение. Пациенты быстрее засыпали, дольше спали и просыпались отдохнувшими. Через 28 дней применения вальдоксана показатели по АСБОС у всех были более 17 баллов, средний балл по группе — 20,0±2,6, показатель депрессии по ГШТД у всех был менее 12 баллов, средний балл по группе — 9,0±2,8, средний показатель тревоги — 8,5±2,4 балла. При этом и сами обследуемые, и их родственники отмечали несомненное улучшение эмоционального статуса больных и оценивали их сон как вполне хороший.
Фибромиалгия. Клиническая картина фибромиалгии складывается из мышечных болей, депрессии и инсомнии. В наших предыдущих исследованиях [2] проводилось изучение действия ежевечернего приема 1,5 мг мелатонина в течение 10 дней на уровень депрессии, субъективную оценку качества ночного сна и его объективные характеристики у 11 больных фибромиалгией. Полисомнография подтвердила нарушения ночного сна в виде затрудненного засыпания, удлинения латентного периода поверхностного сна и парадоксального сна, подавления глубокого сна, уменьшения количества завершенных циклов сна, увеличения периодов бодрствования и движений во сне и т.д. После завершения курса лечения отмечалось субъективное улучшение сна, подтвержденное полиграфической регистрацией: облегчение засыпания, укорочение периодов бодрствования внутри сна, увеличение его времени. Отмечалось также улучшение самочувствия и тонкой моторики рук в дневное время, снижение уровня депрессии.
Оценивалось влияние вальдоксана при лечении 9 больных, 2 мужчин и 7 женщин (средний возраст — 34±7,4 года) с фибромиалгией. У всех пациентов выявлялись не менее 9 болевых точек (по визуальной аналоговой шкале — ВАШ — уровень боли оценивался в 5,7±1,5 балла), нарушения сна по типу инсомнии с пре-, интра-, и постсомническими проявлениями (показатели по АСБОС у всех были менее 19 баллов, средний балл по группе — 13,5±4,2) и депрессия (показатель депрессии по ГШТД у всех был более 11 баллов, средний балл по группе — 14,6±3,4, средний показатель тревоги — 10±2,8). Вальдоксан назначался в дозе 25 мг в 20.00, длительность применения — не менее 28 дней.
Через 2 нед 6 пациентов отметили снижение выраженности болевых ощущений, повышение уровня настроения и более быстрое засыпание. Через 28 дней все вышеперечисленные тенденции нарастали, выраженность боли по ВАШ составила 3,4±0,9 балла. Показатели по АСБОС у всех были выше 18 баллов, средний балл по группе — 20,4±2,2. Уровень депрессии по ГШТД снизился у всех больных и стал менее 11 баллов (средний балл по группе — 8,6±2,4), средний показатель тревоги также снизился и составил 7,3±1,6 балла.
Мигрень. Депрессия и нарушения сна коморбидны мигрени. При этом антидепрессанты наряду с антиконвульсантами являются лидерами в профилактике мигренозных атак, однако в этом случае используется и собственный противоболевой потенциал антидепрессантов. Соотношению нарушений сна и мигрени уделяется меньше внимания, хотя эта проблема несомненно актуальна [7]. Говоря о ней, необходимо учитывать два аспекта: нарушения сна у больных с мигренью, а также мигрень сна (МС) и мигрень бодрствования (МБ).
Показано, что больные с МС характеризуются высоким уровнем депрессии и тревоги, выраженной вегетативной дисфункцией и стойкими нарушениями ночного сна, что определяет значительную дезадаптацию этих пациентов в межприступном периоде и низкое качество их жизни. Подчеркнута роль депрессии в трансформации МБ в МС и в формировании стойких нарушений сна в межприступном периоде у больных с МС. В основе взаимосвязи этих событий лежит предположение о единой роли серотонинергических механизмов, принимающих участие в реализации приступа мигрени, в формировании цикла «сон-бодрствование» и в происхождении депрессии [7].
Оценивалось влияние вальдоксана на 18 больных, все женщины (средний возраст — 32±5,6 года) с мигренью без ауры. Длительность заболевания составляла от 2 мес до 3 лет. У всех пациенток были типичные гемикрании длительностью от 1,5 до 8 ч, пульсирующего характера, с фото- и фонофобией, тошнотой и рвотой (в половине случаев). Частота приступов — не менее 2 в месяц. По шкале ВАШ уровень боли на пике приступа оценивался в 7,2±1,3 балла. В межприступный период у всех пациенток отмечались нарушения сна по типу инсомнии с длительным и нередко мучительным засыпанием (77%), поверхностный сон с частыми пробуждениями (67%), тяжелое утреннее пробуждение с ощущением «невосстановительного сна» (100%). Все пациентки отмечали сниженный фон настроения, быструю утомляемость, сужение круга интересов. Показатели по АСБОС у всех больных были менее 19 баллов, средний балл по группе — 14,8±2,8; показатель депрессии по ГШТД у всех был более 11 баллов, средний балл по группе — 16,3±3,8; средний показатель тревоги по ГШТД — 9,4±3,8. Вальдоксан назначался в дозе 25 мг в 20.00, длительность применения — не менее 28 дней. В период лечения все пациентки заполняли «дневник головной боли».
Через 10-14 дней у половины больных на фоне отсутствия мигренозных атак несколько повысился фон настроения и улучшилось засыпание. Через 28 дней количество мигренозных приступов снизилось на 30-50%. Субъективно улучшился сон, повысились настроение и работоспособность. Показатели по АСБОС у всех стали более 19 баллов, средний балл по группе — 21,9±1,4; показатель депрессии по ГШТД стал менее 13 баллов, средний балл по группе — 10,8±2,1; средний показатель тревоги по ГШТД — 8,3±1,4. Одна пациентка отказалась от приема вальдоксана на 3-й день, мотивируя отсутствием эффекта на возникшую мигренозную атаку. Анамнестически для этой больной были характерны быстрые отказы и от других препаратов. У 3 больных отмечалось нарастание сновиденческой активности, однако содержание сновидений не было неприятным и устрашающим.
«Лекарственные каникулы» при отмене бензодиазепиновых гипнотиков. Для отмены длительно применяемых (как правило, речь идет о сроках более 4 мес) бензодиазепинов следует использовать «лекарственные каникулы» (ЛК). В идеале ЛК должны помочь пациенту полностью отказаться от бензодиазепинов, но это возможно только в 40% случаев. Чаще всего результатом ЛК становится 2-кратное снижение дозы препарата. Сами по себе ЛК мучительны для пациента, в том числе и потому, что значительно нарастают инсомния и депрессия, которые в числе проблем, связанных с отменой препаратов, занимают одно из первых мест [6]. Поэтому для уменьшения этих проблем используются многочисленные приемы, в которые включен и прием вальдоксана [6].
Оценивалось влияние вальдоксана в рамках ЛК на 5 больных, 3 мужчин и 2 женщины (средний возраст — 38±7,6 года) с более чем 12-месячным приемом бензодиазепинов с целью улучшения сна. Бензодиазепины лишь в одном случае были назначены врачом, в 4 случаях это было самостоятельное решение больных. Все пациенты принимали феназепам в нарастающих дозах до 8 мг в сутки (как правило, однократно перед сном). К моменту начала ЛК показатели по АСБОС у всех были менее 18 баллов, средний балл по группе — 12,4±2,5; показатель депрессии по ГШТД у всех был более 13 баллов, средний балл по группе — 21,6±3,7; средний показатель тревоги по ГШТД — 12,2±1,8. Вальдоксан назначался в дозе 25 мг в 20.00 в рамках комплексной терапии (внутривенное капельное введение витаминов, ноотропов и метаболиков, фототерапия).
Через 7 дней после отмены бензодиазепинов субъективно уменьшилась выраженность нарушений сна, повысилась психическая и физическая активность. Тем не менее показатели по АСБОС у всех не превышали 19 баллов, средний балл по группе — 15,6±1,7; показатель депрессии по ГШТД стал менее 16 баллов, средний балл по группе — 13,4±2,8; средний показатель тревоги по ГШТД — 11,2±2,3 балла. Некоторое наступившее улучшение нельзя считать достаточным, что в значительной степени определяется кратковременностью приема препарата.
Таким образом, в случаях сочетания неврологических страданий с клинически выраженными нарушениями сна и депрессией вальдоксан зарекомендовал себя достаточно эффективным и в значительной степени безопасным препаратом. Иногда применение вальдоксана базировалось на предшествующем опыте использования в сходных ситуациях мелатонина. Подобие эффектов разных мелатониномиметиков свидетельствует в пользу необходимости расширения поиска механизма действия агомелатина: повышение нейропластичности, антиноцицептивный и др. Несомненно, что приведенные факты нуждаются в дальнейшей верификации и организации специальных исследований по применению вальдоксана в неврологической практике.
Мы используем файлы cооkies для улучшения работы сайта. Оставаясь на нашем сайте, вы соглашаетесь с условиями
использования файлов cооkies. Чтобы ознакомиться с нашими Положениями о конфиденциальности и об использовании
файлов cookie, нажмите здесь.
Вальдоксан® (Valdoxan®)
💊 Состав препарата Вальдоксан®
✅ Применение препарата Вальдоксан®
Препарат отпускается по рецепту
Входит в список «Жизненно необходимых и важнейших лекарственных
препаратов»
Температура хранения: от 2 до 30 °С
Описание активных компонентов препарата
Вальдоксан®
(Valdoxan®)
Приведенная научная информация является обобщающей и не может быть использована для принятия
решения о возможности применения конкретного лекарственного препарата.
Дата обновления: 2020.02.21
Владелец регистрационного удостоверения:
Код ATX:
N06AX22
(Агомелатин)
Лекарственная форма
|
Препарат отпускается по рецепту |
Вальдоксан® |
Таблетки, покрытые пленочной оболочкой, 25 мг: 28 или 98 шт. рег. №: ЛП-(000528)-(РГ-RU) |
Форма выпуска, упаковка и состав
препарата Вальдоксан®
Таблетки, покрытые пленочной оболочкой оранжево-желтого цвета, продолговатые, двояковыпуклые.
Вспомогательные вещества: лактозы моногидрат, магния стеарат, крахмал кукурузный, повидон (K30), кремния диоксид коллоидный безводный, карбоксиметилкрахмал натрия (тип А), стеариновая кислота.
Состав пленочной оболочки: глицерол, гипромеллоза, краситель железа оксид желтый (E172), макрогол 6000, магния стеарат, титана диоксид (E171).
14 шт. — блистеры (ПВХ/Ал) (2) — пачки картонные с контролем первого вскрытия (при необходимости).
Фармакологическое действие
Антидепрессант, агонист мелатониновых МТ1— и МТ2-рецепторов и антагонист серотониновых 5-НТ2с-рецепторов.
Агомелатин активен на валидированных моделях депрессии (тест приобретенной беспомощности, тест отчаяния, хронический стресс умеренной выраженности), равно как и на моделях с десинхронизацией циркадных ритмов, а также в экспериментальных ситуациях тревоги и стресса. Показано, что агомелатин не влияет на захват моноаминов и не имеет сродства к α-, β-адренорецепторам, гистаминовым рецепторам, холинорецепторам, допаминовым и бензодиазепиновым рецепторам.
Агомелатин усиливает высвобождение допамина и норадреналина, в особенности в области префронтальной коры мозга и не влияет на концентрацию внеклеточного серотонина. В экспериментальных исследованиях на животных со смоделированной десинхронизацией циркадных ритмов было показано, что агомелатин восстанавливает синхронизацию циркадных ритмов через стимуляцию мелатониновых рецепторов.
Агомелатин способствует восстановлению нормальной структуры сна, снижению температуры тела и выделению мелатонина.
Показана эффективность краткосрочного применения агомелатина (терапия 6-8 недель) в дозах 25-50 мг у пациентов с большими депрессивными эпизодами.
Также показана эффективность применения агомелатина у пациентов с более тяжелыми формами депрессивного расстройства (оценка по шкале Гамильтона ≥ 25). Агомелатин был также эффективен при изначально высоких уровнях тревоги, равно как и при сочетании тревожных и депрессивных расстройств.
Подтвержден поддерживающий антидепрессивный эффект агомелатина (при продолжительности исследования 6 мес) в дозе 25-50 мг 1 раз/сут. Результаты исследования подтвердили противорецидивную эффективность агомелатина, которая оценивалась по времени до наступления рецидива заболевания (р=0.0001).
Агомелатин не оказывает отрицательного воздействия на внимательность и память, у пациентов с депрессией агомелатин в дозе 25 мг увеличивает продолжительность фазы медленного сна без изменения количества и продолжительности фаз быстрого сна. Прием агомелатина в дозе 25 мг также способствует более быстрому наступлению сна и улучшению его качества (начиная с первой недели лечения) и снижению частоты сердечных сокращений; при этом заторможенности в дневное время не отмечается. На фоне приема агомелатина отмечена тенденция к снижению частоты сексуальной дисфункции (влияние на возбуждение и оргазм).
Прием агомелатина не оказывает влияния на массу тела, ЧСС и АД, не вызывает сексуальных нарушений, не вызывает синдрома отмены (даже при резком прекращении лечения) и синдрома привыкания.
Фармакокинетика
После приема внутрь агомелатин быстро и хорошо (≥ 80%) всасывается из ЖКТ. Cmax в плазме достигается через 1-2 ч после приема. Абсолютная биодоступность после приема терапевтической дозы низкая (< 5%); межиндивидуальная вариабельность значительная. Биодоступность у женщин выше, чем у мужчин. Биодоступность увеличивается на фоне приема пероральных контрацептивов и снижается на фоне курения.
При применении в терапевтических дозах Cmax агомелатина увеличивалась пропорционально дозе. При приеме в более высоких дозах отмечался более выраженный эффект «первого прохождения» через печень. Прием пищи (как обычной, так и с высоким содержанием жиров) не влиял ни на биодоступность, ни на степень всасывания. На фоне приема пищи с высоким содержанием жиров межиндивидуальная вариабельность показателей увеличивалась.
Vd в равновесном состоянии составлял порядка 35 л. Связывание с белками плазмы — 95% независимо от концентрации агомелатина, возраста или наличия почечной недостаточности.
При печеночной недостаточности отмечалось двукратное увеличение свободной фракции препарата.
После приема внутрь агомелатин подвергается быстрому окислению, в основном за счет CYP1A2 и CYP2C9. Изофермент CYP2C19 также участвует в метаболизме агомелатина, однако его роль менее значима. Основные метаболиты в виде гидроксилированного и деметилированного агомелатина неактивны, быстро связываются и выводятся почками.
T1/2 из плазмы составляет от 1 до 2 ч. Выведение происходит быстро. Метаболический клиренс составляет порядка 1100 мл/мин. Выведение происходит в основном почками (80%) в виде метаболитов. Количество неизмененного препарата в моче незначительно. При неоднократном назначении препарата кинетика не меняется.
У пациентов с почечной недостаточностью тяжелой степени при однократном приеме агомелатина в дозе 25 мг фармакокинетические параметры существенно не изменялись.
При применении агомелатина в дозе 25 мг у пациентов со слабо выраженной (класс А по классификации Чайлд-Пью) и умеренной (класс В по классификации Чайлд-Пью) хронической печеночной недостаточностью на фоне цирроза печени было отмечено увеличение его концентрации в плазме в 70 и 140 раз, соответственно, по сравнению с добровольцами, сопоставимыми по полу, возрасту и отношению к курению, но без печеночной недостаточности.
Показания активных веществ препарата
Вальдоксан®
Лечение большого депрессивного расстройства у взрослых.
Режим дозирования
Способ применения и режим дозирования конкретного препарата зависят от его формы выпуска и других факторов. Оптимальный режим дозирования определяет врач. Следует строго соблюдать соответствие используемой лекарственной формы конкретного препарата показаниям к применению и режиму дозирования.
Для приема внутрь.
Рекомендуемая доза — 25 мг 1 раз/сут вечером. При отсутствии клинической динамики после двухнедельного лечения доза может быть увеличена до 50 мг 1 раз/сут вечером.
Следует контролировать функцию печени в начале терапии, через 6 недель (окончание купирующего периода терапии), 12 недель и 24 недели (окончание поддерживающего периода терапии) после начала терапии, а также в соответствии с клинической ситуацией.
Лекарственную терапию депрессий следует проводить, по крайней мере, еще в течение 6 мес после полного прекращения симптомов.
Побочное действие
Со стороны ЦНС: часто (≥1/100, <1/10) — тревожность, головная боль, головокружение, сонливость, бессонница, мигрень; нечасто (≥1/1000, <1/100) — парестезии; неуточненная частота — суицидальные мысли и поведение.
Со стороны пищеварительной системы: часто (≥1/100, <1/10) — тошнота, диарея, запор, боль в эпигастрии, повышение активности АЛТ и/или ACT более чем в 3 раза по сравнению с ВГН (1.1% на фоне агомелатина в дозе 25/50 мг и 0.7% на фоне плацебо); редко (≥1/10 000, <1/1000) — гепатит.
Дерматологические реакции: часто (≥1/100, <1/10) — потливость; нечасто — экзема; редко — эритематозная сыпь.
Со стороны органа зрения: нечасто (≥1/1000, <1/100) — нечеткое зрение.
Со стороны костно-мышечной системы: часто (≥1/100, <1/10) — боль в области спины.
Прочие: часто (≥1/100, <1/10) — утомляемость.
Противопоказания к применению
Печеночная недостаточность, цирроз, заболевание печени в активной фазе; одновременное применение сильных ингибиторов цитохрома CYP1A2 (таких как флувоксамин, ципрофлоксацин); возраст до 18 лет; повышенная чувствительность к агомелатину.
Применение при беременности и кормлении грудью
Данные о применении агомелатина при беременности отсутствуют. При необходимости применения при беременности требуется осторожность и тщательная оценка ожидаемой пользы терапии для матери и возможного риска для плода.
Неизвестно, выделяется ли агомелатин с грудным молоком у человека. При необходимости применения агомелатина в период лактации грудное вскармливание следует прекратить.
В экспериментальных исследованиях на животных не выявлено прямого или опосредованного вредного воздействия на течение беременности, развитие эмбриона и плода, родовую деятельность и постнатальное развитие. Было показано, что агомелатин и его метаболиты выделяются с грудным молоком.
Применение при нарушениях функции печени
Препарат противопоказан для применения при нарушении функции печени
Применение у детей
Препарат противопоказан для применения у детей и подростков в возрасте до 18 лет
Особые указания
С осторожностью применять при больших депрессивных эпизодах у пациентов с почечной недостаточностью средней и тяжелой степени; при одновременном назначении агомелатина с умеренными ингибиторами изофермента CYP1A2 (такими как пропранолол, грепафлоксацин, эноксацин); у пациентов с маниакальными или гипоманиакальными эпизодами в анамнезе; у пациентов, в анамнезе которых имелись события, связанные с суицидом, а также у пациентов, имевших суицидальные намерения до начала терапии; у пациентов пожилого возраста (65 лет и старше), особенно при лечении больших депрессивных эпизодов с деменцией; пациентам, злоупотребляющим алкоголем или принимающим препараты, способные вызвать нарушение функции печени.
Эффективность применения у пациентов пожилого возраста не установлена.
У пациентов с почечной недостаточностью тяжелой степени существенного изменения фармакокинетических параметров не отмечалось. Однако опыт применения при больших депрессивных эпизодах у пациентов с умеренной или выраженной почечной недостаточностью ограничен.
При появлении симптомов мании следует прекратить прием агомелатина.
При депрессивном состоянии повышен риск суицидальных мыслей, самоповреждений и суицида (событий, связанных с суицидом). Риск сохраняется до наступления отчетливой ремиссии. Пациенты должны находиться под медицинским наблюдением вплоть до улучшения состояния (после начала терапии может пройти несколько недель, прежде чем состояние улучшится). Клинический опыт свидетельствует, что риск суицида может увеличиваться на ранних этапах наступления ремиссии. Пациенты, в анамнезе которых имелись события, связанные с суицидом, а также пациенты, имевшие суицидальные намерения до начала терапии, относятся к группе риска и во время проведения терапии должны находиться под строгим медицинским наблюдением.
В период лечения пациенты, особенно относящиеся к группе риска, должны находиться под строгим медицинским наблюдением, особенно в начале терапии и при изменении дозы препарата. Пациенты (и лица, осуществляющие уход за ними) должны быть информированы о необходимости немедленного обращения к врачу при ухудшении состояния, суицидальном и необычном поведении, а также при появлении суицидальных мыслей.
Результаты мета-анализа клинических исследований антидепрессантов у пациентов с психическими расстройствами свидетельствуют о повышенном риске суицидального поведения у пациентов в возрасте до 25 лет на фоне приема антидепрессантов по сравнению с плацебо.
Следует соблюдать осторожность при одновременном применении агомелатина с умеренными ингибиторами изофермента CYP1A2 (такими как пропранолол, грепафлоксацин, эноксацин) из-за возможности повышения концентрации агомелатина.
Рекомендуется контролировать функцию печени в начале терапии, через 6 недель (окончание купирующего периода терапии), 12 недель и 24 недели (окончание поддерживающего периода терапии) после начала терапии, а также в другое время в соответствии с клинической ситуацией. При повышении активности трансаминаз в сыворотке крови следует провести повторное определение в течение 48 ч. Если активность трансаминаз более чем в 3 раза превышает ВГН, прием агомелатина следует прекратить. В дальнейшем следует регулярно контролировать функциональное состояние печени до нормализации активности трансаминаз.
При развитии симптомов нарушения функции печени следует провести функциональные печеночные тесты. С учетом лабораторных данных и клинической картины следует принять решение о прекращении или продолжении терапии агомелатином. При развитии желтухи необходимо прекратить терапию.
Лекарственное взаимодействие
Агомелатин метаболизируется в печени при участии преимущественно изоферментов CYP1A2 (90%) и при участии CYP2C9/19 (10%). Поэтому любые препараты, метаболизм которых зависит от этих изоферментов, могут повышать или уменьшать биодоступность агомелатина.
Флувоксамин, является сильным ингибитором изофермента CYP1A2 и умеренным ингибитором изофермента CYP2C9 и существенно замедляет метаболизм агомелатина, при этом концентрация агомелатина увеличивается примерно в 60 (12-412) раз. Поэтому одновременное применение агомелатина и сильных ингибиторов изофермента CYP1A2 (таких как флувоксамин, ципрофлоксацин) противопоказано.
Одновременное применение агомелатина и эстрогенов, которые являются умеренными ингибиторами изофермента CYP1A2, приводит к увеличению концентрации агомелатина в несколько раз. Хотя комбинированное применение агомелатина и эстрогенов не сопровождалось ухудшением профиля безопасности проводимой терапии, следует соблюдать осторожность при одновременном применении агомелатина с другими умеренными ингибиторами изофермента CYP1A2 (такими как пропранолол, грепафлоксацин, эноксацин) до накопления достаточного клинического опыта.
Не рекомендуется применение агомелатина совместно с этанолом.
Адрес производителя
|
СЕРВЬЕ РУС , ООО |
Россия |
108828, г. Москва, поселение Краснопахорское, квартал 158, владение 2, стр. 1 |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Если вы не нашли нужной информации среди ответов на этот вопрос, или же ваша проблема немного отличается от представленной, попробуйте задать дополнительный вопрос врачу на этой же странице, если он будет по теме основного вопроса. Вы также можете задать новый вопрос, и через некоторое время наши врачи на него ответят. Это бесплатно. Также можете поискать нужную информацию в похожих вопросах на этой странице или через страницу поиска по сайту. Мы будем очень благодарны, если Вы порекомендуете нас своим друзьям в социальных сетях.
Медпортал 03online.com осуществляет медконсультации в режиме переписки с врачами на сайте. Здесь Вы получаете ответы от реальных практикующих специалистов в своей области. В настоящий момент на сайте можно получить консультацию по 74 направлениям: специалиста COVID-19, аллерголога, анестезиолога-реаниматолога, венеролога, гастроэнтеролога, гематолога, генетика, гепатолога, гериатра, гинеколога, гинеколога-эндокринолога, гомеопата, дерматолога, детского гастроэнтеролога, детского гинеколога, детского дерматолога, детского инфекциониста, детского кардиолога, детского лора, детского невролога, детского нефролога, детского онколога, детского офтальмолога, детского психолога, детского пульмонолога, детского ревматолога, детского уролога, детского хирурга, детского эндокринолога, дефектолога, диетолога, иммунолога, инфекциониста, кардиолога, клинического психолога, косметолога, липидолога, логопеда, лора, маммолога, медицинского юриста, нарколога, невропатолога, нейрохирурга, неонатолога, нефролога, нутрициолога, онколога, онкоуролога, ортопеда-травматолога, офтальмолога, паразитолога, педиатра, пластического хирурга, подолога, проктолога, психиатра, психолога, пульмонолога, ревматолога, рентгенолога, репродуктолога, сексолога-андролога, стоматолога, трихолога, уролога, фармацевта, физиотерапевта, фитотерапевта, флеболога, фтизиатра, хирурга, эндокринолога.
Мы отвечаем на 85.86% вопросов.
Оставайтесь с нами и будьте здоровы!
