
ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ. ВОЗМОЖНЫ ПОБОЧНЫЕ ЭФФЕКТЫ. НЕОБХОДИМА КОНСУЛЬТАЦИЯ СПЕЦИАЛИСТА.
Автор статьи
Долгих Наталия Вадимовна
,
Профессия: провизор
Название вуза: Пермская государственная фармацевтическая академия (ПГФА)
Специальность: фармация
Стаж работы: 5 лет 6 месяцев
Диплом о фармацевтическом образовании: 105924 3510859 рег. номер 31944
Места работы: провизор в аптеке, работа в офисе по снабжению аптек, провизор сервиса Мегаптека
Все авторы
Содержание
- РЛС
- Состав
- Действующее вещество
- Протопик: гормональный или нет?
- Протопик: мазь от чего помогает?
- Побочные действия
- Протопик или Такропик: что лучше?
- Элидел или Протопик: что лучше?
- Краткое содержание
Атопический дерматит — хроническое воспалительное заболевание кожи, которым, по данным ВОЗ, страдает до 20% детей и до 5% взрослых. В основе болезни лежит нарушение проницаемости рогового слоя кожи, а к самому выраженному симптому относится нестерпимый зуд, который значительно ухудшает качество жизни пациентов. Зуд бывает настолько сильным, что приводит к «кровавым» расчесываниям, коростам и вторичному инфицированию кожи. Еще одна опасность атопического дерматита в том, что он становится причиной развития таких заболеваний, как аллергический ринит и бронхиальная астма.
Лечение заболевания складывается из нескольких направлений — это увлажнение сухой кожи, снятие воспаления и уменьшение зуда. Рассказываем о противовоспалительном препарате Протопик для терапии атопического дерматита: составе, действующем веществе, показаниях и побочных действиях. Сравниваем с двумя аналогами: Такропик и Элидел.
РЛС
Согласно Регистру лекарственных средств Протопик — это мазь для наружного применения, которую производит фармацевтическая компания ЛЕО Фарма из Дании. Других лекарственных форм, например, Протопик крем, не существует.
Протопик относится к фармако-терапевтической группе «Противовоспалительные средства для местного применения» и включен в Перечень ЖНВЛП (жизненно необходимых и важнейших лекарственных препаратов). Из аптек отпускается по рецепту врача.
Состав
В состав мази Протопик входит одно действующее вещество — такролимус. Препарат выпускается в двух дозировках:
- 0,03% — для детей с 2 лет и взрослых;
- 0,1% — только для взрослых пациентов.
В качестве вспомогательных веществ мазь содержит парафин мягкий, парафин жидкий, парафин твердый, воск пчелиный, пропиленкарбонат.
Действующее вещество
Такролимус обладает иммуномодулирующим действием. Препарат ингибирует активацию иммунных клеток Т-лимфоцитов и блокирует синтез цитокинов — белковых молекул, играющих важную роль в иммунной системе.
Протопик: гормональный или нет?
Протопик не является гормональным средством, так как в его составе нет гормонов. Наоборот, мазь представляет собой альтернативу местным глюкокортикостероидным средствам, потому что у нее отсутствуют побочные эффекты, свойственные гормональным мазям и кремам:
- атрофия кожи, розацеа, периоральный дерматит, акне;
- повышенное оволосение, медленное заживление ран, кожные инфекции;
- сенсибилизация к кортикостероидам;
- системные реакции при длительном применении или на обширных участках кожи: повышение уровня сахара, глаукома, надпочечниковая недостаточность.
Протопик: мазь от чего помогает?
Показанием для применения мази является лечение атопического дерматита в средней и тяжелой форме в тех случаях, когда у пациента противопоказаны другие местные средства или имеется к ним резистентность. Можно использовать Протопик на лице, в частности, при периоральном дерматите. Других применений мази, например, при псориазе или от прыщей, в официальной инструкции не указано.
Мазь с концентрацией 0,03% используют для лечения детей с 2 лет, а также в терапии взрослых пациентов — по мере улучшения состояния. Препарат с содержанием 0,1% разрешен пациентам старше 16 лет.
Побочные действия
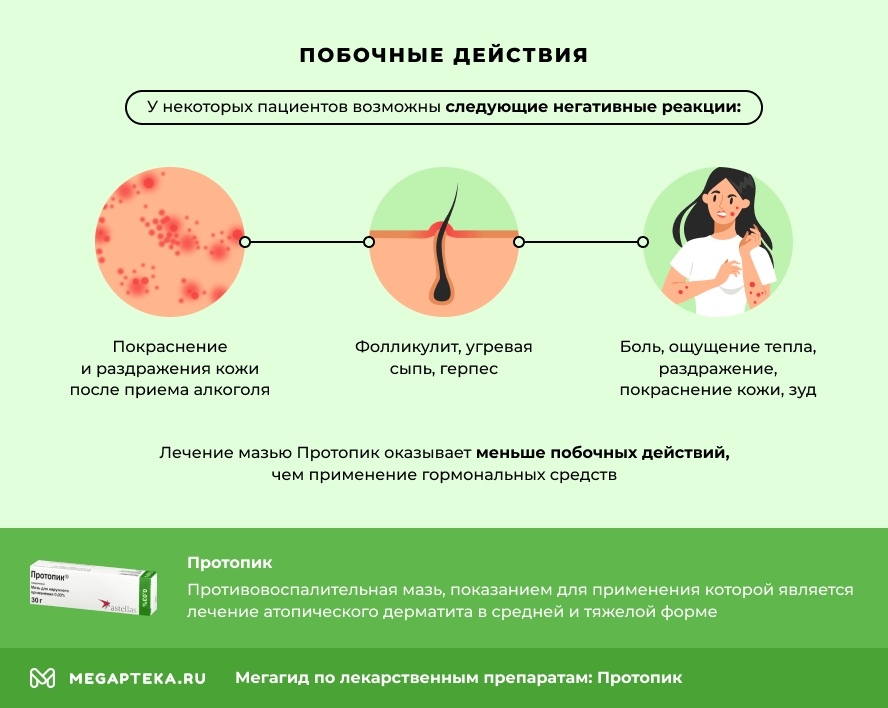
Несмотря на то, что лечение мазью оказывает меньше побочных действий, чем применение гормональных средств, у некоторых пациентов возможны следующие негативные реакции:
- боль, ощущение тепла, раздражение, покраснение кожи, зуд, сыпь, чувство жжения;
- покраснение и раздражения кожи после приема алкоголя;
- фолликулит, угревая сыпь, герпес.
Обычно побочные реакции проявляются в умеренной степени и не требуют отмены мази. В большинстве случаев они проходят через неделю после начала терапии.
Протопик или Такропик: что лучше?
Такропик содержит то же действующее вещество, что и мазь Протопик. Это отечественный аналог датского препарата: у них идентичные форма выпуска, дозировки, показания, противопоказания. Препараты отличаются только ценой.
Элидел или Протопик: что лучше?
Препарат Элидел также предназначен для лечения атопического дерматита. Он содержит активное вещество пимекролимус, который обладает таким же механизмом действия, что и такролимус. Его выпускает немецкая компания Меда Фарма в виде 1% крема.
Несмотря на большую концентрацию действующего вещества, Элидел действует мягче и показан для лечения болезни легкой и средней степени тяжести. Крем можно применять даже грудным детям с 3-месячного возраста. Элидел в меньшей степени проходит через кожный барьер, чем Протопик и не оказывает системных побочных эффектов. Согласно клиническим рекомендациям Элидел является препаратом выбора при лечении атопического дерматита на коже лица, шеи, в местах сгибов.
Оба препарата отпускаются по рецепту врача. Для выбора оптимального средства конкретному пациенту требуется консультация специалиста.
Краткое содержание
- Протопик относится к фармако-терапевтической группе «Противовоспалительные средства для местного применения» и включен в Перечень ЖНВЛП.
- В состав мази входит одно действующее вещество — такролимус. Препарат выпускается в двух дозировках.
- Препарат ингибирует активацию иммунных клеток Т-лимфоцитов и блокирует синтез цитокинов — белковых молекул, играющих важную роль в иммунной системе.
- Не является гормональным средством, так как в его составе нет гормонов.
- Показанием для применения мази является лечение атопического дерматита в средней и тяжелой форме.
- Несмотря на то, что лечение мазью оказывает меньше побочных действий, чем применение гормональных средств, у некоторых пациентов возможны негативные реакции, которые проходят через неделю с начала лечения.
- Такропик содержит то же действующее вещество, что и мазь: у них идентичные форма выпуска, дозировки, показания, противопоказания. Препараты отличаются только ценой.
- Элидел действует мягче и показан для лечения болезни легкой и средней степени тяжести. Крем можно применять даже грудным детям с 3-месячного возраста. Согласно клиническим рекомендациям Элидел является препаратом выбора при лечении атопического дерматита на коже лица, шеи, в местах сгибов.
Задайте вопрос эксперту по теме статьи
Остались вопросы? Задайте их в комментариях ниже – наши эксперты ответят вам. Там же вы можете поделиться своим опытом с другими читателями Мегасоветов.
от 514 ₽
Состав
| Мазь для наружного применения | 100 г |
| активное вещество: | |
| такролимус (в виде такролимуса моногидрата) | 0,03 г |
| 0,1 г | |
| вспомогательные вещества: парафин мягкий белый; парафин жидкий; пропиленкарбонат; воск пчелиный белый; парафин твердый |
в тубах пластиковых по 10, 30 или 60 г; в пачке картонной 1 туба.
Описание
Мазь однородной консистенции от белого до слегка желтоватого цвета.
Фармакодинамика
Такролимус относится к группе ингибиторов кальциневрина. Он связывается со специфическим цитоплазматическим белком иммунофилином (FKBP12), который является цитозольным рецептором для кальциневрина (FK506). В результате этого формируется комплекс, включающий такролимус, FKBP12, кальций, кальмодулин и кальциневрин, что приводит к ингибированию фосфатазной активности кальциневрина. Это делает невозможным дефосфорилирование и транслокацию ядерного фактора активированных Т-клеток (NFAT), необходимого для инициации транскрипции генов, кодирующих продукцию ключевых для Т-клеточного иммунного ответа цитокинов (ИЛ-2 и интерферон-гамма). Кроме того, такролимус ингибирует транскрипцию генов, кодирующих продукцию таких цитокинов, как ИЛ-3, ИЛ-4, ИЛ-5, гранулоцитарно-макрофагальный колониестимулирующий фактор (ГМКСФ) и ФНО-α, которые принимают участие в начальных этапах активации Т-лимфоцитов. Помимо этого, под влиянием такролимуса происходит ингибирование высвобождения медиаторов воспаления из тучных клеток, базофилов и эозинофилов, а также снижение экспрессии FcεRI (высокоаффинный поверхностный рецептор для иммуноглобулина Е) на клетках Лангерганса, что ведет к снижению их активности и презентирования антигена Т-лимфоцитам.
Мазь такролимуса не влияет на синтез коллагена и т.о. не вызывает атрофию кожи.
Фармакокинетика
Абсорбция. Всасывание такролимуса в системный кровоток при местном применении является минимальным. У большинства пациентов с атопическим дерматитом (у взрослых и детей) как при однократном нанесении, так и при многократном применении 0,03 и 0,1% мази такролимуса концентрация его в плазме крови составляла <1 нг/мл. Системная абсорбция зависит от площади поражения и уменьшается по мере исчезновения клинических проявлений атопического дерматита. Кумуляции препарата при длительном применении (до 1 года) у детей и взрослых не отмечалось.
Распределение в организме. В связи с тем что системная абсорбция мази такролимуса низкая, высокая способность связываться с белками плазмы (>98,8%) рассматривается как клинически незначимая.
Метаболизм. Такролимус не метаболизируется в коже. При попадании в системный кровоток такролимус в значительной степени метаболизируется в печени посредством CYP3A4.
Выведение. При многократном местном применении мази такролимуса T1/2 — 75 ч у взрослых и 65 ч у детей.
Протопик: Показания
Мазь Протопик® применяется в дозировке 0,03 и 0,1% у взрослых и только 0,03% у детей от 2 до 16 лет для лечения атопического дерматита (средней степени тяжести и тяжелых форм) в случае его резистентности к иным средствам наружной терапии или наличия противопоказаний к таковым.
Способ применения и дозы
Наружно. Взрослым и детям старше 2 лет мазь Протопик® наносят тонким слоем на пораженные участки кожи. Препарат можно применять на любых участках тела, включая лицо и шею, в области кожных складок. Не следует наносить препарат на слизистые оболочки и под окклюзионные повязки.
Применение у детей (2 года и старше) и подростков до 16 лет
Лечение необходимо начинать с нанесения 0,03% мази Протопик® 2 раза в сутки. Продолжительность лечения по данной схеме не должна превышать 3 нед. В дальнейшем частота применения уменьшается до 1 раза в сутки, лечение продолжается до полного очищения очагов поражения.
Применение у взрослых и подростков 16 лет и старше
Лечение необходимо начинать с применения 0,1% мази Протопик® 2 раза в сутки и продолжать до полного очищения очагов поражения. По мере улучшения, можно уменьшать частоту нанесения 0,1% мази или переходить на использование 0,03% мази Протопик®. В случае повторного возникновения симптомов заболевания следует возобновить лечение 0,1% мазью Протопик® дважды в день. Если позволяет клиническая картина, следует предпринять попытку снизить частоту применения препарата либо использовать меньшую дозировку — 0,03% мазь Протопик®.
Применение у людей пожилого возраста (65 лет и старше)
Особенности применения у людей пожилого возраста отсутствуют.
Обычно улучшение наблюдается в течение 1 нед с момента начала терапии. Если признаки улучшения на фоне терапии отсутствуют в течение 2 нед, следует рассмотреть вопрос о смене терапевтической тактики.
Лечение обострений
Мазь Протопик® может использоваться кратковременно или длительно в виде периодически повторяющихся курсов терапии. Лечение пораженных участков кожи проводится до полного исчезновения клинических проявлений атопического дерматита. Как правило, улучшение наблюдается в течение первой недели лечения. Если признаки улучшения не наблюдаются в течение 2 нед с момента начала использования мази, необходимо рассмотреть другие варианты дальнейшего лечения. Лечение следует возобновить при появлении первых признаков обострения атопического дерматита.
Профилактика обострений
Для предупреждения обострений и увеличения длительности ремиссии у пациентов с частыми (более 4 раз в год) обострениями заболевания в анамнезе рекомендуется поддерживающая терапия мазью Протопик®. Целесообразность назначения поддерживающей терапии определяется эффективностью предшествующего лечения по стандартной схеме (2 раза в день) на протяжении не более 6 нед.
При поддерживающей терапии мазь Протопик® следует наносить 2 раза в неделю (например в понедельник и четверг) на участки кожи, обычно поражаемые при обострениях.
Промежуток времени между нанесением препарата должен составлять не менее 2–3 дней. У взрослых и подростков 16 лет и старше используется 0,1% мазь Протопик®, у детей (2 года и старше) — 0,03% мазь Протопик®. При появлении признаков обострения следует перейти к обычному режиму терапии мазью Протопик® (см. раздел «Лечение обострений»).
Через 12 нед поддерживающей терапии необходимо оценить клиническую динамику и решить вопрос о целесообразности продолжения профилактического использования мази Протопик®. У детей для оценки клинической динамики следует временно отменить препарат и затем рассмотреть вопрос о необходимости продолжения поддерживающей терапии.
Протопик: Противопоказания
гиперчувствительность к такролимусу, вспомогательным веществам, макролидам;
беременность;
грудное вскармливание;
пациенты с генетическими дефектами эпидермального барьера, такими как синдром Нетертона, а также при генерализованной эритродермии в связи с риском прогрессирующего увеличения системной абсорбции такролимуса;
дети и подростки младше 16 лет (в дозировке 0,1%), дети младше 2 лет (в дозировке 0,03%).
Протопик: Побочные действия
Наиболее частыми нежелательными реакциями являются симптомы раздражения кожи (ощущение жжения и зуда, покраснение, боль, парестезии и сыпь) в месте нанесения. Как правило, они выражены умеренно и проходят в течение первой недели после начала лечения.
Часто встречается непереносимость алкоголя (покраснение лица или симптомы раздражения кожи после употребления спиртных напитков).
У пациентов, применяющих мазь Протопик®, отмечается повышенный риск развития фолликулита, акне и герпетической инфекции.
По частоте встречаемости нежелательные реакции делятся на очень частые — >1/10; частые — >1/100, <1/10 и редкие — >1/1000, <1/100. В рамках каждой группы нежелательные реакции представлены в порядке убывания значимости.
Общие расстройства и местные реакции: очень частые — жжение и зуд в месте применения; частые — ощущение тепла, покраснение, боль, раздражение, сыпь в области применения.
Инфекции: частые — герпетическая инфекция (простой герпес лица и губ, варицеллиформная сыпь Капоши).
Кожа и подкожная клетчатка: частые — фолликулит, зуд; нечастые — акне.
Нервная система: частые — парестезии, гиперестезия.
Метаболизм и особенности питания: частые — непереносимость алкоголя (гиперемия лица или симптомы раздражения кожи после употребления спиртных напитков).
За весь период наблюдения препарата были зарегистрированы единичные случаи розацеа, малигнизации (кожные и другие виды лимфом, рак кожи).
Передозировка
При местном применении случаев передозировки не отмечалось.
Лечение: при случайном попадании внутрь необходимо предпринять общепринятые меры, которые включают контроль жизненно важных функций организма и наблюдение за общим состоянием.
Стимуляция рвоты или промывание желудка не рекомендуются.
Взаимодействие
Такролимус не метаболизируется в коже, что исключает риск лекарственных взаимодействий в коже, которые могут повлиять на его метаболизм. Так как системная абсорбция такролимуса при использовании в форме мази минимальна, взаимодействие с ингибиторами CYP3A4 (эритромицин, итраконазол, кетоконазол, дилтиазем и др.) при одновременном применении с мазью Протопик® маловероятно, однако не может быть полностью исключено у пациентов с обширными участками поражения и/или эритродермией.
Влияние мази Протопик® на эффективность вакцинации не изучалось. Однако из-за потенциального риска снижения эффективности вакцинацию необходимо провести до начала применения мази или спустя 14 дней после последнего использования мази Протопик®. В случае применения живой аттенуированной вакцины этот период должен быть увеличен до 28 дней, в противном случае следует рассмотреть возможность использования альтернативных вакцин.
Возможность совместного применения мази Протопик® с другими наружными препаратами, системными ГКС и иммунодепрессантами не изучалась.
Особые указания
Мазь Протопик® нельзя использовать у больных с врожденными или приобретенными иммунодефицитами или у пациентов, которые принимают иммуносупрессивные препараты.
Во время применения мази Протопик® необходимо избегать попадания на кожу солнечных лучей, посещения солярия, терапии УФ-лучами Б или А в комбинации с псораленом (PUVA-терапия).
Мазь Протопик® не должна применяться для лечения участков поражения, которые рассматриваются как потенциально злокачественные или предзлокачественные.
В течение 2 ч на участках кожи, на которые наносилась мазь Протопик®, нельзя использовать смягчающие средства.
Эффективность и безопасность применения мази Протопик® в лечении инфицированного атопического дерматита не оценивалась. При наличии признаков инфицирования до назначения мази Протопик® необходимо проведение соответствующей терапии. Применение мази Протопик® может быть связано с повышенным риском развития герпетической инфекции. При наличии признаков герпетической инфекции следует индивидуально оценить соотношение пользы и риска применения Протопика®.
При наличии лимфоаденопатии необходимо обследовать пациента до начала терапии и наблюдать за ним в период применения мази. При отсутствии очевидной причины лимфаденопатии или при наличии симптомов острого инфекционного мононуклеоза необходимо прекратить применение мази Протопик®.
Необходимо избегать попадания мази в глаза и на слизистые оболочки (в случаях случайного попадания мазь необходимо тщательно удалить и/или промыть водой). Не рекомендуется наносить мазь Протопик® под окклюзионные повязки и носить во время лечения плотную воздухонепроницаемую одежду.
Также, как при использовании любого другого местного ЛС, пациенты должны мыть руки после нанесения мази, кроме тех случаев, когда мазь наносится на область рук с лечебной целью.
Меры предосторожности
Протопик® в значительной степени метаболизируется в печени, и хотя его концентрация в крови при наружном применении очень низкая, у больных с декомпенсированной печеночной недостаточностью мазь используют с осторожностью. Необходимо соблюдать осторожность при использовании мази Протопик® у больных с обширным поражением кожи, особенно длительными курсами, и у детей.
Условия отпуска
Характеристики
Торговое название
Протопик
Действующее вещество (МНН)
Такролимус
Дозировка или размер
0.03%
Форма выпуска
мазь для наружного применения
Первичная упаковка
туба пластиковая
Условия хранения
При температуре не выше 25 °C
Представлено описание активных веществ лекарственного препарата. Описание препарата основано на официально утвержденной инструкции по применению от компании-производителя. Приведенное описание носит исключительно информационный характер и не может быть использовано для принятия решения о возможности применения конкретного лекарственного препарата.
Описание препарата Протопик® (мазь для наружного применения, 0.03%) основано на официальной инструкции, утверждено компанией-производителем в 2019 году
Дата согласования: 14.08.2019
Содержание
- Фотографии упаковок
- Действующее вещество
- ATX
- Фармакологическая группа
- Нозологическая классификация (МКБ-10)
- Состав
- Описание лекарственной формы
- Фармакологическое действие
- Фармакодинамика
- Фармакокинетика
- Показания
- Противопоказания
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Производитель
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Аналоги (синонимы) препарата Протопик®
- Заказ в аптеках Москвы
Фотографии упаковок
14.08.2019
Действующее вещество
ATX
Фармакологическая группа
Состав
| Мазь для наружного применения | 100 г |
| активное вещество: | |
| такролимус (в виде такролимуса моногидрата) | 0,03/0,1 г |
| вспомогательные вещества: парафин мягкий белый; парафин жидкий; пропиленкарбонат; воск пчелиный белый; парафин твердый |
Описание лекарственной формы
Мазь однородной консистенции от белого до слегка желтоватого цвета.
Фармакологическое действие
Фармакодинамика
Такролимус относится к группе ингибиторов кальциневрина. Он связывается со специфическим цитоплазматическим белком иммунофилином (FKBP12), который является цитозольным рецептором для кальциневрина (FK506). В результате этого формируется комплекс, включающий такролимус, FKBP12, кальций, кальмодулин и кальциневрин, что приводит к ингибированию фосфатазной активности кальциневрина. Это делает невозможным дефосфорилирование и транслокацию ядерного фактора активированных Т-клеток (NFAT), необходимого для инициации транскрипции генов, кодирующих продукцию ключевых для Т-клеточного иммунного ответа цитокинов (ИЛ-2 и интерферон-гамма). Кроме того, такролимус ингибирует транскрипцию генов, кодирующих продукцию таких цитокинов, как ИЛ-3, ИЛ-4, ИЛ-5, гранулоцитарно-макрофагальный колониестимулирующий фактор (ГМКСФ) и ФНО-α, которые принимают участие в начальных этапах активации Т-лимфоцитов. Помимо этого, под влиянием такролимуса происходит ингибирование высвобождения медиаторов воспаления из тучных клеток, базофилов и эозинофилов, а также снижение экспрессии FcεRI (высокоаффинный поверхностный рецептор для IgЕ) на клетках Лангерганса, что ведет к снижению их активности и презентирования антигена Т-лимфоцитам.
Мазь такролимуса не влияет на синтез коллагена и т.о. не вызывает атрофию кожи.
Фармакокинетика
Абсорбция. Всасывание такролимуса в системный кровоток при местном применении является минимальным. У большинства пациентов с атопическим дерматитом (у взрослых и детей) как при однократном нанесении, так и при многократном применении 0,03 и 0,1% мази такролимуса концентрация его в плазме крови составляла <1 нг/мл. Системная абсорбция зависит от площади поражения и уменьшается по мере исчезновения клинических проявлений атопического дерматита. Кумуляции препарата при длительном применении (до 1 года) у детей и взрослых не отмечалось.
Распределение в организме. В связи с тем что системная абсорбция мази такролимуса низкая, высокая способность связываться с белками плазмы (>98,8%) рассматривается как клинически незначимая.
Метаболизм. Такролимус не метаболизируется в коже. При попадании в системный кровоток такролимус в значительной степени метаболизируется в печени посредством CYP3A4.
Выведение. При многократном местном применении мази такролимуса T1/2 — 75 ч у взрослых и 65 ч у детей.
Показания
Мазь Протопик® применяется в дозировке 0,03 и 0,1% у взрослых и только 0,03% у детей от 2 до 16 лет для лечения атопического дерматита (средней степени тяжести и тяжелых форм) в случае его резистентности к иным средствам наружной терапии или наличия противопоказаний к таковым.
Противопоказания
- гиперчувствительность к такролимусу, вспомогательным веществам, макролидам;
- пациенты с генетическими дефектами эпидермального барьера, такими как синдром Нетертона, а также при генерализованной эритродермии в связи с риском прогрессирующего увеличения системной абсорбции такролимуса;
- беременность;
- грудное вскармливание;
- дети и подростки младше 16 лет (в дозировке 0,1%), дети младше 2 лет (в дозировке 0,03%).
С осторожностью: больные с декомпенсированной печеночной недостаточностью (несмотря на то что Протопик® в значительной степени метаболизируется в печени, и его концентрация в крови при наружном применении очень низкая); больные с обширным поражением кожи, особенно при применении длительными курсами; детский возраст.
Способ применения и дозы
Наружно. Взрослым и детям старше 2 лет мазь Протопик® наносят тонким слоем на пораженные участки кожи. Препарат можно применять на любых участках тела, включая лицо и шею, в области кожных складок. Не следует наносить препарат на слизистые оболочки и под окклюзионные повязки.
Применение у детей (2 года и старше) и подростков до 16 лет
Лечение необходимо начинать с нанесения 0,03% мази Протопик® 2 раза в сутки. Продолжительность лечения по данной схеме не должна превышать 3 нед. В дальнейшем частота применения уменьшается до 1 раза в сутки, лечение продолжается до полного очищения очагов поражения.
Применение у взрослых и подростков 16 лет и старше
Лечение необходимо начинать с применения 0,1% мази Протопик® 2 раза в сутки и продолжать до полного очищения очагов поражения. По мере улучшения можно уменьшать частоту нанесения 0,1% мази или переходить на использование 0,03% мази Протопик®. В случае повторного возникновения симптомов заболевания следует возобновить лечение 0,1% мазью Протопик® дважды в день. Если позволяет клиническая картина, следует предпринять попытку снизить частоту применения препарата либо использовать меньшую дозировку — 0,03% мазь Протопик®.
Применение у людей пожилого возраста (65 лет и старше)
Особенности применения у людей пожилого возраста отсутствуют.
Обычно улучшение наблюдается в течение 1 нед с момента начала терапии. Если признаки улучшения на фоне терапии отсутствуют в течение 2 нед, следует рассмотреть вопрос о смене терапевтической тактики.
Лечение обострений
Мазь Протопик® может использоваться кратковременно или длительно в виде периодически повторяющихся курсов терапии. Лечение пораженных участков кожи проводится до полного исчезновения клинических проявлений атопического дерматита. Как правило, улучшение наблюдается в течение первой недели лечения. Если признаки улучшения не наблюдаются в течение 2 нед с момента начала использования мази, необходимо рассмотреть другие варианты дальнейшего лечения. Лечение следует возобновить при появлении первых признаков обострения атопического дерматита.
Профилактика обострений
Для предупреждения обострений и увеличения длительности ремиссии у пациентов с частыми (более 4 раз в год) обострениями заболевания в анамнезе рекомендуется поддерживающая терапия мазью Протопик®. Целесообразность назначения поддерживающей терапии определяется эффективностью предшествующего лечения по стандартной схеме (2 раза в день) на протяжении не более 6 нед.
При поддерживающей терапии мазь Протопик® следует наносить 2 раза в неделю (например, в понедельник и четверг) на участки кожи, обычно поражаемые при обострениях. Промежуток времени между нанесением препарата должен составлять не менее 2–3 дней. У взрослых и подростков 16 лет и старше используется 0,1% мазь Протопик®, у детей (2 года и старше) — 0,03% мазь Протопик®. При появлении признаков обострения следует перейти к обычному режиму терапии мазью Протопик® (см. Лечение обострений). Через 12 нед поддерживающей терапии необходимо оценить клиническую динамику и решить вопрос о целесообразности продолжения профилактического использования мази Протопик®. У детей для оценки клинической динамики следует временно отменить препарат и затем рассмотреть вопрос о необходимости продолжения поддерживающей терапии.
Побочные действия
Реклама: ООО «РЛС-Патент», ИНН 5044031277
Наиболее частыми нежелательными реакциями являются симптомы раздражения кожи (ощущение жжения и зуда, покраснение, боль, парестезии и сыпь) в месте нанесения. Как правило, они выражены умеренно и проходят в течение первой недели после начала лечения.
Часто встречается непереносимость алкоголя (покраснение лица или симптомы раздражения кожи после употребления спиртных напитков).
У пациентов, применяющих мазь Протопик®, отмечается повышенный риск развития фолликулита, акне и герпетической инфекции.
По частоте встречаемости нежелательные реакции делятся следующим образом: очень часто — >1/10; часто — >1/100, <1/10 и редко — >1/1000, <1/100. В рамках каждой группы нежелательные реакции представлены в порядке убывания значимости.
Общие расстройства и местные реакции: очень часто — жжение и зуд в месте применения; часто — ощущение тепла, покраснение, боль, раздражение, сыпь в области применения.
Инфекции: часто — герпетическая инфекция (простой герпес лица и губ, варицеллиформная сыпь Капоши).
Кожа и подкожная клетчатка: часто — фолликулит, зуд; нечасто — акне.
Нервная система: часто — парестезии, гиперестезия.
Метаболизм и особенности питания: часто — непереносимость алкоголя (гиперемия лица или симптомы раздражения кожи после употребления спиртных напитков).
За весь период наблюдения препарата были зарегистрированы единичные случаи розацеа, малигнизации (кожные и другие виды лимфом, рак кожи).
Взаимодействие
Такролимус не метаболизируется в коже, что исключает риск лекарственных взаимодействий в коже, которые могут повлиять на его метаболизм. Так как системная абсорбция такролимуса при использовании в форме мази минимальна, взаимодействие с ингибиторами CYP3A4 (в т.ч. эритромицин, итраконазол, кетоконазол, дилтиазем) при одновременном применении с мазью Протопик® маловероятно, однако не может быть полностью исключено у пациентов с обширными участками поражения и/или эритродермией.
Влияние мази Протопик® на эффективность вакцинации не изучалось. Однако из-за потенциального риска снижения эффективности вакцинацию необходимо провести до начала применения мази или спустя 14 дней после последнего использования мази Протопик®. В случае применения живой аттенуированной вакцины этот период должен быть увеличен до 28 дней, в противном случае следует рассмотреть возможность использования альтернативных вакцин.
Возможность совместного применения мази Протопик® с другими наружными препаратами, системными ГКС и иммунодепрессантами не изучалась.
Передозировка
При местном применении случаев передозировки не отмечалось.
Лечение: при случайном попадании внутрь необходимо предпринять общепринятые меры, которые включают контроль жизненно важных функций организма и наблюдение за общим состоянием.
Индукция рвоты или промывание желудка не рекомендуются.
Особые указания
Мазь Протопик® нельзя использовать у больных с врожденными или приобретенными иммунодефицитами или у пациентов, которые принимают иммуносупрессивные препараты.
Во время применения мази Протопик® необходимо избегать попадания на кожу солнечных лучей, посещения солярия, терапии УФ-лучами Б или А в комбинации с псораленом (PUVA-терапия).
Мазь Протопик® не должна применяться для лечения участков поражения, которые рассматриваются как потенциально злокачественные или предзлокачественные.
В течение 2 ч на участках кожи, на которые наносилась мазь Протопик®, нельзя использовать смягчающие средства.
Эффективность и безопасность применения мази Протопик® в лечении инфицированного атопического дерматита не оценивалась. При наличии признаков инфицирования до назначения мази Протопик® необходимо проведение соответствующей терапии. Применение мази Протопик® может быть связано с повышенным риском развития герпетической инфекции. При наличии признаков герпетической инфекции следует индивидуально оценить соотношение пользы и риска применения мази Протопик®.
При наличии лимфоаденопатии необходимо обследовать пациента до начала терапии и наблюдать за ним в период применения мази. При отсутствии очевидной причины лимфаденопатии или при наличии симптомов острого инфекционного мононуклеоза необходимо прекратить применение мази Протопик®.
Необходимо избегать попадания мази в глаза и на слизистые оболочки (при случайном попадании мазь необходимо тщательно удалить и/или промыть водой). Не рекомендуется наносить мазь Протопик® под окклюзионные повязки и носить во время лечения плотную воздухонепроницаемую одежду.
Также как при использовании любого другого местного ЛС, пациенты должны мыть руки после нанесения мази, кроме тех случаев, когда мазь наносится на область рук с лечебной целью.
Форма выпуска
Мазь для наружного применения, 0,03 и 0,1%. По 10, 30 или 60 г мази для наружного применения в пластиковых тубах. По 1 тубе помещают в картонную пачку.
Производитель
Астеллас Тояма Ко. Лтд., Япония.
Упаковка и выпускающий контроль Астеллас Ирланд Ко. Лтд., Ирландия, округ Керри, Киллорглин.
Владелец Регистрационного удостоверения. Астеллас Фарма Юроп Б.В., Нидерланды, Елизабетхоф 19, 2353 EW, Лайдердорп.
Претензии по качеству направлять в представительство компании в Москве. 109147, Москва, Марксистская ул., 16, «Мосаларко Плаза-1» бизнес-центр, 3-й эт.
Тел.: (495) 737-07-55; (495) 737-07-56; факс: (495) 737-07-57.
Условия отпуска из аптек
По рецепту.
Условия хранения
При температуре не выше 25 °C.
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не применять по истечении срока годности, указанного на упаковке.
Описание проверено
-
Крылов Юрий Федорович
(фармаколог, доктор медицинских наук, профессор, академик Международной академии информатизации)
Опыт работы: более 34 лет
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.
Протопик® (Protopic®) инструкция по применению
📜 Инструкция по применению Протопик®
💊 Состав препарата Протопик®
✅ Применение препарата Протопик®
📅 Условия хранения Протопик®
⏳ Срок годности Протопик®
Препарат отпускается по рецепту
Входит в список «Жизненно необходимых и важнейших лекарственных
препаратов»
Температура хранения: от 2 до 25 °С
Описание лекарственного препарата
Протопик®
(Protopic®)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для электронного издания справочника Видаль 2024
года, дата обновления: 2023.07.17
Код ATX:
D11AH01
(Такролимус)
Лекарственные формы
|
Препарат отпускается по рецепту |
Протопик® |
Мазь для наружного применения 0.1%: тубы 10 г, 30 г или 60 г 1 шт. рег. №: ЛСР-001885/10 |
|
Мазь для наружного применения 0.03%: тубы 10 г, 30 г или 60 г 1 шт. рег. №: ЛСР-001885/10 |
Форма выпуска, упаковка и состав
препарата Протопик®
Мазь для наружного применения 0.03% однородная, от белого до светло-желтого цвета.
Вспомогательные вещества: парафин белый мягкий — 774.7 мг, парафин жидкий — 110 мг, пропиленкарбонат — 50 мг, воск пчелиный белый — 35 мг, парафин твердый — 30 мг.
10 г — тубы пластиковые (1) — пачки картонные.
30 г — тубы пластиковые (1) — пачки картонные.
60 г — тубы пластиковые (1) — пачки картонные.
Мазь для наружного применения 0.1% однородная, от белого до светло-желтого цвета.
Вспомогательные вещества: парафин белый мягкий — 774 мг, парафин жидкий — 110 мг, пропиленкарбонат — 50 мг, воск пчелиный белый — 35 мг, парафин твердый — 30 мг.
10 г — тубы пластиковые (1) — пачки картонные.
30 г — тубы пластиковые (1) — пачки картонные.
60 г — тубы пластиковые (1) — пачки картонные.
Фармакологическое действие
Фармакодинамика
Такролимус относится к группе ингибиторов кальциневрина. Он связывается со специфическим цитоплазматическим белком иммунофилином (FKBP 12), который является цитозольным рецептором для кальциневрина (FK 506). В результате этого формируется комплекс, включающий такролимус, FKBP 12, кальций, кальмодулин и кальциневрин, что приводит к ингибированию фосфатазной активности кальциневрина. Это делает невозможным дефосфорилирование и транслокацию ядерного фактора активированных Т-клеток (NFAT), необходимого для инициации транскрипции генов, кодирующих продукцию ключевых для Т-клеточного иммунного ответа цитокинов (ИЛ-2 и интерферон-гамма).
Кроме того, такролимус ингибирует транскрипцию генов, кодирующих продукцию таких цитокинов, как ИЛ-3, ИЛ-4, ИЛ-5, гранулоцитарно-макрофагальный колониестимулирующий фактор (ГМ-КСФ) и фактор некроза опухоли (ФНОα), которые принимают участие в начальных этапах активации Т-лимфоцитов.
Помимо этого, под влиянием такролимуса происходит ингибирование высвобождения медиаторов воспаления из тучных клеток, базофилов и эозинофилов, а также снижение экспрессии FcεRI (высокоаффинный поверхностный рецептор для IgE) на клетках Лангерганса, что ведет к снижению их активности и презентирования антигена Т-лимфоцитам.
Мазь такролимуса не влияет на синтез коллагена и, таким образом, не вызывает атрофию кожи.
Фармакокинетика
Всасывание
Всасывание такролимуса в системный кровоток при местном применении не является значимым. У большинства пациентов с атопическим дерматитом (у взрослых и детей) как при однократном нанесении, так и при многократном применении 0.03% и 0.1% мази такролимуса концентрация его в плазме крови составляла <1.0 нг/мл. Системная абсорбция зависит от площади поражения и уменьшается по мере исчезновения клинических проявлений атопического дерматита. Кумуляции препарата при длительном применении (до 1 года) у детей и взрослых не отмечалось.
Распределение
В связи с тем, что системная абсорбция мази такролимуса низкая, высокая способность связываться с белками плазмы (>98.8%) рассматривается как клинически не значимая.
Метаболизм
Такролимус не метаболизируется в коже. При попадании в системный кровоток такролимус в значительной степени метаболизируется в печени посредством CYP3A4.
Выведение
При многократном наружном применении мази такролимуса T1/2 составляет 75 ч у взрослых и 65 ч у детей.
Показания препарата
Протопик®
Мазь Протопик® применяется в дозировке 0.03% и 0.1% у взрослых и только 0.03% у детей от 2 до 16 лет для лечения атопического дерматита (средней степени тяжести и тяжелых форм) в случае его резистентности к иным средствам наружной терапии или наличия противопоказаний к таковым.
Режим дозирования
Взрослым и детям старше 2 лет мазь Протопик® наносят тонким слоем на пораженные участки кожи. Препарат можно применять на любых участках тела, включая лицо и шею, в области кожных складок. Не следует наносить препарат на слизистые оболочки и под окклюзионные повязки.
Применение у детей (2 года и старше) и подростков до 16 лет
Лечение необходимо начинать с нанесения 0.03% мази Протопик® 2 раза/сут. Продолжительность лечения по данной схеме не должна превышать 3 недель. В дальнейшем частота применения уменьшается до 1 раза/сут, лечение продолжается до полного очищения очагов поражения.
Применение у взрослых и подростков 16 лет и старше
Лечение необходимо начинать с применения 0.1% мази Протопик® 2 раза/сут и продолжать до полного очищения очагов поражения. По мере улучшения можно уменьшать частоту нанесения 0.1% мази или переходить на использование 0.03% мази Протопик®. В случае повторного возникновения симптомов заболевания следует возобновить лечение 0.1% мазью Протопик® 2 раза/сут. Если позволяет клиническая картина, следует предпринять попытку снизить частоту применения препарата, либо использовать использовать меньшую дозировку — 0.03% мазь Протопик®.
Применение у людей пожилого возраста (65 лет и старше)
Особенности применения у людей пожилого возраста отсутствуют. Обычно улучшение наблюдается в течение одной недели с момента начала терапии. Если признаки улучшения на фоне терапии отсутствуют в течение 2 недель, следует рассмотреть вопрос о смене терапевтической тактики.
Лечение обострений
Мазь Протопик® может использоваться кратковременно или длительно в виде периодически повторяющихся курсов терапии. Лечение пораженных участков кожи проводится до полного исчезновения клинических проявлений атопического дерматита.
Как правило, улучшение наблюдается в течение первой недели лечения. Если признаки улучшения не наблюдаются в течение 2 недель с момента начала использования мази, необходимо рассмотреть другие варианты дальнейшего лечения. Лечение следует возобновить при появлении первых признаков обострения атопического дерматита.
Профилактика обострений
Для предупреждения обострений и увеличения длительности ремиссии у пациентов с частыми (более 4 раз в год) обострениями заболевания в анамнезе рекомендуется поддерживающая терапия мазью Протопик®. Целесообразность назначения поддерживающей терапии определяется эффективностью предшествующего лечения по стандартной схеме (2 раза/сут) на протяжении не более 6 недель.
При поддерживающей терапии мазь Протопик® следует наносить 2 раза в неделю (например, в понедельник и четверг) на участки кожи, обычно поражаемые при обострениях.
Промежуток времени между нанесением препарата должен составлять не менее 2-3 дней.
У взрослых и подростков 16 лет и старше используется 0.1% мазь Протопик®, у детей (2 года и старше) — 0.03% мазь Протопик®. При появлении признаков обострения следует перейти к обычному режиму терапии мазью Протопик® (см. «Лечение обострений»).
Через 12 месяцев поддерживающей терапии необходимо оценить клиническую динамику и решить вопрос о целесообразности продолжения профилактического использования мази Протопик®. У детей для оценки клинической динамики следует временно отменить препарат и затем рассмотреть вопрос о необходимости продолжения поддерживающей терапии.
Побочное действие
В клинических исследованиях примерно у 50% пациентов возникали побочные реакции в виде раздражения кожи в месте нанесения. Ощущение жжения и зуд были очень распространены, обычно от легкой до умеренной степени тяжести, и имели тенденцию к разрешению в течение одной недели после начала лечения. Характерным проявлением раздражения кожи была эритема. Также часто наблюдались ощущение тепла, боли, парестезии и сыпь в месте нанесения. Часто встречалась непереносимость алкоголя (покраснение лица или раздражение кожи после употребления алкоголя).
У пациентов может быть повышен риск фолликулита, акне и герпетической инфекции.
Побочные реакции с предполагаемой связью с лечением перечислены ниже по классам систем органов. Частота определяется как очень часто (≥1/10), часто (от ≥1/100 до <1/10) и нечасто (от ≥1/1000 до <1/100). В каждой категории побочные эффекты представлены в порядке убывания серьезности.
Вышеупомянутые побочные реакции наблюдались во время клинических исследований и/или при пострегистрационном использовании.
* О побочных реакциях сообщалось во время исследования после выхода препарата на рынок.
Исследования после выхода препарата на рынок
Сообщалось о спонтанных случаях кожных Т-клеточных лимфом, других типов лимфом и рака кожи у пациентов, применявших мазь такролимуса. Однако общий опыт клинических испытаний, данные крупных пострегистрационных исследований безопасности и наблюдения после выхода препарата на рынок не позволили установить причинно-следственную связь между применением мази такролимуса и злокачественными новообразованиями.
Противопоказания к применению
- гиперчувствительность к такролимусу, к вспомогательным веществам, к макролидам;
- беременность;
- период грудного вскармливания;
- применение у пациентов с серьезными нарушениями эпидермального барьера, в частности, синдромом Нетертона, ламеллярным ихтиозом, кожными проявлениями реакции «трансплантат против хозяина», а также при генерализованной эритродермии в связи с риском увеличения системной абсорбции такролимуса;
- детский и подростковый возраст младше 16 лет (для мази в дозировке 0.1%);
- детский возраст младше 2 лет (для мази в дозировке 0.03%).
С осторожностью
Протопик® в значительной степени метаболизируется в печени, и, хотя его концентрация в крови при наружном применении очень низкая, у больных с декомпенсированной печеночной недостаточностью мазь используют с осторожностью.
Необходимо соблюдать осторожность при использовании мази Протопик® у больных с обширным поражением кожи, длительными курсами, особенно у детей.
Применение при беременности и кормлении грудью
В случае предполагаемой, планируемой или установленной беременности необходимо проконсультироваться с врачом.
Воздействия на новорожденных/младенцев, находящихся на грудном вскармливании, не ожидается, поскольку системный эффект местного применения мази Протопик® незначителен. Следует соблюдать осторожность при использовании мази Протопик® в период грудного вскармливания и не наносить на грудь во время грудного вскармливания.
Применение при нарушениях функции печени
Протопик® в значительной степени метаболизируется в печени и, хотя его концентрация в крови при наружном применении очень низкая, у пациентов с декомпенсированной печеночной недостаточностью мазь следует использовать с осторожностью.
Применение у детей
У детей от 2 года до 16 лет возможно применение только 0.03% мазь Протопик®.
Необходимо соблюдать осторожность при использовании мази у детей.
Применение у пожилых пациентов
Особенности применения у пациентов пожилого возраста (65 лет и старше) отсутствуют.
Особые указания
Мазь Протопик® нельзя использовать у больных с врожденным или приобретенным иммунодефицитом или у пациентов, которые принимают иммуносупрессивные препараты.
Во время применения мази Протопик® необходимо минимизировать попадание на кожу солнечных лучей, посещение солярия, терапии УФ-лучами Б или А в комбинации с псораленом (PUVA-терапия).
Мазь Протопик® не должна применяться для лечения участков поражения, которые рассматриваются, как потенциально злокачественные или предзлокачественные.
В течение 2 ч на участках кожи, на которые наносилась мазь Протопик®, нельзя использовать смягчающие средства.
После местного применения мази Протопик® у пациентов с атопическим дерматитом системное воздействие незначительно или отсутствует. Эффективность и безопасность применения мази Протопик® в лечении инфицированного атопического дерматита не оценивалась. При наличии признаков инфицирования до назначения мази Протопик® необходимо проведение соответствующей терапии. Применение мази Протопик® может быть связано с повышенным риском развития герпетической инфекции. При наличии признаков герпетической инфекции следует индивидуально оценить соотношение пользы и риска применения мази Протопик®.
При наличии лимфаденопатии необходимо обследовать пациента до начала терапии и наблюдать за ним в период применения мази. При отсутствии очевидной причины лимфаденопатии или при наличии симптомов острого инфекционного мононуклеоза необходимо прекратить применение мази Протопик®.
Необходимо избегать попадания мази в глаза и на слизистые оболочки (в случаях случайного попадания мазь необходимо тщательно удалить и/или промыть водой).
Не рекомендуется наносить мазь Протопик® под окклюзионные повязки и носить плотную воздухонепроницаемую одежду.
Также как при использовании любого другого местного лекарственного средства, пациенты должны мыть руки после нанесения мази, кроме тех случаев, когда мазь наносится на область рук с лечебной целью.
Применение у детей
В рамках клинического исследования, проведенного на детях в возрасте от 2 до 11 лет с целью изучения влияния на их находящуюся на стадии развития иммунную систему, было продемонстрировано, что лечение мазью такролимуса 0.03% на фоне вакцинации конъюгированной вакциной против Neisseria menigitidis серотипа С не оказывало влияния на первичный ответ на вакцинацию, индукцию Т-клеточного иммунного ответа и формирование иммунной памяти.
Влияние на способность управлять транспортными средствами, механизмами
Исследования по влиянию мази на способность управлять автомобилем и на быстроту реакции при работе со сложной техникой, требующей повышенного внимания, не проводились. Мазь Протопик® применяется наружно и нет оснований полагать, что она может оказывать влияние на способность управлять автомобилем и работать с механизмами.
Передозировка
При местном применении случаев передозировки не отмечалось.
При попадании внутрь необходимо предпринять общепринятые меры, которые включают контроль жизненно важных функций организма и наблюдение за общим состоянием.
Стимуляция рвоты или промывание желудка не рекомендуются.
Лекарственное взаимодействие
Такролимус не метаболизируется в коже, что исключает риск лекарственного взаимодействия в коже, которое может повлиять на его метаболизм.
Так как системная абсорбция такролимуса при использовании в форме мази минимальна, взаимодействие с ингибиторами CYP3A4 (в т.ч. эритромицин, итраконазол, кетоконазол, дилтиазем) при одновременном применении с мазью Протопик® маловероятно, однако не может быть полностью исключено у пациентов с обширными участками поражения и/или эритродермией.
Влияние мази Протопик® на эффективность вакцинации не изучалось. Однако, из-за потенциального риска снижения эффективности, вакцинацию необходимо провести до начала применения мази или спустя 14 дней после последнего использования мази Протопик®. В случае применения живой аттенуированной вакцины этот период должен быть увеличен до 28 дней, в противном случае следует рассмотреть возможность использования альтернативных вакцин.
Применение у детей
Было проведено исследование по изучению взаимодействия с конъюгированной вакциной против Neisseria menigitidis серотипа С, в котором приняли участие дети в возрасте от 2 до 11 лет. Результаты этого исследования свидетельствуют, что одновременное применение такролимуса не оказывало влияния на первичный ответ на вакцинацию, формирование иммунной памяти, а также гуморальный и клеточный иммунный ответ.
Возможность совместного применения мази Протопик® с другими наружными препаратами, системными глюкокортикостероидами и иммунодепрессантами не изучалась.
Условия хранения препарата Протопик®
Хранить при температуре не выше 25°С. Хранить в недоступном для детей месте.
Срок годности препарата Протопик®
Срок годности — 3 года. Не применять препарат после окончания срока годности, указанного на упаковке.
Условия реализации
Отпускают по рецепту.
ЛЕО ФАРМАСЬЮТИКАЛ ПРОДАКТС ООО
(Россия)
|
125315 Москва, Ленинградский пр-т, д. 72, корп. 2 |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
В XXI в. произошли существенные изменения в изучении атопического дерматита (АД): новейшие методы молекулярной генетики и биологии, междисциплинарный подход, активная научно-исследовательская работа способствовали прогрессу медицины в области патофизиологии и терапии этого заболевания.
Наиболее важные достижения, а также соответствующие рекомендации по лечению и профилактике АД были сформулированы экспертами США и Европейского Союза (ЕС) в согласительном документе «Диагностика и лечение атопического дерматита у детей и взрослых» в 2006 г. [1]. В нем определение заболевания звучит коротко: «АД — хроническое воспалительное заболевание кожи, сопровождающееся зудом». Международная группа ученых рекомендует врачам при планировании лечения больных с АД использовать ступенчатый подход (рис.).
Как видно из представленной схемы, на всех стадиях течения АД больным показано основное лечение, которое включает соответствующий уход за кожей (очищение и гидратацию кожи с помощью увлажняющих/смягчающих средств и исключение/снижение влияния провоцирующих факторов), на фоне которого в дальнейшем назначают противовоспалительные препараты.
Уход за кожей основан на применении особых лечебных средств, достаточно широко представленных на современных фармацевтических рынках России. Местная противовоспалительная терапия включает всего лишь две группы лекарств — топические глюкокортикостероиды (ТГКС) и топические ингибиторы кальциневрина (ТИК). При осложнениях АД бактериальной/грибковой/вирусной инфекциями лечение следует продолжить наружными комбинированными или системными препаратами.
Системную терапию (антибиотики, пероральные кортикостероиды, циклоспорин А, азатиоприн, антигистаминные препараты) назначают больным с тяжелой формой АД, имеющим упорно рецидивирующее течение и/или другие сопутствующие заболевания. Взрослым и детям в возрасте старше 12 лет, страдающим тяжелым течением АД, возможно использование фототерапии. В последнее время рассматривается также целесообразность применения аллерген-специфической иммунотерапии в лечении АД.
Наружная (топическая) терапия является патогенетически обоснованной и абсолютно необходимой для каждого пациента с АД. Такая принципиальная важность топической терапии при АД объясняется несколькими факторами. Во-первых, АД — это хронический воспалительный процесс, который протекает в дерме, поэтому главное место в лечении заболевания должна занимать наружная терапия. Во-вторых, при АД крайне важно достичь восстановления и поддержания целостности кожного барьера, нарушение которой является кардинальным признаком АД, влекущей за собой усиление трансэпидермальной потери воды, а также повышение чувствительности кожи к различным ирритантам и аллергенам [3, 4]. Другим важным подходом является воздействие на сухость (ксероз) кожи при АД. Иными словами, наружная терапия — это именно тот вид лечения, который может изменить течение и исход АД.
Рассмотрим некоторые особенности наружной терапии АД, основанной на поэтапном подходе (рис.). Совершенно очевидно, что прежде следует оценить тяжесть течения заболевания.
Оценка степени тяжести АД
АД, как правило, начинается в раннем детском возрасте. Согласно последней классификации, различают не-атопическую и атопическую формы АД (в англоязычной литературе АД обозначают термином «экзема») (2001). По данным зарубежных исследователей, у 30–50% детей с типичной клинической картиной АД не удается подтвердить наличие атопических механизмов; у 15–45% детей описана преходящая (транзиторная) форма АД с низкими сывороточными уровнями IgE, не сопровождающаяся явной сенсибилизацией [2]. Позднее некоторые случаи так называемой eczema infantum спонтанно разрешаются без развития типичного АД. У другой части детей, напротив, заболевание характеризуется формированием сенсибилизации. Недавно Novembre E. с соавторами, исследовав 111 детей в возрасте 2–11 лет, установили, что по данным кожных прик-тестов лишь через 9 лет более чем у половины из них отрицательные кожные пробы стали положительными [3].
К сожалению, не существует потенциальных и объективных маркеров, которые отражали бы степень тяжести и прогрессирования заболевания и которые могли бы быть использованы для оценки эффективности терапии.
В клинической практике для оценки степени тяжести течения АД чаще всего врачи используют такие критерии, как выраженность эритемы, инфильтрации, папулы (индексы IGA — Investigator’s Global Assessment, EASI — Eczema Area Severity Index), еще раньше с этой целью был предложен индекс SCORAD (Scoring Atopic Dermatitis), рекомендованный Европейской академией аллергологии и клинической иммунологии в 1992 г. (данная система учитывает распространенность кожного процесса, интенсивность клинических проявлений и субъективные симптомы).
Вместе с тем, диагноз АД — прежде всего клинический. Основные подходы к наружной терапии при обеих формах АД одинаковы и ставят своей целью увлажнение/смягчение кожи и облегчение зуда. Лечение сухости кожи у больных АД проводят постоянно, тогда как выбор противовоспалительных средств зависит от степени тяжести течения заболевания.
Увлажняющие/смягчающие средства
Тот факт, что сухость (ксероз) и дефекты барьерной функции кожи влияют на течение АД, вполне очевиден. В результате многих исследований установлено, что существует взаимосвязь между зудом, сухостью и воспалением кожи, однако, что первично в этих процессах, точно не ясно. В последнее время дефекты барьерной функции кожи рассматривают как один из важных фенотипических признаков АД, который приводит не только к ксерозу, но и к снижению уровня антимикробных пептидов в коже и повышению трансэпидермальной потери воды. Но одни ученые рассматривают нарушение эпидермального барьера кожи как первичное звено в развитии АД, что способствует облегчению проникновения аллергенов и ирритантов в кожу, впоследствии инициирующих воспалительный ответ и гиперреактивность кожи. Другие, напротив, полагают, что нарушение барьерной функции кожи является вторичным процессом вследствие воспаления, которое развивается в ответ на проникновение аллергенов и ирритантов в кожу [4].
Нарушение барьерной функции кожи имеет место при обоих типах АД — атопическом и неатопическом (при последнем, возможно, оно выражено в большей степени). Доказано также, что при АД кожа сухая даже вне обострения заболевания [1–3]. В связи с этим обосновано применение увлажняющих/смягчающих средств и в те периоды заболевания, когда его симптомы отсутствуют.
На что влияет сухость кожи? Установлено, что при наличии ксероза восприимчивость кожи к экспозиции окружающих аллергенных и неаллергенных раздражителей, ирритантов, а также бактерий и вирусов существенно повышается. Следует учитывать также тесную взаимосвязь цикла «ксероз–зуд». Кроме того, при сухости кожи отмечается усиление системной абсорбции ТГКС, следовательно, и их побочных действий [5].
Из этих данных следует, что эффективное воздействие на сухость, зуд кожи, а также дефекты ее барьерной функции будет способствовать повышению результатов терапии АД. Однако повлиять на такие причины возникновения ксероза, как изменения в роговом слое, нарушения кератинизации, состава баланса внутриклеточных липидов, метаболизма трансэпидермальной воды, изменения рН кожи и т. п. — весьма сложная задача. Кроме того, ксероз и дефекты барьерной функции кожи характеризуются различными биохимическими, физико-химическими и морфологическими изменениями.
Разработан целый ряд специальных лечебных средств ухода за сухой и атопической кожей. В России в настоящее время доступны очищающие и увлажняющие/смягчающие средства различных лечебно-косметических линий: «Топикрем», «Авен», «Мустела Стелатопия», «Урьяж Cu-Zn», «Биодерма», «Дардия», «Виши» и т. п. При их использовании следует учитывать: полноту серии; возраст, с которого можно использовать наружное средство; способность средства создавать защитную пленку на коже, подавлять рост микроорганизмов; восстанавливать липидный слой в коже; противовоспалительный эффект и т. д. Эффективность увлажняющих/смягчающих средств зависит от дозы (их следует применять регулярно и в достаточном количестве), рН кожи, а также от комплаентности больных.
Способностью восстанавливать и поддерживать нарушенный при АД трансэпидермальный барьер обладают далеко не все увлажняющие/смягчающие средства, присутствующие на рынке. Особый интерес представляет косметическое средство Локобейз Рипеа®, разработанное компанией «Астеллас Фарма». Локобейз Рипеа® — крем типа «вода в жирах», с высоким (63%) содержанием липидов. В составе Локобейз Рипеа® все виды липидов, идентичные липидам кожи, — холестерин, церамиды, свободные жирные кислоты (олеиновая и пальмитиновая) — представлены в соотношении, оптимальном для ускорения восстановления барьерной функции кожи. Это является ключевой особенностью указанного препарата, которая обеспечивает длительно сохраняющееся (до 24 ч) увлажняющее действие при однократном нанесении в сутки.
Локобейз Рипеа® также содержит наночастицы твердого парафина, которые повышают его эффективность, удлиняют время действия и улучшают косметические свойства крема.
Как показывают клинические исследования, за счет восстановления и поддержания нарушенной барьерной функции кожи у пациентов с АД Локобейз Рипеа® ускоряет разрешение симптомов обострения, повышает эффективность ТГКС и уменьшает потребность в их применении.
Локобейз Рипеа® не содержит красители, отдушки и консерванты, что минимизирует риск развития аллергических реакций.
Постоянное использование специально разработанных для базового ухода за атопической кожей препаратов, способных эффективно восстанавливать нарушенный кожный барьер, помогает существенно снизить количество обострений и улучшить качество жизни больных с АД.
Следует отметить, что увлажняющие смягчающие средства не обладают противовоспалительным действием и в меньшей степени облегчают симптомы, определяющие тяжесть течения АД. Со своей стороны, противовоспалительные препараты не предназначены для лечения сухости кожи.
Топические противовоспалительные препараты
ТГКС — хорошо изученная группа лекарственных средств. Несмотря на появление нового класса противовоспалительных средств — ТИК, они остаются препаратами первой линии в лечении обострений заболевания.
Как известно, при бронхиальной астме алгоритм применения ингаляционных кортикостероидов разработан и предусматривает регулярное их использование в качестве поддерживающей терапии больным всех степеней тяжести заболевания. При АД подход к назначению ТГКС иной и связан прежде всего с высоким потенциальным риском развития местных нежелательных реакций. При назначении ТГКС следует учитывать тяжесть заболевания, место локализации и возраст больного.
В педиатрической практике широко используют синтетическое производное гидрокортизона — гидрокортизона-17-бутират (Локоид). Эстерификация гидрокортизона боковым звеном масляной кислоты по С17 позволила улучшить абсорбцию препарата через кожу и усилить его метаболизм. В результате гидрокортизона-17-бутират приобрел уникальное соотношение эффективность/безопасность: препарат относится к сильным стероидам (как бетаметазон 17-валерат или триамцинолон), но его местная и системная безопасности сравнимы с таким слабым стероидом, как гидрокортизон.
Препарат может применяться длительно (до 4 недель), разрешен к применению у детей начиная с 6-месячного возраста.
Отсутствие значимого угнетения гипоталамо-гипофизарно-надпочечниковой системы (ГГНС) при использовании гидрокортизона 17-бутирата у здоровых добровольцев и пациентов с АД подтверждено в ряде клинических исследований [7, 8].
Тормозящее влияние экзогенных кортикостероидов на гипофиз-адреналовую функцию вполне ожидаемо. Вместе с тем, как было недавно показано в оригинальном исследовании Haeck I. с соавторами, низкое содержание кортизола у больных с тяжелым течением АД в большей степени может быть связано со степенью тяжести самого заболевания, чем с применением ТГКС [9]. Авторы сравнивали базальный уровень кортизола в крови у 25 больных с тяжелой формой АД (1-я группа), которым требовалась госпитализация, и 28 амбулаторных больных со средней и тяжелой степенью тяжести АД (группа 2): у 80% пациентов 1-й группы уровень кортизола был достоверно ниже уровня больных 2-й группы (p < 0,001) и коррелировал с активностью заболевания.
Хотя преимущества ТГКС на основе гидрокортизона перед галогенизированными кортикостероидами не ставится под сомнение, влияние ТГКС на течение АД остается недоказанным. Как правило, не показано применение ТГКС с профилактической целью. Хотя в ряде опубликованных работ такой подход рассматривается [11–13].
В настоящее время с целью превентивной терапии обострений АД у детей и взрослых обосновано использование топических ингибиторов кальциневрина (ТИК). Уже можно считать, что на течение АД способна оказать влияние именно эта группа противовоспалительных средств.
ТИК — противовоспалительные препараты нестероидного ряда
В 80-е годы в Японии впервые из почвенных бактерий Streptomyces tsukubaensis была изолирована субстанция FK506, у которой ученые выявили иммуномодулирующее свойство, подобное циклоспорину А. Огромным преимуществом этого вещества явилась возможность его применения местно при воспалительных заболеваниях кожи. Избирательное действие FK506 в коже было основано на ингибировании фосфатазной активности кальциневрина, торможении транскрипции генов и связанной с ними продукции провоспалительных цитокинов (IL-2, IL-4, IL-5, ГМ-КСФ и т. п.), что выражалось в терапевтическом эффекте самого препарата, получившего впоследствии название такролимус. Различие в молекулярном весе (у такролимуса он примерно на 30% меньше, чем у циклоспорина А, и составляет 804 Д) обусловливает способность препарата проникать через поврежденную кожу при АД [14].
В процессе дальнейших исследований из более чем 400 производных аскомицина путем ферментации был изолирован дериват SDZ ASM 981. Вначале данному веществу приписывали фунгицидное действие, однако спустя 20 лет у него было обнаружено иммуномодулирующее действие в коже. В дальнейшем эта субстанция получила название пимекролимус (торговое название Элидел), который выпускается в одной лекарственной форме — 1% крем.
Сегодня такролимус и пимекролимус составляют новый класс противовоспалительных препаратов нестероидного ряда, используемых при лечении АД, — так называемых топических иммуномодулирующих макролидов.
В России ТИК представлен пимекролимус кремом 1%. Такролимус выпускается под торговым наименованием Протопик (Protopic), в форме мази, содержащей 0,03% и 0,1% активного вещества (препарат находится на завершающей стадии регистрации в России).
С момента появления ТИК опубликовано большое количество исследований, в том числе сравнительных. Несомненно, такие результаты строгих клинических испытаний, как уменьшение частоты обострений АД и потребности в ТГКС при использовании ТИК, свидетельствуют о стероидосберегающем эффекте ТИК [15]. У этих препаратов есть также другие преимущества, в частности, ТИК не влияют на ГГНС [16]. Пимекролимус не накапливается в коже даже при длительном применении, в том числе у младенцев; не вызывает атрофогенный эффект в коже, который обычно развивается уже на 8-й день применения ряда ТГКС в результате ингибирования ими синтеза коллагена в коже [17].
Результаты нескольких фармакокинетических исследований такролимуса у детей и взрослых также свидетельствуют о его минимальной абсорбции в системный кровоток. Так, концентрация такролимуса была ниже порогового значения (< 0,5 нг/мл) в 75–90% исследованных образцах крови больных АД [18]. Абсорбция препарата, более выраженная у пациентов с тяжелым АД, значительно уменьшалась по мере заживления очагов поражения [18]. Кроме того, при длительном применении у детей и взрослых сроком до 1 года не наблюдалось кумуляции такролимуса ни в коже, ни в сыворотке крови [18]. Такролимус не подвергается метаболизму в коже, не влияет на содержание церамидов в роговом слое эпидермиса [19].
Превосходство такролимуса над плацебо у детей и взрослых с АД было продемонстрировано в трех крупных многоцентровых клинических исследованиях [22–24]. Так, в исследовании Hanifin J. и соавт. среди 632 взрослых пациентов с АД, применявших такролимус сроком до 12 недель, значительное улучшение на фоне терапии (≥ 90% от исходного) наблюдалось у 37% и 27% пациентов, получавших 0,1% и 0,03% мазь такролимуса соответственно, по сравнению с 7% пациентов в группе плацебо [22]. В исследовании Paller F. и соавт., включавшем 351 ребенка в возрасте от 2 до 15 лет со средней и тяжелой формой АД, обе концентрации мази такролимуса (0,1% и 0,03%) в течение 12 недель терапии также обеспечивали достоверно более выраженное улучшение клинических симптомов заболевания: как минимум умеренное улучшение наблюдалось по окончании лечения у 72,6% больных в группе 0,03% мази такролимуса, у 78% — в группе 0,1% мази такролимуса по сравнению у 26,7% пациентов в группе плацебо [24].
В первом рандомизированном двойном слепом многоцентровом исследовании эффективности и безопасности такролимуса в виде 0,03%, 0,1% и 0,3% мази у пациентов со среднетяжелым и тяжелым АД статистически значимое улучшение по сравнению с плацебо во всех группах наблюдалось уже после трех дней терапии, что свидетельствует о быстром развитии эффекта на фоне терапии такролимусом, не уступающем ТГКС [24]. Данные других сравнительных исследований также показали, что такролимус как минимум сравним или превосходит терапевтическую активность ТГКС при АД как у детей, так и у взрослых. Так, Reitamo S. и соавт. в двойном слепом рандомизированном многоцентровом исследовании у 570 взрослых больных со средней и тяжелой степенью АД показали, что терапевтическая эффективность 0,1% мази такролимуса сравнима с действием ТГКС сильного класса гидрокортизона-17-бутирата [25]. Причем подавление уровня воспалительных клеток, а также экспрессия цитокинов и рецепторов хемокинов наблюдались в большей степени при аппликации такролимуса. Таким образом, такролимус играет важную роль не только в торможении активности цитокинов, но и ИЛ-12-индуцированном переключении Th2- на Th1-цитокиновый профиль, что характерно для хронического течения АД.
Arkwright P. и соавт. у 96 детей со средней и тяжелой формой АД сравнивали эффективность 0,03% мази такролимуса и традиционно применявшихся ТГКС путем нанесения препаратов на два противоположных участка кожи: топический такролимус был эффективнее ТГКС у 72 из 93 больных (77%) [26]. Недавно в Японии было завершено сравнительное исследование по эффективности и безопасности длительного применения такролимуса у 568 взрослых больных: выраженное улучшение симптомов АД через 6 нед терапии диагностировано в 85% случаев, в 91% — через 26 нед и 52 нед, при этом эффективность препарата оставaлaсь высокой на протяжении 2 лет наблюдения [27].
Показания для назначения ТИК
В вышеупомянутом согласительном документе по лечению и профилактике АД совместная международная экспертная группа пришла к заключению о том, что долгосрочный эффект ТИК на иммунную систему не достаточно ясен, в связи с чем следует ограничить применение этих препаратов у детей в возрасте до 2 лет, а также у детей и взрослых, имеющих иммуннокомпрометирующие заболевания [1]. Далее в документе говорится о том, что исследования безопасности ТИК у детей этой возрастной группы в настоящее время продолжаются. В частности, эксперты ссылаются на обширный обзор Paul С. с соавторами, который включает оценку эффективности и безопасности пимекролимуса крема 1%-го у младенцев на основании 4 фармакокинетических и 6 клинических исследований [17]. Эти данные вкратце можно суммировать так: плазменная концентрация пимекролимуса у 35 пациентов была низкой и составляла 1 нг/мл в более 80% образцов, независимо от степени тяжести заболевания и площади поражения кожи; она оставалась низкой на протяжении 1 года лечения. Уровень системной экспозиции пимекролимуса у младенцев был сравним с концентрацией в крови у более старших детей, что свидетельствует о том, что дети раннего возраста не представляют высокий риск для накожной абсорбции пимекролимуса крема 1%-го в зависимости от соотношения поверхности кожи/масса тела.
Особый интерес представляют сравнительные исследования эффективности и безопасности такролимуса и пимекролимуса у детей и взрослых, страдающих АД. Результаты трех сравнительных исследований были обобщены в обзоре Paller A. с соавторами. В рандомизированных, проведенных двойным слепым методом исследованиях приняли участие 1065 взрослых и детей с АД от легкой до очень тяжелой степени тяжести, которые использовали 0,1%-ную (взрослые) и 0,03%-ную (дети) мазь такролимуса в сравнении с 1%-ным кремом пимекролимуса 2 раза в день на протяжении ≤ 6 недель [21]. Лечение такролимусом приводило к более выраженному улучшению показателя EASI, чем лечение пимекролимусом во всех группах, с достоверным различием для взрослых и детей в группе от среднетяжелого до очень тяжелого АД. Клинический успех (исчезновение или почти полное исчезновение) проявлений АД в конце лечения наблюдалось у 45,7% взрослых в группе такролимуса по сравнению с 27,1% в группе пимекролимуса (p < 0,0001); статистически значимое преимущество такролимуса по данному показателю также было выявлено у детей с АД среднетяжелого и тяжелого течения (32,4% против 17,7%, p < 0,01).
Одним из важных свойств ТИК является противозудный эффект, позволяющий предотвратить расчесы кожи (или минимизировать этот процесс), который, в свою очередь, приводит к усилению воспаления, вторичным инфекциям кожи и прогрессированию тяжести течения АД. Взрослые больные АД отмечали уменьшение выраженности зуда в группе пимекролимуса крема 1%-го на 2-е сутки от начала лечения, в группе такролимуса — на 3-й день [28]. По данным других авторов, противозудный эффект пимекролимуса крема 1%-го проявлялся чуть позже, к концу 1-й недели от начала терапии и длился на протяжении всего периода его применения [29]. В целом выраженность основных симптомов АД (зуд, эритема или лихенизация) достоверно снижалась через 3–10 дней в группе, где применяли крем пимекролимуса [30]. По данным упоминавшегося выше обзора сравнительных исследований двух ТИК A. Paller с соавт., уменьшение интенсивности зуда по оценке пациентов было достоверно более выраженным среди пациентов, получавших лечение мазью такролимуса по сравнению с группой получавших крем пимекролимуса 1,0%-ный [21].
Чрезвычайно важен тот факт, что абсорбция ТИК через кожу снижается с продолжением их применения и улучшением кожного процесса [17]. Обнаружено также, что ТИК достоверно снижают степень колонизации кожи Staphylococcus aureus (S. aureus) у больных АД, причем тормозящий эффект отмечен в первую неделю от начала терапии (известно, что ТГКС снижают уровень S. aureus лишь через 2 нед от начала их применения) [31]. На фоне применения ТИК документировано также снижение частоты инфекций кожи [17, 27]. Ингибиторы кальциневрина в топической форме идеальны для лечения АД с локализацией в периорбитальной области, где абсорбция ТГКС наиболее высока и есть опасность повышения внутриглазного давления.
В настоящее время ТИК показаны для лечения всех степеней тяжести течения АД детям в возрасте старше 2 лет и взрослым, пимекролимус чаще используют при легкой и средней степени тяжести [1, 17, 27].
Нежелательные реакции ТИК
Из нежелательных реакций ТИК иногда отмечают усиление гиперемии, транзиторное жжение или зуд кожи в месте аппликации [32]. Пимекролимус, по некоторым данным, в меньшей степени вызывает жжение и зуд, чем такролимус. Такие нежелательные реакции, как незначительные и преходящие ощущения тепла и/или жжения, эритема и зуд в месте нанесения препаратов обычно проходят в течение первой недели терапии.
Andersen K. и Broesby–Olsen S. описали случай тяжелого аллергического дерматита после нанесения пимекролимуса крема 1%-го у взрослого пациента, страдающего рецидивирующим дерматитом рук [33]. Диагностические пэтч-тесты показали, что контактная аллергия была вызвана входящим в состав препарата эмульсификатором алкоголя. В другом случае аллергический контактный дерматит развился у 15-летней девочки с АД на такролимус и на пимекролимус, причем реакцию вызывала активная субстанция препаратов [34].
Переносимость и безопасность
С момента клинического использования ТИК уже накоплен достаточный опыт о переносимости и безопасности лекарственных препаратов этой группы. До недавнего времени особо остро дискутировался вопрос о возможности образования лимфом в результате их применения. Комитет FDA (Food and Drug Administration, США) досконально изучил эту проблему. Анализ проводился в 2005 г. с учетом опыта применения ТИК у 7 млн американцев [36]. Пять независимых экспертов, специализирующихся в области дерматологии, эпидемиологии, посттрансплантационной онкологии, а также педиатр-онколог не подтвердили наличия связи между применением такролимуса и пимекролимуса и повышением риска образования опухоли. Эксперты напоминают о характерных признаках, способствующих возникновению лимфомы при проведении больным иммуносупрессивной или иммуномодулирующей терапии: 1. Лимфомы чаще встречаются в легких и мягких тканях. 2. Клетки Лангерганса полиморфны или плеоморфны, или имеют место морфологические изменения типа лимфомы Ходжкина. 3. Характерно наличие генома Эпштейн-Бара в клетках лимфомы. 4. В-клеточная лимфома формируется через недели/месяцы или даже несколько лет после начала иммуномодулирующей терапии. 5. Лимфома спонтанно разрешается в 30–50% случаев после окончания радиотерапии. Хотя связь между использованием ТИК, развитием лимфом и рака кожи (базально-клеточная эпителиома и плоскоклеточная карцинома) не установлена, тем не менее комитет FDA потребовал внести соответствующее предостережение в инструкции по применению этих лекарственных средств, учитывая отсутствие результатов изучения безопасности длительной терапии ими. М. Naylor и соавторы провели анализ результатов двойных слепых плацебо-контролируемых исследований и двух долгосрочных открытых исследований такролимуса у пациентов с АД. Рассчитанная частота развития рака кожи у пациентов ≥ 40 лет на основании 1718 пациентов-лет применения мази такролимуса 9813 пациентами была сравнимой со средним показателем в CША для популяции аналогичного возраста [37].
Доклинические исследования in vitro или in vivo не продемонстрировали наличие карциногенного, фотокарциногенного или мутагенного эффектов у пимекролимуса крема 1%-го [38]. В экспериментах на животных образование лимфомы было связано с приемом высоких доз пимекролимуса перорально, превышающих в 31–343 раза дозу пимекролимуса крема, применяемого в лечении тяжелой формы АД у детей. Более того, распространенность не-Ходжкина лимфомы среди пациентов, использующих пимекролимус крем 1%-ный, была меньше, чем в общей популяции [1, 17]. В исследованиях in vitro на мышах, стандартной модели фотоканцерогенности у животных, применение мази такролимуса не было связано с увеличением повреждения ДНК в коже после облучения ультрафиолетом-В; уровень повреждения был даже меньше, чем у животных, у которых применялся ультрафиолет-В и мазь-плацебо [39].
Arellano F. и соавторы изучали связь между приемом иммуносупрессивных препаратов (системные и топические кортикостероиды, топические пимекролимус и такролимус) и риском возникновения рака у 293 253 пациентов с АД [40]. Наибольший риск, с которым связано возникновение лимфомы, представляет тяжелая форма АД.
В то же время сам АД может ассоциироваться с опухолью, такой как Т-клеточная лимфома [41]. Ведущий ученый по АД проф. D. Leung напоминает о том, что в некоторых случаях тяжелую форму АД даже следует дифференцировать с Т-клеточной лимфомой (особенно у пациентов в возрасте старше 21 года) [42].
Индукция иммуносупрессии и тем самым повышение риска возникновения опухолей кожи и лимфом в большей степени, возможно, связаны с использованием системных кортикостероидов [43].
В 2005 г. ряд специалистов (Bieber Т. с соавторами) опубликовали заявление-консенсус, в котором выражается их беспокойство по поводу предупреждения FDA, поскольку, с их точки зрения, данных о том, что местное применение мази такролимуса или крема пимекролимуса вызывает злокачественные опухоли, недостаточно [44]. Согласно данному заявлению, как такролимус, так и пимекролимус интенсивно изучались в ходе клинических исследований у около 40 000 пациентов с АД в течение 10 лет; более 7,5 млн пациентов, из них около половины — дети, получали ТИК в рамках пострегистрационных наблюдений. Системная абсорбция этих препаратов очень незначительна и обнаруживаемая концентрация в сыворотке крови недостаточна для развития системной иммуносупрессии даже у маленьких детей с АД и поражением большой площади поверхности тела. Ни мазь такролимуса, ни крем пимекролимуса не были связаны с увеличением риска развития злокачественных опухолей в ходе клинических исследований. Лимфомы, идентифицированные путем спонтанных сообщений о нежелательных явлениях, не обладали характеристиками лимфом, связанных с иммуносупрессивной терапией.
Лечение такролимусом и пимекролимусом не сопровождалось системной иммуносупрессией у детей, одновременно получавших плановые вакцинации, а также увеличением частоты инфекций кожи [45].
Литература
-
Akdis C., Akdis M., Bieber T. et al. Diagnosis and treatment of atopic dermatitis in children and adults: European Academy of Allergology and Clinical Immunology / American Academy of Allergy, Asthma and Immunology /PRACTALLConsensus Report // J. Allergy. Clin. Immunol. 2006; 118: 152–69.
-
Folster-Holst R., Pape M., Buss Y. et al. Low prevalence of the intrinsic form of atopic dermatitis among adult patients // Allergy, 2006; 61: 629–32.
-
Novembre E., Cianferoni A., Lombardi E. et al. Natural history of «intrinsic» atopic dermatitis // Ibid., 2001; 56: 452–53.
-
Leung D. New insights into atopic dermatitis // J. Clin. Invest. 2004; 113: 651–7.
-
Wilkinson S., Cartwright P., English J. Hydrocortisone: an important cutaneous allergen // Lancet, 1991; 337: 761–2.
-
Rampini E. Methylprednisolone aceponate (MPA)— use and clinical experience in children // J. Dermatol. Treatm. 1992; 3 (2): 27–9.
-
Eichenfield L., Charles N., Ellis M. et al. Evaluation of Adrenal Suppression of a Lipid Enhanced, Topical Emollient Cream Formulation of Hydrocortisone Butyrate 0.1% in Treating Children with Atopic Dermatitis // Pediatric Dermatology, 2007; 24: 81–84.
-
Visscher H. //Eur. J. Clin. Pharmacol. 1995; 48: 123–5.
-
Haeck I., Timmer-de Mik L., Lentjes E. et. al. Low basal serum cortisol in patients with severe atopic dermatitis: potent topical corticosteroids wrongfully accused // Br. J. Dermatol. 2007; 156: 979–85.
-
Falk E. // Dtsch. Dermatol. 1994; 42: 747–750.
-
Kirkup M., Weinberg E., Helm K., Kennedy C. Acute and maintenance treatment of atopic dermatitis in children — two comparative studies with fluticasone propionate (0,05%) cream // J. Dermatol. Treat. 2003; 14: 141–8.
-
Peserico A., Stadtler G., Sebastian M. et al. Reduction of relapses of atopic dermatitis with methylprednisolone aceponate cream twice weekly in addition to maintenance treatment with emollient in a multicentre, randomised, double-blind, controlled study [abstr] // 16 th EADV, Мay 2007.
-
Bieber T., Vick K., Folster-Holst R. et al. Efficacy and safety of methylprednisolone aceponate ointment 0.1% compared to tacrolimus 0.03% in children and adolescents with an acute flare of severe atopic dermatitis // Allergy, 2007; 62: 184–9.
-
Nghiem P., Person G., Langley R. Tacrolimus and pimecrolimus: from clever prokaryotes to inhibiting calcineurin and treating atopic dermatitis // J. Am. Acad. Dermatol., 2002; 46: 228–241.
-
Fowler J., Johnson A., Chen M., Abrams K. Improvement in pruritus in children with atopic dermatitis using pimecrolimus cream 1% //Cutis. 2007;79: 65–72.
-
Simon D., Vassina E., Yousefi S. et al. Inflammatory cells numbers and cytokine expression after topical pimecrolimus treatment //Allergy, 2005; 60: 944–51.
-
Paul C., Cork M., Rossi F. et al. Safety and tolerability of 1% pimecrolimus cream among infants: experience with 1133 patients treated for up to 2 years // Pediatrics. 2006; 117: 118–28.
-
Undre N., Green A., Harper J. et al. Tacrolimus pharmacokinetics in paediatric patients with moderate to severe atopic dermatitis after single and repeated application [abstract] // Ann. Dermatol. Venereol., 2002; 129: 1S424.
-
Paslin D., Wertz P. A study to determine the effect of tacrolimus on ceramide levels in the stratum corneum of patients with atopic dermatitis // Int. J. Dermatol. 2006; 45: 352–6.
-
Eichenfield L., Ho V., Matsunaga J. et al. Blood concentrations, tolerability and efficacy of pimecrolimus cream 1% in Japanese infants and children with atopic dermatitis // J. Dermatol., 2007; 34: 231–236.
-
Paller A., Lebwohl M., Fleischer A. et al. Tacrolimus ointment is more effective than pimecrolimus cream with a similar safety profile in the treatment of atopic dermatitis: Results from 3 randomized, comparative studies // J. Am. Acad. Dermatol. 2005; 52: 810–22.
-
Hanifin J. M., Ling M. R., Langley R., Breneman D., Rafal E. Tacrolimus ointment for the treatment of atopic dermatitis in adults patients: Part I, efficacy // J. Am. Acad. Dermatol. 44(1): S28–38 (2001 Jan).
-
Paller A. S., Eichenfield L. F., Leung D. Y. M. et al. A 12 week study of tacrolimus ointment for the treatment of atopic dermatitis //J. Am. Acad. Dermatol. 2001; 44: S47–S57.
-
Ruzicka T., Bieber T., Schopf E. et al. A short-term trial of tacrolimus ointment for atopic dermatitis. European Tacrolimus Multicenter Atopic Dermatitis Study Group // N. Engl. J. Med., 1997; 337: 816–21.
-
Reitamo S., Harper J., Bos J. et al. Therapeutics 0,03% tacrolimus ointment applied once or twice daily is more efficacious than 1% hydrocortisone acetate in children with moderate to severe atopic dermatitis: results of a randomized double-blind controlled trial // Br. J. Dermatol., 2004; 150: 554–62.
-
Arkwright P., Gillespie M., Ewing C., David T. Blinded side-to-side comparison of topical corticosteroid and tacrolimus ointment in children with moderate to severe atopic dermatitis // Clin. Exp. Dermatol. 2007; 32: 145–7.
-
Nakagawa H. Comparison of the efficacy and safety of 0.1% tacrolimus ointment with topical corticosteroids in adult patients with atopic dermatitis: review of randomised, double-blind clinical studies conducted in Japan. // Clin. Drug. Investig. 2006; 26: 235–46.
-
Kempers S., Boguniewicz M., Carter E. et al. A randomized inverstigator-blinded study comparing pimecrolimus cream 1% with tacrolimus 0,03% in the treatment of pediatric patients with moderate atopic dermatitis //J. Am. Acad. Dermatol. 2004; 51: 515–25.
-
Kempers S., Boguniewicz M., Carter E. et al. A randomized inverstigator-blinded study comparing pimecrolimus cream 1% with tacrolimus 0,03% in the treatment of pediatric patients with moderate atopic dermatitis // Ibid. 2004; 51: 515–25.
-
Eichenfield L., Beck L. Elidel (pimecrolimus) cream 1%: a nonsteroidal topical agent for the treatment of atopic dermatitis //J. Allergy Clin. Immunol., 2003; 111: 1153–68.
-
Fukushima H., Hirano T., Shibayama N. et al. The role of immune response to Staphylococcus aureus superantigens and disease severity in relation to the sensitivity to tacrolimus in atopic dermatitis // Int. Arch. Allergy. Immunol. 2006; 141: 281–89.
-
Thestrup-Pedersen K. Tacrolimus treatment of atopic eczema/dermatitis syndrome // Curr. Opin. Allergy Clin. Immunol., 2003; 3: 359–62.
-
Andersen K., Broesby-Olsen S. Allergic contact dermatitis from oleyl alcohol in Elidel cream // Contact Dermatitis. 2006; 55: 354–6.
-
Shaw D., Maibach H., Eichenfield L. Allergic contact dermatitis from pimecrolimus in a patient with tacrolimus allergy // J. Am. Acad. Dermatol. 2007; 56: 342–5.
-
Fery-Blanco C., Pelletier F., Humbert P., Aubin F. Disseminated molluscum contagiosum during topical treatment of atopic dermatitis with tacrolimus: efficacy of cidofovir // Ann. Dermatol. Venereol. 2007; 134: 457–9.
-
Fonacier L., Spergel J., Ernest N. et al. Report of the topical calcineurin inhibitor task force of the American College of Allergy, Asthma and Immunology and the American Academy of Allergy, Asthma and Immunology // J. Allergy Clin. Immunol., 2005; 115: 1249–53.
-
Naylor M. C. E., Jaracz E. J. et al. Non-melanoma skin cancer in patients with atopic dermatitis treated with topical tacrolimus // J. Dermatological. Treat. 2005; 16: 149–53.
-
De Prost Y., Wahn U. Pimecrolimus (SDZ ASM 981) cream 1% reduces the need for topical corticosteroids to treat atopic eczema in children // The 10th Congress of the European Academy of Dermatology and Venereology (EADV). 2001; [Abstract].
-
Ring J., Barker J., Behrendt H. et al. Review of the potential photo-cocarcinogenicity of topical calcineurin inhibitors // Position statement of the European Dermatology Forum. JEADV. 2005; 19: 663–71.
-
Arellano F., Wentworth C., Arana A. et al. Risk of lymphoma following exposure to calcineurin inhibitors and topical steroids in patients with atopic dermatitis //J. Invest. Dermatol., 2006; 9: 32–34.
-
Olesen A., Engholm G., Storm H. et al. The risk of cancer among patients previously hospitalized for atopic dermatitis //J. Invest. Dermatol. 2005; 125: 445–49.
-
Leung D. Atopic dermatitis: new insights and opportunities for therapeutic intervention // J. Allergy Clin. Immunol. 2000; 105: 860–76.
-
Rapaport M., Lebwohl M. Corticosteroid addiction and withdrawal in the atopic: the red burning skin syndrome // Clin. Dermatol. 2003; 21: 201–14.
-
Bieber T., Cork M., Ellis C. et al. Consensus statement on the safety profile of topical calcineurin inhibitors // Dermatology. 2005; 211: 77–78.
-
Fleischer A. B., Ling M., Eichenfield L. et al. Tacrolimus ointment for the treatment of atopic dermatitis is not associated with an increase in cutaneous infections // J. Am. Acad. Dermatol. 2002; 47: 562–70.
Д. Ш. Мачарадзе, доктор медицинских наук, профессор
РУДН, Москва
