Состав
Одна таблетка, покрытая пленочной оболочкой, содержит:
- Дозировка 10 мг
- активное вещество: мемантина гидрохлорид – 10,0 мг;
- вспомогательные вещества: целлюлоза микрокристаллическая – 152,5 мг; кальция гидрофосфат дигидрат – 50,0 мг; кроскармеллоза натрия – 12,5 мг; лактозы моногидрат – 10,0 мг; гипролоза (гидроксипропилцеллюлоза) – 5,0 мг; тальк – 5,0 мг; кремния диоксид коллоидный – 2,5 мг; магния стеарат –
- 2,5 мг; пленочная оболочка: [гипромеллоза – 4,000 мг, гипролоза (гидроксипропилцеллюлоза) – 1,552 мг, тальк – 1,568 мг, титана диоксид – 0,880 мг] или [сухая смесь для пленочного покрытия, содержащая гипро-меллозу (50 %), гипролозу (гидроксипропилцеллюлозу) (19,4 %), тальк (19,6 %), титана диоксид (11 %)] – 8,0 мг.
- Дозировка 20 мг
- активное вещество: мемантина гидрохлорид – 20,0 мг;
- вспомогательные вещества: целлюлоза микрокристаллическая – 142,5 мг; кальция гидрофосфат дигидрат – 50,0 мг; кроскармеллоза натрия – 12,5 мг; лактозы моногидрат – 10,0 мг; гипролоза (гидроксипропилцеллюлоза) – 5,0 мг; тальк – 5,0 мг; кремния диоксид коллоидный – 2,5 мг; магния стеарат – 2,5 мг;
- пленочная оболочка: [гипромеллоза – 4,0000 мг, гипролоза (гидроксипропилцеллюлоза) – 1,5520 мг, тальк – 1,5408 мг, титана диоксид – 0,8696 мг, железа оксид желтый (железа оксид) – 0,0376 мг] или [сухая смесь для пленочного покрытия, содержащая гипромеллозу (50 %), гипролозу (гидроксипропилцеллюлозу) (19,4 %), тальк (19,26 %), титана диоксид (10,87 %), железа оксид желтый (железа оксид) (0,47 %)] – 8,0 мг.
Таблетки, покрытые пленочной оболочкой, 10 мг и 20 мг:
- 10, 15 или 30 таблеток в контурной ячейковой упаковке из пленки поливинилхлоридной и фольги алюминиевой.
- 30 таблеток в банке из полиэтилена высокой плотности.
- 3, 6 или 9 контурных ячейковых упаковок по 10 таблеток, 2, 4 или 6 контурных ячейковых упаковок по 15 таблеток, 1, 2 или 3 контурные ячейковые упаковки по 30 таблеток или одна банка вместе с инструкцией по применению в пачке из картона.
Описание
Продолговатые двояковыпуклые таблетки, имеющие риску с каждой стороны, покрытые пленочной оболочкой белого цвета (дозировка 10 мг) и желтого цвета (дозировка 20 мг). На поперечном разрезе ядро белого или почти белого цвета.
Фармакологическое действие
Деменции средство лечения.
Фармакодинамика
Производное адамантана. Является неконкурентным антагонистом N-метил-D-аспартат (NMDA)-рецепторов, оказывает модулирующее действие на глутаматергическую систему. Регулирует транспорт ионов, блокирует кальциевые каналы, нормализует мембранный потенциал, улучшает процесс передачи нервного импульса.
Фармакокинетика
Всасывание
Прием пищи не влияет на абсорбцию. После приема внутрь мемантин быстро и полностью всасывается из желудочно-кишечного тракта. Максимальная концентрация мемантина в плазме крови достигается через 3-8 часов после приема.
Распределение
Ежедневный прием суточной дозы 20 мг приводит к равновесной плазменной концентрации мемантина 70-150 нг/мл. При применении суточной дозы 5-30 мг было рассчитано отношение средней концентрации в цереброспинальной жидкости к концентрации в плазме крови, равное 0,52.
Объем распределения составляет около 10 л/кг. Около 45 % мемантина связывается с белками плазмы крови. При нормальной функции почек кумуляции мемантина не отмечено.
Метаболизм
80 % циркулирующего в крови мемантина представлено неизменным веществом. Основными метаболитами являются N-3,5-диметилглудантан, смесь изомеров 4- и 6-гидроксимемантина, 1-нитрозо-3,5-диметиладамантан. Метаболиты не обладают собственной фармакологической активностью. При экспериментах in vitro не выявлено метаболизма, осуществляемого изоферментами цитохрома P450.
Выведение
Мемантин выводится преимущественно почками. Выведение происходит однофазно, период полувыведения составляет 60-100 часов. У добровольцев с нормальной функцией почек общий клиренс составляет 170 мл/мин/1,73 м2, часть общего почечного клиренса достигается за счет канальцевой секреции. Почечное выведение также включает канальцевую реабсорбцию, возможно опосредованную катионными транспортными белками. Скорость почечной элиминации мемантина в условиях щелочной реакции мочи может снижаться в 7-9 раз. Защелачивание мочи может быть вызвано резким изменением питания, например, переход с рациона, включающего продукты животного происхождения, к вегетарианской диете, или вследствие интенсивного применения щелочных желудочных буферов.
Линейность
Исследования, проведенные у добровольцев, показали линейность фармакокинетики в диапазоне доз 10-40 мг.
Фармакокинетическая/фармакодинамическая зависимость
При применении мемантина в дозе 20 мг/сут уровень концентрации в цереброспинальной жидкости соответствует величине константы ингибирования, что для мемантина составляет 0,5 мкмоль в области фронтальной коры головного мозга.
Мемантин: Показания
Деменция альцгеймеровского типа умеренной и тяжелой степени.
Способ применения и дозы
Терапию мемантином следует начинать и проводить под наблюдением врача с опытом диагностики и лечения деменции альцгеймеровского типа. Диагноз должен быть установлен в соответствии с действующими рекомендациями. Лечение следует начинать только в том случае, если лицо, осуществляющее постоянный уход за пациентом, будет регулярно контролировать прием препарата пациентом. Переносимость и дозировку мемантина необходимо регулярно пересматривать, желательно в течение первых трех месяцев после начала лечения. После этого клиническая эффективность мемантина и переносимость пациентом лечения должны пересматриваться согласно действующим клиническим рекомендациям. Поддерживающее лечение можно продолжать неопределенно долго при наличии положительного терапевтического эффекта и хорошей переносимости препарата. Прием мемантина следует прекратить при отсутствии положительного терапевтического эффекта или непереносимости пациентом препарата.
Препарат следует принимать внутрь один раз в сутки и всегда в одно и то же время, независимо от приема пищи. Начинать лечение мемантином рекомендуют с применения минимально эффективных доз.
Применяют в течение 1-й недели терапии (дни 1-7) в дозе 5 мг/сут, в течение 2-й недели (дни 8-14) в дозе 10 мг/сут, в течение 3-й недели (дни 15-21) в дозе 15 мг/сут, начиная с 4-й недели – в дозе 20 мг/сут.
Рекомендуемая поддерживающая доза – 20 мг/сут.
Максимальная суточная доза – 20 мг.
Применение при беременности и кормлении грудью
Беременность
Применение при беременности противопоказано, так как данных о влиянии мемантина на течение беременности нет. Экспериментальные исследования, проведенные на животных, указывают на возможность замедления внутриутробного роста при уровне воздействия идентичных или несколько более высоких концентраций мемантина по сравнению с такими у человека. Потенциальный риск для человека неизвестен.
Период грудного вскармливания
Сведений о выделении мемантина с грудным молоком нет, поэтому женщинам, принимающим мемантин, следует прекратить грудное вскармливание.
Мемантин: Противопоказания
- повышенная чувствительность к мемантину или любому из компонентов, входящих в состав препарата;
- печеночная недостаточность тяжелой степени (класс С по классифика ции ЧайлдПью);
- непереносимость лактозы, дефицит лактазы, синдром глюкозогалак тозной мальабсорбции;
- беременность;
- период грудного вскармливания;
- возраст до 18 лет (эффективность и безопасность не установлены).
С осторожностью: тиреотоксикоз; эпилепсия, предрасположенность к эпилепсии; судороги (в том числе в анамнезе); одновременное применение антагонистов NMDA-рецепторов (амантадин, кетамин, декстрометорфан); наличие факторов, повышающих рН мочи (резкая смена диеты, например, переход на вегетарианскую диету, обильный прием щелочных желудочных буферов); почечный канальцевый ацидоз; тяжелые инфекции мочевыводящих путей, вызванных бактериями рода Proteus; инфаркт миокарда (в анамнезе); сердечная недостаточность (III-IV функциональный класс по классификации NYHA); неконтролируемая артериальная гипертензия; почечная недостаточность; печеночная недостаточность (класс А и В по классификации Чайлд-Пью).
Мемантин: Побочные действия
Классификация частоты развития побочных эффектов согласно рекомендациям Всемирной организации здравоохранения (ВОЗ): очень часто > 1/10; часто от > 1/100 до 1/1000 до 1/10000 до
Со стороны центральной нервной системы: часто — головная боль, головокружение, сонливость, нарушение равновесия; нечасто — нарушение походки, спутанность сознания, галлюцинации (галлюцинации наблюдались, главным образом, у пациентов с деменцией альцгеймеровского типа тяжелой степени); очень редко — судороги; частота неизвестна – психотические реакции, нарушение сознания, повышенная возбудимость, депрессия, беспокойство, суицидальные мысли, повышение внутричерепного давления, мышечный гипертонус.
Со стороны сердечно-сосудистой системы: часто – повышение артериального давления; нечасто – венозный тромбоз/тромбоэмболия, сердечная недостаточность.
Со стороны пищеварительной системы: часто — запор; нечасто — тошнота, рвота; частота неизвестна – панкреатит, гепатит.
Со стороны дыхательной системы: часто — одышка.
Со стороны мочеполовой системы: частота неизвестна – острая почечная недостаточность, цистит, повышение либидо.
Аллергические реакции: часто — гиперчувствительность к компонентам препарата; частота неизвестна – аллергические реакции, синдром Стивенса-Джонсона.
Со стороны кожных покровов: частота неизвестна – тромбоцитопеническая пурпура.
Лабораторные показатели: часто – повышение активности «печеночных» ферментов; частота неизвестна – агранулоцитоз, лейкопения (включая нейтропению), панцитопения, тромбоцитопения.
Прочие: нечасто – повышенная утомляемость; редко — грибковые инфекции; частота неизвестна – кандидоз.
Передозировка
Имеются ограниченные данные по передозировке, полученные в ходе клинических исследований и пострегистрационного наблюдения.
Симптомы
Передозировка при приеме относительно больших доз мемантина (200 мг однократно, или 105 мг в сутки в течение 3 дней) выражается симптомами утомляемости, слабости и/или диареи или отсутствием симптомов.
Передозировка при приеме до 140 мг мемантина однократно или неизвестного количества мемантина выражается симптомами, связанными с центральной нервной системой (спутанность сознания, сонливость, головокружение, вертиго, беспокойство, возбуждение, галлюцинации, нарушение походки) и/или желудочно-кишечными нарушениями (рвота, диарея).
В наиболее серьезных случаях передозировки пациент выживал после приема более чем 2000 мг мемантина с нежелательными явлениями со стороны нервной системы (кома в течение 10 дней, позже диплопия, ажитация). Пациент получал симптоматическую терапию и плазмаферез, и выздоровел без последствий.
Другой описанный случай серьезной передозировки – 400 мг мемантина однократно. Пациент выздоровел без последствий. Отмечались нежелательные явления со стороны нервной системы: беспокойство, психоз, зрительные галлюцинации, ступор, приступы судорог, сонливость, бессознательное состояние.
Лечение
Симптоматическая терапия, промывание желудка, прием адсорбентов (активированного угля), подкисление мочи, форсированный диурез (при необходимости). Специфического антидота нет.
Взаимодействие
При одновременном применении мемантина с препаратами леводопы, агонистами дофаминовых рецепторов, антихолинергическими средствами их действие может усиливаться.
При одновременном применении мемантина с барбитуратами, нейролептиками их действие может уменьшаться.
При одновременном применении мемантина с дантроленом или баклофеном, а также со спазмолитиками их действие может изменяться (усилиться или уменьшиться), поэтому дозы препаратов следует подбирать индивидуально.
Следует избегать одновременного применения мемантина с амантадином из-за риска развития психоза. Оба соединения являются антагонистами NMDA-рецепторов. Риск развития психоза также повышен при одновременном применении мемантина с фенитоином, кетамином и декстрометорфаном.
При одновременном применении мемантина с циметидином, ранитидином, прокаинамидом, хинидином, хинином и никотином увеличивается риск повышения концентрации мемантина в плазме крови.
При одновременном применении мемантина с гидрохлортиазидом возможно снижение концентрации гидрохлортиазида в плазме крови за счет увеличения его выведения из организма.
Возможно повышение международного нормализованного отношения (МНО) у пациентов, принимающих одновременно пероральные непрямые антикоагулянты (варфарин). Рекомендуется регулярно проводить мониторинг протромбинового времени или МНО у пациентов, принимающих одновременно непрямые антикоагулянты.
Одновременное применение мемантина с антидепрессантами, селективными ингибиторами обратного захвата серотонина и ингибиторами моноаминооксидазы требует тщательного наблюдения за пациентами.
По данным проведенных фармакокинетических исследований, у молодых здоровых добровольцев при однократном одновременном приеме мемантина с глибенкламидом/ метформином или донепезилом эффектов лекар ственного взаимодействия выявлено не было.
Проведенные клинические исследования также не выявили влияния мемантина на фармакокинетику галантамина у молодых здоровых добровольцев.
В исследованиях in vitro мемантин не ингибировал изоферменты CYP 1A2, 2A6, 2C9, 2D6, 2E1, 3A, монооксигеназу, содержащую флавин, эпоксидгидролазу, а также сульфатирование.
Меры предосторожности
С осторожностью следует применять у пациентов с эпилепсией, почечной недостаточностью, тиреотоксикозом, судорогами в анамнезе, артериальной гипертензией, инфарктом миокарда в анамнезе, сердечной недостаточностью.
При нарушениях функции почек дозу мемантина следует уменьшить.
Условия отпуска
Характеристики
Торговое название
Мемантин
Действующее вещество (МНН)
Мемантин
Дозировка или размер
10 мг
Форма выпуска
таблетки, покрытые пленочной оболочкой
Первичная упаковка
упаковка контурная ячейковая
Условия хранения
При температуре не выше 25 °C
Представлено описание активных веществ лекарственного препарата. Описание препарата основано на официально утвержденной инструкции по применению от компании-производителя. Приведенное описание носит исключительно информационный характер и не может быть использовано для принятия решения о возможности применения конкретного лекарственного препарата.
Болезнь Альцгеймера: лечение мемантином
Статьи
Алексей Кузнецов, клинический фармаколог, Москва
Болезнь Альцгеймера — это самое распространенное нейродегенеративное заболевание пожилого возраста. Общемировая заболеваемость измеряется десятками миллионов и этот показатель постоянно растет. Прогнозируемая заболеваемость болезнью Альцгеймера на 2030 год составляет около 66 млн человек, а к 2050 году число больных вырастет до 115 млн.
Мемантин в лечении болезни Альцгеймера
Согласно Федеральным клиническим рекомендациям по диагностике и лечению болезни Альцгеймера, на стадии умеренной и тяжелой деменции (1++, А) препаратом первого выбора является препарат мемантин. На стадии мягкой деменции мемантин также рекомендуют применять, если отсутствует эффект от холинергической терапии или при наличии в структуре синдрома деменции нарушений моторики (моторная дисфазия, моторная диспраксия) (2++, B).
Клиническая эффективность мемантина при болезни Альцгеймера исследована в многочисленных зарубежных и отечественных исследованиях, которые показали, что 12-недельный курс лечения значимо улучшает когнитивное и повседневное функционирование больных, снижает зависимость от ухода, улучшает поведенческие симптомы у пациентов с умеренной и тяжелой болезни Альцгеймера и хорошо переносится (1++, А)
Выбор мемантина
Мемантин является довольно дорогостоящим препаратом и некоторые семьи пациентов с болезнью Альцгеймера сомневаются в целесообразности его приобретения, что ухудшает прогноз заболевания и приводит к ускорению темпа инвалидизации и полной потере самостоятельности пациентом.
В связи с этим мы решили провести фармакоэкономический анализ, который поможет медицинским специалистам предоставить пациентам исчерпывающую информацию о мемантинах различных производителей, чтобы они могли принять взвешенное решение о его приобретении.
Шаг первый. На апрель 2021 года в России фиксировались продажи 17 производителей мемантинов в коммерции (по данным IQVIA). Для начала исключаем из анализа мемантины, продажи которых составили менее 2000 упаковок в месяц по стране. То есть те, которые сложно найти в городах России.
Шаг второй. Тщательно анализируем сайт ГРЛС (Государственный реестр Лекарственных Средств) по критерию источника поставок субстанции.
Из 11 мемантинов 6 производителей имеют в своем составе субстанции индийского производства. У остальных были указаны только европейские субстанции. Вот «черный список» производителей, зарегистрировавших несколько стран поставщиков, в том числе индийские: Атолл (он же ОЗОН), Канон, Авексима, Акрихин, Изварино.
Использование индийской субстанции при производстве не говорит о плохом качестве препарата, но заставляет задуматься о стандартах, которые используются на производстве. Насколько они строги и соответствуют всем критериям безопасности? Все мы помним скандал с омепразолом из индийской субстанции, в котором была обнаружена примесь миноксидила, из-за чего у детей, принимавших препарат, развился гипертрихоз. Использование индийской субстанции в составе мы считаем скорее минусом, чем плюсом.
Шаг третий. Среди оставшихся 5 производителей, только 2 производят и субстанцию, и сами таблетки полностью в западной Европе. Таким образом у нас выявились два лидера: Акатинол-Мемантин от компании Мерц и препарат Меманталь от производителя Синтон Испания, представляемый в России компанией Сотекс.
Шаг четвертый. Проверяем наличие терапевтической эквивалентности оригинальному препарату.
Оригинальным мемантином является немецкий препарат Акатинол, то есть при сравнении эффективности другие производители должны ориентироваться на него как на эталон. Анализ поиска по научным статьям показывает, что единственным мемантином, доказавшим свою терапевтическую эквивалентность оригинальному препарату, является испанский Меманталь.
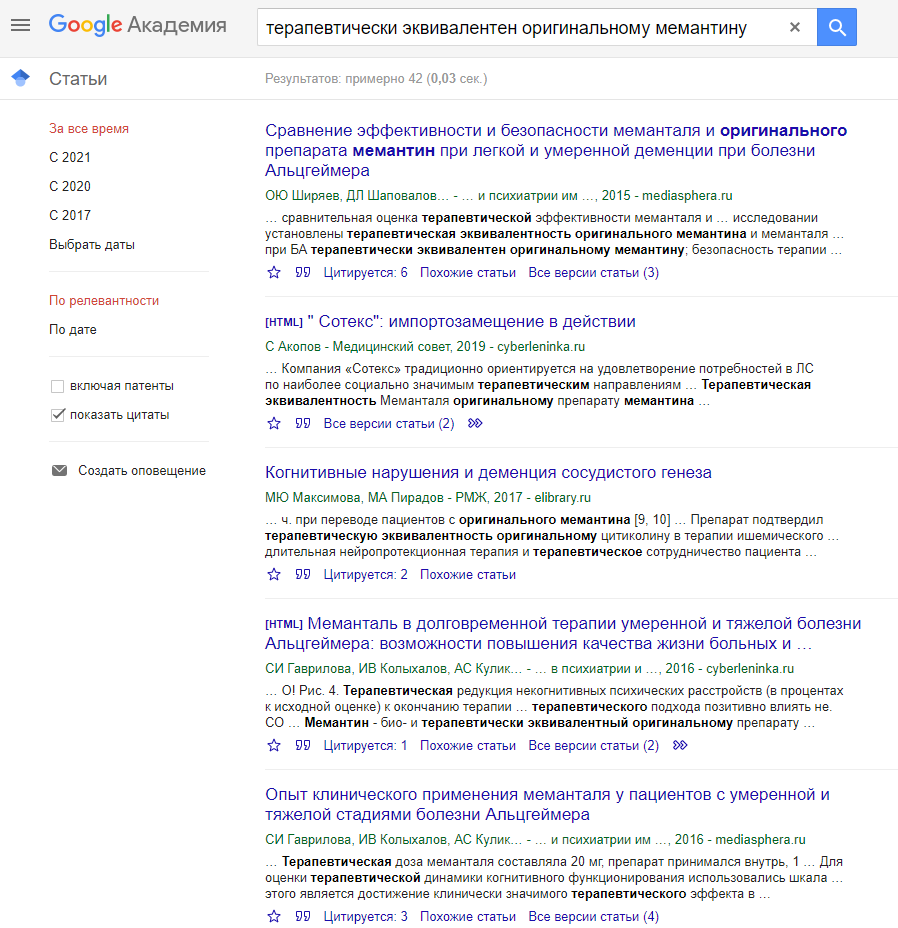
Шаг пятый. Проводим ценовой анализ по сайту аптека.ру на 21 июня 2021 года
|
Название |
Производитель |
Страна производства таблеток |
Наиболее экономичная форма выпуска (кол-во таб.) |
Дозировка, мг |
Цена за упак, по Аптека.ру |
Стоимость года терапии 20 мг/сут |
|
МЕМАНТАЛЬ® |
Синтон (Сотекс) |
ИСПАНИЯ |
90 |
10 |
1159 |
9401 |
|
Мемантин |
Авексима |
Россия |
90 |
10 |
1209 |
9806 |
|
Мемантин |
Рихтер |
Россия |
30 |
10 |
439 |
10682 |
|
Мемантин |
Вертекс |
Россия |
90 |
10 |
1365 |
11072 |
|
Мемантин |
Озон (Атолл) |
Россия |
90 |
10 |
1389 |
11266 |
|
МЕМАНТИНОЛ® |
Герофарм |
Россия |
90 |
10 |
1435 |
11639 |
|
Мемантин |
Акрихин |
Россия |
84 |
10 |
1465 |
12732 |
|
Мемантин |
Канон |
Россия |
90 |
10 |
1596 |
12945 |
|
Мемантин |
Фармзащита |
Россия |
90 |
20 |
3817 |
15480 |
|
МАРУКСА® |
КРКА-РУС |
Россия |
60 |
10 |
1300 |
15817 |
|
ТИНГРЕКС ® |
Гриндекс |
Латвия |
60 |
10 |
1338 |
16279 |
|
Мемантин |
Изварино |
Россия |
90 |
20 |
5502 |
22314 |
|
НООДЖЕРОН® |
Тева |
ИЗРАИЛЬ |
90 |
10 |
3117 |
25282 |
|
АКАТИНОЛ® |
Мерц |
ГЕРМАНИЯ |
98 |
20 |
8466 |
31532 |
Согласно этим данным, лидером стал препарат Меманталь (Синтон, производства Испания), как самый экономически выгодный для курсового применения.
Особенности приема мемантина при болезни Альцгеймера
Мемантин принимают внутрь в таблетках согласно следующему алгоритму:
- первая неделя – начальная доза 5 мг 1 раз в сутки утром
- вторая неделя – доза 10 мг/сут
- третья неделя – доза 15 мг/сут
- четвертая неделя и далее – доза 20 мг/сут
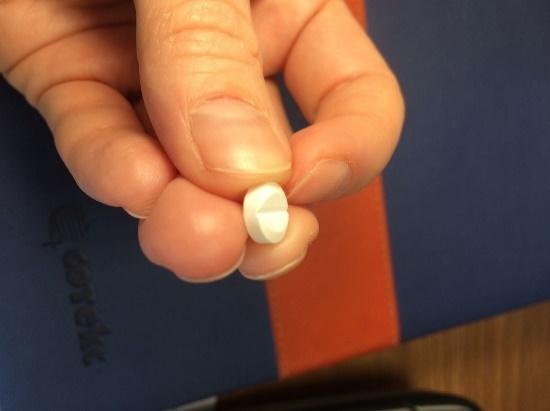
Для титрации мемантина очень важна хорошая делимость таблетки, поэтому на данный критерий тоже стоит обратить внимание при выборе препарата.
Прием терапевтической дозы 20 мг/сут может быть одномоментным утром, либо разделен на 2 приема по 10 мг (утром и днем). Предпочтителен первый вариант, так как это более удобно и снижает риск пропуска приема препарата.
Минимальная длительность лечения мемантином – 3 месяца. У пациентов с тяжелой или умеренно тяжелой деменцией при болезни Альцгеймера (MMSE 5–14 баллов) также может быть эффективна комбинация мемантина и донепезилом (1+, A).
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Вопросы врачам MedAboutMe
|
👍 0 👎 |
Достигнем ли мы положительного результата в лечении деменции?Бабушка 84 года деменция , путается в действиях , не помнит имена , и какие ноотропы можно применять с мемантином , в поликлинике не была всю свою жизнь на учёте ни с чем не стоит , плохоходячая в силу возраста 2749 #1 |
Ответы
|
👍 0 👎 |
Здравствуйте. Не стоит заниматься самолечением, это может не только не дать положительного результата, но и привести к ухудшению. Каждый препарат имеет показания и противопоказания, дозировка и схема приема так же должна подбираться индивидуально. То, что никогда не наблюдались, это зря, но никогда не поздно начать. Выявление и коррекция соматических заболеваний так же может оказать положительное влияние на когнитивные функции. Необходимо обратиться к терапевту, неврологу. В плане обследования общий и биохимический анализ крови, ЭКГ, УЗДС сосудов головы и шеи. По совокупности данных будет определена тактика. |
|
👍 0 👎 |
Здравствуйте. Вам необходимо начать с посещения врача-невролога. К сожалению, вылечить деменцию полностью не получится, однако можно существенно улучшить состояние Вашей бабушки, замедлить прогрессирование болезни. Однако лекарственная терапия может назначаться только после осмотра врачом, прохождения дополнительных обследований. Не затягивайте с посещением специалиста! |
Другие вопросы на схожие темы:
|
👍 0 👎 |
Деменция ли это? 5 ответовздравствуйте! Проблема такая. Свекровь перенесла ишемический инсульт, прошло 3 недели с момента выписки. Из-за короновируса реабилитационный центр пока закрыт, свекровь находится дома. Правая сторона тела восстановилась, она ходит, пишет, даже на одной ноге стоит.Но что-то происходит с ее сознанием. Думает, что идет в туалет, а приходит на балкон, не… |
20 продуктов для иммунитета: рекомендуют диетологи
Диетологи рекомендуют эти продукты для крепкого иммунитета и стройности
|
👍 −1 👎 |
Что можно сделать? 2 ответаЗдравствуйте. Помогите пожалуйста. Моей тёще 67 лет. Лет 5 назад началась небольшая забывчивость. Со временем немного усилилось. 2 года назад умерла её мама и она понемногу перестала занимается домашними делами. Когда у неё поднимается давление до 150 и выше становится злой начинает нести всякую ерунду вы меня не навидете вам нужна моя квартира и т.п.… |
|
👍 0 👎 |
Применение Полисорб для снижения креатинина, мочевины и побочные явления на головной мозг 2 ответаЗдравствуйте, Хочу спросить по поводу мамы. С осени 2001 года, в возрасте 86 лет, стала наблюдаться у нефролога. У нее ХПН, отекали ноги до этого тоже, но никогда не обращалась к врачам. Показатели у нее диализные, год назад пролежала в больнице два месяца, но на диализ не смогли ее перевести — она несознательно все выдергивает с кожи, включая катетеры.… |
Читайте также
Почему вам не хватает энергии? Витамины группы B — ключ к бодрости и ясному уму!
Хроническая усталость и постоянный туман в голове? Возможно, вашему организму не хватает витаминов группы B
Колики у малышей: полезные советы родителям
С коликами, так или иначе, сталкивается подавляющее большинство родителей совершенно здоровых малышей в раннем возрасте.
Малыш, родители и колики: как пережить 100 дней плача?
Часто первой проблемой, пугающей молодых родителей, становятся колики у малыша. Как помочь детям при боли в животике, читайте на MedAboutMe.
Что делать при порезах и ссадинах: советы
Незначительные порезы и царапины обычно не требуют поездки в отделение неотложной помощи. Тем не менее, надлежащий уход необходим, чтобы избежать инфекции или других осложнений.
20 продуктов для иммунитета: рекомендуют диетологи
Диетологи рекомендуют эти продукты для крепкого иммунитета и стройности
Когнитивные расстройства, или расстройства высших психических функций (табл. 1), — одно из самых распространенных и значимых проявлений поражения головного мозга [1]. Это не только индивидуальная проблема со здоровьем, которая может привести к быстрой и полной инвалидизации пациента, но и тяжелое социальное бремя.
Таблица 1
Когнитивные функции [1]

Более 35 миллионов человек во всем мире в настоящее время живут с деменцией [2]. Распространенность легких, а также умеренных (додементных) когнитивных расстройств (УКР) в разы превышает указанное значение, ее сложно оценить из-за недостаточной диагностики и низкой обращаемости к врачу по поводу данной проблемы. Возраст считается главным фактором риска возникновения когнитивных расстройств: к 65 годам распространенность УКР в популяции достигает 12–15%, с каждым следующим годом она увеличивается на 1% [3]. В связи с общим старением населения Земли прогнозируется, что каждые 20 лет количество больных деменцией будет удваиваться [2].
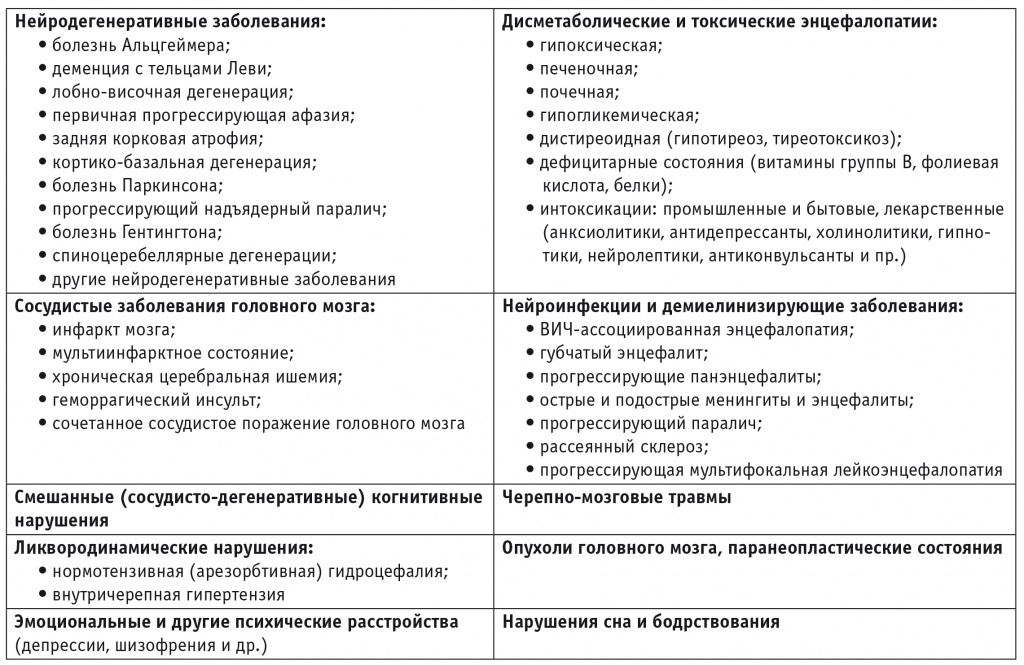
Широкая представленность когнитивных расстройств связана также с множественной этиологией: насчитывается более 100 причин их возникновения (табл. 2), среди них наиболее распространенными являются нейродегенеративные и цереброваскулярные заболевания [4].
Таблица 2
Основные причины когнитивных нарушений [4]
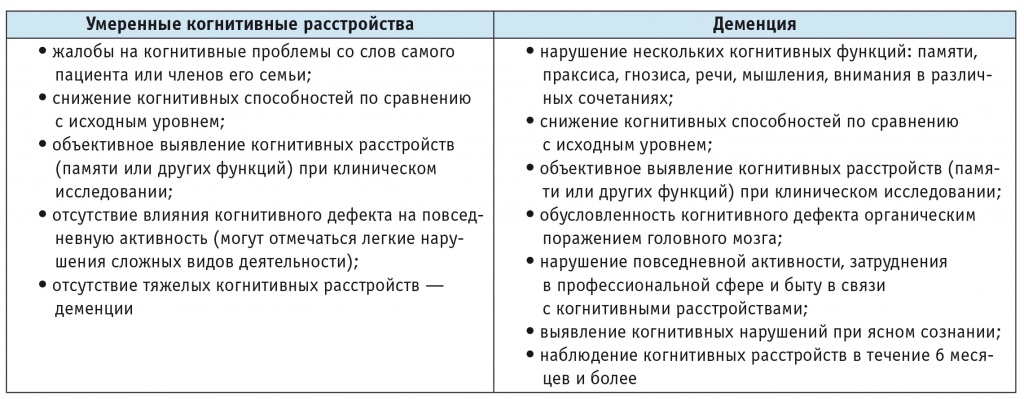
В большинстве случаев когнитивные нарушения нарастают постепенно, какое-то время не снижают социальной и бытовой адаптации человека и не сразу замечаются пациентом и его окружением. Такие нарушения выделяются в отдельный синдром УКР (табл. 3) [1]. Главным отличием УКР от деменции является наличие у пациента возможности независимого функционирования в быту и профессиональной сфере. Выделение УКР в отдельную нозологическую единицу имеет принципиальное значение, поскольку тактика лечения и прогноз при них отличаются от таковых при деменции.
Таблица 3
Основные критерии диагностики умеренных когнитивных расстройств и деменции [1]
Чаще всего когнитивные нарушения, достигшие степени деменции, необратимы: только около 5% случаев деменции регрессируют при своевременном обнаружении и терапии [1]. Основными причинами обратимых когнитивных расстройств являются соматические заболевания (печеночная, уремическая энцефалопатия, эндокринная патология, дефицитарные состояния, алкоголизм, инфекции и пр.). Эти заболевания, многие из которых встречаются прежде всего в практике врача-терапевта, требуют особого внимания в плане своевременной диагностики и предупреждения развития необратимых повреждений головного мозга.
Прогноз УКР менее однозначен: у 5–15% пациентов с УКР в течение года развивается деменция, треть из них умирают в течение шести последующих лет (чаще всего от сопутствующей соматической, прежде всего сердечно-сосудистой, патологии), однако у 20% пациентов с УКР при последующем наблюдении отмечается улучшение когнитивных функций [5]. Диагностика когнитивных расстройств на ранних стадиях позволяет своевременно начать адекватную терапию и тем самым продлить активную жизнь пациента [6].
В настоящее время не существует способа предотвратить или затормозить развитие нейродегенерации, в том числе наиболее распространенной причины деменции — болезни Альцгеймера (БА), — который имел бы доказанную эффективность. Большие надежды возлагаются на коррекцию сосудистых факторов риска и профилактику развития сосудистых когнитивных нарушений. Особое значение придается контролю артериальной гипертензии: установлена статистически значимая взаимосвязь между исходно высокими цифрами систолического давления (180 мм рт. ст. и выше) и развитием тяжелых когнитивных расстройств; с каждым повышением системного артериального давления на 10 мм рт. ст. риск развития когнитивных нарушений возрастает на 7–16%; выраженность когнитивных расстройств зависит от наличия адекватной и постоянной гипотензивной терапии [7]. Надо отметить, что сосудистые факторы риска, такие как гипертоническая болезнь сердца, нарушения сердечного ритма, гиперлипидемия, ожирение, сахарный диабет и пр., провоцируют развитие когнитивных расстройств не только сосудистого, но и нейродегенеративного характера.
Основная цель терапии когнитивных расстройств на сегодняшний день состоит в том, чтобы как можно дольше поддерживать бытовую независимость пациента и отсрочить полную инвалидизацию.
К общим принципам терапии УКР и деменции относятся:
- отмена или минимизация доз средств, ухудшающих когнитивные функции (седативных препаратов, холинолитиков и пр.);
- коррекция сопутствующих заболеваний и факторов риска (сосудистых, аффективных, дисметаболических и других нарушений);
- нейропсихологическая реабилитация, т. е. создание когнитивного резерва, когнитивный тренинг (умственная и физическая активность, социальные контакты, эмоциональная жизнь);
- выбор препарата, улучшающего когнитивные функции;
- длительная терапия с обязательной оценкой ее эффективности.
Общепринятых рекомендаций по специфической фармакотерапии УКР до настоящего времени не разработано, поэтому выбор терапевтической тактики в отношении них всегда сопряжен с определенными трудностями. Препараты, наиболее часто применяемые в клинической практике, представлены в таблице 4.
Таблица 4
Препараты (группы препаратов), применяемые для терапии когнитивных нарушений
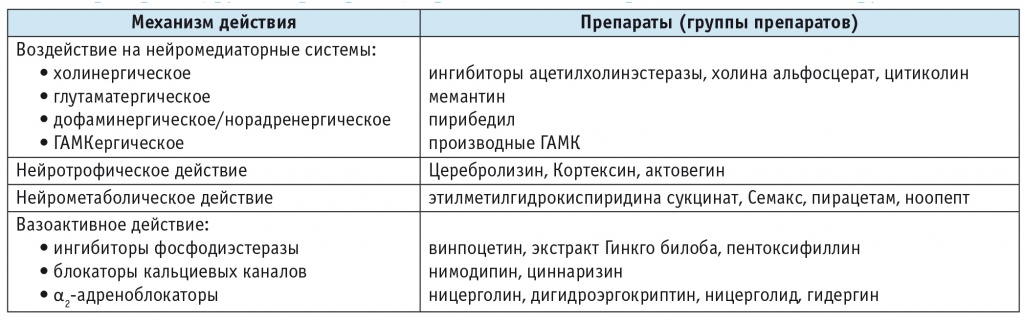
Фармакотерапия деменций основывается на применении двух групп препаратов с доказанной клинической эффективностью: ингибиторов ацетилхолинэстеразы (АХЭ) и антагонистов NMDA-рецепторов к глутамату. Поскольку дисбаланс холинергической системы и феномен эксайтотоксичности (разрушение нервных клеток в результате сверхраздражения) характерны для разных деменций, препараты данных групп широко используются в клинической практике как в виде монотерапии, так и в комбинации. При наличии клинического эффекта и отсутствии противопоказаний лечение проводится пожизненно.
Препараты, модулирующие глутаматергическую передачу, считаются перспективными в плане коррекции когнитивных нарушений различной степени тяжести и этиологии, поскольку патологические механизмы с дисрегуляцией глутамата постоянно участвуют в развитии наиболее частых форм деменции — нейродегенеративной, сосудистой и смешанной.
Глутамат — один из основных возбуждающих медиаторов головного мозга, особенно широко представленный в коре и гиппокампе (областях, непосредственно связанных с когнитивными функциями). Дисрегуляция с локальным повышением концентрации глутамата производит нейротоксический эффект. Накопление глутамата в синапсах связано с нарушением его обратного захвата пресинаптическими нейронами и/или глиальными клетками. Повышенный уровень медиатора приводит к росту постоянной фоновой активации нейронов — так называемого фонового шума (рис. 1А), — что мешает распознавать физиологически нужные сигналы и нарушает когнитивные процессы. Аномальное накопление глутамата в синапсах ведет к постоянной стимуляции NMDA-рецепторов и хронической деполяризации мембраны с избыточным поступлением кальция в клетку, тем самым запускается каскад патологических реакций (рис. 2), заканчивающихся гибелью клетки (феномен эксайтотоксичности) [8].
Рис. 1. Глутаматопосредованная нейропередача в норме (А) и при патологии (при избытке глутамата) с защитным действием мемантина (Б)
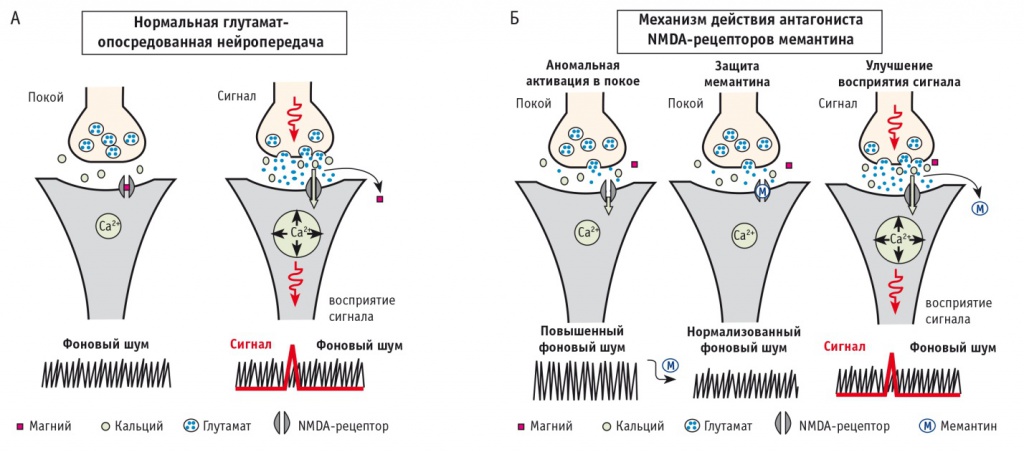
Рис. 2. Механизмы глутаматопосредованной эксайтотоксичности [8]
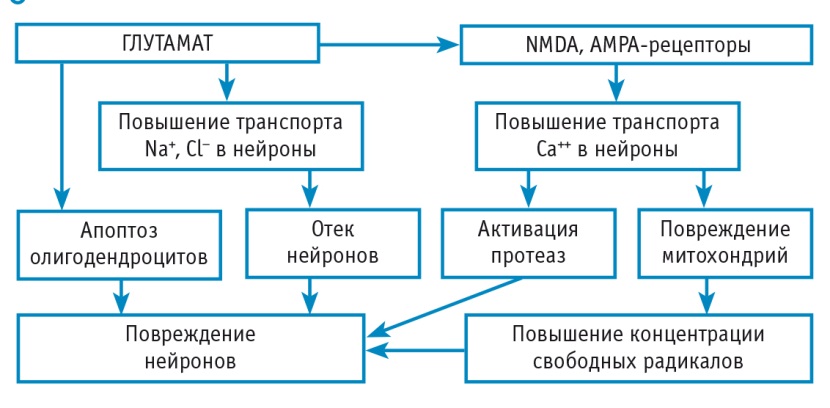
Избыточная стимуляция NMDA-рецепторов особенно вредна в условиях энергодефицита в клетке, например при ишемии. Известно, что активирующая активность L-глутамата играет значимую роль в патогенезе БА и ишемического повреждения при инсульте.
Предотвратить нейротоксическое действие возбуждающих аминокислот возможно с помощью антагонистов NMDA-рецепторов, при этом препарат должен обладать невысокой аффинностью, которая позволит действовать без вмешательства в физиологические эффекты глутамата, необходимые для осуществления процессов памяти и обучения [9].
Мемантин является неконкурентным потенциалзависимым антагонистом NMDA-рецепторов с низкой и средней аффинностью. Он связывается преимущественно с открытыми кальциевыми каналами (рис. 1Б), управляемыми NMDA-рецепторами, в состоянии покоя [10, 11] и блокирует поток ионов, уменьшая негативное влияние патологически повышенного уровня глутамата [12]. При полной деполяризации мембраны мемантин удаляется из канала, что обеспечивает нормальную синаптическую передачу. Соотношение сигнала и шумового фона при этом восстанавливается [5]. Таким образом, мемантин может препятствовать гибели клетки, т. е. оказывать нейропротекторное действие.
Доклинические исследования мемантина на клеточных культурах продемонстрировали следующие нейропротекторные свойства:
- предотвращение гибели корковых, гиппокампальных, мезэнцефальных и мозжечковых нейронов, вызываемой токсическим действием глутамата (показано на культурах);
- защита холинергических нейронов от повреждения, связанного с эксайтотоксическим эффектом, действием β-амилоида, митохондриальной дисфункцией и нейровоспалительным процессом;
- уменьшение аномального гиперфосфорилирования τ-протеина и препятствие образованию нейрофибриллярных клубочков, характерных для БА [13].
Эффективность мемантина при БА, сосудистой и смешанной деменции оценивалась в большом ряде клинических исследований, проведенных на оригинальном препарате.
Часть из этих работ вошла в метаанализ Кокрейна (12 рандомизированных контролируемых исследований, 2006 г.) [14], который показал превосходство мемантина над плацебо при терапии БА от легкой до умеренной и от умеренной до тяжелой степени тяжести (использовалась шкала для оценки нарушений при болезни Альцгеймера — когнитивная подшкала, англ. Alzheimerʹs Disease Assessment Scale — cognitive subscale, ADAS-cog [15]). При этом клинический эффект при сосудистой деменции существенно не отличался от такового при плацебо.
В 2015 г. был проведен метаанализ, включивший более новые исследования эффективности и безопасности монотерапии мемантином при БА [16]. В него вошли 9 рандомизированных плацебо-контролируемых исследований с участием 2433 пациентов (табл. 5) [17–25]. На основании статистически значимых данных было установлено, что мемантин:
- замедляет прогрессирующее снижение когнитивных возможностей (в том числе внимания, узнавания, речи, зрительно-пространственных функций);
- снижает степень выраженности деменции;
- повышает повседневную активность пациентов;
- улучшает общее состояние больных;
- эффективен в отношении поведенческих нарушений (уменьшает выраженность и частоту возникновения ажитации, агрессии, психозов);
- обладает хорошей переносимостью (процент отказа от лечения, количество и выраженность нежелательных явлений при применении мемантина сопоставимы с результатами в группах плацебо).
Таблица 5
Исследования эффективности и безопасности монотерапии мемантином (20 мг/день) при болезни Альцгеймера
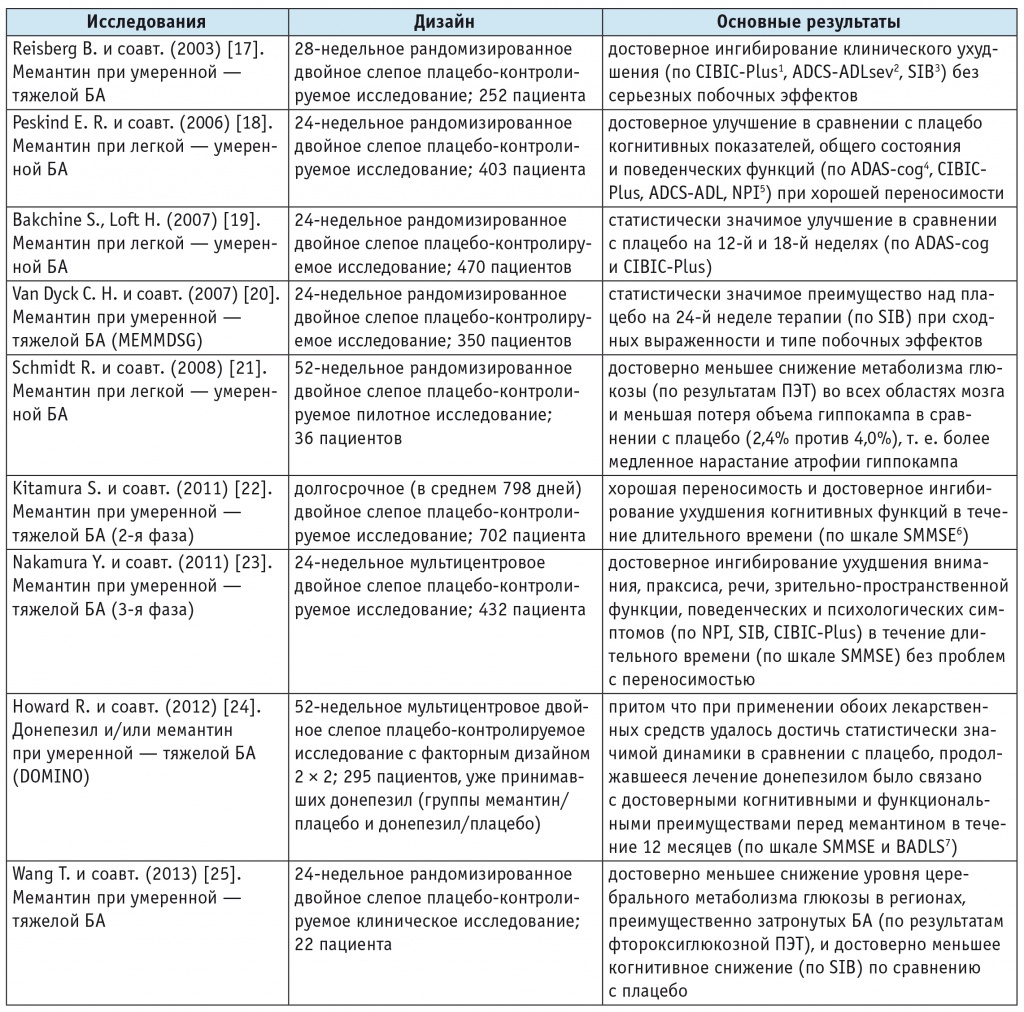
1 Clinician`s Interview-Based Impression of Change Plus Caregiver Input — шкала для оценки клиницистом и опекуном динамики состояния больного.
2 Alzheimer`s Disease Cooperative Study — Activities of Daily Living inventory modified for severe dementia — шкала для оценки повседневной активности при болезни Альцгеймера, модифицированная для тяжелой деменции.
3 Severe Impairment Battery — шкала для оценки тяжести нарушений.
4 Alzheimer`s Disease Assessment Scale — cognitive subscale — шкала для оценки нарушений при болезни Альцгеймера — когнитивная подшкала.
5 Neuropsychiatric Inventory — нейропсихиатрическое обследование.
6 Standardized Mini-Mental State Examination (SMMSE) — стандартизированная краткая шкала оценки психического статуса.
7 Bristol Activities of Daily Living Scale — Бристольская шкала оценки повседневной жизненной активности.
Примечание. БА — болезнь Альцгеймера; ПЭТ — позитронно-эмиссионная томография.
Эти данные согласуются с результатами множества работ, не вошедших в метаанализ [26–30]. Терапевтический эффект сохраняется длительное время — в долгосрочном исследовании средняя продолжительность лечения составляла 798 дней [22]. С клинической точки зрения выраженность положительного эффекта оказалась не слишком высокой. Тем не менее, поскольку механизм действия мемантина отличается от такового у ингибиторов АХЭ, ожидается, что он будет эффективен у пациентов со слабым действием ингибиторов АХЭ и расширит терапевтические возможности для пациентов с БА.
На основании проведенного анализа [16] сделан вывод о том, что мемантин можно эффективно использовать в качестве монотерапии БА, а также при отсутствии или неадекватном эффекте терапии ингибиторами АХЭ, при непереносимости последних и наличии противопоказаний к их назначению (например, при нарушении проводимости сердца или синдроме слабости синусового узла). В настоящее время препарат официально одобрен Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (англ. Food and Drug Administration, FDA) для лечения БА средней и тяжелой степени тяжести.
Наибольший опыт применения мемантина накоплен у пациентов с умеренной и тяжелой БА, однако ряд исследований свидетельствует о его эффективности на ранних стадиях [18, 19, 21], что открывает новые перспективы для применения препарата у пациентов с УКР.
Эффективность мемантина в терапии УКР активно изучается, исследования затрудняются гетерогенностью и вариабельностью течения данных расстройств. В ряде открытых клинических испытаний [31, 32] показана способность мемантина улучшать состояние когнитивных функций при УКР. По данным российских авторов, на фоне лечения мемантином у пациентов с УКР амнестического типа отмечается не только стабилизация когнитивной дисфункции, но и положительная динамика нейрохимического маркера нейродегенерации β-амилоида [32], что свидетельствует о возможности влияния при применении этого препарата на нейродегенеративные процессы. Необходимы дальнейшие исследования эффективности мемантина и его нейропротективных возможностей у пациентов с УКР. Вопрос о целесообразности назначения мемантина при УКР остается открытым и решается индивидуально для каждого пациента. При высоком риске конверсии УКР в деменцию применение мемантина может быть вполне оправданным [5].
Эффективность мемантина в терапии сосудистых когнитивных нарушений, как отмечено выше, не столь очевидна, как при БА. Исследований применения мемантина по данному показанию значительно меньше. Препарат был протестирован в двух плацебо-контролируемых исследованиях у пациентов с сосудистой деменцией при 28-недельном периоде лечения [33, 34]. В первом исследовании у 321 пациента лечение мемантином привело к лучшим по сравнению с плацебо показателям шкалы ADAS-cog (разница в 2,0 балла), но статистически значимых различий по шкале клинического впечатления (шкала для оценки клиницистом и опекуном динамики состояния больного, англ. Clinicianʹs Interview-Based Impression of Change Plus Caregiver Input, CIBIC-Plus) не обнаружилось (60% против 52%) [33]. Во втором исследовании у 579 пациентов лечение мемантином привело к лучшим, чем при применении плацебо, показателям ADAS-cog (разница в 1,8 балла, p < 0,001), но различий по шкале CIBIC-Plus опять-таки получено не было [34]. Результаты этих двух клинических исследований были объединены и подтверждены в рамках Кокрейновского метаанализа [14]. Надо отметить, что эффективность ингибиторов АХЭ при терапии сосудистых когнитивных нарушений также недостаточна и значительно ниже, чем при БА, что по сей день вызывает споры о целесообразности применения этих лекарственных средств при чисто сосудистой деменции [35].
Комбинированная терапия мемантином и ингибиторами АХЭ, по некоторым данным, дает максимально выраженный положительный эффект. Нежелательных взаимодействий между препаратами не возникает. Наоборот, в доклинических испытаниях показано, что антагонист NMDA-рецепторов и ингибиторы АХЭ действуют синергично, чем можно объяснить повышение их клинической эффективности, наблюдаемое при совместном применении [36, 37]. Обычно данная комбинация препаратов назначается при недостаточной эффективности монотерапии или снижении клинического эффекта в силу прогрессирования заболевания. При наблюдении с 1983 по 2004 г. за 943 пациентами с БА было показано, что добавление мемантина к терапии ингибиторами АХЭ изменяет клиническое течение болезни, значительно удлиняя период до госпитализации, т. е. дает возможность больному дольше оставаться дома. Пациенты, находившиеся на комбинированной терапии, демонстрировали более высокие когнитивные и функциональные возможности по сравнению с группой монотерапии, и сиделкам было проще за ними ухаживать. К сожалению, данных об увеличении продолжительности жизни при комбинированном лечении получено не было [38]. К таким же выводам пришли ученые в ряде коротких (от 12 до 24 месяцев) исследований [39, 40], однако требуется более длительное наблюдение, чтобы в полной мере оценить эффективность и перспективы комбинированного лечения. В настоящее время активно ведутся разработки новых молекул, сочетающих в себе антагонизм NMDA-рецепторов и усиление холинергической активности посредством ингибирования АХЭ [41].
Тактика назначения мемантина. В настоящее время практикуется однократный прием полной дозы мемантина, длительный период полужизни препарата позволяет следовать этой тактике без потери эффективности при высокой комплаентности и сохранении хорошей переносимости.
Титрация дозы мемантина стандартна:
- 1-я неделя — 5 мг (1 табл.) утром;
- 2-я неделя — 10 мг утром;
- 3-я неделя — 15 мг утром;
- 4-я неделя и далее постоянно — 20 мг утром.
При необходимости через несколько месяцев терапии дозу можно увеличить до 30 мг в день [5]. Оценка клинического эффекта должна осуществляться через 2–3 месяца после назначения и производиться с учетом динамики не только когнитивных, но и функциональных, поведенческих нарушений.
Мемантин обычно хорошо переносится пациентами. Он более безопасен в использовании, чем препараты группы ингибиторов АХЭ, что подтверждено FDA на основе клинических данных с помощью статистической системы оценки неблагоприятных событий [42].
Мемантин не влияет на частоту сердечных сокращений, может применяться в терапевтических дозах у пациентов с заболеваниями почек, печени, редко вызывает желудочно-кишечные расстройства. Поскольку мемантин может оказывать легкое психостимулирующее действие, его не рекомендуется назначать на ночь [3].
ЗАКЛЮЧЕНИЕ
Когнитивные расстройства в настоящее время являются одной из наиболее распространенных и значимых проблем в неврологии. Количество пациентов с данной патологией растет из года в год, и они требуют максимально ранней диагностики и лечения, включающего применения нелекарственных методов и постоянной медикаментозной терапии.
Существуют различные подходы к ведению пациентов с умеренными когнитивными расстройствами и деменцией. Для деменций терапией выбора на сегодняшний день являются ингибиторы ацетилхолинэстеразы и антагонисты NMDA-рецепторов, в частности мемантин. Эффективность мемантина у пациентов с деменцией доказана в ходе множества доклинических и клинических исследований: он способен замедлять прогрессирующее снижение когнитивных возможностей и уменьшать степень его выраженности, улучшать общее состояние и повседневную активность пациентов, а также снижать частоту и выраженность поведенческих нарушений. Благодаря доказанной эффективности и хорошей переносимости мемантин рекомендуется для лечения деменций как в качестве монотерапии, так и в сочетании с препаратами группы ингибиторов ацетилхолинэстеразы.
« Назад
РЕЗУЛЬТАТЫ КЛИНИЧЕСКОГО НАБЛЮДЕНИЯ ПО ПРИМЕНЕНИЮ ПРЕПАРАТА МЕМАНТИН ПРИ ЛЕЧЕНИИ ДЕМЕНЦИИ 25.10.2019 14:21
Одной из наиболее актуальных проблем современной неврологии и психиатрии является лечение деменции, частота встречаемости которой у лиц пожилого возраста весьма высока и имеет тенденцию к дальнейшему росту. Традиционно поиски адекватных терапевтических средств для лечения деменции в основном были сосредоточены на различных способах коррекции холинергической недостаточности в корковых и иных отделах головного мозга (использование предшественников ацетилхолина, ингибиторов аце-тилхолинэстеразы). В последние годы большое внимание уделяется изучению роли глугаматергических систем мозга в патогенезе деменции. В результате был предложен и стал широко применяться низкоаффинный неконкурентный антагонист NMDA-ре-цепторов и агонист NMDA-рецепторов глугамата — Мемантин.
Механизм действия Мемантина является комплексным и заключается как в предотвращении эксайтотоксич-ности (нейропротективный эффект), так и в положительном влиянии на процессы обучения и запоминания. Противодементное действие Мемантина обусловлено его магнийподоб-ным эффектом, который заключается в блокировании патологической им-пульсации (подавление “шума”), в то время как физиологические стимулы в структурах, связанных с мышлением ипамятью, продолжают активировать рецепторы.
Мемантин применяется с 1976 г. в Германии и европейских странах в основном для лечения двигательных нарушений (детский церебральный паралич, паркинсонизм). В последнее время
Мемантин стали активно использовать в терапии болезни Альцгеймера. Среди работ, выполненных в США по данной проблеме, выделяется обстоятельное многоцентровое двойное слепое плацебоконтролируемое исследование эффективности Мемантина у 252 пациентов со среднетяжелой формой болезни Альцгеймера из32 центров: было показано улучшение клинической картины и, в частности, улучшение показателей когнитивной сферы по шкалам CIBIC-Plus, ADCS-ADLsev и теста SIB (Severe Impairment Battery). Ряд других авторов провели оценку эффективности и безопасности Мемантина у пациентов с мягкой и умеренной сосудистой деменцией. Так, J.M. Orgogozo etal. (2002) обнаружили, что Мемантин в дозе 20 мг/сут после 28-недель-ного применения приводил к значительному улучшению познавательных способностей по данным шкал MMSE, CIBIC-Plus, ADAS-cog; при этом побочные эффекты были незначительны и сравнимы с группой плацебо. Опубликованы результаты исследований, в которых отмечается положительный эффект использования Мемантина для лечения постабстинентных расстройств (синдрома ангедонии) у больных героиновой наркоманией.
Выполнены работы по фармакоэко-номическим аспектам применения Мемантина. Так, например,
на выборке из 166 пациентов с болезнью Альцгеймера показано, что на фоне улучшения клинического состояния в группе больных отмечается снижение общих экономических расходов по сравнению с группой плацебо — на сумму 823,77 доллара США в месяц.
Следует отметить, что абсолютное большинство работ по анализу эффективности Мемантина выполнено на примере пациентов с болезнью Альцгеймера, имеющих различную степень тяжести когнитивных нарушений. При сосудистой деменции (СД) такие исследования единичны. В связи с этим целью настоящей работы была оценка терапевтического действия Мемантина на выборке больных с легкой и умеренной СД, определяемой по шкале ^С. Могпб.
Материал и методы исследования
Нами обследованы 17 больных (9 мужчин, 8 женщин) в возрасте 54-77 лет, соответствующих критериям сосудистой деменции. У 10 пациентов (7 мужчин, 3 женщин) была установлена легкая степень деменции, у 7 (2 мужчин, 5 женщин) — умеренная деменция (таблица).
Основной диагноз у обследованных пациентов — дисциркуляторная энцефалопатия П-Ш стадии на фоне церебрального атеросклероза (изолированного или в сочетании с артериальной гипертензией). У части больных в анамнезе имели место перенесенные острые нарушения мозгового кровообращения. Больным проводили базовую патогенетическую терапию в соответствии с основным заболеванием.
Исследование проводилось по четкому формализованному протоколу. На первом этапе ставился предварительный диагноз деменции по доказательной унифицированной схеме с перечнем ключевых симптомов (нарушения памяти, длительность симптомов не менее 6 мес, хроническое прогрессирующее течение и др.)-по критериям. Затем определя-
лась причинная (временная) связь между наличием деменции и сосудистым поражением головного мозга. Окончательный диагноз СД устанавливали с помощью шкалы Хачинского — при наличии 7 баллов и выше (в среднем 12-14), а также соответствующих данных МРТ-визуализации (наличие атрофии мозга, множественных инфарктов и т.д.). При этом обязательным было исключение из исследования болезни Альцгеймера и деменции, обусловленной единичными инфарктами в стратегически значимых зонах мозга. Все испытуемые проходили предварительное обследование по специальной тестирующей шкале ММЭЕ [8] с целью определения степени когнитивных нарушений.
Процедура тестирования по шкале ММЭЕ повторялась трижды с интервалом в 1 мес. Во время всех посещений параллельно проводили оценку динамики общего состояния и когнитивной сферы на основании комплекса параметров (памяти, ориентировки, суждений, логики, социального взаимодействия, повседневной активности, самообслуживания). Использовались по-луколичественные оценки: —
■ Легкая деменция
■ Все пациенты
■ Умеренная деменция
ухудшение, “0” — без динамики, “+” -улучшение, “++” — значительное улучшение; на основании этих оценок специалист давал итоговое заключение об эффективности терапии.
Математическая оценка результатов исследования проводилась с использованием пакета программ Statistica 5.0.
Все больные на протяжении 3 мес получали препарат Меман-тин в конечной дозировке 20 мг/сут.
Результаты и обсуждение
Однонаправленные позитивные изменения наблюдались как в целом по группе, так и в отдельных подгруппах больных -т.е. в равной степени у пациентов с легкой и умеренной степенью деменции. Наиболее четкие изменения касались первых двух пунктов (ориентировка во времени и в местонахождении), а также величины суммарной оценки (общего балла).
Важно отметить, что уже на промежуточных этапах исследования (оценки MMSE во время первого и второго посещений) наблюдалось улучшение отдельных когнитивных параметров
и увеличение общего балла шкалы.
При анализе интегральных полу-количественных оценок общего состояния и когнитивной сферы было отмечено повышение социальной адаптации пациентов, имевшее место на фоне улучшения мнестических способностей и концентрации внимания.
В течение всего курса лечения Мемантином каких-либо изменений со стороны соматического статуса и клинических лабораторных показателей отмечено не было. Лишь в 2 случаях на 2-м и 3-м месяце лечения наблюдались побочные эффекты в виде изменений психического состояния (фобии, депрессивные эпизоды), связь которых с проводимой терапией не вполне очевидна; в этих случаях снижение дозировки (до 10 мг/сут) и симптоматическое лечение в течение нескольких дней позволили полностью купировать возникшие нарушения.
Общая характеристика обследованных больных
Группы больных
Характеристики легкая деменция умеренная деменция всего
Количество больных 10 7 17
Средний возраст 65 69 67
(54-77 лет) Пол
мужской 7 2 9
женский 3 5 8
Возраст начала заболевания
до 60 лет 3 4 7
до 65 лет 4 1 5
65 лет и старше 3 2 5
Таким образом, полученные нами данные, свидетельствующие о положительном терапевтическом эффекте Мемантина при мягкой и умеренной СД, хорошо согласуются с результатами ранее проведенных работ аналогичного профиля у данной категории больных. Полученные результаты о степени влияния препарата на когнитивную сферу сопоставимы и с результатами работ по влиянию Мемантина на деменцию альцгеймеровского типа. Интересно отметить, что при болезни Альцгеймера доля случаев с улучшением когнитивных функций на фоне применения Мемантина при легкой деменции в 1,3 раза выше, чем при умеренной (соответственно, 100 и 77,8%); при этом общее число больных с позитивным лечебным эффектом составляет 83,3%.
Согласно нашему опыту, препарат хорошо переносится больными, что
также подтверждается данными литературы.
Применение теста ММЭЕ для оценки тяжести когнитивных нарушений при дисциркуляторной энцефалопатии рекомендовано рядом авторов, в том числе Н.Н. Яхно и др. (2001), и проведенное нами исследование может служить подтверждением надежности и адекватности данного метода в условиях длительного клинического испытания.
В перспективе мы предполагаем проанализировать взаимосвязь лечебного действия препарата с половыми, возрастными факторами и разнообразной сочетанной патологией.
