Октреотид инструкция по применению, дозировка и побочные эффекты
Черенёва Анастасия Дмитриевна
20 декабря 2021

ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ. ВОЗМОЖНЫ ПОБОЧНЫЕ ЭФФЕКТЫ. НЕОБХОДИМА КОНСУЛЬТАЦИЯ СПЕЦИАЛИСТА.
Автор статьи
Черенёва Анастасия Дмитриевна
,
Профессия: провизор
Название вуза: Пермская государственная фармацевтическая академия (ПГФА)
Специальность: провизор- технолог. Интернатура на кафедре фармацевтическая технология лекарственных средств.
Стаж работы: 10 лет
Диплом о фармацевтическом образовании: 105924 1197961, рег. номер 30504
Места работы: провизор в аптеке, заведующая аптекой, провизор сервиса Мегаптека
Все авторы
Содержание
- Особенности и механизм действия октреотида
- Инструкция к применению «Октреотида»
- «Октреотид» при панкреатите: поможет ли?
- Противопоказания и побочные действия лекарства
- Октреотид побочные действия
- Терапевтическая дозировка «Октреотида»
Утром наше тело выше, а к вечеру становится на пару сантиметров короче. Это происходит из-за гравитации. В течение дня под ее воздействием сокращается расстояние между позвонками. Такой процесс является нормой.
Рост человека регулируется гормоном соматотропином. Под его влиянием мы растем вверх и набираем мышечную массу. Но иногда этого гормона слишком много. Для подавления его избытка используют соматостатин — искусственно полученный антагонист гормона роста. Рассказываем о препарате соматостатина «Октреотид».
Особенности и механизм действия октреотида
Активным веществом препарата «Октреотид» выступает одноименный компонент – октреотида ацетат. Лекарство выпускается в форме раствора для внутривенных и подкожных инъекций. Вспомогательными компонентами служат очищенная вода и хлорид натрия.
Основное действующее вещество обладает родством с естественным гормоном соматостатином, и относится к группе синтетических октапептидов. Он несет те же эффекты, но отличается более продолжительным действием.
«Октреотид» блокирует избыточную продукцию гормона роста, вне зависимости от этиологии нарушения. Препарат одинаково хорошо действует и при патологически повышенной секреции соматотропина, и при избыточной продукции гормона роста, опосредованной высокими физическими нагрузками, инсулиновой гипогликемией и аргинином.
Помимо этого, «Октреотид» несет следующие эффекты:
- снижает секрецию гормона тиреотропина, который стимулирует выработку гормонов щитовидной железы;
- подавляет выработку инсулина, гастрина и серотонина (в случаях патологического повышения);
- сокращает концентрацию гормона роста в плазме крови у пациентов с акромегалией;
- улучшает состояние пациентов с секретирующими опухолями ЖКТ и поджелудочной железы, карциноидными опухолями, глюкагономами, инсулиномами и другими опухолями;
- снижает частоту осложнений после операций на поджелудочной железе.
Это позволяет применять лекарство при различных гормональных заболеваниях и эндокринных опухолях внутренних органов.
Инструкция к применению «Октреотида»
Ключевым показанием к применению «Октреотида» является акромегалия. Препарат снижает уровни соматотропного гормона и инсулиноподобного фактора роста в крови, помогая контролировать развитие заболевания. Его также назначают пациентам, в отношении которых неэффективны хирургические вмешательства и лучевая терапия. «Октреотид» широко применяют в случаях, когда операции противопоказаны, а также между сеансами лучевой терапии до достижения ее стабильного эффекта.
«Октреотид» оказывает симптоматическое действие в отношении следующих эндокринных опухолей желудочно-кишечного тракта и поджелудочной железы:
- глюкагономы;
- ВИПомы;
- гастриномы;
- ульцерогенные аденомы поджелудочной железы;
- карциноидные опухоли;
- инсулиномы;
- соматолибериномы.
Обратите внимание, что «Октреотид» не относится к противоопухолевым препаратам и не способен излечить больных с перечисленными патологиями. Лекарство только контролирует и предупреждает симптомы данных заболеваний.
«Октреотид» используют в сочетании с эндоскопической склерозирующей терапией варикозного расширения вен в органах ЖКТ у пациентов с циррозом печени. Такой подход позволяет существенно сократить вероятность внутрибрюшных кровотечений.
При кишечных свищах «Октреотид» могут применять для снижения секреции желудочно-кишечного тракта и контроля их выхода. Но клинически эффективность такого метода не доказана. Кроме того, он грозит потенциальным риском развития побочных эффектов.
«Октреотид» при панкреатите: поможет ли?
Панкреатит не является показанием к применению препарата. «Октреотид» используют с целью профилактики осложнений после операций на поджелудочной железе.
Противопоказания и побочные действия лекарства
«Октреотид» противопоказан людям со следующими заболеваниями:
- индивидуальная непереносимость октреотида или любых других компонентов в составе;
- период лактации;
- детский и подростковый возраст (младше 18 лет).
Препарат с осторожностью назначают при сахарном диабете и желчнокаменной болезни.
Относительным ограничением являются периоды беременности и лактации. Влияние лекарства на плод при беременности недостаточно изучено, поэтому терапию назначают только в исключительных случаях, когда предполагаемая польза для матери выше потенциальных рисков для плода. Если лечение потребовалось во время лактации, грудное вскармливание следует прекратить.
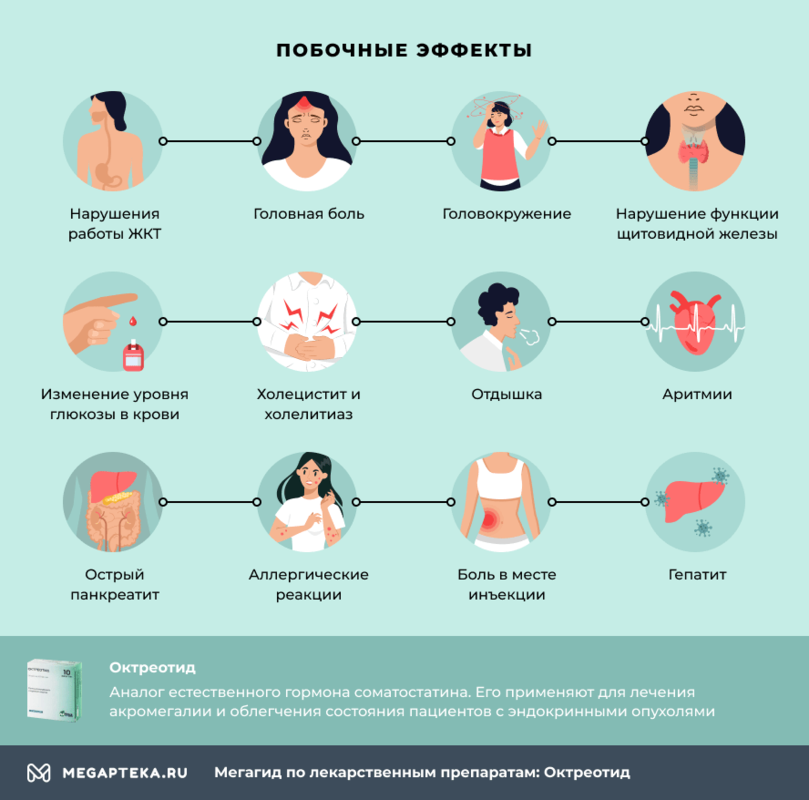
Среди побочных эффектов лечения «Октреотидом» часто встречаются следующие нарушения:
- нарушения работы ЖКТ: диарея, боль в животе, тошнота, рвота, запор, вздутие;
- головная боль и головокружение;
- гипотиреоз и нарушение функции щитовидной железы;
- повышение и понижение уровня глюкозы в крови;
- холецистит и образование камней в желчном пузыре;
- отдышка;
- аритмии: учащение или урежение сердечного ритма;
- острый панкреатит;
- аллергические реакции;
- боль в месте инъекции;
- гепатит.
Октреотид побочные действия
Терапевтическая дозировка «Октреотида»
Дозировки «Октреотида» индивидуальны, и зависят от конкретных показаний.
Стартовой дозировкой препарата для больных с акромегалией является 0,5-0,1 мг октреотида, вводимые с интервалом в 8-12 часов. Максимальное количество препарата в сутки не должно превышать 1,5 мг.
При опухолях органов ЖКТ «Октреотид» вводят в количестве 0,5 мг 1-2 раза в сутки. Затем дозу корректируют исходя из достигнутого эффекта.
Перед введением подкожно раствор нагревают до комнатной температуры, если он хранился в холодильнике. Так инъекция будет менее болезненной. Оптимально использовать лекарство сразу после вскрытия.
И лечебные, и поддерживающие дозы «Октреотида» рассчитываются строго индивидуально. Лечение необходимо проходить амбулаторно или стационарно, под чутким контролем доктора.
«Октреотид» – гормональный препарат, который требует обязательного врачебного назначения перед использованием. В основном его применяют как симптоматическое средство, но в определенных случаях он воздействует и на причину заболеваний. Проходит терапию лекарством нужно под контролем врача, следя за ответом организма, диагностическими показателями и субъективными изменениями самочувствия.
Состав
В составе раствора содержится активный компонент октреотид, представленный как свободный пептид. Вспомогательные компоненты: натрия хлорид и вода д/и.
Октреотид-Депо включает в свой состав: активное вещество – Октреотид, вспомогательные компоненты: сополимер DL-молочной и гликолевой кислот, D-маннит, карбоксиметилцеллюлозы натриевая соль, полисорбат-80, манит и вода для инъекций.
Октреотид-Лонг состоит из активного вещества октреотида ацетата и дополнительных составляющих: DL-молочной и гликолевой кислот сополимер, D-маннитол, кармеллоза натрия, полисорбат-80.
Форма выпуска
Лекарство выпускается в виде раствора для инъекций, помещённого в ампулы по 1 мл или флаконы по 5 мл.
Октреотид-Депо и Октреотид-Лонг выпускаются в форме лиофилизированного порошка или уплотненной и пористой массы в виде таблетки светлого цвета различной дозировки. Дополнительно прилагается бесцветный прозрачный растворитель и восстановленная суспензия, представляющая собой гомогенную суспензию светлого оттенка.
Также эти лекарственные вариации могут предлагаться в виде лиофилизата для приготовления суспензии, предназначенной для внутримышечного введения с пролонгированным действием по 0,01-0,03г активного компонента в тёмных стеклянных флаконах. Кроме того, в упаковке прилагается 2 мл ампула с растворителем, одноразовый шприц, стерильные иглы и спиртовые тампоны. Один комплект предназначен для выполнения одной инъекции.
Фармакологическое действие
Препарат обладает соматостатиноподобным действием.
Фармакодинамика и фармакокинетика
Данное лекарственное средство является синтетическим аналогом соматостатина, имеющее похожие фармакологические эффекты, но более длительное действие.
Лечение Октреотидом выполняется, когда требуется подавление секреции гормона роста, повышенной патологически или вызванной аргинином, инсулиновой гипогликемией или физической нагрузкой. В результате сокращается секреция инсулина, гастрина, глюкагона и серотонина, которая также может быть повышена патологически или вызвана приёмами пищи. Отмечено подавление секреции инсулина и глюкагона, которую стимулирует аргинин, снижение секреции тиреотропина, вызванной тиреолиберином.
Использование препарата перед или во время операций на поджелудочной железе позволяет снизить частоту характерных послеоперационных осложнений, к примеру: панкреатических свищей, сепсиса, абсцессов, острого послеоперационного панкреатита.
Терапия кровотечений из варикозно-расширенных вен в ЖКТ у пациентов, страдающих циррозом печени в сочетании со специфическим лечением – склерозирующим и гемостатическим, способствует эффективно остановить кровотечения и провести профилактику повторных кровотечений.
Внутри организма происходит быстрое и полноценное всасывание активного вещества. При этом максимальная концентрация Октреотида в составе плазмы крови достигается через 30 минут. Компонент на 65% связывается с белками плазмы, но его связь с форменными элементами крови весьма незначительна. Выведение препарата происходит в несколько фаз через кишечник и при помощи почек.
Показания к применению
Препараты на основе Октреотида назначаются при:
- акромегалии, если отмечена неэффективность агонистов дофамина, а также если невозможно выполнить хирургическую или лучевую терапию;
- эндокринных опухолях гастроэнтеропанкреатической системы;
- глюкагономах, гастриномах;
- инсуломах, соматолибериномах;
- рефрактерной диарее у больных СПИДом;
- операциях на поджелудочной железе, в том числе, при профилактике осложнений;
- кровотечениях, предупреждении рецидивов в случаях варикозного расширения вен пищевода при циррозе печени и так далее.
Противопоказания к применению
Основным противопоказанием к применению данного препарата является гиперчувствительность.
Требуется соблюдать осторожность при лечении больных холелитиазом, сахарным диабетом, при лактации и беременности.
Побочные эффекты
При лечении Октреотидом могут возникать нарушения в работе органов ЖКТ в виде: рвоты, тошноты, анорексии, болевых ощущений, метеоризма, диареи, стеатореи, кишечной непроходимости, острого гепатита без холестаза, повышения активности печёночных трансаминаз, гипербилирубинемии, острого панкреатита и других.
Также может развиваться алопеция и аллергические реакции. Не исключены и местные проявления: болезненность, зуд, жжение, покраснения или припухлость. Длительное применение нередко сопровождается образованием желчных камней, понижением толерантности к глюкозе, стойкой гипергликемией, гипогликемией.
Октреотид, инструкция по применению (Способ и дозировка)
Препарат Октреотид предназначен для внутривенного, внутримышечного или подкожного введения. Дозировка устанавливается индивидуально, с учётом характера заболевания и особенностей пациента. Например, акромегалия и опухоли гастроэнтеропанкреатической системы требуют подкожного введения ежесуточно 1-2 раза по 50–100 мкг. Проведение профилактики осложнений в результате перенесённых операций на поджелудочной железе, предполагает подкожное введение первой дозы за час до лапаротомии, далее вводится ежесуточно по 3 раза по 100 мкг в течение недели. Когда требуется остановить кровотечения из варикозно расширенных вен ЖКТ вводятся непрерывные внутривенные инфузии по 25 мкг/ч не менее 5 дней.
Инструкция по применению Октреотид-Депо и Октреотид-Лонг ФС сообщает, что они предназначены для глубокого внутримышечного введения в ягодичную мышцу. Когда у пациентов подкожное введение Октреотида позволяет адекватно контролировать проявление заболевания, назначают начальную дозу препарата Депо и Лонг по 20мг, через каждые 4 недели на протяжении 3-х месяцев. Затем дозировка корректируется в зависимости от биологических маркеров болезни и клинических симптомов.
Если раньше больные не получали подкожно Октреотид, то следует начинать терапию именно этим средством и способом на протяжении 2 недель. Такой подход позволит оценить его эффективность и переносимость, после этого можно выполнять лечение Октреотид-Депо или Лонг.
Передозировка
В случае передозировки Октреотидом или Октреотидом-Лонг может возникать: кратковременное урежение ЧСС, абдоминальные боли спастического характера, тошнота, приливы крови к лицу, диарея. При этом проводится симптоматическое лечение.
Случаи передозировки Октреотидом-Депо в клинической практике не описаны.
Взаимодействие
Одновременное применение препарата с Циклоспорином понижает его уровень в составе сыворотки, замедляет абсорбцию циметидина и полезных компонентов из ЖКТ. Если Октреотид назначается вместе с инсулином, пероральными гипогликемическими препаратами, бета-адреноблокаторами, БКК и мочегонными средствами, необходимо выполнить корректировки их дозирования. Одновременное применение с Бромокриптином может повысить его биодоступность.
Установлено, что данный препарат снижает метаболический клиренс веществ, которые метаболизируются ферментами цитохрома Р450, вызванных супрессией гормона роста. Поэтому при назначении подобных препаратов следует соблюдать осторожность.
Условия продажи
Каждая форма препарата отпускается строго по рецепту
Условия хранения
Для хранения данных препаратов необходимо обеспечить сухое, тёмное место с температурой 2-8 градусов, хорошо защищённое от детей.
Срок годности
Лиофилизат и растворитель можно применять 3 года.
Формы Депо и Лонг сохраняют пригодность – 2 года. Готовый препарат сохраняет свою эффективность не дольше 6 часов.
Аналоги Октреотида
Совпадения по коду АТХ 4-го уровня:
В фармакологии встречаются многочисленные аналоги Октреотида, основной из них – Сандостатин.
Подобным действием обладают: Соматостатин, Диферелин и Серморелин.
Алкоголь
Как известно, алкоголь способен подавлять синтез гормонов, поэтому его применение с любой формой Октреотида противопоказано.
Отзывы об Октреотиде
Следует отметить, что обсуждения в сети, касающиеся применения данного препарата и его эффективности встречаются нечасто. Обычно пользователи задают вопросы специалистам, в которых интересуются, насколько действенным оказывается терапия того или иного нарушения.
Тем не менее, в клинической практике преимущественно используется Депо-форма. При этом отзывы на Октреотид-Депо показывают, что его применяют при панкреатите, а также острых и хронических формах этого нарушения. Конечно, это средство назначается только специалистом и следует ожидать, что лечение будет проводиться не менее недели.
Цена Октреотида, где купить
Купить в Москве Октреотид-Лонг ФС 10 мг в виде микросферы для приготовления лекарственной суспензии, предназначенной для внутримышечного введения можно в пределах 30-32 тыс. рублей.
Цена Октреотид-Депо 20 мг составляет 46-48 тыс. рублей.
- Интернет-аптеки РоссииРоссия
ЗдравСити
-
Октреотид раствор для в/в и п/к введ. 100мкг/мл 1мл 10штДеко Компания ООО
-
Октреотид раствор для в/в и п/к введ. 100мкг/мл 1мл 5штФарм-Синтез ЗАО/Компания Деко ООО
-
Октреотид-лонг лиофилизат для приг. суспензии для в/м введ. с пролонг. высвобожд. 20мг+Растворитель 2мл+Шприц+Иглы+СалфеткиФармстандарт
-
Октреотид-депо+растворитель лиофилизат для приг. суспензии для в/м введ. пролонг. действия 20мгФарм-Синтез ЗАО/Компания Деко ООО
-
Октреотид-депо+р-ль лиофилизат для приг. суспензии для в/м введ. пролонг. действия 20мгКомпания Деко ООО/Фарм-Синтез АО
показать еще
Кафедра хирургии Института последипломного образования Ярославской государственной медицинской академии, Ярославль, Россия
Балныков С.И.
Ярославская государственная медицинская академия Федерального агентства по здравоохранению и социальному развитию
Шубин Л.Б.
Ярославский государственный медицинский университет, Ярославль, Россия

Оценка роли октреотида в лечении панкреонекроза (с комментарием)
Авторы:
Колотушкин И.А., Балныков С.И., Шубин Л.Б.
Как цитировать:
Колотушкин И.А., Балныков С.И., Шубин Л.Б. Оценка роли октреотида в лечении панкреонекроза (с комментарием). Хирургия. Журнал им. Н.И. Пирогова.
2015;(6):21‑25.
Kolotushkin IA, Balnykov SI, Shubin LB. Estimation of the role of octreotide in treatment of severe pancreatic necrosis. Pirogov Russian Journal of Surgery. 2015;(6):21‑25. (In Russ.)
https://doi.org/10.17116/hirurgia2015621-25
Введение
В Российской Федерации октреотид считается обязательным препаратом в лечении острого панкреатита [1, 3]. В протоколах лечения панкреатита Японии, Великобритании, Международной ассоциации панкреатологов и Американской ассоциации панкреатологов его не рекомендуют применять [7, 10—12]. Это обосновывается результатами рандомизированных исследований, не выявивших улучшения результатов лечения больных при использовании препарата [5, 6, 8, 9]. Наиболее значимым и самым крупным (302 больных) из таких исследований было мультицентровое (32 центра в Европе), рандомизированное двойное слепое исследование, выполненное W. Uhl и соавт. [9].
Однако в исследовании есть ряд недостатков, позволяющих считать представленные авторами результаты не вполне адекватными. Во-первых, анализ проводился на общей совокупности больных, крайне разнородных по тяжести своего состояния. Такой подход к исследованию мог не выявить дифференцированной реакции отдельных групп пациентов на применение препарата. Во-вторых, некорректным выглядит сравнение результатов лечения группы, получавшей октреотид в дозе 100 и 200 мкг 3 раза в сут, так как тяжесть состояния больных в последней была на 2 балла по APACE II выше (7 баллов и 9 баллов соответственно). В-третьих, наиболее существенным недочетом явился статистический анализ полученных в ходе исследования данных. Он основывался на одномерном подходе без учета действия на исход заболевания других (помимо октреотида) потенциальных предикторов (факторов тяжести состояния и лечебных факторов). Все эти недостатки самого важного исследования по изучаемой проблеме позволяют утверждать, что оценка эффективности октреотида при лечении больных панкреонекрозом остается актуальной.
Нами проведено исследование, целью которого являлась оценка влияния октреотида на динамику летальности и распространенность некроза поджелудочной железы и парапанкреатической клетчатки при изначально тяжелом течении деструктивного панкреатита (9 и более баллов по шкале APACHE II).
Выбор категории пациентов для исследования основывался на высокой частоте их неблагоприятных исходов заболевания.
Материал и методы
В мультицентровое исследование включены 204 больных с тяжелым течением панкреонекроза, лечившихся в хирургических отделениях Ярославской областной клинической больницы (с 1996 по 2011 г.), городской больницы № 1 Вологды (с 2005 по 2010 г.), городской больницы № 2 Костромы (с 2008 по 2009 г.) и городской больницы № 1 Рыбинска (с 2008 по 2009 г.).
Критерии включения пациентов в исследование были следующие: 1) обнаружение некроза поджелудочной железы и парапанкреатической клетчатки в ходе операции; 2) наличие некроза поджелудочной железы и парапанкреатической клетчатки на вскрытии трупов умерших неоперированных больных; 3) наличие у неоперированных больных жидкостного образования с секвестрами по результатам ультразвукового исследования, компьютерной томографии и магнитно-резонансной томографии; 4) тяжесть состояния при поступлении 9 и более баллов по шкале APACHE II.
Критериями исключения пациентов из исследования являлись: 1) наличие злокачественного новообразования; 2) отсутствие некрозов поджелудочной железы во время операции, при вскрытии трупов умерших, при ультразвуковом исследовании, МРТ, КТ; 3) тяжесть состояния при поступлении менее 9 баллов по шкале APACHE II.
Важным условием проведения исследования была полная выборка пациентов с тяжелым течением панкреонекроза за весь календарный год в каждом из указанных стационаров, что фактически позволило считать его проспективным по принципу состояния на момент времени в прошлом [2].
В ходе проведения исследования пользовались международной классификацией острого панкреатита, в соответствии с которой определяли прогнозируемую тяжесть течения заболевания [4].
В начале исследования использовали традиционный подход к анализу, аналогичный применявшемуся W. Uhl и соавт. [9]. Больные были разбиты на две группы: основную (n=114), в которой применяли октреотид в стандартных дозах (100 мкг 3 раза в сутки подкожно и внутримышечно), и контрольную (n=90), в которой препарат не применяли. Методами одномерной статистики сравнивали показатели летальности и распространенности некроза в основной и контрольной группах. Для корректной интерпретации полученных результатов группы дополнительно (в отличие от исследования W. Uhl и соавт.) сравнивали еще и по другим потенциальным предикторам (факторам тяжести состояния при поступлении в стационар и лечебным факторам), которые также могли влиять на исход заболевания.
Распространенным считали некроз, захватывающий один из отделов поджелудочной железы или существенный объем парапанкреатической клетчатки. Распространенность некроза устанавливали во время оперативного вмешательства или (у неоперированных больных) по результатам вскрытия. Кроме того, очаговым считали панкреонекроз у больных, для излечения которых не требовалось оперативное вмешательство.
Факторами тяжести состояния являлись возраст (количество лет), пол (1 — мужской, 0 — женский), тяжесть органных дисфункций по шкале APACHE II (в баллах), величина температуры тела (°С), частота пульса (в 1 мин), значение среднего артериального давления (в мм рт.ст.), частота дыхания (в 1 мин), уровень сознания по шкале Глазго (в баллах), количество лейкоцитов крови (тыс. ·109/л), палочкоядерных нейтрофилов (в %), уровень в крови креатинина (в мг/дл), калия (в ммоль/л), натрия (в ммоль/л), глюкозы (в ммоль/л), парциальное напряжение кислорода крови (в мм рт.ст.), значения pH крови. Эти параметры оценивали при поступлении.
Из лечебных предикторов оценивали и сравнивали методики антибактериальной профилактики (аминогликозиды, пенициллины и цефалоспорины первого поколения — код 1; цефалоспорины третьего и четвертого поколения — код 2; фторхинолоны и карбопенемы — код 3), частоту применения кваматела (1 — применяли, 0 — не применяли), антиферментной терапии (1 — применяли, 0 — не применяли), ранней нутритивной поддержки (1 — применяли, 0 — не применяли), нутритивной поддержки при гнойных осложнениях (1 — применяли, 0 — не применяли).
Сравнивали результаты лечения больных основной и контрольной групп только в случае отсутствия достоверных различий этих групп по указанным выше факторам тяжести состояния и лечебным факторам. Достоверными считали различия, если значение p для используемого критерия было ниже 0,05. Использовали t-критерий Стьюдента при нормальном распределении значения признака, U-критерий Манна—Уитни при сравнении групп с отличным от нормального распределения значения признака, критерий χ2 при сравнении групп по качественному признаку.
На втором этапе исследования применяли альтернативный вариант анализа, не требующий формирования групп сравнения и их рандомизации, как в исследовании W. Uhl и соавт., — определение совокупного влияния факторов на исход лечения. Результатом его являлась модель прогноза вероятности наступления события (изменения результата лечения) по имеющимся факторам тяжести состояния при поступлении в стационар и факторам проводимого лечения.
Для оценки динамики летальности использовали модель пропорциональных рисков Кокса. Ее особенностью являлась оценка влияния этих параметров при каждом случае законченного наблюдения за временем жизни больных, т. е. до момента смерти.
Совокупное влияние факторов на распространенность некроза оценивали методом логистической регрессии.
При отборе переменных в модели для регрессионного анализа использовали метод обратного исключения [2].
Влияние вошедших в модель предикторов и точность всей модели в целом считали достоверными, если значения p критерия χ2 были меньше критического значения (0,05) для всех вошедших факторов и в целом для модели.
Степень влияния предиктора определяли по величине регрессионного коэффициента. Большие его числовые значения свидетельствовали о большей силе влияния. Направленность влияния оценивали по знаку коэффициента. При отрицательном значении регрессионного коэффициента считали влияние параметра тяжести состояния или лечения обратнозависимым, т. е. его увеличение снижало вероятность летального исхода, при положительном значении коэффициента увеличение действия фактора указывало на увеличение вероятности летального исхода.
Статистическую обработку материала проводили с помощью программы StatSoft, Inc. (2007), Statistica version 8.0 и MedCalc, версия 10.5.0.0.
Результаты и обсуждение
Уже на этапе одномерного анализа, т. е. при простом сравнении групп, выявлена достоверно меньшая летальность в группе больных, получавшей октреотид, по сравнению с группой, его не получавшей (52% против 72%; критерий χ2; p=0,003). При сравнении групп по распространенности некроза поджелудочной железы и парапанкреатической клетчатки также установлено, что в основной группе распространенный некроз встречался достоверно реже, чем в контрольной (64% против 77%; критерий χ2; p=0,051). Таким образом, оценка эффективности октреотида методом одномерного статистического анализа, применяемого только у больных с прогностически тяжелым течением заболевания, а не на общем числе больных панкреатитом, как в исследовании W. Uhl и соавт., показала уменьшение летальности и распространенности некроза.
Для адекватной интерпретации этого результата и исключения возможности опосредованной корреляции было проведено сравнение групп по остальным потенциальным предикторам, которые тоже могли влиять на летальность и распространенность некроза. Анализ тяжести состояния пациентов обеих групп при поступлении практически не выявил их различий (табл. 1). Интегральный показатель органных дисфункций (по шкале APACHE II) в обеих группах не различался (12,0±3,3 балла в основной против 12,0±3,3 балла в контрольной; t-тест; p=0,959) (см. рисунок).


Однако различия по лечебным факторам были существенны. Исключить тот факт, что выявленное снижение летальности и распространенности некроза в группе пациентов, получавших октреотид, было обусловлено более частым применением на ранней стадии заболевания нутритивной поддержки (критерий χ2; p=0,000) и панкреотропных антибиотиков (U-тест; p=0,000) (табл. 2), а не использованием октреотида, оказалось невозможным. В связи с этим для установления совокупного с другими факторами влияния октреотида на летальность был использован способ статистического анализа — модель пропорциональных рисков Кокса.

Анализ Кокса (табл. 3) позволил построить значимую модель факторов лечения и тяжести состояния, влияющих на летальность (р=0,000). Октреотид входил в состав модели предикторов (р=0,000).

Более того, регрессионный коэффициент у октреотида оказался наибольшим из числа всех предикторов, входящих в модель (β= –0,8). Это означало, что сила его влияния на изменение летальности являлась наибольшей среди всех факторов, входящих в модель. Знак регрессионного коэффициента «–» указывал на то, что факт законченности наблюдения за временем жизни пациента (соответствие факту летального исхода) и назначение октреотида находятся в обратной зависимости, т. е. назначение октреотида уменьшало вероятность летального исхода у больных деструктивным панкреатитом.
Для определения влияния назначения октреотида на распространенность некроза поджелудочной железы и парапанкреатической клетчатки использовали логистический регрессионный анализ (табл. 4), который позволил построить значимую модель взаимного влияния факторов (p=0,0001). В эту модель наряду с другими предикторами, взаимно влияющими на развитие распространенного некроза, вошел октреотид (p=0,033) как фактор с самым сильным влиянием, регрессионный коэффициент составил –0,875. Знак регрессионного коэффициента «–» указывал на то, что изменение распространенности некроза поджелудочной железы и назначение октреотида находятся в обратной зависимости, т. е. назначение октреотида уменьшало вероятность распространенности некроза у пациентов с деструктивным панкреатитом.

Таким образом, при использовании модели пропорциональных рисков Кокса выявлена закономерность, которая заключалась в том, что применение октреотида оказывает очень сильное влияние на снижение летальности при изначально тяжелых формах панкреонекроза. При использовании логистической регрессии установлено, что октреотид является самым значимым фактором, влияющим на уменьшение распространенности некроза поджелудочной железы и парапанкреатической клетчатки у больных с тяжелым течением панкреонекроза.
Данные проведенного исследования позволяют рекомендовать назначение октреотида больным с изначально тяжелым течением панкреонекроза.
Комментарий
Улучшение результатов лечения больных панкреонекрозом является актуальной задачей, поэтому хирурги, работающие в хирургических «скоропомощных» стационарах, постоянно стремятся найти способы уменьшения количества осложнений и летальности при этом заболевании. Одним из эффективных направлений в улучшении результатов лечения панкреонекроза является стандартизация тактики лечения этого заболевания. Именно с этой целью на протяжении 2013—2014 гг. в нашей стране разрабатываются национальные рекомендации лечения больных панкреонекрозом (Съезд Российского общества эндоскопических хирургов, Москва, февраль 2013 г.; Согласительная конференция, Санкт-Петербург, ноябрь 2014 г.). Использование в комплексном медикаментозном лечении октреотида включено в терапевтический алгоритм национальных рекомендаций.
Авторы вышеизложенной статьи, являясь сторонниками применения октреотида в лечении панкреонекроза, ставят под сомнение результаты классических рандомизированных и мультицентровых исследований, проведенных в различных странах, в которых убедительно демонстрируется отсутствие значимого эффекта от применения этого препарата. Категоричность такого заявления вызывает удивление и чувство неловкости за коллег.
В своем исследовании авторы подвергли анализу результаты лечения больных панкреонекрозом, находившихся в различных стационарах, при этом временные рамки колеблются от 1996 до 2009 г., что ставит под сомнение корректность полученных результатов. В работе отсутствует информация о количестве оперированных больных в сравниваемых группах. Обсуждая эффективность применения октреотида, необходимо учитывать длительность заболевания до начала применения октреотида, что не сделано авторами. Маловероятно, что найдутся сторонники применения октреотида на стадии гнойных осложнений заболевания. В то же время, по-видимому, применение аналогов соматостатина в первые часы от начала заболевания могут уменьшить объем поражения паренхимы поджелудочной железы и парапанкреатической клетчатки.
Публикации, освещающие результаты лечения больных панкреонекрозом и направленные на уменьшение летальности, заслуживают поощрения. Однако при обсуждении собственных данных и результатов, полученных в других хирургических клиниках, следует соблюдать корректность и избегать категоричных суждений.
Член правление Российского общества хирургов, профессор А.Г. Кригер
Мы используем файлы cооkies для улучшения работы сайта. Оставаясь на нашем сайте, вы соглашаетесь с условиями
использования файлов cооkies. Чтобы ознакомиться с нашими Положениями о конфиденциальности и об использовании
файлов cookie, нажмите здесь.
Елена Александровна Полуэктова, врач, кандидат медицинских наук:
– Мы возвращаемся к гастроэнтерологии, и сообщение сделает доктор медицинских наук, профессор Олег Самуилович Шифрин «Новые возможности в противоболевой и заместительной терапии хронического панкреатита».
Олег Самуилович Шифрин, профессор, доктор медицинских наук:
– Глубокоуважаемые коллеги, рабочей группой Российской гастроэнтерологической ассоциации были разработаны рекомендации по ведению пациентов с хроническим панкреатитом. Обратите внимание, красным цветом обозначены очень важные принципиальные положения, которые должен учитывать врач в ведении подобного рода пациентов. Это определение причины боли, абдоминальной боли при хроническом панкреатите и ее лечение. Вторым важным направлением выступает лечение внешнесекреторной недостаточности поджелудочной железы. Вот эти вопросы и положены в основу моего сообщения.
Итак, при дебюте хронического панкреатита абдоминальная боль занимает очень важное место, это кардинальный признак. Она встречается гораздо чаще, чем проявления внешнесекреторной недостаточности, симптомы панкреатогенного диабета, желтуха и прочее. Почти у 90% больных при различных формах панкреатита, независимо от этиологии, боль занимает центральное ведущее место при дебюте заболевания. При развернутой стадии заболевания на первый план может выступать внешнесекреторная недостаточность, и это важно учитывать.
Клинический пример. К нам в клинику обратился мужчина 54 лет с жалобой на выраженные абдоминальные боли в верхних отделах живота полуопоясывающего характера, чаще возникающие где-то через 30-40 минут после еды, на выраженное мучительное вздутие живота и на появившуюся диарею (неоформленный стул где-то 2-3 раза в день). Следует отметить, что пациент в течение 2-3 десятков лет злоупотреблял алкоголем, выпивал где-то 2-3 бутылки крепких спиртных напитков в неделю, много курил. Индекс курильщика 240 баллов. Мы остановимся чуть позже на взаимодействии этих двух крайне важных панкреотоксических факторов: алкоголь и курение.
Итак, в анализах мочи у пациента выявлялся 2-3-кратный уровень гиперамилазурии. Терапия дротаверином, блокаторами секреции, фесталом оказалась неэффективна.
Какие вопросы следует поставить, берясь лечить данного пациента? Во-первых, следует уточнить диагноз: панкреатит ли это. Не секрет, что панкреатит, к сожалению, очень часто как недодиагностируется, так и гипердиагностируется. Далее, при подтверждении диагноза надо поставить вопрос: какой это панкреатит? Очень важно определить этиологию и морфологическую форму заболевания. Необходимо выявить, выделить основные клинические синдромы заболевания. И, наконец, при наличии абдоминальной боли, а у нашего пациента выраженная абдоминальная боль, следует установить ее характер. Это принципиально важно в дальнейшем при назначении оптимальной терапии.
Следует сказать, что по Хайдельбергской классификации, так называемой классификации M-ANNHEIM, немецкие коллеги выделяют полиэтиологичную чаще всего причину развития панкреатита. То есть различные факторы сочетаются в разной пропорции, и очень редко мы сталкиваемся с моноэтиологичной формой заболевания.
У нашего пациента четко (уже при расспросе его) выделяются два панкреотоксических фактора: это злоупотребление алкоголем и курение. При взаимодействии эти факторы взаимно усиливают друг друга, вызывают быстрое развитие и прогрессирование заболевания.
При объективном статусе отмечалась болезненность в проекции поджелудочной железы, вздутие живота. В остальном каких-то выраженных изменений найдено не было. В анализах обращало внимание двукратное повышение уровня амилазы мочи. Обратите внимание, что, несмотря на явные проявления внешнесекреторной недостаточности, фекальная эластаза в пределах нормы.
При компьютерной томографии обращает внимание неоднородная структура поджелудочной железы, но каких-то выраженных локальных изменений типа псевдокист выявлено не было.
Говоря о причинах боли у пациента, следует выделить боль, связанную с собственно воспалением ткани поджелудочной железы, неважно преобладают ли процессы экссудации, когда воспалительный отек сдавливает нервные ганглии, или при преобладании в воспалительном субстрате альтеративных процессов, когда биологически активные вещества воздействуют на оболочку нервных ганглиев и разрушают ее. В этих случаях ведущее значение в генезе боли имеет собственно воспаление. Это боль типа А, на ней мы остановимся чуть позже.
В случае же осложнений собственно воспаления ткани поджелудочной железы при развитии псевдокист, в которых агрессивный панкреатический сок воздействует на обнаженные нервные окончания, при сдавлении увеличенной вследствие воспаления головкой поджелудочной железы желчных протоков или 12-перстной кишки или вследствие сдавления вирсунгового протока участками фиброза, возникает боль В-типа.
В чем же их отличие? Боль А-типа, то есть боль, вызванная собственно воспалением ткани поджелудочной железы, отличает относительно недлительная продолжительность, обычно где-то менее двух недель, длительные светлые промежутки по нескольку месяцев. И эффект наступает от консервативной терапии, неважно, будь то назначение нескольких таблеток парацетамола или госпитализация пациента в отделении интенсивной терапии с проведением комплекса мероприятий по лечению тяжелого обострения панкреатита. Но исцеление, улучшение состояния в данном случае приносит консервативная тактика, то есть такие пациенты находятся в ведении гастроэнтерологов и терапевтов.
Боль В-типа. Клинически ее отличает длительный период обострения, обычно не менее двух месяцев, короткие светлые промежутки и эффект наступает или от хирургических, или эндоскопических методов лечения.
Иной механизм абдоминальной боли при хроническом панкреатите. Уже на относительно ранних этапах заболевания уменьшается выработка поджелудочной железой (поджелудочная железа, напомню, весит где-то всего лишь 60-80 грамм) раствора бикарбоната. А здоровая поджелудочная железа производит в сутки полтора-два литра раствора бикарбоната. Вследствие уменьшения выработки раствора бикарбоната происходит ацидификация начальных отделов 12-перстной кишки, вследствие закисления среды в кишке инактивируются ферменты, возникают проявления экзокринной недостаточности. И все это сопровождается тяжелыми нарушениями моторики и развития метеоризма, которые подчас пациенты не могут отличить от чувства абдоминальной боли. Напомню, что у нашего пациента выраженный метеоризм, резко снижающий качество его жизни.
Итак, какие основные направления лечения боли, консервативные направления? Я подчеркиваю, это лечение боли А-типа. Отказ от курения и употребления алкоголя при любой форме панкреатита, не обязательно при токсических формах, и при билиарном, и при наследственном, при любом панкреатите следует отказаться от дополнительных панкреотоксических факторов, удалить их. Первым этапом назначаются легкие анальгетики, далее могут назначаться «легкие» опиоиды типа трамадола, но это редко бывает, и еще реже в исключительных случаях при панкреатите, в отличие от рака поджелудочной железы, назначаются уже классические наркотические препараты. Это крайнее средство, каждый раз данный подход требует очень тщательного обсуждения и оценки всей глубины ситуации в отношении конкретного пациента. Трициклические антидепрессанты – так называемая лекарственная денервация поджелудочной железы – эффективный метод лечения абдоминальной боли А-типа.
Вот обратите внимание, ингибиторы секреции, которые мы очень часто используем в лечении абдоминальной боли при хроническом панкреатите, а также сандостатин, не показывают свою эффективность при лечении болевого панкреатита при контролируемых исследованиях. Очевидно, это связано с тем, что в исследуемую группу попадают пациенты как с А-болью, так и с В-болью, то есть происходит смешение разных типов боли. И соответственно при обработке статистических данных не удается получить достоверных результатов. Хотя все мы, клиницисты, прекрасно знаем, что лечить абдоминальную боль мы начинаем, прежде всего, комбинацией ферментных препаратов и ингибиторов секреции.
Итак, остановимся на ферментных препаратах. Классическими работами конца прошлого века было показано, что традиционные таблетки панкреатина обладают большей эффективностью в лечении абдоминальной боли А-типа при хроническом панкреатите, а также они достоверно снижают давление в протоках поджелудочной железы. В то же время капсулированные, микрогранулированные препараты панкреатина не уменьшают достоверно уровень абдоминальной боли А-типа и не уменьшают достоверно повышенное давление в протоковой системе панкреас.
За неимением времени я не буду останавливаться на патогенезе действия таблетированных и микрогранулированных препаратов. Но суть в том, что таблетированные препараты в большей степени задействуют рилизинг-систему, механизм обратной связи, потому что панкреатин, который содержится в таблетках, протеазы начинают действовать раньше в начальных отделах 12-перстной кишки, где, собственно, и осуществляется механизм обратной связи, где функционирует рилизинг-система.
Вернемся к нашему пациенту. Хронический панкреатит в стадии обострения, обусловленный токсическими факторами (алкоголь и курение), первая стадия по Кембриджской классификации. Синдром избыточного микробного роста в тонкой кишке. Экзогенно-конституциональное ожирение первой степени, это тоже нередко встречается при панкреатите. Не надо обязательно думать, что эти все пациенты должны быть обязательно крайне исхудавшими.
Какие направления лечебной тактики? Мы убедили пациента, воздействовав, в том числе, и на его родственников, что ему полностью необходимо отказаться от алкоголя и курения. Пациенту проводилась дезинтоксикационная терапия в достаточном объеме. Мы назначили ему препарат мезим 20000 по две таблетки 3 раза в день до улучшения его состояния, в дальнейшем мы несколько уменьшили эту дозировку, и омепразол. Добавлю, что коротким курсом с учетом синдрома избыточного микробного роста было назначено также семидневное лечение рифаксимином, антибактериальным препаратом.
В нашей клинике было проведено исследование, сравнивали анальгезирующее воздействие классических таблеток панкреатина мезима 10000 и капсулированного панкреатина в виде микросфер, содержащего такое же количество липазы – 10000 в одной капсуле. Отмечено, что мезим 10000 чаще эффективно уменьшал уровень боли и даже совсем ее прекращал, мезим 10000 реже вызывал развитие запоров и достаточно эффективно мезим 10000 снижал уровень метеоризма, часто беспокоящего наших пациентов. Таким образом, мезим 10000 и вновь появившийся где-то около года назад на рынке мезим 20000 позволяют эффективно купировать абдоминальную боль А-типа, и они обеспечивают при умеренно выраженной внешнесекреторной недостаточности ее эффективное нивелирование. Кроме того, следует отметить, что на фоне таблетированных препаратов панкреатина в виде мезима 10000 и мезима 20000 реже возникает такое осложнение ферментативной терапии как запоры.
Еще раз вернемся к основным направлениям лечения хронического панкреатита. Помимо устранения токсических факторов мы должны назначать ферментные препараты в адекватной дозе, это при лечении абдоминальной боли, прежде всего, таблетированными препаратами. Если же абдоминальная боль сочетается с тяжелой степенью экзокринной недостаточности, присоединяются уже капсулированные препараты.
Я хочу сказать, что вот сейчас на нашем рынке появляется новый препарат панкреатина – микротаблетки панкреатина заключенные в капсулы – пангрол препарат. Он будет представлен 10000-ми капсулами панкреатина по содержанию липазы и, соответственно, пангрол 25000 единиц, которые содержат липазу в 2,5 раза больше. Мы остановимся чуть позже более подробно на этом препарате.
Кроме того, обязательно используются блокаторы протонной помпы. Здесь следует учитывать, что при наличии, скажем, билиарного панкреатита октреотид, который вызывает сгущение желчи, должен использоваться с осторожностью, но тем не менее он обладает хорошим антисекреторным воздействием в плане самой поджелудочной железы.
При лечении спастических расстройств (они чаще всего имеют место при панкреатите) безусловно нужно использовать спазмолитики, лекарственные денервации поджелудочной железы, назначаем трициклические антидепрессанты. И обязательное лечение трофологической недостаточности, синдрома избыточного микробного роста, который очень часто сочетается с хроническим панкреатитом, и, наконец, антиоксидантная терапия.
Каково преимущество препарата мезим 20000? Он содержит более эффективный ферментативный комплекс по сравнению с мезимом 10000, позволяет уменьшить количество таблеток, которое мы назначаем пациенту, а это очень важно, поскольку в данном случае у пациента повышается желание следовать указаниям врача. Пациенты не любят принимать большое количество таблеток, повышается комплаентность пациентов, настроенность их на лечение.
Препарат пангрол представляет, как я уже сказал, капсулы наполненные минитаблетками. Каждая минитаблетка содержит 500 единиц липазы. Две формы выпуска – это капсулы 10000 единиц и капсулы 25000 единиц. Очень важно, что минитаблетки покрыты не только кишечнорастворимой оболочкой, устойчивой к воздействию кислого желудочного сока, но и функциональной мембраной. Вот эта функциональная мембрана, выполненная на основе дериватов метакриловой кислоты, позволяет выделяться препарату в тонкой кишке равномерно. То есть вы видите, проводилось сравнение, как выделяются ферменты, в частности липаза, из минитаблеток и из минимикросфер. Оказалось, что из минитаблеток ферменты выделяются более равномерно, что очень важно в отношении лечения внешнесекреторной недостаточности поджелудочной железы.
Кроме того, минитаблетки обеспечивают равномерное перемешивание с пищей, и происходит оптимальная активация ферментов в разных участках тонкого кишечника.
Оказалось, что пангрол достоверно снижает стеаторею уже на 5 день лечения, причем у пациентов с тяжелой формой внешнесекреторной недостаточности поджелудочной железы.
Очень важно, что на фоне терапии у большинства пациентов к шестому месяцу лечения нормализуется масса тела, нормализуется уровень сывороточного альбумина.
И заключить свое выступление я хотел тем, что, несмотря на то, что появились новые современные препараты в лечении хронических панкреатитов, в частности ферментативные препараты, работа гастроэнтеролога, работа терапевта не стала менее трудной. Но то, что появились новые эффективные препараты, позволяет сделать ее более эффективной, то есть помочь большему количеству наших пациентов.
Октреотид
Octreotide
Регистрационный номер
Торговое наименование
Октреотид
Международное непатентованное наименование
Лекарственная форма
раствор для внутривенного и подкожного введения
Состав
1 мл раствора содержит:
активное вещество: октреотида ацетат (в пересчёте на октреотид) 0,050 мг, 0,100 мг и 0,300 мг;
вспомогательные вещества: натрия хлорид 9,0 мг, вода для инъекций до 1,0 мл.
Описание
Прозрачная бесцветная жидкость без запаха.
Фармакотерапевтическая группа
Код АТХ
Фармакологические свойства
Фармакодинамика
Октреотид — синтетический октапептид, производное естественного гормона соматостатина, обладает сходными с ним фармакологическими эффектами, но со значительно большей продолжительностью действия. Октреотид подавляет как патологически повышенную секрецию гормона роста (ГР), так и вызываемую аргинином, физической нагрузкой и инсулиновой гипогликемией. Препарат подавляет секрецию серотонина, гастрина, инсулина и глюкагона и других пептидов, продуцируемых в гастроэнтеропанкреатической эндокринной системе. У больных, которым проводятся операции на поджелудочной железе, применение октреотида во время операции и после неё снижает частоту типичных послеоперационных осложнений (острого послеоперационного панкреатита, панкреатических свищей, абсцессов, сепсиса).
При кровотечениях из варикозно расширенных вен пищевода и желудка у больных циррозом печени применение октреотида в составе комплексной терапии приводит к эффективной остановке кровотечения, профилактике раннего повторного кровотечения и улучшению выживаемости. Механизм действия октреотида связан с уменьшением органного кровотока посредством подавления вазоактивных гормонов (вазоактивного интестинального пептида, глюкагона).
Фармакокинетика
После подкожного введения октреотид быстро и полностью всасывается. Известно, что максимальная концентрация в плазме достигается в пределах 30 мин. Связывание с белками плазмы составляет около 65 %. Связывание октреотида с форменными элементами крови крайне незначительно.
Большая часть препарата выводится кишечником, около трети введённого октреотида выводится в неизменном виде почками. Период полувыведения (T½) после подкожной (п/к) инъекции около 100 мин. После внутривенного (в/в) введения, выведение осуществляется в две фазы. У пожилых пациентов снижается клиренс, период полувыведения увеличивается. При тяжёлой почечной недостаточности клиренс уменьшается вдвое.
Показания
— Профилактика и лечение осложнений после операций на поджелудочной железе и гастродуоденальной зоне;
— в составе комплексной терапии для остановки кровотечений и профилактики повторного кровотечения из варикозно расширенных вен пищевода у больных с циррозом печени;
— лечение острого панкреатита;
— остановка кровотечений при язвенной болезни желудка и 12-перстной кишки.
Противопоказания
Повышенная чувствительность к компонентам препарата.
С осторожностью
Сахарный диабет, желчнокаменная болезнь.
Применение при беременности и в период грудного вскармливания
Адекватных и контролируемых исследований не проводилось. Применение во время беременности и в период лактации только по абсолютным показаниям, с учётом соотношения риск/польза, то есть когда предполагаемая польза для матери превышает предполагаемый риск для плода или грудного ребёнка.
Способ применения и дозы
При лечении острого панкреатита Октреотид вводится п/к в дозе 100 мкг 3 раза/сут в течение 5–7 суток. Возможно назначение до 1200 мкг/сут, подбор дозы основан на определении концентрации амилазы, липазы, воспалительных цитокинов крови.
Для профилактики осложнений после операций на поджелудочной железе первую дозу Октреотида 100 мкг вводят п/к за 1 час до лапаротомии; затем после операции вводят п/к по 100 мкг 3 раза/сут на протяжении 7 последующих дней.
Для остановки кровотечения из варикозно расширенных вен пищевода препарат вводят в/в в дозе 25 мкг/ч в виде продолжительных инфузий в течение 5 дней.
Для остановки кровотечений при язвенной болезни желудка и 12-перстной кишки рекомендуется вводить Октреотид в виде в/в инфузий в дозе 25 мкг/ час в течение 5 дней.
У больных пожилого возраста нет необходимости в снижении дозы Октреотида.
У пациентов с нарушением функции почек коррекция режима дозирования октреотида не требуется.
У пациентов с нарушением функции печени рекомендуется коррекция поддерживающей дозы, так как имеются данные об увеличении T½ октреотида у больных циррозом печени.
Опыт применения октреотида у детей очень ограничен.
Правила приготовления и введения раствора
Для уменьшения явлений дискомфорта в месте введения, раствор Октреотида перед введением должен иметь комнатную температуру.
При п/к введении препарата следует избегать нескольких инъекций в одно и то же место через короткие интервалы времени. Ампулы с препаратом следует открывать непосредственно перед введением, неиспользованное количество раствора следует уничтожить.
При в/в введении следует внимательно осмотреть раствор на предмет прозрачности, наличия частиц, осадка, изменения цвета. Нельзя применять препарат, если он является мутным, содержит частицы, осадок. Октреотид в течение 24 часов сохраняет физическую и химическую стабильность в стерильном 0,9 % растворе натрия хлорида при температуре от 8 до 25 °C. Во избежание микробного загрязнения разведенные растворы следует использовать сразу после приготовления. Если раствор не будет использован сразу, его следует хранить при температуре от 2 до 8 °C вплоть до его применения. Перед использованием раствор следует подержать при комнатной температуре.
Общее время между разведением, хранением в холодильнике и окончанием введения раствора не должно превышать 24 ч.
При необходимости в/в введения содержимое одной ампулы, содержащей 300 мкг октреотида, должно быть разведено в 60 мл 0,9 % раствора натрия хлорида, приготовленный раствор следует вводить в/в капельно. Инфузии повторяют с необходимой частотой в соответствии с рекомендованной длительностью лечения. Октреотид также можно вводить и в более низких концентрациях.
Побочное действие
Местные реакции: в месте инъекции возможны боль, ощущение зуда или жжение, краснота и припухлость (обычно проходят в течение 15 минут).
Со стороны ЖКТ, поджелудочной железы, печени и желчного пузыря: возможны — анорексия, тошнота, рвота, спастические боли в животе, ощущение вздутия живота, избыточное газообразование, жидкий стул, диарея и стеаторея. Хотя выделение жира с калом может возрастать, нет указаний на то, что длительное лечение октреотидом может приводить к нарушению всасывания (мальабсорбции). В редких случаях могут отмечаться явления, напоминающие острую кишечную непроходимость: прогрессирующее вздутие живота, выраженная боль в эпигастральной области, напряжение брюшной стенки.
Длительное использование октреотида может приводить к образованию камней в желчном пузыре.
Известны отдельные случаи острого гепатита без холестаза (нормализация показателей трансаминаз после отмены октреотида), а также гипербилирубинемии в сочетании с увеличением активности щелочной фосфатазы, гамма-глутамилтрансферазы и др. трансаминаз.
Имеются отдельные сообщения о редких случаях острого панкреатита, который развивался в первые часы или дни применения октреотида.
Со стороны сердечно-сосудистой системы: в отдельных случаях — тахикардия, брадикардия.
Со стороны обмена веществ: возможно нарушение толерантности к глюкозе после приёма пищи (октреотид оказывает подавляющее Действие на образование ГР, глюкагона и инсулина), гипогликемия; в редких случаях при длительном лечении возможно развитие персистирующей гипергликемии.
Прочие: редко — аллергические реакции, алопеция; в отдельных случаях — анафилактические реакции.
Передозировка
Известно, что введение октреотида в дозе до 2000 мкг в виде п/к инъекции 3 раза в течение нескольких месяцев переносилось хорошо.
Максимальная разовая доза при в/в болюсном введении взрослому пациенту составляла 1000 мкг. При этом отмечались такие симптомы, как снижение частоты сердечных сокращений, «приливы» крови к лицу, абдоминальная боль спастического характера, диарея, тошнота, ощущение пустоты в желудке. Все эти симптомы разрешились в течение 24 часов с момента введения препарата.
Одному пациенту по ошибке методом длительной инфузии была введена избыточная доза октреотида 250 мкг/ч (вместо 25 мкг/ч), что не сопровождалось побочными эффектами.
При острой передозировке не было отмечено каких-либо опасных для жизни реакций.
Лечение: симптоматическая терапия.
Взаимодействие с другими лекарственными средствами
Октреотид уменьшает всасывание циклоспорина, замедляет всасывание циметидина.
Необходима корректировка доз одновременно применяемых мочегонных средств, бета-адреноблокаторов, блокаторов «медленных» кальциевых каналов, инсулина, пероральных гипогликемических препаратов.
При одновременном применении Октреотида и бромокриптина биодоступность последнего повышается.
Препараты, метаболизирующиеся ферментами системы цитохрома P450 и имеющие узкий терапевтический диапазон доз (например, хинидин, терфенадин) следует назначать с осторожностью.
Особые указания
У больных сахарным диабетом 1 типа (получающих инсулин), октреотид может снижать потребность в инсулине. У пациентов без нарушения углеводного обмена и больных сахарным диабетом 2 типа введение препарата может приводить к постпрандиальной гликемии. Пациентам с сахарным диабетом на фоне гипогликемической терапии рекомендуется проводить контроль концентрации глюкозы в крови.
У некоторых пациентов октреотид может изменять абсорбцию жиров в кишечнике. На фоне применения октреотида отмечается снижение содержания цианокобаламина (витамина B12) и отклонение от нормы показателей теста всасывания цианокобаламина (тест Шиллинга).
У пациентов с дефицитом витамина B12 в анамнезе при применении октреотида рекомендуется контролировать содержание цианокобаламина.
Если на фоне применения октреотида развивается брадикардия, необходимо снизить дозы бета-адреноблокаторов, блокаторов «медленных» кальциевых каналов или препаратов, влияющих на водно-электролитный баланс.
До назначения октреотида больные должны пройти исходное УЗИ желчного пузыря.
Если камни в желчном пузыре выявлены перед началом лечения, вопрос о применении Октреотида решается индивидуально, в зависимости от соотношения потенциального лечебного эффекта препарата и возможными факторами риска, связанными с наличием камней в желчном пузыре.
Во время лечения октреотидом следует проводить УЗИ желчного пузыря, с интервалом 6–12 месяцев.
Ведение больных, у которых камни желчного пузыря образуются в процессе лечения октреотидом
а) Бессимптомные камни желчного пузыря.
Применение октреотида можно прекратить или продолжить — в соответствии с оценкой соотношения польза/риск. В любом случае не требуется никаких других мер, кроме продолжения проведения осмотров, сделав их, при необходимости, более частыми.
б) Камни желчного пузыря с клинической симптоматикой.
Применение октреотида можно прекратить или продолжить — в соответствии с оценкой соотношения польза/риск. В любом случае больного следует лечить так же, как и в других случаях желчнокаменной болезни с клиническими проявлениями.
Побочные эффекты со стороны ЖКТ могут быть уменьшены, если инъекции Октреотида делать в промежутках между приёмами пищи или перед сном.
Необходима коррекция режима дозирования одновременно применяемых диуретиков, бета-адреноблокаторов, блокаторов «медленных» кальциевых каналов, инсулина, пероральных гипогликемических средств, глюкагона.
Влияние на способность управлять транспортными средствами, механизмами
На сегодняшний день не имеется данных о влиянии октреотида на способность водить автомобиль и работать с механизмами.
Форма выпуска
Раствор для внутривенного и подкожного введения, 50 мкг/мл, 100 мкг/мл, 300 мкг/мл.
При производстве на ООО «Натива», Россия
По 1 мл в ампулы нейтрального стекла НС-1 или стекла I гидролитического класса. Возможна упаковка в ампулы, имеющие кольцо натяжения для вскрытия или точку разлома.
По 5 ампул в контурную ячейковую упаковку из плёнки полимерной.
1 или 2 контурные ячейковые упаковки, нож для вскрытия ампул или скарификатор ампульный и инструкцию по применению помещают в картонную пачку.
При упаковке раствора в ампулы, имеющие кольцо натяжения для вскрытия, или в ампулы с точкой разлома нож или скарификатор ампульный не вкладывают.
При производстве на ОАО «Фарм-стандарт-УфаВИТА», Россия.
По 1 мл в ампулы из стекла I гидролитического класса.
По 5 ампул в контурную ячейковую упаковку из плёнки поливинилхлоридной и фольги алюминиевой или без фольги.
1 или 2 контурные ячейковые упаковки вместе с инструкцией по применению помещают в пачку из картона.
Хранение
В защищённом от света месте при температуре не выше 25 °C. Не замораживать.
Хранить в недоступном для детей месте.
Срок годности
2 года.
Не использовать по истечении срока годности.
Условия отпуска из аптек
Отпускают по рецепту
