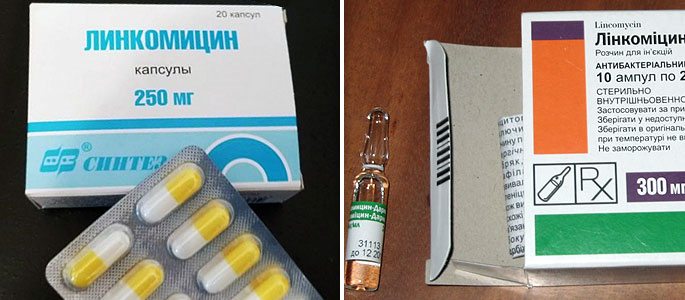
Линкомицин – это антибиотик широкого спектра действия, принадлежащий к группе линкозамидов и обладающий в большой концентрации хорошим бактерицидным эффектом в отношении бактерий вызывающих гайморит и прочие инфекционные заболевания.
Лучше всего препарат действует на анаэробные грамположительные бактерии. Своей максимальной концентрации в крови линкомицин достигает через 3 часа после применения. Но прежде чем читать дальше, ознакомьтесь с тем каких ошибок, стоит избегать при использовании антибактериальных препаратов.
Общая информация о препарате
Линкомицин выпускают в твёрдой форме, в виде капсул и в форме для инъекций, лиофилизата, из которого можно приготовить жидкость для уколов. Механизм действия линкомицина при гайморите обусловлен торможением выработки протеинов клетками бактерий. Препарат эффективно борется против многих патогенных микроорганизмов, таких как:
- Стафилококки;
- Стрептококки;
- Микоплазма;
- Гемофилюс;
- Клостридии;
- Колибактерии.
Линкомицин способен уничтожить даже те микробы, против которых бессильны тетрациклины и стрептомицины. Но абсолютно бесполезен в случае большинства грамотрицательных бактерий, возбудителей вирусов, простейших и грибков.
Врачи отмечают, что линкомицин является эффективным антибактериальным препаратом, применяемым для лечения гайморита, особенно в случаях, когда заболевание вызвано чувствительными к нему микроорганизмами. Этот антибиотик обладает высокой активностью против грамположительных бактерий, включая стафилококки и стрептококки, что делает его полезным в терапии синуситов, вызванных этими патогенами. Однако специалисты подчеркивают, что перед началом лечения необходимо провести микробиологическое исследование, чтобы определить чувствительность возбудителя к препарату. Кроме того, важно учитывать возможные побочные эффекты и противопоказания, такие как аллергические реакции или заболевания печени. Врачи рекомендуют строго следовать назначенной дозировке и курсу лечения, чтобы избежать развития резистентности и обеспечить максимальную эффективность терапии.

Линкомицин капсулы инструкция по применению препарата: Показания, как применять, обзор препарата
Действие на организм
При приёме внутрь, препарат очень быстро абсорбируется из желудка. Около 40% лекарства всасывается в кровь и распространяется по всему организму, проникая в ткани и жидкости. Одновременный приём пищи снижает всасываемость лекарства, что в свою очередь, снижает его эффективность.
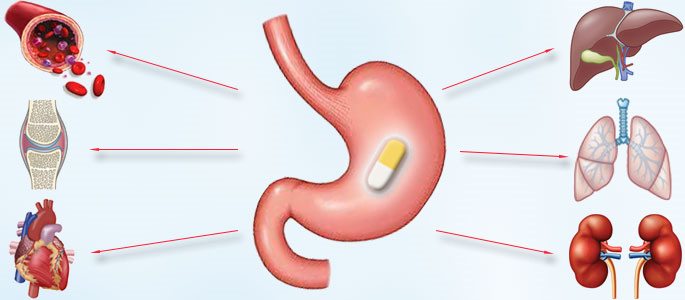
Самая высокая концентрация препарата наблюдается в почках, слюне, сердечной мышце, печени, половых органах, костных тканях и бронхах. Он способен преодолеть плацентарный барьер и попадает в грудное молоко.
Время выведения линкомицина из организма составляет 5–6 часов, у пациентов, имеющих заболевания почек, это время может быть больше.
Препарат препятствует росту болезнетворных бактерий, которые вызывают гайморит. Он также предотвращает развитие заболевания и опасных осложнений гайморита, таких, как менингит, остеомиелит и воспаление глазных нервов.
Применение и дозировка
- Время приёма.
-
Таблетки принимают за 1,5 часа до еды или через 3 часа после.
- Детям.
-
Линкомицин назначается детям начиная с 1 месяца. Дозировка суточного приёма для детей до 14 лет составляет 30–60 мг на 1 кг массы тела (в 2–3 приёма с перерывами 8–12 часов).
- Взрослым.
-
Взрослые могут принимать до 2000 мг препарата в сутки, по 500 мг 3–4 раза.
- Продолжительность.
-
Длительность приёма лекарства зависит от динамики заболевания и в среднем составляет 1–2 недели.
Линкомицин также можно использовать в виде уколов, внутривенно и внутримышечно. При инъекционной форме приёма препарата максимальная суточная доза для взрослого человека не должна превышать 1200 мг. Уколы делают два раза в день. При осложнённом течении гайморита врач может увеличить дозировку до 1800 мг в сутки, разделённых на три приёма. Антибактериальные уколы, как правило, делают в больнице, так что проводить такие манипуляции самому, не рекомендуется.
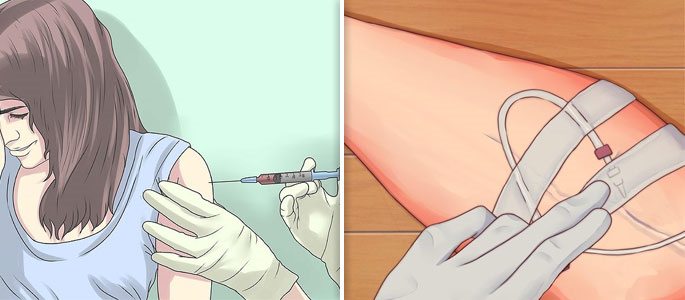
Дозу препарата для инъекции детям подбирают из расчёта 10–20 мг на 1 кг веса тела. Если приём назначается внутривенно, то вводить лекарство можно только при помощи капельницы через каждые 8–12 часов. Взрослые пациенты получают по 600 мг препарата 1–2 раза в сутки внутримышечно или в виде капельницы по 600 мг в 250 мл растворе хлорида натрия. При применении линкомицина пациент должен обязательно придерживаться следующих правил:
- При необходимости длительной терапии данным препаратом необходимо время от времени делать анализ мочи и крови;
- При внутримышечном введении лекарства, прокол должен быть очень глубоким, чтобы предотвратить образование тромбов и отмирание тканей;
- Не использовать препарат внутривенно, не разведя его предварительно специальными составами.
Линкомицин – это антибиотик, который часто обсуждается в контексте лечения гайморита. Многие пациенты отмечают его эффективность в борьбе с инфекциями, вызванными чувствительными к нему микроорганизмами. В отзывах упоминается, что препарат помогает быстро облегчить симптомы, такие как заложенность носа и головная боль. Однако некоторые пользователи также сообщают о побочных эффектах, включая расстройства пищеварения и аллергические реакции. Важно отметить, что линкомицин не всегда является первым выбором для лечения гайморита, и его назначение должно основываться на результатах анализов и рекомендациях врача. Пациенты подчеркивают, что самостоятельное лечение может привести к осложнениям, поэтому консультация со специалистом является необходимой.

Лечение гайморита народными средствами. Быстрый способ, может помочь быстро вылечить гайморит.
Побочные действия
Среди побочных эффектов приёма линкомицина выделяют следующие:
- Головная боль;
- Головокружения;
- Снижение АД;
- Тошнота и рвота;
- Нарушение пищеварения;
- Зуд, покраснение кожных покровов, сыпь;
- Кандидоз;
- Анафилактический шок.
Также могут наблюдаться такие нежелательные явления, как боли в области желудка, стоматит, язвы на слизистой ротовой полости. Если терапия проводится длительное время, то возможно изменение в составе крови.
Противопоказания
Противопоказаниями к применению линкомицина являются:
- Серьёзные нарушения функции почек и печени;
- Дети до 1 месяца;
- Беременность и период кормления грудью;
- Повышенная чувствительность к некоторым компонентам препарата.
Важно! При появлении признаков индивидуальной непереносимости линкомицина, его приём следует немедленно прекратить. Использование линкомицина при инфекциях слизистых оболочек, должно производиться только под контролем лечащего врача.
В условиях развития новых современных препаратов, антибактериального действия, линкомицин применяется всё реже. Неудобная форма дозировки и быстрый период выведения делает этот препарат менее конкурентным в борьбе с возбудителями заболеваний. Исключением являются случаи, когда пациент обладает выраженной аллергической реакцией к другим антибиотикам. В этом случае линкомицин становится подходящей альтернативой.

Как вылечить гайморит в домашних условиях/ ПРОВЕРЕНО НА СЕБЕ
Вопрос-ответ
Какие болезни лечит Линкомицин?
Линкомицин эффективен в отношении грамположительных микроорганизмов (стафилококков, стрептококков, пневмококков, палочки дифтерии) и некоторых анаэробов, в том числе возбудителей газовой гангрены и столбняка. Активен также в отношении микоплазм. На грамотрицательные бактерии, грибы и вирусы не действует.
Кому нельзя Линкомицин?
Линкомицин следует с осторожностью назначать пациентам, у которых в анамнезе есть заболевания ЖКТ, особенно колит. Линкомицин нельзя применять для лечения больных менингитом, поскольку уровни препарата в спинномозговой жидкости недостаточны.
Как быстро помогает Линкомицин?
Максимальная концентрация антибиотика в крови достигается через 20-40 минут после инъекции и сохраняется на протяжении 3-6 часов, а терапевтическая концентрация — на протяжении 24 часов. Линкомицин быстро и хорошо всасывается из места инъекции и проникает во все органы и ткани организма, в том числе и костную ткань.
Когда начинает действовать антибиотик Линкомицин?
Линкомицин начинает действовать уже после пары часов после приема. Кроме того, препарат способен содействовать укреплению зубной эмали и стать прекрасным профилактическим средством для различного рода воспалительных процессов.
Советы
СОВЕТ №1
Перед началом лечения линкомицином обязательно проконсультируйтесь с врачом. Самолечение может привести к неправильной дозировке и ухудшению состояния.
СОВЕТ №2
Обратите внимание на возможные побочные эффекты линкомицина, такие как расстройства пищеварения или аллергические реакции. Если вы заметили что-то необычное, немедленно сообщите об этом врачу.
СОВЕТ №3
Соблюдайте режим приема препарата, не пропуская дозы и не превышая рекомендованную продолжительность курса лечения. Это поможет избежать развития устойчивости бактерий к антибиотику.
СОВЕТ №4
Дополнительно используйте методы поддерживающей терапии, такие как промывание носа солевыми растворами и ингаляции, чтобы облегчить симптомы гайморита и улучшить общее состояние.
Внешний вид упаковки может отличаться от фотографии
Средняя цена в аптеках
126 ₽
Среди
4861
аптеке,
подключенных к Ютеке в вашем регионе
Оплата и способы получения
в Москве
Самовывоз
Сегодня бесплатно
из 712 аптек
Завтра или позже бесплатно
из 4861 аптеки
Оплата картой или наличными в аптеке
Доставка
Конкретный срок и стоимость доставки зависят от вашего адреса
Информация о товаре
Действующее вещество:
Линкомицин
Количество в упаковке:
20 шт.
Страна:
Россия
Страна производства может отличаться, проверяйте при получении заказа
Инструкция на Линкомицин 250 мг, капсулы, 20 шт.
Состав
| Капсулы | 1 капс. |
| линкомицина гидрохлорида моногидрат | 0,25 г |
| вспомогательные вещества: крахмал картофельный; пудра сахарная |
в контурной ячейковой упаковке 10 шт.; в пачке картонной 2 упаковки.
Описание
Капсулы с белым корпусом и желтой крышкой. Содержимое капсул — гранулы белого цвета.
Фармакодинамика
В терапевтических дозах действует бактериостатически. При более высоких концентрациях оказывает бактерицидное действие. Подавляет синтез белка в микробной клетке. Активен преимущественно в отношении грамположительных бактерий: аэробных Staphylococcus spp. (в т.ч. продуцирующих пенициллиназу); Streptococcus spp., в т.ч. Streptococcus pneumoniae (за исключением Enterococcus faecalis), Corynebacterium diphtheriae; анаэробных спорообразующих бактерий Clostridium spp. Линкомицин активен также в отношении грамотрицательных анаэробных бактерий: Bacteroides spp., Mycoplasma spp. Heчувствительны к линкомицину большинство грамотрицательных бактерий, грибы, вирусы, простейшие. Устойчивость вырабатывается медленно. Между линкомицином и клиндамицином существует перекрестная резистентность.
Фармакокинетика
После приема внутрь 30–40% всасывается из ЖКТ. Прием пищи замедляет скорость и степень всасывания. Линкомицин широко распределяется в тканях (включая костную) и жидкостях организма. Проникает через плаценту. Частично метаболизируется в печени. T1/2 — около 5 ч. Выводится в неизмененном виде и в виде метаболитов с мочой, желчью и калом.
Линкомицин: Показания
септические состояния, вызванные стафилококками и стрептококками;
острый и хронический остеомиелит;
пневмония;
гнойные инфекции кожи и мягких тканей;
рожистое воспаление;
отит и другие инфекции, вызванные чувствительными к этому антибиотику микроорганизмами.
Характеристика
Антибиотик из группы линкозамидов.
Способ применения и дозы
Внутрь, за 1–2 ч до еды или через 2–3 ч после еды, обильно запивая водой 2–3 раза в день с интервалом 8–12 ч.
Разовая доза для взрослых — 500 мг, суточная — 1–1,5 г. Детям в возрасте от 3 до 14 лет внутрь — 30–60 мг/кг/сут. Продолжительность лечения устанавливается врачом.
Применение при беременности и кормлении грудью
Линкомицин проникает через плаценту, выделяется с грудным молоком. Применение при беременности противопоказано. При необходимости применения в период лактации следует решить вопрос о прекращении грудного вскармливания.
Линкомицин: Противопоказания
повышенная чувствительность к линкомицину и клиндамицину;
выраженные нарушения функции печени и/или почек;
беременность;
лактация (грудное вскармливание);
Линкомицин: Побочные действия
Со стороны пищеварительной системы: тошнота, рвота, боли в эпигастрии, диарея, глоссит, стоматит; транзиторное повышение уровня печеночных трансаминаз и билирубина в плазме крови; при длительном применении в высоких дозах возможно развитие псевдомембранозного колита.
Со стороны системы кроветворения: обратимая лейкопения, нейтропения, тромбоцитопения.
Аллергические реакции: крапивница, эксфолиативный дерматит, отек Квинке, анафилактический шок.
Эффекты, обусловленные химиотерапевтическим действием: кандидоз.
Прочие: снижение АД, головокружение, слабость (при быстром в/в введении).
Взаимодействие
При одновременном применении с пенициллинами, цефалоспоринами, хлорамфениколом или эритромицином возможен антагонизм противомикробного действия. При одновременном применении со средствами для ингаляционного наркоза или миорелаксантами периферического действия отмечается усиление нервно-мышечной блокады, вплоть до развития апноэ.
Особые указания
При нарушении функции печени и/или почек следует уменьшить разовую дозу линкомицина на 1/3–1/2 и увеличить интервал между приемами. При длительном применении препарата необходим систематический контроль функции почек и печени. В случае развития псевдомембранозного колита линкомицин следует отменить и назначить ванкомицин или бацитрацин.
Характеристики
Торговое название
Линкомицин
Действующее вещество (МНН)
Линкомицин
Дозировка или размер
250 мг
Первичная упаковка
упаковка контурная ячейковая
Производитель
Производство медикаментов
Условия хранения
В сухом, защищенном от света месте, при температуре не выше 25 °C
Представлено описание активных веществ лекарственного препарата. Описание препарата основано на официально утвержденной инструкции по применению от компании-производителя. Приведенное описание носит исключительно информационный характер и не может быть использовано для принятия решения о возможности применения конкретного лекарственного препарата.
Сертификаты Линкомицин 250 мг, капсулы, 20 шт.
Все товары на сайте имеют сертификат соответствия.
Подробнее о гарантии
Дозировки и формы выпуска Линкомицин
• В наличии в
4939 аптеках
• Самовывоз сегодня
• Доставка недоступна
• В наличии в
4114 аптеках
• Самовывоз сегодня
• Доставка недоступна
• Самовывоз сегодня
• Доставка недоступна
Цены в аптеках на Линкомицин 250 мг, капсулы, 20 шт.
История стоимости Линкомицин 250 мг, капсулы, 20 шт.
минимальнаясредняямаксимальная
Указана средняя стоимость товара в аптеках региона Москва и МО за период и разница по сравнению с предыдущим периодом
Цены Линкомицин и наличие в аптеках в Москве
250 мг, капсулы, 20 шт.
Отзывы о Линкомицин
У данного товара ещё нет отзывов
Ваш может стать первым!
Популярные товары в категории
Популярные товары в Ютеке
Купить Линкомицин, 250 мг, капсулы, 20 шт. в Москве с доставкой в аптеку или домой, сделав заказ через Ютеку
Цена Линкомицин, 250 мг, капсулы, 20 шт. в Москве от 70 руб. на сайте и в приложении
Подробная инструкция по применению Линкомицин, 250 мг, капсулы, 20 шт.
Информация на сайте не является призывом или рекомендацией к самолечению и не заменяет консультацию специалиста (врача), которая обязательна перед назначением и/или применением любого лекарственного препарата.
Дистанционная торговля лекарственными препаратами осуществляется исключительно аптечными организациями, имеющими действующую лицензию на фармацевтическую деятельность, а также разрешение на дистанционную торговлю лекарственными препаратами. Дистанционная торговля рецептурными лекарственными препаратами, наркотическими и психотропными, а также спиртосодержащими лекарственными препаратами запрещена действующим законодательством РФ и не осуществляется.
На информационном ресурсе применяются
рекомендательные технологии
.
Антибиотики при гайморите у взрослых
Обновлено: 16.01.2025

Каменских Кирилл
Врач-стоматолог, челюстно-лицевой хирург. Опыт работы 26 лет. Закончил Омскую государственную медицинскую академию в 1999 г. (специальность «Стоматология»). Кирилл Валерьевич занимается, в том числе исследованиями и научной работой.
Проверено:

Гришова Елена
Врач-стоматолог (терапевт, ортопед) – с опытом работы 25 лет. Является врачом-экспертом в лечении корневых каналов зубов с использованием стоматологического операционного микроскопа, протезировании зубов.
Из этой статьи Вы узнаете:
- наиболее эффективные антибиотики при гайморите (синусите),
- уколы цефтриаксона при гайморите,
- инструкция по применению, почему может не помогать,
- как избежать диареи после приёма антибиотиков.
Антибиотики при гайморите (синусите) – выбираются с учётом длительности заболевания, тяжести клинической симптоматики, а также чувствительности типичных возбудителей этой болезни к различным группам антибиотиков. Наиболее эффективные антибиотики при гайморите у взрослых – это β-лактамные лактомазозащищённые синтетические пенициллины (например, препараты на основе амоксициллина и клавулановой кислоты), а также цефалоспорины III-IV поколения, современные фторхинолоны, а в некоторых случаях – еще и макролиды.
Многие проводят лечение гайморита цефтриаксоном, который относится к цефалоспоринам III поколения и предназначен для парентерального введения (в/м или в/в). Этот антибиотик действительно является одним из самых эффективных препаратов для лечения тяжёлой формы гайморита, но в ряде случаев он не является оптимальным выбором и может быть даже неэффективен. Поэтому ниже мы также расскажем – из-за чего цефтриаксон при гайморите может вам не помочь.
Разные формы гайморита на КТ –
Рентгеновский снимок придаточных пазух носа. Стрелкой показан уровень жидкости в гайморовой пазухе справа (на снимке – она слева). В совокупности с др. симптомами был поставлен диагноз: «Острый гнойный гайморит», что является показанием к проведению антибиотикотерапии.
Компьютерная томография верхнечелюстных (гайморовых) пазух. Стрелки показывают на значительное утолщение слизистой оболочки одной из гайморовых пазух. Воспалительный процесс локализован в области дна пазухи (вблизи верхушек корней 5-6-7-8 верхних зубов). Диагноз предварительный – Односторонний хронический катаральный гайморит (одонтогенного происхождения).
Какие антибиотики при гайморите у взрослых – будут наиболее эффективны? Выбор напрямую зависит от формы вашего гайморита (он может быть острым, хроническим, рецидивирующим и т.д.), а также от причины его возникновения. Гайморит может быть риногенного или одонтогенного происхождения, т.е. он может быть связан – либо с инфекцией в носовых ходах, либо с воспалением у корней верхних боковых зубов. Во всех этих случаях – в пазухах будет абсолютно разный состав возбудителей инфекции.
Разные группы антибиотиков – имеют свойство с разной эффективностью действовать на разные виды патогенных бактерий. Поэтому лучший антибиотик при гайморите – можно выбрать только на основе анализа каждого клинического случая в отдельности. Например, при остром гайморите анаэробы высеиваются только в 10% случаев, в то время как при хроническом риногенном гайморите – уже до 48% случаев. А при любых формах гайморита одонтогенного происхождения (связанного с зубами) – в пазухе будет значительно преобладать именно анаэробная инфекция.
По течению воспалительного процесса – гайморит делят на следующие формы:
- острый гайморит;
- острый рецидивирующий гайморит;
- хронический гайморит;
- обострение хронического гайморита.
Реклама
ООО «Илатан», ИНН 7709918259, erid=2VfnxxdpKKn
Есть противопоказания. Посоветуйтесь с врачом.
Выбор антибиотика зависит от формы гайморита (от состава микрофлоры в пазухе) –
Если развитие острого гайморита происходит на фоне ОРВИ, то, соответственно, первичным будет вирусное инфицирование пазухи. В этом случае вирусы – как бы «прокладывают дорогу» бактериальной инфекции, которая обычно присоединяется лишь на 3-4 день заболевания. Соответственно, при остром гайморите (остром риносинусите) вирусной природы – в первые 3 дня приём антибиотиков не показан.
Состав бактериальной микрофлоры:
Острые формы гайморита
Основными возбудителями будут – Streptococcus pneumoniae, Haemophilus influenzae. Реже – Moraxella catarrhalis, Streptococcus pyogenes, Staphylococcus aureus, а также анаэробы. Хотя от 8 до 25% от всех случаев – могут высеваться и внутриклеточные возбудители (Mycoplasma pneumoniae, Chlamydia pneumoniae).
Хронический риногенный гайморит
При этой форме гайморита резко увеличивается количество анаэробов. Если при острых формах анаэробов около 10%, то при хроническом риногенном гайморите их высеиваются уже (по данным разных авторов) – от 20 до 48% от всех случаев. Прежде всего это – Prevotella sрр., Fusobacterium sрр., Bacteroides sрр., анаэробные стрептококки и другие. А вот среди аэробных возбудителей при хроническом риногенном гайморите высеваются – Streptococcus sрр., Haemophilus influenzae, Prevotella aeruginosa, Staphylococcus aureus, Moraxella catarrhalis.
Одонтогенный гайморит
Одонтогенный гайморит практически всегда имеет первично-хронический характер, и поэтому здесь в ещё большей степени преобладают анаэробы (в более чем 68% случаев) – прежде всего это Bacteroides и Fusobacterium, а также Peptostreptococcus spp.. Среди аэробных микроорганизмов при одонтогенном гайморите высеваются прежде всего Staphylococcus haemolyticus и Staphylococcus auricularis. Также примерно в 50% случаев высеваются и грибы рода Candida (!!!)
→ Состав микрофлоры при одонтогенном гайморите
* Соответственно, зная форму гайморита и предполагая состав возбудителей, врач сможет назначить вам оптимальный антибиотик. Ниже вы можете увидеть подробную информацию о том – как выбрать эффективный антибиотик при гайморите у взрослых.
Наиболее эффективные антибиотики при гайморите –
Антибиотики выбора для лечения гайморита:
- β-лактамные лактомазозащищённые синтетические пенициллины, и прежде всего это амоксициллин + клавулановая кислота (антибиотики Аугментин, Амоксиклав), но также подойдут и следующие комбинации – «ампициллин + сульбактам», или «пиперациллин + тазобактам», «цефоперазон + сульбактам», «тикарциллин + клавулановая кислота», либо уже карбапенемы (имипенем или меропенем);
- макролиды (азитромицин, кларитромицин);
- фторхинолоны III-IV поколения (левофлоксацин, моксифлоксацин);
- цефалоспорины III-IV поколения (цефтриаксон, цефтибутен, цефепим);
- оксазолидоны (линезолид) – только после посева на микрофлору и выделении мультирезистентной флоры.
Схема: наиболее эффективные антибиотики при гайморите (синусите). Выбор зависит – исключительно от формы гайморита и степени тяжести воспалительного процесса. Обратите внимание, что все применяемые при гайморите антибиотики – принято делить на препараты 1-го и 2-го выбора.
Важно: при хроническом гайморите одонтогенного происхождения (связанном с зубами) – помимо антибиотика необходимо принимать и противогрибковый препарат, эффективный против грибов рода Candida. При этой форме гайморита – грибковая микрофлора присоединяется к бактериальной примерно в 50% случаев. Симбиоз грибковой и бактериальной микрофлоры – делает бактерии менее чувствительными к любым антибиотикам, что значительно ослабит эффект от антибиотикотерапии.
Антибиотики при лёгкой и среднетяжёлой формах острого гайморита –
С учётом американских клинических рекомендаций – препаратом 1-го выбора будет либо комбинация амоксициллина с клавулановой кислотой (амоксиклав, аугментин), либо цефалоспорины II и III поколений (например: цефтибутен, цефаклор). Клиническая эффективность амоксициллина с клавулановой кислотой – составляет 93,5%, а цефалоспоринов – порядка 85-87%. Получается, что наиболее эффективным будет применение именно комбинации амоксициллина с клавулановой кислотой.
Антибиотик АМОКСИКЛАВ. Каждая таблетка содержит – 500 мг амоксициллина + 125 мг клавулановой кислоты. Амоксиклав при гайморите нужно принимать – по 1 таб. х 3 раза в день (каждые 8 часов). Длительность приёма – от 7-8 дней и до 10-14 дней, что зависит от формы гайморита и его тяжести.
Антибиотик АУГМЕНТИН (имеет такой же состав, высокое качество, но при этом стоит дешевле). Схема приёма – аналогична. При одонтогенном/ гнойном гайморите – Аугментин или Амоксиклав нужно принимать только в сочетании с Метронидазолом (последний следует принимать по схеме – 500 мг х 3 раза в день).
Итак, чтобы усилить действие Амоксиклава и Аугментина в отношении анаэробных бактерий (что особенно важно при одонтогенном происхождении гайморита, гнойном гайморите) – их можно и нужно комбинировать с метронидазолом. Эффективность любого варианта терапии оценивается через 3 дня, и при отсутствии положительной динамики основных симптомов заболевания – проводится замена антибиотика. Менять нужно на антибиотик, который будет эффективен против внутриклеточных возбудителей (типа Mycoplasma pneumoniae, Chlamydia pneumoniae).
И в этом случае выбор падает – либо на антибиотик из группы макролидов (азитромицин или кларитромицин), либо на современные фторхинолоны (левофлоксацин или монофлоксацин).
Нужно отметить, что против внутриклеточных возбудителей β-лактамные лактомазозащищённые синтетические пенициллины (Амоксиклав, Аугментин), а также цефалоспорины – вообще неэффективны. При этом в ряде научных работ отмечается, что внутриклеточные возбудители высеваются при острой/ острой рецидивирующей формах гайморита – от 8 до 25% от всех случаев. Т.е. тут сразу не угадаешь.
Важные моменты.
1. При наличии у пациента пенициллин-резистентных штаммов пневмококков (Streptococcus pneumoniae) – эффективность цефалоспоринов II-го поколения в отношении них будет заметно ниже. Тоже самое касается и макролидов. Поэтому при «острой» и «острой рецидивирующей» формах гайморита – антибиотик 1-го выбора это всё-таки «амоксициллин с клавулановой кислотой» (аугментин или амоксиклав), либо цефалоспорины III поколения (цефтибутен). В качестве антибиотиков 2-го выбора – использовать современные фторхинолоны (левофлоксацин или монофлоксацин).
2. При аллергии на β-лактамные антибиотики (пенициллины и цефалоспорины) – препаратами 1-го выбора будут макролиды, а в качестве антибиотиков 2-го выбора – современные фторхинолоны (левофлоксацин или монофлоксацин). И ещё раз напомним, что при лёгком и среднетяжёлом течении «острого» и «острого рецидивирующего» гайморита – антибиотики назначаются только в таблетках.
Какие антибиотики назначать нельзя.
Очень часто врачи допускают ошибки, назначая пациентам с гайморитом следующие препараты: сульфаниламиды, доксициклин, гентамицин, тетрациклин, линкомицин, либо метронидазол – в виде монотерапии. Также ошибкой является назначение таких таблеток от гайморита как ципрофлоксацин (т.к. фторхинолоны 2-го поколения имеют очень низкую эффективность против бактерии S.pneumoniae).
Также при назначении антибиотика стоит учитывать опыт их назначения в прошлом. Например, многие пациенты отмечают, что у них ранее при приёме таких препаратов как Амоксиклав или Аугментин (т.е. комбинации амоксициллин + клавулановая кислота) – развивалась диарея. Учитывая такой анамнез, лучше всего сразу назначить такому пациенту современные фторхинолоны III-IV поколения.
Антибиотики при тяжёлом течении острого гайморита –
Тяжёлое течение гайморита – это показание к госпитализации пациента (особенно при наличии тяжёлой сопутствующей патологии, иммунодефицитных состояний, а также при подозрении на риск развития осложнений). В данном случае антибиотики должны вводиться только парентерально – внутривенно или внутримышечно. Причём оптимальным является именно внутривенный путь введения, но по мере улучшения состояния – пациента можно перевести на пероральный приём антибиотика.
Эффективные антибиотики при остром гайморите:
- β-лактамные лактомазозащищённые синтетические пенициллины – это та же самая комбинация амоксициллин + клавулановая кислота (антибиотик Амоксиклав – только во флаконах для в/в введения), а также такие комбинации как «ампициллин + сульбактам», «пиперациллин + тазобактам», «цефоперазон + сульбактам», «тикарциллин + клавулановая кислота», а также карбапенемы (имипенем или меропенем);
- цефалоспорины III-IV поколения (цефтриаксон, цефотаксим, цефепим, цефпиром);
- фторхинолоны III-IV поколения (левофлоксацин, спарфлоксацин, моксифлоксацин).
Амоксиклав флаконы для в/в введения. В каждом флаконе – 1000 мг амоксициллина, 200 мг клавулановой кислоты (это разовая доза препарата – для взрослых и детей от 12 лет). Инфузии проводят с интервалом 8 час., но в случае тяжёлого течения инфекции – с интервалом 6 часов. Стоимость 1 упаковки – от 620 рублей (в уп. 5 флаконов).
При выборе между этими группами антибиотиков – стоит опираться на происхождение гайморита (источник инфицирования). При риногенном гайморите – частота выделения анаэробной флоры значительно меньше, поэтому антибиотиками 1-го выбора могут считаться β-лактамные лактомазозащищённые синтетические пенициллины, т.е. амоксиклав. Препараты 2-го выбора – цефалоспорины III-IV поколения, карбапенемы.
Но при непереносимости пациентом β-лактамных антибиотиков (либо если высеваются внутриклеточные возбудители) – в этом случае назначают современные фторхинолоны III-IV поколения. Также есть нюансы назначения антибиотиков при одонтогенной природе гайморита, либо когда происходит сочетанное инфицирование пазухи (и со стороны полости носа, и со стороны боковых зубов верхней челюсти). Об этих нюансах мы расскажем в следующем разделе.
Антибиотики при обострении хронического гайморита –
Путь введения антибиотиков в этом случае также только парентеральный (в/м или в/в). Применяются всё те же самые антибиотики как и при тяжёлом течении «острого» и «острого рецидивирующего» гайморита, но с небольшими нюансами.
1) Если эта форма гайморита имеет риногенное происхождение – тут по данным разных авторов анаэробные бактерии в этом случае высеваются с частотой от 20 до 48%. Исходя из этого, антибиотиками 1-го выбора тут будут по-прежнему β-лактамные лактомазозащищённые синтетические пенициллины (амоксиклав, причём его можно комбинировать с метронидазолом). Антибиотиками 2-го выбора – цефалоспорины III-IV поколения. Тут стоит учесть, что цефалоспорины III поколения (например, цефтриаксон) обладают большей активностью в отношении анаэробов, чем цефалоспорины IV поколения.
2) При хроническом гайморите одонтогенного происхождения (связанного с очагами воспаления у верхушек корней 5-6-7-8 верхних зубов) – ситуация будет немного другой. Здесь в ещё большей степени будут преобладать анаэробы (около 68% от всех случаев одонтогенного гайморита) – прежде всего это Bacteroides и Fusobacterium, + в минимум в 50% случаев высеваются ещё и грибы рода Candida. Как правило, пациенты с хроническим одонтогенным гайморитом имеют за плечами много курсов антибактериальной терапии (как в результате самолечения, так и ошибок при диагностике одонтогенной природы гайморита Лор-врачами).
У таких пациентов антибиотиками 1-го выбора будут – комбинация «амоксициллин + клавулановая кислота», а 2-го выбора – это фторхинолоны III-IV поколения. Современные фторхинолоны будут предпочтительнее и цефалоспоринов III-IV поколения (которые можно было при риногенном гайморите), т.к. они имеют более выраженную активность в отношении анаэробов – прежде всего это Bacteroides и Fusobacterium. Кроме того, если пациент с хроническим одонтогенным гайморитом уже неоднократно принимал цефалоспорины, то с большой вероятностью указанные анаэробы + Staphylococcus haemolyticus – могли приобрести к ним устойчивость.
→ Состав микрофлоры при одонтогенном гайморите
Что делать, если у пациента одонтогенный гайморит –
При одонтогенном инфицировании пазухи будет недостаточно ограничиться только лишь назначением сильного антибиотика, плюс промывать пазуху при помощи синус-катетера Ямик. Дело в том, что в этом случае мы будем иметь очаг воспаления у верхушек корней одного из 5-6-7 зубов, что связано с наличием инфекции в корневых каналах причинного зуба. Приём антибиотиков не позволяет санировать корневые каналы. Поэтому при обнаружении воспалительных очагов у верхушек корней и плохо запломбированных корневых каналов – необходима санация корневых каналов.
В этом случае причинный зуб вскрывается, проводится дезинфекция корневых каналов, в которых на срок до 1-1,5 месяца оставляется препарат на основе гидроксида кальция. Если этого не сделать – инфицирование пазухи будет продолжаться, и со временем мы получим новые случаи обострения хронического гайморита. В ряде случаев (по причине того, что корневые каналы запломбированы неидеально сразу у нескольких зубов в проекции пазухи) – необходимо санировать сразу все боковые зубы.
Очень важно: целью антибиотикотерапии заключается в полной эрадикации (удалении) возбудителя инфекции из пазухи. Ошибки лор-врачей в диагностике одонтогенной причины гайморита приводят к тому, что антибиотикотерапия не приводит к эрадикации возбудителя, и пациент получает лишь временное улучшение. По статистике, если взять все случаи одонтогенного гайморита за 100%, то ошибки в установлении одонтогенной причины инфицирования пазухи – достигают порядка от 50 до 80%.
Ещё один важный момент – он касается примерно от 25 до 40% пациентов, которые являются носителями метициллин-резистентного Золотистого стафилококка (Staphylococcus aureus или MRSA). Эта бактерия может обитать в носовых ходах, гайморовых пазухах, а также верхней части дыхательных путей, и при снижении иммунитета – приводить к рецидивам гайморита. Ниже мы расскажем, что с этим делать.
Антибиотик Цефтриаксон при гайморите –
Антибиотик Цефтриаксон относится к цефалоспоринам III-го поколения. Препараты цефтриаксона высокого качества – это безусловно Роцефин (Hoffman La Roche) и Лендацин (Lek), но это не только дорогие препараты, но они к тому же ещё и стали недоступны для российского рынка. Из приемлемых по качеству препаратов – можно назвать «Цефтриаксон Каби» (производство Португалия). Стоимость 1 упаковки 10 флаконов с дозировкой 1000 мг – составит от 1100 рублей. И мы не советуем делать выбор в пользу дешёвых российских дженериков, которые стоят по 30-40 рублей за флакон 1000 мг (1 г). Разница в эффективности, а также рисках развития антибиотико-ассоциированной диареи – просто огромная.
Цефтриаксон Каби, флаконы 1000 мг (1 г). Показан как для в/м, так и для в/в введения. Стандартная схема применения для взрослых – по 2 г х 1 раз в сутки. Длительность терапии зависит от формы гайморита и степени его тяжести (от 7-8 дней и в среднем – до 14 дней).
→ Как правильно делать инъекции внутримышечно
Подробная схема применения.
Давайте разберёмся как принимать Цефтриаксон при гайморите. Этот препарат может применяться только парентерально (т.е. либо внутримышечно, либо внутривенно). Его назначают только при тяжёлом течении острого гайморита или обострении хронического, но в ряде случаев он может быть назначен даже при средне-тяжёлой форме. Стандартная дозировка цефтриаксона при гайморите у взрослых и детей старше 12 лет – составляет по 2 г х 1 раз в сутки (при отсутствии угрозы осложнений и отсутствии иммунодефицитных состояний).
Сколько дней колоть взрослому Цефтриаксон при гайморите – будет зависеть от тяжести течения болезни. Если речь идёт о среднетяжёлой форме гайморита, то инъекции обычно делаются внутримышечно в течение 3-х дней (после этого определяется эффективность антибиотикотерапии) и далее пациента переводят на приём похожего антибиотика только перорально (в таблетках). В общей сложности антибиотикотерапия при среднетяжёлой форме острого гайморита обычно длится 7-8 дней (но если речь идёт не об острой форме гайморита, а об обострении хронического – иногда и до 14 дней).
При тяжёлом течении гайморита препарат оптимально вводить внутривенно. Стандартная суточная дозировка по прежнему 2 г, но в случае угрозы осложнений, при наличии тяжелой сопутствующей патологии, иммунодефицитных состояний – дозировка может быть увеличена до 4 г, но в этом случае эта дозировка разделяется на 2 приёма (внутривенные инфузии в течение 30 минут) – с интервалом 12 часов. Общая продолжительность антибиотикотерапии тяжёлых форм острого гайморита обычно составляет 10 дней, иногда до 14 дней.
Но, если речь идёт о тяжёлой форме обострения хронического гайморита – тут длительность приёма антибиотиков может составить даже до 3 недель. Причём во всех вышеуказанных случаях по-прежнему оптимально использовать так называемую «ступенчатую антибиотикотерапию», когда после периода внутримышечного или внутривенного введения пациент переводится на пероральный приём аналогичного препарата (с аналогичным спектром антибактериальной активности).
→ Другие группы препаратов для лечения гайморита
В каких случаях цефтриаксон не помогает при гайморите –
- Если ваш гайморит был вызван внутриклеточными возбудителями (по данным разных авторов – от 8 до 20% от всех случаев) – такими как Mycoplasma pneumoniae и Chlamydia pneumoniae. Либо ваш гайморит был вызван метициллин-устойчивыми штаммами Staphylococcus aureus, либо микроорганизмами, полный список которых вы найдёте в конце этого раздела. Во всех этих случаях цефалоспорины, включая цефтриаксон, будут совершенно неэффективны.
- Если пациент в прошлом уже проходил лечение цефалоспоринами III- IV поколения, то есть риск развития к ним устойчивости анаэробной микрофлоры (особенно у таких как – Bacteroides и Fusobacterium).
- Если у вас одонтогенный гайморит (связанный с наличием воспаления у верхушек корней верхних боковых зубов). В этом случае цефтриаксон может быть недостаточно эффективен просто из-за того, что при одонтогенном гайморите чаще высеваются анаэробы, в отношении которых этот антибиотик в принципе действует не так хорошо, как хотелось бы.
Кроме того, при одонтогенном гайморите в 55,8% случаев – у пациента высеваются ещё и грибы рода Candida. Симбиоз бактериальной и грибковой микрофлоры имеет интересный эффект – грибы способны снижать чувствительность своих подельников (бактерий) к антибиотикам, т.е. защищают их. Поэтому, если цефтриаксон назначается при одонтогенном гайморите, то его хотя бы нужно комбинировать с системными противогрибковыми препаратами.
- При ошибке в диагнозе (например, когда врач ошибочно определил, что ваш гайморит имеет риногенное происхождение, а на самом деле – он одонтогенный). По статистике – одонтогенный гайморит составляет не менее 32% от всех случаев гайморита у взрослых. Ещё у 8% пациентов – имеет место комбинированное инфицирование пазух (и со стороны носовых ходов, и со стороны верхушек корней зубов). Наличие такой смешанной флоры в пазухе – существенно повышает устойчивость патогенных бактерий к антибактериальной терапии.
Практически все одонтогенные гаймориты имеют первично-хронический характер воспаления, и очень часто Лор-врачи принимают «обострение хронического одонтогенного гайморита» – за «острый» или «острый рецидивирующий» гайморит риногенного происхождения. Это приводит к тому, что источник инфицирования пазухи (боковые зубы верхней челюсти) – сохраняется, и пациент годами лечится от якобы острого рецидивирующего гайморита риногенного происхождения. Лечится безуспешно. Регулярный приём антибиотиков в данном случае приводит только к временному улучшению, но не позволяет добиться полной эрадикации возбудителей из пазухи. Это способствует формированию устойчивости к антибиотикам – у таких микроорганизмов как Bacteroides, Fusobacterium, Peptostreptococcus, Staphylococcus haemolyticus, соответственно, что приводит к утяжелению симптомов последующих обострений гайморита.
Устойчивые виды к цефтриаксону –
- все метициллин-устойчивые штаммы Staphylococcus aureus (!!!);
- грамположительные аэробы: Enterococcus spp., Listeria monocytogenes;
- грамотрицательные аэробы: Acinetobacter baumannii, Pseudomonas aeruginosa, Stenotrophomonas maltophilia;
- другие: Chlamydia spp., Mycoplasma spp., Legionella spp., Ureaplasma urealyticum, Clostridium difficile.
Виды, которые могут приобретать устойчивость к цефтриаксону –
- Анаэробы: Bacteroides spp., Fusobacterium spp., Peptostreptococcus spp., Clostridium perfringens;
- грамположительные аэробы: Staphylococcus epidermidis, Staphylococcus haemolyticus, Staphylococcus hominis;
- грамотрицательные аэробы: Citrobacter freundii, Enterobacter aerogenes, Enterobacter cloacae, Escherichia colic; Klebsiella pneumoniae, Klebsiella oxytoca, Morganella morganii, Proteus vulgaris, Serratia marcescens.
Антибиотик Цефтриаксон при гайморите работает хорошо, только если соблюдаются следующие правила: – 1) Это гайморит риногенного происхождения; 2) Вы не являетесь носителем метициллин-устойчивых штаммов Staphylococcus aureus, т.е. золотистого стафилококка. Сдать анализ на носительство этой бактерии – можно в любой медицинской лаборатории.
Кроме того, цефтриаксон не будет оптимальным выбором при гайморите любого происхождения, если пациент ранее занимался длительным самолечением гайморита, неконтролируемо принимал антибиотики (без/с назначением врача), либо неоднократно принимал антибиотики группы цефалоспоринов в прошлом.
Эффективный антибиотик при гайморите, если вы носитель MRSA (Staphylococcus aureus) –
По статистике – 20-45% людей являются носителями метициллин-резистентных штаммов золотистого стафилококка (MRSA). Если вы из них, то цефалоспорины (включая цефтриаксон), а также антибиотики класса карбапенемов, а также β-лактамные пенициллины – не будут как-то особо эффективны для лечения вашего гайморита. В данном случае оптимальный выбор – это всё-таки фторхинолоны III-IV поколения (левофлоксацин, спарфлоксацин, моксифлоксацин).
Что касается дополнительного средства, которое может быть полезным (для лечения и профилактики обострений гайморита у пациентов, являющихся носителями метициллин-устойчивых штаммов Staphylococcus aureus) – это масляный раствор препарата Хлорофиллипт. Он достаточно часто назначается лор-врачами для проведения влажных ингаляций с использованием небулайзера или ингалятора.
Хлорофиллипт масляный раствор 2%. Активное вещество – экстракт листьев эвкалипта. Этот препарат полезен именно для носителей золотистого стафилококка (Staphylococcus aureus), включая его антибиотико-резистентные штаммы. Что касается др. видов бактерий и вирусов, то он уже не будет как-то особо полезен.
Проблема с носительством золотистого стафилококка в том, что добиться эрадикации (полного удаления) этого возбудителя из дыхательных путей (даже с помощью полного курса антибиотиков) – невозможно. Можно лишь добиться выздоровления, но при очередном снижении иммунитета – у вас может возникнуть новый рецидив гайморита (24stoma.ru). Поэтому периодические курсы ингаляций с помощью масляного раствора препарата Хлорофиллипт – могут быть полезны для предотвращения очередного рецидива.
Но есть ещё один препарат, который позволяет держать MRSA – под контролем. Это мазь с антибиотиком мупироцин, которая показана в том числе и для интраназального применения при носительстве стафилококковой инфекции в носовой полости (включая метициллин-резистентные штаммы Staphylococcus aureus). Пример – мазь Бондерм.
Ну и конечно, мы рекомендуем всем пациентам с риногенным гайморитом (частыми его обострениями) – сдать анализ на носительство метициллин-устойчивых штаммов Staphylococcus aureus (MRSA).
Антибиотик-ассоциированная диарея у взрослых:
Антибиотик-ассоциированная диарея – это термин, отражающий причину возникновения диареи (в данном случае это приём антибиотиков). Главные антибиотики, которые лидируют по риску развития диареи – это производные пенициллинов и цефалоспорины, и ниже вы можете увидеть подробную статистику. Кроме того риск диареи выше именно при приёме таблетированных антибиотиков, но она также возможна и после в/м или в/в введения антибиотиков. Основной возбудитель, который ответственен за диарею после приёма антибиотиков – это Clostridium perfringens.
Развитие диареи происходит прежде всего – в результате подавления антибиотиками не только патогенной флоры, но также и бифидобактерий, лактобактерии, энтерококков, кишечной палочки. Поэтому так важно параллельно с приёмом антибиотиков принимать и пробиотики (специальные препараты, содержащие полезные бактерии для нашего кишечника). Пробиотики могут содержать энтерококки, бифидобактерии или лактобактерии, либо их сочетания. Одни из лучших пробиотиков – препараты Линекс и Бифиформ.
Пробиотик Бифиформ (30 капсул). Внутри каждой капсулы содержатся полезные бактерии для кишечника: Enterococcus faecium – в объёме не менее 1х 10*7 КОЕ, Bifidobacterium longum – не менее 1х10*7 КОЕ. Цена около 700 рублей (уп. 30 капсул), и от 350 рублей – за упаковку 15 капсул.
Однако механизм развития диареи может быть комплексным, т.е. связанным не только с подавлением полезной микрофлоры. Например, при приёме антибиотиков с клавулановой кислотой – последняя может стимулировать диарею за счёт увеличения моторики кишечника (гиперкинетическая диарея). При назначении цефалоспоринов (например, цефиксима или цефоперазона) – из-за неполного их всасывания из просвета кишечника может возникать так называемая «гиперосмолярная диарея».
Какие антибиотики чаще вызывают диарею –
- 10-25% – при назначении амоксициллина/клавуланата,
- 15-20% – при назначении цефиксима (цефалоспорин),
- 5-10% – при назначении ампициллина или клиндамицина,
- 2-5% – при назначении остальных цефалоспоринов (кроме цефиксима) или макролидов (эритромицина, кларитромицина),
- и только 1-2% – при назначении фторхинолонов.
Выводы: при риске развития у пациента антибиотико-ассоциированной диареи – оптимально назначать именно современные фторхинолоны (например, левофлоксацин или моксифлоксацин), к которым чувствительна в том числе и Clostridium perfringens.
Также выделяют особый вид тяжёлой антибиотико-ассоциированной диареи, называемой термином «псевдомембранозный колит», развитие которого связано с другим микроорганизмом – Clostridium difficile. Развитие псевдомембранозного колита в первую очередь ассоциировано с приёмом клиндамицина, ампициллина и цефалоспоринов. Если нужно назначить антибиотик при диарее, связанной с приёмом других антибиотиков, то в тяжёлых случаях это Ванкомицин, в лёгких – можно ограничиться Метронидазолом. Надеемся, что наша статья: Цефтриаксон инструкция по применению при гайморите – оказалась вам полезной!
Дата обновления статьи: 16.01.2025

Врач-стоматолог, челюстно-лицевой хирург. Опыт работы 26 лет. Закончил Омскую государственную медицинскую академию в 1999 г. (специальность «Стоматология»). Кирилл Валерьевич занимается, в том числе исследованиями и научной работой.
Источники:
1. Высшее медицинское образование автора статьи,
2. Но основе личного опыта работы челюстно-лицевым хирургом,
3. National Library of Medicine (Национальная медицинская библиотека США),
4. «Острый синусит» (Шадыев, Изотова),
5. «Комплексное лечение одонтогенных верхнечелюстных синуситов» (Шульман Ф.),
6. «Практические рекомендации по антибактериальной терапии синусита» (Янов, Рязанцев и др.),
7. «Клинические рекомендации по диагностике и лечению острого риносинусита» (Лопатин, Свистушкин).
Положительный опыт комплексного консервативного лечения острого и хронического гайморита в стадии обострения
Статьи
Д. м. н., проф. А.Ю. Овчинников, к. м. н. М.А. Панякина
Первый МГМУ им. И.М. Сеченова, кафедра болезней уха, носа и горла, Москва
Проблема воспалительных заболеваний околоносовых пазух на сегодняшний день крайне актуальна и имеет большое социальное значение. Помимо того, что риносинусит является крайне распространенным заболеванием, он наносит весьма ощутимый финансовый урон обществу, так как наибольшее число больных — люди в возрасте от 18 до 55 лет, то есть наиболее активная и трудоспособная часть населения. В последнее время отмечается ежегодный прирост заболеваемости на 1,5-2%. В силу определенных анатомических особенностей чаще других поражаются верхнечелюстные пазухи.
Рост воспалительных заболеваний околоносовых пазух происходит в первую очередь из-за серьезных экологических сдвигов, в частности, возросшей загрязненности и загазованности воздушной среды, увеличения числа респираторных вирусных инфекций, количества ингалируемых аллергенов, снижения резервных возможностей верхних дыхательных путей, возросшей резистентности флоры в результате нерационального применения антибиотиков.
Физиология
Приступая к обсуждению этиологии и патогенеза синусита, следует определиться с терминологией и классификацией. Чаще всего бактериальный синусит развивается у здорового человека на фоне респираторной вирусной инфекции, и лечение заболевания проводится в амбулаторных условиях. Эту основную по численности группу синуситов называют внебольничными. Помимо нее существуют госпитальные, одонтогенные синуситы, а также синуситы, развившиеся у больных с иммунодеффицитными состояниями. Возбудители и патогенез этих форм принципиально различаются.
Риносинусит — это воспаление слизистой оболочки носа и околоносовых пазух, практически всегда вызываемое застоем секрета, нарушением аэрации пазух и, как следствие, инфицированием. Острые риносинуситы обычно имеют вирусную или бактериальную этиологию, хронические -бактериальную, реже грибковую. Пусковым моментом в развитии острого синусита, как правило, бывает вирусная инфекция, причем наиболее типичным возбудителем являются риновирусы (более 80% случаев). Исследования, проведенные с использованием компьютерной, магнитно-резонансной томографии, а также в результате реоэнцефалографии и биомикроскопии, показали, что почти у 90% больных ОРВИ в слизистой оболочке околоносовых пазух выявляются изменения в виде отека, нарушения микроциркуляции и застоя секрета. Однако лишь у 0,5-2% больных развивается бактериальный воспалительный процесс. Для возникновения инфекционного процесса ведущее значение, наряду с вирулентными свойствами возбудителя, имеет состояние макроорганизма. Оно определяется сложным комплексом факторов и механизмов, тесно связанных между собой, и характеризуется как чувствительность и резистентность к инфекции. Не менее важную роль в развитии синусита (и особенно для его хронизации) играют аномалии строения внутриносовых структур и решетчатого лабиринта. Нарушение нормальных анатомических взаимоотношений в полости носа изменяет аэродинамику, способствуя попаданию неочищенного воздуха в околоносовые пазухи, повышая тем самым риск развития воспаления. Полипы, отечная слизистая оболочка, искривленная перегородка носа, шипы и гребни перегородки носа (расположенные на уровне среднего носового хода), булла и парадоксальный изгиб средней носовой раковины, патологические варианты строения крючковидного отростка нарушают проходимость естественных отверстий околоносовых пазух и приводят к стагнации секрета и снижению парциального давления кислорода в околоносовых пазухах. Дополнительное соустье верхнечелюстной пазухи в задней фонтанелле также является патологическим фактором, предрасполагающим к развитию синусита. Из-за противоположной направленности мукоциллиарного транспорта на внутренней и внешней поверхностях фонтанеллы наличие двух или более отверстий создает условия для рециркуляции, то есть заброса побывавшей в полости носа и инфицированной слизи обратно в верхнечелюстную пазуху.
Переходя к рассмотрению микробного пейзажа синусита, следует подчеркнуть, что вирусное инфицирование является лишь первой фазой заболевания, и оно «прокладывает путь» бактериальной инфекции. В условиях нормального функционирования механизма мукоциллиарного транспорта бактерии не имеют возможности для достаточно длительного контакта с клетками эпителия полости носа. При поражении слизистой оболочки вирусом продлевается время контакта патогенных бактерий с клетками и становится возможным вторичное бактериальное инфицирование.
Ранее существовало представление о стерильности околоносовых пазух. Однако это вряд ли возможно, так как согласно законам нормальной физиологии околоносовые пазухи имеют постоянный контакт с другими отделами верхних дыхательных путей, где постоянно вегетирует самая разнообразная микрофлора. Возбудителями инфекционного синусита могут быть как патогенные, так и условно-патогенные микроорганизмы. Последние являются естественными обитателями организма человека и вызывают заболевания при снижении местного и общего иммунитета. Именно представители условно-патогенной микрофлоры являются наиболее значимыми возбудителями бактериального синусита, подтверждая положение, что при любом синусите в той или иной степени страдает иммунитет.
Среди возбудителей синусита наиболее значимыми в настоящее время являются S.pneumoniae, H.influenzae, реже встречается Moraxella catarrhalis.
Streptococcus pneumoniae — это грамположительный кокк из группы α-гемолитических стрептококков. Различные серотипы пневмококка, последовательно сменяя друг друга, колонизируют носоглотку сразу после рождения. По мере выработки в организме соответствующих факторов иммунитета и элиминации одного микроорганизма его сменяет другой, причем период персистенции конкретного серотипа может длиться от одного до двеннадцати месяцев. Поскольку Streptococcus pneumoniae имеет более 90 различающихся по антигенным свойствам серотипов, этот микроорганизм может присутствовать в полости носа годами и способен в любой момент вызвать развитие бактериального синусита. Некоторые авторы отмечают, что серьезные внутричерепные и орбитальные осложнения при остром синусите обычно являются результатом инфицирования S.pneumoniae.
H.influenzae — мелкая грамотрицательная палочка, более вирулентная и резистентная к антибиотикам, чем пневмококк. С ней также связывают развитие внутричерепных осложнений. Так же как и пневмококк, ее разные штаммы, сменяя друг друга, колонизируют носоглотку.
Нарушение нормальных анатомических взаимоотношений в полости носа изменяет аэродинамику, способствуя попаданию неочищенного воздуха в околоносовые пазухи, повышая тем самым риск развития воспаления.
Среди других возбудителей выделяют Moraxella catarrhalis (примерно в 4% случаев у взрослых и 12% у детей) и стрептококки других групп.
В процентном соотношении при остром синусите в 44,9% случаев выделяется S.pneumoniae, в 17,3% -H.influenzae, в 10,2% — анаэробы, в 7,1% — ассоциации аэробов (S.pneumoniae и H.influenzae). Приведенные данные коррелируют с исследованиями, проведенными в других странах. Существует и альтернативное мнение о том, что самой многочисленной группой микроорганизмов, вызывающих воспалительные заболевания слизистой оболочки полости носа и околоносовых пазух, являются стафилококки, составляя 77% всех посевов, при этом около 40% принадлежит эпидермальному, а 60% — золотистому стафилококку. Однако, по мнению других авторов, золотистый стафилококк не относится к типичным возбудителям острого синусита, несмотря на высокую частоту высеваемости. Этот микроорганизм является «путевой» флорой, попадая на тампон или пункционную иглу с волосков преддверия полости носа. Считается, что S.aureus ответственен за наиболее тяжелые случаи госпитального (нозокомиального) синусита.
При хронических синуситах микробная флора отличается большим разнообразием, и спектр возбудителей несколько смещается в пользу анаэробной флоры. Так, по данным ряда исследований, в 52% случаев выделяются аэробы (различные стрептококки — 21%, гемофильная палочка — 16%, синегнойная палочка — 15%, золотистый стафилококк и моракселла — по 10%), и в 48% случаев — анаэробы (Prevotella — 31%, анаэробные стрептококки — 22%, Fusobacterium -15% и др.).
В условиях нормального функционирования механизма мукоциллиарного транспорта бактерии не имеют возможности для достаточно длительного контакта с клетками эпителия полости носа. При поражении слизистой оболочки вирусом продлевается время контакта патогенных бактерий с клетками и становится возможным вторичное бактериальное инфицирование.
Препараты терапии
Антибиотики для местного воздействия. Многочисленные исследования показали, что препараты для местного воздействия особенно эффективны в лечении синусита в тех случаях, когда хорошо проходимы естественные соустья пазух. Кроме того, существует целый ряд работ, показывающих целесообразность использования местных препаратов у больных после различных операций в полости носа и околоносовых пазухах, когда особенности течения послеоперационного периода диктуют необходимость проведения именно местного лечения. Преимуществами местной терапии в данном случае являются: непосредственное воздействие на послеоперационную область, возможность создания оптимальной концентрации препарата в очаге, отсутствие системного действия за счет крайне низкой их системной абсорбции.
Системная антибиотикотерапия является основным направлением в лечении инфекционных синуситов за рубежом. Наличие широкого выбора эффективных антибактериальных средств, исчерпывающей информации о чувствительности и природной резистентности к ним микроорганизмов, с определенной частотой ассоциированных с тем или иным заболеванием, а также отсутствие надежных методов ускоренной бактериологической диагностики превращают эмпирическую антибактериальную терапию в наиболее рациональную стратегию этиотропной терапии в период возникновения острых гнойных или обострения хронических синуситов на начальном этапе их лечения.
Огромный арсенал современных антибиотиков, безусловно, расширяет возможности клинициста. Успешной реализации указанных задач способствует хорошая ориентированность в спектре действия, в фармакокинетике, микробиологическом влиянии препарата, а также информированность о его доказанной эффективности и безопасности. Большинство ошибок при назначении антибиотика в амбулаторной практике связано именно с неправильным выбором препарата. Главным критерием при этом по-прежнему является возможность воздействия на основных возбудителей воспаления. Приоритетом для выбора того или иного препарата служит не широкий, а оптимальный спектр антибактериальной активности, то есть тот, что охватывает наиболее значимые по статистическим данным в настоящее время и наиболее вероятные именно для данного больного возбудители. Другая проблема при назначении антибиотиков заключается в отсутствии учета уровня приобретенной резистентности возбудителей в популяции. Бесконтрольное и зачастую необоснованное применение ряда антибактериальных средств привело к росту региональной резистентности, что нашло отражение в исследованиях по данной проблеме. Сведения об активности различных групп антибиотиков в отношении «главного» возбудителя острого синусита Streptococcus pneumoniae показывают следующее: имеется тенденция к снижению чувствительности к бета-лактамам. Устойчивость к пенициллину в России не превышает 2%, но штаммы с умеренной чувствительностью составляют 10-20%. Бета-лактамы сохраняют полную клиническую эффективность в отношении пенициллин-резистентных пневмококков, но определяется снижение эффективности цефалоспоринов 1-2-го поколения.
Существует тревожная тенденция — рост устойчивости к макролидам: в Европе — от 8 до 35%, в России — около 12%. Наблюдается крайне высокая резистентность в России к котримоксазолу и тетрациклинам (более 50%), очень низкая активность в отношении ранних фторхинолонов, существенное увеличение частоты резистентных штаммов к этим антибиотикам. Приведенные данные позволяют избежать ошибок при выборе конкретного препарата, например, назначения сульфаниламидов, линкомицина, доксициклина, ципрофлоксацина и других антибактериальных средств, широко применяемых до сих пор на уровне поликлиники. Уменьшение нерационального приема антибиотиков в ряде стран Европейского сообщества за последние годы позволило несколько улучшить ситуацию в отношении уровня резистентности Streptococcus pneumoniae, что проявилось в снижении с 20 до 13% пенициллин-резистентных штаммов данного микроорганизма.
Проблема резистентности в отношении Haemophilus influenzae заключается в следующем: продукция бета-лактамаз в мире составляет от 1 до 40%, в России — не превышает 10%. Практически не отмечено резистентности к аминозащищенным пенициллинам, цефалоспоринам второго-четвертого поколений, фтрохинолонам. Следует обратить внимание на низкую активность цефалоспоринов первого поколения в отношении данного возбудителя.
Спектр значимых возбудителей и характер резистентности в отношении антибактериальных препаратов в настоящее время таковы, что для терапии гнойных синуситов на современном этапе используют β-лактамы, фторхинолоны и макролиды.
Достаточно высокой эффективностью при лечении синуситов обладают цефалоспорины, которые на протяжении 40 лет занимают ведущие позиции среди антибиотиков. Достоинствами, объясняющими такое долголетие, являются:
Пероральные цефалоспорины 3-й генерации. Супракс (цефиксим) хорошо зарекомендовал себя как препарат с удобным режимом дозирования (1 раз в сутки), а также высоким уровнем антибактериальной активности по сравнению с цефалоспоринами предыдущих поколений, в отношении пенициллин-резистентных пневмококков, а также β-лактам-устойчивых гемофиллов и моракселл. Достоинством препарата Супракс (цефиксим) является оптимальная фармакокинетика в ЛОР-органах, позволяющая сохранять высокие концентрации действующего вещества в слизистой оболочке околоносовых пазух.
Флюдитек (карбоцистеин) — единственный препарат среди отхаркивающих средств, обладающий одновременно мукорегулирующим и муколитическим эффектами. Препарат нормализует количественное соотношение кислых и нейтральных сиаломуцинов бронхиального секрета, что восстанавливает вязкость и эластичность слизи. Данный эффект достигается за счет фермента сиаловой трансферразы, вырабатываемого бокаловидными железами слизистой оболочки.
На фоне применения препарата восстанавливается секреция IgA, улучшается мукоцилиарный транспорт, происходит регенерация структур слизистой оболочки. Действие препарата распространяется на слизистую оболочку всех отделов дыхательного тракта. Одновременное назначение карбоцистеина и антибиотиков потенцирует лечебную эффективность последних при воспалительных процессах в области как верхнего, так и нижнего отдела дыхательного тракта. Кроме того, Карбоцистеин взаимно повышает эффективность глюкокортикостероидной терапии, усиливает бронхолитический эффект теофиллина. Активность Карбоцистеина ослабляют противокашлевые и атропиноподобные средства.
Материалы и методы
Для подтверждения тезиса о возможности консервативной терапии синуситов нами проведено обследование и лечение 65 больных, страдающих острым или хроническим гайморитом в стадии обострения, диагноз которого устанавливался на основании жалоб, анамнестических данных, результатов оториноларингологического осмотра, лабораторного и инструментального обследования.
Следует отметить, что данная группа была сформирована из больных, отказавшихся от проведения им пункционного метода лечения. Для лечения 39 больных нами была использована следующая схема лечения:
Распределение больных по полу было приблизительно одинаковым. Среди них было 39 женщин (60%) и 26 мужчин (40%) в возрасте от 18 до 63 лет (39 ± 10,82 лет). Следует отметить, что 67% больных находились в активном трудоспособном возрасте (20-50 лет).
У 45 больных (69,2%) данной группы был диагностирован острый гайморит, из них у 22 больных -двусторонний, у 23 больных — односторонний процесс. У 20 (30,8%) больных отмечалось обострение хронического гайморита, в том числе у 16 больных — двусторонний, у 4 больных — односторонний процесс.
На неэффективность предшествующей амбулаторной антибиотикотерапии указывали 26 (40%) больных. В 6 случаях принимали амоксициллин по 500 мг 2-3 раза в день в течение 7 дней, в 9 случаях — котримоксазол-480 по 2 таблетки 2 раза в сутки в течение 7-9 дней, в 3 случаях — амоксициллин/клавуланат по 375 мг 3 раза в сутки в течение 7-10 дней, в 5 случаях — ципрофлоксацин по 250 мг 2 раза в сутки в течение 5 дней, в 3 случаях — цефазолин внутримышечно по 500 мг 2 раза в сутки в течение 7-9 дней.
На неэффективность предшествующего пункционного лечения указывали 18 (28,1%) больных. У 60 (92,3%) больных после проведенного микробиологического исследования была выявлена патогенная микрофлора (табл. 1).
Таблица 1.
Число штаммов микроорганизмов, выделенных до начала лечения
| Возбудитель | Число штаммов | % |
| Streptococcus pneumoniae | 14 | 17 |
| Haemophilus influenzae | 12 | 14,6 |
| Streptococcus pyogenes | 11 | 13,4 |
| Streptococcus viridans | 8 | 9,8 |
| Staphylococcus epidermidis | 8 | 9,8 |
| Candida albicans | 7 | 8,5 |
| Staphylococcus aureus | 6 | 7 |
| Moraxella catarrhalis | 6 | 7 |
| Mycoplasma pneumoniae | 5 | 6 |
| Chlamydia pneumoniae | 3 | 4,6 |
| Всего | 82 | 100 |
Микробные ассоциации отмечены у 20 (30,7%) больных. При проведении сахаринового теста для оценки транспортной функции мерцательного эпителия, у подавляющего числа больных — 56 человек (86%) — выявлено увеличение времени появления сладкого привкуса во рту (>13 мин), что может свидетельствовать о снижении мукоциллиарного клиренса.
У 7 из 65 больных на третьи сутки после начала лечения отсутствовала положительная динамика субъективных и объективных симптомов гайморита. Этим больным дополнительно назначен курс пункционного лечения до получения результатов микробиологического исследования ввиду опасности развития внутричерепных осложнений. 4 из них после получения данных бактериологического исследования была произведена коррекция схемы лечения в соответствии с антибиотикограммой. У 2 больных был выделен золотистый стафилококк, резистентный к большинству антибиотиков. Назначен ципрофлоксацин по 500 мг 2 раза в сутки в течение 5 дней. У 2 больных выявлен также резистентный к большинству антибиотиков эпидермальный стафилококк. Антибиотиком 2-го ряда стал левофлоксацин по 500 мг 1 раз в сутки в течение 5 дней. У 3 оставшихся больных возбудители не были идентифицированы, назначен антибактериальный препарат 2-го ряда (Моксифлоксацин в дозировке 500 мг 1 раз в сутки в течение 5 дней). У остальных больных, схема лечения не претерпела каких либо изменений (рис. 1).
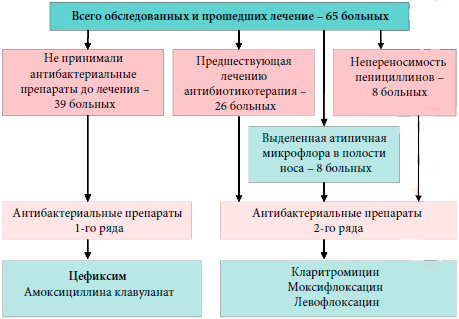
Рис. 1. Схема антибактериальной терапии больных
В результате проведенного лечения у всех больных отмечена нормализация картины периферической крови, что выражалось в статистически значимом (р<0,01) уменьшении относительного количества лейкоцитов и скорости оседания эритроцитов (рис. 2, 3).
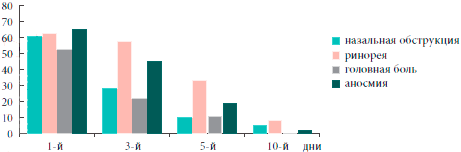
Рис. 2. Динамика субъективных симптомов гайморита
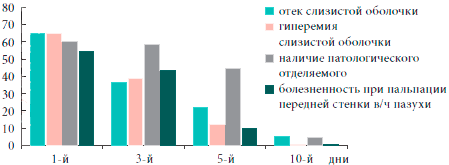
Рис. 3. Динамика объективных симптомов гайморита
Повторное бактериологическое исследование проводилось на 10-е сутки после начала лечения, а повторная диагностика методом полиразмерной цепной реакции (ПЦР-диагностика) — на 30-е сутки после лечения (ввиду того, что на более ранних сроках возможны ложноположительные результаты из-за высокой чувствительности метода) (табл. 2).
Таблица 2.
Результаты микробиологического исследования после лечения
| Параметр | Кол-во больных |
| Эррадикация | 28 |
| Предположительная эррадикация (отсутствие патологического отделяемого) | 37 |
| Персистирование | 0 |
При сравнении показателей риноманометрии, проведенной всем больным до начала лечения и после его окончания, у большинства больных (45-69,2%) отмечено улучшение. Данные изменения статистически достоверны (р<0,01).
Таким образом, на фоне проводимого лечения с 3-го дня установлена устойчивая тенденция (р=0,055) к снижению, а к 5-м суткам значительное уменьшение субъективной и объективной симптоматики гайморита, к 10-м суткам определялись бактериологическая санация носового секрета (в отношении атипичных возбудителей — к 30-м суткам) и статистически достоверное улучшение функции мерцательного эпителия (р<0,01). Положительная динамика патологических изменений в пазухах по данным ультразвукового исследования начиналась с 3-х суток. А к 30-м суткам у большинства больных результаты рентгенологического и ультразвукового исследований соответствовали норме (рис. 4). Данные изменения были статистически достоверны (р< 0,05).
Рис. 4. Динамика изменений в околоносовых пазухах по данным рентгенографии и компьютерной томографии через 30 дней после начала лечения
Клинический пример
Больная К., 44 года, (история болезни № 28385/04) поступила в клинику с жалобами на выделения гнойного характера из обеих половин носа, умеренную заложенность носа с обеих сторон, периодическую головную боль, нарастающую к вечеру, гипосмию. Длительность заболевания составляла 7 дней, в течение которых больная закапывала сосудосуживающие капли в нос. Обратилась в клинику в связи с отсутствием улучшения состояния. 5 лет назад также по поводу двустороннего острого гайморита больной амбулаторно проводился курс консервативного лечения, включая пункции верхнечелюстных пазух.
При осмотре слизистая оболочка полости носа гиперемирована, средние и нижние носовые раковины сильно увеличены в объеме за счет отека, средний носовой ход значительно сужен, в общем, носовом ходе большое количество слизисто-гнойного отделяемого содержимого.
При обследовании в общем анализе крови отклонений от нормы не выявлено. При эндоскопии полости носа видимых патологических изменений в области остиомеатального комплекса не выявлено. Бактериологическое исследование показало рост Streptococcus pneumoniae (107).
Заключение оториноларинголога: Острый двусторонний гнойный гайморит. Аллергический рино-синусит.
Заключение пульмонолога: скрытая бронхоконстрикция.
Больная принимала Супракс (цефиксим) по 400 мг 1 раз в день в течение 10 дней, Флюдитек (карбоцестеин) по 750 мг (15 мл сиропа) 3 раза в сутки в течение 10 дней. Ксилометазолина гидрохлорид 0,1%-ный по 2-3 капли в каждую ноздрю 3 раза в день на протяжении 7 дней.
Через 2 дня после начала лечения головная боль прекратилась, периоды затрудненного носового дыхания сократились, появились обильные выделения из носа слизисто-гнойного характера. Через 5 дней насморк не прекратился, однако выделения приобрели слизистый характер, значительно уменьшился отек и гиперемия слизистой оболочки, восстановилось обоняние.
За последующие 5 дней слизистая оболочка полости носа приобрела равномерную розовую окраску, полностью исчез ее отек и стали обозримы средние носовые ходы. Сохранялись периодические слизистые выделения из носа.
При повторном бактериологическом исследовании роста микрофлоры выявлено не было. Сахариновое время для правой и левой половин носа уменьшилось соответственно до 17 и 15 мин.
Спустя 30 дней больная жалоб не предъявляла, а риноскопическая картина полностью нормализовалась.
Однако по-прежнему многие практические врачи крайне скептически относятся к попыткам беспункционного лечения гайморита, называя в качестве главного аргумента неизбежную хронизацию процесса при использовании только системной антибактериальной терапии. Ошибочная постановка знака равенства между пункцией и антибактериальной терапией нередко приводит к нежелательным последствиям. В случае консервативного, неинвазивного лечения должна быть найдена альтернатива пункции как дренирующему мероприятию для эвакуации патологического секрета из пазухи, начиная с медикаментозных средств и заканчивая щадящими инструментальными пособиями. А индивидуальный подход к каждому конкретному больному с учетом частой сопутствующей патологии со стороны нижних дыхательных путей позволит в значительной мере оптимизировать результаты лечения и избежать частых обострений и рецидивов со стороны как верхнего, так и нижнего отдела дыхательной системы.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Воспаление каждой из околоносовых пазух называют по ее анатомическому названию (этмоидит, фронтит, сфеноидит). Лишь одна из форм заболевания названа по имени автора, ее описавшего, т. е. гайморит вместо «воспаление верхнечелюстной пазухи».
Воспаления в околоносовых пазухах практически имеют одинаковый этиопатогенетический механизм, а различия заключаются лишь в их анатомическом расположении. Общим анатомическим образованием для всех околоносовых пазух является орбита. В то же время при воспалении лобной пазухи велика опасность поражения мозговых оболочек и мозга, расположенных непосредственно у внутренней стенки этой пазухи. При воспалении же основной пазухи страдают в первую очередь находящиеся в анатомической близости зрительные нервы, а при воспалении клеток решетчатого лабиринта (этмоидит) раньше всего начинается воспаление тканей орбиты.
Анатомически верхнечелюстная пазуха граничит с глазницей, клетками решетчатой кости и крылонебной ямкой, где имеются скопления нервной ткани в виде крылонебного узла и ветви тройничного нерва. Следовательно, если речь идет о распространении воспаления, оказываются затронуты эти структуры с характерной неврологической симптоматикой. Микробный фактор имеет главенствующее значение в генезе воспаления верхнечелюстной пазухи. В большинстве случаев выявляются микробные ассоциации. В эти ассоциации помимо традиционных аэробных стафилококков и стрептококков входят и различные анаэробы, грибы и даже простейшие. Кроме них заметную роль играют также вирусы.
Имеются указания на то, что выделяемая из полости глотки флора не идентична с микрофлорой носа. Это необходимо учитывать при подборе антибиотиков и проводить микробиологические исследования носа и глотки раздельно.
В то же время у трети заболевших при микробиологическом исследовании роста микроорганизмов не обнаруживают, что объясняется применением антибиотиков самим больным до выполнения исследования, а также наличием в исследуемом материале анаэробных бактерий или вирусов, для идентификации которых необходимы специальные аппаратура и условия.
Патогенность каждого из микроорганизмов играет важную роль, но не менее существенное значение имеет и уровень иммунной защиты самого больного. Доказано, что у детей и взрослых воспалительные заболевания носа и околоносовых пазух сопровождаются изменениями в гуморальных и клеточных факторах иммунологического аспекта САИР, которые вызываются нарушениями в опсоно-фагоцитарных реакциях нейтрофилов. Поэтому как острый гайморит, так и обострение хронической формы этого заболевания чаще возникают в периоды, когда снижен уровень иммунитета из-за частых респираторных заболеваний, наблюдающихся в осенне-зимний и зимне-весенний периоды. Нельзя сбрасывать со счетов также пониженное содержание витаминов в пище в эти периоды и естественное снижение инсоляции. Конечно, необходимо учитывать и другие, чаще индивидуальные факторы. К ним следует отнести проявления у многих пациентов аллергии, т. е. повышенной чувствительности к различным раздражителям, профессиональные вредности и неблагоприятную экологическую обстановку. Такое многообразие факторов делает заболевание больного поливалентным и говорит о необходимости индивидуального подхода к лечению пациентов, страдающих хроническим гайморитом.
Хронический синусит может развиваться после острого синусита при понижении общей сопротивляемости организма, на почве авитаминоза, аллергии, вследствие узости носовых ходов (при искривлении перегородки носа) или уменьшения просвета выводных отверстий воспаленной или гипертрофированной слизистой общего, среднего носового хода; развитие хронического синусита у детей провоцирует также аденоидные разрастания.
Хронический гайморит изолированно поражает верхнечелюстную пазуху; у детей он чаще встречается в сочетании с патологией решетчатого лабиринта. В отличие от взрослых, у детей чаще имеют место катаральная или полипозно-гнойная формы, чем исключительно гнойная.
Морфологически определяются, как правило, утолщение слизистой оболочки за счет отека и инфильтрации лимфоцитов, полинуклеотидов и плазменных клеток. Иногда наблюдается очаговая гиперплазия слизистой с формированием полипозных выростов.
Клинические проявления сводятся к затруднению носового дыхания и к односторонним слизистым или слизисто-гнойным выделениям, появляющимся преимущественно в зимнее время. Частым симптомом является кашель, особенно по ночам. Нередки обострения среднего отита, вызванные стеканием гноя из пазухи по заднебоковой стенке носоглотки. Боли в области пазухи отсутствуют. Родители обращаются прежде всего к педиатру по поводу рецидивирующего бронхита, шейного лимфаденита и нередко к офтальмологу — по поводу упорного конъюнктивита и кератита.
Полоска гноя в среднем носовом ходе наблюдается не всегда. Ее легко обнаружить после анемизации среднего носового хода при наклоне головы в здоровую сторону и вперед.
Большое значение имеют косвенные признаки: диффузный отек средней носовой раковины, слизистые выделения в среднем носовом ходе, бледная окраска нижней носовой раковины, плохое ее сокращение после смазывания адреналином, светлое отделяемое пенистого характера в носовых ходах — все это свидетельствует об аллергическом характере процесса.
Обострения, как правило, связаны с перенесенным острым респираторным заболеванием и сопровождаются усилением головной боли, новым повышением температуры тела, слабостью и резким затруднением носового дыхания. При этом выделения из носа могут отсутствовать. Головная боль либо носит локальный характер и проецируется в лобные области, либо проявляется чувством давления за глазом (при одностороннем поражении пазухи). Очень часто ощущение тяжести возникает при попытке поднять веки. Гораздо реже имеются пульсирующие болевые ощущения в проекции самой пазухи, на щеке. Хотя чаще боль характерна при одонтогенном генезе заболевания, когда имеются кариозные зубы на верхней челюсти. При одномоментном поражении ветвей тройничного нерва боли носят острый характер с иррадиацией в глаз, небо. Анальгетики в этих случаях не купируют боль. Катаральное воспаление через несколько часов или дней переходит в гнойное, которое проявляется в виде обильных гнойных выделений со слабо выраженным одновременным снижением болевых ощущений. Гнойные выделения из полости носа чаще попадают в носоглотку, хотя при высмаркивании выделяются и из носа. Накопление их в пазухе осуществляется довольно быстро, и через несколько часов пазуха вновь оказывается заполненной. Емкость ее (у взрослых — в пределах 20 мл) у детей, естественно, заметно меньше, вследствие чего возобновление головной боли, а также риносинусогенные орбитальные внутричерепные осложнения распространены у них гораздо больше, чем среди взрослых. При этом у мужчин они наблюдаются в два раза чаще, чем у женщин.
Субпериостальные абсцессы при эмпиемах гайморовой пазухи у детей наблюдаются чаще, чем у взрослых, что обусловлено не столько патологическим процессом в гайморовой полости, сколько поражениями зубов и остеомиелитными изменениями верхнечелюстной пазухи.
Клинические проявления абсцесса, вызванного эмпиемой гайморовой полости, определяются местом его расположения. При субпериостальных абсцессах, образующихся вблизи орбитального края, наблюдаются покраснение, отечность, припухлость нижнего века, а иногда и щеки, а также хемоз нижнего отдела конъюнктивы.
Диагностика гайморита определяется совокупностью клинических и рентгенологических данных и устанавливается на основании характерных жалоб, данных объективного осмотра и дополнительных методов обследования. Опираться при установлении диагноза только на данные рентгенологического исследования нельзя. Вследствие общего кровоснабжения и сходства гистологического строения, набухание слизистой оболочки носа и верхнечелюстной пазухи происходит почти одновременно. У детей слизистая оболочка значительно толще, чем у взрослых, а объем ее увеличивается более интенсивно. Этим и объясняется частое наблюдающееся при рентгенологическом исследовании у детей, страдающих хроническим ринитом, а также аллергическим ринитом, нарушение воздушности верхнечелюстных пазух, что нередко расценивается как признак гайморита. О рефлекторно-вазомоторном характере набухания слизистой оболочки верхнечелюстной полости у детей с хроническим ринитом можно судить по быстрому изменению рентгенологической картины. В сомнительных случаях для уточнения диагноза делают рентген после введения в пазуху контрастного вещества (липоидол, йодлипол). Окончательное суждение о поражении придаточных пазух носа у детей должно выноситься на основании совокупности данных клинических и рентгенологических исследований. Большое диагностическое значение имеет пункция верхнечелюстной пазухи, которую производят у детей старше шести лет. У детей моложе шести лет при проведении этой процедуры возможны повреждения нижней стенки глазницы, а также травмирование зачатков постоянных зубов.
К наркозу прибегают в исключительных случаях. Ребенка готовят к пункции под местной анестезией. Предварительно анемизируют средний носовой ход. После тщательной анестезии латеральной стенки носа непосредственно под нижней носовой раковиной иглу с мандреном вводят в общий носовой ход. Концом иглы упираются в латеральную стенку нижнего носового хода на самой высшей его точке, примерно на 1-1,5 см вглубь от переднего конца от передней носовой раковины. Игле придают косое положение (по направлению к наружному углу глаза этой же стороны), и, надавив на латеральную стенку носа, легко вводят ее в пазуху. Для определения наличия или отсутствия в пазухе экссудата производят легкую аспирацию. Иногда оттягивание поршня затруднено, что указывает на нахождение кончика иглы в толще слизистой оболочки. Продвигая иглу несколько вперед или назад, добиваются ее правильного положения. При введении промывной жидкости, больной должен находиться в сидячем положении с наклоненной вперед головой, во избежание попадания жидкости в дыхательные пути.
В промывной жидкости часто обнаруживается желатинообразный зеленоватый слизисто-гнойный комок. Если затемнение на рентгенограмме было обусловлено набуханием слизистой оболочки пазухи, промывная жидкость оказывается чистой и стерильной.
Пункция верхнечелюстной пазухи — процедура, легко выполняющаяся врачом и переносящаяся больным. Возможны, однако, и осложнения. К наиболее частым осложнениям относится эмфизема щеки, возникающая в тех случаях, когда конец пункционной иглы проникает через переднюю стенку пазухи, и воздух при продувании поступает в мягкие ткани щеки. Если воздух попадает в орбиту, образуется эмфизема вокруг глаза, нередко экзофтальм. Введение жидкости при этих условиях может привести к развитию флегмоны и абсцесса орбиты, а в тяжелых случаях — к слепоте и внутричерепным осложнениям. В результате попадания воздуха в кровеносный сосуд может развиться самое тяжелое и опасное осложнение — воздушная эмболия. В связи с возможными указанными осложнениями продувание пазухи недопустимо, как до ее промывания, так и после него. Иногда при пункции наблюдается обморочное состояние, у больного выступает холодный пот, отмечается бледность кожных покровов. Все перечисленные осложнения, как правило, связаны с техническими погрешностями при проведении пункции, а также с плохой подготовкой больного ребенка. Введение антибиотика в пазуху иногда вызывает аллергическую реакцию у детей в виде аллергической сыпи, крапивницы, отека лица, гортани.
Рентгенологическое исследование является одним из наиболее важных и наиболее распространенных методов в ринологии, в частности при диагностике различных форм гайморита. Появившиеся в настоящее время новые способы исследований (стереография, прямое увеличение рентгеновского изображения, электрорентгенография, послойное исследование и, наконец, один из наиболее точных и перспективных методов — компьютерная томография) помогли существенно усовершенствовать диагностику синуситов. Однако рентгенография в прямой проекции, явившаяся одним из первых примеров прикладного использования открытых К. Рентгеном Х-лучей как в настоящее время, так и, вероятно, в будущем, сохранит за собой ведущие позиции в рентгенодиагностике синуситов из-за своей доступности.
Однако необходимо подчеркнуть, что толкование полученных рентгенологических данных часто бывает весьма упрощенным и не всегда позволяет раскрыть все возможности этого метода. Основным и главным симптомом считают понятия «затемнение», «помутнение», «снижение розрачности», «завуалированность» и т. д. Но данная трактовка дает лишь общее представление о чисто физическом проявлении, т. е. задержке прохождения рентгеновских лучей через все ткани лицевого скелета и, как следствие, большем или меньшем попаданием рентгеновских лучей на фоточувствительный материал — рентгенопленку. Однако образующийся фотографический эффект не может соответствовать характеру патологического состояния и, тем более, степени его выраженности. Высказывать суждения о наличии воспалительного процесса либо о переходе его в стадию рубцевания в этих случаях некорректно.
Снижение прозрачности верхнечелюстной пазухи на рентгенограмме может быть связано с содержанием в пазухе патологического секрета, утолщением слизистой оболочки, с полипами, кистозными и другими новообразованиями. Кроме этого, снижение прозрачности гайморовой пазухи может быть связано и с утолщением ее костных стенок.
Как известно, внутренняя поверхность костных стенок гайморовой пазухи не имеет надкостницы, ее роль выполняет самый глубокий слой слизистой оболочки (мукопериост). Из-за этого воспалительный процесс в слизистой оболочке пазухи достаточно быстро распространяется и на костные стенки пазухи, где наблюдаются продуктивные изменения. Данное обстоятельство позволяет оценивать на рентгенограмме состояние костных стенок пазухи. Вследствие проекционного искажения и явлений суперпозиции, носовая и глазничная стенки не могут служить объектом такой оценки при традиционной укладке при выполнении прямого снимка. В этом случае может оцениваться только состояние переднебоковой стенки пазухи. Лишь при повороте головы пациента по отношению к пленке на 25—30° в сторону исследуемой пазухи, при тангенциальном ходе пучка рентгеновских лучей к передней стенке изучаемой пазухи можно дать оценку состояния как передней, так и глазничной и задней стенок пазухи. В норме боковая костная стенка верхнечелюстной пазухи, а на «косой» рентгенограмме соответственно глазничная и задняя стенки представляются четко очерченной тонкой тенью, нормальную воздушность просвета пазухи подчеркивает ровный внутренний контур. В случаях, когда имеет место равномерное снижение прозрачности верхнечелюстной пазухи малой или средней интенсивности, сохранена четкость контура костной стенки и не отмечается ее утолщения, можно говорить об утолщении слизистой оболочки пазухи или о наличии в ней воспалительного экссудата. Эта картина характерна для острого гайморита без вовлечения в патологический процесс костной ткани.
При наличии понижения прозрачности пазухи и уплотнения тени боковой костной стенки следует считать воспалительный процесс хроническим. Для уточнения формы гайморита, его стадии (обострения или ремиссии) необходимо обращать внимание на характер и степень перехода рисунка внутреннего контура утолщенной кости к рисунку утолщенной слизистой оболочки. Я. А. Фастовский, М. Г. Румянцева (1986) выделили три наиболее характерных скиалогических варианта.
- Если удается четко разграничить утолщенную слизистую оболочку и изображение утолщенной костной стенки пазухи, есть основание думать о наличии длительно протекающего хронического воспалительного процесса в стадии ремиссии.
- Постепенный, плавный переход тени костной стенки пазухи к тени утолщенной слизистой оболочки служит указанием на обострение хронического гайморита.
- В ряде наблюдений удается выявить дополнительный контур, как бы «сопровождающий» костную стенку пазухи и отличающийся по интенсивности своего рисунка как от утолщенной слизистой, так и от плотности костной стенки. Таких дополнительных «контуров» может быть несколько. Подобная рентгенологическая картина может служить указанием на перенесенное обострение воспалительного процесса с исходом в рубцевание слизистой оболочки.
Различная выраженность реакции слизистой оболочки, как проявление воспалительного процесса в виде ее утолщения, достаточно четко определяется на рентгенограммах. Далеко не всегда наблюдается полное исчезновение воздушности пазухи. Обычно в ее центре определяется участок просветления, имеющий форму, размер так называемой «остаточной» воздушной полости, зависящий от степени утолщения слизистой оболочки. Учитывая данные анамнеза и клиники в сопоставлении с другими рентгенологическими признаками (реакция костных стенок), можно выдвинуть предположение, что эти изменения обусловлены гиперплазией слизистой оболочки, характерной для хронического воспалительного процесса. При этом существенное значение имеет оценка контура «остаточной» воздушной полости. Наличие нечетких границ «остаточной» воздушной полости отображает текущий воспалительный процесс либо его обострение, в то время как четкость контура «остаточной» воздушной полости свидетельствует о ремиссии. Рентгенологическое исследование, проводимое в динамике, в процессе консервативного лечения либо вскоре после его завершения может подтвердить достоверность этого рентгенологического признака.
Симптом «сопровождающей тени» отмечается не только в начале заболевания, но и в стадии выздоровления, после стихания воспалительных явлений. Поэтому на основании однократного рентгенологического исследования трудно установить, имеем ли мы дело с начальной фазой заболевания или с остаточными явлениями. Только данные серийного исследования в сопоставлении с клиническими признаками могут правильно оценить картину заболевания.
При подозрении на одонтогенный гайморит и наличие свищевого хода на боковой поверхности альвеолярного отростка КТ-исследование переводиться с целью исключения или подтверждения наличия гнойного процесса верхнечелюстной пазухи. При подозрении на злокачественную опухоль верхнечелюстной пазухи КТ-исследование нужно для определения границ распространения новообразования и выбора тактики лечения. Однако для определения морфологической структуры нельзя использовать КТ-плотностные показатели; необходимо провести гистологическое исследование.
Достоверная дифференциальная диагностика между злокачественной опухолью и деструктивным полипозным процессом околоносовых пазух, полости носа затруднена. КТ-исследование может констатировать лишь разрушение костных стенок пазух, проникновение новообразования в окружающие области. На основании КТ-плотностных показателей тканей косвенно можно судить о наличии доброкачественного процесса.
При расшифровке рентгенологических данных следует учитывать, что после ликвидации воспаления прозрачность пазухи обычно восстанавливается.
При хроническом процессе контуры пазухи стушевываются, затемнение становится интенсивным. При эмпиеме тень густая, диффузная, а при разлитом полипозе она не имеет гомогенного характера, даже если вся полость заполнена полипами. При подозрении на эмпиему рекомендуется производить исследование в положении сидя. Обнаружение одной или нескольких округлых теней может указывать как на полип, так и на кисту. В пользу полипа обычно говорит одновременное присутствие полипов в носу. Увеличиваясь в размере, киста может заполнить большую часть верхнечелюстной пазухи, а иногда и всю пазуху целиком.
При вовлечении в процесс костной стенки и нарушении ее целостности может образоваться свищ. Выявление на снимке костного дефекта в направлении свищевого хода возможно лишь после введения в свищ зонда.
Для проведения лечения прежде всего необходимо обеспечить хороший отток отделяемого из пораженной пазухи путем анемизации среднего носового хода несколько раз в день. Хорошие результаты получены при УЗ-терапии. Аденоидные разрастания подлежат обязательному удалению. Нередко полное выздоровление наступает через две-три недели после аденотомии.
Современные концепции этиопатогенетической терапии
Для ликвидации блокады соустий околоносовых пазух из-за отека слизистой оболочки используются различные сосудосуживающие средства, включающие растворы, приготовленные из растительного сырья, содержащие эфедрин, кокаин, танин и другие алкалоиды.
В настоящее время это направление представлено различными фармакологическими препаратами, изготавливаемыми в виде носовых капель, аэрозолей, гелей, мазей или пероральных таблеток, пастилок и т. д.
Дополнительно к сосудосуживающим препаратам в эти средства вводят и специальные формы антибиотиков, концентрация которых, достигаемая при местном применении, осуществляет бактерицидную концентрацию грамположительных и грамотрицательных микроорганизмов. К таким патентованным препаратам относятся носовые cпреи. Полидекса, содержащая антибиотики неомицин и пилимиксин, а также кортикостероидный препарат дексаметазон и сосудосуживающий фенилэфрин. Другими cпреями, обладающими местными противовоспалительными действиями являются зофра, содержащий антибиотик фрамицидин и биопарокс, в состав которого входит фюзафунжин. Последний помимо антибактериального действия обладает и антимикотической активностью.
Однако наиболее частой и общепринятой является общая антибиотикотерапия. Она осуществляется как перорально ампициллином или его улучшенным составом за счет присоединения b-лактамаз клавулановой кислоты — амоксиклавом или аугментином.
В то же время высокой активностью обладают и цефалоспорины II и III типов, а также фторхинолоны.
При аллергии к β-лактамазам рекомендуются макролиды (азитромицин, рокситромицин и др.). Эффективность в лечении синусита имеют и тетрациклины, в частности доксициклин, рондомицин (метациклин).
При одонтогенном характере процесса необходимо сочетание антибиотиков, обладающих тропизмом к костно-хрящевым тканям. Такими являются, в частности, линкомицин, фузидин натрия. При назначении одного из них следует добавить метронидазол (трихопол). Длительное использование высокоэффективных антибиотиков подавляет рост грамположительных и грамотрицательных микроорганизмов и активизирует рост дрожжей и других грибов. Поэтому следует считать не только оправданным, но и необходимым назначение антимикотических препаратов. Самыми простыми и наиболее употребительными считаются нистатин, леворин.
В случае легкого и среднетяжелого проявления заболевания терапию возможно применять перорально, но при тяжелом или затянувшемся течении необходимо использование внутривенного способа введения препаратов, и лишь спустя три—пять дней при улучшении как местного, так и общего статуса можно переходить на пероральный путь введения препаратов.
Длительность терапии при остром и рецидивирующем остром синусите составляет 10—14 дней, при обострении хронического до трех-четырех недель. При хроническом синусите антибактериальная терапия имеет меньшее значение, чем комплексная, а иногда и оперативное вмешательство. В то же время необходимо, чтобы выбор препаратов основывался на результатах бактериологического исследования содержимого синусов и чувствительности выделенных возбудителей к антимикробным препаратам. Обязательно следует выполнять пункцию и дренирование синусов. Одним из комбинированных антибактериальных препаратов для местного применения является флуимуцил антибиотик. Введение в состав препарата фермента и антибиотика делает его использование особенно важным для скорейшего удаления из пазухи гнойно-некротических масс. Для введения в пазухи применяется 250 мг флуимуцила антибиотика однократно в сутки в течение семи дней. Возможно также использование этого препарата ингаляционным методом в количестве шести–восьми инъекций.
Введение растворов ферментов (трипсина и хемотрипсина) способствует разжижению густого гнойного содержимого. Для введения антибиотиков в верхнечелюстную пазуху используют также метод «перемещения» растворов антибиотиков из полости носа. После тщательной анемизации среднего носового хода больного укладывают на стол с максимально запрокинутой головой, повернутой на 45° в сторону локализации процесса. Полость носа на стороне поражения заполняется при помощи шприца раствором антибиотика (3—5 мл), после чего ноздря зажимается. Во вторую ноздрю вставляется олива, соединенная со сжатой рукой баллоном. После этого ребенок произносит «кук-кук» (небная занавеска закрывает вход в носоглотку), и баллон наполняется воздухом, в полости носа и придаточных пазухах создается отрицательное давление. Мгновенное отнятие оливы и разжатие второй ноздри приводит к выравниванию давления в пазухах и обеспечивает проникновение в них растворов антибиотика. Разумеется, для успешного применения методики «перемещения» необходимо наладить контакт с ребенком, найти с ним общий язык. Хороший результат получен при применении внутрь антигистаминных препаратов.
В упорных, не поддающихся консервативному лечению случаях хронического гайморита приходится прибегать к хирургическому вмешательству. При помощи бора или троакара делают отверстие под нижней носовой раковиной, в которое вставляют мягкий катетер, фиксирующийся пластырем. Промывание пазухи раствором из антибиотика производится через катетер, а после его удаления (спустя пять–семь дней) — через образовавшееся отверстие. В последние годы для дренажа верхнечелюстной пазухи с успехом используют полиэтиленовые трубки, которые вводят через пункционную иглу. После извлечения пункционной иглы дренажная трубка остается на месте на все время лечения. Подобное вмешательство более щадящее, чем оперативное вскрытие пазухи, которое производилось преимущественно у взрослых и лишь в исключительных случаях — у детей старшего возраста. Все шире применяется у детей эндоназальное вскрытие верхнечелюстной пазухи, при котором создается соустье между пазухой и полостью носа при минимальном травмировании слизистой полости носа (Б. В. Шеврыгин).
Радикальная операция верхнечелюстной пазухи у детей старшего возраста
После разреза слизистой оболочки десны под верхней губой и отслоения мягких тканей с обнажением костно-лицевой стенки, через которую проникают в пазуху, удаляют гной и патологически измененную слизистую оболочку. Удаляя части внутренней стенки на уровне нижнего носового хода, устанавливают постоянное соустье с полостью носа. Через это отверстие производится, при показаниях, промывание верхнечелюстной пазухи.
В последние десятилетия в ЛОР-практике стали применяться более щадящие методы, такие, как установка постоянных катетеров в полость пазухи с последующим активным введением лекарственных веществ; лазерное воздействие по введенному кварц-полимерному волокну, а также использование низкочастотного ультразвука для кавитационной обработки стенок пазухи. С целью уменьшения осложнений, связанных с пункционными методами лечения, была предложена система баллонного частичного закрытия общего носового хода с последующей аспирацией и промыванием пазухи через ее анатомическое естественное соустье с носом, так называемый «синус-катетер». Эта конструкция, изготовленная из различных видов резины, не имеет острых, режущих или колющих деталей и позволяет выполнять санирующие пазуху процедуры: аспирировать, промывать и вводить лекарственные препараты. С помощью синус-катетера весьма успешно лечатся многие формы хронического и острого гайморита.
Последним достижением в лечении гайморита следует считать метод фотодинамической терапии. Последнюю осуществляют следующим образом: гайморову пазуху освобождают от содержимого, вводят в нее фотосенсибилизатор (ФС). При этом в качестве ФС используют порфирины хлоринового ряда. Проводят облучение стенок пазухи лазером, с длиной волны, совпадающей с длиной волны пика поглощения используемого ФС, в течение 10—60 мин и с мощностью 0,10—0,35 Вт. Применяют лазерное излучение длиной волны 654—670 Нм и дозой облучения 10—1000 Дж/см2.Облучение стенок пазухи проводят через 2 ч после введения ФС. Дозу облучения увеличивают поэтапно, с перерывами в 20—30 с, во время которых пазуху продувают, освобождая от скапливающейся слизи. Пазуху перед и через 2 ч после введения в нее ФС промывают физиологическим раствором. В течение трех–пяти дней после лечения пазуху промывают физиологическим раствором. Этот способ обеспечивает полную санацию гайморовой пазухи, сокращает сроки лечения и предотвращает рецидивы.
В литературе имеются указания и на использование других ФС, а также лазеров с другой длиной волны. Эти исследования, несомненно, интересны и в научном, и особенно в практическом плане, однако для оценки отдаленных результатов такого лечения требуется время.
Дело в том, что многие ринохирурги считают, что, если больной больше к ним не обращается — значит, он выздоровел. При этом совершенно безосновательно игнорируется возможность обращения таких больных к другим специалистам и в другие клиники, где им выполняют другие, часто более радикальные вмешательства.
В. Г. Зенгер, доктор медицинских наук, профессор
МОНИКИ, Москва
