Гиперактивный мочевой пузырь у женщин (ГАМП)
Гиперактивный мочевой пузырь у женщин – это синдром, характеризующийся внезапной потребностью помочиться, непроизвольным выделением урины, частыми позывами на мочевыделение, в том числе, ночью (ноктурия). Иногда симптомы встречаются изолированно. Диагностика опирается на данные УЗИ мочевого пузыря, почек, цистоскопии, уродинамических исследований; для исключения инфекционно-воспалительного процесса назначают ОАМ, бакпосев. Лечение базируется на изменении поведенческих реакций, использовании фармакологических средств, реже – проведении хирургических вмешательств.
Общие сведения
Гиперактивный мочевой пузырь (ГАМП, гиперактивность/гиперрефлексия детрузора) у женщин – расстройство мочеиспускания, нарушающее качество жизни, препятствующее социализации. Патология встречается у миллионов пациенток во всем мире, вне зависимости от расы. Распространенность увеличивается с возрастом, однако императивные позывы, частое мочеотделение, ноктурия не являются нормальными признаками старения. Женщины старше 75 лет сталкиваются с везикальной гиперактивностью в 30-50%. Доказано, что чем выше индекс массы тела, тем больше риск развития синдрома.
Гиперактивный мочевой пузырь у женщин
Причины ГАМП
Гиперактивный мочевой пузырь – нервно-мышечная дисфункция, при которой детрузор избыточно сокращается во время фазы наполнения при малом объеме урины. Идиопатическую форму устанавливают в отсутствие основных неврологических, метаболических или урологических причин, которые могут имитировать диагноз, например, при раке, цистите или обструкции уретры. Гиперактивный ответ наиболее часто вызывают:
- Неврологические состояния. Травма спинного мозга, демиелинизирующие заболевания (рассеянный склероз), медуллярные поражения могут привести к везико-уринарной дисфункции, вызвать недержание. Аналогичные изменения происходят при диабетической и алкогольной полинейропатии.
- Прием лекарств. Признаки ургентного расстройства вызывают некоторые препараты. Так, мочегонные средства провоцирует инконтиненцию из-за быстрого наполнения резервуара. Прием прокинетика бетанехола усиливает перистальтику кишечника, мочевыводящих путей, что в ряде наблюдений сопровождается гиперрефлексией.
- Прочие патологии. Сердечная недостаточность, заболевания периферических сосудов в стадии декомпенсации сопровождаются симптомами гиперактивности. В течение дня у таких пациентов избыток жидкости депонируется в тканях. В ночное время большая часть этой жидкости мобилизуется, всасывается в кровяное русло, тем самым увеличивая ночной диурез.
Факторы риска
К факторам риска развития гиперактивного пузыря относят:
- осложненные роды (наложение щипцов, разрыв мышц)
- урогинекологические оперативные вмешательства
- депрессию
- возраст женщины >75 лет
- ожирение
- употребление алкоголя, кофеина (вызывают транзиторную гиперрефлексию детрузора за счет раздражающего действия).
У некоторых женщин характерные симптомы развиваются в климактерический период, что связано с дефицитом эстрогенов. С другой стороны, заместительная гормонотерапия при раке молочной железы у молодых пациенток увеличивает риск появления детрузорной гиперчувствительности.
Патогенез
Кора головного мозга, мост, спинальные центры с периферической автономной, соматической, афферентной и эфферентной иннервацией обеспечивают нормальное функционирование мочевых путей за счет скоординированности ряда процессов. Изменения (функциональные или морфологические) на любом уровне провоцируют нарушения мочевыделения.
Данная патология – многофакторное расстройство, как по этиологии, так и по патофизиологии. В основе лежит сверхчувствительность детрузора нейрогенно-мышечного, миогенного или идиопатического генеза, в результате которой возникают императивные позывы и/или недержание. Определенная роль в развитии гиперактивного детрузора на фоне обструкции и повреждения спинного мозга принадлежит М-2 рецепторам.
Взаимодействие ацетилхолина с рецептором М-3 активирует фосфолипазу С посредством связывания с белками G. Это вызывает высвобождение кальция, сокращение гладких мышц. Повышенная чувствительность к стимуляции мускариновых рецепторов обусловливает гиперрефлексию. Ацетилхолин способствует сокращению детрузора, активации сенсорных афферентных волокон, вследствие чего развивается гиперактивный ответ в виде поллакиурии, ноктурии, срочности мочевыделения.
Классификация
В клинической урологии выделяют «сухой» гиперактивный мочевой пузырь и «мокрый», сопровождающийся инконтиненцией на фоне ургентных позывов. Гиперрефлексия протекает изолированно или сочетается со стрессовым недержанием. Также патологию систематизируют с помощью оценки выраженности симптоматики, для этого пациенты предварительно заполняют специальную анкету, где отмечают особенности мочевыделения в течение трех суток. Согласно полученным данным устанавливают:
- Легкую степень. Частота суточных мочеиспусканий незначительно выше нормы. Допускается единичный императивный позыв; недержание, связанное с ургентностью, эпизодично (раз в неделю или реже). Количество выделяемой мочи за раз около 80-100 мл. Гиперактивный мочевой пузырь сохраняет нормальный объем (250-300 мл).
- Умеренную степень. Количество суточных мочеиспусканий равно или более 10, императивные позывы – 2 и более, есть эпизоды инконтиненции, выделяемый объем – 60-75 мл, емкость органа 200-220 мл.
- Тяжелую степень. Количество мочеиспусканий за сутки – 15 и более, императивных позывов от 5 и выше, множество эпизодов недержания (постоянно необходимо использовать урологические прокладки или памперсы). Количество мочи – 50-60 мл, гиперактивный пузырь вмещает 200 мл и менее.
Симптомы ГАМП у женщин
Клинические проявления коррелируют с тяжестью процесса. Основные признаки включают учащенное мочеиспускание при незаполненном мочевом пузыре малыми порциями, императивные позывы (внезапно возникшее, непреодолимое желание на мочевыделение), ургентное недержание урины. Часто есть необходимость ночного посещения туалета более чем 2 раза (ноктурия).
Желание помочиться провоцирует звук льющейся воды, в легких случаях теряется несколько капель жидкости, в тяжелых – весь объем. Поллакиурия и ноктурия могут присутствовать изолированно, без проявления инконтиненции. Иногда после мочевыделения сохраняется ощущение дискомфорта в промежности.
Осложнения
ГАМП приводит к нарушению социализации. Постоянный страх не успеть в туалет, подтекание урины во время сексуального контакта, сопровождающий инконтиненцию неприятный запах инициируют развитие депрессивного состояния. Неконтролируемое мочевыделение провоцирует мочевой дерматит, экзему.
Постоянное присутствие патогенной микрофлоры способствует рецидивирующим инфекциям мочевыводящей системы. Мочевой пузырь часто утрачивает нормальный объем, т.е. формируется микроцист, что в самых серьезных случаях может привести к органоуносящей операции, инвалидизации.
Диагностика
Диагноз «гиперактивный мочевой пузырь» устанавливает врач-уролог на основании данных физикального осмотра, анамнеза, лабораторно-инструментального обследования. Женщине предлагается заполнить анкету (дневник мочеиспусканий). В некоторых случаях обоснована консультация невролога, гинеколога. Алгоритм исследований включает:
- Лабораторные анализы. При выявлении в ОАМ патологических изменений (лейкоцитурии, бактериурии) выполняют культуральный посев для идентификации возбудителей, определения их чувствительности к лекарствам. Цитологию проводят при обнаружении большого количества эритроцитов для исключения неопластического процесса. Глюкозурия требует обследования на сахарный диабет.
- Инструментальную диагностику. УЗИ мочевыводящих органов с контролем остаточной мочи, цистоскопия, комплексные уродинамические исследования показаны при рефрактерных к лечению случаях нейрогенной этиологии, а также при подозрении на патологию, провоцирующую симптомы ургентной инконтиненции – воспаление, опухоль, блокирующий камень.
Дифференциацию выполняют с другими формами недержания, опухолевым процессом, циститом, атрофическим вагинитом на фоне снижения уровня эстрогена. Сходные симптомы регистрируют при пролапсе матки, пузырно-влагалищном свище.
Лечение гиперактивного мочевого пузыря у женщин
Если определена конкретная причина патологии, все меры направлены на ее устранение. Например, лечение инфекции мочевыводящих путей подразумевает назначение антибиотиков, при атрофическом уретрите используют крем, содержащий эстрогены. Для идиопатической формы существует три основных терапевтических подхода: изменение поведенческих реакций, прием препаратов, хирургическое вмешательство. Лечение зависит от серьезности симптомов, их влияния на образ жизни.
Консервативная терапия
При легкой и средней степени возможно проведение консервативных мероприятий. Их варианты:
- Поведенческая терапия. Лечение первой линии, иногда сочетается с приемом медикаментов. Рекомендуют отказаться от приема жидкости за 3 часа до сна, исключить алкоголь, кофе, острые блюда, газированные напитки. Разрабатывают план мочеиспусканий: даже при отсутствии желания необходимо посетить туалет в определенное время. При позыве следует потерпеть несколько минут (на фоне приема лекарств это доступно), постепенно промежутки между актами мочевыделения увеличивают.
- Лечебная физкультура. ЛФК в лечении гиперактивного пузыря подразумевает выполнение упражнений для укрепления мышц тазового дна. Гимнастика эффективна при регулярном выполнении особенно у молодых пациенток. Также возможно использование вагинальных приспособлений (конусов). Женщина сокращает мышцы таза, чтобы удержать тренажер трансвагинально, постепенно его вес увеличивают. В течение 4-6 недель положительную динамику отмечают у 70%.
- Электростимуляция тазового дна. Процедура подразумевает подачу электрических импульсов, чтобы вызвать сокращения определенной группы мышц. Ток доставляется с помощью анального или вагинального зонда. Электростимуляцию выполняют в сочетании с лечебной физкультурой, продолжительность курса составляет несколько месяцев.
Медикаментозное лечение гиперактивного мочевого пузыря у женщин относят ко второй линии. В рамках лекарственной терапии назначают:
- Антимускариновые/антихолинергические препараты: тропсиум хлорид, солифенацин, дарифенацин, оксибутинин. Обладают пролонгированным антиспазмическим, анестезирующим эффектом, блокируют чувствительность М-холинорецепторов гладкомышечных волокон.
- Селективные агонисты бета-3 адренорецепторов (мирабегрон). Расслабляют мускулатуру в фазу накопления путем воздействия на бета-3 адренорецепторы, за счет чего восстанавливается (увеличивается) емкость органа. По результатам исследования, комбинация мирабегрона и солифенацина более эффективна по сравнению с монотерапией.
- Десмопрессин и его аналоги. Назначают при неврологическом генезе ГАМП, для которого типично снижение продукции антидиуретического гормона и мелатонина, что вызывает ночную полиурию. Дополнительно возможно назначение антихолинэргических средств.
- Альфа-1-адреноблокаторы (тамсулозин, альфузозин, силодозин, доксазозин). Применяют при детрузорно-сфинктерной диссинергии для уменьшения внутриуретрального сопротивления и количества остаточной мочи. Подавляют активность постсинаптических альфа-1-адренорецепторов шейки, артерий, сфинктера уретры.
- Трициклические антидепрессанты. Обоснованы исключительно в комбинированных схемах по рекомендации невролога или психиатра.
Хирургическое лечение
Хирургические вмешательства зарезервированы для самых сложных случаев, устойчивых к консервативной терапии, или если есть противопоказания к приему лекарств. Цистэктомию в настоящее время выполняют редко. Операции и манипуляции при ГАМП:
- аугментационная цистопластика: подразумевает увеличение емкости органа за счет использования собственных тканей (замещение кишечным резервуаром);
- сакральная и пудендальная невротомия: проводится пересечение нервов, провоцирующих гиперактивный мочевой пузырь, их блокада анестетиками;
- пиелостомия, эпицистостомия: выполняются для альтернативного отведения урины, если произошло сморщивание пузыря с развитием/угрозой присоединения хронической почечной недостаточности;
- сакральная нейромодуляция: проводится стимуляция крестцового нерва слабым электротоком высокой частоты с помощью имплантированного электрода, соединенного с генератором импульсов. Это позволяет восстановить скоординированность мочеиспускательного акта.
- введение ботулотоксина А: нормализует мышечный тонус за счет ингибирования высвобождения ацетилхолина из нервных окончаний, происходит блокировка передачи сигнала от нервной клетки к мышце. Нейротоксин вводят в сфинктер или детрузор во время цистоскопии. К недостаткам относят необходимость повторных манипуляций через 8-12 месяцев.
Прогноз и профилактика
При своевременном обращении и прохождении диагностики возможно избежать осложнений. Гиперактивный мочевой пузырь оказывает влияние на качество жизни женщин. Комбинированный подход эффективен у 92%, синдром рассматривают как хроническое расстройство, требующее длительного приема лекарств.
Профилактика включает активный образ жизни, отказ от никотина и алкоголя, контроль уровня сахара, сбалансированное питание. Препараты, которые могут спровоцировать симптомы гиперактивного расстройства мочеиспускания у женщины, должен назначать врач. Своевременная консультация специалиста при первом появлении урологических жалоб, выявление причины, адекватное лечение — значимые факторы для благоприятного прогноза.
|
Литература 1. Императивные позывы к мочеиспусканию — ведущий симптом гиперактивности мочевого пузыря/ Аль-Шукри С. Х., Кузьмин И. В.// Материалы IV Международной научно-практической конференции «Малоинвазивные методы диагностики и лечения в современной урологии». – 2007. 2. Классификация гиперактивности мочевого пузыря при степени тяжести симптоматики// И. В. Кузьмин, С. Х. Аль-Шукри// Урологические ведомости. – 2012 – №3. 3. Распространенность императивных нарушений мочеиспускания среди женщин старше 40 лет/ Аляев Ю. Г., Балан В. Е., Гаджиева З. К.// Материалы Пленума Всероссийского общества урологов. – 2005. |
Код МКБ-10 N31 |
Гиперактивный мочевой пузырь у женщин — лечение в Москве
Дата публикации 7 октября 2023Обновлено 27 ноября 2023
Определение болезни. Причины заболевания
Нейрогенный мочевой пузырь, или нейрогенная дисфункция нижних мочевыводящих путей (НДНМП; Neurogenic lower urinary tract dysfunction) — это собирательный термин, который обозначает нарушение нервной регуляции работы мочевого пузыря. При этом мочеиспускание может быть затруднено или полностью отсутствовать либо возникает недержание мочи.
Обычно «нейрогенный мочевым пузырём» называют нарушение регуляции работы мочевого пузыря на уровне главного центра — головного мозга. Однако для полноты картины мы рассмотрим и другие уровни. Ведь зачастую на практике под нейрогенным мочевым пузырём подразумевают нейрогенную дисфункцию нижних мочевыводящих путей в целом. В англоязычной литературе эти термины являются синонимами.
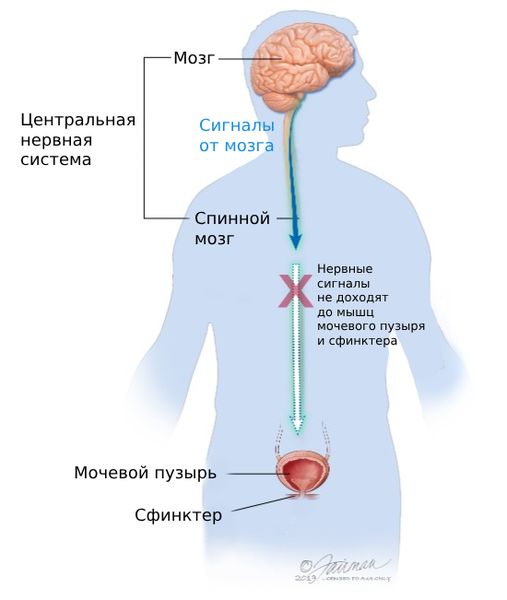
Нейрогенная дисфункция нижних мочевыводящих путей
Распространённость
Официальной статистики по этому заболеванию нет ни в нашей стране, ни за рубежом, так как сложно посчитать количество людей с НДНПМ среди неоднородной группы пациентов с урологическими, неврологическими и травматологическими заболеваниями. Согласно аналитическому обзору, в 2020 году приблизительное количество всех больных нейрогенным мочевым пузырём в России составляло не менее 1,5 млн человек. Из них около 140–180 тыс. — люди с травмами спинного мозга, 60–130 тыс. — с рассеянным склерозом, 78–151 тыс. — с болезнью Паркинсона, 150–370 тыс. — после инсультов. Примерно у четверти больных с сахарным диабетом (а их в РФ около 4,5 млн человек) нарушена регуляция мочевого пузыря из-за вегетативной полинейропатии [1].
Что касается врождённых аномалий, то, по статистике, из 10 000 новорождённых у 3–4 есть пороки развития спинного мозга, у 80–96 % из них нарушена работа мочевого пузыря [1][13].
Причины НДНМП
Причины нейрогенной дисфункции нижних мочевыводящих путей условно разделяют на три группы в зависимости от того, какой уровень нервной регуляции поражён:
- Поражения нервной системы выше моста головного мозга. Может произойти из-за повреждения верхней лобной извилины при гидроцефалии нормального давления, рассеянном склерозе, инсульте, опухоли, черепно-мозговой травме, деменции. Сюда же относится поражение базальных ганглиев (при болезни Паркинсона и мультисистемной атрофии) и гипоталамуса, врождённые нарушения строения нервной системы: дефект закрытия позвоночного столба (spina bifida), атрезия крестца или врождённое органическое поражение головного мозга, симптомом которого является ДЦП [5][6].
- Поражение спинного мозга выше крестца. Развивается на фоне травмы позвоночника выше крестцового отдела, при инсульте, воспалении, демиелинизации или опухоли спинного мозга.
- Поражение спинного мозга на уровне крестца (так называемый конский хвост). Связано с выпадением грыжи межпозвонкового диска, спиной бифида, нейросифилисом (спинной сухоткой) и другими инфекциями спинного мозга. Также к этой группе относят поражение периферических нервов, идущих от спинного мозга к мочевому пузырю: опухоли, диабетические полинейропатии, поражение тазового сплетения или нерва во время операции или при переломе костей таза [4][9].
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы нейрогенного мочевого пузыря
Пациенты с НДНМП жалуются либо на полное отсутствие мочеиспускания, либо на затруднённое мочеиспускание, либо на недержание мочи. Другие жалобы зависят от фазы мочеиспускания, которая страдает. Так, может быть нарушена фаза накопления мочи, опорожнения мочевого пузыря или обе эти фазы сразу. Какая из фаз будет дефектной, зависит от области поражения нервной системы. Рассмотрим эти области подробнее.
Для поражения нервной системы выше моста головного мозга характерны трудности в накоплении мочи (фаза опорожнения при этом не страдает):
- незамедлительное непроизвольное мочеиспускание даже при минимальных позывах (императивное мочеиспускание);
- учащённое мочеиспускание или недержание при обычном суточном объёме мочи;
- отсутствие остаточной мочи — жидкости, которая в норме остаётся в мочевом пузыре после мочеиспускания (у взрослых это 50 мл) [2][9]; определяется с помощью УЗИ мочевого пузыря.
При поражении на уровне спинного мозга выше крестца появляются как симптомы нарушения накопления мочи, так и трудности с опорожнением мочевого пузыря (дефектные фазы и накопления мочи, и опорожнения мочевого пузыря):
- прерывистое мочеиспускание;
- большое количество остаточной мочи;
- учащённое мочеиспускание с недержанием мочи или её задержкой [2][9].
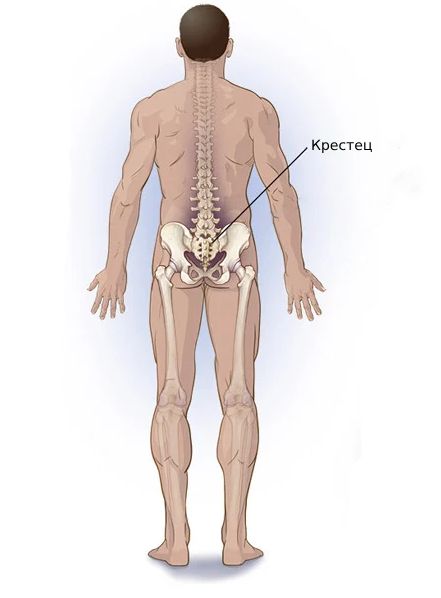
Крестец
При поражении на уровне крестца и ниже нарушается опорожнение мочи (фаза накопления при этом в норме):
- контролируемое мочеиспускание затруднено или отсутствует;
- большое количество остаточной мочи сразу после мочеиспускания;
- недержание от переполнения мочевого пузыря;
- непроизвольное выделение мочи из уретры при физическом усилии, чихании и/или кашле [2][9].
Также при проблемах с мочеиспусканием или мочевыделением могут возникать сопутствующие симптомы: эректильная дисфункция, запоры и нарушение болевой чувствительности в области промежности. Об этих нарушениях нужно обязательно рассказать врачу [2].
Все жалобы у пациентов с когнитивным снижением (проблемами с памятью, вниманием и т. п.) или психическими заболеваниями следует подтверждать инструментальными исследованиями [2].
Патогенез нейрогенного мочевого пузыря
Для нормального мочеиспускания необходима сбалансированная работа:
- вегетативной, или автономной, нервной системы (не зависящей от воли человека);
- соматической нервной системы (подвластной сознанию);
- мышц тазового дна.
В норме наполнение мочевого пузыря стимулирует рецепторы растяжения мышц, которые находятся в стенке мочевого пузыря. Возбуждённые рецепторы отправляют импульсы по периферическим нервам крестцового нервного сплетения в спинной мозг, а тот передаёт сигнал в чувствительную кору полушарий, где осознаётся необходимость мочеиспускания.
Работа наружного сфинктера мочевого пузыря регулируется сознанием (соматической нервной системой). Обычно он находится в сокращённом состоянии, пока человек не захочет помочиться [10]. Когда решение принято, произвольные сигналы в двигательной коре инициируют мочеиспускание. Для этого импульсы передаются в центр мочеиспускания, находящийся под большими полушариями в варолиевом мосту головного мозга.
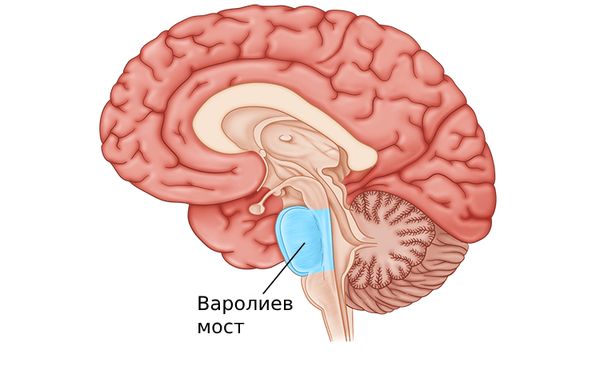
Варолиев мост
Затем варолиев мост передаёт сигнал в крестцовый отдел спинного мозга, в систему, непосредственно выпускающую мочу из мочевого пузыря. При этом одновременно сокращаются гладкие мышцы мочевого пузыря, расслабляется его внутренний и наружный сфинктер, а также мышцы тазового дна [10]. Остановимся подробнее на этой системе.
Система, выпускающая мочу из мочевого пузыря, состоит из детрузора (мышц стенок мочевого пузыря), уретры, внутреннего и наружного сфинктера мочевого пузыря. Управляет этой системой, как говорилось выше, головной и спинной мозг, а также вегетативная нервная система, которая делится на симпатическую и парасимпатическую.
Альфа- и бета-адренорецепторы симпатического отдела вегетативной нервной системы под воздействием норадреналина обеспечивают накопление мочи в мочевом пузыре. Холинергические рецепторы парасимпатической нервной системы через ацетилхолин инициируют эвакуацию содержимого мочевого пузыря [10].
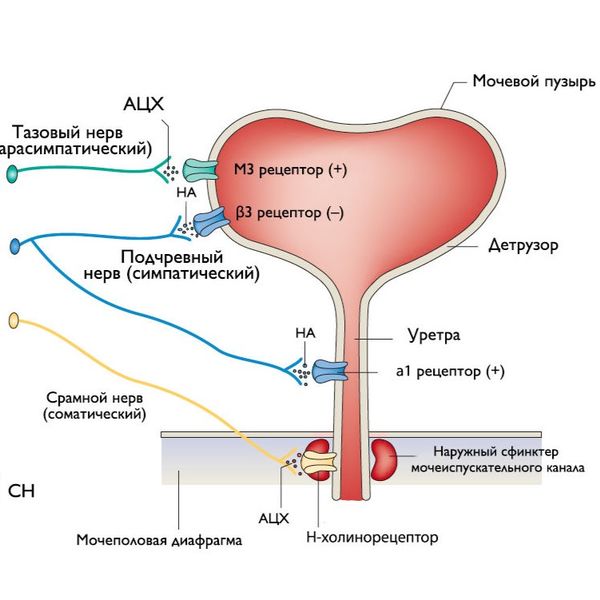
Иннервация мочевого пузыря
Если говорить конкретно об иннервации, т. е. связи с центральной нервной системой, участков мочевого пузыря, то следует отметить:
- Детрузор при активации парасимпатической нервной системы вызывает сокращение мочевого пузыря. Симпатическая нервная система, наоборот, расслабляет его и позволяет накопить мочу.
- Внутренний сфинктер через симпатическую нервную систему сокращает выходное отверстие мочевого пузыря. Связи с парасимпатической системой у него нет.
- Наружный сфинктер под контролем воли человека расслабляется через соматическую (ответственную за произвольные движения) и парасимпатическую систему. Симпатической иннервации у него нет [3].
От того, какое звено нарушено, зависит вид патологии мочевого пузыря и жалобы пациента.
Классификация и стадии развития нейрогенного мочевого пузыря
Существует несколько классификаций нейрогенного мочевого пузыря. Из них наиболее ценными для врачей являются:
- классификация Международного общества по борьбе с недержанием мочи;
- классификация Лапида;
- общее руководство по неврологическим заболеваниям и дисфункциям мочевыводящих путей [6].
Классификация Международного общества по борьбе с недержанием основана на уродинамических различиях и делит работу мочевого пузыря на фазу накопления мочи и фазу мочеиспускания. Каждая характеристика мочевого пузыря (функция, активность, ощущение, ёмкость, податливость и т. д.) измеряется и идентифицируется как для фазы хранения, так и для фазы мочеиспускания [6].
Классификация Лапида, пожалуй, самая простая и узнаваемая, но многие пациенты не вписываются в эти категории, и она не включает нарушение функции уретры.
По этой классификации выделяют следующие типы:
- Сенсорный нейрогенный мочевой пузырь — развивается из-за разрушения волокон, идущих от мочевого пузыря к головному мозгу. Иннервация от мозга к мочевому пузырю при этом сохранена. Примерами могут служить сахарный диабет, спинная сухотка и B12-дефицитная анемия. Со временем эти нарушения вызывают хроническое перерастяжение, приводящее к гипотоническому (вялому) мочевому пузырю.
- Моторный паралитический нейрогенный мочевой пузырь — возникает из-за повреждения моторных нервов в стенке мочевого пузыря. Это может произойти в результате травмы, обширной операции или опоясывающего герпеса. Хроническое перерастяжение, как правило, приводит к увеличению ёмкости мочевого пузыря — это связано с большим количеством остаточной мочи из-за слабо сокращающейся мышечной стенки.
- Расторможенный нейрогенный мочевой пузырь — чаще всего связан с инсультом, опухолью головного мозга, поражением позвоночника, болезнью Паркинсона или демиелинизирующим заболеванием. Симптомами обычно являются частое мочеиспускание и императивное недержание мочи. Чувствительность мочевого пузыря при этом нормальная, объёмы остаточной мочи после опорожнения обычно низкие.
- Рефлекторный нейрогенный мочевой пузырь чаще всего наблюдается при травматических повреждениях спинного мозга, поперечном миелите, обширном демиелинизирующем заболевании или любом значительном поражении головного мозга. При таких нарушениях мышцы стенок мочевого пузыря непроизвольно сокращаются даже при небольшом объёме мочи, но ощущение наполненности мочевого пузыря не возникает и нет произвольных сокращений. Это означает, что пациент не может сознательно управлять мочеиспусканием, и мочевой пузырь может начать сокращаться и выделять небольшой объём мочи даже без его желания. Рефлекторный нейрогенный мочевой пузырь может развиваться в случае полного поражения верхнего двигательного нейрона в коре головного мозга. При этом типе нейрогенного мочевого пузыря детрузор и сфинктер перестают работать согласованно.
- Автономный нейрогенный мочевой пузырь представляет собой полное нарушение двигательного контроля и чувствительности. Чаще всего это наблюдается при патологических процессах, поражающих крестцовый отдел спинного мозга или тазовые нервы. Человек при этом не способен инициировать мочеиспускание и не ощущает наполненность мочевого пузыря. Это вызывает его перерастяжение с небольшой сократимостью мышц стенки [6].
Также существует ещё одна классификация, которая составлена согласно Общему руководству по неврологическим заболеваниям и дисфункциям мочевыводящих путей, модифицированная Паникером [12]. Это руководство основано на анатомическом расположении основного неврологического дефекта и частично упоминалось при перечислении причин заболевания.
В этой классификации сопоставляется уровень поражения с клинической картиной:
- Супрапонтинные поражения (выше моста головного мозга):
- проблемы с накоплением мочи;
- обычно низкие объёмы остаточной мочи после опорожнения;
- перенапряжённые мышцы мочевого пузыря.
- Поражения позвоночника до крестца:
- симптомы нарушения накопления мочи и мочеиспускания;
- увеличенные объёмы остаточной мочи после опорожнения;
- детрузор перенапряжён, может нарушаться координация между сокращением мышц мочевого пузыря и расслаблением сфинктера;
- если поражение находится на уровне 6-го грудного позвонка или выше (см. раздел «Осложнения», автономная дисрефлексия), возможны гипертонические кризы.
- Крестцовые и внутрикрестцовые поражения:
- обычно только проблемы с мочеиспусканием: не получается инициировать опорожнение, нет рефлексов мочеиспускания и ощущения наполненности мочевого пузыря;
- избыточные объёмы остаточной мочи после опорожнения;
- детрузор сокращается слабо или не сокращается вовсе;
- возможен синдром конского хвоста — возникает из-за сжатия или повреждения нижних нервных корешков спинного мозга, проявляется болью или онемением нижней части спины, ягодиц и ног, снижением силы и чувствительности в ногах, что может затруднять ходьбу.
Осложнения нейрогенного мочевого пузыря
Инфекции мочевыводящих путей — это самое распространённое осложнение у людей с нейрогенной дисфункцией нижних мочевыводящих путей.
Течение инфекции при этом имеет свои особенности:
- частые обострения (до четырёх раз в год);
- развитие штаммов, устойчивых к большинству антибиотиков;
- наличие постоянных условий для инфицирования;
- необходимость постоянного или периодического дренирования мочевого пузыря;
- формирование биоплёнок — высокоорганизованных сообществ бактерий, которые вызывают хронические инфекции, устойчивые к антибиотикам [4]
К осложнениям НДНМП также относится острая и хроническая задержка мочеиспускания [4]. В первом случае мочеиспускание отсутствует совсем, во втором — мочевой пузырь опорожняется не полностью, его стенки постоянно перерастягиваются и за сутки в нём скапливается больше мочи.
Другим осложнением является парадоксальная ишурия [4]. При этом состоянии самостоятельное мочеиспускание отсутствует, и моча по каплям выделяется из переполненного и атоничного мочевого пузыря. Пациенты зачастую считают, что у них развилось недержание мочи.
Автономная дисрефлексия — ещё одно осложнение нейрогенной дисфункции нижних мочевыводящих путей. Развивается, если основное заболевание поражает спинной мозг на уровне 6-го грудного позвонка и выше. В ответ на перерастяжение мочевого пузыря, переполнение кишечника, эрекцию, сильную боль, цистит, цистоскопию или уродинамическое исследование происходит гиперстимуляция симпатической системы, спазм периферических сосудов и резко повышается артериальное давление (АД). Но головной мозг в ответ на это не может дать сигнал по травмированному спинному мозгу о расширении сосудов для снижения АД. На фоне высокого давления возникает головная боль, нечёткость зрения, покраснение лица и заложенность носа. Активация симпатической системы скелетных мышц и кожи приводит к повышенному потоотделению и покраснению кожи выше уровня поражения, бледной и холодной коже ниже уровня поражения. Такое состояние требует неотложного приёма лекарств для снижения давления.
Главным отсроченным, но грозным осложнением НДНМП является хроническая почечная недостаточность (ХПН) различной степени тяжести; 4-я степень ХПН требует гемодиализа.
Диагностика нейрогенного мочевого пузыря
Если симптомы появились впервые в жизни, то в первую очередь стоит обратиться к врачу-урологу или нейроурологу. При инсультах, травмах спинного мозга в прошлом и подозрении на неврологические заболевания следует начать с консультации невролога.
Сбор жалоб и осмотр
На приёме врач уточнит, на что жалуется пациент и предложит заполнить специальные опросники (IPSS, LISS, Medsen, Боярского).
Также доктор проведёт осмотр области промежности, чтобы определить поверхностную чувствительность кожи этой зоны с обеих сторон. Кроме того, при подозрении на НДНМП проводится проверка следующих рефлексов:
- бульбокавернозного (реакции, которая возникает при механической стимуляции уретры или влагалища и проявляется напряжением влагалища или полового члена);
- кремастерного (возникает при лёгком прикосновении к внутренней поверхности бедра, вызывает поднятие мошонки у мужчин за счёт сокращения кремастеровой мышцы);
- анального;
- коленного;
- лодыжечного;
- подошвенного [4].
Снижение этих рефлексов говорит о поражении нервных волокон выше или на уровне крестца.
Также проводится ректальный и вагинальный осмотр мышц тазового дна. У женщин, чтобы выявить опущение мышц влагалища, проводится гинекологическое обследование.
Лабораторная диагностика
Рекомендуется сдать общие анализы крови, мочи и биохимический анализ мочи с определением общего белка, альбумина, мочевины, креатинина и электролитов.
При наличии боли, повышенной температуры и крови в моче рекомендуется выполнить дополнительные обследования: микробиологическое исследование средней порции мочи и бакпосев мочи. Но важно понимать, что при проведении предварительной катетеризации мочевого пузыря в моче может появиться бактерии и кровь, поэтому результаты анализов могут быть ложными.
Также может проводиться исследование секрета предстательной железы на предмет воспаления.
Инструментальная диагностика
Для объективной оценки нарушения проведения нервного импульса выполняется:
- Электромиография мышц тазового дна, уретрального и/или анального сфинктера.
- Исследование проводимости по срамному нерву (нерву, который проходит через тазовую область). Выполняется электронейромиографом или электромиографом.
- Определение латентного периода бульбокавернозного и анального рефлекса (т. е. временного интервала между стимуляцией соответствующих областей и появлением рефлекторной реакции).
- Определение вызванных потенциалов со срамного нерва [12]. Это исследование позволяет оценить скорость распространения стимула по срамному нерву от клитора/члена к головному мозгу.
Также необходимо оценить общее состояние мочевой системы. Для этого проводится УЗИ почек, предстательной железы и мочевого пузыря, оценивается объём остаточной мочи.
К другим возможным инструментальным методам диагностики этой патологии можно отнести электромиографию тазовых мышц, МРТ таза, крестцового сплетения, спинного мозга и вещества головного мозга.
Специальным методом при подозрении на НДНМП является комплексное уродинамическое исследование (КУДИ). Его проводят вне острого воспалительного процесса в нижних мочевыводящих путях. Метод позволяет определить функциональное состояние мочевого пузыря и уретры в фазе накопления, хранения и опорожнения мочи.
КУДИ может состоять из одного или нескольких этапов:
- Урофлоуметрия — исследование, при котором пациент при позыве к мочеиспусканию производит его в специально оборудованный унитаз с датчиками. Датчики считывают информацию о времени мочеиспускания, его средней и максимальной скорости, времени достижения максимального потока, объёме выделяемой мочи (норма 150–400 мл). Далее данные визуализируются с помощью графической кривой. Остаточный объём мочи считается по УЗИ мочевого пузыря после мочеиспускания.

Урофлоуметрия
- Цистометрия — мочевой пузырь с помощью катетера наполняют тёплым физиологическим раствором, а затем определяют тонус мышц стенок мочевого пузыря и создаваемое этим тонусом давление. Метод позволяет выявить непроизвольное сокращение мышц в фазу накопления. Для этого давление измеряют в начале исследования, при первом и наиболее сильном позыве к мочеиспусканию, а также измеряют ургентное давление (когда сдержать поток мочи уже невозможно). Кроме того, определяется максимальная вместимость мочевого пузыря. Нормальным является равномерное нарастание давления в пузыре по мере его заполнения, но не резкое повышение. Давление может резко повышаться при гиперактивности детрузора, что ведёт к непроизвольному выделению жидкости, введённой в мочевой пузырь, — подобное состояние трактуется как императивная форма недержания при гиперактивном детрузоре.
- Профилометрия — проводится после цистометрии и позволяет оценить работу и стабильность сфинктера уретры и наличие стрессового недержания мочи. Для этого измеряется давление в мочевыводящем канале в разных его частях. При профилометрии вводится тонкий катетер, такой же катетер вводится и в прямую кишку. Во время исследования мочевой пузырь наполняют стерильной жидкостью. Когда он наполнится, пациента попросят его опорожнить. Именно это исследование позволяет выявить главную причину недержания мочи или затруднения мочеиспускания. Также этот метод позволяет определить общую и функциональную длину уретры и максимальные показатели давления внутри уретры [4].
Лечение нейрогенного мочевого пузыря
Назначение лекарств зависит от вида НДНМП. Обычно консервативное лечение сочетается с другими видами немедикаментозного лечения.
Медикаментозное лечение
Пациентам с «вялыми» мышцами мочевого пузыря ранее широко назначались ингибиторы холинэстеразы (Дистигмина бромид, Пиридостигмина бромид, Прозерин, Галантамин). В теории повышение концентрации нейромедиатора ацетилхолина вызывает позывы и облегчает начало мочеиспускания, в результате уменьшается объём остаточной мочи. Однако последние клинические рекомендации не рекомендуют широко назначать эти лекарства, так как их эффективность не доказана [7] и результаты могут быть непредсказуемыми [8].
Чтобы подавить чрезмерную сократительную активность мышц мочевого пузыря, в первую очередь используют антихолинергические средства, или М-холиноблокаторы (Солифенацин, Троспий, Оксибутинин, Толтеродин, Фезотеродин) [2]. Оксибутинин проникает через гематоэнцефалический барьер — барьер между кровотоком и головным мозгом, что нужно учитывать у пациентов с когнитивным дефицитом (дефицит может прогрессировать).
Препараты второй линии — альфа-1-адреноблокаторы (Тамсулозин, Силодозин) [2]. Их следует с осторожностью применять у пациентов с нестабильным уровнем артериального давления (как при гипертонии, так и при гипотонии). Эффект наступает через 3–4 дня после начала приёма — благодаря расслаблению шейки мочевого пузыря и сфинктера уретры облегчается начало мочеиспускания и уменьшается объём остаточной мочи.
Также, чтобы подавить чрезмерную сократительную активность, в мышцы мочевого пузыря под контролем уретроскопа вводят 200 ЕД ботулотоксина. Эту процедуру называют «внутридетрузорной инъекцией ботулинического токсина».
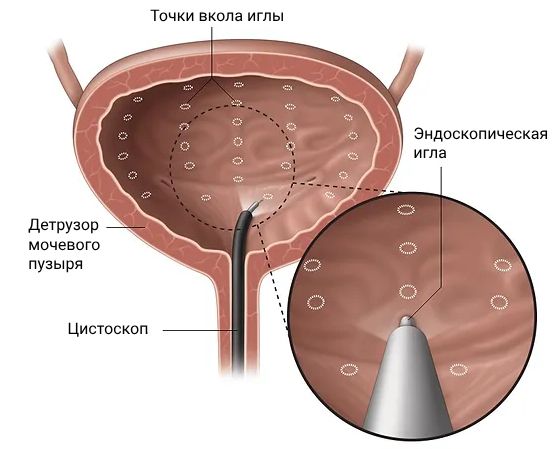
Внутридетрузорная инъекция ботулинического токсина
Она назначается, если консервативное лечение не помогает [2].
В дополнение к традиционным лекарствам, которые нацелены на рецепторы в мышцах уретры или мочевого пузыря, разрабатываются и новые методы лечения этого класса заболеваний, направленные на чувствительные нервные клетки, двигательные нервные окончания, уротелиальные клетки и отделы центральной нервной системы [11].
Приёмы для искусственной стимуляции
Приём Креде (надавливание на брюшную стенку выше мочевого пузыря) относят к методам искусственной рефлекторной стимуляции начала опорожнения мочевого пузыря.
Кроме приёма Креде, к ним относятся:
- надавливание на мочевой пузырь (в отличие от приёма Креде, точка надавливания другая);
- приём Вальсальвы;
- мочеиспускание после постукивания по лонной кости.
Подобные методы могут быть применены в крайних случаях из-за осложнений — недостаточность работы мышц тазового дна может прогрессировать, что усилит стрессовое недержание мочи. Триггерный рефлекс (постукивания по лонной кости) может вызвать автономную дизрефлексию. При использовании этих методов необходим строгий контроль за уродинамикой.
Немедикаментозное лечение
К ним относится электромагнитная и электрическая стимуляция срамного и тибиального нерва, гимнастика для укрепления мышц тазового дна [2]. Эти методы дополняют вышеописанное медикаментозное лечение.
Другие методы лечения
В некоторых случаях (чаще при очаговых поражения спинного или головного мозга) понадобится дренирование мочевого пузыря при помощи постоянного катетера Фалея, эпицистостомы или периодической катетеризации с использованием одноразовых катетеров. Последний способ снижает риск осложнений со стороны почек.

Катетеризация мочевого пузыря
При стрессовом нейрогенном недержании мочи у женщин активно используют субуретральный слинг [2], а у мужчин — имплантацию искусственного сфинктера мочевого пузыря. Субуретральный слинг — это небольшая лента из мягкой сетки, которую вводят внутрь тела для изменения положения уретры и поддержки окружающих мышц.
К другим хирургическим методам относят рассечение урогенитального сфинктера и аугментацию мочевого пузыря [2]. В ходе аугментации создаётся дополнительная ёмкость пузыря, часто путём добавления части другого тканевого или синтетического материала. Это позволяет увеличить способность мочевого пузыря вмещать мочу и улучшить функцию мочеиспускания.
Прогноз. Профилактика
При внимательном наблюдении и лечении нейрогенного мочевого пузыря пациенты могут заметить значительное улучшение качества жизни [5].
НДНМП всегда является следствием заболеваний или травм нервной системы и не возникает сама по себе. Поэтому профилактики этой группы заболеваний не существует [2]. Всё сводится к тому, чтобы не пропустить начало нарушения мочеиспускания у неврологических больных. Если установлено НДНМП, то рекомендовано ежегодно посещать уролога.
Также пациентам важно знать о признаках развития смертельных осложнений: парадоксальной ишурии и автономной дисрефлексии (см. раздел «Осложнения»).Знание их симптомов позволит вовремя заподозрить развитие этих патологий и обратиться к врачу.
Гиперактивный мочевой пузырь — заболевание, которое распространено значительно сильнее, чем принято думать. Около 17% людей среднего возраста страдают от данной болезни. Однако лишь немногие готовы обратиться к врачу с этой проблемой. Что следует знать об этом заболевании и как его можно избежать?
Причины развития гиперактивного мочевого пузыря

Гиперактивный мочевой пузырь (ГМП) — патология, которая характеризуется сильными и внезапными позывами к мочеиспусканию, но не связана с инфекциями нижних мочевых путей.
Синдром гиперактивного мочевого пузыря не несет угрозы жизни человека, однако значительно ухудшает ее качество. Статистика говорит, что данному состоянию подвержены, как мужчины, так и женщины средних лет. Но представительницы слабого пола чаще подвержены ему в более молодом возрасте.
В большинстве случаев синдром развивается самостоятельно и не связан с другими возможными патологиями. Однако врачи относят к причинам, влияющим на появление ГМП, наличие заболеваний неврологического характера (деменцию, болезнь Паркинсона), а также повреждения кровоснабжения головного мозга (инсульты) и межпозвоночные грыжи спинного мозга.
Обратив внимание на участившиеся позывы к мочеиспусканию, которые принимают хронический характер, следует пройти соответствующие медицинские обследования. Они позволят исключить инфекционные заболевания, диабет, доброкачественные или злокачественные образования в органах малого таза, мочекаменную болезнь. После того, как будет установлен точный диагноз, можно начинать соответствующее лечение мочевого пузыря.
Врачи также обращают внимание, что люди, у которых была обнаружена эта патология часто допускают ряд серьезных ошибок.
- Считают, что это временное явление
Это в корне ошибочное мнение. ГМП — болезнь, которая нуждается в обязательном лечении. Занимается этой деликатной проблемой врач-уролог.
- Самостоятельно устанавливают диагноз
Зачастую женщины принимают симптомы данной патологии за цистит и начинают самостоятельное, некорректное лечение мочевого пузыря. Оно не только не помогает, но и способствует прогрессированию заболевания и усилению имеющегося дискомфорта.
- Не учитывают медикаментозное воздействие
В некоторых случаях проблемы с мочевым пузырем у женщин могут свидетельствовать о злоупотреблении антигистаминными или мочегонными препаратами.
Симптомы гиперактивного мочевого пузыря у женщин
Наличие синдрома ГМП серьезно осложняет жизнь женщины. Весь распорядок дня приходится соотносить с возможностью быстрого доступа к туалетной комнате. Даже звук льющейся воды может вызвать острое желание посетить уборную.
Для того чтобы самостоятельно оценить масштаб проблемы, необходимо знать основные симптомы гиперактивного мочевого пузыря у женщин. К ним относят.
- Императивные позывы
Для них характерно резкое возникновение желания посетить туалет, без постепенного нарастания потребности в мочеиспускании. Также возможно бесконтрольное подтекание мочи, когда человек не успевает дойти до уборной.
- Слишком частое мочеиспускание
О повышенной частоте мочеиспускания принято говорить тогда, когда мочевой пузырь у женщин опорожняется чаще 8 раз.
- Чувство переполненности мочевого пузыря
Такое ощущение — один из наиболее распространенных симптомов ГМП. При этом среднесуточный объём мочи остается в пределах нормы. Обычно это количество равняется полутора литрам.
- Ноктурия
Данное состояние характеризуется преобладанием ночного диуреза над дневным. Об учащенном ночном мочеиспускании говорят, когда человек совершает более двух походов в туалет за ночь, прерывающих сон, на протяжении длительного времени.
Обнаружив тревожные симптомы, до посещения соответствующего специалиста следует провести некоторые самостоятельные оценочные действия. Так, например, врачи рекомендуют завести дневник, в который будут записываться данные об особенностях процесса мочеиспускания. Они позволят урологу составить более полную картину о состоянии пациента и назначить требуемое лечение мочевого пузыря. В записях должно быть указано:
- общее количество мочеиспусканий (с указанием временных меток);
- объём мочи при каждом посещении туалета;
- все эпизоды подтекания мочи с указанием их причины (пробежка, чихание, кашель и т. д.);
- число нестерпимых позывов к мочеиспусканию;
- количество потребляемой за день жидкости (включая первые блюда);
- число использованных за сутки гигиенических прокладок.
Дневник заполняют на протяжении всего дня: от утреннего пробуждения и до отхода ко сну. Информацию о ночных визитах в туалет вносят утром следующего дня. Заполнять данные следует не менее трех дней подряд.
Частые позывы в туалет: профилактика и лечение мочевого пузыря

Уменьшить дискомфорт при гиперактивном мочевом пузыре возможно, воспользовавшись простыми мерами профилактики:
- посещать туалет сразу по требованию (воздержание повышает риск развития инфекций мочеполовых путей);
- своевременно лечить (наблюдать за состоянием) диабет или нервные расстройства;
- составить график посещения туалета и максимально его придерживаться, чтобы тренировать мочевой пузырь;
- регулярно пользоваться гигиеническими прокладками и стараться избегать смущающих инцидентов;
- регулярно практиковать упражнения Кегеля, способствующие укреплению мышц тазового дна;
- не допускать избыточной массы тела (лишние килограммы значительно нагружают мочевой пузырь у женщин);
- отказаться от курения, которое повышает риск развития рака органов малого таза.
Уровень развития современной медицины позволяет эффективно лечить ГМП. Традиционное лечение гиперактивного мочевого пузыря представлено следующими видами терапии:
- Медикаментозной
Она представляет собой прием препаратов, блокирующих определенные рецепторы внутренней поверхности мочевого пузыря, что уменьшает частоту позывов к мочеиспусканию. Недостатком такого лечения является усиление сухости всех слизистых оболочек организма, а также негативное воздействие на нервную систему.
- Тибиальной электростимуляцией
Этот метод лечения представляет собой точечное воздействие электрическим током на большеберцовый нерв. Данная аппаратная процедура проводится курсами и требует ежегодного повторения.
- Введением ботулинического токсина
Еще одним из способов лечения ГМП являются инъекции ботокса в определенные участки мочевого пузыря. Они способствуют снижению случаев недержания мочи и уменьшению неконтролируемых позывов к мочеиспусканию. Повторять процедуру необходимо 1-2 раза в год.
Урология / Лопаткин Н.А., Камалов А.А., Аполихин О.И. и др. – 2012
Клиническая неврология / Никифоров А.С., Гусев Е.И. – 2007
Гиперактивный мочевой пузырь (ГМП), проявлениями которого являются симптомы учащения мочеиспускания, императивные позывы и императивное недержание мочи, — частый повод обращения к гинекологам и урологам. Состояние требует длительного лечения, первой линией которого специалисты единодушно считают поведенческую терапию [1].
Применение поведенческой терапии при ГМП основано на предположении, что это состояние вызвано утратой выработанного в детстве контроля коры головного мозга над мочеиспускательным рефлексом или наличием патологически сформированного рефлекса. Известно, что больше половины пациенток с ГМП имеют выраженные психические и социальные проблемы, а у 20% из них гиперактивность связана именно с неправильной моделью мочеиспускания. Чтобы восстановить этот контроль, устанавливают определенный ритм мочеиспусканий и постепенно увеличивают интервалы между ними. Перед началом лечения пациентке объясняют, что в норме диурез составляет 1500–2500 мл/сут, средний объем мочеиспускания — 250 мл, функциональная емкость мочевого пузыря — 400–600 мл, допустимое количество мочеиспусканий — в среднем 7–8 раз в сутки. Если этот объем превышает норму, необходимо научить пациентку избегать употребления жидкости без необходимости: пить только во время приема пищи, отказаться от кофе и чая, особенно вечером, ограничить употребление острой пищи и соли, которые вызывают жажду. Исключением являются пациентки, принимающие диуретики. Важно обосновать и необходимость отказа от «вредных» привычек: мочиться «на всякий случай», перед едой или выходом из дома. Целью тренировки мочевого пузыря является постепенное удлинение интервалов между мочеиспусканиями (в начале лечения интервалы между мочеиспусканиями должны быть короткими, например 1 ч, постепенно их доводят до 2,5–3 ч) и увеличение функциональной емкости мочевого пузыря. Таким образом, больная «приучает» свой мочевой пузырь опорожняться только произвольно. Ночью больной разрешается мочиться только в том случае, когда она просыпается из-за позыва на мочеиспускание.
Основным инструментом при таком методе лечения является дневник регистрации мочеиспусканий, в котором должны быть отмечены не только объем выделенной мочи и время мочеиспускания, но и эпизоды недержания мочи (НМ) и смена прокладок. Дневник в обязательном порядке должен изучаться и обсуждаться с врачом на плановых регулярных осмотрах.
Поведенческая терапия особенно эффективна при идиопатической гиперактивности детрузора. Прогноз, безусловно, определяется тем, насколько точно больная следует рекомендациям врача. Высокая эффективность лечения ГМП отмечается при сочетании тренировки мочевого пузыря и медикаментозной терапии.
Упражнения для укрепления мышц тазового дна имеют большое значение не только при стрессовом НМ, когда с их помощью может быть увеличено уретральное давление. Клиническое применение упражнений при ГМП основано на эффекте рефлекторного торможения сокращений детрузора при произвольных и достаточных по силе сокращениях мышц тазового дна [2].
Система выполнения упражнений Кегеля включает поочередное сокращение и расслабление мышц, поднимающих задний проход. Упражнения выполняются 3 раза в сутки. Длительность сокращений постепенно увеличивают: от 1–2 с, 5 с, 10–15 с и от 30 с до 2 мин. Иногда для контроля правильности выполнения упражнений используют перинеометр. Он состоит из баллончика, соединенного с манометром. Больная вводит баллончик во влагалище и определяет силу мышечных сокращений во время упражнений по манометру. «Функциональные» упражнения в дальнейшем предполагают их выполнение не только в позиции релаксации, но и в ситуациях, провоцирующих НМ: при чихании, вставании, прыжках, беге. Несмотря на простоту и широкую известность, упражнения Кегеля в настоящее время применяют редко. Иногда врач советует больной по нескольку раз в день прерывать и возобновлять мочеиспускание. Однако такие упражнения не только устраняют НМ, но и приводят к нарушениям мочеиспускания.
Основное условие эффективности терапии — регулярное выполнение упражнений и врачебный контроль с постоянным наблюдением и обсуждением результатов.
| Рисунок 1. Влагалищные конусы |
Пациенткам, которые не могут идентифицировать необходимые группы мышц, вследствие чего оказываются не в состоянии корректно выполнять упражнения, рекомендуется использовать специальные устройства: влагалищные конусы, баллоны и др. (рис. 1). Конусы имеют одинаковый размер и разную массу (от 20 до 100 г). Больная вводит конус наименьшей массы во влагалище и удерживает его в течение 15 мин. Затем используют более тяжелые конусы [3].
По данным различных исследователей, количество пациенток, не способных сокращать m. pubococcygeus, достигает 40% [4]. Это послужило одной из причин широкого использования метода биологической обратной связи (БОС), целью которого является обучение навыкам сокращения специфических групп мышц и обеспечение обратной связи с пациенткой. Эффективность методики обусловлена активной ролью пациенток в процессе лечения путем вовлечения зрительного (картинки, фильмы, анимация) или слухового (голосовая поддержка) анализаторов. Осуществление обратной связи может проводиться моно- и мультиканально путем регистрации активности тазового дна, абдоминального и детрузорного давлений.
| Рисунок 2. Видео-компьютерный комплекс |
Нами накоплен опыт проведения тренировки мышц тазового дна (ТМТД) в режиме БОС на видео-компьютерном комплексе «УРОПРОКТОКОР» (рис. 2), представляющем собой стационарный прибор, оснащенный периферийным оборудованием, необходимым для лечения расстройств функций тазового дна, и обладающий возможностями мотивационного подкрепления.
Технология использования прибора заключается во введении во влагалище специального датчика, измеряющего электромиограмму (ЭМГ) окружающих мышц, который выполнен из фарфора с золотым напылением. Его можно использовать многократно после предварительной стерилизации. ЭМГ-сигнал анализируется компьютером, который производит построение графиков на экране монитора, информируя пациентку о том, как работают мышцы промежности. Пациентка периодически напрягает и расслабляет мышцы тазового дна («втягивание» ануса) по командам прибора. При этом размеры кривых на мониторе увеличиваются и достигают индивидуально установленного порога. Для максимальной эффективности процедуры используют технологию мотивационного подкрепления: каждое правильно выполненное упражнение сопровождается показом фильма, слайдов и т. п. При некачественном выполнении задания все поощряющие факторы минимизируются, что стимулирует пациентку к более активной работе мышц. Курс лечения состоит из 15–20 получасовых сеансов.
После проведения ТМТД в режиме БОС нами отмечено: уменьшение количества микций с 14 до 8 раз в сутки, эпизодов НМ — с 4 до 1 раза в сутки; показатель порога абдоминального давления увеличился с 38 до 59 см; H2О, средний объем потери мочи уменьшился с 52 до 8 мл. При анализе данных миографии получены следующие результаты: процент правильной работы мышцами тазового дна при первом сеансе составил 60,1% + 10,2%, при 8-м сеансе — 73% + 8,7%, а к 15-му занятию этот показатель равнялся 82,8% + 7,3% (р < 0,05). При анализе полученных клинических данных стало очевидным влияние терапии БОС как на симптомы гиперактивности мочевого пузыря, так и на состояние тазового дна.
Перспективность терапии БОС заключается не только в ее высокой эффективности и отсутствии побочных эффектов, но и в возможности проведения терапии в домашних условиях с использованием индивидуальных портативных приборов. БОС остается методом выбора для пациенток с тяжелыми сопутствующими соматическими заболеваниями, когда другие виды лечения, в том числе медикаментозный, не могут быть применены [5].
Электрическая стимуляция (ЭС) также является эффективным методом лечения ГМП. Она применяется с целью снижения чувствительности мочевого пузыря и увеличения его функциональной емкости, что достигается путем прямого или опосредованного раздражения нервных волокон слабым электрическим током [6]. Электрод вводят либо во влагалище, либо в прямую кишку, возможно использование наружных накладных электродов. Электрические импульсы подаются непрерывно или периодически. Точками приложения являются: уретральный и анальный сфинктеры, мышцы тазового дна, корешки сакрального отдела спинного мозга. В последнее время популярным методом является тибиальная ЭС. Стимуляция афферентных волокон соматической периферической нервной системы, входящих в состав нервных стволов, вызывает торможение парасимпатической активности тазового нерва и увеличение симпатической активности надчревного нерва, в результате чего снижается сократительная активность детрузора.
При выраженной нейрогенной гиперактивности детрузора ЭС производится путем хирургической имплантации системы для ЭС переднего сакрального корешка S3. Побочными действиями могут быть неприятные ощущения во время процедуры, болевые реакции и ощущение неудобства [7].
Медикаментозная терапия, как и поведенческая, является одним из самых распространенных методов лечения ГМП. Такая терапия направлена на устранение беспокоящих симптомов и улучшение уродинамических показателей, т. е. снижение активности детрузора, увеличение функциональной емкости мочевого пузыря. Центральными мишенями терапии являются зоны контроля мочеиспускания в спинном и головном мозге, а периферическими — мочевой пузырь, уретра, периферические нервы и ганглии. На данные «мишени» могут воздействовать следующие препараты:
- лекарственные средства, воздействующие на ионные каналы клеточных мембран;
- антимускариновые/антихолинергические препараты, в том числе двойного миотропного спазмолитического действия;
- антиадренергические;
- трициклические антидепрессанты;
- ингибиторы синтеза простагландинов;
- аналоги вазопрессина;
- афферентные ингибиторы.
Одна из современных классификаций лекарственных средств, снижающих симптомы ГМП, предлагает разделение таких препаратов на четыре типа [8]:
1-й тип — препараты, снижающие эфферентную стимуляцию детрузора (М-холинолитики, a1-адреноблокаторы);
2-й тип — препараты, повышающие ингибирующий контроль, полисинаптические ингибиторы (антидепрессанты);
3-й тип — препараты, снижающие чувствительность мочевого пузыря (токсины);
4-й тип — препараты, снижающие мочеобразование (например, аналоги вазопрессина).
М-холиноблокаторы (оксибутинин, толтеродин, троспиум) признаны одними из наиболее эффективных средств, использующихся для лечения ГМП. Накоплен большой опыт их применения, а безопасность и эффективность оценена в ходе множества сравнительных, плацебо-контролируемых мультицентровых исследований. Используются селективные М-холиноблокаторы. Препарат атропин, не являющийся селективным, в настоящее время применяется редко из-за выраженного системного действия (только введение путем электрофореза).
Рекомендации Европейской Ассоциации урологов по ГМП и императивному недержанию мочи предлагают М-холиноблокаторы в качестве первой линии терапии, а по оценке с точки зрения доказательности препараты этой группы относят к категории «А» (высокая степень доказательности). В России лекарственными средствами группы М-холиноблокаторов, разрешенными к применению и широко назначаемыми, являются оксибутинин, толтеродин, троспиум (неретардированные формы). Изучены аспекты безопасности и эффективности данных лекарственных средств в различных группах больных.
Основной тенденцией, характеризующей современный подход к применению оксибутинина (дриптан, оксибутин), является изменение дозировки и режима дозирования с целью снижения количества побочных эффектов. Препарат с успехом применяется в дозе 3 мг/сут, предлагается схема приема оксибутинина в дозе 5 мг/сут, в случае хорошей переносимости с последующим увеличением на 2,5 мг каждые 2 нед до достижения клинического эффекта. С целью достижения максимальной эффективности и улучшения переносимости рекомендуется внутрипузырное или трансдермальное применение оксибутинина. Проводятся клинические исследования эффективности и безопасности оксибутинина замедленного высвобождения, который при равной эффективности демонстрирует более благоприятный профиль безопасности.
Последние клинические исследования, посвященные препарату толтеродину (детрузитол), подтвердили его высокую клиническую эффективность при симптомах ГМП. Препарат применяется в стандартной дозировке 2 мг 2 раза в день. Многообещающей можно признать и практику применения толтеродина замедленного высвобождения, который также имеет более высокую эффективность в отношении учащения мочеиспускания и императивного недержания мочи по сравнению со стандартными неретардированными формами препарата.
Особого внимания заслуживает также троспиум (спазмекс), который, являясь четвертичным аммониевым соединением, при хорошей клинической эффективности не имеет побочных эффектов со стороны ЦНС. Так, в ходе исследования на добровольцах, отличные от группы плацебо побочные эффекты проявлялись лишь при дозировках, превышающих 180 мг, что как минимум в 4 раза превосходит стандартное дозирование (H. P. Breuel, S. Bondy). Проведенное нами сравнительное исследование двух дозировок троспиума хлорида (спазмекс, PRO. MED. CS, Praha) — 15 мг/сут и 45 мг/сут показало, что на фоне преобладающей эффективности дозы 45 мг/сут, частота побочных эффектов была сравнимой, а побочные эффекты со стороны ЦНС отсутствовали.
Помимо известных М-холинолитиков, на европейском рынке появляются современные селективные препараты, не так давно прошедшие крупномасштабные плацебо-контролируемые исследования. В их числе — солифенацин, который эффективно снижает количество эпизодов ургентного недержания мочи и частоту мочеиспусканий. Доказана высокая эффективность и безопасность препарата (дозировка: 5, 10, 20 мг 1 раз в день). Отмечен минимальный процент выбывания из исследования по причине побочных эффектов. Исследования также показали хорошие фармакокинетические и фармакодинамические параметры этого средства на фоне высокого профиля безопасности при применении 1 раз в день. Фармакокинетика солифенацина при приеме пищи не изменяется.
При ГМП с успехом также могут использоваться препараты, воздействующие на симпатические рецепторы. Известно, что α1-адреноблокаторы: тамсулозин (омник), теразозин (корнам, сетегис, хайтрин), доксазозин (зоксон, камирен, кардура), альфузозин (дальфаз) — снижают симптоматику при расстройствах мочеиспускания, связанных с наличием гиперплазии предстательной железы у мужчин, оказывают влияние на гиперактивность детрузора, возникающую на фоне инфравезикальной обструкции. В ходе открытого проспективного исследования (S. Serels,1998) был проведен сравнительный анализ эффективности α1-блокатора и холинолитика у женщин. Была показана высокая эффективность применения α1-адреноблокатора при симптомах «императивности». Препараты данной группы могут применяться для лечения симптомов ГМП как у мужчин, так и у женщин, особенно в случаях возникновения симптомов ГМП на фоне уродинамически подтвержденной функциональной инфравезикальной обструкции (ИВО). Полученные данные (А. В. Сивков, 2001; Д. Ю. Пушкарь, 2002) говорят о достоверной эффективности α1-адреноблокаторов при симптомах ГМП у женщин на фоне функциональной ИВО. Так, в группе наблюдения частота мочеиспусканий в сутки снизилась на 25–30%, а ночная поллакиурия — на 50%. Назначение α1-блокаторов проводится с учетом вазоактивности. У пациенток молодого возраста препаратом выбора является тамсулозин (0,4 мг/сут). При назначении вазоактивных α1-блокаторов необходимо титрование дозы.
Трициклические антидепрессанты (имипрамин, амитриптилин) обладают центральным и периферическим антихолинергическим и α-адренергическим действием, а также тормозящим влиянием на ЦНС. Они эффективны при пероральном применении (150 мг/сут) у пациенток пожилого возраста с симптомами ГМП. К группе антидепрессантов относится и дулоксетин — комбинированный ингибитор обратного захвата серотонина и норадреналина. Он воздействует на центры контроля мочеиспускания в пояснично-крестцовом отделе спинного мозга (ядра Онуфа). В этих ядрах осуществляется интеграция активности сфинктера и мочевого пузыря. При ингибировании норадреналина повышается тонус сфинктера, а при блокаде серотонина снижается активность мочевого пузыря. В настоящее время рассматривается возможность применения препарата при стрессовых недержаниях мочи. Вывод о целесообразности его использования при гиперактивном мочевом пузыре можно будет сделать лишь по окончании широкомасштабных клинических исследований.
В последние годы возник интерес к применению токсинов при ГМП. Токсин ботулина (торговые названия botox, dysport), используемый в эстетической медицине, способен нормализовать тонус мышцы путем ингибирования высвобождения ацетилхолина из нервного окончания. Показаниями к его применению являются сфинктерные дисфункции и нейрогенная гиперактивность детрузора. Токсин назначается в виде внутрипузырных инъекций (в среднем 30 точек) под цистоскопическим контролем. Противопоказаниями считаются инфекция мочевых путей и гиперчувствительность к препарату, хотя лишь у 2% пациентов образуются антитела к ботулотоксину.
Аналоги вазопрессина (4-й тип лекарственных средств), такие, как десмопрессин (минирин, эмосинт), имеют весьма ограниченную область применения. Основным показанием к их назначению остается смещение диуреза в сторону ночных часов (никтурия) и связанные с ним нарушения мочеиспускания. В настоящий момент проводится исследование по использованию аналогов вазопрессина для коррекции императивного недержания мочи.
В лечении женщин старшей возрастной группы с ГМП определенное место занимает заместительная гормональная терапия. Дефицит эстрогенов приводит к ряду изменений в мочеполовой системе женщины в виде атрофии влагалища, снижения тонуса сфинктеров и повышения чувствительности мочевого пузыря [9]. Однако многие из положительных эффектов эстрогенотерапии, за исключением воздействия на признаки остеопороза, до настоящего времени недостаточно аргументированы, а мнения по этому поводу следует признать противоречивыми [10]. Эффективность эстрогенотерапии в лечении ГМП можно считать спорной. Исследователи отстаивают целесообразность проведения исследований в соответствии с принципами доказательной медицины и качественной клинической практики.
При выборе метода медикаментозного лечения ГМП необходимо принимать во внимание наличие сопутствующих заболеваний, результаты предшествующего лечения, способность и возможность пациентки следовать назначениям врача. Это поможет осуществить правильный подбор препарата и обеспечить высокую эффективность лечения.
После подбора адекватной и эффективной терапии ГМП требуется последующее диспансерное наблюдение и контрольные обследования с интервалами в 3–6 мес.
В. В. Ромих
И. А. Аполихина, кандидат медицинских наук
В. М. Андикян
НЦАГиП РАМН, ММА имени И. М. Сеченова, НИИ урологии, Москва
Литература
- Janssen C. C., Lagro-Janssen A. L., Felling A. J. The effects of physiotherapy for female urinary incontinence: individual compared with group treatment // BJU. Int. — 2001. — Vol. 87. — N 3. — P. 201–206.
- Hay-Smith E., Вo К., Berghmans L. et al. Pelvic floor muscle training for urinary incontinence in women (Cochrane review) // Oxford: The Cochrane Library, 2001.
- Herbison P., Plevnik S., Mantle J. Weighted vaginal cones for urinary incontinence // Cochrane Database Syst. Rev. — 2000. — Vol. 2. — CD002114.
- Gordon D., Luxman D., Sarig Y., Groutz A. Pelvic floor exercise and biofeedback in women with urinary stress Incontinence // Harefuah. — 1999. — Vol. 136. — N 8. — P. 593–596.
- Wang A. C. Bladder-sphincter biofeedback as treatment of detrusor instability in women who failed to respond to oxybutynin // Yi. Xue. Za. Zhi. — 2000. — Vol. 23. — N 10. — P. 590–599.
- Appell R.A. Electrical stimulation for the treatment of urinary incontinence // Urology. — 1998. — Vol. 51. — 2A Suppl. — P. 24–26.
- Bosch R., Groen J., Sacral (S3) segmental nerve stimulation as a treatment for urge incontinence in patients with detrusor instability: results of cronic electrical stimulation using an implantable neural prothesis //J. Urol. — 1995. — Vol. 154, N2. — PP. 504–507.
- Lai H., Boone T., Appell R. Selecting a medical therapy for overactive bladder. Reviews in urology, 2002; 4 (4): 28–37.
- Grady D., Brown J.S., Vittinghoff E. et al. Postmenopausal hormones and incontinence: the Heart and Estrogen/Progestin Replacement Study // Obstet. Gynecol. — 2001. — Vol. 97. — P. 116–120.
- Kuchel G.A., Tannenbaum C., Greenspan S.L., Resnick N.M. Can variability in the hormonal status of elderly women assist in the decision to administer estrogens? // J. Womens Health Gend. Based Med. — 2001. — Vol. 10. — N 2. — P. 109–116.
Введение
Гиперактивный мочевой пузырь (ГАМП) — довольно распространенный синдром, сопровождающийся рядом симптомов нижних мочевыводящих путей. Симптомы этого заболевания могут быть проявлением нейрогенной дисфункции мочевого пузыря, но могут иметь и идиопатический характер. Синдром ГАМП имеет достаточно точные клинические характеристики: учащенное мочеиспускание в дневное или ночное время, сочетающееся с ургентными позывами и недержанием мочи.
Первую линию медикаментозной терапии ГАМП представляют препараты, относящиеся к группе м-холинолитиков. Препараты этой группы могут проникать через гематоэнцефалический барьер и влиять на когнитивные функции, что делает их небезопасными, особенно для пациентов пожилого возраста.
При лечении пожилых пациентов существует угроза развития полипрагмазии, последствия которой трудно предугадать [1]. Поэтому так важно при назначении терапии опираться на принципы гериатрической медицины, которая предлагает различные критерии выбора препарата, наиболее безопасного для пожилого пациента. В рамках безопасной стратегии лечения пожилых пациентов разрабатываются различные критерии и списки, к наиболее известным из них относят списки Бирса [2]. Для оценки безопасности препаратов, применяемых пожилыми пациентами, используется классификация FORTA (Fit fOR the Aged) 2008 г. [3]. Классификация FORTA предлагает несколько классов препаратов для пожилых пациентов с учетом реальной практики, а не только исследований, основанных на принципах доказательной медицины. Ни одному препарату для лечения ГАМП не присвоен самый высокий класс безопасности (класс А) по системе FORTA. Фезотеродин — единственный препарат из группы м-холинолитиков, который по безопасности и эффективности отнесен к классу В. К классу B (B-eneficial) в системе FORTA отнесены препараты, имеющие некоторые ограничения по эффективности или безопасности, но показывающие наибольшую доказанную или очевидную эффективность при лечении пожилых людей [4].
Приводим клинические случаи ГАМП, различных по этиологии и характеру течения, у пациентов разного пола, возраста и с различным коморбидным фоном.
Клиническое наблюдение № 1
Мужчина, 74 года, обратился в клинику с жалобами на учащенные позывы к мочеиспусканию, затрудненное мочеиспускание небольшими порциями, часто носящее неотложный характер, ночное мочеиспускание до 3–4 раз. Сопутствующее заболевание — сахарный диабет 2 типа. Пациент постоянно принимает метформина гидрохлорид.
В анамнезе у пациента два эпизода острой задержки мочеиспускания, длительный период неэффективной терапии симптомов опорожнения мочевого пузыря. За 2 мес. до обращения он перенес трансуретральную резекцию (ТУР) предстательной железы в связи с ее доброкачественной гиперплазией (ДГПЖ). Пациент отметил, что жалобы, указанные при обращении, появились у него через несколько дней после операции. В течение 2 мес. он получал антибактериальное и противовоспалительное лечение без должного эффекта. Лейкоцитоз в общем анализе крови отсутствовал. Глюкоза крови — 4,9 ммоль/л. В общем анализе мочи лейкоцитов 15–20 в поле зрения, эритроцитов — 1–5 в поле зрения, бактерий не обнаружено. При бактериологическом исследовании мочи роста микрофлоры не получено. По данным трансректальной ультрасонографии предстательной железы суммарный объем ее составил 22 см3 (по данным амбулаторной карты, объем предстательной железы до операции составлял 74 см3), контуры четкие и ровные, капсула непрерывная, прослеживается по всей поверхности. Структура центральной доли предстательной железы умеренно диффузно неоднородная, с наличием мелких фокусов повышенной эхоплотности. В простатическом отделе определяется дефект до 9 мм вследствие ТУР. Структура периферической зоны однородная, средней эхогенности, без очаговых изменений. УЗИ не выявило остаточной мочи.
По данным дневников мочеиспускания, пациент выделяет мочу порциями до 90 мл 11–12 раз в сутки, мочеиспускание носит императивный характер, периодически сопровождается подтеканием мочи небольшими порциями. Тестирование по шкале I-PSS показало 13 баллов с преобладанием симптомов накопления мочевого пузыря (по данным амбулаторной карты, I-PSS до операции составлял 27 баллов). Данные урофлоуметрии нерепрезентативны из-за небольшого объема выделяемой мочи.
Учитывая симптомы ГАМП, в качестве монотерапии пациенту был назначен фезотеродин (Товиаз®) в дозе 8 мг/сут на 3 мес. Рекомендованы контроль остаточной мочи и ведение дневников мочеиспускания в течение 3 сут не реже 2 раз в месяц. Значительный эффект был достигнут уже к концу первого месяца лечения. Пациент отметил снижение частоты дневных (до 4–5 раз) и ночных (до 2 раз) микций, исчезновение императивных позывов и недержания мочи, снижение показателя I-PSS до 7 баллов. Контрольное УЗИ не выявило остаточной мочи.
Представленное клиническое наблюдение демонстрирует возможность использования фезотеродина, представителя м-холинолитиков, для купирования дизурии после оперативного лечения ДГПЖ. Симптомы накопления у этого пожилого пациента были связаны не только с перенесенным оперативным лечением, но и с длительно существовавшей до операции инфравезикальной обструкцией. Фезотеродин использовался в качестве монотерапии, с отменой принимавшихся до этого уросептиков, α1-адреноблокаторов и противовоспалительных препаратов.
Интересно, что симптомы ГАМП на фоне доброкачественной гиперплазии предстательной железы также могут быть основанием для назначения м-холинолитиков, что подтверждается рекомендациями EAU [5].
Клиническое наблюдение № 2
Мужчина, 54 года, несколько лет наблюдается у уролога по месту жительства с диагнозом «хронический простатит». Жалобы на учащение мочеиспускания днем (через каждые 2 ч) и в ночное время (от 2 до 3 раз), вялую струю мочи, периодически возникающие резкие, трудно сдерживаемые позывы к мочеиспусканию. Считает себя больным в течение последних двух лет, когда впервые обратил внимание на появление указанных жалоб после переохлаждения. Проходил неоднократные курсы лечения хронического простатита без значимого эффекта.
По шкале I-PSS суммарный показатель составил 24 балла с преобладанием симптомов накопления, QoL 4 балла. В сыворотке крови уровень общего простатического специфического антигена (ПСА) составил 1,630 нг/мл, свободного ПСА — 0,580 нг/мл, соотношение свободный/общий составило 35,6%. В общем анализе мочи лейкоцитурии и эритроцитурии нет. При микроскопии секрета предстательной железы 1–2 лейкоцита в поле зрения. При пальцевом исследовании предстательная железа безболезненная, имеет четкие и ровные контуры, сглаженную срединную борозду, тугоэластическую консистенцию, увеличена в размерах незначительно. По данным трансректального УЗИ, предстательная железа имеет четкие и ровные контуры, четко дифференцируемую на всем своем протяжении капсулу. Объем предстательной железы — 36 см3, эхоструктура диффузно неоднородная, средней эхогенности, с узлом гиперплазии, состоящим из боковых и средней долей, общий объем — 11 см3. Периферические отделы предстательной железы не имеют очаговых изменений. По данным урофлоуметрии, максимальная скорость мочеиспускания (Qmax) — 11,8 мл/с, средняя скорость мочеиспускания (Qave) — 8,6 мл/с. Остаточная моча — 98 мл. Перед выбором метода лечения был проанализирован дневник мочеиспускания, который пациент вел в течение
3 сут. Сведения из дневника: мочился от 9 до 15 раз в сутки с 3–4 эпизодами ургентности, 3 ночными микциями, объем мочи — от 50 до 210 мл.
Пациенту была назначена терапия м-холинолитиками в сочетании с α1-адреноблокатором. В качестве м-холинолитика был выбран фезотеродин (Товиаз®) в начальной дозе 4 мг/мл. Проводился ежемесячный динамический контроль состояния пациента с контролем остаточной мочи. При контрольном обследовании через 3 мес. лечения балл I-PSS снизился до 9, балл QoL — до 1. У пациента отмечено увеличение объема порций мочи до 300–400 мл. Снизилось количество суточных мочеиспусканий до 8–9, и исчезли эпизоды ургентности. Остаточная моча — в пределах 70–80 мл. При контрольной урофлоуметрии Qmax — 14,2 мл/с, Qave — 8,8 мл/с.
М-холинолитики могут быть назначены мужчинам с ДГПЖ [6] при условии, что объем остаточной мочи не превышает 150 мл. При таком объеме остаточной мочи риск острой задержки мочеиспускания минимальный. Приведенный пример указывает не только на возможность эффективного лечения симптомов ГАМП при ДГПЖ, но и демонстрирует возможность того, что у ряда пациентов клинический эффект в подавлении ургентности и учащении мочеиспускания может быть достигнут приемом 4 мг/сут препарата. При недостаточной эффективности доза препарата может быть увеличена в 2 раза [7].
Клиническое наблюдение № 3
Женщина, 36 лет, в течение последнего года стала отмечать учащенное мочеиспускание в дневное время, постоянные позывы на мочеиспускание, эпизоды императивных позывов на мочеиспускание. У пациентки в анамнезе двое неосложненных родов, острые циститы, возникавшие с периодичностью 1 раз в 2–3 года. Хронические заболевания отрицает, регулярно посещает гинеколога при диспансеризации. Около месяца назад перенесла цистоскопию, при которой не выявлено изменений со стороны слизистой мочевого пузыря, за исключением небольшого линейного участка метаплазии в области треугольника Льето.
По данным проведенного обследования не выявлено изменений со стороны верхних мочевыводящих путей, в общем анализе мочи 1–2 лейкоцита в поле зрения. При осмотре в кресле: влагалище рожавшей женщины, пролапса тазовых органов нет, непроизвольного подтекания мочи при кашлевой пробе нет. УЗИ мочевого пузыря не выявило изменений стенки органа, остаточной мочи нет. По данным дневника мочеиспусканий, пациентка мочится небольшими порциями до 18 раз за сутки, с 2–3 ургентными позывами, ночные микции отсутствуют.
Выполнено комплексное уродинамическое исследование (КУДИ), выявившее фазовую детрузорную гиперактивность с максимальным детрузорным давлением 35 см вод. ст. и снижением цистометрической емкости до 250 мл. Был назначен фезотеродин (Товиаз®) в дозе 4 мг/сут. Через 4 нед. пациентка отмечала сохранение симптомов учащенного мочеиспускания на фоне заметного снижения частоты ургентности и выраженности позывов к мочеиспусканию. Доза препарата была увеличена до 8 мг/сут. Оценка эффективности лечения проведена через 3 мес. Из дневника мочеиспускания: пациентка мочилась в среднем от 5 до 7 раз в сутки, ургентные позывы к мочеиспусканию отсутствовали. По данным контрольного КУДИ, максимальное детрузорное давление составило 10 см водн. ст.,
цистометрическая емкость восстановилась, эпизодов детрузорной гиперактивности не выявлено. К побочным эффектам препарата она отнесла легкую сухость в полости рта, при этом отметила, что сухость в меньшей степени влияет на качество жизни, нежели постоянные позывы на мочеиспускание.
Приведенный пример демонстрирует эффективное лечение идиопатической формы ГАМП.
Клиническое наблюдение № 4
Женщина, 68 лет, обратилась в клинику в сопровождении дочери, по направлению невролога, у которого наблюдается с диагнозом «лобно-височная деменция с кортикобазальным синдромом». Основные жалобы при обращении касались учащения мочеиспускания днем и в ночное время. Позывы к мочеиспусканию значительно усиливались при звуке падающей воды. Пациентка не успевала дойти до туалетной комнаты, как у нее непроизвольно начинала выделяться моча, что вынуждало использовать абсорбирующие средства.
Заболевание началось в апреле 2019 г., когда у пациентки возникло нарушение речи, ограничения в движении ноги и руки слева на фоне эмоционального потрясения. Из сопутствующих заболеваний можно
выделить медикаментозно компенсированную артериальную гипертонию, аутоиммунный тиреоидит (находится на заместительной гормональной терапии). По данным МРТ: признаки прогрессирующей атрофии коры больших полушарий, преимущественно за счет правых отделов с заместительным расширением желудочков мозга. На момент обращения, кроме гипотензивной терапии и левотироксина, принимала мемантин 20 мг/сут и троспия хлорид 45 мг/сут.
Неврологический статус: ходит самостоятельно, речь представлена простыми односложными фразами. Память на события жизни грубо не нарушена, нет явных нарушений краткосрочной памяти (по шкале MoCA 21 балл). Отмечается апраксия копирования с рук. Имеются оптико-пространственные нарушения. Изменения мимической мускулатуры за счет центрального пареза лицевого нерва слева. Небольшой тремор покоя языка. Оценка чувствительности рук не показала аномалий по всем модальностям. Тонус правой руки не изменен. Тонус левой руки: спастика с элементами ригидности, легкий парез. Рефлексы: слева 3+, справа 2+. Правая нога с нормальным тонусом, слева спастика с положительным рефлексом Бабинского. Рефлексы: слева 3+, справа 2+. Атаксия и брадикинезия слева. Чувствительность нижних конечностей не нарушена.
Урологический статус: принимает троспия хлорид в дозе 45 мг/сут в течение 2 мес., без значимого эффекта. Мочится небольшими порциями на фоне ургентных позывов на мочеиспускание до 25 раз в сутки, с недержанием мочи. Область почек и мочевого пузыря при осмотре и пальпации не изменена. При осмотре в кресле выявлено ректоцеле 1, цистоцеле 0, шейка матки не изменена. Непроизвольного выделения мочи из уретры при кашлевой пробе нет. Уретральным катетером из мочевого пузыря забрана моча для бактериологического исследования, так как в представленном общем анализе мочи выявлено 15–20 лейкоцитов в поле зрения. Последующее исследование не выявило роста бактериальной флоры в моче. При УЗИ мочевыделительной системы не выявлено остаточной мочи и иных изменений со стороны почек и мочевого пузыря. По данным КУДИ, у пациентки гиперсенсорный мочевой пузырь с терминальной гиперактивностью на фоне наполнения до 120 мл и непроизвольным выделением мочи из уретры, помимо ее оттока по уродинамическому катетеру. На фоне приема фезотеродина у пациентки уменьшилось количество мочеиспусканий в дневное и ночное время. Она отказалась от использования урологических прокладок днем, отметила сокращение числа эпизодов ургентности и недержания мочи более чем в 2 раза.
Нейрогенная гиперактивность мочевого пузыря в результате острого и хронического нарушения мозгового кровообращения и демиелинизирующих заболеваний ограничивает применение м-холинолитиков из-за их способности проникать через гематоэнцефалический барьер и влиять на когнитивные функции. Выбор м-холинолитиков для лечения таких пациентов ограничен несколькими препаратами, среди которых троспия хлорид и фезотеродин [8]. Ввиду недостаточной эффективности троспия хлорида было принято решение о смене его на фезотеродин (Товиаз®) в дозе 8 мг/сут. Низкая липофильность и высокая молекулярная масса препятствуют проникновению фезотеродина через гематоэнцефалический барьер, что делает его безопасным [9]. В приведенном клиническом примере не отмечено нежелательных эффектов препарата. Известно, что такие эффекты зависят не только от проницаемости гематоэнцефалического барьера, степени дегенерации холинергических нейронов, общей нагрузки антихолинергическими препаратами, но и от исходного когнитивного статуса пациента [10].
Фезотеродин успешно применяется при нейрогенной гиперактивности мочевого пузыря, которая встречается при различных заболеваниях головного мозга, а также при поражениях спинного мозга выше спинальных центров микции [11]. Особенностью ГАМП при супраспинальном уровне повреждения спинного мозга является опасность развития детрузорно-сфинктерной диссинергии. Это состояние часто приводит к осложнениям со стороны верхних мочевыводящих путей [12]. Кроме этого, острые и хронические нарушения мозгового кровообращения чаще развиваются у пациентов пожилого возраста, что также требует применения безопасного препарата, показанного геронтологическим больным. Одним из наиболее эффективных методов лечения таких пациентов является подавление детрузорной гиперактивности с последующим переводом пациента на режим периодической катетеризации мочевого пузыря.
Клиническое наблюдение № 5
Пациент, 28 лет, обратился с жалобами на появившиеся затруднения при мочеиспускании, периодически возникающие в ответ на переполнение мочевого пузыря, головные боли, гиперемию кожных покровов лица и шеи, обильное потоотделение, сопровождающиеся подъемами артериального давления до 180/100 мм рт. ст.
Из анамнеза известно, что в январе 2015 г. мужчина получил позвоночно-спинномозговую травму на уровне позвонков С4–С5 с ушибом спинного мозга. Оперирован, перенес спондилодез С4–С6. С февраля 2015 г. состояние пациента позволило начать активную реабилитацию. С апреля 2015 г. отмечено значительное улучшение состояния, он смог стоять без опоры. В первые 2 мес. после оперативного лечения у пациента стоял цистостомический дренаж. Затем к нему вернулось чувство позыва к мочеиспусканию, восстановилось непроизвольное мочеиспускание небольшими порциями, носящее ургентный характер. Цистостомический свищ был заживлен, и пациент начал использовать уропрезерватив. С мая 2018 г. состояние ухудшилось, и появились указанные выше симптомы. При неврологическом осмотре определен уровень повреждения нервной системы как моторный с уровня сегмента С4, сенсорный — с сегмента С5, рефлексы 4+ во всех пробах на всех конечностях. Клонус с кистей больше, чем со стоп. Тонус мышц оценен как спастика в 2 балла по шкале Ашфорта на ногах, в 3 балла на руках. Оценка по шкале ASIA — С. Может с минимальной поддержкой встать с кресла. Требуется время для инициации ходьбы. Может сидеть без опоры. Ходьба спастического типа. Признаки выраженной автономной диcрефлексии на холод и на переполнение мочевого пузыря.
В анализе мочи признаков воспаления и бактериального загрязнения нет. По данным ультрасонографии, структурных изменений мочевыводящих путей нет. Средний объем остаточной мочи — 200 мл. При нейроурологическом осмотре: яркие бульбокавернозный и анальный рефлексы. Мочеиспускание небольшими порциями носит частый и ургентный характер, инициируется раздражением кожных покровов передней брюшной стенки в области мочевого пузыря. Эпизоды головной боли с гиперемией кожных покровов и высоким артериальным давлением (до 180/100 мм рт. ст. при базовом артериальном давлении 110/70 мм рт. ст.) возникают 1–2 раза в сутки. Указанные симптомы расценены как автономная диcрефлексия, главной характеристикой которой является подъем артериального давления на 20 мм рт. ст. от базового значения в ответ на триггеры, в данном случае триггером служило переполнение мочевого пузыря. По данным уродинамического исследования, у пациента фазовая детрузорная гиперактивность с максимальным значением детрузорного давления 79 см вод. ст. Максимальное давление в точке утечки составило 69 см вод. ст.
С целью купирования нейрогенной детрузорной гиперактивности пациенту назначен фезотеродин (Товиаз®) на постоянной основе в дозировке 8 мг/сут, с переводом на периодическую катетеризацию мочевого пузыря. При контрольном осмотре через месяц у пациента исчезли эпизоды автономной дисрефлексии, связанные с переполнением мочевого пузыря. Он отметил значительное улучшение качества жизни. Контрольное уродинамическое исследование через 3 мес. показало значительное снижение максимального детрузорного давления и детрузорного давления в точке утечки.
Этот клинический пример показал возможность м-холинолитика в купировании нейрогенной детрузорной гиперактивности и автономной дисрефлексии. Автономная дисрефлексия возникает при высоком уровне повреждения спинного мозга, выше сегмента Тh6 [13]. Она имеет крайне негативные последствия для качества жизни пациента и значительно ухудшает его коморбидный фон. Сегодня ведутся исследования применения фезотеродина для купирования автономной дисрефлексии и облегчения страданий у наиболее сложных пациентов — инвалидов с травмой спинного мозга [14].
Заключение
Во всех представленных клинических наблюдениях была успешно применена медикаментозная терапия ГАМП м-холиноблокатором фезотеродином (Товиаз®). Применение фезотеродина позволило добиться выраженного клинического эффекта в виде подавления ургентности и снижения частоты позывов к мочеиспусканию при идиопатическом и нейрогенном ГАМП. Фезотеродин демонстрирует эффективность в купировании симптомов накопления у пациентов с ДГПЖ в составе комбинированной терапии с α1-адреноблокатором. Он может применяться у пациентов с дизурическими расстройствами после перенесенной ТУР предстательной железы, а также при неэффективности другого м-холинолитика в комбинации с ним или с его заменой.
Фезотеродин (Товиаз®) применяется в дозе 4 мг и 8 мг. Лечение лучше начать с 4 мг c последующим увеличением дозы препарата при необходимости или сразу с 8 мг по показаниям. Выбор должен быть сделан индивидуально, в зависимости от клинической ситуации. Обычно нейрогенный ГАМП требует применения более высоких доз м-холинолитика.
Фезотеродин может применяться у геронтологических больных, он единственный из м-холинолитиков по безопасности и эффективности отнесен к классу В по классификации FORTA. Липофильные свойства и высокая молекулярная масса фезотеродина ограничивают его проникновение через гематоэнцефалический барьер, что позволяет минимизировать центральные побочные эффекты, к которым относятся и когнитивные нарушения. Таким образом, фезотеродин может быть применен у пожилых пациентов и пациентов с ГАМП при нарушениях мозгового кровообращения.
Особенностью применения м-холинолитиков у некоторых пациентов со спинальным уровнем поражения нервной системы является необходимость дополнительного дренирования мочевого пузыря, метод выбора — периодическая катетеризация. Новым перспективным показанием к применению фезотеродина может стать автономная дисрефлексия, но это предположение требует дальнейших исследований.
Благодарность
Редакция благодарит компанию Pierre Fabre за помощь в обеспечении взаимодействия между авторами настоящей публикации.
