Статьи
Опубликовано в журнале:
«Терапевтический архив», 1, 2019, с. 114-120.
Ж.М. Сизова, Е.В. Ших, А.А. Махова
ФГАОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России (Сеченовский Университет), Москва, Россия
Аннотация
В обзоре представлены результаты целого ряда экспериментальных и клинических исследований, доказывающих перспективность применения L-карнитина в клинике внутренних болезней. Дополнительный прием L-карнитина за счет антиоксидантных и антиги-поксантных свойств в дополнение к основной этиопатогенетической терапии назначается кардиологами, нефрологами, неврологами, геронтологами. Ранее проведенные нами экспериментальные исследования показали отсутствие влияния L-карнитина на активность системы Р450 CYP 3А4, что снижает вероятность возникновения межлекарственного взаимодействия на уровне метаболизма лекарственных препаратов, метаболизирующихся Р450 3А4. При использовании L-карнитина в составе комплексной фармакотерапии, препарат обладает повышенным профилем безопасности у коморбидных пациентов, принимающих L-карнитин.
Ключевые слова: L-карнитин, Р450 CYP 3А4, хроническая сердечная недостаточность, инфаркт миокарда, хроническая почечная недостаточность, межлекарственное взаимодействие, антиоксидант, антигипоксант.
Significance of L-carnitine in internal medicine
Zh.M. Sizova, E.V. Shikh, A.A. Makhova
I.M. Sechenov First Moscow State Medical University of the Ministry of Health of the Russian Federation (Sechenov University), Moscow, Russia
The review presents the results of a number of experimental and clinical studies proving the prospects of using L-carnitine in the clinic of internal diseases. Due to the antioxidant and antihypoxant properties, the additional use of L-carnitine in addition to the main etiopatho-genetic therapy is prescribed by cardiologists, nephrologists, neurologists, gerontologists. Experimental studies we conducted earlier showed no effect of L-carnitine on the activity of the P450 CYP 3A4 system, which reduces the likelihood of drug-drug interaction at the level of metabolism of drugs metabolized by P450 3A4. When using L-carnitine as part of complex pharmacotherapy, the drug has an increased safety profile in comorbid patients taking L-carnitine.
Keywords: L-carnitine, P450 CYP 3А4, chronic heart failure, myocardial infarction, chronic renal failure, inter-drug interaction, antioxidant, antihypoxant.
АТФ — аденозинтрифосфорная кислота
АФК — активные формы кислорода
БАД — биологически активные вещества
ВРС — взвешенная разность средних
ДИ — доверительный интервал
ДЭ — дисциркуляторная энцефалопатия
ИИ — ишемический инсульт
ИМ — инфаркт миокарда
КДО — конечный диастолический объем
КСО — конечный систолический объем
ЛЖ — левый желудочек
ЛС — лекарственные средства
МСКТ — мультиспиральная компьютерная томография
ОКС — острый коронарный синдром
ОШ — отношение шансов
РКИ — рандомизированные контролируемые исследования
УЗДГ — ультразвуковая диагностика
ФВ — фракция выброса
ХСН — хроническая сердечная недостаточность
ЭКГ — электрокардиография
ЭПО — эритропоэтин
BNP — мозговой натрийуретический пептид
NAD — никотинамидадениндинуклеотид
NIHSS — шкала оценки тяжести инсульта Национального института здоровья США
NKF — Национальный фонд почек
NT-proBNP — N-терминальный мозговой натрийуретический пропептид
В настоящее время фокус клинической медицины смещается в сторону персонализированной медицины, основу которой составляют повышение эффективности и безопасности лекарственной терапии за счет индивидуализации. При назначении комбинированной фармакотерапии особое внимание уделяется вопросам взаимодействия лекарственных средств (ЛС) [1].
Витамины и витаминоподобные вещества являются жизненно необходимыми органическими соединениями, участвующими в основных биохимических процессах в организме человека, и широко применяются в клинической практике, чаще в составе комбинированной терапии для лечения и коррекции целого ряда патологических состояний. Однако, как правило, врачами не учитывается возможное влияние витаминов и витаминоподобных веществ на активность изоферментов цитохрома, метаболизирующих ЛС, что, как было показано в целом ряде исследований, может приводить к изменениям фармакологического ответа на лекарственную терапию [1,2].
L-карнитин — производное аминокислоты лизина, получил свое название в связи с тем, что впервые был выделен из мяса (carnis). В последние годы биологическая роль L-кар-нитина в организме человека прицельно изучается в связи с широкими перспективами его клинического применения [3].
У здоровых людей гомеостаз L-карнитина поддерживается посредством многостадийного эндогенного биосинтеза L-карнитина из аминокислот лизина и метионина, его абсорбции из пищи и дальнейшей элиминации и реабсорбции почками. Хотя биодоступность L-карнитина из пищи довольно высока, при пероральном приеме биологически активных веществ (БАД), содержащих L-карнитин, абсорбция его составляет 14-18% от общей дозы [3- 5]. Поиск соединений L-карнитина с более высокой биодоступностью привел к разработке ацетилированной формы L-карнитина, биодоступность которой при пероральном приеме выше, чем у L-карнитина [6]. Так, в частности, показано, что прием L-карнитина в дозе 2,0 г/сут в течение 50 дней увеличивает плазменный уровень L-карнитина на 43% [3].
В норме большая часть L-карнитина реабсорбируется почками, в связи с чем экскреция его обычно низкая. Однако некоторые состояния (диета с повышенным содержанием белка и жиров, беременность) способствуют снижению реабсорбции L-карнитина и, соответственно, приводят к увеличению его экскреции и уменьшению содержания в организме [7].
L-карнитин синтезируется главным образом в печени, но также и в почках, а затем транспортируется в другие ткани, особенно использующие жирные кислоты в качестве основного субстрата для образования аденозинтрифосфорной кислоты (АТФ), такие как скелетная мускулатура и сердечные мышцы. Одна из основных функций L-карнитина — транспорт жирных кислот (преимущественно длинноцепочечных) через внутреннюю мембрану в матрикс митохондрии для образования АТФ в процессе p-окисления [3]. С этой целью одни специфические митохондриальные ферменты переносят жирные кислоты на L-карнитин с образованием ацилкарнитинов, другие -транспортируют это эфирное соединение в митохондриальный матрикс [8].
У здоровых людей без нарушений обмена веществ, как правило, синтезируется достаточное количество L-карни-тина, даже у строгих вегетарианцев (веганов) не обнаруживаются признаки дефицита L-карнитина [3, 9]. Однако младенцы, особенно недоношенные, рождаются с низкими запасами L-карнитина, что ставит их в группу риска по дефициту карнитина, учитывая высокие темпы роста в данной возрастной группе.
Первичный дефицит карнитина
Генерализованная форма первичного дефицита L-кар-нитина. Первичный системный дефицит карнитина представляет собой редкое аутосомно-рецессивное расстройство, вызванное мутациями в гене для транспортного белка L-карнитина OCTN2, что приводит к низкой абсорбции L-карнитина и нарушению его реабсорбции почками — повышению потери L-карнитина с мочой [10-12]. Расстройство обычно проявляется в раннем детстве и характеризуется низким уровнем L-карнитина в плазме крови, прогрессирующей кардиомиопатией, скелетной миопатией, гипогликемией и гипоаммониемией [3, 10, 12]. Без лечения первичный системный дефицит L-карнитина является фатальным заболеванием. Лечение состоит из назначения фармакологических доз L-карнитина. Такая терапия корректирует кардиомиопатию и устраняет мышечную слабость [11].
Миопатическая форма первичного дефицита L-карни-тина — редкое генетическое заболевание, при котором дефицит L-карнитина ограничен скелетной и сердечной мышцами. Симптомы, включая мышечную боль и прогрессирующую мышечную слабость, начинаются в детстве или в подростковом возрасте при обычно нормальном плазменном уровне L-карнитина [12]. Клиническая картина менее выражена, чем при генерализованной форме.
Вторичный дефицит карнитина
Вторичный дефицит L-карнитина может быть результатом генетических или приобретенных состояний. Наследственные причины включают генетические дефекты в обмене аминокислот (например, пропионовой кислоты) и дефекты в липидном обмене (например, дефицит ацил-КоА-дегидрогеназы средней цепи) [13]. Такие генетические нарушения могут приводить к накоплению органических кислот, которые впоследствии удаляются из организма в форме ацилкарнитиновых эфиров с мочой, что может привести к системному истощению L-карнитина [3]. Системное снижение обеспеченности L-карнитином может также возникать при нарушениях его реабсорбции почками, как, например, при синдроме Фанкони (врожденная или приобретенная диффузная дисфункция проксимальных извитых почечных канальцев). Одним из примеров исключительно приобретенного дефицита L-карнитина является хроническое применение пивалат-конъюгирован-ных антибиотиков. Пивалат представляет собой жирную кислоту с разветвленной цепью, которая метаболизируется с образованием эфира ацил-КоА, который в свою очередь при помощи специфических ферментов переносится на L-карнитин и затем выводится с мочой в виде пивалоильного эфира L-карнитина. Ежедневные потери L-карнитина по такому метаболическому пути могут в 10 раз превышать ежедневное поступление L-карнитина, приводя к системному снижению запасов L-карнитина [11]. Кроме того, пациенты с почечной недостаточностью, которые находятся на гемодиализе, подвергаются риску вторичного дефицита L-карнитина, поскольку гемодиализ удаляет L-карнитин из крови [14].
Независимо от этиологии, вторичный дефицит L-карни-тина характеризуется клинически низкими концентрациями свободного L-карнитина в плазме (менее 20 мкмоль/л) и повышенным соотношением ацилкарнитин/свободный L-кар-нитин (более 0,4) [13]. Вторичные дефициты встречаются чаще, чем первичные формы дефицита L-карнитина.
Эндогенный биосинтез L-карнитина катализируется согласованным действием пяти различных ферментов. Для этого процесса требуются две незаменимые аминокислоты (лизин и метионин), железо (Fe2+), витамин B6, ниацин в форме никотинамидадениндинуклеотида (NAD) и также витамин C [12]. Один из самых ранних симптомов дефицита витамина С — усталость, является проявлением снижения синтеза L-карнитина [15].
Связь L-карнитина с процессом старения
Известно, что c возрастом угасает митохондриальная функция и увеличивается производство митохондриальных окислителей. Установлено, что уровень L-карнитина в тканях с возрастом у людей и животных также снижается [16]. В одном из исследований доказано, что кормление ацетил-L-карнитином пожилых крыс (ALCAR) повышает уровень L-карнитина в тканях, а также нивелирует ряд возрастных изменений в функционировании митохондрий печени, митохондрий в скелетной и сердечной мышцах [17-19]. Исследования показали, что добавление в рацион питания пожилым крысам ALCAR приводит к снижению окислительного стресса и улучшению когнитивных функций [20, 21].
Сердечно-сосудистые заболевания
L-карнитин в составе комплексной фармакотерапии острого коронарного синдрома (ОКС). Применение L-кар-нитина в составе комплексной терапии сразу после диагностики инфаркта миокарда (ИМ) улучшало клинические результаты в нескольких небольших клинических исследованиях. В одном из исследований половина из 160 мужчин и женщин с диагнозом ИМ рандомизированы для приема 4 г/сут перорального L-карнитина в дополнение к стандартной фармакологической терапии. После одного года лечения смертность оказалась значительно ниже в группе дополнительного приема L-карнитина по сравнению с контрольной группой (1,2% против 12,5%), а приступы стенокардии были статистически значимо менее частыми [22].
В контролируемом клиническом исследовании у 96 пациентов с сердечной недостаточностью применение внутривенного L-карнитина (5 г болюсно с последующим введением 10 г/сут в течение 3 дней) после ИМ позволило достигнуть более выраженного снижения уровня таких маркеров повреждения сердечной мышцы, как креатинкиназа-МБ и тропонин-I [23].
В рандомизированном двойном слепом плацебо-контро-лируемом исследовании 60 мужчинам и женщинам с диагнозом острого ИМ назначался либо внутривенный L-кар-нитин (6 г/сут) в течение 7 дней, затем перорально 3 г/сут в течение 3 мес либо плацебо [24]. Через 3 мес смертность между двумя группами не различалась. В более крупном плацебо-контролируемом исследовании с участием 472 пациентов, которым проводили терапию в отделении интенсивной терапии в течение 24 ч после первичного ИМ: случайным образом назначали либо внутривенную терапию L-карнитином (9 г/сут) в течение 5 дней, а затем пероральный L-карнитин (6 г/сут) в течение 12 мес либо плацебо. Обе группы также получали стандартную комплексную терапию [25, 26]. Несмотря на отсутствие значительных различий в смертности или частоте формирования хронической сердечной недостаточности (ХСН), объем левого желудочка (ЛЖ) был значительно ниже в группе, получавшей L-карнитин, в конце одного года наблюдения, что свидетельствует о том, что терапия L-карнитином может ограничивать неблагоприятные исходы острого ИМ на сердечной мышце. На основании этих данных проведено рандомизированное плацебо-контролируемое исследование у 2330 пациентов с острым ИМ.
Цель исследования — определить влияние добавления к фармакотерапии L-карнитина на частоту формирования сердечной недостаточности через 6 мес после ИМ. Лекарственная терапия L-карнитином снижала на 39% риск летального исхода в первые 5 дней (р=0,04), когда L-карни-тин применяли внутривенно по 9 г/сут, и не влияла на частоту формирования сердечной недостаточности и частоту летальных исходов при дальнейшем пероральном приеме по 4 г/сут до окончания исследования [27]. В проспективном открытом контролируемом исследовании изучалась эффективность и безопасность инъекционной формы отечественного препарата L-карнитина (Элькар раствор для внутривенного и внутримышечного введения 100 мг/мл, компания ПИК-ФАРМА) в условиях отделения реанимации и интенсивной терапии при синдроме малого выброса у больных с острым ИМ. Инъекции препарата Элькар при остром ИМ снижали на 82% содержание тропонина в крови на 5-7-й день госпитализации (р<0,01). Фракция выброса (ФВ) ЛЖ в группе L-карнитина ускоренно нарастала к 5-7-м суткам с 35,5±0,9 до 45,4±1,2% по сравнению с контрольной группой — с 35,8±0,7 до 40,1±0,9% (р<0,05) [28]. Заслуживают внимания результаты пилотного плаце-бо-контролируемого исследования эффективности и безопасности инъекций L-карнитина (Элькар раствор для внутривенного и внутримышечного введения 100 мг/мл) при лечении ОКС. Терапия L-карнитином снижала дисперсию корригированного интервала QT (AQTc) начиная со вторых суток лечения (р=0,008), и на 12-14-е сутки наблюдения межгрупповое различие составило 27,6% (р<0,0001) [29].
В группе пациентов, получавших L-карнитин, уменьшение QTc наблюдалось уже на 2-е сутки заболевания и составило 32,8 мс (р<0,0001). Значения выраженности снижения QTc на протяжении всего периода наблюдения были достоверно в пользу назначения L-карнитина и к 12-14-му дню составили в группе L-карнитина 9,3±7,3%, в группе плацебо — 2,0±8,2% (р=0,002) [30].
Лечение L-карнитином приводило к достоверному (р<0,0001) уменьшению конечного систолического (КСО) и конечного диастолического объемов (КДО), тем самым способствуя повышению сократительной функции миокарда ЛЖ сердца, в то время как введение плацебо приводило к менее выраженному уменьшению КСО, но к значительному увеличению КДО (р=0,0004). Наиболее выраженные изменения ФВ отмечены у пациентов с исходно сниженной ФВ, причем достоверное увеличение отмечено только у пациентов, получавших L-карнитин (р=0,00002). Эти данные позволяют полагать, что введение L-карнитина уменьшает степень раннего постинфарктного ремоделирования ЛЖ [31].
Сердечная недостаточность
Известно, что L-карнитин является прямым антиоксидантом, удаляющим образовавшиеся радикалы кислорода, а также подавляет их генерацию ферментами в цитоплазме клеток и непосредственно в дыхательной цепи митохондрий, поскольку L-карнитин образует комплексы с ионами Fe2+ и Cu2+ в их активных центрах. Снижение уровня активных форм кислорода (АФК) под влиянием L-карнитина тормозит образование пероксинитрита — цитотоксического агента, необратимо взаимодействующего с различными белковыми мишенями, который образуется при действии супероксид-анионов на радикалы NO. Таким образом, L-карнитин увеличивает биодоступность NO — универсального регулятора эндотелиальных клеток как периферических сосудов, так и коронарных артерий, тем самым снижая нагрузку на сердце при ИМ [32].
Недавно показано, что L-карнитин в фармакологических концентрациях обладает антиокислительной активностью и способен дозозависимым образом снижать системный окислительный стресс у пациентов с постинфарктным кардиосклерозом. Добавление L-карнитина (Элькар раствор для внутривенного и внутримышечного введения 100 мг/мл) в образцы крови этих пациентов значимо снижало спонтанное и индуцированное химическим агентом образование радикалов кислорода предактивированными фагоцитами крови [33].
Добавление L-карнитина к стандартной комплексной терапии сердечной недостаточности изучено в нескольких клинических исследованиях. Рандомизированное плацебо-контролируемое исследование у 70 пациентов с сердечной недостаточностью показало, что трехлетняя выживаемость была значительно выше в группе, получавшей L-карнитин перорально в дозе 2 г/сут, по сравнению с группой, получавшей плацебо [34]. Для оценки эффективности применения L-карнитина при лечении пациентов с ХСН проведен мета-анализ рандомизированных контролируемых исследований (РКИ) [35]. В исследование включены результаты 17 РКИ с участием 1625 пациентов с ХСН. Применение L-карнитина в лечении ХСН связано со значительным улучшением общей эффективности [отношение шансов (ОIII)=3,47; р<0,01], увеличением ФВ ЛЖ [взвешенная разность средних (ВРС): 4,14%; _р=0,01], ударного объема (ВРС: 8,21 мл; p=0,01), сердечного выброса (ВРС: 0,88 л/мин; _р<0,01) и соотношения E/A (ВРС: 0,23; р<0,01). Терапия L-карнитином значительно снизила уровень мозгового натрийуретического пептида (BNP) в крови (ВРС: -124,60 пг/мл; _р=0,01), уровень N-терминального мозгового натрийуретического пропептида (NT-proBNP; ВРС: -510,36 пг/мл; _р<0,01), конечно-систолического размера ЛЖ (ВРС: -4,06 мм; _р<0,01), конечно-диастолического размера ЛЖ (ВРС: -4,79 мм; р<0,01) и КСО ЛЖ [ВРС: -20,16 мл; 95% доверительный интервал (ДИ) от -35,65 до -4,67; р<0,01]. Однако не выявлено межгрупповых различий по таким показателям, как смертность от любых причин, тест 6-минутной ходьбы и количество нежелательных явлений. Авторы заключили, что терапия L-карнитином у пациентов с ХСН эффективна для улучшения клинических симптомов и функций сердца, снижает уровень BNP и NT-proBNP и хорошо переносится пациентами.
Стенокардия
Рандомизированное плацебо-контролируемое исследование у 200 пациентов со стенокардией напряжения показало, что назначение дополнительно к стандартной комплексной терапии 2 г/сут L-карнитина в течение 6 мес значительно снижало экстрасистолию в состоянии покоя, а также повышало переносимость физической нагрузки [36]. Кроме того, рандомизированное плацебо-контролируемое перекрестное исследование у 44 мужчин со стенокардией напряжения показало, что пероральный прием 2 г/сут L-кар-нитина в течение 4 нед значительно повышал толерантность к физической нагрузке, регистрируемую путем изучения депрессии сегмента ST во время тренировки по сравнению с группой плацебо [37]. В более раннем рандомизированном плацебо-контролируемом исследовании у 47 мужчин и женщин со стабильной стенокардией напряжения добавление к стандартной терапии 2 г/сут L-карни-тина перорально в течение 3 мес увеличило продолжительность дозированной физической нагрузки и уменьшило время, необходимое для восстановления сегмента ST после физической нагрузки, по сравнению с плацебо [38]. Таким образом, в ряде исследований установлено, что добавление перорального L-карнитина в комплексную терапию пациентов со стабильной стенокардией напряжения улучшает переносимость физической нагрузки и снижает электрокардиографические признаки ишемии во время физических нагрузок. Выполненный мета-анализ 13 исследований (3629 больных) показал, что L-карнитин у больных с ИМ снижает шанс смерти от любых причин на 27% (р=0,05), риск желудочковых нарушений ритма на 65% (р<0,0001) и на 40% — риск приступов стенокардии (р<0,00001) [39].
Эти многообещающие результаты еще раз подтверждают необходимость проведения дальнейших масштабных исследований для определения клинической значимости применения L-карнитина у данной группы пациентов.
Хроническая почечная недостаточность /гемодиализ
При гемодиализе дефицит L-карнитина возникает вследствие удаления данного вещества и его предшественников из системы кровообращения. Также нарушение реабсорбции L-карнитина почками может способствовать дефициту L-карнитина у пациентов с терминальной стадией заболевания почек, находящихся на гемодиализе. Управление по контролю за продуктами и лекарствами США (FDA) одобрило использование L-карнитина у пациентов с гемодиализом для профилактики и лечения дефицита L-карни-тина [40]. Уменьшение запасов L-карнитина в организме может привести к развитию ряда патологических состояний, наблюдаемых у пациентов, находящихся на диализе, включая мышечную слабость и усталость, аномалии липидного спектра плазмы и рефрактерную анемию. В систематическом обзоре, содержащем анализ результатов 18 рандомизированных исследований с участием 482 пациентов, находящихся на диализе, продемонстрировано, что лечение L-карнитином повышает уровень гемоглобина в исследованиях, проведенных до назначения рекомбинантного эритропоэтина (ЭПО), обычно применяемого для лечения анемии у пациентов с диализом. Также показано, что регулярное применение L-карнитина уменьшает необходимую дозу ЭПО и снижает резистентность к ЭПО [41]. Более того, в двух последних исследованиях использована терапия L-карнитином на гемодиализе с уменьшенной госпитализацией [42, 43]. Национальный фонд почек (NKF) не рекомендует рутинное введение L-карнитина всем пациентам, находящимся на диализе [44]. Однако NKF и другие консенсусные группы предлагают введение L-кар-нитина пациентам на гемодиализе, которые не отвечают на стандартную терапию и/или имеют определенные симптомы, такие как мышечные судороги или гипотония во время диализа, сильную усталость, слабость скелетных мышц или миопатию, кардиомиопатию и анемию, требующую больших доз ЭПО [44]. Для пациентов, находящимся на гемодиализе, рекомендовано внутривенное введение L-карни-тина в дозе 20 мг/кг массы тела в конце сеанса диализа [45]. Пероральный прием L-карнитина не рекомендуется использовать у пациентов на гемодиализе из-за возможного накопления потенциально токсичных метаболитов [46].
Дисциркуляторная энцефалопатия. Ишемический инсульт (ИИ)
Поскольку L-карнитин обладает мощными антиоксидантными и нейропротективными свойствами, доказанными по результатам исследований in vitro, в экспериментах на животных, его активно изучают в неврологической практике у пациентов со снижением когнитивных функций и при терапии инсультов. Известна и доказана токсическая роль свободных жирных кислот при острой и хронической ишемии, а также выявлена прямая корреляция между концентрацией свободных жирных кислот в спинномозговой жидкости и вероятностью ИИ, особенно при кардиоэмболическом подтипе [47].
В.И. Головкин и соавт. провели исследование внутривенного введения отечественного препарата L-карнитина (Элькар раствор для внутривенного и внутримышечного введения 100 мг/мл) у мужчин (основная группа) старческого возраста, страдающих дисциркуляторной энцефалопатией (ДЭ) II и III степени с кардиоцеребральным синдромом, по сравнению с контрольной группой, в которой принимали стандартную терапию [48].
В группе исследования левокарнитин применялся в дозе 1 г/сут однократно в течение 10 дней в комплексе с основной этиопатогенетической терапией. Проведено как всестороннее клиническое и инструментальное [мультиспиральная компьютерная томография (МСКТ), ультразвуковая диагностика (УЗДГ), электрокардиография (ЭКГ)] исследование, так и применены специальные опросники для диагностики когнитивных нарушений и 6-минутный тест ходьбы для оценки толерантности к физической нагрузке. Через 10 дней терапии увеличилась дистанция ходьбы, статистически значимо повысились когнитивные функции у пациентов по данным неврологических тестов (таблица Шульте, тест Мини-Ког, рисование часов). Ученые рекомендуют прием L-карнитина за счет его кардиотропных, метаболических и нейропротекторных свойств к широкому применению у больных с ДЭ и кардиоцеребральным синдромом [48].
За счет своих антиоксидантных свойств предполагается, что левокарнитин препятствует развитию апоптоза и предотвращает дальнейшее повреждение нервной ткани в результате ИИ; снижает уровень лактата в ишемическом очаге возможно за счет переключения энергетического ресурса с анаэробного гликолиза на цикл Кребса [49]. Применение препарата Элькар раствор для внутривенного и внутримышечного введения 100 мг/мл исследовано у пациентов в остром периоде ИИ, находившихся на максимально унифицированной терапии в соответствии с рекомендациями Европейской организации по проблемам инсульта. В двух группах вмешательства Элькар вводился внутривенно 2 раза в сутки в дозах 500 и 1500 мг в течение 10 дней. Затем в течение 10 дней больные принимали препарат Элькар 20% раствор для приема внутрь перорально по 1 чайной ложке 2 раза в сутки. На начало исследования группы вмешательства и группа контроля статистически не отличались по клиническим характеристикам пациентов. В ходе исследования между группами на терапии препаратом Элькар и группой контроля выявлены достоверные различия в выраженности регресса неврологического дефекта по шкале NIHSS (шкала оценки тяжести инсульта Национального института здоровья США), в то время как у пациентов группы контроля разница по шкале NIHSS на 1-е и 21-е сутки наблюдения была недостоверна. У пациентов с кардиоэмболическим патогенетическим вариантом инсульта, получавших Элькар, тяжесть заболевания уменьшалась достоверно в большей степени, чем у пациентов с атеротромботическим вариантом. В группе контроля таких различий не выявлено. При мониторинге функционального восстановления пациентов к 21-м суткам наблюдалась статистически значимая тенденция к увеличению индекса Бартела (индекс повседневной активности) в группах, получавших Элькар, по сравнению с группой контроля. Между группами с различным режимом дозирования препарата Элькар достоверных различий в динамике тяжести инсульта и каких-либо различий по значению индекса Бартела не выявлено [50]. В исследовании безопасности и эффективности применения L-карнитина у больных в раннем восстановительном периоде ИИ использовали внутримышечное введение препарата Элькар раствор для внутривенного и внутримышечного введения 100 мг/мл по 500 мг 2 раза в сутки в течение 7 дней с повторным курсом через 10 дней в комплексной терапии II этапа постинсультной реабилитации. Эффективность лечения оценивали на 1-, 7-10-и 28-30-й дни терапии по шкалам: NIHSS, MFI-20, HADS и ВАШ (визуальная аналоговая шкала) и по индексу Бартела. Применение L-карнитина у больных с ИИ заметно повысило их удовлетворенность своим состоянием. На фоне терапии значимо снизилась частота жалоб как церебрального, так и общесоматического характера, что сочеталось с достоверным уменьшением тяжести неврологического дефицита по шкале NIHSS. Кроме того, значимо снизился уровень общей астении и психоэмоциональных нарушений, что привело к уменьшению доли больных, зависимых от посторонней помощи (индекс Бартела) [51].
Результаты проведенных клинических исследований показывают перспективность применения L-карнитина в клинике внутренних болезней. Назначение L-карнитина проводится в качестве дополнения к основной патогенетической терапии. При этом вопрос межлекарственных взаимодействий остается не изученным.
Безопасность применения L-карнитина в составе комплексной фармакотерапии с точки зрения возможного взаимодействия с ЛС на уровне CYPР450 3А4
Для прогнозирования межлекарственных взаимодействий на уровне метаболизма, скрининга возможных субстратов, индукторов, ингибиторов изоферментов цитохрома, нами использована экспериментальная электрохимическая методика in electrode. Она характеризуется воспроизводимостью измерений, которые могут использоваться для исследования субстрат-ингибиторного потенциала CYP 3A4, поскольку не требует реконструирования электрон-транспортной системы; донором электронов для восстановления цитохрома Р450 и начала каталитической реакции служит электрод [52].
Ранее нами при помощи электроанализа исследовано влияние на электрохимическое восстановление цитохрома Р450 3А4 витаминов-антиоксидантов (А, С, Е) и витаминоподобных веществ таурина; комплекса Кудесан, содержащего коэнзим Q10 и витамин Е, а также лекарственных препаратов этоксидола, мексидола, цитохрома С [53]. Мы выявили модулирующее действие данных групп препаратов на каталитическую активность цитохрома Р450 3А4, в связи с этим хотелось бы отметить возможное влияние данных лекарственных соединений-антиоксидантов на метаболизм одновременно назначаемых препаратов при их применении в составе комплексной фармакотерапии.
При изучении влияния L-карнитина на каталитическую активность цитохрома Р450 3А4 электрохимическими методами с целью прогнозирования возможных взаимодействий с лекарственными препаратами на уровне метаболизма показано, что этот препарат не влияет на каталитический ток, регистрируемый при взаимодействии маркерного субстрата с ферментом, т.е. не оказывает модулирующего действия на цитохром Р450 3А4. Таким образом, это снижает вероятность возникновения межлекарственного взаимодействия на уровне метаболизма лекарственных препаратов, метаболизирующихся Р450 3А4, при использовании L-карнитина в составе комплексной фармакотерапии [52].
Заключение
Результаты многочисленных экспериментальных и клинических исследований показывают перспективность применения L-карнитина в клинике внутренних болезней. Назначение L-карнитина проводится в составе стандартной комплексной фармакотерапии. Проведенные нами экспериментальные исследования показали отсутствие влияния L-карнитина на активность системы CYP 3А4 Р450, которая метаболизирует большинство лекарственных препаратов, что говорит о хорошем профиле безопасности данного препарата с точки зрения межлекарственных взаимодействий. Данную информацию необходимо учитывать врачам различных специальностей при выборе оптимального препарата с антиоксидантными и антигипоксантными свойствами при назначении его в комплексной терапии у коморбидных пациентов.
Авторы заявляют об отсутствии конфликта интересов.
Сведения об авторах:
Ших Евгения Валерьевна — д.м.н., проф., зав. каф. клинической фармакологии и пропедевтики внутренних болезней;
Махова Анна Александровна — к.м.н., доцент каф. клинической фармакологии и пропедевтики внутренних болезней;
ЛИТЕРАТУРА/REFERENCES
1. Кукес В.Г., Сычев Д.А. Персонализированная медицина: новые возможности для повышения бeзoпacнocти фapмaкoтepaпии. Ремедиум. 2010;(10):38-40 [Kukes VG, Sychev DA. Personalized medicine: new possibilities to improve the safety of pharmacotherapy. Chem. 2010;(10):38-40 (In Russ.)].
2. Мaxoвa A.A. Влияние нaгpyзoчныx доз витаминов группы B на фapмaкoкинeтикy и фapмaкoдинaмикy НПВС: дис. … канд. мед. нayк. М., 2010; 107 с. [Makhova AA. Influence of therapeutic doses of vitamins B on the pharmacokinetics and pharmacodynamics of the NSAIDs: diss. … Phd. M., 2010; 107 p. (In Russ.)].
3. Rebouche CJ. Carnitine. In: Shils ME, Shike M, Ross AC, Caballero B, Cousins RJ, eds. Modern Nutrition in Health and Disease. 10th ed. Philadelphia: Lippincott, Williams & Wilkins; 2006:537-544.
4. Rebouche CJ. Kinetics, pharmacokinetics, and regulation of L-carnitine and acetyl-L-carnitine metabolism. Ann NY Acad Sci. 2004;1033:30-41.
5. De Grandis D, Minardi C. Acetyl-L-carnitine (levacecarnine) in the treatment of diabetic neuropathy. A long-term, randomised, double-blind, placebo-controlled study. Drugs RD. 2002;3(4):223-31.
6. Gross CJ, Henderson LM, Savaiano DA. Uptake of L-carnitine, D-carnitine and acetyl-L-carnitine by isolated guinea-pig enterocytes. Biochim Biophys Acta. 1986;886(3):425-33.
7. Foster DW. The role of the carnitine system in human metabolism. Ann NY Acad Sci. 2004;1033:1-16.
8. Асташкин Е.И., Глезер М.Г. Роль L-карнитина в энергетическом обмене кардиомиоцитов и лечении заболеваний сердечно-сосудистой системы. Кардиология и сердечно-сосудистая хирургия. 2012;6(2):58-65 [Astashkin EI, Glezer MG. Effed of L-carnitine on oxydative stress at cardiovascular diseases. Cardiology and Cardiovascular Surgery. 2012;6(2):58-65 (In Russ.)].
9. Lombard KA, Olson AL, Nelson SE, Rebouche CJ. Carnitine status of lactoovovegetarians and strict vegetarian adults and children. Am J Clin Nutr. 1989;50(2):301-6.
10. Nezu J, Tamai I, Oku A, et al. Primary systemic carnitine deficiency is caused by mutations in a gene encoding sodium ion-dependent carnitine transporter. Nat Genet. 1999;21(1):91-4.
11. Stanley CA. Carnitine deficiency disorders in children Ann NY Acad Sci. 2004;1033:42-51.
12. Seim H, Eichler K, Kleber H. L(-)-Carnitine and its precursor, gamma-butyrobetaine. In: Kramer K, Hoppe P, Packer L, eds. Nutraceuticals in Health and Disease Prevention. New York: Marcel Dekker, Inc; 2001:217-256.
13. Pons R, De Vivo DC. Primary and secondary carnitine deficiency syndromes. J Child Neurol. 1995;10(Suppl 2):8-24.
14. Calvani M, Benatti P, Mancinelli A, et al. Carnitine replacement in end-stage renal disease and hemodialysis. Ann NY Acad Sci. 2004;1033:52-66.
15. Food and Nutrition Board, Institute of Medicine. Vitamin C. Dietary Reference Intakes for Vitamin C, Vitamin E, Selenium, and Carotenoids. Washington D.C.: National Academy Press; 2000:95-185.
16. Costell M, O’Connor JE, Grisolia S. Age-dependent decrease of carnitine content in muscle of mice and humans. Biochem Biophys Res Commun. 1989;161(3):1135-43.
17. Hagen TM, Ingersoll RT, Wehr CM, et al. Acetyl-L-carnitine fed to old rats partially restores mitochondrial function and ambulatory activity. Proc Natl Acad Sci USA. 1998;95(16):9562-6.
18. Pesce V, Fracasso F, Cassano P, Lezza AM, Cantatore P, Gadaleta MN. Acetyl-L-carni-tine supplementation to old rats partially reverts the age-related mitochondrial decay of soleus muscle by adivating peroxisome proliferator-activated receptor gamma coactiva-tor-1alpha-dependent mitochondrial biogenesis. Rejuvenation Res. 2010;13(2-3):148-51.
19. Gomez LA, Heath SH, Hagen TM. Acetyl-l-camitine supplementation reverses the age-related decline in camitine palmitoyltransferase 1 (CPT1) activity in interfibrillar mitochon-dria without changing the l-carnitine content in the rat heart. Mech Ageing Dev. 2012;133(2-3):99-106.
20. Hagen TM, Liu J, Lykkesfeldt J, et al. Feeding acetyl-L-carnitine and lipoic acid to old rats significantly improves metabolc function while decreasing oxidative stress. Proc Natl Acad Sci USA. 2002;99(4):1870-5.
21. Liu J, Head E, Gharib AM, et al. Memory loss in old rats is associated with brain mito-chondrial decay and RNA/DNA oxidation: partial reversal by feeding acetyl-L-carni-tine and/or R-alpha -lipoic acid. Proc Natl Acad Sci USA. 2002;99(4):2356-61.
22. Davini P, Bigalli A, Lamanna F, Boem A. Controlled study on L-carnitine therapeutic efficacy in post-infarction. Drugs Exp Clin Res. 1992;18(8):355-65.
23. Xue YZ, Wang LX, Liu HZ, Qi XW, Wang XH, Ren HZ. L-carnitine as an adjunct therapy to percutaneous coronary intervention for non-ST elevation myocardial infarction. Cardiovasc Drugs Ther. 2007;21(6):445-8.
24. Iyer R, Gupta A, Khan A, Hiremath S, Lokhandwala Y. Does left ventricular function improve with L-carnitine after acute myосardial infarction? J Postgrad Med. 1999;45(2): 38-41.
25. Colonna P, Iliceto S. Myocardial infarction and left ventricular remodeling: results of the CEDIM trial. Carnitine Ecocardiografia Digitalizzata Infarto Miocardico. Am Heart J. 2000;139(2 Pt 3):124-30.
26. Iliceto S, Scrutinio D, Bruzzi P, et al. Effects of L-carnitine administration on left ventricular remodeling after acute anterior myocardial infarction: the L-Carnitine Ecocar-diografia Digitalizzata Infarto Miocardico (CEDIM) Trial. J Am Coll Cardiol. 1995;26(2):380-7.
27. Tarantini G, Scrutinio D, Bruzzi P, Boni L, Rizzon P, Iliceto S. Metabolic treatment with L-Carnitine in acute anterior ST segment elevation myocardial infarction. A randomized controlled trial. Cardiology. 2006;106(4):215-23.
28. Семиголовский Н.Ю., Верцинский Е.К., Азанов Б.А., Иванова Е.В. Положительные инотропные свойства левокарнитина при синдроме малого выброса у больных острым инфарктом миокарда. Кардиология и cердечно-сосудистая хирургия. 2013;(3):43-6 [Semigolovskiy NYu, Vertinskiy EK, Azanov BA, Ivanova EV. Positive inotropic properties of levocarnitine in low ejection syndrome among patients wiht acute myocardial infarction. Cardiology and Cardiovascular Surgery. 2013;(3):43-6 (In Russ.)].
29. Глезер М.Г., Киселева А.Е., Асташкин Е.И. Влияние L-карнитина на дисперсию интервала QT у пациентов с острым коронарным синдромом. Кардиология. 2015;55(3):4-9 [Gleser MG, Kiseleva AE, Astashkin EI. The effect of L-carnitine on the dispersion of the QT interval in patients with acute coronary syndrome. Cardiology. 2015;55(3):4-9 (In Russ.)].
30. Глезер М.Г., Киселева А.Е., Асташкин Е.И Влияние L-карнитина на ЧCC и QТ у пациентов с острым коронарным синдромом. Сердце. 2015;14(2/82):78-84 [Glezer MG, Kiseleva AE, Astashkin EI. Effect of L-carnitine on CV and QT in patients with acute coronary syndrome. The heart. 2015;14(2/82):78-84 (In Russ.)].
31. Глезер М.Г., Киселева А.Е., Прокофьева Е.Б., Асташкин Е.И. Влияние L-карнити-на на эхокардиографические показатели у пациентов с острым коронарным синдромом. Журнал Сердечная Недостаточность. 2015;16(4):234-40 [Glezer MG, Kiseleva AE, Prokofieva EB, Astashkin EI. Effect of L-carnitine on echocardiographic parameters in patients with acute coronary syndrome. Heart Failure J. 2015;16(4):234-40 (In Russ.)].
32. Асташкин Е.И., Глезер М.Г. Влияние L-карнитина на оксидативный стресс при сердечно-сосудистых заболеваниях. Медицинский Совет. 2016;10:94-100 [Astashkin EI, Glezer MG. The effect of L-carnitine on oxidative stress in cardiovascular diseases. Medical advice. 2016;10:94-100 (In Russ.)].
33. Асташкин Е.И., Глезер М.Г., Орехова Н.С., Грачев С.В., Киселева А.Е. Влияние L-карнитина на образование радикалов кислорода фагоцитами крови пациентов с постинфарктным кардиосклерозом. Кардиоваскулярная терапия и профилактика. 2016;15(5):28-32 [Astashkin EI, Glezer MG, Orekhova NS, Grachev SV, Kiseleva AE. Influence of L-carnitine on reactive oxygen species produdion by blood phago-суtes in postinfarction cardiosclerosis patients. Cardiovascular therapy and prevention. 2016;15(5):28-32 (In Russ.)].
34. Rizos I. Three year survival of patients with heart failure caused by dilated cardiomyopathy and L-carnitine administration. Am Heart J. 2000;139(2 Pt 3):120-3.
35. Xiaolong Song, Huiyan Qu, Zongguo Yang, Jingfeng Rong, Wan Cai and Hua Zhou. Efficacy and Safety of L-Carnitine Treatment for Chronic Heart Failure: A MetaAnalysis of Randomized Controlled Trials. BioMed Research International. 2017;(2017). Article ID 6274854, 11 p. doi:10.1155/2017/6274854
36. Cacciatore L, Cerio R, Ciarimboli M, et al. The therapeutic effect of L-carnitine in patients with exercise-induced stable angina: a controlled study. Drugs Exp Clin Res. 1991;17(4):225-35.
37. Cherchi A, Lai C, Angelino F, et al. Effects of L-carnitine on exercise tolerance in сhronic stable angina: a multicenter, double-blind, randomized, placebo controlled crossover study. Int J Clin Pharmacol Ther Toxicol. 1985;23(10):569-72.
38. Iyer RN, Khan AA, Gupta A, Vajifdar BU, Lokhandwala YY. L-carnitine moderately improves the exercise tolerance in сhronic stable angina. J Assoc Physicians India. 2000;48(11):1050-2.
39. DiNicolantonio JJ, Lavie CJ, Fares H, et al. L-carnitine in the secondary prevention of cardiovascular disease: systematic review and meta-analysis. Mayo Clin Proc. 2013;88(6):544-51.
40. Guarnieri G, Situlin R, Biolo G. Carnitine metabolism in uremia. Am J Kidney Dis. 2001;38(4 Suppl 1):63-7.
41. Hurot JM, Cucherat M, Haugh M, Fouque D. Effects of L-carnitine supplementation in maintenance hemodialysis patients: a systematic review. J Am Soc Nephrol. 2002;13(3):708-14.
42. Kazmi WH, Obrador GT, Sternberg M, et al. Carnitine therapy is associated with decreased hospital utilization among hemodialysis patients. Am J Nephrol. 2005;25(2):106-15.
43. Weinhandl ED, Rao M, Gilbertson DT, Collins AJ, Pereira BJ. Protective effect of intravenous levocarnitine on subsequent-month hospitalization among prevalent hemodialysis patients, 1998 to 2003. Am J Kidney Dis. 2007;50(5):803-12.
44. Clinical practice guidelines for nutrition in сhronic renal failure. K/DOQI, National Kidney Foundation. Am J Kidney Diseases. 2000;35(6 Suppl 2):1-140.
45. Eknoyan G, Latos DL, Lindberg J. Practice recommendations for the use of L-carnitine in dialysis-related carnitine disorder. National Kidney Foundation Carnitine Consensus Conference. Am J Kidney Dis. 2003;41(4):868-76.
46. Schreiber B. Safety of oral carnitine in dialysis patients. Semin Dial. 2002;15(1):7
47. Wei X-J, Han M, Wei G-C, Duan C-H. Prognostic value of cerebrospinal fluid free fatty add levels in patients with acute ischemic stroke. Frontiers in Human Neuroscience. 2015;9:402. doi: 10.3389/fnhum.2015.00402.
48. Головкин В., Зуев А., Привалова М. и др. Когнитивные нарушения и кардиореспираторная дисфункция при дисциркуляторной энцефалопатии с кардиоцеребральным синдромом. Врач. 2018;29(4):51-3 [Golovkin V, Zuev A, Privalova M, et al. Cognitive impairment and cardiorespiratory dysfunction in dyscirculatory encephalopathy with cardiocerebral syndrome. Vrach (The Doctor). 2018;29(4):51-3 (In Russ.)]. doi: 10.29296/25877305-2018-04-09
49. Гусев Е.И., Кузин В.М., Колесникова Т.Н. и др. Карнитин — ведущий фактор регенерации нервной ткани. Медицинский информационный вестник. 1999 (февраль):11-23 [Gusev E., Kuzin VM, Kolesnikova TN. Carnitine is a leading factor in the regeneration of nervous tissue. Medical Information Bulletin. 1999 (February):11-23 (In Russ.)].
50. Бодыхов М.К., Стаховская Л.В., Салимов К.А., Сун Чер И. Оценка безопасности и эффективности препарата «Элькар» (левокарнитин) у пациентов в остром периоде ишемического инсульта в каротидной системе. РМЖ — Неврология. 2011;11:3-6 [Bodikhov MK, Stakhovskaya LV, Salimov KA, Sun Cher I. Evaluation of the safety and efficacy of the drug Elkar (l-carnitine) in patients with acute ischemic stroke in the carotid system. Breast Cancer — Neurology. 2011;11:3-6 (In Russ.)].
51. Чичановская Л.В., Бахарева О.Н., Сорокина К.Б. Исследование безопасности и эффективности L-карнитина у больных в раннем восстановительном периоде ишемического инсульта. Журнал неврологии и психиатрии им С.С. Корсакова. 2017;12(Вып. 2):65-9 [Chichanovskaya LV, Bakhareva ON, Sorokina KB. The study of the safety and efficacy of L-carnitine in patients in the early recovery period of is-chemic stroke. J Neurology and Psychiatry named after SS Korsakov. 2017;12(Vol. 2):65-9 (In Russ.)].
52. Makhova AA, Shich EV, Kukes VG, Sizova OS, Ramenskaya GV, Shumyantseva VV, Bulko TV, Archakov AI, Usanov SA. Electroanalysis of cytochrome P450 3A4 catalytik properties with nanostructured electrodes: the influence of vitamin B group on diclofenac metabolism. BioNanoScience. 2011;1(1-2):46-52.
53. Махова А.А., Шумянцева В.В., Ших Е.В., Булко Т.В., Супрун Е.В., Кузиков А.В., Кукес В.Г., Арчаков А.И. Регуляция активности ферментов метаболизма лекарственных препаратов — цитохромов Р450 3А4 и 2С9 — биологически активными соединениями. Молекулярная медицина. 2013;(5):49-53 [Makhova AA, Shumyantseva VV, Shikh EV, Bulko TV, Suprun EV, Kuzikov AV, Kukes VG, Ar-chakov AI. Regulation of the activity of drug metabolism enzymes — cytochromes P450 3A4 and 2C9 — biologically active compounds. Molecular medicine. 2013;(5):49-53 (In Russ.)].
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
L-карнитин: что это такое
L-карнитин
(левокарнитин) — это органическое соединение, которое участвует в обмене веществ и помогает переносить жирные кислоты в митохондрии клеток для последующего окисления.
Карнитин содержится в продуктах питания в виде различных соединений:
- L-карнитин. Это наиболее распространенная форма карнитина, которая содержится в продуктах животного происхождения, таких как мясо, рыба, птица, молоко и яйца.
- Ацилкарнитин. Форма карнитина, которая содержится в продуктах растительного происхождения, таких как зерновые, бобовые и овощи.
- Карнитиновые эфиры. Форма карнитина, которая содержится в некоторых продуктах животного происхождения, таких как мясо и рыба.
- Гидроксикарнитин. Форма карнитина, которая содержится в некоторых продуктах растительного происхождения, таких как бобовые и овощи.
Справочно
Кроме продуктов животного и растительного происхождения, левокарнитин также может содержаться в витаминно-минеральных добавках, энергетических напитках и спортивных добавках.
Формы карнитина могут различаться по своей биодоступности и эффективности. L-карнитин является наиболее изученной и эффективной формой карнитина.
Приставка «L» обозначает, что молекула имеет определенную пространственную конфигурацию, которая является биологически активной формой карнитина. В организме человека преобладает именно эта форма.
Марият Мухина
д. м. н., диетолог
— Левокарнитин в организме синтезируется из аминокислот лизина и метионина при участии витаминов С, В6, ниацина и железа. В противном случае, при нехватке этих веществ, он не синтезируется. Также L-карнитин поступает к нам с пищей, преимущественно с мясом (баранина, говядина, свинина, курица). При интенсивных физических нагрузках, при тренировке, стрессе или заболеваниях может потребоваться дополнительный прием этого вещества в виде добавок. Но учитывайте, что препарат дает эффект синергии, когда 1 + 1 = 5, только в комплексной терапии!
Обычно за сутки у взрослого человека синтезируется около 20 мг карнитина (10% от необходимого), остальное количество (150-180 мг) должно поступать с пищей.
L-карнитин накапливается преимущественно в скелетных мышцах и миокарде. При его недостатке могут развиваться различные заболевания, связанные с нарушением обмена веществ.
Для чего нужен левокарнитин
L-карнитин участвует в обмене веществ. В энергетическом и липидном обмене он переносит длинноцепочечные жирные кислоты через внутреннюю мембрану митохондрий для последующего их окисления. В процессе окисления жирные кислоты расщепляются, высвобождается энергия.
— Энергия, полученная при участии L-карнитина, используется организмом для различных целей, таких как поддержание жизнедеятельности клеток и тканей, сокращение мышц и т. д., — добавляет Марият Мухина.
Функции левокарнитина в организме:
- транспортирует жирные кислоты в митохондрии клеток, где происходит их окисление с последующим выделением энергии;
- влияет на белковый и жировой обмен;
- поддерживает работу сердечно-сосудистой системы;
- стимулирует регенерацию тканей;
- повышает общую физическую выносливость и работоспособность организма;
- способствует снижению избыточной массы тела.
Польза для организма
О пользе L-карнитина буквально ходят легенды. Но все же авторы исследований схожи в одном: левокарнитин эффективен не в одиночестве, а в составе комплексной терапии.
Разберемся, когда показано дополнительно принимать левокарнитин. Его прием назначают:
- Для реабилитации после операций или травм, в том числе для ускорения регенерации тканей.
- При сердечно-сосудистых заболеваниях, сопровождающихся недостатком карнитина или его повышенной потерей (миопатии, кардиомиопатии, митохондриальные заболевания).
- При хронической почечной недостаточности для пациентов, находящихся на гемодиализе.
- При болезнях, сопровождающихся потерей мышечной массы (кахексия, саркопения, маразм).
- При болезни Альцгеймера.
- При бесплодии у мужчин.
- При повышенном уровне холестерина в крови.
Перед приемом левокарнитина необходима консультация с врачом, поскольку препарат может взаимодействовать с другими препаратами и иметь противопоказания.
— При ожирении левокарнитин может помочь уменьшить массу тела, улучшив функцию метаболизма, но речь здесь идет не о десятках килограммов, — предостерегает доктор Мухина. — Это всего лишь 1–2 кг, не более. И похудеть, уменьшив жировую прослойку только за счет употребления L-карнитина, не удастся.
Также рекомендуют прием левокарнитина при интенсивных и длительных физических и психоэмоциональных нагрузках, чтобы повысить работоспособность, выносливость, снизить утомляемость. Кроме того, его советуют включать в рацион спортсменов, при интенсивных спортивных тренировках, для улучшения силы, скорости, координации и для увеличения мышечной массы.
L-карнитин оптимизирует физическую форму, ускоряя восстановление после интенсивных нагрузок и смягчая мышечную усталость за счет снижения уровня аммиака и лактата
.
Но надо понимать, что эффект от приема на тренировках не такой значительный, как многие думают. По сообщению Роспотребнадзора, метаанализ 2021 года показал, что при тренировках с очень высокой интенсивностью и высоким потреблением кислорода в течение шести месяцев ежедневного приема добавок наблюдается лишь небольшое уменьшение усталости и утомляемости.
В мире науки изучение L-карнитина все еще продолжается. Так, в статье «Влияние биологически активных добавок на основе L-карнитина на свободнорадикальные процессы в модельных системах»
приводятся данные о применении L-карнитина при заболеваниях почек, эректильной дисфункции и бесплодии у мужчин. Обсуждается роль левокарнитина в профилактике и лечении хронической усталости и других состояний, связанных с нарушением обмена веществ.
В статье упоминаются исследования, которые показали эффективность L-карнитина в урологии, в лечении заболеваний почек, но при дополнении к основной терапии. Также L-карнитин может оказывать благотворное влияние при эректильной дисфункции. Это связано с тем, что L-карнитин влияет на улучшение кровообращения и обменные процессы в тканях полового члена.
В статье «Левокарнитин в лечении полиморбидных пациентов», опубликованной на сайте CyberLeninka, приведены результаты ретроспективного анализа данных о пациентах с полиморбидностью, которые получали левокарнитин в качестве части комплексного лечения.
Полиморбидность — это наличие у пациента нескольких хронических заболеваний одновременно.
Результаты исследования показали, что левокарнитин оказывал положительное воздействие на здоровье полиморбидных пациентов:
- Улучшение показателей сердечно-сосудистой системы.
- Снижение уровня холестерина и триглицеридов в крови.
- Улучшение функции почек.
- Снижение частоты и тяжести приступов стенокардии.
L-карнитин — любимец педиатров в качестве кардиопротектора. Новейшие научные исследования подтверждают его эффективность в лечении детей с наследственными миопатиями, врожденными заболеваниями сердца и метаболическими нарушениями.
Например, при наследственных митохондриальных миопатиях и кардиомиопатиях L-карнитин улучшает функции сердца у детей
.
При врожденных заболеваниях сердца L-карнитин эффективен в улучшении параметров сердечной функции и снижении уровня серологических маркеров повреждения миокарда
.
При дилатационной кардиомиопатии L-карнитин улучшает сократительную функцию сердца и может значительно улучшить клиническое состояние и продолжительность жизни детей с этой патологией
.
L-карнитин также оказывает положительное влияние на кардиопротекцию у детей с метаболическими нарушениями, улучшая общий энергетический баланс сердечной мышцы, что важно для управления метаболическими кардиомиопатиями
.
Эти исследования подчеркивают важность дальнейшего изучения и применения L-карнитина в педиатрии как средства защиты и улучшения сердечной функции у детей с различными заболеваниями сердца и метаболическими нарушениями.
Проведено и опубликовано немало исследований о влиянии карнитина, например, на сердечно-сосудистую систему у пациентов с гипертонией; на мышечную силу и выносливость у спортсменов; на когнитивные функции у пациентов с болезнью Альцгеймера
; на функцию почек у пациентов с хронической почечной недостаточностью; на уровень холестерина у пациентов с гиперхолестеринемией.
Применение L-карнитина может оказывать антидиабетический эффект. Исследования показывают улучшение глюкозного метаболизма и увеличение чувствительности к инсулину при использовании левокарнитина, что делает его перспективным для применения при лечении диабета 2-го типа
.
Что касается когнитивных функций, L-карнитин способен защитить нейроны и улучшить когнитивные способности, поэтому его применение может быть эффективным в профилактике деменции и болезни Альцгеймера. Это связано со способностью L-карнитина снижать уровень окислительного стресса в головном мозге
.
Как мы видим, L-карнитин демонстрирует широкий спектр положительных эффектов на здоровье и метаболизм, открывая новые возможности для его применения в медицине и спорте.
Тем не менее нельзя утверждать, что левокарнитин является чудодейственным средством. Да, в большинстве случаев выводы исследований говорят о том, что L-карнитин может быть потенциально полезен, но в сочетании с комплексной терапией. И чаще всего для подтверждения этих результатов необходимы дополнительные исследования.
— Во многих обзорах L-карнитина, безусловно, может присутствовать конфликт интересов фармкомпаний, — отмечает доктор Мухина. — Для здорового человека достаточно сбалансированного питания, без дополнительного приема препаратов и лекарств с этим веществом. Однако дефициты тех или иных элементов есть сейчас буквально у каждого второго и прием L-карнитина может стать необходимостью. Стоит учесть, если у вас в организме нехватка витаминов С, В6, ниацина и железа, принимать L-карнитин следует только в комплексе с ними.
Сколько нужно карнитина организму?
Согласно Методическим рекомендациям MP 2.3.1.0253-21 «Нормы физиологических потребностей в энергии и пищевых веществах для различных групп населения Российской Федерации», адекватный уровень потребления L-карнитина:
для взрослых
- 300 мг/сутки;
для детей
- 0–12 месяцев — 10–15 мг/сутки;
- 1–3 лет — 30–50 мг/сутки;
- 4–6 лет — 60–90 мг/сутки;
- 7–18 лет — 100–300 мг/сутки.
Причины дефицита левокарнитина
Причинами возможного дефицита карнитина в организме могут быть:
- Нарушения его синтеза (ранний детский возраст, заболевания печени, почек и др.);
- Недостаточное поступление с пищей (строго вегетарианское питание, голодание, полное парентеральное питание);
- Повышенные расходы левокарнитина (физические и спортивные нагрузки, травмы, беременнось, гемодиализ и др.).
Может ли быть вреден левокарнитин?
Левокарнитин, содержащийся в продуктах питания, не представляет опасности для здоровья. Но препарат левокарнитина может быть назначен врачом для лечения различных заболеваний, а также в составе комплексной терапии при восстановлении после болезней и операций. Чаще всего левокарнитин назначают пациентам с генетическими дефектами или с хроническими заболеваниями почек.
Как и любое лекарственное средство, левокарнитин имеет противопоказания и побочные действия.
Побочные действия от приема препарата проявляются крайне редко. Они могут включать аллергические реакции, диспептические расстройства, легкое беспокойство. В частности, левокарнитин (levocarnitine) может иметь побочные эффекты, такие как гастралгия, диспепсия, диарея, тошнота и рвота, боли в животе, головные боли, усталость, миастенические расстройства, сыпь, дерматит.
Среди противопоказаний к приему левокарнитина — индивидуальная непереносимость компонентов препарата с левокарнитином, беременность и кормление грудью. Также препараты с левокарнитином не рекомендуется применять детям до 18 лет, за исключением случаев, когда лечение назначено врачом.
Следует помнить, что у пациентов с выраженным нарушением функции почек регулярный прием высоких доз левокарнитина может вызывать повышение концентрации потенциально токсичных метаболитов, триметиламина и триметиламина-N-оксида.
Взаимодействие с другими препаратами:
Левокарнитин может уменьшить эффективность противоэпилептических и гипогликемических препаратов.
Левокарнитин может увеличить риск кровотечений при приеме антикоагулянтов.
При одновременном приеме с анаболиками они усиливают эффект левокарнитина.
При одновременном применении глюкокортикостероидов ГКС способствуют накоплению левокарнитина в тканях (кроме печени).
В каких продуктах питания содержится левокарнитин? Где его больше всего?
В научных источниках данные немного расходятся. Однако, мясо, в том числе мясо птицы — все же основной источник левокарнитина для организма человека.
Согласно приведенным данным в одном из исследований, из пищевых продуктов наиболее богаты L-карнитином баранина (около 210 мг на 100 г), говядина (около 70 мг на 100 г).
Намного меньше карнитина в свинине (30 мг на 100 г) и курином мясе (примерно 8 мг на 100 г).
В молоке и молочных продуктах, куриных яйцах, хлебе, фруктах и овощах содержание карнитина очень низкое (менее 3 мг на 100 г).
В другом источнике есть следующие данные о содержании L-карнитина в мясном сырье.
- Говядина: мышцы — 64,6-78,6 мг/100 г; ребра 226 мг/100 г; печень10,7 мг/ 100 г.
- Телятина: лопатка — 78,2 мг/ 100 г; вырезка 132,8 мг/100 г; печень 6,5 мг/100 г.
- Свинина: плечо — 21,1 мг/100 г; нога 17,7 мг/100 г; ребра 40,2 мг/100 г; печень 10,7 мг/ 100 г.
- Баранина — 190 мг/100 г
- Курица — филе 13-34,4 мг/100 г; печень 69,2 мг/100 г.
- Индейка — 51,4-200 мг/100 г.
Примечание: Содержание L-карнитина в продуктах питания может варьировать в зависимости от источника и метода определения, значения являются примерными.
Можно ли варить и жарить продукты, содержащие L-карнитин?
Левокарнитин (L-карнитин) является относительно стабильным соединением и обычно не разрушается при термической обработке.
Степень стабильности левокарнитина при термической обработке:
При температуре до 180 °C (356 °F) левокарнитин остается стабильным и не разрушается.
При температуре выше 180 °C (356 °F) левокарнитин может начать разрушаться, но это происходит очень медленно.
— Старайтесь не переваривать и не зажаривать продукты питания в принципе. Хотя левокарнитин и стабилен, но другие вещества, например многие витамины, могут разрушаться при термической обработке, что может повлиять на общее качество и питательную ценность продукта, — поясняет доктор Мухина.
Описание
L-карнитин относится к витаминоподобным веществам. Присутствует в животных тканях, растениях, микроорганизмах (дрожжах). Особенно высоко его содержание в мышцах, где он впервые был обнаружен В.Г. Гулевичем.
Животные и человек способны к собственному синтезу L-карнитина. В организме человека карнитин синтезируется из аминокислот лизина и метионина.
Источники L-карнитина
Традиционными пищевыми источниками L-карнитина являются мясо, рыба, птица, молоко, сыр, творог. Также вещество может быть получено путем биотехнологического или химического синтеза или из пищевого сырья.
Признаки недостаточности
Специфических признаков недостаточности L-карнитина нет.
Неспецифически дефицит L-карнитина может проявляться:
- общей слабостью;
- быстрой утомляемостью;
- низкой переносимостью физических нагрузок;
- снижением когнитивных способностей.
Физиологическое значение
L-карнитин участвует в процессе энергообразования за счет окисления жирных кислот. Основная метаболическая функция L-карнитина — это транспорт длинноцепочечных жирных кислот через митохондриальную мембрану. В митохондриях они подвергаются окислению и дальнейшему метаболизму с образованием АТФ. Уровень синтеза АТФ зависит от поступления жирных кислот внутрь митохондрий. Жирные кислоты не способны самостоятельно проникать внутрь митохондрий, и L-карнитин выступает в роли «челнока», переносящего их через мембраны. От содержания L-карнитина в клетках зависит эффективность энергетического обмена с участием жиров. Энергетическое действие L-карнитина благоприятно сказывается на состоянии печени, в результате чего печень усиливает свою дезинтоксикационную и белково-синтетическую функцию, увеличивается содержание в печени гликогена.
Таким образом, L-карнитин влияет на эффективность энергетического обмена с участием жиров, активирует жировой обмен, мобилизует жир из жировых депо, способствует повышению выносливости, повышению переносимости физических нагрузок, восстановлению работоспособности после длительных физических нагрузок. Способствует снижению уровня холестерина и триглицеридов в крови, избыток которых является потенциальным фактором риска развития ряда сердечно-сосудистых заболеваний.
Показана роль карнитиновой недостаточности в развитии синдрома хронической усталости (СХУ). Основные проявления этой распространенной патологии представлены немотивированной выраженной слабостью, трудностью концентрации внимания, головокружением, сонливостью; большую роль играют дефицит макро- и микронутриентов, пищевая аллергия, чрезмерные психические и физические нагрузки, инфекции. Установлена четкая связь между уровнем L-карнитина в плазме крови и риском развития СХУ. Степень дефицита L-карнитина прямо связана со степенью выраженности симптомов СХУ: чем меньше L-карнитина содержится в плазме крови человека, тем ниже его работоспособность и хуже самочувствие.
Ряд исследователей указывают на эффективность ацетил-L-карнитина при лечении пациентов со старческой депрессией и возрастными нарушениями памяти.
L-карнитин находит применение при тяжелых физических или спортивных нагрузках.
Суточная потребность в L-карнитине
Адекватный уровень потребления L-карнитина для взрослых составляет 300 мг в сутки. Верхний допустимый уровень потребления L-карнитина для взрослых составляет 900 мг в сутки («Единые санитарно-эпидемиологические и гигиенические требования к товарам, подлежащим санитарно-эпидемиологическому надзору (контролю)» Таможенного союза ЕврАзЭС).
Недавние данные, полученные F. Bäckhed и коллегами (Meat-metabolizing bacteria in atherosclerosis. Nature Medicine 19,533–534 (2013)) подтверждают, что нутриент L-карнитин, обнаруженный в красном мясе и парентеральном питании, добавляемый для улучшения обменных процессов, ускоряет развитие атеросклероза вследствие формирования кишечными бактериями токсина триметиламина (ТМА), который в дальнейшем превращается в N-триметиламиноксид (ТМАО).
Две другие статьи (W.H. Wilson Tang, Zeneng Wang. Intestinal Microbial Metabolism of Phosphatidylcholine and Cardiovascular Risk. New England Journal of Medecine. 2013;368:1575-84 и Wang Z, Klipfell E, Bennett BJ, et al.Gut flora metabolism of phosphatidylcholine promotes cardiovascular disease. Nature 2011;472:57-63) с множеством тех же авторов посвящены обсуждению трансформации холина и фосфатидилхолина в ТМАО с негативными кардиоваскулярным последствиями. В этих работах утверждается, что человек, употребляющий мясо, продуцирует больше ТМАО, чем веретарианцы (люди, исключившие из рациона мясные продукты и морепродукты животного происхождения) и веганы (люди, употребляющие в пищу продукты исключительно растительного происхождения). Эта разница, возможно, связана с большим приемом L-карнитина, чем вегетарианцами. Однако, существует и альтернативная точка зрения относительно роли L-карнитина во взаимодействии с сердечно-сосудистой системой. В частности, в статье D.Clouatre et al. утверждается, что L-карнитин обладает кардиопротективным эффектом. Таким образом, представляется убедительным лишь то, на сегодня требуется больше исследований, чтобы прийти к общему знаменателю в решении данного вопроса.
L-карнитин и исследования на популяции людей
Сердце нуждается в L-карнитине в процессе метаболизма для нормальной работы. Фактически, более 95% L-карнитина накапливается в сердце и скелетных мышцах. В норме в сердце взрослого человека производится 50-70% АТФ путем окисления жирных кислот, таким образом, L-карнитин требуется в качестве топлива в метаболизме жирных кислот. В более чем 2 000 статей на ПабМед в поиске «карнитин» и «сердце» не обнаруживается связь с прямым доказательством вреда L-карнитина. Наоборот, исследования обычно демонстрируют его положительный и протективный эффект для сердца. Например, в рандомизированном двойном слепом плацебоконтролируемом исследовании с использованием L-карнитина у пациентов с ожидаемым острым инфарктом миокарда выяснено, что общие кардиальные события в группе, получавшей карнитин (2 г в день в течение 28 дней) составляли 15.6% против 26.0% в группе плацебо (p ≤ 0.05). Также прием 2 г карнитина в день улучшал 3-летнюю выживаемость у пациентов с сердечной недостаточностью, обусловленной дилятационной кардиомиопатией. В другом исследовании ученые давали 4 г карнитина в день отобранному рандомизацией 81 пациенту в течение 12 месяцев в дополнение к обычному медикаментозному лечению. После 12 месяцев при сравнении с контрольной группой наблюдалось улучшение частоты сердечных сокращений, систолического АД и диастолического АД, снижение частоты ангинозных приступов, нарушения ритма и клинических проявлений, нарушения сократительной активности миокарда (p<0.005). Смертность была значительно ниже в группе, получавшей L-карнитин (1.2% против 12.5%).
Мета-анализ по теме «L-карнитин и сердечно-сосудистые заболевания» обнаруживает схожие результаты. При сравнении с плацебо, повышение в диете L-карнитина ассоциировано со снижением смертности на 27% в целом, 65% снижением при желудочковых аритмиях, 40% снижением ангинозных приступов у пациентов с высоким риском развития острого инфаркта миокарда. Однако, основываясь на клинической доказательности, назначение 4 г L-карнитина в день и более не только улучшает функцию сердца, но также повышает предполагаемую продолжительность жизни. Таким образом, сложно понять, каким образом другие связывают получаемый с пищей L-карнитин с ухудшением исходов заболеваний сердца.
Связь с ТМА/ТМАО
Опасения о возможных негативных последствиях для здоровья вследствие приема L-карнитина как предшественника образования ТМА не являются новыми. Исследователи в течение многих десятилетий рассматривали связь между ТМА и рядом патологических состояний, включая кардиоваскулярные заболевания и рак. У индивидов с нормальной функцией почек не возникает трудности с экскрецией ТМА/ТМАО. Быстрый клиренс в этом случае способствует тому, что прием пищи, содержащей L-карнитин, не играет существенной роли в нарастании токсического уровня ТМА/ТМАО. Также похоже, что связь между ССЗ и повышенной концентрацией L-карнитина в крови, а также его составляющего холина указывает на нарушение функции где-то еще и не является частой. Значительное количество этого субстрата обнаружено в яйцах, печени и многих овощах. Согласно данным USDA Databasе, наибольшее количество холина содержат: говяжья печень, яйца, шпинат, брокколи, брюссельская капуста, томатная паста. Нет доказательств, что существует связь диеты, содержащей ТМА/ТМАО с сердечным риском. В одном из исследований уровни ТМА/ТМАО в моче были незначительными после приема 45 различных пищевых продуктов из различных диет, включающих мясо, фрукты, овощи обычные и диетические продукты, содержащие L-карнитин. Показано, что уровень ТМА/ТМАО в крови человека напрямую связан с ежедневным приемом рыбы. У людей, не питающихся рыбой, уровень ТМА/ТМАО в 10 раз ниже, чем у тех, кто питается рыбой. Koeth et al. показали, что уровень холина у пациентов с атеросклерозом не связан напрямую с диетой. Таким образом, утверждение о том, что прием L-карнитина является причиной сердечно-сосудистой дисфункции, спорно.
Роль пробиотиков
Koeth et al. выявили бактерии, ответственные за продукцию и ТМАО у человека, используя радиоактивно меченый карнитин. Исследуемые субъекты-невегетарианцы принимали порцию отбитой говядины и 250 мг L-карнитина (количество, содержащееся в 1.5 фунтах красного мяса). После 24 часов уровень ТМАО в крови поднимался до 1.8 на миллион. Вегетарианцы, которые следовали тому же протоколу, производили незначительно меньше ТМАО (p<0.05). Когда обеим группам были назначены антибиотики, уровень ТМАО не определялся. Это исследование демонстрирует, что ТМАО производится кишечными бактериями и ассоциируется с употреблением красного мяса.
Интересное продолжение этого опыта иллюстрирует влияние привычного выбора пищи. Через 3 недели после приема антибиотиков, исследуемым была назначена та же диета (стейк и L-карнитин). Кишечные бактерии у невегетарианцев производили ТМАО в 7 раз выше, чем обнаружено ранее, обнаруживая тем самым повторное заселение бактерий в кишке после антибиотикотерапии. Таким образом, частое использование антибиотиков может вести к изменению нормальной микрофлоры, проявляющемуся повышением производства ТМАО у невегетарианцев и, возможно, повышая риск развития сердечно-сосудистых заболеваний. Чтобы подтвердить данную гипотезу, однако, требуется больше информации. Но представляется ясным тот факт, что разница концентрации ТМАО у вегетарианцев и невегетарианцев невысока. 75% невегетарианцев имеют тот же самый уровень экскреции ТМАО, как и 90% вегетарианцев, что значит, что у 25% невегетарианцев и 19% вегетарианцев определяется повышение уровня ТМАО. Это позволяет предположить, что мясо само по себе не является причиной повышения уровня ТМАО, однако, определенные кишечные бактерии являются. Субъекты с высоким гастроинтестинальным уровнем бактерий Prevotella и низким уровнем Bacteroides имеют трехкратное повышение уровня ТМАО в сравнении с теми, у кого наблюдается обратное соотношение. Оба вида, и Prevotella, и Bacteroides, являются участниками микробиома в норме и входят в состав пробиотиков, однако данное исследование демонстрирует важность баланса между ними. Эти выводы позволяют судить о роли пробиотиков для коррекции кишечного дисбаланса, однако широкой доказательной базы на данный момент в мире не представлено.
Заключение
- Ни L-карнитин, обнаруженный в красном мясе, ни холин и фосфатидилхолин, обнаруженные в печени, яйцах, брокколи при нормальном состоянии не способствуют выраженному подъему уровня ТМАО.
- Рыба является первичным источником ТМАО среди продуктов, но доказан кардиопротективный эффект приема рыбы, объяснение данного противоречия требует дальнейших исследований.
- Кишечная микрофлора способствует формированию ТМАО, этому способствует не только регулярно употребление красного мяса, но и антибиотиков.
Таким образом, на сегодня вопрос о диагностической значимости повышения концентрации ТМАО в крови и моче остается открытым. Полученные в разных исследованиях данные относительно влияния повышенного уровня ТМАО на сердечно-сосудистую систему противоречивы и требуют дальнейшего изучения. Однако большинство исследователей сходится во мнении относительно значительной роли микрофлоры в изменении метаболизма человека с последующими негативными сердечно-сосудистыми событиями, а значит, и косвенно положительной роли пробиотиков для предотвращения развития этих событий. ПМГМУ им. И.М. Сеченова также планирует внести свой вклад в прояснение этого вопроса, в настоящий момент на кафедре пропедевтики внутренних болезней под руководством академика Ивашкина В.Т. начато исследование относительно роли ТМАО в развитии сердечно-сосудистых заболеваний у больных с заболеваниями кишечника.
Источник: Dallas L. Clouatre and Stacey J. Bell
Статья на конкурс «био/мол/текст»: Обильное потребление мясных продуктов в развитых странах связывают с повышенным риском сердечнососудистых заболеваний, объясняя это высоким содержанием насыщенных жиров и холестерина в мясе. Но так ли это? Исследования 2013 года не подтвердили связи между потреблением насыщенных жиров и повышенным риском развития сердечнососудистых заболеваний [1], что подтолкнуло ученых к поиску других факторов, приводящих к патологии. Тут-то и вспомнили про еще одну особенность мясных продуктов — обильное содержание L-карнитина.
Думайте, что покупаете!
Рисунок 1. Участие L-карнитина в транспорте жирных кислот из цитоплазмы в митохондрию для β-окисления и получения энергии. CPT — карнитин—пальмитоилтрансфераза, CT — карнитин—ацилкарнитинтранслоказа, CoA — кофермент A.
Впервые L-карнитин был выделен двумя русскими учеными в 1905 году. Следовательно, сейчас идет уже второй век с момента открытия и начала изучения роли этой молекулы в организме человека [2]. Это один и самых исследуемых компонентов пищи. Пища, а именно красное мясо — основной источник карнитина у всеядных животных; тем не менее, немного L-карнитина синтезируется из лизина и в самом организме.
Кроме того, все больше и больше людей потребляет L-карнитин в качестве пищевых добавок. Помимо интернет-магазинов, магазинов спортивного питания и аптек, карнитин стал встречаться даже на полках продуктовых магазинов нашей страны, в том числе и в составе витаминов, энергетических напитков, шоколадных батончиков и прочего. Купить L-карнитин или продукты с его содержанием может кто угодно. В большинстве случаев L-карнитин принимают, видимо, в надежде интенсифицировать разрушение жиров, так как считается, что он осуществляет транспорт жирных кислот в митохондриальный матрикс, где происходит их разрушение с выделением энергии (рис. 1).
Реклама L-карнитина обещает быстрое похудение, увеличение мышечной массы, улучшение умственной и физической формы, устойчивости к стрессу, детоксикацию организма и многое другое. Надо сказать, что многие положительные эффекты карнитина действительно научно доказаны, но не стоит забывать о том, что до сих пор неизвестно, вреден ли избыток карнитина для здоровья.
Норма потребления L-карнитина для взрослого человека составляет 300 мг, тогда как для похудения и улучшения спортивных показателей оптимальными считаются дозы от 500 мг до 2 г в сутки. В надежде же обрести идеальное тело, прилагая при этом минимум усилий, люди в несколько раз превышают норму, не задумываясь о возможных последствиях. А зря. Ведь мы знаем, что метаболические пути в организме недостаточно изучены, и что практически все лекарства — да что там, даже витамины при их чрезмерном употреблении — имеют побочные действия. И L-карнитин не является исключением! Исследования 2013 года показали, что метаболит L-карнитина — триметиламин оксид (ТМАО) — вещество, способствующее развитию атеросклероза [3].
Задуматься о возможной связи L-карнитина с развитием атеросклероза заставило открытие 2011 года, показавшее связь метаболизма холина — структурного аналога L-карнитина — с патогенезом сердечнососудистых заболеваний [3]. Главным источником холина служит фосфатидилхолин — одна из самых распространенных молекул клеточных мембран, в больших количествах содержащаяся пище животного происхождения.
Как оказалось, холин используется некоторыми кишечными бактериями для синтеза интермедиата триметиламина (ТМА) (рис. 2). В свою очередь, ТМА быстро абсорбируется и окисляется ферментами семейства FMO (флавинмонооксигеназа, FMO3 — главный фермент процесса) в печени до ТМАО, вызывающего развитие атеросклероза.
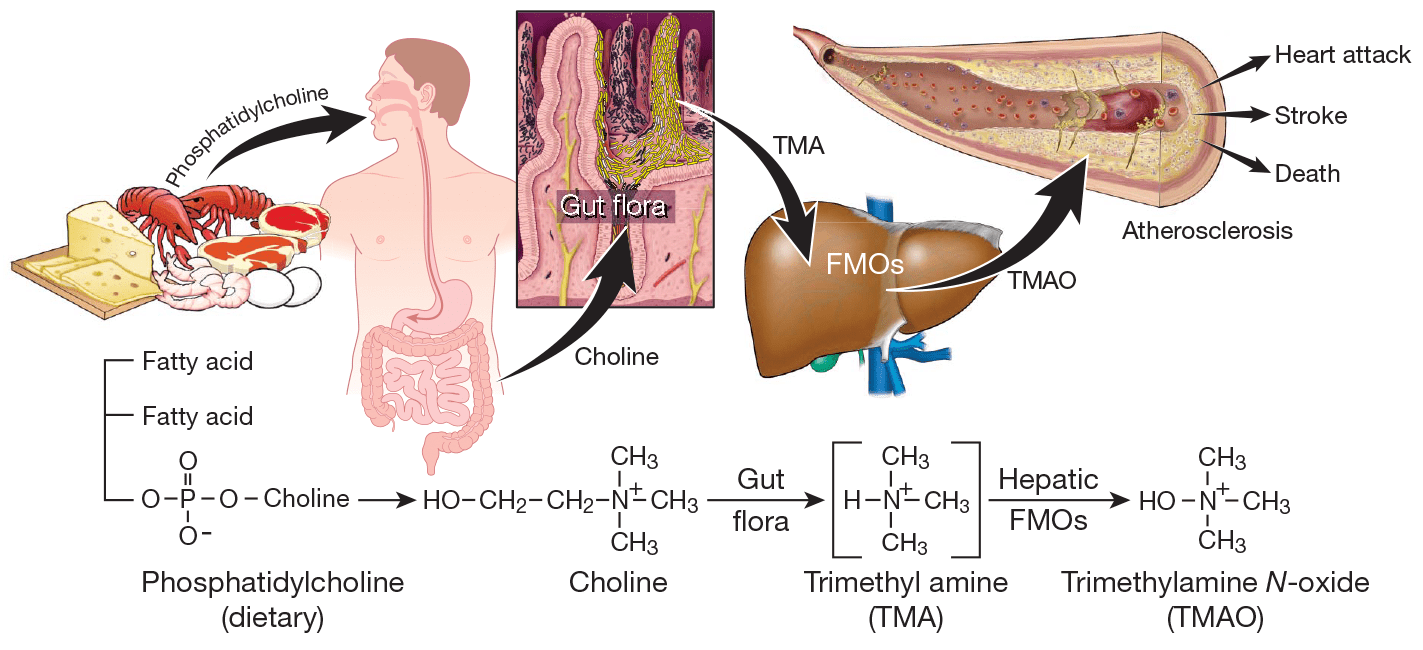
Рисунок 2. Схема синтеза кишечной флорой метаболита фосфатидилхолина, стимулирующего развитие атеросклероза. Фосфатидилхолин служит источником холина, который некоторые бактерии кишечника способны использовать для синтеза ТМА. ТМА, в свою очередь, быстро преобразуется ферментом флавинмонооксигеназой в ТМАО, уровень которого показал строгую корреляцию с развитием атеросклероза.
Использование бактериями триметиламинной группы холина для синтеза ТМА поднимает вопрос о существовании подобных метаболических путей для аналогичных соединений, включающих эту группу. Одна из таких молекул — как раз карнитин (рис. 3). Возникшее предположение о связи продукции ТМАО из L-карнитина подтвердилось исследованиями 2013 года [1], хотя предшествующие эксперименты на крысах не выявляли такой связи [4].
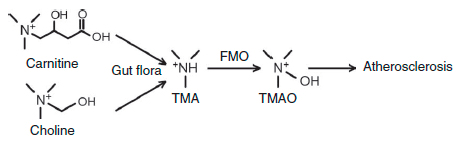
Рисунок 3. Схема синтеза ТМАО, приводящего к развития атеросклероза. Карнитин и холин — триметиламины, получаемые с пищей, — используются для синтеза ТМА микрофлорой кишечника, который быстро окисляется флавинмонооксигеназой до ТМАО.
Два независимых клинических исследования показали связь концентрации L-карнитина и ТМАО в плазме крови с развитием коронарной и периферической недостаточностей, а также сердечнососудистых заболеваний в целом. В первом исследовании участвовала группа из 2595 человек [1], во втором — проводился трехлетний кардиологический контроль 4000 пациентов [5].
Исследования на мышах также подтверждают корреляцию высокого уровня L-карнитина и ТМАО с развитием патологий сердечнососудистой системы [1]. С четырехнедельного возраста четыре группы мышей получали питание определенного типа: 1) обычное, 2) с повышенным содержанием карнитина, 3) с добавлением антибиотиков или 4) с повышенным содержанием карнитина и добавлением антибиотиков. Сравнение ткани корней аорты у мышей по достижении 19-недельного возраста выявило двойное увеличение области атеросклеротического повреждения при добавлении L-карнитина в корм (рис. 4, 5а). У мышей, получающих L-карнитин в комплексе с антибиотиками, нарушений не возникало. Следовательно, виновники развития сердечнососудистых нарушений — бактерии, участвующие в образовании ТМАО, уровень которого значительно возрастает при потреблении L-карнитина (рис. 5б) и коррелирует с развитием атеросклероза.
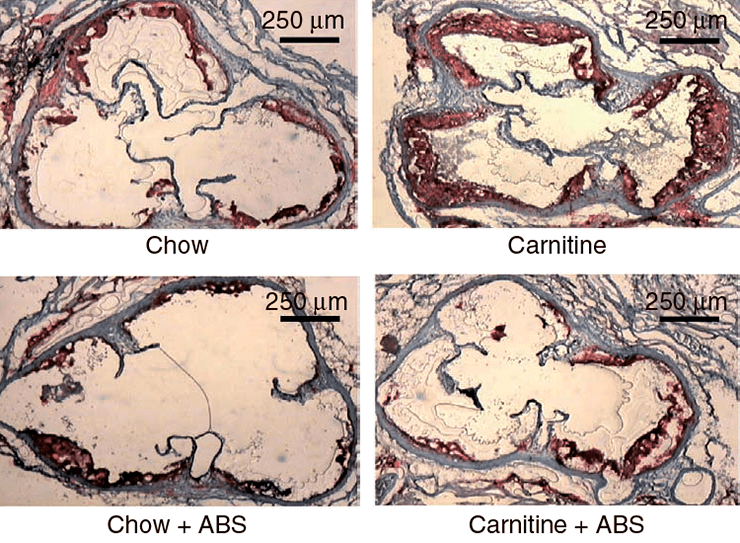
Рисунок 4. Срезы корней аорты 19-недельных мышей. Окраска гематоксилином. Chow — нормальное питание, ABS — отсутствие антибиотика.
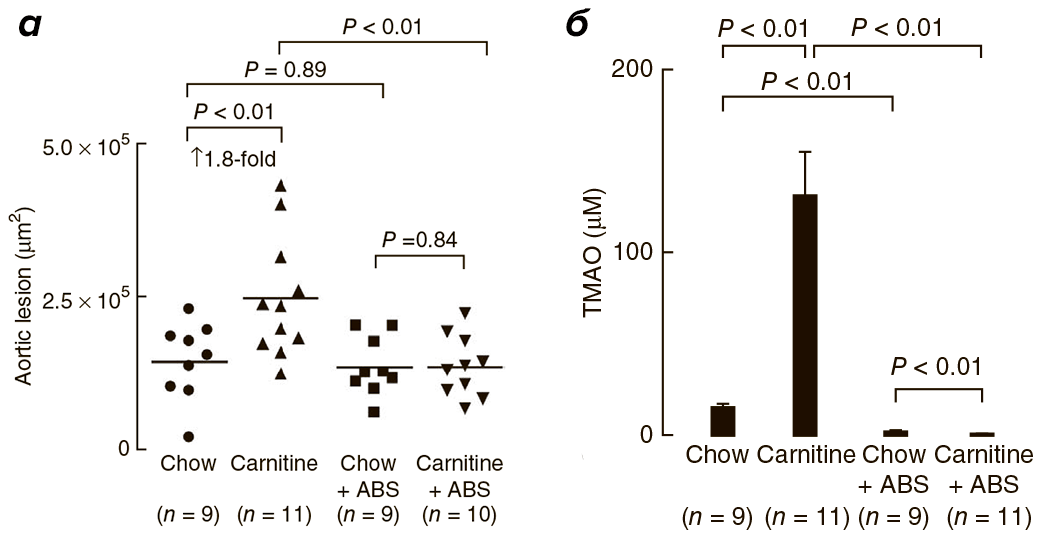
Рисунок 5. а — Оценка площади атеросклеротического повреждения корней аорты у мышей в зависимости от типа питания. б — Зависимость уровня ТМАО от типа питания мышей. Chow — нормальное питание, ABS — отсутствие антибиотика.
Вспомним про веганов (радикальные вегетарианцы, не употребляющие никаких продуктов животного происхождения) и вегетарианцев, не употребляющих красное мясо с высоким содержанием L-карнитина, и задумаемся, есть ли у них в кишечнике группа бактерий, ответственная за образование ТМА, окисляющегося до ТМАО (рис. 3)?
Не секрет, что пищевые предпочтения определяют состав микробиоты [6]. Так, продолжительный избыток карнитина в пище приводит к изменениям состава флоры кишечника, способствуя процветанию бактерий, участвующих в синтезе ТМАО [1]. Сниженное потребление L-карнитина и холина у веганов и вегетарианцев, напротив, не дает им развиваться. Бактерий, синтезирующих ТМАО, практически не остается, и даже при включении L-карнитина в рацион людей, длительное время соблюдающих растительную диету, уровень ТМАО в плазме крови и моче остается низким (рис. 6).
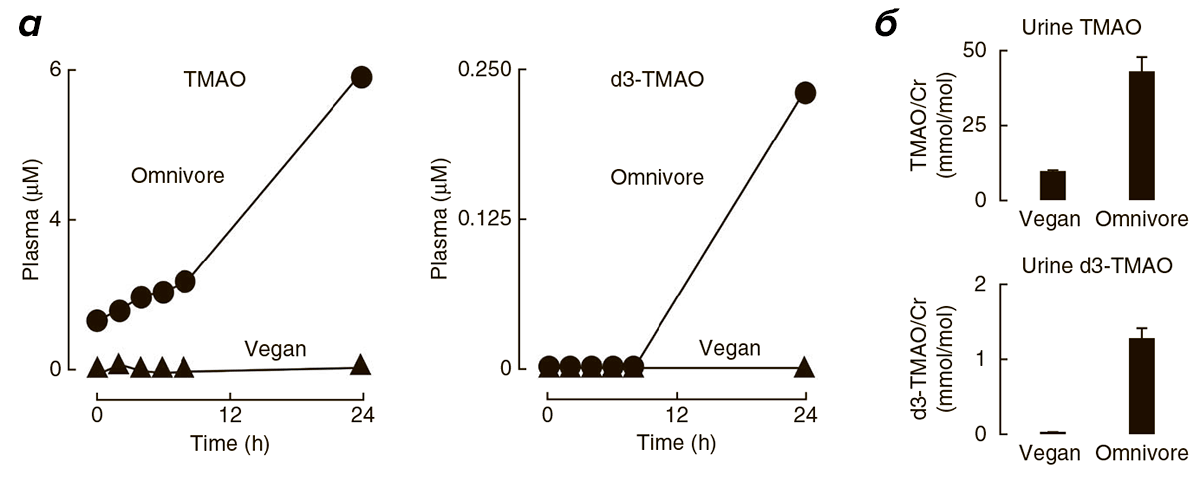
Рисунок 6. Сравнение уровней ТМАО в плазме крови (а) и в моче (б) после приема L-карнитина у веганов и людей, практически ежедневно потребляющих продукты из красного мяса. Синтез ТМАО (или его d3-меченного аналога) после потребления мясного стейка и L-карнитина (или d3-метил карнитина) незначителен у веганов (больше 5 лет отказывающихся от животных продуктов), в отличие от людей, регулярно потребляющих красное мясо. Полученные данные были дополнительно проверены и подтверждены на людях, следующих обычной диете, и людях, ведущих веганский или вегетарианский образ жизни более года.
Из этого можно предположить, что низкий уровень ТМАО и есть основная причина хорошего состояния сердечнососудистой системы веганов и вегетарианцев. Ведь статистика показывает нам более редкую встречаемость сердечнососудистых заболеваний [7], [8] и на 29% сокращенный риск смерти от ишемии сердца для людей этой группы [8].
Эксперименты также говорят о том, что соблюдение сбалансированной растительной диеты приводит к снижению давления, уровня холестерина в крови и риска возникновения атеросклероза [8–10]. Так, отказ от животной пищи может сократить прием лекарств при сердечнососудистых нарушениях. В одном из исследований группе пациентов с атеросклерозом был предложен полный переход на растительную пищу. Через год уже у 82% группы наблюдались улучшения [11]. Повторение эксперимента приводило к сходным результатам [12].
Но, быть может, преимущества соблюдения растительной диеты связаны вовсе не с отсутствием синтеза ТМАО, а с низким содержанием насыщенных жиров и холестерина в рационе? Ведь широко бытует мнение о том, что именно потребление большого количества насыщенных жиров и холестерина является главным фактором риска развития атеросклероза. Однако исследования 2013 года не подтвердили данной связи [1]. Примечательно также, что развитие атеросклеротических поражений у мышей происходило в отсутствие изменений в составе и содержании липидов, липопротеинов, глюкозы и уровня инсулина. Более того, у таких мышей не удалось выявить и признаков ожирения.
Так что возможно, кишечные бактерии, участвующие в синтезе ТМАО, — главные виновники развития атеросклероза. Если это так, то использование антибиотиков — новый возможный способ борьбы с сердечнососудистыми заболеваниями, а также их предотвращения. Как для человека, так и для мышей уже определены роды бактерий, предположительно участвующих в синтезе ТМАО. И хотя полученных данных пока недостаточно для выявления общего таксона, ответственного за синтез ТМАО, дальнейшие исследования вскоре прояснят ситуацию.
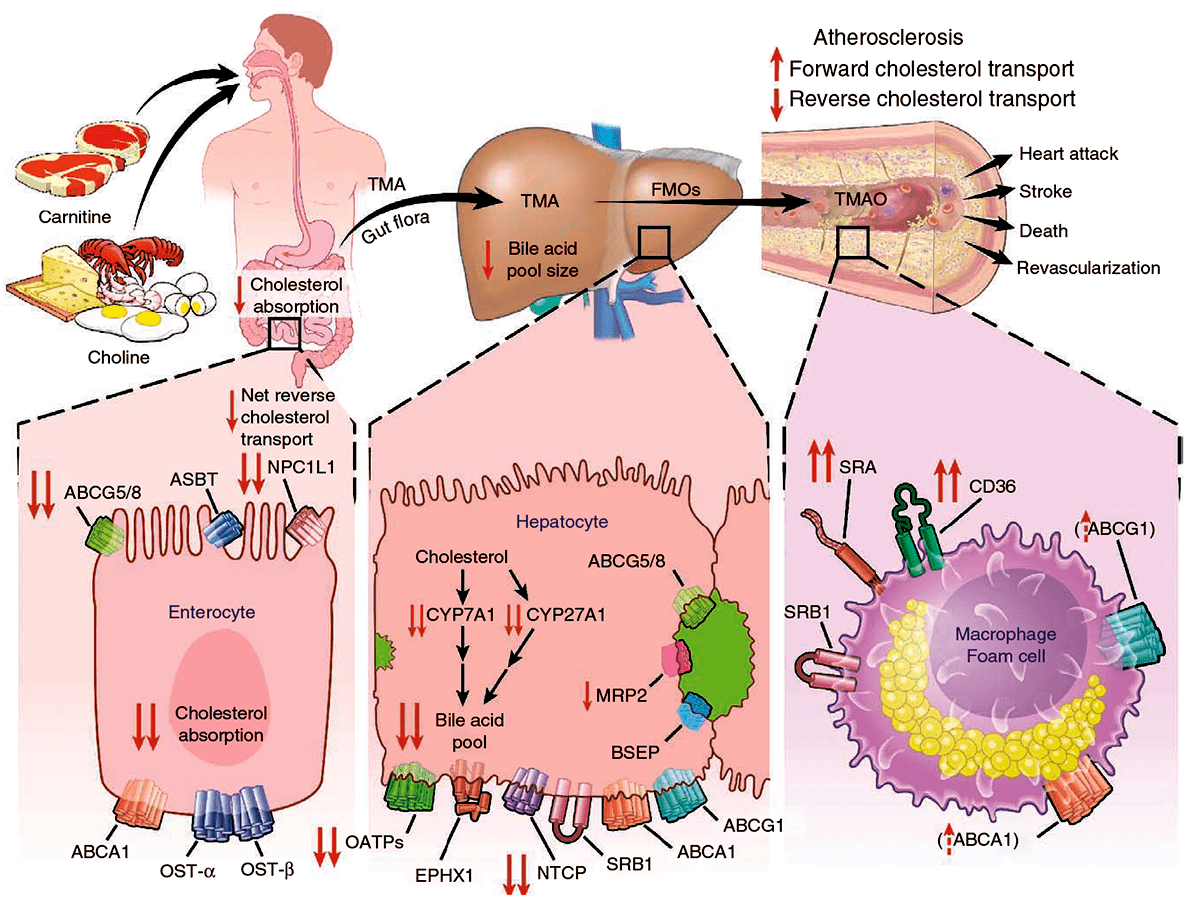
Рисунок 7. Общая схема предполагаемого метаболического пути, посредством которого микробиота влияет на развитие атеросклероза. Кишечные бактерии усваивают L-карнитин и холин, формируя ТМА, а затем ТМАО. ТМАО воздействует на метаболизм холестерина и стерина в макрофагах, печени и кишечнике. Он подавляет обратный транспорт холестерина, увеличивает экспрессию рецепторов SRA и CD36 макрофагов, способствуя образованию пенистых клеток.
Заключение
Вероятно, метаболический путь L-карнитина с участием кишечной микробиоты — главная причина давно замеченной взаимосвязи между обильным потреблением красного мяса и возникновением атеросклероза. Антибиотики, ингибирующие синтез ТМА кишечной флорой, могут стать новым оружием для борьбы и предотвращения сердечнососудистых заболеваний. К тому же открытие синтеза ТМАО из L-карнитина ставит под сомнение убежденность общества в абсолютной безвредности L-карнитина для здоровья и показывает необходимость его дальнейшего исследования.
Литература
- Robert A Koeth, Zeneng Wang, Bruce S Levison, Jennifer A Buffa, Elin Org, et. al.. (2013). Intestinal microbiota metabolism of l-carnitine, a nutrient in red meat, promotes atherosclerosis. Nat Med. 19, 576-585;
- Gulewitsch W., Krimberg R. (1905). Zur Kenntnis der Extrakivstoffe der Muskein, II Mitteilung. Uber das Carnitin. Hoppe-Seyler’s Z. Physiol. Chem. 45, 326–330;
- Zeneng Wang, Elizabeth Klipfell, Brian J. Bennett, Robert Koeth, Bruce S. Levison, et. al.. (2011). Gut flora metabolism of phosphatidylcholine promotes cardiovascular disease. Nature. 472, 57-63;
- Rebouche C.J., Mack D.L., Edmonson P.F. (1984). l-Carnitine dissimilation in the gastrointestinal tract of the rat. Biochemistry 23, 6422–6426;
- W.H. Wilson Tang, Zeneng Wang, Bruce S. Levison, Robert A. Koeth, Earl B. Britt, et. al.. (2013). Intestinal Microbial Metabolism of Phosphatidylcholine and Cardiovascular Risk. N Engl J Med. 368, 1575-1584;
- R. E. Ley, M. Hamady, C. Lozupone, P. J. Turnbaugh, R. R. Ramey, et. al.. (2008). Evolution of Mammals and Their Gut Microbes. Science. 320, 1647-1651;
- Tao Huang, Bin Yang, Jusheng Zheng, Guipu Li, Mark L. Wahlqvist, Duo Li. (2012). Cardiovascular Disease Mortality and Cancer Incidence in Vegetarians: A Meta-Analysis and Systematic Review. Ann Nutr Metab. 60, 233-240;
- Report of the Dietary Guidelines Advisory Committee on the dietary guidelines for Americans, 2010: to the Secretary of Agriculture and the Secretary of Health and Human Services. (2010). Washington, DC: Agriculture Research Service, US Department of Agriculture, US Department of Health and Human Services;
- Philip Tuso. (2013). Nutritional Update for Physicians: Plant-Based Diets. permj. 17, 61-66;
- Yoshiko Takahashi, Satoshi Sasaki, Shunji Okubo, Masato Hayashi, Shoichiro Tsugane. (2006). Blood pressure change in a free-living population-based dietary modification study in Japan. Journal of Hypertension. 24, 451-458;
- D. Ornish, S.E. Brown, J.H. Billings, L.W. Scherwitz, W.T. Armstrong, et. al.. (1990). Can lifestyle changes reverse coronary heart disease?. The Lancet. 336, 129-133;
- M. de Lorgeril, P. Salen, J.-L. Martin, I. Monjaud, J. Delaye, N. Mamelle. (1999). Mediterranean Diet, Traditional Risk Factors, and the Rate of Cardiovascular Complications After Myocardial Infarction : Final Report of the Lyon Diet Heart Study. Circulation. 99, 779-785;
- Мировой отчет по неинфекционным заболеваниям. (2010). ВОЗ;
- Global atlas on cardiovascular disease prevention and control. (2011). WHO;
- Russell Ross. (1993). The pathogenesis of atherosclerosis: a perspective for the 1990s. Nature. 362, 801-809;
- Холестериновая страшилка, которая правит миром;
- Хороший, плохой, злой холестерин;
- Maria Febbraio, Eugene A. Podrez, Jonathan D. Smith, David P. Hajjar, Stanley L. Hazen, et. al.. (2000). Targeted disruption of the class B scavenger receptor CD36 protects against atherosclerotic lesion development in mice. J. Clin. Invest.. 105, 1049-1056;
- Hiroshi Suzuki, Yukiko Kurihara, Motohiro Takeya, Nobuo Kamada, Motoyukl Kataoka, et. al.. (1997). A role for macrophage scavenger receptors in atherosclerosis and susceptibility to infection. Nature. 386, 292-296.
