Курбатов Д.Г.
ФГУ Эндокринологический научный центр, Москва
Кравцова Н.С.
ФГБУ «Эндокринологический научный центр» Минздрава России, Москва, Россия

Дифференциально-диагностическое, прогностическое и терапевтическое значение пробы с кломифеном у мужчин с гипогонадизмом
Авторы:
Роживанов Р.В., Курбатов Д.Г., Кравцова Н.С.
Как цитировать:
Роживанов Р.В., Курбатов Д.Г., Кравцова Н.С. Дифференциально-диагностическое, прогностическое и терапевтическое значение пробы с кломифеном у мужчин с гипогонадизмом. Проблемы эндокринологии.
2016;62(1):35‑37.
Rozhivanov RV, Kurbatov DG, Kravtsova NS. Differential and diagnostic, predictive and therapeutic value of test with clomifene in men with a Hypogonadizm. Problems of Endocrinology. 2016;62(1):35‑37. (In Russ.)
https://doi.org/10.14341/probl201662135-37

Гипогонадизм у мужчин — клинический и биохимический синдром, связанный с низким уровнем тестостерона, оказывающий негативное воздействие на множество органов и систем и ухудшающий качество жизни. Основным видом лечения мужского гипогонадизма является андрогенная терапия [1]. Она абсолютно показана мужчинам с первичным гипогонадизмом, сопровождающимся повышением уровней гонадотропинов, а также при необратимом выпадении их секреции гипофизом. Тем не менее в ряде случаев гипогонадизм на фоне снижения уровня гонадотропинов в крови или при нормальном их уровне обратим [2]. В таких случаях (например, у молодых людей с алиментарным ожирением или декомпенсацией углеводного обмена) терапия тестостероном не показана, так как восстановление уровня тестостерона возможно путем изменения образа жизни, снижения массы тела и лечения основного заболевания [3]. Для дифференциальной диагностики потенциальной обратимости гипогонадизма предлагается проба с антиэстрогеном кломифеном.
Цель исследования — оценка дифференциально-диагностического, прогностического и терапевтического значения пробы с кломифеном у мужчин с гипогонадизмом.
Материал и методы
В исследование включены 55 совершеннолетних мужчин с уровнем тестостерона менее 12 нмоль/л, прошедших клиническое обследование в отделении андрологии и урологии и отделе стационарзамещающих технологий ФГБУ ЭНЦ Минздрава России. В исследование не включались пациенты с исходно повышенным уровнем ЛГ, а также мужчины с выпадением его секреции. Характеристика больных представлена в табл. 1.

После исходного определения уровней тестостерона и ЛГ, всем мужчинам была проведена проба с кломифена цитратом (Клостилбегит, «Эгис», Венгрия), который назначали по 50 мг внутрь ежедневно утром в течение 10 дней. На 11-й день повторно определяли уровень тестостерона и Л.Г. Проба считалась положительной при условии нормализации уровня этих гормонов. Уровень Л.Г. (норма 2,5—11,0 ЕД/л) и тестостерона (норма 12,0—33,3 нмоль/л) определяли на автоматическом анализаторе Vitros ECi («Johnson and Johnson», Великобритания) методом усиленной хемилюминесценции. Кровь для исследования брали в пробирки типа «вакутейнер» в утреннее время натощак из локтевой вены. Гормональная диагностика осуществлялась на базе лаборатории биохимической эндокринологии и гормонального анализа ФГБУ ЭНЦ Минздрава Р.Ф. (зав.— проф. Н.П. Гончаров).
Для статистической обработки данных использовали пакет прикладных программ Statistica («StatSoft Inc.» США, версия 8.0). Сравнение по количественным признакам осуществлялось непараметрическим методом с использованием U-критерия Манна—Уитни для независимых групп и теста Вилкоксона для зависимых групп. Статистически значимыми считали различия при p<0,05.
Результаты и обсуждение
Проба с кломифеном устраняла гипогонадизм у 47 (85,5%) пациентов, что позволяет говорить о ее терапевтическом значении при обратимом гипогонадизме. При этом тест являлся безопасным: ни у одного из пациентов побочных эффектов не отмечалось. Данные пациентов в зависимости от результатов пробы представлены в табл. 2.

Мужчины с отрицательным результатом пробы имели статистически значимо большую массу тела и были значительно старше пациентов с положительным результатом теста, что подтверждает роль возрастного компонента в патогенезе гипогонадизма. Следует отметить, что несмотря на изменение образа жизни в течение 3 мес гипогонадизм у этих пациентов не устранялся; масса тела статистически значимо не снизилась (табл. 3).

Полученные результаты свидетельствуют о необратимости гипогонадизма у пациентов с отрицательной пробой с кломифеном, что диктует необходимость назначения андрогенной терапии.
Мужчинам с положительным результатом теста были даны рекомендации по изменению образа жизни, снижению массы тела, и они были повторно обследованы через 3 мес. Обследование выявило рецидив гипогонадизма у 14 (29,8%) пациентов. Таким образом, проведенный тест в сочетании с изменением образа жизни обусловил полное устранение гипогонадизма в 40% случаев (табл. 4).

Согласно полученным результатам, пациенты с рецидивом гипогонадизма и без такового статистически значимо различались по исходному уровню тестостерона; имела место тенденция к увеличению возраста мужчин с рецидивом гипогонадизма. Однако у пациентов этой группы не отмечалось значимого снижения массы тела, в отличие от мужчин, стойко избавившихся от гипогонадизма. Возможно, при достижении целевых показателей массы тела число рецидивов гипогонадизма было бы меньше. Однако это не умаляет вклада возраста и исходной степени гипогонадизма в прогноз лечения заболевания [4].
Заключение
Проведенное исследование продемонстрировало важное диагностическое значение пробы с кломифеном при оценке обратимости мужского гипогонадизма. В случаях отрицательного результата пробы следует сделать вывод о необратимости гипогонадизма и рекомендовать постоянную андрогенную терапию. При положительном результате пробы следует обратить внимание на возраст пациента и исходный уровень тестостерона. При выраженном снижении уровня тестостерона и большом возрасте пациента возможен рецидив гипогонадизма, особенно если не удается изменить образ жизни пациента и обеспечить снижение массы тела. У молодых пациентов с небольшим снижением уровня тестостерона проба в сочетании с изменением образа жизни является безопасным видом лечения гипогонадизма, так как, судя по полученным данным, гипогонадизм стойко устраняется в 40% случаев.
Конфликт интересов отсутствует.
Финансирование проведенных лабораторно-инструментальных исследований проведено при поддержке ФГБУ «Эндокринологический научный центр» Минздрава России.
Участие авторов:
Концепция и дизайн исследования — Р.В. Роживанов.
Сбор и обработка материала, статистическая обработка данных, написание текста — Р.В. Роживанов.
Концепция и дизайн исследования, редактирование — Д.Г. Курбатов.
Сбор и обработка материала — Н.С. Кравцова.
Мы используем файлы cооkies для улучшения работы сайта. Оставаясь на нашем сайте, вы соглашаетесь с условиями
использования файлов cооkies. Чтобы ознакомиться с нашими Положениями о конфиденциальности и об использовании
файлов cookie, нажмите здесь.
Аннотация
Распространённость мужского бесплодия в настоящее время в различных регионах мира прогрессивно увеличивается, при этом нижняя граница нормы содержания сперматозоидов по рекомендациям ВОЗ снизилась с 40 до 20 млн/мл [1,2]. Среди Европейских стран наибольшая распространенность бесплодия отмечена в Великобритании, а наименьшая в Финляндии [3 6]. В Германии примерная распространенность бесплодия превышает 15% всех пар репродуктивного возраста [7,8]. При этом мужское бесплодие обнаруживается у половины бесплодных пар, т.е. примерно 7% всех мужчин на протяжении жизни сталкиваются с проблемами нарушенной фертильности [9]. Следовательно, частота встречаемости нарушений репродуктивной функции у женщин и мужчин приблизительно одинакова [10]. Данные, полученные за последние 20 лет, показывают, что приблизительно в 30% случаев возникновения проблем с зачатием играет роль только мужской фактор, и примерно в 20% нарушения обнаруживаются как у мужа, такиу жены [11]. Таким образом, мужской фактор, хотя бы частично, по данным разных авторов, играет роль в30 50% случаев бесплодия [10 12].В Российской Федерации на долю мужского бесплодия отводится от 15 до 30% случаев, а частота бесплодных браков, по данным неполных эпидемиологических исследований, колеблется от 10 до 19% [9,13,14]. При этом в большинстве случаев мужское бесплодие связано со снижением количества и качества сперматозоидов, но у 25 40% мужчин с бесплодием ставится диагноз идиопатического мужского бесплодия, когда причину установить не удается [15,16].
Для цитирования:
Кравцова Н.С.,
Роживанов Р.В.,
Курбатов Д.Г.
Современные методы гормональной стимулирующей терапии нарушений сперматогенеза у мужчин. Вестник репродуктивного здоровья. 2010;(3-4):9-13. https://doi.org/10.14341/brh20103-49-13
For citation:
Kravtsova N.S.,
Rozhivanov R.V.,
Kurbatov D.G.
Sovremennye metody gormonal’noy stimuliruyushchey terapii narusheniy spermatogeneza u muzhchin. Bulletin of Reproductive Health. 2010;(3-4):9-13.
(In Russ.)
https://doi.org/10.14341/brh20103-49-13
В основе патогенеза бесплодия у большинства пациентов лежит снижение сперматогенеза, что часто сопровождается олигоспермией и азооспермией [15]. У пациентов с тяжелой олигоспермией и азооспермией в настоящее время широко используются различные вспомогательные репродуктивные технологии, например интрацитоплазматическая инъекция сперматозоида (ИКСИ) [17]. Однако для успешного проведения оплодотворения необходимо наличие зрелого сперматозоида в эякуляте или яичке. Поэтому еще в начале 90–х годов П.Г. Морозовым было высказано предложение о целесообразности проведения гормональной стимуляции сперматогенеза в процессе подготовки супружеских пар в программах вспомогательной репродукции [18]. В настоящий момент из препаратов для гормональной стимулирующей терапии используются антиэстрогены и гонадотропины хорионический гонадотропин и рекомбинантные препараты лютеинизирующего гормона (ЛГ) и фолликулостимулирующего гормона (ФСГ) [15]. Кломифен, тамоксифен или гонадотропины могут быть эффективны, только когда уровни ФСГ и ЛГ низкие или находятся в пределах нормы [19]. Поскольку такие состояния в сочетании с олигоспермией широко распространены, на практике использовались различные методы гормональной стимуляции в попытке улучшить показатели спермограммы и повысить фертильность [20]. Одним из таких методов лечения является применение антиэстрогенов, так как антиэстрогены встраиваются в отрицательную обратную связь половых стероидов на уровне гипоталамуса и гипофиза и повышают секрецию ФСГ и ЛГ [21]. В свою очередь ФСГ и ЛГ стимулируют сперматогенез с возможным улучшением фертильности. Так, А. Hussein и соавт. (2005 г.) доказали эффективность применения кломифена цитрата при подготовке пациентов к процедуре ИКСИ: 42 пациентам в возрасте от 25 до 39 лет с задержкой созревания сперматозоидов (42,9%) и сниженным сперматогенезом (57,1%), по данным биопсии яичка, был назначен кломифен цитрат 50 мг в день, с последующим титрованием доз в зависимости от уровня тестостерона. После терапии кломифеном от 3 до 9 мес у 64,3% пациентов концентрация сперматозоидов увеличилась от 1 до 16 млн/мл, средняя величина составила 3,8 млн/мл. Достаточное количество сперматозоидов для проведения ИКСИ появилось у всех пациентов. К тому же назначение кломифена цитрата вызвало статистически значимое повышение количества более успешных случаев получения сперматозоидов путем их экстракции из яичка [22]. S. Patankar и соавт. (2000 г.) исследовали влияние кломифена цитрата на повышение концентрации сперматозоидов у мужчин с выраженной (группа 1) и умеренной (группа 2) олигоспермией. Кломифен назначали в дозе 25 мг/день в течение 25 дней с 5–дневным перерывом циклами по 3 мес. В группе 1 средняя концентрация сперматозоидов увеличилась с 3,84 +/0,32 до 8,2 +/1,58 (p < 0,05), в группе 2 от 13,05 +/0,48 до 24,55 +/1,73 (p < 0,001). Средние значения подвижности сперматозоидов увеличились от 1,74 +/0,25 до 3,92 +/0,83 (p < 0,05) в группе 1 от 8,27 +/0,40 до 10,05 +/0,56 (p < 0,01) и в группе 2. Таким образом, терапия кломифеном увеличивала как количество, так и подвижность сперматозоидов [23]. М. Hammami (1996 г.) в своем исследовании также изучал влияние терапии кломифеном цитратом на количество сперматозоидов у мужчин с частичной утратой фертильности при идиопатической олигозооспермии. Так, 17 пациентов с идиопатической олигозооспермией (средняя концентрация сперматозоидов 7,3 +/1,2 * 10(6) /мл, среднее значение ФСГ 5 +/0,5 МЕ/л) были включены в исследование. Оценку параметров спермы 9 ВЕСТНИК Репродуктивного Здоровья •• Декабрь •• 2010 проводили в среднем через 7,2 +/0,6 мес терапии кломифеном. Терапия кломифена цитратом привела к значительному повышению общего числа сперматозоидов (среднее процентное изменение 261 +/117, p = 0,02) и их подвижности (370 +/216, p = 0,03) [24]. Следует отметить, что, по данным литературы, среди мужчин с бесплодием при гипогонадотропном гипогонадизме и олиго азооспермии лучше всего отвечают на терапию кломифена цитратом пациенты с идиопатической формой гипогонадотропного гипогонадизма [25]. Исходя из того, что концентрация подвижных сперматозоидов коррелирует с концентрацией фруктозы в секрете семенных пузырьков, G. Gonzales (2001 г.) провел исследование, в котором 42 пациента с астеноспермией и бесплодием получали кломифен в дозе 100 мг в день в течение 5 дней. Подвижность сперматозоидов улучшалась после лечения кломифеном, если увеличивалась концентрация фруктозы семенной жидкости. У мужчин, у которых функция семенных пузырьков улучшилась, выраженность астеноспермии уменьшилась от 50,0 до 28,6% (p < 0,002), тогда как у пациентов, не ответивших на лечение кломифеном, астенозооспермия не уменьшилась [26]. С другой стороны, в литературе описаны исследования, в которых продемонстрировано отсутствие позитивного влияния кломифена на сперматогенез. Так, К. Matsumiya и соавт. (1998 г.) проводили исследование по сравнению эффективности и безопасности терапии кломифеном и аналогом гонадотропин-рилизинггормона (ГнРГ) у мужчин с идиопатической нормогонадотропной олигоастенозооспермией (ИНОА). Из них 36 пациентов получали аналог ГнРГ (15 мг бусерелина ацетата 1 раз в день интраназально) и 23 пациента получали кломифена цитрат 50 мг в день перорально. Отмечено повышение среднего показателя концентрации сперматозоидов от 13,7 * 10(6)/мл до 22,1 * 10(6)/мл (p < 0,01) и увеличения их подвижности от 35,9 до 43,9% (p < 0,05) в группе, получавшей ГнРГ-аналог, тогда как в группе, получавшей кломифен цитрат, не получено значительных изменений этих показателей [27]. W. Krause и соавт. (1992 г.) изучали применение другого антиэстрогена тамоксифена при идиопатической олигоспермии. Были включены в исследование 76 мужчин, имевших концентрацию сперматозоидов в сперме 2 20 * 10(6)/мл, подвижность сперматозоидов 20 50% и количество патологических форм между 50 80%. Из них 39 пациентов получали тамоксифен в дозе 30 мг в день и 37 пациентов плацебо. Концентрация сперматозоидов в процессе лечения увеличилась от 9,3 +/11,7 до 11,4 +/13,7 * 10(6) в группе тамоксифена, и от 9,1 +/7,1 до 9,3 +/8,8 * 10(6) в группе плацебо. Однако эти различия не были статистически значимыми, процент подвижных сперматозоидов и патологических форм не различался в обеих группах [28]. D. Adamopoulos и соавт. (1997 г.) изучали влияние терапии тестостерона ундеканоатом в комбинации с тамоксифена цитратом и каждого по отдельности на параметры спермы при идиопатической олигоспермии. В исследование были включены 80 пациентов. Пациентов рандомизировали в группу плацебо, группу получающих тестостерон ундеканоат 40 мг 3 раза в день, группу получающих тамоксифен цитрат 10 мг 2 раза в день и группу комбинированной терапии. В группе комбинированной терапии получено улучшение общего числа 10 сперматозоидов и их подвижности через 3 и 6 мес. В сравнении с другими группами, получавшими терапию, обнаружено значительное увеличение объема подвижных сперматозоидов и их функциональных форм [29]. В другом исследовании D. Adamopoulos и соавт. (2003 г.) также изучали эффективность комбинированной терапии тамоксифена цитратом и тестостерона ундеканоатом у мужчин с олигоспермией. В исследование были включены 212 мужчин с идиопатической олигозооспермией и 82 с нормозооспермией. Пациенты с олигоспермией были разделены на 2 группы, группа 1 (n =106) получала тамоксифен 20 мг/день в сочетании с тестостероном ундеканоатом 120 мг/день, группа 2 (n =106) плацебо в течение 6 мес. В группе, мужчин, получающих активное лечение, были зафиксированы: увеличение концентрации (исходно 9,4 54,0 * 10(6) /мл, и 28,2 119,6 * 10(6) /мл через 6 мес), увеличение подвижности (29,7% +/12,0% исходно и 41,6% +/13,1% через 6 мес) и числа сперматозоидов с нормальной морфологией (41,2% +/14,0% исходно и 56,6% +/11,5% через 6 мес). В группе плацебо и у пациентов с нормозооспермией не отмечено значимых изменений. Спонтанная беременность наступила в 33,9% случаев в группе, мужчин, получающих активное лечение, по сравнению с 10,3% в группе плацебо. Таким образом, комбинированная терапия тамоксифеном и тестостероном у пациентов с идиопатической олигоспермией улучшала показатели спермы и увеличивала количество случаев спонтанной беременности [30,31]. Отечественные ученые С.Е. Василевская и А.В. Куренков (1999 г.) также проводили оценку терапии тестостерона ундеканоатом и тамоксифена цитратом мужчин в бесплодных парах. В исследование был включен 21 мужчина в возрасте от 25 до 42 лет с нормальным физическим развитием и с нормальным содержанием гормонов в крови. Пациентам был назначен курс лечения тамоксифена цитратом (20 мг в сутки, 30 дней) в сочетании с тестостерона ундеканоатом (120 мг в сутки, 90 дней). Значимых различий концентрации сперматозоидов и процента активно подвижных форм до и после лечения не наблюдали, но увеличение процента морфологически нормальных форм сперматозоидов являлось статистически значимым (р<0,05). После лечения жены у 2 пациентов забеременели. У 1 мужчины после лечения появилась устойчивая азооспермия. По медицинским показаниям 9 супружеским парам были рекомендовано процедура экстракорпорального оплодотворения (ЭКО) [32]. I. Kotoulas и соавт. (1994 г.) также изучали эффективность монотерапии тамоксифеном нарушений сперматогенеза. В их исследовании мужчинам с бесплодием был назначен тамоксифен 10 мг дважды в день в течение 3 мес группа А (n=122) и плацебо терапия группа В (n=117). Через 3 мес после окончания лечения оценивали концентрацию, подвижность, жизнеспособность и морфологию сперматозоидов. Средние показатели количества сперматозоидов значительно улучшились в группе А от исходного уровня, что было особенно заметно у мужчин с выраженной олигоспермией, а также в сравнении с группой В. Количество мертвых сперматозоидов после терапии тамоксифеном значительно уменьшилось в группе А, также было установлено значительное снижение этого показателя по сравнению с группой В. Однако не было выявлено влияния тамоксиВЕСТНИК Репродуктивного Здоровья •• Декабрь •• 2010 Обзор литературы фена на улучшение подвижности и морфологии сперматозоидов [33]. Т. Kadioglu и соавт. (1999 г.) изучали эффективность тамоксифена при мужском бесплодии у пациентов с нормогонадотропной и гипергонадотропной олигоспермией, а также идиопатической олигоспермией (136 пациентов) или после оперативного лечения варикоцеле (84 пациента). Всем пациентам был назначен тамоксифен цитрат 10 мг 2 раза в день. Уровни ФСГ, ЛГ и тестостерона увеличились во всех группах, получающих тамоксифена цитрат. У нормогонадотропных пациентов отмечено значительное повышение числа сперматозоидов и их концентрация, тогда как незначительное повышение у гипергонадотропных пациентов было статистически незначимым. Исследователи пришли к выводу, что применение тамоксифена является экономической и практической альтернативой у пациентов с нормогонадотропной олигоспермией до применения вспомогательных репродуктивных технологий [34]. D. Farmakiotis и соавт. (2007 г.) изучали влияние еще одного препарата из группы антиэстрогенов торемифена на показатели сперматогенеза при идиопатической олигозооспермии. У 100 пациентов с утратой фертильности и олигозооспермией применяли торемифен 60 мг в сутки в течение 3 мес. Назначение торемифена привело к увеличению оцениваемых показателей спермограммы у всех пациентов. В 22% случаев беременность наступила в течение 2 мес после окончания лечения. В конце 3-го месяца уровень сывороточного ФСГ был значительно выше у пациентов (78%), у которых партнерши не достигли беременности, при этом общее количество сперматозоидов и количество нормальных морфологических форм было значительно ниже у этих пациентов по сравнению с теми, у которых партнерши забеременели [35]. Таким образом, авторы сделали вывод об эффективности торемифена в терапии олигозооспермии. Следует отметить, что за рубежом проводились неоднократные рандомизированные исследования по применению антиэстрогенов в течение 3 мес и более в сравнении или без сравнения с плацебо-терапией у мужчин с олигои/или астеноспермией, в бесплодных парах с мужским фактором бесплодия, не продемонстрировавшие положительного влияния терапии на количество беременностей [36]. Всего оценено 10 исследований по применению кломифена или тамоксифена, в которые были включены 738 мужчин [36]. В 5 из этих исследований не было специфических методов отбора. Установлено, что антиэстрогены оказывают положительный эффект на эндокринные показатели, в частности на уровень тестостерона, ЛГ и ФСГ, а также показатели сперматогенеза. Однако не было разницы в количестве беременностей между группами, получавшими антиэстрогены, и контрольных группах (относительный риск 1,26, 95% доверительный интервал (ДИ) 0,99 1,56). Количество беременностей в этих 5 исследованиях составило 15,4% в сравнении с 12,5% в контрольной группе [36]. Наряду с изучением эффективности антиэстрогенов в терапии мужского бесплодия проведены исследования, направленные на изучение эффекта терапии гонадотропинами. Так, исследовали влияния рекомбинантного человеческого ФСГ на параметры спермы и количество спонтанных беременностей в парах с мужским фактором бесплодия [37]. Пациентам с идиопатической олигоспермией был назначен рекомбинантный ФСГ 100 МЕ через день в течение 3 мес. В группе пациентов, хорошо ответивших на лечение (48,4%), отмечена значительное повышение числа сперматозоидов. В течение 3 мес после отмены ФСГ в группе хорошо реагирующих пациентов отмечено увеличение количества спонтанных беременностей (16,7%) по сравнению с группами, не отвечающими на лечение (3,1%) и не получавших ФСГ (4,0%) [37]. В. Baccetti и соавт. (2004 г.) оценивали влияние терапии ФСГ на качество сперматозоидов, а также исследовали их структуру и функцию у бесплодных мужчин. Из 81 пациента, включенного в исследование, 15 получали плацебо, у 19 терапия оказалась неэффективной. У остальных 47 пациентов было достигнуто улучшение изучаемых параметров, при этом 9 достигли улучшения показателей спермы, приближенного к порогу фертильности [38]. В другом исследовании установлено положительное влияние терапии ФСГ на структуру и функцию сперматозоидов (увеличивалось количество сперматозоидов с нормальной морфологией) в дозе 150 МЕ в течение 12 нед [39]. J. Ashkenazi. и соавт. (1999 г.) изучали роль ФСГ в терапии бесплодия у мужчин при подготовке к ИКСИ [40]: 79 пациентов основной и 39 пациентов контрольной группы получали терапию ФСГ в дозе 75 МЕ в сутки в течение 50 дней и более. Количество успешных процедур оплодотворения и беременностей было больше в основной группе (68,0 и 35,9% соответственно), по сравнению с контрольной (59,0 и 17,9% соответственно) однако статистически значимой разницы не достигнуто. В основной группе число успешных случаев имлантации было значимо выше: 15,5% против 6,5% в контрольной. Таким образом, терапия ФСГ у бесплодных мужчин перед ИКСИ значительно увеличивала вероятность имплантации эмбриона и количество беременностей [40,41]. В другом исследовании также был установлен положительный эффект применения рекомбинантного ФСГ в дозе 150 МЕ в течение 3 мес при подготовке к ИКСИ, который проявлялся в виде улучшения тестикулярного объема и параметров спермы [42]. Кроме того, было отмечено, что длительное применение очищенного ФСГ 150 МЕ 3 раза в неделю в течение 6 мес при идиопатической олигоспермии с нормальными уровнями сывороточных гормонов увеличивает концентрацию сперматозоидов и их подвижность [43]. Наряду с препаратами ФСГ изучали влияние на сперматогенез и других гонадотропинов. Так, М. Depenbusch и соавт. (2002 г.) исследовали эффективность монотерапии хорионическим гонадотропином человека (ХГЧ) для стимуляции и поддержания сперматогенеза у пациентов с гипогонадотропным гипогонадизмом. У 13 пациентов вначале для индукции сперматогенеза были назначены ХГЧ/ХМГ (n=12) и ГнРГ (n=1). После достижения индукции сперматогенеза пациенты получали только ХГЧ для поддержания сперматогенеза и вторичных половых признаков. После успешной индукции сперматогенеза монотерапию ХГЧ проводили от 3 до 24 мес. Через 12 мес концентрации сперматозоидов снизились, однако оставались в пределах нормы у всех пациентов, кроме 1 пациента с азооспермией. Тестикулярный объем снизился незначительно и составил 87% от объе11 ВЕСТНИК Репродуктивного Здоровья •• Декабрь •• 2010 ма, достигнутого терапией ХГЧ/ХМГ. Во время монотерапи ХГЧ уровни ЛГ и ФСГ были подавлены и оставались в пределах, заданных исследованием. Таким образом, авторами сделан вывод о том, что однажды индуцированный сперматогенез у пациентов с вторичным гипогонадизмом может поддерживаться монотерапией ХГЧ на качественном уровне у большинства пациентов в течение длительного периода [44,45]. Н. Fuse и соавт. (1996 г.) также изучали применение гонадотропинов для индукции сперматогенеза у мужчин с гипогонадотропным гипогонадизмом. У 16 пациентов применяли заместительную гормональную терапии гонадотропинами. Из них 2 пациента получали только ХГЧ и достигли улучшения сперматогенеза через2и 12 мес после начала лечения, 3 пациента, получавшие комбинированную терапию гонадотропинами, достигли улучшения сперматогенеза через 6 28 мес. Пациенты, которые имели объем яичек 4 мл и более, достигли высокой концентрации сперматозоидов и оплодотворили своих партнерш, хотя не было установлено связи между тестикулярным объемом до лечения и появлением сперматогенеза [46]. Е. Vicari и соавт. (1992 г.) изучали эффекты длительной терапии ХГЧ (14 120 мес) у 17 пациентов с изолированным гипогонадотропным гипогонадизмом на тестикулярный объем, уровень тестостерона в плазме и концентрацию сперматозоидов. В среднем объем яичек увеличился от 3,8 +/0,2 до 14,9 +/1,1 мл после 22,2 +/2,3 мес терапии ХГЧ. Кроме того, для оценки тестикулярного объема пациенты были разделены на 2 группы в зависимости от исходного объема яичек: меньше 4 мл (1-я группа) и больше 4 мл (2-я группа). Уровни тестостерона на протяжении всей терапии были в пределах возрастной нормы и значительно не различались в обеих группах. У 13 пациентов (70%) было достигнуто улучшение сперматогенеза во время монотерапии ХГЧ, у 5 (60%) из 9 1-й группыиу8 (90%) из 9 2-й. К тому же пациенты 2-й группы имели лучшие показатели сперматогенеза, чем 1-й. Концентрация сперматозоидов положительно коррелировала с достигнутым объемом яичек и не зависела от возраста, продолжительности лечения и первоначального тестикулярного объема. Дополнительное назначение менопаузального гонадотропина у 9 пациентам привело к увеличению у них объема яичек, однако средний объем яичек не отличался от среднего объема при окончании монотерапии ХГЧ, а также у этих пациентов не было выявлено различий в концентрации сперматозоидов по сравнению с таковой на фоне терапии ХГЧ. Только 1 пациент достиг улучшения сперматогенеза после назначения менопаузального гонадотропина. Среди пациентов с улучшением сперматогенеза при попытке зачатия 7 из 10 достигли успеха, 2 из них были из 1-й группы. Это исследование продемонстрировало эффективность монотерапии ХГЧ для индукции сперматогенеза у пациентов с изолированным гипогонадотропным гипогонадизмом независимо от первоначального тестикулярного объема. Тем не менее, определенному числу пациентов показано назначение менопаузального гонадотропина для увеличения тестикулярного объема, продукции спермы и достижения фертильности [47]. G. Beretta и соавт. (2005 г.) в своем исследовании использовали менопаузальный гонадотропин для стимуляции сперматогенеза при идиопатической олигоас12 тенотератоспермии. У 18 пациентов с олигоастенотератоспермией и объемом яичек 12-15 мл проводили терапию менопаузальным гонадотропином (75 МЕ ФСГ и 75 МЕ ЛГ) 3 раза в неделю в течение 90 дней, по окончании терапии оценивали параметры спермы и объем яичек в сравнении с контрольной группой из 13 мужчин, ожидающих ИКСИ и не получающих какой-либо медикаментозной терапии. В результате лечения получено статистически значимое увеличение концентрации сперматозоидов (p = 0,016) и уменьшение их атипичных форм (p = 0,040). Также были получены данные, что терапия менопаузальным гонадотропином положительно влияет на качество эмбрионов, полученных в ходе последующих ИКСИ [48]. Р. Liu и соавт (2008 г.) определяли предикторы успешной индукции сперматогенеза и восстановления фертильности у пациентов с гипогонадизмом и бесплодием в ответ на лечение гонадотропинами: у 75 мужчин, 72 из которых желали достигнуть фертильности, применяли различные препараты гонадотропинов по 16 курсов с 1981 по 2008 г. Оценку показателей спермы проводили каждые 3 мес. Стали отцами 39 мужчин. Среднее время достижения появления первых сперматозоидов было 7,1 (95% ДИ6,3 10,1) мес, а время достижения зачатия 28,2 (95% ДИ21,6 38,5) мес. Средний показатель концентрации сперматозоидов для достижения спонтанной беременности составлял 8,0 (95% ДИ0,2 59,5) млн/мл. При этом больший объем яичек до лечения гонадотропинами являлся независимым предиктором более быстрого ответа на терапию [49]. Другие исследователи также изучали возможность комбинированной терапии мужского бесплодия препаратами гонадотропинов. Так, 100 пациентов с идиопатическим и приобретенным гипогонадотропным гипогонадизмом получали терапию ХГЧ в течение 3 6 мес, а затем комбинированную терапию ХГЧ и ФСГ 150 МЕ трижды в неделю в течение 18 мес. У 81 мужчины после терапии ХГЧ сохранялась азооспермия, однако были достигнуты нормальные уровни тестостерона. А после комбинированной терапии у 68 (84%) из них в эякуляте появились сперматозоиды и у 56 (69,1%) пациентов была достигнута концентрация сперматозоидов 1,5 и более * 10(6)/мл. Больший исходный объем яичек, низкий индекс массы тела и достижение половой зрелости были предикторами хорошего ответа на терапию. Таким образом, терапия рекомбинантным человеческим ФСГ в сочетание с ХГЧ являлась эффективной для восстановления фертильности у большинства мужчин с гипогонадотропным гипогонадизмом [50]. М. Bakircioglu и соавт (2007 г.) в своем исследовании использовали комбинированную терапию гонадотропинами для стимуляции сперматогенеза перед ИКСИ. У 25 пациентов с азооспермией был установлен диагноз гипогонадотропный гипогонадизм. Все пациенты получали ХГЧ в течение 1 мес, в сочетании с рекомбинантным ФСГ в последующие месяцы терапии. Уровень общего тестостерона и объем яичек значимо увеличились после терапии гонадотропинами (р < 0,001). Сперматозоиды стали определяться в эякуляте в среднем через 10 мес. Спонтанная беременность наступила у 4 пар. У 18 пар проведено 22 процедуры ИКСИ с использованием сперматозоидов из эякулята или яичка, в результате было получено 12 (54,5%) беременностей. Данные результаты, по мнению авторов, свидетельствуВЕСТНИК Репродуктивного Здоровья •• Декабрь •• 2010 Обзор литературы ют об успешном лечении бесплодия при гипогонадотропном гипогонадизме комбинированной терапией гонадотропинами в сочетании с ИКСИ [51]. Подобная эффективность комбинированной терапии была продемонстрирована и в других исследованиях [52,53]. Так, применение монотерапии ХГЧ в течение 16 нед у 61% пациентов с гипогонадотропным гипогонадизмом приводило к нормализации уровня тестостерона в крови, однако у пациентов оставалась азооспермия. После добавления рекомбинантного ФСГ в дозе 225 МЕ 2 раза в неделю и 150 МЕ 3 раза в неделю индукция сперматогенеза была достигнута в 47% случаев, в среднем через 5,5 мес терапии [53]. Э.М. Китаев и соавт. (1999 г.) в своем исследовании проводили краткосрочную гормональную стимуляцию сперматогенеза у 19 мужчин в возрасте 36,3±0,8 года. Гормональная стимуляция сперматогенеза состояла из 2 инъекций препарата, содержащего по 150 МЕ ФСГ и 150 МЕ ЛГ и назначаемого на 5 и 10-й дни менструального цикла партнерши, находящейся на стимуляции суперовуляции, либо из 2 инъекций препарата с интервалом 5 дней. На фоне терапии достоверное улучшение показателей сперматогенеза было достигнуто у 73,6% мужчин [54]. В итоге в 2007 г. был проведен анализ 4 рандомизированных контролируемых исследований по эффективности применения гонадотропинов при идиопатическом мужском бесплодии. В анализ были включены 278 пациентов. По сравнению с плацебо или отсутствием лечения на фоне терапии гонадотропинами было продемонстрировано более высокое количество беременностей (относительный риск (ОР) 4,17, 95% ДИ1,30 7,09). Но, по мнению авторов, количество проведенных исследований является недостаточным для формирования окончательных выводов [55]. Таким образом, приведённые в литературе сведения отечественных и зарубежных исследователей по применению методов гормональной стимулирующей терапии нарушений сперматогенеза свидетельствуют о значительном прогрессе в изучении данной проблемы. Однако в литературе отсутствуют детальные данные об эффективности стимулирующей терапии в различных группах пациентов с патоспермией и бесплодием, что требует дальнейшего изучения. Литература
Список литературы
1. Всемирная организация здравоохранения (ВОЗ). Руководство по лабораторному исследованию спермы человека и взаимодействию спермы с цервикальной слизью. Тбилиси, 1988.
2. Гоголевский П.А. ИКСИ: существует ли риск возрастания частоты врожденных пороков развития? Пробл. репрод. 1998; 6: 9–13.
3. Ginsburg J, Okolo S, Prelevic G, Hardman P. Residence in the London area and sperm density. Lancet.1994;343: 230.
4. Irvine S, Cawood E, Richardson D et al. Evidence of deteriorating semen quality in the United Kingdom: birth cohort study in Scotland over 11 years. Brit Med J. 1996; 312: 467-70.
5. Jensen T K, Giwermann A, Carlsen E et al. Semen quality among mem-bers of organic food associations in Zealand, Denmark. Lancet.1996;.347:1844.
6. Vierula M, Niemi M, Keiski A, Saaranen M. Saarikoski S., Suominen J. High and unchanged sperm counts of Finnish men. Int J Androl.1996; 19:11-7.
7. Bruckert E. How frequent is unintentional childlessness in Germany? Androl. 1991; 23: 245-50.
8. Juul S, Karmaus W,Olsen J. and The Europen Infertility and Subfecundety Study Group. Regional differences in waiting time to pregnancy: pregnancy-based surveys from Denmark, France, Germany, Italy and Sweden. Hum Reprod.1999; 14:1250-4.
9. Тер-Аванесов Г.В. Андрологические аспекты бесплодного брака. Диc. докт. мед. наук. М., 2002.
10. Кулаков В.И., Назаренко Т.А., Тер-Аванесов Г.В. Бесплодный брак: достижения, проблемы, перспективы. Тезисы конференции «Мужское здоровье», 2003 (Web-репринт).
11. Morell V. Basic infertility assessment. Prim Care. 1997; 24:195.
12. Тер-Аванесов Г.В. Андрологические аспекты бесплодного брака. Бол. органов репродукт. системы. 2004;3 (Web-репринт).
13. Селезнева И.Ю. Бесплодный брак. Эпидемиологическое исследование. Диc. канд. мед. наук. М., 1999: 3349.
14. Филиппов О.С. Бесплодный брак в Западной Сибири. Диc. докт. мед. наук. М., 1999: 27–48.
15. Андрология. Мужское здоровье и дисфункция репродуктивной системы. Под ред. Э Нишлага, Г.М. Бере. М.,2005.
16. Артифексов С. Б. Андрологические аспекты бесплодного брака. Урол. и нефрол. 1996; 4:39.
17. Palermo G, Joris H, Devroey P et al. Pregnancies after intracytoplasmic injection of single spermatozoon into an oocyte. Lancet. 1993; 240:17.
18. Морозов П.Г. Новые перспективы клинического применения гонадотропинов в андрологии. Androl. reproductol. sexol. 1993; 2 (3): 29-33.
19. CheckJH Treatment of male infertility. Clin Exp Obstet Gynecol. 2007; 34(4): 201-6.
20. Sokol R Z. Medical and endocrine therapy of male factor infertility. Infertil Reprod Med Clin North Am. 1992; 3:389.
21. Ioannidou-Kadis S, Wright PJ, Neely RD, Quinton R. Complete reversal of adult-onset isolated hypogonadotropic hypogonadism with clomiphene citrate. Fertil Steril 2006; 86(5):1513.e5-9.
22. Hussein A, Ozgok Y, Ross L, Niederberger C. Clomiphene Administration for Cases of Nonobstructive Azoospermia: A Multicenter Study. J Androl 2005; 26(6): 787-91.
Цель. Исследование методов лечения, направленных на увеличение количества сперматозоидов в эякуляте.
Материалы и методы. В исследовании использовали кломифен и рекомбинантный ФСГ в комбинации с хорионическим гонадотропином у 60 мужчин с бесплодием.
Результаты. Эффективность монотерапии кломифеном составила 20% в отношении зачатия и 63% в отношении олиготератозооспермии. Эффективность комбинированной терапии ХГЧ в сочетании с рекомбинантным ФСГ составила 40% в отношении зачатия и 87% в отношении олиготератозооспермии. Эффективность комбинированной терапии препаратом ФСГ и ХГЧ в случаях предшествующей неэффективности монотерапии ХГЧ и кломифеном в отношении олиготератозооспермии составила 65%.
Заключение. Наиболее эффективна комбинированная терапия препаратом ФСГ и ХГЧ. При этом исследованные виды стимулирующей терапии являются безопасными и не приводят к развитию побочных эффектов.
Актуальность. В течение последних 50 лет концентрация сперматозоидов в эякуляте здоровых мужчин, проживающих в технологически развитых странах, постоянно снижалась, при этом в большинстве случаев мужское бесплодие было связано со снижением количества и качества сперматозоидов [1]. В связи с этим часто возникает вопрос о необходимости применения методов лечения, направленных на увеличение количества сперматозоидов в эякуляте, в том числе и гормональной стимулирующей терапии.
В настоящий момент из препаратов для гормональной стимулирующей терапии используются: хорионический гонадотропин (ХГЧ), антиэстрогены, рекомбинантные препараты фолликулостимулирующего гормона (ФСГ), а также их комбинации [2, 3].
Цель: исследование эффективности и безопасности разных видов стимулирующей терапии у пациентов с патоспермией и бесплодием.
Материалы и методы исследования. В проспективное когортное исследование были включены 60 бесплодных мужчин с олигоастенотератозооспермией, сочетавшейся с нормальными или сниженными уровнями лютеинезирующего и фолликулостимулирующего гормонов. Критериями исключения являлись наличие в анамнезе травм или хирургических вмешательств на половых органах, криптозооспермия, азооспермия, любые формы обструктивного бесплодия, гипергонадотропный гипогонадизм, гипотиреоз, гиперпролактинемия, гиперкортицизм, нарушения кариотипа, делеции AZF, опухоли яичек, опухоли гипофиза, варикоцеле, урогенитальные инфекции, воспалительные заболевания половых желез, бактериоспермия, лейкоспермия, носительство антиспермальных антител. Включенные в исследование пациенты были рандомизированы в сопоставимые группы путем стратифицированной рандомизации, табл. 1.

Пациенты первой группы (группа кломифена, n=30) получали кломифена цитрат (Клостилбегит, «Эгис»; Венгрия) 50 мг перорально утром ежедневно. Пациенты второй (группа ХГЧ+ФСГ, n=30) получали комбинированную терапию препаратами Хорионический гонадотропин в индивидуально подобранной дозе, которая составила от 1000 до 3000 ЕД 1 раз в 3 дня внутримышечно и рекомбинантный препарат ФСГ (Гонал-Ф, «Мерк Сероно», Швейцария) в дозе 75 ЕД подкожно через день. Доза ХГЧ определялась путем оценки уровня общего тестостерона утром натощак после инъекции препарата (целевым значением являлось 20–33 нмоль/л).
Первичная эффективность лечения оценивалась через 3 месяца стимулирующей терапии. Под эффективностью терапии понималось наличие зачатия и/или устранение олиготератозооспермии. Пациенты, от которых наступило зачатие на фоне исследуемого лечения, в дальнейшее исследование не включались. Мужчины, от которых зачатие на фоне лечения не наступило, но было достигнуто устранение олиготератозооспермии, продолжили получать назначенную терапию еще 3 месяца с дальнейшей оценкой ее эффективности.
Кроме того, в исследовании оценивалась эффективность комбинированной терапии препаратами ХГЧ в сочетании с ФСГ, аналогичной той, которая применялось во второй группе, у 17 пациентов с первичной неэффективностью кломифена цитрата и монотерапии ХГЧ.
С целью оценки объема яичек проводилось ультразвуковое исследование на аппарате Aloka ProSound SSD-α 10 с использованием линейного датчика с частотой 10 МГц. При лабораторном обследовании состояния половых желез проводилось определение лютеинезирующего гормона (ЛГ), фолликулостимулирующего гормона (ФСГ), общего тестостерона и ингибина В в трех аликвотах сыворотки крови. Уровни ЛГ (норма 2,5–11,0 ЕД/л), ФСГ (норма 1,6–9,7 ЕД/л) и тестостерона (норма 12,0–33,3 нмоль/л) определялись на автоматическом анализаторе «Vitros ECi» (Johnson and Johnson [Великобритания]) методом усиленной хемилюминесценции, а уровни ингибина В (норма – 25–325 пг/мл) методом иммуноферментного анализа с использованием тест-системы DSL (США). Кровь для исследования забиралась в пробирки типа «вакутейнер» в утреннее время натощак из локтевой вены.
Оценка качества эякулята осуществлялась в соответствии с рекомендациями ВОЗ (2010 г.) путем световой микроскопии с помощью микроскопа Olimpus 41 CX (Япония) и камеры Маклера того же производителя. Учитывая, что на параметры спермограммы может влиять множество различных факторов, ее анализировали двухкратно (ориентировались на лучший результат) и оценивались наиболее «стабильные» показатели: количество сперматозоидов в 1 млн эякулята (норма – 15 млн и более), количество морфологически нормальных форм (норма – 4% и более [критерий Крюгера]), подвижность А+В (норма 40% и более). Кроме того, проводилось электронно-микроскопическое исследование эякулята (ЭМИС) путем центрифугирования, этаноловой, далее эпоксидной фиксации клеток эякулята с дальнейшим электронным микроскопированием х16000–18000 для исследования органоидов и х20000–25000 для исследования жгутиков. Оценивались: число интактных головок (норма >4%), содержание сперматозоидов с недостаточно конденсированным хроматином (норма <30%), содержание многоядерных сперматозоидов (норма <5%), содержение сперматозоидов с патологией акросомы (норма <20%), жгутика (норма <30%), деградирорвавших сперматозоидов. Забор эякулятата осуществлялся в стерильные контейнеры путем мастурбации (половое воздержание – 3–5 суток).
Статистическая обработка полученных данных была проведена с использованием пакета прикладных программ STATISTICA (StatSoft Inc. США, версия 8.0). Сравнение по количественным признакам осуществлялось непараметрическим методом с использованием U критерия Манна–Уитни для независимых групп, и теста Вилкоксона – для зависимых групп. Сравнение групп по качественным признакам осуществлялось непараметрическим методом путем анализа таблиц сопряженности с использованием точного критерия Фишера для независимых групп. Статистически значимыми считали различия при p<0,05.
Результаты и обсуждение. При одинаковых исходных данных пациентов проводимая стимулирующая терапия оказывала разный эффект в зависимости от выбранного препарата. Эффективность монотерапии препаратом кломифена представлена в табл. 2.

Терапия кломифеном наряду с увеличением уровня тестостерона, гонадотропинов и ингибина В, приводила не только к статистически значимому увеличению числа сперматозоидов в 1 мл эякулята, но и к статистически значимому улучшению их морфологии. При этом отмечалась тенденция к улучшению подвижности, однако различия не являлись статистически значимыми. Препарат устранил олиготератозооспермию у 73% пациентов (22 человека). Из них от 2 мужчин на 3-м месяце лечения наступило зачатие. Беременность окончилась естественными родами здоровых детей женского пола.
Таким образом, эффективность монотерапии кломифеном через 3 месяца в отношении олиготератозооспермии составила 73% (22 человека) и в отношении наступления зачатия – 7% (2 человека). Оставшиеся 8 пациентов были переведены на комбинированную терапию ХГЧ и рекомбинантным ФСГ. Двадцать человек, от которых не наступило зачатия, но отмечалось устранение олиготератозооспермии, продолжили терапию кломифеном в прежнем режиме и были повторно обследованы еще через 3 месяца, табл. 2.
На фоне продолжающейся еще 3 месяца терапии кломифена цитратом было выявлено дальнейшее статистически значимое увеличение уровней гонадотропинов и ингибина В при тенденции к увеличению уровня тестостерона, что сопровождалось улучшением подвижности сперматозоидов, но статистически значимых различий в отношении концентрации сперматозоидов или их морфологии дополнительно к промежуточной точке исследования (3 месяца) выявлено не было. Тем не менее еще от 4 пациентов на фоне 6 месяцев лечения кломифеном наступило зачатие. Беременности окончились естественными родами здоровых детей (три женского пола, один мужского).
У 13 пациентов зачатия достигнуто не было, но олиготератозооспермия была устранена, из них у 4 мужчин в анамнезе имелись дети. Таким образом, суммарная эффективность терапии кломифеном составила 20% (6 человек) в отношении зачатия и 63% (19 человек) в отношении олиготератозооспермии. Пациентам с устраненной олиготератозооспермией, но не достигшим зачатия, было рекомендовано использование вспомогательных репродуктивных технологий (ВРТ).
Терапия кломифеном являлась безопасной, нами не было выявлено побочных эффектов, однако на фоне продолжающейся терапии кломифеном у 3 пациентов было выявлено ухудшение достигнутых ранее показателей – персистирование олиготератозооспермии. Этим пациентам была рекомендована криоконсервировация эякулята и использование ВРТ.
Исследования других авторов, использовавших антиэстрогены для стимуляции сперматогенеза, были объеденены в мета-анализе, проведенном в 2013 г. [4]. В результате было показано, что использование антиэстрогенов приводило к статистически значимому повышению частоты наступления беременности по сравнению с контрольной группой. При этом отмечалось значительное увеличение концентрации сперматозоидов и их подвижности. Данные изменения сопровождались повышением сывороточных концентраций ФСГ и тестостерона. Не было отмечено существенной разницы в количестве нежелательных эффектов между группами, получавшими терапию антиэстрогенами и группами контроля. Таким образом, как результаты проведенного исследования, так и приведенный мета-анализ свидетельствуют о том, что антиэстрогены в качестве медицинской эмпирической терапии идиопатического мужского бесплодия могут обеспечить наступление спонтанной беременности, увеличить концентрацию сперматозоидов и их подвижность с низким риском несерьезных побочных эффектов. Это подтверждается и отечественными исследователями [5].
Хорошие результаты лечения также отмечались при использовании комбинированной терапии ХГЧ в сочетании с рекомбинантным ФСГ, табл. 3.
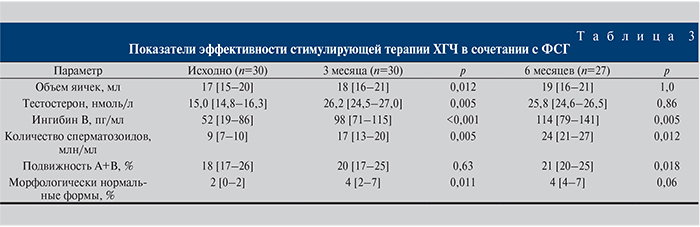
Комбинированная терапия гонадотропинами наряду с увеличением уровня тестостерона и ингибина В приводила как к статистически значимому увеличению числа сперматозоидов в 1 мл эякулята, так и статистически значимому улучшению их морфологии. На подвижность сперматозоидов лечение не повлияло. Препараты устранили олиготератозооспермию у 70% пациентов (21 человек). Из них от 3 мужчин на 3-м месяце лечения наступило зачатие. Беременности окончились естественными родами здоровых детей мужского пола.
Таким образом, эффективность комбинированной терапии через 3 месяца в отношении олиготератозооспермии составила 70% (21 человек) и в отношении наступления зачатия – 10% (3 человека). Пациенты с ненаступившим зачатием продолжили терапию гонадотропинами в прежнем режиме и были повторно обследованы еще через 3 месяца, табл. 3.
На фоне продолжающейся еще 3 месяца комбинированной терапии гонадотропинами у 9 мужчин с отсутствием олиготератозооспермии наступило зачатие, закончившееся рождением здоровых детей (5 женского, 4 – мужского пола), у 6 из этих мужчин в анамнезе имелись дети. Еще у 5 мужчин было отмечено устранение олиготератозооспермии, но зачатия не наступило (у 3 из этих мужчин в анамнезе также имелись дети). У 4 пациентов эффекта от лечения не отмечалось, олиготератозооспермия сохранялась.
Таким образом, суммарная эффективность комбинированной терапии гонадотропинами составила 40% (12 человек) в отношении зачатия и 87% (26 человек) в отношении олиготератозооспермии. Пациентам, не достигшим зачатия, было рекомендовано использование ВРТ. Комбинированная терапия гонадотропинами являлась безопасной, нами не было выявлено побочных эффектов, кроме нерезких тянущих болей в области яичек, на которые жаловались 4 пациента. Боли отмечались в начале лечения, купировались самостоятельно, не требовали отмены терапии и были связаны с увеличением объема яичек.
Другие исследователи, использовавшие терапию гонадотропинами для стимуляции сперматогенеза, также продемонстрировали хорошие результаты [6, 7]. Так, в исследовании М. А. Amirzargar и др. (2012) было показано, что комбинированная терапия препаратами ХГЧ в сочетании с ФСГ приводит к большему числу беременностей – 57%, нежели чем монотерапия ХГЧ – 32% [6]. К подобному выводу пришли и A.A. Sinisi и др. (2010), в исследовании которых было установлено, что использование рекомбинантного ФСГ у пациентов с гипогонадотропным гипогонадизмом, в дополнение к лечению ХГЧ способствует лучшей индукции сперматогенеза по сравнению с монотерапией последним [8]. Это подтверждается и результатами нашего исследования пациентов с первичной неэффективностью кломифена цитрата и монотерапии ХГЧ на фоне лечения комбинацией гонадотропинов, которые представлены в табл. 4.

Комбинированная терапия гонадотропинами, назначенная после использования других препаратов, привела как к статистически значимому увеличению уровня ингибина В, так и числа сперматозоидов в 1 мл эякулята, а также к статистически значимому улучшению их морфологии. На подвижность сперматозоидов лечение не повлияло. Препараты устранили олиготератозооспермию у 65% (11 человек) – у 5 из группы кломифена (62,5% от всех ранее получавших кломифен) и у 6 из группы ХГЧ (67% от всех ранее получавших монотерапию ХГЧ). Из этих пациентов у 3-х мужчин из группы кломифена и 3 из группы ХГЧ в анамнезе имелись дети. При этом от 2 мужчин из группы ХГЧ и от 1 из группы кломифена с устраненной олиготератозооспермией на 5-м и 4-м месяцах лечения, соответственно, наступило зачатие. Беременности окончились естественными родами здоровых детей женского пола. Всем пациентам с ненаступившим зачатием было рекомендовано использование ВРТ. Побочных эффектов при смене стимулирующей терапии не отмечено.
С целью уточнонения аспектов эффективности используемой терапии в отношении ее влияния на сперматогенез проведено сравнение мужчин с достигнутым эффектом от лечения (устранение олиготератозооспермии) и без такового, табл. 5.

Были выявлены статистически значимые различия в наличии детей в анамнезе, объеме яичек, уровне тестостерона, ингибина В и параметрах сперматогенеза. Все эти показатели в группе пациентов с недостигнутым эффектом были существенно хуже таковых в группе с хорошим результатом лечения. Следует отметить, что у пациентов с недостигнутым эффектом в большинстве случаев отмечалась тотальная тератозооспермия. Кроме того, при проведении ЭМИС было установлено, что у пациентов с отсутствием эффекта от стимулирующей терапии исходные показатели числа интактных головок, а также «конденсации» хроматина и патологии жгутиков статистически значимо хуже таковых по сравнению с больными, для которых лечение было эффективным. Полученные нами результаты подтверждаются другими авторами. Так, S. Belloc и соавт. (2014) в своем исследовании, посвященном изучению факторов риска и нарушению сперматогенеза при мужском бесплодии, пришли к выводу о том, что тератозооспермия является одним из наиболее негативных факторов, приводящих к невозможности спонтанного зачатия [9]. С ними согласены C. Krausz и C. Giachini (2007), которые также считают тератозооспермию одним из основных факторов риска мужского бесплодия [10].
Заключение. Проведенное нами исследование продемонстрировало, что все исследованные виды стимулирующей терапии приводят к повышению уровня тестостерона, ингибина В и концентрации сперматозоидов, являясь безопасными и не приводящими к развитию побочных эффектов. В отношении устранения олиготератозооспермии и достижения спонтанного зачатия наиболее эффективна комбинированная терапия гонадотропинами (ХГЧ в сочетании с ФСГ), при этом длительность лечения должна составлять 3–6 месяцев. Эта терапия может быть с успехом использована в случаях неэффективного лечения другими видами стимулирующей терапии.
1. The world Health Organization laboratory manual for the examination and processing of human semen – 5th ed. 2010; 271p.
2. Nieschlag E., Behre H.M., Nieschlag S. Andrology: Male reproductive health and disfunction. Springer-Verlag Berlin Heidelberg. 2010;629. ISBN: 978-3-540-78354-1.
3. Yang L., Zhang S.X., Dong Q., Xiong Z.B., Li X. Application of hormonal treatment in hypogonadotropic hypogonadism: more than ten years experience. Int. Urol. Nephrol. 2012; 44:393–399.
4. Chua M.E., Escusa K.G., Luna S., Tapia L.C., Dofitas B., Morales M. Revisiting oestrogen antagonists (clomiphene or tamoxifen) as medical empiric therapy for idiopathic male infertility: a meta-analysi. Andrology. 2013;1(5):749.
5. Bozhedomov V.A., Rokhlikov I.M., Tret’yakov A.A., Lipatova N.A., Vinogradov I.V., Nikonov E.L. Topical issues of helping couples with male factor childless marriage: clinical, organizational and methodological aspects. Andrologiya i genital’naya khirurgiya. 2013;4:4–13. Russian (Божедомов В.А., Рохликов И.М., Третьяков А.А., Липатова Н.А., Виноградов И.В., Никонов Е.Л. Актуальные вопросы оказания помощи парам с мужским фактором бездетного брака: клинические и организационно-методические аспекты. Андрология и генитальная хирургия. 2013;4:4–13).
6. Amirzargar М.А., Yavangi М., Basiri А., Babbolhavaeji Н., Amirzargar N., Moadabshoar L. Comparison of recombinant human follicle stimulating hormone (rhFSH), human chorionic gonadotropin (HCG) and human menopausal gonadotropin (HMG) on semen parameters after varicocelectomy: a randomized clinical trial. Iran J. Reprod. Med. 2012;10(5):441–452.
7. Zagarskikh E.Yu., Labygina A.V., Kurashova N.A. Experience in the treatment of normogonadotropic infertility in men. Urologiya. 2014;5:87–89. Russian (Загарских Е.Ю., Лабыгина А.В., Курашова Н.А. Опыт лечения нормогонадотропного бесплодия у мужчин. Урология. 2014;5:87–89).
8. Sinisi A.A., Esposito D., Bellastella G., Maione L., Palumbo V., Gandini L., Lombardo F., De Bellis A., Lenzi A., Bellastella A. Efficacy of recombinant human follicle stimulating hormone at low doses in inducing spermatogenesis and fertility in hypogonadotropic hypogonadism. J. Endocrinol. Invest. 2010;33(9):618–623.
9. Belloc S., Benkhalifa M., Cohen-Bacrie M., Dalleac A., Chahine H., Amar E., Zini A. Which isolated sperm abnormality is most related to sperm DNA damage in men presenting for infertility evaluation. J. Assist. Reprod. Genet. 2014;31(5):527–532.
10. Krausz C., Giachini C. Genetic risk factors in male infertility. Arch. Androl. 2007;53(3):125–133.
Автор для связи: Р.В. Роживанов – д.м.н., главный научный сотрудник отделения урологии и андрологии ФГБУ ЭНЦ Минздрава РФ; e-mal: rrozhivanov@mail.ru
Сведения об авторах:
Роживанов Р.В. – д.м.н., главный научный сотрудник отделения урологии и андрологии ФГБУ ЭНЦ Минздрава РФ, e-mal: rrozhivanov@mail.ru
Кравцова Н.С. – аспирант отделения урологии и андрологии ФГБУ ЭНЦ Минздрава РФ
Курбатов Д.Г. – д.м.н., профессор, заведующий отделением урологии и андрологии ФГБУ ЭНЦ Минздрава РФ
Внешний вид упаковки может отличаться от фотографии
Средняя цена в аптеках
692 ₽
Среди
6719
аптек,
подключенных к Ютеке в вашем регионе
Оплата и способы получения
в Москве
Самовывоз
Сегодня бесплатно
из 3809 аптек
Завтра или позже бесплатно
из 6719 аптек
Оплата картой или наличными в аптеке
Доставка
Конкретный срок и стоимость доставки зависят от вашего адреса
Информация о товаре
Действующее вещество:
Кломифен
Количество в упаковке:
10 шт.
Страна:
Венгрия
Страна производства может отличаться, проверяйте при получении заказа
Инструкция на Клостилбегит 50 мг, таблетки, 10 шт.
Состав
| Таблетки | 1 табл. |
| активное вещество: | |
| кломифена цитрат | 50 мг |
| вспомогательные вещества: желатин — 2 мг; магния стеарат — 2 мг; стеариновая кислота — 2 мг; тальк — 5 мг; крахмал картофельный — 39 мг; лактозы моногидрат — 100 мг |
Способ применения и дозы
Внутрь.
При бесплодии доза и продолжительность курса лечения зависят от чувствительности (реакции на препарат) яичников. Пациенткам с регулярным менструальным циклом рекомендуется начать лечение с 5-го дня цикла (или на 3-й день цикла при ранней овуляции или продолжительности фолликулярной фазы менее 12 дней). При аменорее лечение можно начинать в любой день.
Схема I. По 50 мг в день в течение 5 дней с одновременным контролем реакции яичников при помощи клинических и лабораторных исследований. Обычно овуляция происходит между 11-м и 15-м днем цикла. Если такое лечение не приводит к овуляции, следует применить схему II.
Схема II. С 5-го дня следующего цикла по 100 мг в сутки в течение 5 дней. Если в это время овуляция не наблюдается, следует еще раз повторить ту же схему (по 100 мг в день). В случае неудачи прием препарата следует прервать на 3 мес, а затем повторить лечение в течение 3 мес. При неэффективности второго курса последующее лечение препаратом неэффективно. Общее количество препарата, принимаемого на протяжении каждого курса, не должно превышать 750 мг.
При поликистозе яичников, в связи с тенденцией к гиперстимуляции, лечение следует начинать с дозы 50 мг в день.
При отсутствии менструаций в связи с длительным применением контрацептивов следует назначать по 50 мг в день, 5-дневный курс лечения обычно является результативным уже при первой попытке.
Мужчинам назначают по 50 мг 1–2 раза в день в течение 6 нед (необходим систематический контроль спермограммы).
Форма выпуска
Таблетки, 50 мг. По 10 табл. во флаконе коричневого стекла с ПЭ-крышкой с контролем первого вскрытия и амортизатором-гармошкой. 1 фл. в картонной пачке. По 10 табл. в блистере из ПВХ/ПВДХ/алюминиевой фольги. 1 блистер в картонной пачке.
Условия отпуска
Производитель
ЗАО «Фармацевтический завод ЭГИС». 1106, Будапешт, ул. Керестури, 30-38, Венгрия.
Тел.: (36 1) 803-55-55; факс: (36 1) 803-55-29.
Представительство ЗАО «Фармацевтический завод ЭГИС» (Венгрия) в Москве. 121108, Москва, ул. Ивана Франко, 8.
Тел.: (495) 363-39-66.
Характеристики
Торговое название
Клостилбегит
Действующее вещество (МНН)
Кломифен
Дозировка или размер
50 мг
Первичная упаковка
флакон темного стекла
Условия хранения
При температуре 15–25 °C
Представлено описание активных веществ лекарственного препарата. Описание препарата основано на официально утвержденной инструкции по применению от компании-производителя. Приведенное описание носит исключительно информационный характер и не может быть использовано для принятия решения о возможности применения конкретного лекарственного препарата.
Сертификаты Клостилбегит 50 мг, таблетки, 10 шт.
Все товары на сайте имеют сертификат соответствия.
Подробнее о гарантии
Цены в аптеках на Клостилбегит 50 мг, таблетки, 10 шт.
История стоимости Клостилбегит 50 мг, таблетки, 10 шт.
минимальнаясредняямаксимальная
Указана средняя стоимость товара в аптеках региона Москва и МО за период и разница по сравнению с предыдущим периодом
Цены Клостилбегит и наличие в аптеках в Москве
50 мг, таблетки, 10 шт.
09:30-19:00 Пн-Пт, 09:30-17:00 Сб-Вс
Достоинства: Поднял тестостерон с 11 до 22.5 нмоль/л. Принимал 25мг через день. Через 2 недели сдал анализы. ЛГ поднялся с 4 до 9.5. Эстрадиол так же вырос с 62 пмоль/л до 133. Перестали болеть колени
Недостатки: Никаких
Комментарий: Продолжу принимать
Недостатки: не помогли.
Комментарий: здоровье попортили хорошо
Достоинства: таблетки помогли поднять мужу СГ за месяц на 50% это просто чудо какое-то
Недостатки: нет
Смотреть все отзывы
Популярные товары в категории
Популярные товары в Ютеке
Купить Клостилбегит, 50 мг, таблетки, 10 шт. в Москве с доставкой в аптеку или домой, сделав заказ через Ютеку
Цена Клостилбегит, 50 мг, таблетки, 10 шт. в Москве от 587 руб. на сайте и в приложении
Подробная инструкция по применению Клостилбегит, 50 мг, таблетки, 10 шт.
Информация на сайте не является призывом или рекомендацией к самолечению и не заменяет консультацию специалиста (врача), которая обязательна перед назначением и/или применением любого лекарственного препарата.
Дистанционная торговля лекарственными препаратами осуществляется исключительно аптечными организациями, имеющими действующую лицензию на фармацевтическую деятельность, а также разрешение на дистанционную торговлю лекарственными препаратами. Дистанционная торговля рецептурными лекарственными препаратами, наркотическими и психотропными, а также спиртосодержащими лекарственными препаратами запрещена действующим законодательством РФ и не осуществляется.
На информационном ресурсе применяются
рекомендательные технологии
.
Медицинский препарат Кломифен цитрат широко используется в сфере репродуктологии для лечения бесплодия у женщин. В его состав входят антиэстрогенные компоненты. Основные зоны воздействия кломифен цитрата – гипоталамус и яичники.
Описание и воздействие на организм
Лекарственный препарат влияет на организм посредством стимуляции секреторной деятельности гонадотропинов. Он провоцирует повышение активности половых желез и способствует выработке гормонов в гипофизе. Кломифен также оказывает влияние на другие функции организма:
- Стимулирует молокоотделение.
- Оптимизирует процесс созревания яйцеклетки.
- Вызывает образование желтых тел в яичниках.
Все эти процессы способствуют созреванию яйцеклетки, готовой к процессу зачатия. В результате употребления лекарственного средства стабилизируется процесс овуляции. Если в организме содержится малое количество эстрогенов эндогенного типа, препарат увеличивает их количество, доводя общее число до нормы, необходимой для эффективного оплодотворения. Когда уровень эстрогенов повышается, Кломифен цитрат оказывает блокирующее действие, препятствуя их циркуляции. Подобное свойство медикамента способствует улучшению динамики гонадотропинов. Важным в применении препарата оказывается тот факт, что он не обладает андрогенным или гестагенным эффектом.
Применение
Благодаря своему фармакологическому действию, Кломифен цитрат рекомендуют в качестве эффективного стимулятора овуляции. Препарат оказывается актуальным не только для тех, кто столкнулся с диагнозом бесплодие, но и при маточных кровотечениях дисфункционального характера, нарушении функциональности яичников, отсутствии менструального цикла, а также при других патологических заболеваниях, которые провоцирует некорректное функционирование яичников и другие причины гормонального дисбаланса.
Кломифен цитрат нередко прописывают в качестве диагностического средства для определения нарушения функций гипофиза, которые влияют на стимулирование и динамику желез половых органов (гонадотропная функция гипофиза).
Сочетание с другими препаратами
Кломифен цитрат допустимо употреблять с другими препаратами, воздействующими на количество гонадотропных гормонов в организме. Таким образом можно обеспечить наиболее эффективное распространение медикамента по организму. Лекарственное средство постепенно выводится из организма женщины, но срок, который в медицине принято называть периодом полувыведения, составляет порядка 5 дней! В это время препарат проявляет максимальное действие. Употребление Кломифен цитрата в комплексе с другими препаратами рекомендуют при диагностировании новообразования в молочных железах и при раннем выявлении онкологических заболеваний.
Показания к применению
Кломифен цитрат можно использовать без привязки к приему пищи. Первый курс лечения предполагает дозировку в 50 мг/сутки (1 таблетка). Начало приема должно совпадать с 5 сутками менструального цикла. Первый курс лечения продолжается в течение пяти дней, после чего употребление препарата прекращается. На 11-й день цикла (реже 15-й) должна наступить овуляция. В случае если этого не происходит, врачи рекомендуют повторный курс лечения. Дозировка увеличивается в два раза (100мг в сутки) и пациентка принимает препарат в течение 6 дней. Если овуляция не наступила, необходимо сделать трехмесячный перерыв, после чего приступить к третьему курсу. В 85% случаев эти методы помогают добиться желаемого результата, а в противном случае, врач на основании показаний анализов делает выводы об эффективности препарата и предлагает новые методы лечения.
Существует иной вариант курса лечения, который предлагают при диагностировании рака молочной железы. Женщинам, которые столкнулись с диссеминированным раком, который характеризует распространение пораженных клеток в другие органы и ткани, назначают годовой курс лечения, подразумевающий прием Кломифен цитрата на протяжении 12 месяцев. Дозировка составляет 200 мг/сутки (4 таблетки по 50мг). В это время необходимо контролировать функционирование яичников и регулярно проходить обследования у лечащего врача. Если в работе яичников происходят сбои, прохождение курса приостанавливают и после возобновления функционирования продолжают лечение.
Терапия с использованием Кломифен цитрата является актуальной и при мужских заболеваниях. Представителям сильного пола назначают курс лечения с дозировкой по 50-100 мг/в день (в зависимости от веса и возраста). Курс лечения сопровождается строгим контролем качественного состава спермы и результатов необходимых исследований. Препарат употребляют в течение шести недель.
Противопоказания
Кломифен цитрат противопоказан беременным женщинам, а также пациентам, у которых диагностировано наличие злокачественных и доброкачественных новообразований. Кроме того, применение медикамента запрещают при:
- Наличии сопутствующих заболеваний.
- Болезнях нервной системы.
- Печеночной или почечной недостаточности.
- Склонности к образованию тромбов.
Употребление препарата не рекомендуют людям, профессиональная деятельность которых связана со стрессами и серьезными психоэмоциональными нагрузками.
Специалисты нашей клиники «Центр ЭКО» в Екатеринбурге предоставляют полную консультацию по действию Кломифен цитрата и возможным реакциям организма, которые зависят от индивидуальных предрасположенностей.
Здесь вы сможете пройти обследования, узнать результаты анализов и получить медицинские предписания, актуальные для вашей ситуации.
При лечении бесплодия, а также опухолей и других заболеваний, главным фактором успешного лечения является своевременная диагностика! Внимание к собственному самочувствию, а также обращение к профильному врачу поможет вам получить объективную информацию о заболевании и восстановить здоровье, избежав неприятных последствий.
