Антихеликобактерная терапия: сегодня и завтра
Статьи
Опубликовано в издании:
«МЕДИЦИНСКИИ ВЕСТНИК » 2009, № 31/500. Клацид (кларитромицин) — антибактериальный препарат, входящий в первую линию терапии язвенной болезни желудка и 12-перстной кишки по всем существующим Европейским и Российским рекомендациям. Как выглядит эволюция подходов к антихеликобактерной терапии, почему именно Клацид, амоксициллин и омепразол на протяжении многих лет занимают первые позиции в лечении язвенной болезни желудка и 12-перстной кишки, а также новости антихеликобактерной терапии обсуждались на симпозиуме «Антихеликобактерная терапия: сегодня и завтра», который проходил в рамках пятнадцатой гастроэнтерологической недели 14 октября 2009 года под председательством В.Т. ИВАШКИНА и И.В. МАЕВА.
Эволюция подходов к антихеликобактерной терапии. От случайных открытий до III Маастрихтского соглашения.
Человечество всю свою историю борется с различными болезнями. Эволюционируют взгляды на причины возникновения и лечение различных заболеваний. Профессор кафедры пропедевтики внутренних органов и гастроэнтерологии МГМСУ И.В. Маев рассказал в своем докладе о том, как сложно порой ввести во врачебную практику новые идеи. Впервые бактерию, похожую на Helicobacter pylori, обнаружили немецкие ученые в слизистой оболочке желудка человека в 1875 году. Через 24 года польский профессор Валерий Яворский предположил патогенетическую роль этого микроорганизма в развитии заболеваний желудка. Однако следующие работы по изучению этой бактерии в связи с заболеваниями желудка были проведены лишь в 1983 году (84 года спустя). Чтобы доказать, что H. pylori вызывает язву желудка, одному из исследователей, Барри Маршалу, пришлось выпить суспензию этих бактерий и долго лечить полученный острый гастрит. Это позволило ему стать автором первой эффективной антихеликобактерной терапии (висмута субсалицилат + метронидазол, 14 дней). Профессор Маев отметил, что подвиги Барри Маршала были вознаграждены: он и его коллега Робин Уоррен получили Нобелевскую премию по медицине за открытие бактерии Helicobacter pylori и исследование ее роли при гастрите и язве желудка.
После того как стало ясно, что большинство язв желудка и гастритов с повышенной кислотностью вызываются H. pylori, были разработаны схемы диагностики и лечения этой инфекции. На сегодняшний день известно, что с H. pylori связано 95% случаев хронического гастрита типа В, 80—85% случаев язвенной болезни желудка, 90% случаев рака желудка и 90% случаев MALT-лимфомы желудка. III Маастрихтское соглашение предусматривает, что следует проводить обследование на наличие H. pylori и антихеликобактерную терапию при длительном приеме НПВП и ингибиторов протонной помпы, ишемической болезни сердца, иммунной тромбоцитопении и железодефицитной анемии, необъяснимой другими причинами.
Антихеликобактерная терапия: почему кларитромицин?
Основной схемой эрадикации 1-й линии является тройная терапия: ингибитор протонной помпы (ИПП), кларитромицин (Клацид) и амоксициллин (или метронидазол). В качестве схемы эрадикации 2-й линии сохранила свое значение квадротерапия: ИПП, тетрациклин, метронидазол и препараты висмута. Эта схема эффективна и в случаях резистентности штаммов H. pylori к метронидазолу. Выбор препарата для резервных схем определяется результатами бактериологического исследования с определением чувствительности, в том числе и к препаратам первых линий, использовавшимся ранее.
Выбор Клацида для первой линии антихеликобактерной терапии объясняется целым рядом причин: его высокой биодоступностью, не зависящей от приема пищи; хорошей переносимостью и высокой кислотоустойчивостью. Клацид проявляет синергизм с ингибиторами протонной помпы у 91% изученных штаммов H. pylori и эффективно санирует ткани пародонта при их контаминации этим микроорганизмом у больных язвенной болезнью. Среди прочих макролидов Клацид имеет самую низкую (0,03 мкг/ мл) минимальную подавляющую концентрацию в отношении H. pylori и обладает высокой способностью проникать в клетки и накапливаться в слизистой оболочке желудка и 12-перстной кишки. Он обеспечивает самую высокую степень эрадикации в сравнении с монотерапией любым другим антибиотиком. Схема, в которую входит Клацид (оригинальный кларитромицин), обеспечивает самую высокую степень эрадикации H. pylori — 95%. А сочетание в антихеликобактерной терапии Клацида и препаратов висмута позволяет эффективно воздействовать даже на штаммы H.pylori, устойчивые к этому антибиотику.
Профессор И.В. Маев подчеркнул, что высокая эффективность эрадикационных схем, включающих Клацид, возможно, объясняется дополнительными, «неантибиотическими» свойствами этого препарата. Так, Клацид проявляет противовоспалительную активность, снижая синтез медиаторов воспаления, а совсем недавно было открыто новое свойство Клацида — разрушать матрикс биопленки, образуемый H. pylori.
Порой микроорганизмы повышают свою устойчивость к антибиотикам различными путями: изменяют мишень, на которую действует антибиотик, уменьшают проницаемость клеточной стенки для антибиотиков и вырабатывают специальный механизм выброса антибиотиков.
Профессор кафедры пропедевтики внутренних болезней и гастроэнтерологии МГМСУ А. А. Самсонов затронул тему резистентности H. pylori к кларитромицину и другим компонентам эрадикационной терапии. Эта проблема крайне актуальна для ряда европейских стран и американского континента. В то же время в России макролидные антибиотики и, в частности, кларитромицин назначаются в разы реже. В частности, в 2002 г. объем назначения макролидов в США был в 20 раз выше, чем в России в 2009.
Профессор А.А. Самсонов также подчеркнул, что не всегда данные о резистентности, продемонстрированные в исследованиях in vitro, соответствуют реальной клинической практике. Это связано с особенностями фармакокинетики и фармакодинамики препаратов в организме человека: высокими тканевыми концентрациями, наличием активных метаболитов, лекарственного взаимодействия, различными точками приложения, определяющими синергизм in vivo, и др. В ходе доклада были предложены следующие пути профилактики и преодоления резистентности к кларитромицину, в частности: адекватное лечение больных, которые лечатся впервые; использование последовательной схемы терапии с кларитромицином; применение препаратов висмута или более мощных схем лечения больных с резистентными штаммами; семейная терапия (ликвидация возможности обмена резистентными штаммами).
Профессор А.А. Самсонов резюмировал свой доклад информацией о том, что резистентность к кларитромицину сегодня составляет 13,8%, что значительно ниже критического порога. При столь благополучных данных по резистентности к кларитромицину его эффективность оставляет данный антибиотик именно препаратом первой линии, так как антихеликобактерные схемы, включающие Клацид, обеспечивают наивысший процент эффективности — 80—95%.
Недавно открытому эффекту влияния Клацида на биопленки был посвещен доклад Т.Л. Лапиной из клиники пропедевтики внутренних болезней, гастроэнтерологии и гепатологии им. В.Х. Василенко ММ А им. И.М. Сеченова. Одним из способов защиты бактерий от иммунной системы и других факторов внешней среды является формирование сообщества бактерий, которое получило название биопленки. H. pylori формирует в желудке биопленку, что объясняет высокую устойчивость этого микроорганизма к антибактериальным препаратам.
Клацид способен разрушать матрикс биопленки, более того, оказалось, что Клацид разрушает биопленку даже у штаммов, которые устойчивы к нему как к антибиотику. Клацид потенцирует активность других антибиотиков, поскольку нарушает один из механизмов защиты бактерий. Клацид — единственный антибиотик для эрадикации, разрушающий матрикс биопленки. Может, и в этом секрет столь высокой степени эрадикации именно в схемах с использованием Клацида?
Все докладчики рекомендовали отказаться от использования дженериков в пользу хорошо зарекомендовавших себя лекарственных форм ведущих производителей, поскольку такая тактика обеспечивает максимальный эффект при минимальной вероятности проявления побочных эффектов препаратов. Так, исследование более чем 65 дженериков кларитромицина из 18 стран мира (фромилид и др.) показало, что 20% исследованных дженериков не содержат указанного на упаковке количества активного кларитромицина, 68% дженериков высвобождают меньшее количество активного кларитромицина по сравнению с Клацидом, у 98% дженериков в содержании обнаружилось количество примесей, значительно превышающее возможное, что является опасным для пациента.
В финале симпозиума после заданных вопросов профессора резюмировали доклады и пришли к совместному выводу о том, что Клацид продолжает оставаться препаратом первой линии терапии язвенной болезни желудка и 12-перстной кишки, так как схемы, включающие Клацид, обеспечивают наибольшую эффективность эрадикации: 80—95%.
При этом Клацид обладает противовоспалительным эффектом и является единственным антибиотиком для эрадикации, разрушающим матрикс биопленки.
Ярослав Андреев
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)

В.И. ПОПАДЮК, д.м.н., профессор, А.И. ЧЕРНОЛЕВ, к.м.н., И.А. КОРШУНОВА, к.м.н., Российский университет дружбы народов, Москва
Патология полости носа и околоносовых пазух воспалительного характера является одной из самых актуальных в современной оториноларингологии. Среди пациентов, находящихся на стационарном лечении в оториноларингологических отделениях, воспалительные заболевания околоносовых пазух составляют до 36%. Современные макролиды (прежде всего кларитромицин и азитромицин) относятся к числу наиболее часто применяемых в амбулаторной практике антибиотиков. Возрождение интереса к макролидным антибиотикам было обусловлено возросшим клиническим значением в инфекционной патологии внутриклеточных патогенов, в отношении которых макролиды демонстрировали беспрецедентную активность.
Риносинуситом называют воспаление слизистой оболочки полости носа и околоносовых пазух [1]. Основными возбудителями острого бактериального риносинусита считаются Streptococcus pneumoniae и Haemophilus influenzae. Среди прочих возбудителей называют Moraxella catarrhalis, Staphylococcus aureus, Streptococcus pyogenes, Streptococcus viridans и др. Основными анаэробными возбудителями риносинусита являются анаэробные стрептококки [1, 6, 7]. Однако спектр возбудителей острого бактериального риносинусита может существенно варьировать в зависимости от географических, социально-экономических и прочих условий. Перечень возбудителей внутрибольничных, развившихся на фоне иммунодефицитных состояний и одонтогенных риносинуситов, наряду с упомянутыми выше бактериями, включает Staphylococcus epidermidis, Proteus, а также сапрофитные бактерии и грибковую микрофлору. В последние годы обсуждается роль хламидий и другой атипичной микрофлоры в этиологии риносинусита [2—5].
Пусковым моментом в развитии острого бактериального риносинусита обычно бывает ОРВИ. Выявлено, что почти у 90% больных ОРВИ в околоносовых пазухах выявляются изменения в виде отека слизистой оболочки и застоя секрета. Однако лишь у 1—2% таких больных развивается острый бактериальный риносинусит.
В развитии хронического риносинусита, помимо нарушений мукоцилиарного транспорта, важную роль играют аномалии строения внутриносовых структур и решетчатого лабиринта, блокирующие проходимость естественных отверстий околоносовых пазух и нарушающие механизмы очищения пазух [1, 6, 7]. Наличие двух или более соустий верхнечелюстных пазух также создает условия для заброса уже побывавшей в полости носа и инфицированной слизи обратно в пазуху. В условиях хронического воспаления в слизистой оболочке происходит очаговая или диффузная метаплазия многорядного цилиндрического эпителия в многослойный, лишенный ресничек и утративший способность удалять со своей поверхности бактерии и вирусы путем активного мукоцилиарного транспорта [1].
В настоящее время для лечения синуситов активно применяются антибиотики группы макролидов. Всего известно более 20 макролидов. Основу химической структуры макролидов составляет макроциклическое лактонное кольцо, связанное с одним или несколькими углеводными остатками. В зависимости от числа атомов углерода в гетероциклической структуре макролидные антибиотики подразделяются на 14-членные (природные — эритромицин, олеандомицин, полусинтетические — кларитромицин, рокситромицин, диритромицин), 15-членные (азалиды) — азитромицин (полусинтетический препарат) и 16-членные — природные (спирамицин, джозамицин) и полусинтетические (рокитамицин и мидекамицин).
Современные макролиды, прежде всего кларитромицин и азитромицин, относятся к числу наиболее часто применяемых в амбулаторной практике антибиотиков. В США в период с 1992 по 2000 г. было отмечено 4-кратное возрастание частоты назначений кларитромицина на фоне сокращения использования аминопенициллинов и эритромицина [3, 4]. Негативным эффектом широкого использования данной группы антибиотиков является повсеместный рост устойчивости к макролидам у возбудителей внебольничных инфекций [5—7].
Кларитромицин в экспериментах in vitro уступает азитромицину по активности в отношении Haemophilus influenzae, однако in vivo его антибактериальное действие усиливается за счет активного метаболита 14-гидрокси-кларитромицина. Препарат демонстрирует также наилучший эффект при инфекции, вызванной метициллиночувствительными штаммами S. aureus. И наконец, устойчивость кларитромицина в кислой среде эндосом повышает активность препарата в отношении таких внутриклеточных паразитов, как Legionella pneumophila и Chlamydophila pneumoniae. Препарат демонстрирует высокую и сравнимую с другими макролидами активность в отношении Mycoplasma pneumoniae. Грамотрицательные бактерии семейства Enterobacteriaceae, Pseudomonas и Acinetobacter обладают природной устойчивостью ко всем макролидным антибиотикам [6]. Бета-лактамазы не влияют на активность кларитромицина.
Нами было проведено открытое сравнительное рандомизированное клиническое испытание эффективности, переносимости и безопасности лекарственного средства Экозитрин, таблетки, покрытые оболочкой 500 мг, производства ОАО «АВВА РУС» (Россия) и оригинального лекарственного средства Клацид, таблетки, покрытые оболочкой 500 мг, производства Abbott S.r.l. (Италия) у пациентов, страдающих острым бактериальным синуситом и обострением хронического синусита средней степени тяжести в параллельных группах пациентов с активным контролем. Экозитрин, помимо кларитромицина, содержит пребиотик лактулозу. Лактулоза является синтетическим дисахаридом, молекула которого состоит из остатков галактозы и фруктозы. Лактулоза в желудке и верхних отделах кишечника не всасывается и не гидролизуется. Высвобождающаяся из таблеток Экозитрина лактулоза в качестве субстрата ферментируется нормальной микрофлорой толстого кишечника, стимулируя рост бифидобактерий и лактобацилл. В результате гидролиза лактулозы в толстом кишечнике образуются органические кислоты — молочная, уксусная и муравьиная, подавляющие рост патогенных микроорганизмов и уменьшающие вследствие этого продукцию азотсодержащих токсических веществ [9]. Таким образом, лактулоза в составе Экозитрина оказывает протективное действие на нормальную микрофлору кишечника, уменьшает явления интоксикации и нивелирует риск развития побочных эффектов, связанных с дисбиозами. Кроме того, существует ряд данных, позволяющих предполагать участие некоторых пребиотиков (в т. ч. и лактулозы) в повышении иммунного ответа [10].
Лактулоза, входящая в состав Экозитрина, не оказывает влияние на основные фармакокинетические параметры, характеризующие биодоступность кларитромицина.
Целью нашего исследования являлась оценка сравнительной эффективности, переносимости и безопасности лекарственного средства Экозитрин и оригинального лекарственного средства Клацид у пациентов с острым бактериальным синуситом и обострением хронического синусита средней степени тяжести.
В обеих сформированных группах проводилась терапия по одинаковой схеме: внутрь по 500 мг (Экозитрин или Клацид) 2 раза в день через 12 ч в течение 10 дней. Продолжительность участия пациента в испытании не менее 24 дней. Из них: период пребывания в стационаре составлял 10 дней (период лечения) и последующее наблюдение — 14 дней.
Критериями включения в исследование были:
1) возраст 18—65 лет,
2) клинически, лабораторно и инструментально верифицированный диагноз острого бактериального синусита или обострения хронического синусита средней степени тяжести любой локализации с гнойным или слизисто-гнойным отделяемым,
3) способность пациента выполнять предписания врача и соблюдать необходимые рекомендации,
4) Наличие подписанного информированного согласия пациента.
Количество скринированных пациентов — 61 (30 человек в основной и 31 — в контрольной группе). Количество рандомизированных пациентов — 61 (30 человек в основной и 31 — в контрольной группе). Включено в анализ эффективности — 60 (30 человек в основной и 30 — в контрольной группе). Включено в анализ безопасности — 61 (30 человек в основной и 31 — в контрольной группе).
Критерии эффективности были установлены следующие:
— показатель клинической эффективности определялся по оценке клинических симптомов заболевания на момент начала лечения и на момент окончания лечения на основании:
— субъективной оценки пациента: наличие выделений из носа, заложенности носа, умеренной боли (чувства давления, наполнения) в области лица и периорбитальных областях, которая может также проявляться локализованной или диффузной головной болью,
— объективных данных клинического осмотра: наличие лихорадки, признаков воспалительного процесса в ОНП по данным риноскопии;
— динамика уровня лейкоцитов крови, показателей лейкоцитарной формулы, СОЭ, СРБ;
— динамика показателей рентгенографического исследования;
— процент пациентов с клиническим выздоровлением в каждой группе;
— процент пациентов с клинической неэффективностью;
— процент пациентов с клиническим рецидивом либо обострением в каждой группе;
— процент пациентов с неопределенным результатом.
Открытое сравнительное рандомизированное клиническое испытание эффективности и безопасности в параллельных группах пациентов с активным контролем проводилось до достижения 60 законченных случаев лечения пациентов с острым бактериальным синуситом и обострением хронического синусита средней степеней тяжести.
Средний возраст пациентов составил 36,8 ± 14,1 года в группе 1 (Экозитрин) и 35,0 ± 15,0 года в группе 2 (Клацид), р = 0,484. В исследование были включены 12/30 (40,0%) мужчин и 18/30 (60,0%) женщин, которые были рандомизированы в группу 1, и 15/31 (48,4%) мужчин и 16/31 (51,6%) женщин, которые были рандомизированы в группу 2. По представленным данным статистически значимых различий между группами лечения выявлено не было.
Клиническое выздоровление определяли согласно протоколу как полное исчезновение всех субъективных и объективных клинических признаков заболевания (лихорадка, головная боль, болезненность при пальпации, заложенность носа, гнойное отделяемое, изменения лабораторных показателей крови) после завершения антимикробной терапии и в отдаленный период. На рентгенограмме на 10-й день отсутствует затемнение и горизонтальные уровни жидкости в пазухах, может сохраняться пристеночное затемнение.
Клиническую неэффективность определяли как отсутствие улучшения состояния пациента после 72-часового лечения или невозможность продолжать лечение из-за серьезных нежелательных явлений. Рецидив определяли как повторное появление клинической картины заболевания или возникновение новых клинических проявлений синусита в первые 14 дней после завершения лечения.
Неопределенный результат констатировали, если по тем или иным причинам не удавалось интерпретировать результаты лечения как эффективность или неэффективность.
На момент окончания исследования клиническое выздоровление наблюдалось у 24/30 (80%) пациентов в группе 1 и у 26/30 (86,7%) пациентов в группе 2. Неопределенный результат наблюдался у 6/30 (20%) пациентов в группе 1 и у 4/30 (13,3%) пациентов в группе 2. Случаев клинической неэффективности не наблюдалось. Случаев рецидива заболевания не наблюдалось. Отношение шансов для клинического выздоровления составило 0,62 (95% ДИ от 0,15 до 2,45). Отношение шансов для неопределенного результата составило 1,63 (95% ДИ от 0,41 до 6,47). Статистически значимых различий по эффективности терапии между основной и контрольной группами выявлено не было (табл. 1).
| Таблица 1. Оценка эффективности | ||||
| Параметр |
Группа 1 Экозитрин (n = 30) |
Группа 2 Клацид (n = 30) |
Размер эффекта, ОШ (95% ДИ) |
р-величина |
| Клиническое выздоровление | 24 (80%) | 26 (86,7%) | 0,62 (от 0,15 до 2,45) | 0,729 |
| Неопределенный результат | 6 (20%) | 4 (13,3%) | 1,63 (от 0,41 до 6,47) | 0,729 |
| Клиническая неэффективность | 0 (0%) | 0 (0%) | — | — |
Статистически значимые различия по изменению показателей общего анализа крови (ОАК) на последнем визите по отношению к первому в группе 1 наблюдались по показателям: СОЭ (р = 0,001), лейкоциты (р = 0,002), нейтрофилы палочкоядерные (р = 0,012). Статистически значимые различия по изменению показателей ОАК на последнем визите по отношению к первому в группе 2 наблюдались по показателям: СОЭ (р < 0,001), моноциты (р < 0,001), нейтрофилы сегментоядерные (р = 0,026). Полученные результаты можно объяснить положительной динамикой состояния пациентов и нормализацией значений показателей ОАК во время лечения. Статистически значимые различия по изменению показателей ОАК на последнем визите по отношению к первому между группами 1 и 2 наблюдались по показателю процента моноцитов (р = 0,003), по остальным показателям ОАК статистически значимые различия отсутствовали (табл. 2).

Эти изменения, возможно, связаны с эффектами лактулозы, входящей в состав препарата Экозитрин, поскольку, как уже упоминалось, существует ряд данных об иммуномодулирующем действии лактулозы. Так, большой интерес представляют данные о стимуляции лактулозой В-лимфоцитов MALT-системы (отдельные клеточные лимфоидные элементы, ассоциированные со слизистой оболочкой), в результате чего повышается продукция секреторного IgA, в то же время ингибируется синтез ФНО-α (фактор некроза опухоли-альфа) макрофагами и Т-лимфоцитами. Последнее может быть связано с подавлением механизмов транслокации бактерий, а также с упомянутым выше сокращением количества Еnterobacteriaceae, что уменьшает образование внутрипросветного и системного эндотоксина [11—15]. Противовоспалительные эффекты лактулозы были исследованы и на некоторых моделях животных с интестинальным воспалением. У мыши с генетически обусловленным дефицитом IL-10 спонтанно развивается колит. Сразу после рождения модифицированные мыши имеют пониженный уровень лактобацилл в толстом кишечнике. Пероральное введение лактулозы приводило к нормализации количества лактобацилл в фекалиях и предупреждало развитие колита [16]. Изучения на животных и данные, полученные в клеточной культуре in vitro, подтвердили возможность определенных пребиотиков (в т. ч. и лактулозы) препятствовать воспалительным и злокачественным процессам в толстом кишечнике [17]. Предполагается, что использование пребиотиков (лактулозы), способствует стимуляции синтеза короткоцепочечных жирных кислот (кишечной формы ассоциированной с лимфоидной тканью) которые могут оказывать влияние на иммунную модуляцию благодаря способности увеличивать продукцию IL-10 и TGF-β1, которые являются противовоспалительными цитокинами, играющими важную роль в уменьшении аллерген-индуцируемых ответов [17]. Недавние исследования на крысах также показали, что пробиотики увеличивают выработку кишечных противовоспалительных цитокинов (таких, как IL-10 и TGF-β1), уменьшая при этом выработку провоспалительных цитокинов, а пребиотики (лактулоза) могут способствовать усилению данного эффекта [18]. В ряде клинических исследований было показано, что дети, получавшие пребиотики, по сравнению с плацебо, имели меньшее количество различных диагнозов и эпизодов инфекции верхних отделов респираторного тракта и меньше случаев назначения антибиотков [19, 20]. Данные исследования свидетельствуют о положительном влиянии пребиотических продуктов (лактулозы) на иммунную систему.
Нельзя исключить, что эффекты лактулозы суммируются с иммуномодулирующим действием кларитромицина. В экспериментальных моделях [21] было показано, что при внутривенном применении сывороточные концентрации кларитромицина близки к 10 мкг/мл, что является существенной предпосылкой подавления ядерного фактора каппа B (NFkB) in vitro , который регулирует гены провоспалительных цитокинов и экспрессию фактора некроза опухоли (TNF-α). По сравнению с группой контроля значительно снижается содержание сывороточного TNF-α и оксидантный статус у животных, получавших кларитромицин. При этом ранний апоптоз моноцитов крови связан с благоприятным исходом.
Выявленные в нашем исследовании изменения содержания моноцитов представляют научный и клинический интерес и требуют дальнейших исследований.
Статистически значимых различий между группами 1 и 2 по показателю СРБ на первом и последнем не наблюдалось. В обеих группах наблюдалось статистически значимое снижение уровня СРБ на последнем визите по отношению к первому (р < 0,001).
Статистически значимых различий между группами 1 и 2 по показателям рентгенологического исследования (наличие горизонтального уровня жидкости или пристеночного затемнения в околоносовых пазухах) на первом визите и последнем не наблюдалось. В обеих группах наблюдалось статистически значимое различие по показателям «Наличие горизонтального уровня жидкости в околоносовых пазухах» (р = 0,003 в группе 1) и «Наличие пристеночного затемнения в околоносовых пазухах» (р < 0,001 и р = 0,015 соответственно) на последнем визите по отношению к первому.
Длительность воздействия препарата
Полный курс применения исследуемого препарата и препарата сравнения по протоколу составил 10 дней. За период исследования кумулятивная доза препарата Экозитрин составила 9,9±0,28 г, кумулятивная доза препарата Клацид составила 9,7 ± 0,70 г. Более детальная информация по кумулятивной дозе препаратов исследования представлена в таблице 3.
| Таблица 3. Препараты исследования. Кумулятивная доза | ||
| Категория |
Группа 1 Экозитрин (n = 30) |
Группа 2 Клацид (n = 31) |
| N | 30 | 31 |
| Среднее, г | 9,90 | 9,70 |
| Медиана, г | 10,0 | 10,0 |
| Минимум, г | 9,00 | 7,00 |
| Максимум, г | 10,5 | 10,5 |
| 25 процентиль, г | 10,0 | 9,50 |
| 75 процентиль, г | 10,0 | 10,0 |
| Ст. откл., г | 0,28 | 0,70 |
За время исследования изменения дозы или перерыва в назначении препарата в группе Экозитрина не отмечено, в группе Клацида один пациент (3,2%) прекратил прием препарата по причине появления диспептических явлений после 7-го дня терапии.
Таким образом, статистически значимых различий по переносимости препарата, по нашему мнению, между основной и контрольной группами выявлено не было. Подробная информация представлена в таблице 4. Хорошая переносимость была отмечена у 17/30 (56,7%) пациентов в группе 1 и у 15/31 (48,4%) пациентов во группе 2. Удовлетворительная переносимость была отмечена у 13/30 (43,3%) пациентов в группе 1 и у 15/31 (48,4%) пациентов в группе 2. Неудовлетворительная переносимость была отмечена у 1 человека (3,2%) в группе 2.
| Таблица 4. Общее заключение исследователя о переносимости препарата | |||
| Параметр |
Группа 1 Экозитрин (n = 30) |
Группа 2 Клацид (n = 31) |
р-величина |
| Хорошая | 17 (56,7%) | 15 (48,4%) | 0,517 |
| Удовлетворительная | 13 (43,3%) | 15 (48,4%) | 0,692 |
| Неудовлетворительная | 0 (0%) | 1 (3,2%) | 1 (3,2%) |
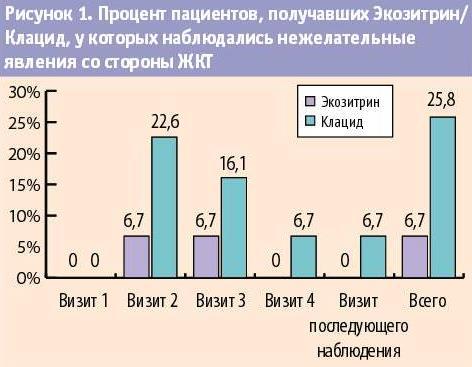
В ходе исследования одно нежелательное явление было зарегистрировано в группе Экозитрина — у 13/30 (43,3%) пациентов, в группе Клацида — у 16/31 (51,6%) пациентов. Чаще всего нежелательные явления, зарегистрированные в ходе исследования, были связаны с изменениями лабораторных показателей. В группе 1 данные нежелательные явления отмечались у 7/30 (23,3%) пациентов и у 8/31 (25,8%) пациентов в группе Клацида. Кроме того, были зарегистрированы нарушения со стороны желудочно-кишечного тракта, крови и лимфатической системы, почек и мочевыводящих путей, сердца. Следует отметит
ь, что у пациентов, получавших Экозитрин, нежелательные явления со стороны желудочно-кишечного тракта наблюдались в 4 раза реже. Так, нежелательные явления в основной группе были зарегистрированы только у 2 пациентов (6,7%), в то время как в группе пациентов, получавших Клацид — у 8 человек (25,8%). Этот факт может свидетельствовать о более высоком профиле безопасности Экозитрина в сравнении с Клацидом в отношении развития симптомов дисбактериоза кишечника в условиях курсового приема антибиотиков (табл. 5, рис. 1). Из нежелательных явлений большинство имело легкую степень тяжести. Большая часть нежелательных явлений имела как минимум возможную связь с исследуемым препаратом.
| Таблица 5. Количество пациентов, получавших Экозитрин/Клацид, у которых наблюдались нежелательные явления со стороны ЖКТ | ||
|
Группа 1 Экозитрин (n = 30) x/N (%) пациентов |
Группа 2 Клацид (n = 31) x/N (%) пациентов |
|
| Визит 1 | 0/30 (0%) | 0/31 (0%) |
| Визит 2 | 2/30 (6,7%) | 7/31 (22,6%) |
| Визит 3 | 2/30 (6,7%) | 5/31 (16,1%) |
| Визит 4 | 0/30 (0%) | 2/30 (6,7%) |
| Визит последующего наблюдения | 0/30 (0%) | 2/30 (6,7%) |
| Всего | 2/30 (6,7%) | 8/31 (25,8%) |
Результаты проведенного исследования позволили сделать следующие выводы:
Эффективность исследуемого препарата Экозитрин сопоставима с эффективностью препарата Клацид у пациентов с острым бактериальным синуситом и обострением хронического синусита средней степени тяжести. Полученные данные позволяют сделать вывод об удовлетворительном профиле безопасности и переносимости препарата Экозитрин в сравнении с препаратом Клацид. Более того, результаты исследования дают основания говорить о более высоком профиле безопасности Экозитрина в сравнении с Клацидом в отношении развития симптомов дисбактериоза кишечника в условиях курсового приема антибиотиков.
Экозитрин относится к экоантибиотикам — инновационным средствам, позволяющим минимизировать нежелательные лекарственные реакции, отмечаемые при приеме противомикробных средств. Экоантибиотики содержат традиционные антибиотики в сочетании с самым эффективным на сегодняшний день пребиотиком — лактулозой ангидро (используется в пребиотических дозировках и не влияет на моторику ЖКТ), которая избирательно ускоряет рост и активность бифидобактерий. Лактулоза представляет собой питательный субстрат немикробного происхождения для колонизации, стимуляции и роста нормальной кишечной флоры. Применение Экозитрина — препарата с повышенным профилем безопасности и сравнимой эффективностью может повысить приверженность пациентов к лечению.
Литература
1. Пальчун В.Т., Крюков А.И. Оториноларингология: Руководство для врачей. М.: Медицина, 2001: 616.
2. Bryskier A, Butzler J-P. Macrolides. In: R.G.Finch, D.Greenwood, S.R.Norrby, R.J.Whitley, editors. Antibiotic and Chemotherapy. Anti-infective agents and their use in therapy. Churchill Livingstone, 8th edition. 2003: 310–25.
3. Chey WD, Wong BCY. American College of Gastroenterology Guideline on the Management of Helicobacter pylori Infection. Am J Gastroenterol, 2007, 102: 1808-25.
4. Neu HC. The development of macrolides: clarithromycin in perspective. J. Antimicrob Chemother., 1991, 27 (Suppl A): 1–9.
5. Mazzei T, Mini E, Novelli A, Periti P. Chemistry and mode of action of macrolides. J. Antimicrob Chemother, 1993, 31 (Suppl C): 1–9.
6. Leclercq R. Mechanisms of resistance to macrolides and lincosamides: nature of the resistance elements and their clinical implications. Clin Infect Dis 2002, 34: 482–92.
7. Edelstein PH. Pneumococcal resistance to macrolides, lincosamides, ketolides, and streptogramin B agents: molecular mechanisms and resistance phenotypes. Clin Infect Dis 2004, 38 (Suppl. 4): 322–7.
8. Kozlov RS, Bogdanovitch TM, Appelbaum PC et al. Antistreptococcal activity of telithromycin compared with seven other drugs in relation to macrolide resistance mechanisms in Russia. Antimicrob Agents Chemother 2002, 46: 2963–8.
9. Дюфалак (лактулоза). Научная монография. М., 2001.
10.Практические рекомендации Всемирной Гастроэнтерологической организации (WGO). Пробиотики и пребиотики, 2008.
11. Grewe JWM, Gouma DJ, Buurman WA: Complications in obstructive jaundice: Role of endotoxins. Scand J Gastroenterol 1992, 27(Suppl 194): 8–12.
12. van Leeuwen PAM, Hong RW, Rounds JD, Wilmore DW, Wesdorp RIC: Hepatic failure and coma following liver resection is reversed by manipulation of gut contents: the role of endotoxin. Surgery 1991, 110: 169–75.
13. Huchzermeyer H, Schumann C: Lactulose – a multifaceted substance. Z Gastroenterol 1997, 35: 945–55.
14. Kudoh K, Shimizu J, Wada M et al.: Effect of indigestable saccharides on B lymphocyte response of intestinal mucosa and cecal fermentation in rats. J Nutr Sci Vitaminol 1998, 44: 103–12.
15. Pain JA, Cahill CJ, Gilbert JM, Johnson CD, Trapnell JE, Bailey ME: Prevention of postoperative renal dysfunction in patients with obstructive jaundice: a multicentre study of bile salts and lactulose. Br J Surg 1991, 78: 467–9.
16. Madsen KL, Doyle JS, Jewell LD, Tavernini MM & Fedorak RN. Lactobacillus species prevents colitis in interleukin 10 gene–deficient mice. Gastroenterology. 1999. 116, 1107–1114.
17. Fleige1 S, Preisinger W, Meyer1 HHD, Pfaffl1 MW. Lactulose: effect on apoptotic- and immunological-markers in the gastro-intestinal tract of pre-ruminant calves. Veterinarni Medicina. 52, 2007 (10): 437–444.
18. Ewaschuk JB, Dieleman LA. Probiotics and prebiotics in chronic inflammatory bowel diseases. World Journal of Gastroenterology. 2006. 12, 5941–5950.
19. Bruzzese E, Volpicelli M, Squeglia V, et al. A formula containing galacto- and fructo-oligosaccharides prevents intestinal and extra-intestinal infections: an observational study. Clin Nutr. 2009. 28, 156–161.
20. Arslanoglu S, Moro GE & Boehm G. Early supplementation of prebiotic oligosaccharides protects formula-fed infants against infections during the first 6 months of life. J. Nutr., 2007, 137: 2420-2424.
21. Evangelos J. Giamarellos-Bourboulis, Theodoros Adamis et al., Clarithromycin is an effective immunomodulator when administered late in experimental pyelonephritis by multidrug-resistant Pseudomonas aeruginosa. BMC Infectious Diseases, 2006, 6: 31-39.
Источник: Медицинский совет, № 15, 2014
Клацид СР: инструкция по применению
Подойницына Алёна Андреевна
26 июня 2024

ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ. ВОЗМОЖНЫ ПОБОЧНЫЕ ЭФФЕКТЫ. НЕОБХОДИМА КОНСУЛЬТАЦИЯ СПЕЦИАЛИСТА.
Автор статьи
Подойницына Алёна Андреевна
,
Профессия: провизор
Название вуза: Пермская государственная фармацевтическая академия (ПГФА)
Специальность: фармация
Стаж работы: 5 лет
Диплом о фармацевтическом образовании: 105924 3510722 рег. номер 31917
Места работы: провизор в аптеке, преподаватель ПГФА на кафедре Управления и экономики фармации, провизор сервиса Мегаптека
Все авторы
Содержание
- Состав препарата
- Действующее вещество
- Побочные действия
- Что лучше: Панцеф, Супракс или Клацид?
- Панцеф, Супракс или Клацид ребенку: что лучше?
- Краткое содержание
Антибиотики — это мощные лекарства, которые помогают бороться с бактериальными инфекциями, включая опасные для жизни человека. Однако их использование не лишено рисков, так как они могут оказывать серьезные побочные эффекты и даже вызывать новые проблемы со здоровьем, особенно при неправильном и нерациональном применении.
Очень важно принимать антибиотики только по назначению врача, который подбирает наиболее результативный препарат для лечения конкретной инфекции и определяет нужную дозировку и продолжительность курса лечения. Неправильное использование антибиотиков может привести к развитию устойчивости бактерий к их действию. Это означает, что возбудители инфекции могут стать невосприимчивыми к препарату, а лечение может стать более сложным или не дать никакого результата.
С ознакомительной целью рассказываем в статье об антибиотике Клацид СР: составе, действующем веществе, показаниях и побочных действиях. Сравниваем таблетки Клацид СР с препаратами Панцеф и Супракс.
Состав препарата
Клацид СР производится немецкой фармацевтической компанией Эбботт Лэбораториз ГмбХ в виде таблеток пролонгированного действия. На особую технологию изготовления данной формы таблеток указывает аббревиатура СР, от английского SR — slow release, то есть медленно высвобождающийся. Такая лекарственная форма позволяет создавать постоянную концентрацию лекарства в крови, принимая его всего один раз в сутки.
Каждая таблетка содержит 500 мг кларитромицина — антибиотика из группы макролидов, а также вспомогательные вещества (лимонная кислоту, алгинат натрия и кальция, лактозу, повидон, стеарат магния, тальк, стеариновую кислоту, гипромеллозу, макрогол 400 и 8000, диоксид титана, краситель хинолиновый желтый (E104) и др.).
Из-за лактозы в составе препарата его не назначают пациентам с непереносимостью некоторых сахаров.
Действующее вещество
Кларитромицин — это полусинтетический бактериостатический антибиотик-макролид, подавляющий синтез белков в бактериальной клетке и действующий против определенных видов бактерий.
Кларитромицин малотоксичен, создает высокие концентрации в тканях и действует даже против внутриклеточных организмов (микоплазм, хламидий и др.).
Побочные действия
Некоторые побочные реакции у отдельных пациентов могут быть серьезными и порой опасными для жизни. В следующих случаях необходимо немедленно прекратить лечение и обратиться к доктору:
- пожелтение кожи, темный цвет мочи, потеря аппетита и боль в области живота;
- длительный понос, присутствие в кале крови или слизи;
- стеснение в груди, головокружение, слабость (анафилактическая реакция или шок);
- ангионевротический отек;
- сыпь в виде пузырей или язв на слизистых оболочках;
- аритмия или необычные ощущения в области сердца;
- мышечные боли.
Еще часто (в 10% случаев) возникают такие побочные реакции:
- сыпь на коже;
- проблемы со сном;
- головная боль;
- изменение вкусовых ощущений;
- тошнота, рвота, понос, диспепсия;
- избыточное потоотделение;
- отклонения в анализах «печеночных» ферментов.
Обращаем внимание, что для снижения риска развития побочных эффектов необходимо в точности соблюдать рекомендации лечащего врача. А также не употреблять одновременно Клацид СР и алкоголь: этанол снижает эффективность действия антибиотика, а препарат может негативно влиять на выведение токсичных метаболитов спирта.
Что лучше: Панцеф, Супракс или Клацид?
Препараты Панцеф и Супракс содержат антибиотик из другой группы. Это цефиксим, который относится к цефалоспоринам III поколения, имеющим более широкий спектр действия и действующим бактерицидно.
Решить, Клацид СР или Супракс — что лучше при фарингите, при ангине или при пневмонии — может только медицинский специалист. Если вы заболели бактериальной инфекцией, обязательно обратитесь к врачу. Не занимайтесь самолечением и не принимайте антибиотики без назначения. Это важно для вашего здоровья и для предотвращения развития устойчивости бактерий к антибиотикам.
Панцеф, Супракс или Клацид ребенку: что лучше?
Назначить лечение антибиотиками ребенку может только врач. Клацид СР 500 мг, согласно инструкции по применению, показан только взрослым и детям старше 12 лет. А Панцеф и Супракс имеют лекарственные формы (гранулы для приготовления суспензии для приема внутрь) и показания для применения детям с 6 месяцев. Поэтому для лечения маленьких детей препаратами выбора будет лекарства на основе цефиксима.
Краткое содержание
- Каждая таблетка с пролонгированным высвобождением Клацид СР содержит 500 мг кларитромицина — антибиотика из группы макролидов, а также вспомогательные вещества.
- Кларитромицин — это полусинтетический бактериостатический антибиотик-макролид, подавляющий синтез белков в бактериальной клетке и действующий против определенных видов бактерий.
- При приеме Клацид СР часто (в 10% случаев) возникают такие побочные реакции, как сыпь на коже; проблемы со сном; головная боль; изменение вкусовых ощущений; тошнота, рвота, понос, диспепсия; избыточное потоотделение; отклонения в анализах «печеночных» ферментов.
- Препараты Панцеф и Супракс содержат антибиотик из другой группы. Это цефиксим, который относится к цефалоспоринам III поколения, имеющим более широкий спектр действия и действующим бактерицидно. Решить, Клацид СР или Супракс — что лучше при фарингите, при ангине или при пневмонии — может только медицинский специалист.
- Панцеф и Супракс имеют лекарственные формы (гранулы для приготовления суспензии для приема внутрь) и показания для применения детям с 6 месяцев. Поэтому для лечения маленьких детей препаратами выбора будет лекарства на основе цефиксима.
Задайте вопрос эксперту по теме статьи
Остались вопросы? Задайте их в комментариях ниже – наши эксперты ответят вам. Там же вы можете поделиться своим опытом с другими читателями Мегасоветов.
Антибиотик из группы макролидов кларитромицин широко используется в педиатрической практике, поскольку обладает высокой эффективностью при многих инфекционных заболеваниях и имеет благоприятный профиль безопасности.
Общая характеристика препарата
Кларитромицин — полусинтетический препарат, относящийся к 14-членным макролидам. Как и другие макролиды, кларитромицин обладает высокой активностью в отношении многих грамположительных бактерий — Staphylococcus (метициллин-чувствительных), Streptococcus (включая пневмококки), Enterococcus, Listeria monocytogenes, Corynebacterium diphtheriae. К кларитромицину чувствительны некоторые грамотрицательные бактерии — Moraxella catarrhalis, Bordetella pertussis, Neisseria, Campylobacter jejuni, Helicobacter pylori (активность против последнего микроорганизма выше, чем у других макролидов). Кларитромицин является одним из двух макролидов (наряду с азитромицином), обладающих клинически значимой активностью в отношении Haemophilus influenzae. Как и другие макролиды, кларитромицин высокоактивен в отношении атипичных бактерий — Mycoplasma, Ureaplasma, Chlamydia, Legionella, Rickettsia. Важной особенностью кларитромицина является высокая активность в отношении атипичных микобактерий (Mycobacterium avium complex). Также препарат активен в отношении некоторых анаэробных бактерий и токсоплазм [1–2]. Особенностью кларитромицина является образование в организме активного метаболита — 14-гидроксикларитромицина (14-ГОКМ), который также обладает антибактериальной активностью. В отношении чувствительных возбудителей у кларитромицина и его активного метаболита наблюдается аддитивный или синергический эффект. В связи с этим эффект антибиотика in vivo может быть выше, чем in vitro. В частности, активность самого кларитромицина против гемофильной палочки in vitro невелика, однако она усиливается in vivo за счет действия 14-ГОКМ [1–2].
Кларитромицин оказывает преимущественно бактериостатическое действие, но в высоких дозах препарат может оказывает бактерицидное действие на ряд возбудителей — S. pyogenes, S. pneumoniae, H. influenzae, M. catarrhalis, L. pneumophila и M. avium. Помимо основного антибактериального эффекта, обусловленного нарушением синтеза белка на рибосомах бактерий, у кларитромицина имеются выраженные дополнительные антимикробные свойства:
- постантибиотический эффект в отношении некоторых возбудителей (S. pneumoniae, H. influenzae и M. catarrhalis) [1–2];
- подавление факторов вирулентности Pseudomonas aeruginosa — кларитромицин способен подавлять у данного возбудителя двигательную активность и способность к формированию биопленок [3].
Кларитромицин обладает целым рядом терапевтически выгодных неантибактериальных эффектов — иммуномодулирующим, противовоспалительным, мукорегуляторным, которые имеют важное значение для лечения респираторных заболеваний, причем не только бактериальной, но и вирусной этиологии, а также заболеваний неинфекционной природы.
В экспериментальных исследованиях были установлены механизмы неантибактериальных эффектов кларитромицина:
- усиление фагоцитоза апоптотических нейтрофилов альвеолярными макрофагами ведет к предотвращению выделения нейтрофильных протеаз и их воздействию на дыхательные пути [4];
- ингибирование активации ядерного фактора транскрипции (NF-каппа-B) в мононуклеарных клетках крови и клетках легочного эпителия сопровождается подавлением выработки провоспалительных цитокинов — фактора некроза опухоли-альфа (ФНО-альфа), интерлейкинов ИЛ-6, ИЛ-8 и др. [6];
- подавление экспрессии генов, кодирующих индуцибельную синтазу оксида азота (iNOS), ведет к снижению образования NO в эпителии дыхательных путей и альвеолярных макрофагах [5];
- снижение уровня ИЛ-4 с повышением соотношения Т-хелперов 1-го и 2-го типа (Th1/Th2) [7];
- снижение влияния липополисахарида (бактериального эндотоксина) на бокаловидные клетки эпителия дыхательных путей ведет к уменьшению гиперсекреции слизи [8];
- торможение гиперплазии бокаловидных клеток в дыхательных путях, индуцируемой ИЛ-13, также ведет к уменьшению гиперсекреции слизи [9].
Фармакокинетика кларитромицина хорошо изучена. Биодоступность препарата при пероральном приеме составляет 52–55%, при этом пища не снижает этот показатель. Максимальная концентрация препарата в крови после приема внутрь наблюдается в среднем через 2–3 часа. Кларитромицин активно метаболизируется в печени при участии цитохрома P450 с образованием различных метаболитов, прежде всего 14-ГОКМ. Связывание препарата с белками плазмы составляет от 42% до 70%, что зависит от концентрации в крови. Кларитромицин и 14-ГОКМ создают высокие концентрации в различных органах, тканях и биологических жидкостях, в том числе в назальном секрете, миндалинах, жидкости среднего уха, легочной ткани, мокроте. Высокие концентрации препарата и его активного метаболита наблюдаются в фагоцитах [1–2]. Важные данные были получены при исследовании внутрилегочной фармакокинетики кларитромицина в сравнении с азитромицином, ципрофлоксацином и цефуроксимом у 68 добровольцев. Через 6 часов после однократного приема стандартной дозы препаратов (500 мг для каждого) у кларитромицина и 14-ГОКМ отмечались очень высокие концентрации в альвеолярных клетках (азитромицин был обнаружен в них только через 12 часов). При этом высокие концентрации кларитромицина и 14-ГОКМ сохранялись и в сыворотке крови (в сумме они превышали концентрации всех остальных антибиотиков). Кроме того, кларитромицин был единственным антибиотиком, обнаруженным в жидкости, выстилающей легочный эпителий [10]. Период полувыведения кларитромицина составляет от 3 до 8 часов, что зависит от дозы. От 20% до 40% препарата выводится с мочой в неизмененном виде, 10–15% — в виде метаболитов. Около 40% препарата выводится со стулом [1–2].
Рекомендации по применению в педиатрии
Кларитромицин рекомендован для применения у детей при инфекциях различной локализации, вызванных чувствительными бактериями:
- заболевания верхних дыхательных путей и ЛОР-органов — стрептококковый тонзиллофарингит, бактериальный риносинусит, острый средний отит [1–2, 11];
- заболевания нижних дыхательных путей — острый бронхит, обострение хронического бронхита, пневмония (препарат включен в стандарты медицинской помощи больным острым бронхитом и пневмонией Минздравсоцразвития РФ для взрослых и детей в амбулаторно-поликлинических условиях) [1–2, 12–14];
- заболевания желудочно-кишечного тракта, ассоциированные с H. pylori (в составе эрадикационной терапии) [1–2];
- заболевания кожи и мягких тканей [1–2];
- заболевания, вызванные M. avium (профилактика и лечение) [1–2].
Также в литературе представлены результаты клинических исследований, рассматривавших применение кларитромицина при других респираторных заболеваниях. Учитывая способность макролидов подавлять факторы вирулентности P. aeruginosa, наличие у них противовоспалительного и иммуномодулирующего эффектов, в последние годы проводятся исследования эффективности длительных курсов макролидов у больных с муковисцидозом. В научной литературе представлены результаты исследования по применению макролидов в лечении бронхиальной астмы. Применение антибиотиков данного класса обусловлено как активностью в отношении бактерий, играющих роль в патогенезе бронхиальной астмы, так и наличием у препаратов неантибактериальных эффектов, терапевтически выгодных при бронхиальной астме [1–2].
Оригинальный препарат кларитромицина — Клацид® зарегистрирован в России для использования у детей в виде таблеток, покрытых оболочкой (250 и 500 мг), и порошка для приготовления суспензии для приема внутрь (125 мг/5 мл и 250 мг/5 мл). Препарат в пероральной форме не имеет возрастных ограничений, но таблетки могут использоваться у детей с 3-летнего возраста. У детей до 12 лет предпочтительно применение суспензии в дозе 7,5 мг/кг каждые 12 часов (не более 500 мг в сутки), старше 12 лет по 250–500 мг каждые 12 часов. Обычный курс лечения составляет от 5 до 14 дней.
Профиль безопасности
Безопасность лекарственных препаратов имеет особое значение в педиатрии, поскольку у детей возможно развитие нежелательных реакций, несвойственных для пациентов во взрослом возрасте. Макролиды относятся к числу наиболее безопасных антибактериальных препаратов. Они крайне редко вызывают тяжелые нежелательные реакции [1, 15].
Безопасность кларитромицина, в том числе в педиатрической практике, хорошо изучена в многочисленных клинических исследованиях. У детей чаще всего отмечаются нежелательные реакции со стороны желудочно-кишечного тракта (диарея, тошнота и рвота, боли в животе) — их частота около 15%, а также головные боли — их частота около 1,6%. Также при использовании кларитромицина может отмечаться повышение уровня трансаминаз. Остальные реакции встречались в единичных случаях. Нежелательные реакции при использовании препарата обычно носят легкий непродолжительный характер и редко требуют отмены препарата [1–2].
Данные научной литературы свидетельствуют о том, что макролидные антибиотики редко вызывают аллергические реакции [1, 16]. Установлено, что в реальной клинической практике аллергия на макролиды встречаются существенно реже, чем аллергия на пенициллины [17].
В ретроспективном исследовании большой популяции (около 150 тыс. человек) был оценен риск кожной реакции на различные антибактериальные препараты. За период в 1,5 года более 13 тыс. человек (в том числе более 2000 детей) получали почти 20 тыс. курсов антибактериальной терапии. В целом кожная реакция отмечалась у 135 пациентов, что составило примерно 1%. Однако частота кожных реакций на отдельные группы препаратов имела отличия — реже всего она отмечалась при использовании макролидов, она была существенно меньше (в 3 и более раза), чем на пенициллины, фторхинолоны и ко-тримоксазол (рис.) [18].

Особым вопросом безопасности макролидов является их гепатотоксичность, поскольку в научной литературе описаны случаи серьезного поражения печени при их использовании [1]. В недавнем обзоре научной литературе были проанализированы данные о безопасности различных антибиотиков для печени. Установлено, что гепатотоксические реакции при использовании фторхинолонов, тетрациклинов, макролидов и пенициллина наблюдаются существенно реже, чем при использовании амоксициллина/клавуланата, ко-тримоксазола, сульфаниламидов, препаратов для лечения туберкулеза. В частности, частота нежелательных эффектов со стороны печени при использовании эритромицина и кларитромицина составляет менее 4 случаев на 100 тыс. назначений, что меньше средней частоты гепатотоксических реакций на антибактериальные препараты в целом. При этом отмечено, что гепатотоксичность антибиотиков обычно проявляется при длительном курсе применения, использовании высоких доз препарата, у пожилых людей, у пациентов с исходной патологией печени, при одновременном применении гепатотоксических лекарственных средств и алкоголя [19].
При использовании кларитромицина необходимо учитывать, что препарат оказывает ингибирующее действие на цитохром P450, который участвует в метаболизме многих лекарственных средств. При одновременном использовании с такими средствами может повышаться их концентрация в крови и возникать риск токсического эффекта, а также снижаться эффективность кларитромицина [1–2]. Необходимо отметить, что частота и выраженность лекарственных взаимодействий при использовании кларитромицина ниже, чем при использовании эритромицина [20].
Таким образом, более 20-летний опыт использования кларитромицина (Клацид®) в клинической практике и, в частности, в педиатрии свидетельствует о высокой эффективности и безопасности препарата.
Литература
- Страчунский Л. С., Козлов С. Н. Макролиды в современной клинической практике. Смоленск: Русич, 1998. 303 с.
- Рачина С. А., Страчунский Л. С., Козлов Р. С. Кларитромицин: есть ли потенциал для клинического применения в XXI веке? // Клин. микробиол. антимикроб. химиотер. 2005, т. 7, № 4, 369–392.
- Wozniak D. J., Keyser R. Effects of subinhibitory concentrations of macrolide antibiotics on Pseudomonas aeruginosa // Chest. 2004, vol. 125, suppl. 2, p. 62–69.
- Yamaryo T., Oishi K., Yoshimine H. et al. Fourteen-member macrolides promote the phosphatidylserine receptor-dependent phagocytosis of apoptotic neutrophils by alveolar macrophages // Antimicrob. Agents Chemother. 2003, vol. 47, № 1, р. 48–53.
- Tamaoki J. The effects of macrolides on inflammatory cells // Chest. 2004, vol. 125, suppl. 2, p. 41–50.
- Ichiyama T., Nishikawa M., Yoshitomi T. et al. Clarithromycin inhibits NF-kappa B activation in human peripheral blood mononuclear cells and pulmonary epithelial cells // Antimicrob. Agents Chemother. 2001, vol. 45, № 1, р. 44–47.
- Williams A. C., Galley H. F., Watt A. M., Webster N. R. Differential effects of three antibiotics on T helper cell cytokine expression // J. Antimicrob. Chemother. 2005, vol. 56, № 3, р. 502–506.
- Tamaoki J., Takeyama K., Yamawaki I. et al. Lipopolysaccharide-induced goblet cell hypersecretion in the guinea pig trachea: inhibition by macrolides // Am. J. Physiol. 1997, vol. 272, p. 15–19.
- Tanabe T., Kanoh S., Tsushima K. et al. Clarithromycin inhibits interleukin-13-induced goblet cell hyperplasia in human airway cells // Am. J. Respir. Cell Mol. Biol. 2011, vol. 45, № 5, 1075–1083.
- Conte J. E. Jr., Golden J., Duncan S. et al. Single-dose intrapulmonary pharmacokinetics of azithromycin, clarithromycin, ciprofloxacin, and cefuroxime in volunteer subjects // Antimicrob. Agents Chemother. 1996, vol. 40, № 7, р. 1617–1622.
- Баранов А. А., Богомильский М. Р., Волков И. К. и др. Применение антибиотиков у детей в амбулаторной практике: практические рекомендации // КМАХ. 2007, т. 9, № 3, c. 200–210.
- Внебольничная пневмония у детей: распространенность, диагностика, лечение, профилактика. Научно-практическая программа. М.: Оригинал-макет, 2011. 64 с.
- Приказ Министерства здравоохранения и социального развития Российской Федерации от 12 февраля 2007 г. № 108 «Об утверждении стандарта медицинской помощи больным с острым бронхитом».
- Приказ Министерства здравоохранения и социального развития Российской Федерации от 8 июня 2007 г. № 411 «Об утверждении стандарта медицинской помощи больным с пневмонией, вызванной Streptococcus pneumoniae; пневмонией, вызванной Haemophilus influenzae (палочкой Афанасьева–Пфейффера); бактериальной пневмонией, неклассифицированной в других рубриках; пневмонией, вызванной другими инфекционными возбудителями, неклассифицированной в других рубриках; пневмонией без уточнения возбудителя; абсцессом легкого с пневмонией (при оказании специализированной помощи)».
- Periti P., Mazzei T., Mini E., Novelli A. Adverse effects of macrolide antibacterials // Drug Saf. 1993, vol. 9, № 5, p. 346–364.
- Araujo L., Demoly P. Macrolides allergy // Curr. Pharm. Des. 2008, vol. 14, № 27, p. 2840–2862.
- Lutomski D. M., Lafollette J. A., Biaglow M. A., Haglund L. A. Antibiotic allergies in the medical record: effect on drug selection and assessment of validity // Pharmacotherapy. 2008, vol. 28, № 11, p. 1348–1353.
- Van der Linden P. D., van der Lei J., Vlug A. E., Stricker B. H. Skin reactions to antibacterial agents in general practice // J. Clin. Epidemiol. 1998, vol. 51, № 8, p. 703–708.
- Andrade R. J., Tulkens P. M. Hepatic safety of antibiotics used in primary car // J. Antimicrob. Chemother. 2011, vol. 66, № 7, p. 1431–1446.
- Principi N., Esposito S. Comparative tolerability of erythromycin and newer macrolide antibacterials in paediatric patients // Drug Saf. 1999, vol. 20, № 1, p. 25–41.
Н. А. Геппе, доктор медицинских наук, профессор
И. А. Дронов, кандидат медицинских наук
ГБОУ ВПО Первый МГМУ им. И. М. Сеченова Минздравсоцразвития России, Москва
Контактная информация об авторах для переписки: geppe@mma.ru
Содержание
- Клацид описание препарата
- Лекарство Клацид при гастрите желудка
- Отзывы о препарате Клацид
- Частые вопросы
- Полезные советы
Клацид — лекарственный препарат, который используется в комплексном лечение гастрита. Он активен в отношении бактерии гастрита Хеликобактер Пилори, применять препарат следует по назначению врача в сочетании с другими лекарственными средствами. Отзывы о применении Клацида при гастрите показывают его эффективность, это подтверждают слова и пациентов и докторов. На сайте https://odb2k.ru// подробно описано как принимать Клацид при гастрите.
Клацид описание препарата
Лекарственный препарат Клацид – полусинтетическое антибиотическое средство, относящееся к группе макролидных антибиотиков. Основное действующее вещество препарата – кларитромицин, обладающий антибактериальным и бактериостатическим действием, которое происходит в процессе взаимодействия с рибосомальными единицами клеток микроорганизмов и ингибирования белкового синтеза.
Это лекарство фармацевтические компании выпускают в виде таблеток, в которых действующим веществом является кларитромицин (дозировка – 250 и 500 мг). Кроме того, под этим названием выпускаются растворы для внутривенного введения.
Для взрослых людей максимальная суточная доза препарата составляет не более 2 г. Детская доза за сутки в 2 раза меньше. Для людей, страдающих заболеваниями, связанными с нарушением деятельности печени и почек, допустимая доза уменьшается в 2 раза. Разовая доза для больных старше 12 лет колеблется в интервале от 0,25 до 1 мг. Осуществляется прием 2 раза в сутки. Если пациент младше 12 лет, то величина дозировки рассчитывается в соответствии с весом ребенка. В среднем доза находится в пределах от 7,5 до 15 мг/кг при двукратном приеме в сутки.
Кларитромицин быстро проникает в межклеточное пространство и ткани организма, где через 3-4 часа после его употребления достигает максимальной концентрации. В пищеварительной системе он быстро адсорбируется даже при наличии большого количества пищи. Вывод препарата осуществляется через почки. Он выходит с мочой в неизменном виде или после трансформации в метаболит. Препарат обладает широким спектром воздействия на микроорганизмы.
Отдельно выпускается препарат «Клацид СР», представленный таблетками в оболочке с пролонгированным воздействием. Они характеризуются овальной формой и желтым цветом. Такие таблетки продаются в пачках от 5 до 56 штук.
Клацид» выпускают в трех разных вариантах:
- порошок для суспензии: он помещен во флакон емкостью 60 или 100 мл с меткой в виде линии и представлен почти белыми гранулами с запахом фруктов. После смешивания с водой из него образуется белая непрозрачная жидкость, которая пахнет фруктами. Эта форма производится в двух разных дозировках, позволяющих использовать медикамент для деток разного возраста. К флакону прилагается пластиковая ложечка или шприц с делениями, чтобы точно отмерять нужное количество сладкого лекарства;
- таблетки: у них желтая оболочка и выпуклая с двух сторон овальная форма. Такие таблетки тоже производятся в двух дозировках и упакованы в блистеры по 7, 10 или 14 штук. Одна пачка содержит от 7 до 42 таблеток;
- лиофилизат для уколов: он представлен белым порошком с незначительным специфическим запахом. Это средство помещено в герметически закрытые стеклянные флаконы, которые продают по 1 штуке или в пачке по 121 штуке.
Клацид или Клацид СР в чем разница
Лекарство Клацид – антибиотик для взрослых с содержанием активного вещества 250 и 500 мг, для детей. Является оригинальной, запатентованной формой.
Другая форма с приставкой СР продленного действия, также содержащая 500 мг активного вещества – кларитромицина. Разница между аналогами в кратности приема: обычный пьют дважды в сутки, продленный Клацид СР 500 – раз в день в одно и то же время. Эта форма наиболее удобна для взрослых. При этом нельзя разламывать и раскусывать таблетки.
Клацид для детей
Клацид для детей может применяться с трехлетнего возраста. В большинстве случаев детям назначается суспензия Клацид. Отзывы для детей свидетельствуют, что это препарат является достаточно эффективным. При этом цена суспензии достаточно высокая. Дозировка для детей следующая: 7.5 мг средства на 1 кг веса ребенка дважды в сутки. Наибольшая суточная доза — 500 мг.
Лекарство Клацид при гастрите желудка
https://youtu.be/HSWkb7747rE
Клацид – это антибиотик, разработанный немецкой фармацевтической компанией. В состав медикамента входит кларитромицин, который оказывающий бактерицидное и бактериостатическое действие, нарушает внутриклеточный синтез белка.
Антибиотик Клацид выпускается в таблетках, гранулах и порошке для приготовления суспензии. Растворимые формы применяются в детском возрасте и отличаются быстротой действия. Подбор аналогов дешевле для детей и взрослых должен осуществлять врач, согласно результатам анализа на резистентность к бактериям.
Лекарство используется в комплексной терапии при ирридикации Хеликобактер пилори, вызывающей гастрит и язву желудка. Применяется совместно с Де-Нолом и ингибиторами протонной помпы (Омепразолом, Пантопразолом, Эзомепрозолом).
Инструкция по применению при гастрите
Медикамент и аналоги на основе Кларитромицина применяется по назначению врача. Пьются дважды в сутки, через 12 часов. При пропуске приема нельзя удваивать дозировку.
Курс лечения зависит от заболевания и в среднем составляет 5–7 дней. Точная дозировка подбирается исходя из личных данных пациента (ребенок или взрослый, вес, пожилой возраст), наличия в анамнезе других заболеваний (печеночной и почечной недостаточности). Ограничением к назначению является беременность и грудное вскармливание, тяжелые нарушения работы сердца, печеночная недостаточность.
Лекарство Клацид, согласно инструкции, можно принимать независимо от приема пищи. После использования возможно возникновение тошноты, рвоты, болей в желудке, расстройства кишечника (запор, диарея, метеоризм), аллергических реакций. Для предотвращения нежелательных эффектов антибиотик рекомендуется пить после еды, запивая достаточным количеством обычной воды.
Прием препарата для эрадикации Нelicobacter pylori :
- комбинированное лечение тремя препаратами: кларитромицин по 500 мг 2 раза в сутки + лансопразол по 30 мг 2 раза в сутки + амоксициллин по 1000 мг 2 раза в сутки в течение 10 дней; кларитромицин по 500 мг 2 раза в сутки + омепразол по 20 мг в сутки + амоксициллин по 1000 мг 2 раза в сутки в течение 7-10 дней;
- комбинированное лечение двумя препаратами: кларитромицин по 500 мг 3 раза в сутки + омепразол 40 мг в сутки в течение 14 дней с назначением в течение следующих 14 дней омепразола в дозе 20-40 мг в сутки; кларитромицин по 500 мг 3 раза в сутки + лансопразол 60 мг в сутки в течение 14 дней. Для полного заживления язвы может потребоваться дополнительное снижение кислотности желудочного сока.
Применение при беременности и кормлении грудью
Безопасность применения кларитромицина при беременности и в период лактации не изучена. Известно, что кларитромицин выделяется с грудным молоком. Поэтому применять препарат Клацид при беременности и в период лактации следует только в тех случаях, когда нет более безопасной альтернативы, а риск, связанный с самим заболеванием, превышает возможный вред для матери и плода.
Отзывы о препарате Клацид
Отзывы о данном препарате говорят о нем, как об эффективном и результативном лекарстве.
Клацид довольно быстро всасывается в ткани организма и сохраняется в них до 2-х суток.Период полувыведения лекарственных метаболитов составляет 5–10 часов (зависит от дозы и продолжительности лечения).
Клацид» (суспензия) — говорят отзывы — имеет приятный вкус. Удобно, что детям ее можно давать вместе с молоком. Стоит такой препарат примерно 400 рублей за 60 мл. Лекарство в таблетках (10 шт по 250 мг) можно приобрести за 600 рублей. Инфузии — рассказывают пациенты — назначаются достаточно редко. Стоимость ампулы дозировкой 500 мг составляет 650-700 руб.
Мнение врачей и отзывы пациентов о приеме препарата Клацид при гастрите:
- Никита, 44 года, гастроэнтеролог, Тюмень: Амоксиклав и Клацид назначаю одновременно при гастрите, вызванном хеликобактер пилори. В комплексное лечение входит еще Омепразол. Терапия дает положительные результаты. Пациенты, соблюдающие все рекомендации, на побочные эффекты жалуются редко;
- Кузнецова Е.Н. гастроэнтеролог: прекрасный оригинальный препарат кларитромицина, эффективен при эрадикационной терапии, хеликобактерной инфекции, лечении обострения холецистита и синдрома избыточного бактериального роста в кишечнике. Выраженные побочные эффекты в виде тошноты, горечи во рту, диспептических явлений. Достаточно высокая цена;
- Дьяконова М.А. терапевт: антибиотик макролидного ряда. Имеет широкий спектр активности. Эффективен в схемах при проведении эррадикационной терапии. Весьма неплох при лечении заболеваний лор-органов. Очень часто проявляются побочные эффекты. В частности, боли в животе, тошнота и диарея, которые зачастую приводят к тому, что пациент самостоятельно завершает начатое лечение и приходится препарат заменять. Из побочных эффектов некоторые пациенты отмечали слабость, головокружение, нарушение сна(бессонницу), появление тревожности, крапивницу. Конечно, не у 100% отмечаются выраженные побочные эффекты. И если курс лечения завершён, то эффект отличный. Но всё- таки… не очень я люблю этот препарат назначать.
Источники:
- https://zavorota.ru/pankreatit/kladtsid-ili-klatsid-sr.html
- https://lekanalog.ru/klatsid-analogi/
- https://odb2k.ru/instrukciya-otzyvy.ru/242-klacid-po-primeneniyu-analogi-tabletki-sr-poroshok-dlya-prigotovleniya-suspenzii-ukoly-v-ampulah.html
- https://upraznenia.ru/klatsid-ikb-amoksiklav.html
- https://sigareta16.ru/analizy/luchshii-analog-klacida-sravnenie-preparatov-i-otzyvy-o-nih-pri-kakih.html
- https://protabletky.ru/klacid/
Частые вопросы
Как действует Клацид при гастрите?
Клацид (кларитромицин) является антибиотиком, который борется с бактериями, вызывающими гастрит, такими как Helicobacter pylori. Он также имеет противовоспалительные свойства, которые могут помочь снизить воспаление слизистой оболочки желудка.
Как часто следует принимать Клацид при гастрите?
Обычно Клацид принимают два раза в день в течение 7-14 дней в комбинации с другими препаратами, такими как ингибитор протонных насосов и антациды, для лечения гастрита, вызванного Helicobacter pylori.
Какие побочные эффекты может вызвать приём Клацида при гастрите?
Некоторые из возможных побочных эффектов при приёме Клацида включают тошноту, рвоту, диарею, изменение вкусовых ощущений, а также редко возможны боли в животе, аллергические реакции и другие нежелательные эффекты.
Полезные советы
СОВЕТ №1
Перед началом приема препарата Клацид при гастрите, обязательно проконсультируйтесь с врачом, чтобы получить рекомендации по дозировке и продолжительности курса лечения.
СОВЕТ №2
Следуйте инструкции по применению препарата Клацид, принимая его в указанное время и соблюдая рекомендованную дозировку. Не прекращайте прием препарата досрочно, даже если симптомы гастрита улучшились.
СОВЕТ №3
Избегайте употребления алкоголя во время приема препарата Клацид, так как это может усилить побочные эффекты и ухудшить состояние желудка.
