Внешний вид упаковки может отличаться от фотографии
Средняя цена в аптеках
1 061 ₽
Среди
6837
аптек,
подключенных к Ютеке в вашем регионе
Оплата и способы получения
в Москве
Самовывоз
Сегодня бесплатно
из 5028 аптек
Завтра или позже бесплатно
из 6837 аптек
Оплата картой или наличными в аптеке
Доставка
Конкретный срок и стоимость доставки зависят от вашего адреса
Информация о товаре
Действующее вещество:
Инозин пранобекс
Количество в упаковке:
20 шт.
Страна:
Португалия
Страна производства может отличаться, проверяйте при получении заказа
Аналоги Изопринозин
• В наличии в
2827 аптеках
• Самовывоз сегодня
• Доставка недоступна
• В наличии в
5965 аптеках
• Самовывоз сегодня
• Доставка недоступна
• В наличии в
5753 аптеках
• Самовывоз сегодня
• Доставка недоступна
• В наличии в
6121 аптеке
• Самовывоз сегодня
• Доставка недоступна
• В наличии в
5700 аптеках
• Самовывоз сегодня
• Доставка от 2 часов
• В наличии в
4557 аптеках
• Самовывоз сегодня
• Доставка недоступна
• В наличии в
4816 аптеках
• Самовывоз сегодня
• Доставка недоступна
• В наличии в
4772 аптеках
• Самовывоз сегодня
• Доставка недоступна
Посмотреть все аналоги Изопринозин
Инструкция на Изопринозин 500 мг, таблетки, 20 шт.
Состав
1 таблетка содержит:
действующее вещество: инозин пранобекс (изопринозин) — 500 мг;
вспомогательные вещества: маннитол 67,0 мг, крахмал пшеничный 67,0 мг, повидон К 30 10,0 мг, магния стеарат 6,0 мг.
Описание
Таблетки: продолговатые, двояковыпуклой формы белого или почти белого цвета с легким аминовым запахом, с риской на одной стороне.
Фармакодинамика
Изопринозин — синтетическое комплексное производное пурина, обладающее иммуностимулирующей активностью и неспецифическим противовирусным действием. Восстанавливает функции лимфоцитов в условиях иммунодепрессии, повышает бластогенез в популяции моноцитарных клеток, стимулирует экспрессию мембранных рецепторов на поверхности Т-хелперов, предупреждает снижение активности лимфоцитарных клеток под влиянием ГКС, нормализует включение в них тимидина. Изопринозин оказывает стимулирующее влияние на активность цитотоксических Т-лимфоцитов и естественных киллеров, функции Т-супрессоров и Т-хелперов, повышает продукцию IgG, интерферона-гамма, ИЛ-1 и ИЛ-2, снижает образование провоспалительных цитокинов — ИЛ-4 и ИЛ-10, потенцирует хемотаксис нейтрофилов, моноцитов и макрофагов.
Препарат проявляет противовирусную активность in vivo в отношении вирусов Herpes simplex, ЦМВ и вируса кори, вируса Т-клеточной лимфомы человека типа III, полиовирусов, гриппа А и В, ЕСНО-вируса (энтероцитопатогенный вирус человека), энцефаломиокардита и конского энцефалита. Механизм противовирусного действия Изопринозина связан с ингибированием вирусной РНК и фермента дигидроптероатсинтетазы, участвующего в репликации некоторых вирусов, усиливает подавленный вирусами синтез мРНК лимфоцитов, что сопровождается подавлением биосинтеза вирусной РНК и трансляции вирусных белков, повышает продукцию лимфоцитами обладающих противовирусными свойствами интерферонов-альфа и -гамма. При комбинированном назначении усиливает действие интерферона-альфа, противовирусных средств ацикловира и зидовудина.
Фармакокинетика
После приема внутрь препарат хорошо всасывается из желудочно-кишечного тракта. Максимальная концентрация ингредиентов в плазме крови определяется через 1-2 часа. Быстро подвергается метаболизму и выделяется через почки. Метаболизируется аналогично эндогенным пуриновым нуклеотидам с образованием мочевой кислоты. N-N-диметиламино-2-пропранолон метаболизируется до N-оксида, а пара-ацетамидобензоат — до о-ацилглюкуронида. Не обнаружено кумуляции препарата в организме. Период полувыведения составляет 3,5 часа для N-N-диметиламино-2-пропранолона и 50 минут — для пара-ацетамидобензоата. Элиминация препарата и его метаболитов из организма происходит в течение 24-48 часов.
Изопринозин: Показания
лечение гриппа и других ОРВИ;
инфекции, вызываемые вирусом Herpes simplex 1, 2, 3 и 4-го типов: генитальный и лабиальный герпес, герпетический кератит, опоясывающий лишай, ветряная оспа, инфекционный мононуклеоз, вызванный вирусом Эпштейна-Барр;
цитомегаловирусная инфекция;
корь тяжелого течения;
папилломавирусная инфекция: папилломы гортани/голосовых связок (фиброзного типа), папилломавирусная инфекция гениталий у мужчин и женщин, бородавки;
контагиозный моллюск.
Способ применения и дозы
Внутрь, после еды, запивая небольшим количеством воды.
Рекомендуемая доза взрослым и детям с 3 лет (масса тела от 15–20 кг) составляет 50 мг/кг/сут, разделенная на 3–4 приема. Взрослым — по 6–8 табл./сут, детям — по 1/2 табл./5 кг массы тела/сут. При тяжелых формах инфекционных заболеваний доза может быть увеличена индивидуально до 100 мг/кг/сут, разделенных на 4–6 приемов. Максимальная суточная доза для взрослых — 3–4 г/сут, для детей — 50 мг/кг/сут.
Продолжительность лечения
При острых заболеваниях: продолжительность лечения у взрослых и детей обычно от 5 до 14 дней. Лечение необходимо продолжать до момента исчезновения клинических симптомов и в течение еще 2 дней уже при отсутствии симптомов. При необходимости длительность лечения может быть увеличена индивидуально под контролем врача.
При хронических рецидивирующих заболеваниях у взрослых и детей лечение необходимо продолжать несколькими курсами по 5–10 дней с перерывом в приеме в 8 дней.
Для проведения поддерживающей терапии доза может быть снижена до 500–1000 мг в сутки (1–2 табл.) в течение 30 дней.
При герпетической инфекции взрослым и детям назначают в течение 5–10 дней до исчезновения симптомов заболевания, в бессимптомный период — по 1 табл. 2 раза в день в течение 30 дней для уменьшения числа рецидивов.
При папилломавирусной инфекции взрослым препарат назначают по 2 табл. 3 раза в день, детям — по 1/2 табл./5 кг массы тела/сут в 3–4 приема в течение 14–28 дней в виде монотерапии.
При рецидивирующих остроконечных кондиломах взрослым препарат назначают по 2 табл. 3 раза, детям — по 1/2 табл./5 кг массы тела в 3–4 приема в день либо в качестве монотерапии, или в комбинации с хирургическим лечением в течение 14–28 дней, далее с трехкратным повторением указанного курса с интервалами в 1 мес.
При дисплазии шейки матки, ассоциированной с вирусом папилломы человека, назначают по 2 табл. 3 раза в день в течение 10 дней, далее проводят 2–3 аналогичных курса с интервалом в 10–14 дней.
Применение при беременности и кормлении грудью
Не рекомендуется применять препарат во время беременности и в период кормления грудью, т.к. безопасность применения не исследовалась.
Изопринозин: Противопоказания
– повышенная чувствительность к компонентам препарата;
– подагра;
– мочекаменная болезнь;
– аритмии;
– хроническая почечная недостаточность;
– детский возраст до 3 лет (масса тела до 15-20 кг);
– беременность и период грудного вскармливания.
Изопринозин: Побочные действия
В соответствии с классификацией Всемирной организации здравоохранения (ВОЗ) все реакции распределены по системам органов и частоте развития: очень часто (> 1/10); часто (> 1/100, <1/10); нечасто (> 1/1000, <1/100); редко (> 1/10000, <1/1000); очень редко (<1/10000); частота неизвестна (невозможно определить на основании доступных данных).
Нарушения со стороны иммунной системы:
нечасто: крапивница, ангионевротический отек; частота неизвестна: реакции гиперчувствительности, анафилактические реакции, анафилактический шок.
Нарушения со стороны нервной системы:
часто: головная боль, головокружение, утомляемость, плохое самочувствие, слабость; нечасто: нервозность, сонливость, бессонница.
Нарушения со стороны желудочно-кишечного тракта (ЖКТ):
часто: тошнота, рвота, боль в эпигастрии, снижение аппетита; нечасто: диарея, запор.
Нарушения со стороны печени и желчевыводящих путей:
часто: временное повышение активности трансаминаз и щелочной фосфатазы в плазме крови, повышение концентрации мочевины в плазме крови.
Нарушения со стороны кожи и подкожных тканей:
часто: кожный зуд, сыпь; нечасто: макулопапулезная сыпь; частота неизвестна: эритема.
Нарушения со стороны почек и мочевыводящих путей:
нечасто: полиурия.
Общие расстройства и нарушения в месте введения:
часто: боль в суставах, обострение подагры.
Влияние на результаты лабораторных и инструментальных исследований:
часто: повышение концентрации азота мочевины в крови.
Передозировка
При передозировке показано промывание желудка и симптоматическая терапия.
Взаимодействие
Иммунодепрессанты могут снижать эффективность действия препарата. Ингибиторы ксантиноксидазы и урикозурические средства (в т.ч. диуретики) могут способствовать риску повышения уровня мочевой кислоты в сыворотке крови пациентов, принимающих Изопринозин.
Особые указания
Изопринозин, как и другие противовирусные средства, наиболее эффективен при острых вирусных инфекциях, если лечение начато на ранней стадии болезни (предпочтительно, с первых суток заболевания).
После двух недель применения препарата следует провести контроль концентрации мочевой кислоты в сыворотке крови и в моче.
Также при длительном применении рекомендуется периодически контролировать концентрацию мочевой кислоты в сыворотке крови и моче.
Пациенты со значительно повышенной концентрацией мочевой кислоты в организме могут одновременно принимать препараты, понижающие ее концентрацию.
Необходимо контролировать концентрацию мочевой кислоты в сыворотке крови при назначении препарата одновременно с препаратами, увеличивающими концентрацию мочевой кислоты или препаратами, нарушающими функцию почек.
При длительном применении после четырех недель приема целесообразно каждый месяц проводить контроль функции печени и почек (активность трансаминаз, уровень креатинина, мочевой кислоты в плазме крови).
Препарат следует с осторожностью применять у пациентов с острой печеночной недостаточностью, поскольку он подвергается метаболизму в печени.
Форма выпуска
Таблетки 500 мг.
По 10 таблеток в блистер ПВХ/ПВДХ и фольги алюминиевой. По 2, 3 или 5 блистеров вместе с инструкцией по применению помещают в пачку картонную. На пачку картонную дополнительно могут быть нанесены защитные наклейки.
Срок годности
Условия отпуска
По рецепту.
ISPR-RU-00266-DOK-PHARM
Производитель
Техническое фармацевтическое общество «Лузомедикамента», С.А., Португалия
ул. Консильери Педрозу, 69-В, Келуз де Байшу, 2730-055 Баркарена, Португалия
Характеристики
Торговое название
Изопринозин
Действующее вещество (МНН)
Инозин пранобекс
Дозировка или размер
500 мг
Первичная упаковка
блистер
Условия хранения
В сухом, защищенном от света месте, при температуре не выше 25 °C
Представлено описание активных веществ лекарственного препарата. Описание препарата основано на официально утвержденной инструкции по применению от компании-производителя. Приведенное описание носит исключительно информационный характер и не может быть использовано для принятия решения о возможности применения конкретного лекарственного препарата.
Сертификаты Изопринозин 500 мг, таблетки, 20 шт.
Все товары на сайте имеют сертификат соответствия.
Подробнее о гарантии
Дозировки и формы выпуска Изопринозин
• В наличии в
6866 аптеках
• Самовывоз сегодня
• Доставка недоступна
• В наличии в
6847 аптеках
• Самовывоз сегодня
• Доставка недоступна
• В наличии в
6234 аптеках
• Самовывоз сегодня
• Доставка от 2 часов
Цены в аптеках на Изопринозин 500 мг, таблетки, 20 шт.
Мелодия здоровья
от 1 005 ₽
Социальная Аптека
от 1 018 ₽
История стоимости Изопринозин 500 мг, таблетки, 20 шт.
минимальнаясредняямаксимальная
Указана средняя стоимость товара в аптеках региона Москва и МО за период и разница по сравнению с предыдущим периодом
Цены Изопринозин и наличие в аптеках в Москве
500 мг, таблетки, 20 шт.
09:30-19:00 Пн-Пт, 09:30-17:00 Сб-Вс
Достоинства: единственное что сейчас помогает при ОРВИ и гриппа. пробовали разные противовирусные, при начале заболевания. но болезнь прогрессировала и дело заканчивалось антибиотиками. И только изопринозил останавливает развитие заболевания на 3й день приёма! Спасибо педиатру из платной клиники, за совет. Никаких денег не жалко, когда ребёнок болел неделями и это приводило к пневмонии.
Достоинства: Помогает при простуде. Как только заболела (сопли, чихание) начала принимать по 3 таблетки в день и к концу второго дня уже чувствовала себя хорошо, принимала еще по 2-е таблетки 2 дня. Хватило всего 10 таб, чтобы простуда исчезла.
Смотреть все отзывы
Популярные товары в категории
Популярные товары в Ютеке
Купить Изопринозин, 500 мг, таблетки, 20 шт. в Москве с доставкой в аптеку или домой, сделав заказ через Ютеку
Цена Изопринозин, 500 мг, таблетки, 20 шт. в Москве от 703 руб. на сайте и в приложении
Подробная инструкция по применению Изопринозин, 500 мг, таблетки, 20 шт.
Информация на сайте не является призывом или рекомендацией к самолечению и не заменяет консультацию специалиста (врача), которая обязательна перед назначением и/или применением любого лекарственного препарата.
Дистанционная торговля лекарственными препаратами осуществляется исключительно аптечными организациями, имеющими действующую лицензию на фармацевтическую деятельность, а также разрешение на дистанционную торговлю лекарственными препаратами. Дистанционная торговля рецептурными лекарственными препаратами, наркотическими и психотропными, а также спиртосодержащими лекарственными препаратами запрещена действующим законодательством РФ и не осуществляется.
На информационном ресурсе применяются
рекомендательные технологии
.
Опыт применения Изопринозина при заболеваниях шейки матки на фоне папилломавирусной инфекции у подростков и молодых женщин
Статьи
Опубликовано в журнале:
«РУССКИЙ МЕДИЦИНСКИЙ ЖУРНАЛ»; ТОМ 16; № 19; 2008; стр. 1-4.
Л.И. Линаск, Е.Е. Григорьева
ГОУ ВПО «Алтайский государственный медицинский университет»
Комитет по делам здравоохранения администрации, Барнаул,
МУЗ «Детская городская поликлиника № 9», Барнаул
Последние десятилетия характеризуются высоким ростом вирусной инфекции, вследствие чего возрастает частота папилломавирусных поражений шейки матки. Вирус папилломы человека (ВПЧ) инициирует и поддерживает хронические воспалительные процессы нижнего отдела гениталий. Исследования отечественных и зарубежных авторов свидетельствуют о значимости вируса папилломы человека в развитии диспластических процессов шейки матки.
Главной особенностью ВПЧ-инфекции считают ее широкое распространение среди подростков и молодых женщин преимущественно до 25 лет [3]. Низкая сексуальная культура населения, частая смена половых партнеров, незащищенный секс, вредные привычки (курение, токсикомания, алкоголизм) увеличивают риск развития ВПЧ-инфекции, что способствует росту числа воспалительных заболеваний генитального тракта, нарушению репродуктивной функции, невынашиванию беременности и внутриутробного инфицирования плода, а также формированию цервикальной интраэпителиальной неоплазии шейки матки. Вместе с тем отмечено, что у подростков и молодых женщин происходит более быстрое самопроизвольное очищение (элиминация) от ВПЧ и регрессия имеющейся ВПЧ-ассоциированной патологии по сравнению с женщинами более позднего возраста. По результатам исследований, среднее время элиминации ВПЧ у подростков составляет 8 месяцев (CDC, 1999). По наблюдениям С.И. Роговской и В.Н. Прилепской (2006), в возрасте 18-25 лет этот период увеличивается до 1,5-2 лет у каждой второй пациентки. Локальные показатели инфицированности взаимосвязаны с другими генитальными инфекциями: трихомониазом, хламидиозом, микоуреаплазмозом, кандидозом и т.д. [7,8].
Большинство исследователей отмечают значительное разнообразие типов папилломавирусов. Чаще всего обнаруживается вирус 16 типа, следующим по частоте является вирус типа 18. На долю этих вирусов приходится около 50% от общего числа ВПЧ. Вирус папилломы человека может оказывать продуктивное (с образованием кондилом и папиллом) и непродуктивное действие на эпителий. Результатом непродуктивного действия являются внутриэпитеальные поражения, такие как цервикальная интраэпителиальная неоплазия, рак [3,11].
Наиболее уязвимым участком для воздействия вируса является зона трансформации — участок замещения цилиндрического эпителия плоским. Возможно, тропность ВПЧ к клеткам, претерпевающим метаплазию, связана с их повышенной чувствительностью к вирусной инфекции [9,11], поэтому наличие эктопии и других заболеваний на фоне вирусной инфекции является отягощающим обстоятельством для развития рака шейки матки.
Многообразие типов вирусов, возможность вызывать как продуктивное, так и непродуктивное действие на эпителий, формирование различных патологических процессов на шейке матки и наружных половых органах, сочетание вирусов с другими инфекционными агентами требуют дифференцированного подхода к консервативному лечению и избирательной оценке необходимости инвазивных методик.
По результатам исследований Е.Б. Рудаковой (2001), частота псевдоэрозий в структуре гинекологической заболеваемости женщин разных возрастных групп составляет 38,8%. При наличии гинекологических заболеваний этот процент повышается до 49,2, а у подростков и нерожавших женщин до 24 лет составляет от 52,2 до 90%. Наряду с нарушением гормонального баланса, воспалением, травмой, в генезе псевдоэрозий шейки матки существенное значение имеет нарушение местного иммунитета. Авторами доказана роль местного иммунитета в защите от возникновения и прогрессирования рака шейки матки.
По мнению В.А. Головановой и соавт. (1998), высокая частота патологии шейки матки у подростков и юных женщин связана с биологической незрелостью шейки матки, небольшим промежутком времени между менархе и началом половой жизни, ранним половым дебютом, наличием более 5 половых партнеров, что может стать фактором риска развития цервикальной интраэпителиальной неоплазии. Значимыми факторами риска для возникновения папилломавирусной инфекции являются эктопия и бактериальный вагиноз.
Комплексная диагностика ВПЧ-инфекции применительна к патологии шейки матки, хорошо разработана и предполагает использование следующих методов: клинико-визуальный, кольпоскопия, ВПЧ-тест и один из морфологических методов (цитологический -РАР-тест или гистологическое исследование прицельно взятого биоптата шейки матки).
Несмотря на расширение диапазона методов лечения (химио-, крио-, лазеро-, электродеструкция), которые применяются при доброкачественных заболеваниях шейки матки, не существует единых подходов к выбору метода и значимых критериев преимущества одной методики перед другой. Эффективность терапии во многом зависит от выбора метода лечения, использования иммунокорригирующей терапии и целесообразности комбинированного лечения с применением деструктивного воздействия на шейку матки. Большинство исследователей подчеркивают неудачу методов локальной деструкции, отмечают частые рецидивы ВПЧ инфекции на фоне иммунодефицита, обосновывают целесообразность иммунотерапии [2].
В.Н. Прилепская и С.И. Роговская предлагают комбинированное деструктивное лечение папилломавирусных поражений шейки матки проводить на фоне приема иммунопрепаратов, снижающих активность вируса и повышающих иммунитет. Разумная иммунокоррекция повышает эффективность терапии и снижает вероятность рецидива [3,4,7].
Наиболее широкое применение получили интерфероны и их индукторы, иммуномодуляторы. Эти препараты стимулируют неспецифический иммунитет, усиливают продукцию интерлейкинов, повышая синтез антител, стимулируют хемотаксическую и фагоцитарную активность моноцитов, макрофагов и полиморфно-ядерных клеток.
В настоящее время имеется большой выбор препаратов — активаторов иммунитета. Противовирусный препарат Изопринозин (производства «Тева фармацевтические предприятия Лтд.», Израиль), содержит активное вещество — инозин пранобекс, который подавляет репликацию ДНК и РНК вирусов посредством связывания с рибосомой клетки и изменения ее стереохимического строения. Кроме противовирусного действия, препарат обладает и иммуномодулирующим свойством за счет комплекса инозина, что повышает его доступность для лимфоцитов.
Целью настоящего исследования явилось изучение клинической эффективности препарата Изопринозин в монотерапии и комплексном лечении заболеваний шейки матки при ВПЧ-инфекции у подростков и юных женщин.
Материалы и методы
Всего обследовано 74 пациентки с патологией шейки матки на фоне ВПЧ-инфекции в возрасте от 15 до 25 лет (средний возраст 19,4±0,2 лет). Всем пациенткам проведено комплексное обследование, включающее изучение анамнеза, общий и гинекологический осмотр, расширенную кольпоскопию, бактериоскопию вагинальных мазков, окрашенных по Граму, ПЦР-типирование, цитологическое исследование соскобов с шейки матки.
Всем обследованным в монотерапии или при комбинированном лечении назначался Изопринозин.
Возрастная структура обследуемых: подростки в возрасте до 18 лет — 35 (47,3%), молодые женщины 19-25 лет — 38 (51,9%), в основном учащаяся молодежь (студентки ВУЗов и колледжей).
Нами проведена оценка среднего возраста начала половой жизни, количества и частоты смены половых партнеров. Анализ показал, что средний возраст начала половой жизни составил 15,9±0,1 лет. На рисунках 1 и 2 представлены диаграмма полового дебюта и полигамности половых связей. Только каждая третья имела постоянного полового партнера, у каждой четвертой отмечена полигамность половых связей (более 5 партнеров). У 52 (70,3%) менархе отмечено до 14 лет, у 22 (29,7%) после 14 лет, причем у каждой третьей наблюдалось позднее менархе. У большинства женщин — 54 (72,9%) менструальный цикл имел регулярный характер, у каждой пятой месячные были нерегулярные (опсо- или гиперполименореи).
Рис. 1. Возраст сексуального дебюта у девушек-подростков и молодых женщин (n=74)
Рис. 2. Число сексуальных партнеров у девочек-подростков и молодых женщин (n=74)
При изучении соматического анамнеза установлено, что хронический тонзиллит и другие очаги инфекции носоглотки имели место у 21 (28,4%) пациентки, заболевания желудочно-кишечного тракта — у 20 (27%), вегето-сосудистая дистония — у 25 (33,8%). Индекс соматических заболеваний составил 1,2 на 1 пациентку. Изучение анамнеза перенесенных детских инфекций показал, что каждая вторая девочка-подросток и молодая женщина переболела ветряной оспой, каждая третья — коревой краснухой; респираторно-вирусные инфекции были у 38 (51,3%) пациенток. Высокий инфекционный индекс, составляющий более 1,5 на 1 пациентку, свидетельствует о возможных изменениях иммунного статуса.
Особый интерес представляло изучение гинекологического анамнеза, при котором установлено, что воспалительные процессы наружных и внутренних половых органов составили более 85%. Несмотря на молодой возраст обследуемых, у 5 (6,8%) имел место острый эндометрит, у 3 (4,1%) — воспалительный процесс придатков матки и у 56 (75,7%) отмечался вульвовагинит. При всех эпизодах воспалительных заболеваний ранее проводилось лечение.
При гинекологическом осмотре в 100% выявлена патология шейки матки (эрозия, цервициты, лейкоплакии и т.д.). Определение инфекций, передаваемых половым путем, методом ПЦР и бактериоскопии, позволило установить не только различное типирование ВПЧ-инфекции, но и многофакторные причины воспалительных изменений на шейке матки. Моноинфекция имела место лишь у 18 (24,3%), два инфекционных фактора отмечены у 31(41,9%) пациентки, три и более инфекционных агента выявлены у 25 (33,8%) обследуемых. На одну пациентку приходится 2,4 возбудителя.
Как видно из таблицы 1, чаще всего определялся вирус папилломы человека 16,18 типа, который выявлен в 93,2%; ВПЧ 31,33 типа и ВПЧ 6,11 установлены в 14,9 и 17,6% соответственно. Следует отметить, что вирус папилломы человека, как моноинфекция, был только у каждой четвертой, у остальных 75% наиболее частыми сочетаниями являлись уреа — и микоплазменные возбудители. Процент микоплазмоза составил 28,4, а уреаплазмоза — 39,2. Хламидии определены у каждой пятой, трихомонады выявлены у 3 (4%), кандиды — у 11 (14,9%).
Таблица 1.
Основные виды ИППП
| Вид инфекции | Всего (n=74) | |
| абс. | % | |
| Трихомониаз | 3 | 4,1 |
| Микоплазмоз | 21 | 28,4 |
| Уреаплазмоз | 29 | 39,2 |
| Хламидиоз | 14 | 18,9 |
| ВПЧ 16,18 | 69 | 93,2 |
| ВПЧ 31,33 | 11 | 14,9 |
| ВПЧ 6,11 | 13 | 17,6 |
| ВПГ 1,2 | 5 | 6,8 |
| Кандидоз | 11 | 14,9 |
Всем пациенткам до начала лечения и после него проводилась простая и расширенная кольпоскопия. На начальном этапе обследования выявлены разнообразные кольпоскопические картины: эктопия с зоной трансформации, множественными открытыми и закрытыми протоками желез, признаки очагового и диффузного кольпита, зона трансформации с атипичным эпителием в виде лейкоплакии, йоднегативные зоны, мозаика в различных сочетаниях друг с другом. При цитологическом исследовании соскобов с шейки матки I тип цитограммы установлен у 39,2% обследованных, II тип — у 60,8%.
Высокий процент инфицированности, наличие цитограммы воспаления значительно повышают риск развития дисплазий. Учитывая молодой возраст пациенток, гистологическое исследование проводилось лишь по особым показаниям при осложненных формах эктопии, лейкоплакии и цитологически установленной дисплазии. Дисплазия установлена у 6 (8,1%), причем умеренно выраженная дисплазия составила 33,3%, то есть имела место у каждой третьей из шести. Также у каждой третей из всех обследованных имела место лейкоплакия. Проведенные углубленные исследования (кольпоскопическая визуализация и цитологическая диагностика) явились показанием для взятия гистологических исследований у 28 (37,8%) юных и молодых женщин. В подавляющем большинстве определена простая лейкоплакия, прогрессирующий эндоцервикоз.
Несмотря на то, что у всех пациенток выявлена ВПЧ инфекция, специфическая противовирусная терапия Изопринозином назначалась сразу только 18 пациенткам, остальным потребовались антибактериальная и санационная терапии, направленные на элиминацию возбудителей патогенной и условно-патогенной флоры. При верификации инфекции проводилась специфическая терапия основного инфекционного заболевания. При урео- и микоплазмозе, хламидиозе использовались антибактериальные препараты, при кандидозе -противогрибковые, при бактериальном вагинозе — коррекция биоценоза по общим терапевтическим схемам.
После проведения противовоспалительного лечения и контрольной кольпоскопии пациенткам назначался Изопринозин по 1,0 г 3 раза в сутки в течение 10 дней. По основному заболеванию шейки матки 31-й (41,9%) из обследованных женщин потребовалось комбинированное лечение с использованием радиоволновой терапии.
Эффективность монотерапии Изопринозином оценивалась по лабораторным исследованиям ПЦР-диагностики ВПЧ-инфекции через 1,5-2 месяца по окончанию терапии. Полученные результаты свидетельствуют, что полная элиминация вируса составила 95,3%, что подтверждено клинико-лабораторным выздоровлением в 41 случае из 43-х, что свидетельствует о высокой эффективности препарата.
При проведении комбинированной терапии с использованием радиоволновой методики воздействия на шейку матки и иммунокорригирующих препаратов эффективность лечения оценивалась через 2 месяца и полгода. Кольпоскопия показала, что у 30 (96,8%) обследуемых установлена нормальная кольпоскопическая картина, рецидив ВПЧ-инфекции имел место лишь в одном случае.
Кроме клинической эффективности, проведена оценка переносимости препарата Изопринозин. Установлено, что у 4 (5,4%) пациенток отмечалось легкое недомогание и тошнота, которые купировались на второй день приема препарата и не потребовали его отмены. Две пациентки жаловались на кратковременную головную боль, возможно, связанную с приемом препарата (рис. 3.). Других побочных проявлений и аллергических реакций не отмечено.
Рис. 3. Характер побочных реакций применения Изопринозина
Таким образом, исследование, проведенное в группе подростков и молодых женщин с заболеваниями шейки матки на фоне папилломавирусной инфекции, и оценка эффективности изопринозина в монотерапии и комбинированном лечении позволяет сделать следующие выводы:
1. Большинство пациенток с папилломавирусной инфекцией имели отягощенный соматический и гинекологический анамнезы.
2. Папилломавирусная инфекция чаще сочетается с уреаплазмозом, микоплазмозом и кандидозом, которые в совокупности составили более 80% всех других возбудителей.
3. Изопринозин является высокоэффективным препаратом для лечения ВПЧ-инфекции при заболеваниях шейки матки у подростков и молодых женщин.
4. Эффективность в монотерапии Изопринозином составляет 95,3%. При использовании Изопринозина в сочетании с радиоволновой терапией эффективность достигает 96,8% при контроле через полгода, несмотря на выраженные первоначальные морфологические изменения шейки матки.
5. Учитывая высокую эффективность препарата, хорошую переносимость и отсутствие побочных явлений, Изопринозин может быть использован при лечении девочек-подростков и юных женщин.
Литература
1. Голованова В.А., Гуркин Ю.А., Новик В.И. // Актуальные вопросы детской и подростковой гинекологии: материалы и тез. докл. Всерос. науч.-практ. конф. — Новосибирск, 1998. — С. 148-150.
2. Минкина Г.Н. Предрак шейки матки /Г.Н. Минкина, И.Б. Манухин, Г.А. Франк. — М., 2001. -С. 69-72.
3. Прилепская В.Н. Генитальные инфекции и патология шейки матки. Клинические лекции / B.Н. Прилепская, Е.Б. Рудакова. — Омск: ИПЦ ОмГМА, 2004. — 212 с.
4. Прилепская В.Н. Заболевания шейки матки, влагалища и вульвы/В.Н. Прилепская. — М.: МЕД пресс-информ, 2005. — 432 с.
5. Прилепская В.Н. Вирус папилломы человека: современный взгляд на проблему / В.Н. Прилепская // Медицинский вестник. — 2007. — № 29 (414). — С. 9-10.
6. Рудакова Е.Б. Псевдоэрозии шейки матки: автореф. дис…. д-ра мед. наук/Е.Б. Рудакова. — Омск, 1996. — 34 с.
7. Роговская С.И. Оптимизация лечения хронических цервицитов с помощью изопринозина / C.И. Роговская, В.Н. Прилепская//Гинекология. — 2006. — Т. 8, № 1. — С. 4-7.
8. Тихонова Л.И. Общий обзор ситуации с инфекциями, передаваемыми половым путем / Л.И. Тихонова// Вестн. дерматологии и венерологии. — 1999. — № 2. — С. 4-7.
9. Auborn K.J. Treatment of human papillomavirus gynecologic infections/K.J. Auborn, T.H. Carter // Clin Lab Med. — 2000. — Vol. 20, N 2. — P 407-422.
10. Guidelines 2002 for treatment of sexually transmitted diseases / CDC Alanta. — USA. — 400 p. Workowski, K.A. Sexually Transmitted Diseases Treatment Guidelines — 2002/K.A. Workowski, W.C. Levine//MMWR Recomm Rep. — 2002.-Vol. 51 (RR-6). — P. 1-78.
11. Nagai Y. Persistence of human papillomavirus infection after therapeutic conization for CIN 3: is it an alarm for disease recurrence?/ Y. Nagai, T. Maehama, T. Asato, K. Kanazawa // Gynecol Oncol. — 2000. — Vol. 79, N 2. — P. 294-299.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Над описанием клинического случая, представленного доктором
работали
литературный редактор
Елизавета Отмахова,
научный редактор
Сергей Федосов
и
шеф-редактор
Маргарита Тихонова
Дата публикации 4 сентября 2023 г.Обновлено 18 сентября 2023
Вступление
7 ноября 2022 года в рязанский медицинский центр «Мегаклиника» обратилась 23-летняя девушка с множественными мелкими образованиями на коже.
Жалобы
Пациентка рассказала, что образования, похожие на папилломы, в области наружных половых органов и вокруг ануса не причиняли боли. Сыпь сопровождалась обильными выделениями из влагалища.
Состояние кожи ухудшалось из-за бритья с помощью станка. Девушка перестала бриться после того, как нечаянно срезала одно образование, которое начало кровоточить.
Анамнез
Впервые одиночное папилломоподобное образование пациентка заметила за 3 месяца до обращения, но не придала этому значения. Однако их становилось всё больше, поэтому девушка решила обратиться к гинекологу.
Выяснилось, что 8 месяцев назад у пациентки появился новый половой партнёра. Пара презервативом не пользовалась, практиковала прерванный половой акт.
Менструация умеренная и регулярная, идёт раз в 28–30 дней, длится по 5–6 дней, безболезненная. Ранее не беременела. От папилломавирусной инфекции (ВПЧ) не вакцинировалась.
Девушка живёт с родителями. С половым партнёром встречается 3–4 раза в неделю. У него жалоб нет.
Обследование
При осмотре наружные половые органы развиты правильно. На коже половых губ, в области промежности и вокруг ануса отмечалось много безболезненных бородавок телесного цвета. На слизистых половых губ также появились мелкие остроконечные кондиломы.
Слизистая влагалища чистая, умеренно красная. Есть обильные молочные выделения с нерезким кислым запахом.
Шейка матки цилиндрической формы с эктопией вокруг цервикального канала. Тело матки в нормальном положении, не увеличено, безболезненное. Придатки справа и слева не увеличены, своды свободные.
В мазке на микрофлору обнаружили повышенный уровень лейкоцитов (30–40 в п/зр). Сама флора была смешанной, т. е. в ней было умеренное количество палочковидных и кокковых микроорганизмов. Споры грибов и трихомонады не выявлены.
Цитологическое исследование соскоба с цервикального канала показало косвенные признаки папилломавирусной инфекции: группы и разрозненные клетки поверхностного и промежуточного плоского эпителия, группы клеток цилиндрического эпителия, элементы воспаления и смешанная флора.
Комплексное исследование микрофлоры урогенитального тракта (Фемофлор 16) выявил:
- лактобактерии — 10–17 % (значительно ниже нормы);
- стрептококки — 103,2 КОЕ/мл;
- стафилококки — 104,2 КОЕ/мл;
- гарднерелла вагиналис — 104,8 КОЕ/мл;
- мобиликус + коринебактерии — 104,3 КОЕ/мл;
- пептострептококк — 103,4 КОЕ/мл;
- вагинальный атопобиум — 102,5 КОЕ/мл;
- микоплазма хоминис — 102,3 КОЕ/мл;
- уреаплазма (уреалитикум + парвум) — 104,9 КОЕ/мл.
Дрожжеподобных грибов и патогенных микроорганизмов не было.
ПЦР-диагностика ВПЧ-инфекции высокоонкогенного риска показала наличие HPV-16 (4,3 Lg, ВПЧ/105 клеток) и HPV-51 (2,5 Lg, ВПЧ/105 клеток). Другие типы ВПЧ не обнаружены.
Диагноз
Цервицит, связанный с уреаплазмой. Бактериальный вагиноз. ВПЧ 16 и 51-го типов. Аногенитальные бородавки. Кондилломатоз половых губ. Невоспалительная болезнь шейки матки.
Лечение
Пациентке назначили:
- Доксициклин 100 мг — по 2 таблетки в сутки на протяжении 10 дней;
- Орнидазол 500 мг — по 2 таблетки в сутки на протяжении 5 дней;
- Эльжина — по свече в сутки во влагалище на протяжении 9 дней;
- Проваг — по капсуле в сутки на протяжении 20 дней;
- Лактожиналь — по свече в сутки во влагалище на протяжении двух недель;
- Изопринозин — по 2 таблетки 3 раза в сутки на протяжении 28 дней;
- Генферон 1000000 ЕД — по свече в сутки ректально на протяжении 10 дней.
Её половому партнёру также рекомендовали пройти лечение. Кроме того, девушке посоветовали в дальнейшем использовать барьерную контрацепцию.
После проведённого противовоспалительного лечения пациентке сделали кольпоскопию, которая показала нормальную кольпоскопическую картину, эктопию цилиндрического эпителия и единичные открытые протоки желёз.
Через неделю от начала лечения количество выделений уменьшилось, а через 2 недели они исчезли полностью. Новые кондилломы на наружных половых органах не появлялись.
Через полтора месяца после лечения провели контрольное обследование:
- мазок на микрофлору: лейкоциты снизились до 5–7 в п/зр, умеренное количество палочковидных микроорганизмов, споры грибов и трихомонады не обнаружены;
- цитологическое исследование соскоба с цервикального канала шейки матки: группы и разрозненные клетки поверхностного и промежуточного слоёв плоского эпителия, группы клеток цилиндрического эпителия, слизь, лейкоциты в пределах нормы;
- ПЦР-анализ на уреаплазму: не обнаружено.
После того как сыпь перестала распространяться, девушке выполнили криодеструкцию бородавок и остроконечных кондилом на слизистой половых губ. Процедуру проводили с помощью газа, который при температуре -196 °С охлаждается и становится жидким.
После манипуляции пациентке назначили спрей Панавир: распылять его 4 раза в день по 2–3 нажатия над пролеченными участками в течение 5 суток.
На контрольном осмотре через 2 недели кожа вокруг ануса и в области наружных половых губ оставалась чистой. Обследование на ВПЧ показало снижение активности вируса 16-го типа до клинически незначимых показателей, 51-й тип не обнаружили.
Основываясь на достигнутом результате, девушке назначили Генферон 1000000 ЕД по одной свече на ночь ректально.
На контрольном осмотре через 3 месяца пациентка была полностью здорова. Однако ей рекомендовали пройти ещё одно обследование на ВПЧ через полгода.
Заключение
Этот клинический случай показывает, как важно своевременно обратиться к гинекологу, чтобы он смог назначить комплексное лечение ВПЧ и не допустить развития серьёзных осложнений, например дисплазии шейки матки, которая в свою очередь может перейти в рак.
Чтобы не допустить заражения вирусом папилломы человека, необходимо:
- использовать барьерную контрацепцию, особенно если вы сменили полового партнёра и не знаете, здоров ли он;
- соблюдать интимную чистоплотность (отдавать предпочтение моногамным отношениям);
- регулярно посещать гинеколога.
Папилломавирусная инфекция (ПВИ) широко распространена среди различных слоев населения. Инфицированность ВПЧ лиц молодого и среднего возраста составляет 20–60%[1, 8, 12]. В 50% случаев ВПЧ выводится из организма (спонтанная регрессия) в период от 1 года до 4 лет. Инфекция передается преимущественно половым путем при медицинских манипуляциях, вертикальным путем во время беременности, а также при прохождении новорожденного через инфицированные родовые пути матери[12, 15]. Инкубационный период — от 1 до 6 месяцев, максимальное содержание вируса в пораженных тканях обнаруживается на шестой месяц. Нередко результатом инфекции являются заболевания аногенитальной области: рак шейки матки (РШМ), рак вульвы, влагалища, перианальной области и генитальные кондиломы[8, 15, 16]. Считается, что 20% злокачественных опухолей у женщин и 10% у мужчин обусловлены ВПЧ. РШМ — второе по частоте злокачественное заболевание женщин: ежегодно в мире регистрируется более 500 тысяч случаев РШМ и более 300 тысяч больных женщин умирают[12, 16, 20]. ВПЧ — единственная группа вирусов, в отношении которых доказано, что они индуцируют образование опухолей у человека в естественных условиях.
Клональная экспансия инфицированных ВПЧ клеток базального слоя, прошедших первичную стадию дифференцировки, связана с их трансформацией и последующей иммортализацией, которые контролируются генами ВПЧ, кодирующими ранние (Е — early) белки Е6 и Е7 — онкопротеины[1, 12, 15]. Патогенетической основой вирусиндуцированного онкогенеза являются интеграция вирусной ДНК в хромосому инфицированных клеток с активным синтезом онкобелка Е7 и способность трансформированных клеток метаболизировать эстрадиол с образованием 16α-гидроксистерона — агрессивного метаболита, который активирует экспрессию гена Е7 (и способствует высокому устойчивому синтезу вирусного онкобелка Е7). Указанный метаболит обеспечивает пролиферативную активность формирующегося опухолевого клона за счет генетической нестабильности (мутаций (делеций) и эпигенетических модификаций), а также подавление системы иммунологического надзора (общего и местного иммунного статуса организма)[1]. Так, у женщин с цервикальной интраэпителиальной неоплазией (cervical intraepithelial neoplasia — CIN) I–II доказаны дисбаланс цитокиновой регуляции локального иммунного ответа со статистически значимым преобладанием противовоспалительных цитокинов (ИЛ-4, ИЛ-10) и резким снижением концентраций провоспалительных цитокинов (ИЛ-2, ИЛ-6, ФНО-α, а ИФН-γ — в 6,3 раза), а также другие нарушения иммунитета[18]. Все они являются важными факторами, поддерживающими персистенцию ВПЧ в эпителии шейки матки и способствующими развитию и прогрессированию CIN[17]. Высокая распространенность ПВИ и возможность ее исхода в рак указывают на важное медико-социальное значение этой инфекции для современного здравоохранения.
Цель исследования:
оценка эффективности инозина пранобекс (Изопринозина) в комплексной терапии ПВИ.
МАТЕРИАЛЫ И МЕТОДЫ
Проведено проспективное рандомизированное открытое несравнительное исследование. Под наблюдением в 2010–2012 гг. в поликлиниках НИИ экспериментальной медицины им. Пастера и Первого Санкт-Петербургского государственного медицинского университета им. акад. И. П. Павлова находились 90 женщин с аногенитальной ПВИ в возрасте от 19 до 50 лет (средний возраст составил 29,3 ± 2,1 года). Из них 50 пациенток (первая группа) получали инозин пранобекс (Изопринозин), 40 женщинам (вторая группа) проводился лишь вирусологический мониторинг в течение года.
ПВИ диагностировали на основании данных анамнеза, характерных клинических проявлений заболевания, результатов цитологического исследования мазков и иммунологического исследования крови, а также ПЦР с качественным
и количественным определением ВПЧ.
Критерии исключения:
- любая противовирусная терапия в течение 6 месяцев до начала исследования;
- серьезные сопутствующие заболевания;
- беременность и кормление грудью;
- интеллектуальные или другие нарушения, влияющие на способность осознанно дать согласие на исследование или адекватно следовать диагностическим и лечебным рекомендациям;
- аллергические реакции на любой ингредиент применяемых лекарственных препаратов;
- злокачественные новообразования в анамнезе.
У пациенток были исключены протозойные, бактериальные и вирусные заболевания урогенитального тракта помимо ПВИ.
Соскобы с измененных участков слизистых оболочек (отделяемого из уретры, цервикального канала и шейки матки) и из полости рта производили при помощи универсального пробозаборника («ИнтерЛабСервис», Швеция) и помещали в специальную транспортную среду. Выявление и количественное определение ДНК ВПЧ высокого канцерогенного риска (16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59-го типов) в клиническом материале осуществляли методом ПЦР с детекцией в режиме реального времени с использованием набора реагентов производства ООО «ИнтерЛабСервис» (Москва). Флуоресцентную детекцию продуктов амплификации делали на термоциклере Rotor-Gene 6000 (Corbett Research Pty Ltd, Австралия)[4–6].
Содержание металлопротеидов (трансферрина — ТФ, церулоплазмина — ЦП) в сыворотке крови пациенток изучали методом радиальной иммунодиффузии в агаровом геле по Манчини (1965) [18, 19]. Использовали антицерулоплазминовые (полученные В. В. Туркиным) и стандартные (Sevac, Прага) антитрансферриновые сыворотки[19]. Для оценки неферментативной антиоксидантной активности определяли коэффициент ТФ/ЦП. Металлоферменты ЦП и ТФ являются важными компонентами неспецифической защиты организма. Показана их клиническая значимость при вирусных заболеваниях[7], в том числе продемонстрирована роль коэффициента ТФ/ЦП: его повышение коррелирует с клиническим улучшением и, что важно, показывает степень восстановления иммунобиологической резистентности организма.
Для анализа субпопуляций иммунокомпетентных клеток периферической крови пациенток использовали метод непрямой иммунофлюоресценции с моноклональными антителами, полученными к дифференцировочным антигенам, локализованным на поверхности исследуемых клеток[17, 19]. Определяли уровни продукции ИФН-γ и ИФН-α/β (спонтанный и индуцированный) лейкоцитами периферической крови пациенток[6]. Содержание ИЛ-4 в сыворотке крови измеряли с помощью набора реагентов ProCon (ТОО «Протеиновый контур», Санкт-Петербург) методом твердофазного ИФА.
Схема терапии.
Лечение проводили в два этапа. Сначала с помощью химической деструктивной терапии удаляли папилломатозные элементы: Солкодерм — 2 сеанса с интервалом 4–5 дней. На втором этапе у 50 пациенток проводили противорецидивный курс: инозин пранобекс — 2 таблетки 3 раза в день после еды в течение 10 дней. Одновременно на места бывших поражений наносили гель Алломедин 2–3 раза в день в течение 7–10 дней.
Для лечения использовали инозин пранобекс (Изопринозин, «ТЕВА», Израиль). Одна таблетка содержит 500 мг этого вещества. Химическая структура: комплекс инозина и диметиламино-2-пропанол р-ацетамидо-бензоата в соотношении 1 : 3. После приема препарата внутрь в дозе 1,5 г максимальная концентрация инозина достигается через час. Инозин пранобекс имеет широкий спектр действия. Он подавляет репликацию ДНК- и РНК-вирусов посредством связывания с рибосомой клетки и изменения ее стереохимического строения, а также блокирует их репродукцию путем повреждения генетического аппарата. Оказывает иммуномодулирующее действие: стимулирует функции Т-лимфоцитов (в частности, Т-хелперов), NK-клеток. Увеличивает продукцию ИЛ, стимулирует фагоцитоз и синтез антител. Препарат обладает бифункциональными свойствами: доказанной противовирусной и иммуномодулирующей активностью.
Инозин пранобекс эффективен при лечении и профилактике вирусных инфекций у пациентов с нормальной и ослабленной иммунной системой: при гриппе и ОРВИ, кори, герпетической и цитомегаловирусной инфекции, инфицировании вирусом Эпштейна — Барр, ПВИ и др.[2, 3]. Дозу препарата определяют индивидуально в зависимости от характера течения и степени тяжести заболевания. Суточная доза составляет: взрослым — по 2 таблетки 3–4 раза в день; детям с 3 лет — 50–100 мг/кг в 3–4 приема. Курс лечения при ПВИ с учетом клинических проявлений — от 14 до 28 дней либо 3–4 повторных 10–14-дневных курса с интервалами 10 дней. Препарат применяется как в виде монотерапии, так и в комплексе с деструктивными методами с целью повышения их эффективности.
Математическую обработку полученных данных осуществляли с использованием компьютерных программ Excel (Microsoft Inc.), Statistica for Windows в версии 5.0 (StatSoft Inc., 1995) и с применением непарного двустороннего t-теста Стьюдента. Различия считали статистически значимыми при p < 0,05.
РЕЗУЛЬТАТЫ
В ходе исследования у пациенток второй группы (в том числе из слюны и в мазках из ротоглотки) ВПЧ-16 был выделен в 21 (52,5%) наблюдении, а ВПЧ-18 — в 11 (27,5%). Значительно реже — в пробах у 3 (7,5%) женщин — обнаруживали ВПЧ 31, 50, 59-го типов. ВПЧ-33 был обнаружен только у двух женщин. Следует отметить, что у 6 (15,0%) пациенток зарегистрировали несколько серотипов вируса одновременно: в двух пробах были выделены ВПЧ 16-го и 18-го типов, в трех — ВПЧ 16-го и 50-го типов, в одной пробе — ВПЧ 16, 31 и 39-го типов. У большинства пациенток ВПЧ выделяли в течение года[4, 8, 9]. Полученные данные указывают на существенную роль орально-генитальных контактов в распространении ПВИ, в том числе вирусов высокого канцерогенного риска, а также могут косвенно свидетельствовать о повышении риска развития злокачественных заболеваний полости рта и гортани у женщин, практикующих орально-генитальные контакты[4, 8].
По результатам ПЦР-анализа у 5 (10%) женщин основной группы не удалось установить генотип ВПЧ. У 45 пациенток при определении типа ВПЧ получили следующие результаты: 18 (40,0%) участниц имели ВПЧ-11; 5 (11,1%) — ВПЧ-16; 3 (6,7%) — ВПЧ-18; 19 (42,2%) — ВПЧ 2, 7, 31 и 33-го типов. Клинически регистрировали формы ПВИ: остроконечные кондиломы (по МКБ-10: А63.0 — аногенитальные (венерические) бородавки) у 22 женщин и плоские бородавки (по МКБ-10: В07 — вирусные бородавки) — у 28.
На фоне терапии инозином пранобекс после деструкции отмечено заживление раневой поверхности в течение 8,8 ± 0,6 дня. У пациенток первой группы также статистически значимо повышались показатели неспецифической резистентности организма — уровни CD4+, NK-клеток, ТФ, синтеза эндогенных ИФН (табл.). ВПЧ методом ПЦР через 30–35 дней после окончания курса лечения в этой группе выявляли статистически значимо реже: у 6 (12%) женщин против 45 (90%) пациенток перед началом лечения (р < 0,05). Использование инозина пранобекс в комплексной терапии ПВИ позволило снизить частоту рецидивов ПВИ с 49 до 14% в течение 6 месяцев после курса терапии.
Таблица
Иммунологические показатели у пациенток первой группы до и после лечения
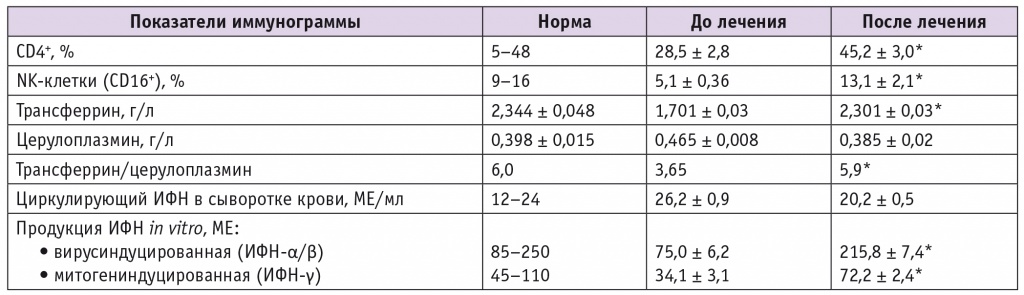
* Различия с показателями до лечения статистически значимы (р < 0,05).
Примечание: ИФН — интерферон.
ОБСУЖДЕНИЕ
Лечение больных с различными формами ПВИ не позволяет избежать рецидивов заболевания в 20–50% случаев[2, 4, 12, 20]. Поскольку полного излечения достичь трудно, считают, что целью терапии должна быть не элиминация возбудителя, а устойчивая ремиссия (клиническое выздоровление). В связи с этим предлагается разрушение папилломатозных очагов (деструктивные методы) с последующей противорецидивной терапией противовирусными (инозин пранобекс, индолкарбинол) и патогенетическими (системная энзимотерапия, антиоксиданты, про- и пребиотики) средствами[3, 4, 8, 12, 14].
Локальная деструкция очагов при клиническом и субклиническом течении ПВИ, направленная на удаление поверхностного слоя эпидермиса без санации клеток базального слоя, позволяет излечить только участок эпителия, где произошла манифестация инфекции. В окружающих тканях остается резервуар ВПЧ в неактивном состоянии или недиагностированной субклинической форме, который может быть причиной рецидивов болезни. В ходе пятилетнего наблюдения за пациентками с инфекционным поражением шейки матки, обусловленным ВПЧ, в 21,4% случаев нами отмечена прогрессия латентной стадии ПВИ в клиническую или субклиническую форму, причем клиническая манифестация инфекции происходила у женщин с персистенцией ВПЧ на фоне дисбаланса показателей иммунитета. Важно отметить, что в случае использования ВПЧ-тестирования в постоперационном мониторинге, в частности у пациенток с CIN2+, выявление вируса даже с низкой нагрузкой может быть ранним маркером рецидива[10]. Адекватная иммунотерапия инозином пранобекс способствует эрадикации ВПЧ из организма, снижая частоту рецидивов и уменьшая риск развития предраковых состояний и РШМ у пациенток с латентной ПВИ.
В литературе имеются данные об успешном применении инозина пранобекс при лечении остроконечных кондилом, генитального герпеса, ПВИ шейки матки, CIN и РШМ[3, 11, 13, 15]. Следует отметить, что доза препарата 50–100 мг/кг (взрослым по 2 таблетки 3–4 раза в день) является лечебной, а дозу 20–50 мг/кг (взрослым по 1 таблетке 2 раза в день) мы используем в течение 2–4 месяцев для профилактики рецидивов. При остроконечных кондиломах проводится лечение обоих партнеров. Рекомендуется воздерживаться от половых контактов в период приема лекарств и использовать барьерную контрацепцию в течение 6 месяцев после завершения терапии.
Известно, что ВПЧ угнетает синтез ИФН, а инфицирование вызывает слабый иммунный ответ[1, 12]. Доказано развитие иммунодефицитных состояний, обусловленных недостаточностью различных звеньев иммунной системы, поэтому для повышения эффективности комплексного лечения назначают ИФН и различные иммуномодуляторы[3, 8, 12, 15]. Однако ИФН-терапия не приводит к стойкой клинической ремиссии. Эффективность лечения напрямую зависит от уровня синтеза онкобелка Е7, который нейтрализует противовирусную активность ИФН, блокируя большинство генов, индуцируемых ИФН. Кроме того, Е7 внутриклеточно инактивирует фактор регуляции ИФН, включающий транскрипцию генов, кодирующих синтез противовирусных белков.
ЗАКЛЮЧЕНИЕ
Полученные результаты позволяют считать обоснованным и перспективным использование препарата инозин пранобекс в комплексной терапии пациентов с различными формами папилломавирусной инфекции (ПВИ) как в острый период болезни, так и для последующей продолжительной профилактики.
Приходится констатировать, что ни один из методов лечения ПВИ не является безупречным, так как при использовании любого из них возможно рецидивирование инфекционного процесса[8, 9, 15, 16]. По-видимому, в ряде случаев (при профилактике рака шейки матки) более эффективной может быть вакцинация. Однако придется найти ответы на многие вопросы, прежде чем новые технологии будут разработаны и внедрены в клиническую практику.
