- /
- /
Генно-инженерная терапия при ревматоидном артрите
Дата публикации: 14.02.2025
Ревматоидный артрит (РА) – заболевание хронического типа, которое прогрессирует и вызывает деструктивные процессы в соединительных тканях. От этой патологии страдает около 0,7% населения в мире. Заболевание чаще поражает людей в возрасте от 35 до 50 лет и проявляется болью, отеком, ограничением подвижности. Без своевременного адекватного лечения артрит приводит к инвалидности. Кроме физических страданий, патология вызывает хронический стресс, тревожные и депрессивные расстройства.
РА – заболевание аутоиммунного происхождения, когда своя же иммунная система вредит суставам, вызывая в них постоянное воспаление. У базовой терапии эффективность низкая, она часто приводит к побочным эффектам, поэтому медицина разрабатывает новые поколения лекарств. Для лечения РА и других аутоиммунных заболеваний перспективное направление – генно-инженерная биологическая терапия (ГИБТ). Многие лекарства, полученные таким способом, показали свою высокую эффективность.

Традиционные подходы и их недостатки
В терапии РА при базовом подходе применяют противовоспалительные соединения, нестероидного типа (НПВС), глюкокортикоиды. НПВС направлены на устранение основных симптомов болезни – отечности, боли, скованности. Их применение в виде моно средства не эффективно, поскольку не останавливает прогресс заболевания. Глюкокортикоиды хорошо купируют воспаление, но длительный прием преднизолона и дексаметазона имеет много побочных эффектов, включая переломы, гипергликемию, инфекции.
Основные противовоспалительные лекарства (цитостатики, средства с золотом, производные аминосалициловой кислоты) способны обеспечить длительную ремиссию, но обладают значительной токсичностью.
Вам помогут наши врачи
Как действуют препараты ГИБП при ревматоидном артрите
Новые методы лечения, к которым относится генно-инженерное лечение артрита, продиктованы негативными свойствами базовых препаратов: стойкость к лечению, недостаточно длительная ремиссия, токсичность, большой перечень противопоказаний и побочных проявлений. Лекарства, полученные генной технологией, влияют непосредственно на механизм развития патологии. Их преимущества:
- снижение активности заболевания, замедление его прогресса;
- уменьшение числа обострений;
- улучшение общего самочувствия и качества жизни пациента;
- избирательность воздействия;
- безопасность при долгосрочном приеме.
ГИБТ оказывает влияние на элементы развития аутоиммунного воспалительного процесса: ФНО-а, лимфоциты Т и В, ИЛ-1, ИЛ-6. Они ингибируют, причем селективно, синтез провоспалительных цитокинов, подавляют активность лимфоцитов. Препараты этой группы не угнетают иммунную систему в целом, не повреждают другие органы, кроме своих мишеней, и это считается основным преимуществом генно-инженерной терапии ревматоидного артрита.
Генно-инженерные препараты для лечения ревматоидного артрита
Клинический эффект от приема лекарств у некоторых пациентов заметен в первые дни терапии, у большинства регистрируется через 3-6 месяцев. Максимальный результат можно получить при назначении лечения на ранних стадиях, в комбинации со стандартными подходами терапии РА, например, сочетанием инфликсимаба и метотрексата. Степень торможения деструкции костных структур прямо зависит от назначаемой дозы средств.
Тоцилизумаб
Это лекарство относится к категории гуманизированных моноклональных тел. При введении в организм вещество связывается с рецепторами ИЛ-6. Его высокая эффективность доказана клиническими исследованиями, в которых сравнивали результативность тоцилизумаба и традиционного подхода – метотрексата. Через 12 недель приема терапия тоцилизумабом позволила добиться нормализации уровня С-реактивного белка.
У контрольной группы, которая принимала в адекватной дозе метотрексат, этот параметр все равно оставался выше нормы. Японские исследования, проведенные в течение 3 лет, доказали безопасность лекарства при длительном приеме, хотя у некоторых пациентов было отмечено повышение печеночных ферментов, развитие инфекции (пневмонии), что требует постоянного мониторинга лабораторных показателей при терапии.
Ритуксимаб
Действие этого препарата базируется на связывании CD-20 с В-клетками, что вызывает апаптоз и избирательное их периферическое истощение. Ритуксимаб относится к моноклональным антителам. Его действие было исследовано в контрольных группах, принимавших по 500 мг и по 1000 мг.
Обе группы продемонстрировали клиническую эффективность. При этом первая группа показала на первом и на втором году исследования выраженное снижение повреждений костных структур, что подтверждалось рентгеном. Но его применение как единственного препарата не практикуется, поскольку максимально выраженный эффект можно получить при комбинации с базисным средством при артрите метотрексатом или лефлуномидом.
Оставьте заявку, и мы свяжемся с вами: поможем подобрать правильного врача и запишем на консультацию!
Инфликсимаб
Инфликсимаб входит в группу химерных моноклональных тел, способных связывать факторы некроза опухоли (растворимые, связанные с мембраной). Действие лекарства проверяли на группе пациентов, у которых прием только метотрексата не дал нужного отклика. Лекарство вводили с интервалом от 4 до 8 недель в концентрации по 3-9 мг. Эффект оценивали по уровню сывороточного инфликсимаба и цитокинов.
Уровень ИЛ-6 и ИЛ-10 показал эффективность лечения и устойчивую ремиссию. Хотя у препарата было доказано отсутствие генотоксичности, но среди побочных проявлений регистрировалась головная боль и инфекции дыхательной системы.
Этанерцепт
Лекарство ингибирует факторы некроза опухоли, демонстрирует эффективность у пациентов с ревматоидным артритом среднего и тяжелого уровня. Испытания проводили на группе лиц, которые ранее принимали адалимумаб и не получили нужного ответа. Пациентам прописали этанерцепт одновременно с метатрексатом. Уже чрез 3 месяца у трети людей было отмечено улучшение. Побочные проявления от этого лекарства такие же, как и у других лекарств для ГИБТ: высыпания в месте укола, головная боль, инфекции верхних дыхательных путей.
Препараты, полученные генной инженерией, доказывают высокую результативность в терапии ревматоидного артрита, многие генно-инжереные препараты в ревматологии получают хорошие отзывы от специалистов. Для усиления эффекта их целесообразно комбинировать с базовыми средствами. Лечение по ГИБТ требует проверки пациентов на все виды инфекций, включая скрытую, стертую форму, поскольку методика повышает риски развития острых вирусных, бактериальных процессов.
Автор публикации
Вам также может быть интересно
Карта клиникВидеоролики о РЗО проектеИстории об артритеНа одной сторонеЗадать вопросПолезные ссылкиФармаконадзор
© 2025. Все права на материалы сайта принадлежат компании АО «БИОКАД»
- Условия использования сайта
- Политика в отношении обработки ПДн
- Политика Cookies
Информация на данном сайте не должна использоваться для самостоятельной диагностики и лечения и не может быть заменой очной консультации врача
Статья на конкурс «био/мол/текст»: Вам когда-нибудь снились кошмары о том, как организм разъедает себя изнутри? А что если это становится реальностью? Именно процессы аутофагии лежат в основе развития ревматических заболеваний. В борьбе с аутоиммунным воспалением медицина слишком часто проигрывала… пока не появились они. Моноклональные антитела.
Конкурс «био/мол/текст»-2017
Эта работа опубликована в номинации «Биомедицина сегодня и завтра» конкурса «био/мол/текст»-2017.
Генеральный спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Спонсором приза зрительских симпатий и партнером номинации «Биомедицина сегодня и завтра» выступила фирма «Инвитро».
«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Системные ревматические заболевания — это патологии, которые возникают из-за агрессивного воздействия иммунитета на собственные ткани. В основе их развития лежит ошибка иммунной системы , которая неправильно распознает нормальные составляющие человеческого тела — аутоантигены. Иммунные клетки принимают их за чужеродные агенты, в которых видят угрозу для организма. Активируется защитная функция, и начинается «бомбардировка» здоровых клеток факторами иммунной системы — аутоантителами (рис. 1).
Основы нормального иммунитета и аутоиммунного процесса в доступной форме изложены на «Биомолекуле» в статье «Иммунитет: борьба с чужими и… своими» [1].
Рисунок 1. Схема строения антител. Антитела представляют собой белки-иммуноглобулины, имеющие две H-цепи (тяжелые) и две L-цепи (легкие). В каждой молекуле белка есть специфические Fab-фрагменты. Эти области отвечают за связывание с антигеном — «мишенью», на которую воздействует антитело. Структура Fab-фрагмента очень вариабельна, что позволяет ей подстраиваться под активные центры антигена — эпитопы. Между антителом и антигеном формируются химические связи (ионные, водородные, гидрофобные). Другой конец молекулы — Fc-фрагмент — отвечает за связывание образовавшихся иммунных комплексов с Fc-рецептором, расположенным на мембранах иммунных клеток (нейтрофилов, макрофагов, тучных клеток). Активация компонентов иммунитета запускает «реакцию уничтожения» по отношению к чужеродному антигену. Таким путем осуществляется антителозависимая цитотоксичность.
Теорию аутоиммунитета сформулировал еще столетие назад немецкий исследователь Пауль Эрлих. За последующие годы описано множество аутоиммунных заболеваний. К ним относятся ревматоидный артрит, системная красная волчанка (СКВ), системная склеродермия, миопатии, васкулиты и прочие патологии .
Подробнее о механизмах развития некоторых ревматических заболеваний можно почитать в статьях: «Системная красная волчанка: болезнь с тысячью лиц» [2] и «Ревматоидный артрит: изменить состав суставов» [3].
Болезни, ассоциированные с аутоиммунным компонентом, — серьезная проблема современного общества . Их распространенность в мировой популяции составляет примерно 5%. Заболевания быстро переходят в хроническую форму, из-за чего снижается качество жизни пациентов. Аутоиммунные патологии часто приводят к инвалидизации больных [1], [4].
В 2017 году «Биомолекула» опубликовала спецпроект, посвященный аутоиммунным заболеваниям.
Несмотря на многолетний поиск новых путей фармакотерапии, современная медицина не может предложить способов лечения, непосредственно влияющих на причину возникновения аутоиммунитета. Врачи способны лишь замедлить прогрессирование патологии и снизить выраженность клиники — провести патогенетическое и симптоматическое лечение. Для этого разработана базисная терапия, которая применяется уже многие годы. Однако не всегда проверенные препараты работают так, как надо.
Почему необходимо искать новые способы лечения?
Для лечения аутоиммунных заболеваний используют широкий арсенал противоревматических лекарств. Классическая терапия включает нестероидные противовоспалительные средства, глюкокортикоиды, цитостатики. В зависимости от особенностей развития заболевания подбирают препараты из той или иной группы [4].
Разберемся, почему нужны новые лекарства. В качестве примера можно рассмотреть классическую терапию одного из самых распространенных аутоиммунных заболеваний — ревматоидного артрита [3]. Современные стратегии борьбы с этой патологией должны соответствовать концепции Treat to target — «лечение до достижения поставленной цели». Она направлена на ремиссию (исчезновение симптомов) заболевания или резкое снижение активности артрита [5], [6].
«Золотым стандартом» в терапии заболевания является метотрексат (рис. 2). Препарат входит в группу базисных противовоспалительных средств.
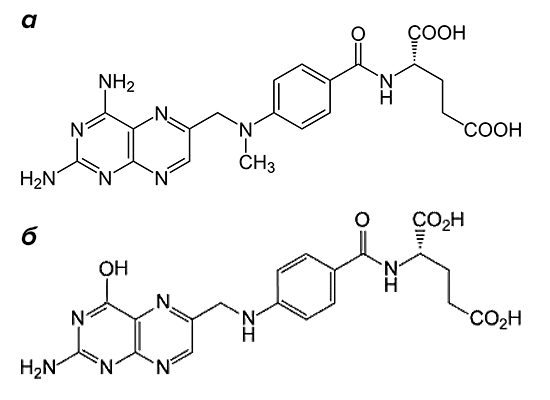
Рисунок 2. Структурные формулы метотрексата и фолиевой кислоты. Препарат (а) по строению похож на фолиевую кислоту (б). Он состоит из птеридиновых групп и парааминобензойной кислоты. Действующий компонент метотрексата отличается от структуры фолата отсутствием гидроксильной группы (–OH) и наличием дополнительного метильного радикала (–CH3).
«Википедия»
По механизму действия метотрексат относится к антиметаболитам. Препараты этой группы тормозят физиологические реакции в организме, связываясь с ферментами и выключая их активность. Вещество, которое в норме участвует в реакции, уже не может попасть в биохимический круговорот из-за повышенной конкуренции с компонентами лекарства. Основной мишенью для действия метотрексата является фермент, расщепляющий фолиевую кислоту, — дигидрофолатредуктаза (ДГФ). Этот белок воздействует на поступающий в организм фолат, переводя его в активную форму. При этом образуется тетрагидрофолиевая кислота. Она участвуют в синтезе строительного материала для ДНК — пуриновых оснований и тимидилата.
Метотрексат вклинивается в цепочку реакций благодаря структурному сходству с молекулой фолиевой кислоты (рис. 2). Конкуренция за фермент приводит к тому, что содержание активного фолата в ткани значительно снижается. Нет строительного материала — нет и новых молекул ДНК, без которых клетки не могут размножаться. Повышенной чувствительностью к воздействию лекарства обладают те ткани, структурные элементы которых постоянно делятся. К ним относятся и компоненты костного мозга, из которых формируются будущие иммунные клетки.
Еще один важный момент в работе метотрексата связан с активностью его полиглутамированных метаболитов. Эти молекулы формируются после активации препарата непосредственно в клетках человеческого организма. Они ингибируют другие ферменты, которые взаимодействуют с фолиевой кислотой. В эту группу входят тимидилсинтетаза и АИКАР-трансамилаза. Активность производных метотрексата запускает процесс выработки аденозина. Он оказывает мощное противовоспалительное действие, благодаря чему снижается выраженность симптомов ревматоидного артрита [7].
Метотрексат удобно использовать — он легко дозируется и может назначаться длительными курсами. Кроме того, важное преимущество этого препарата — низкая цена, в сравнении с современными лекарствами импортных фармкомпаний [8]. Несмотря на все достоинства, лечение метотрексатом не всегда приводит к снижению активности заболевания. У многих пациентов использование препарата неэффективно даже в комбинации с другими классическими средствами [5]. Это подтверждается при анализе статистики. Исследования показали, что при проведении лечения метотрексатом и комбинациями базисных препаратов только половина пациентов достигла ремиссии [9], [10].
Несостоятельность классической терапии заставляет ученых искать новые способы лечения ревматоидного артрита. Стоит отметить, что, несмотря на новые разработки, борьбу с заболеванием все же начинают с назначения метотрексата и его аналогов. Дополнительные препараты используют только при высокой активности аутоиммунного процесса. У таких пациентов применение одного лекарства часто бывает неэффективно [7]. В зависимости от особенностей течения патологии подбирают подходящую схему терапии (рис. 3).
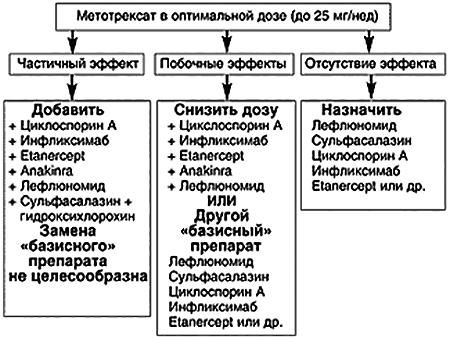
Рисунок 3. Тактика ведения пациента с ревматоидным артритом при неэффективности использования метотрексата.
Неэффективность препаратов базисной терапии встречается не только при ревматоидном артрите, но и при других заболеваниях аутоиммунного происхождения (системной красной волчанке, склеродермии, болезни Бехтерева). Это мотивирует специалистов-ревматологов разрабатывать другие лекарства и подбирать новые схемы терапии.
Генно-инженерные препараты: дополнение к базисной терапии
По-новому взглянуть на лечение аутоиммунных заболеваний позволила разработка терапевтических моноклональных антител [11]. Принципиально новый класс препаратов получен благодаря достижениям генной инженерии. Для понимания механизма действия этих лекарств стоит вспомнить о том, как работают иммунные клетки в норме и при патологии [1], [12].
Иммунная система — это сложный механизм, состоящий из множества «винтиков» — иммунных клеток. Каждая из них имеет свои функции и занимает определенное место в общей структуре защитной системы. В ответ на поступление «вражеского» агента (антигена) включаются компоненты врожденного иммунитета — неспецифические факторы защиты. Это нейтрофилы, эозинофилы и базофилы, которые первыми стоят на пути у вредного воздействия.
Винтики крутятся — активируются новые компоненты иммунной системы. В борьбу с патогеном вступают Т- и В-лимфоциты. Они включают более тонкие механизмы защиты — специфическую цитотоксичность. Вырабатываются антитела, ищут себе «жертву» Т-киллеры… Тонкая регуляция процесса с помощью цитокинов позволяет быстро достигнуть поставленной цели. Согласованное действие всех компонентов иммунитета приводит к выполнению программы — уничтожению патологического агента.
Во время подбора подходящих «деталей» для механизма — при селекции лимфоцитов — неизбежно возникают ошибки. Иммунная система производит аутореактивные клоны — клетки, которые специфичны к антигенам тканей организма. В норме они отсеиваются в «мастерских» — тимусе и лимфатических узлах. Те клоны лимфоцитов, которые не различают собственные и чужеродные антигены, сразу же уничтожаются еще до того, как они приступят к выполнению своей функции. Но что происходит, если «винтики» выпадают из машины иммунитета? Поломка возникает в специфической части механизма — в работе Т- и В-лимфоцитов. При нарушении процесса селекции аутореактивные клетки выходят в кровь. Они ищут своих «жертв» и находят их в нормальных элементах собственных тканей.
В зависимости от типа реакции отличается патофизиологический процесс, лежащий в основе аутоиммунной агрессии. Т-лимфоциты могут самостоятельно убивать клетки тела, а могут и работать «чужими руками» — активировать выработку аутоантител В-лимфоцитами. При поражении В-клеточного иммунитета аутофагия реализуется через систему комплемента, а также путем формирования цитотоксических иммунных комплексов [13], [14]. Подробнее о механизмах нормального и измененного иммунного ответа можно почитать на «Биомолекуле» [1], а также в статьях [15], [16].
При аутоиммунных заболеваниях можно подавлять сразу весь сложный механизм иммунитета, что и делают препараты классической терапии. Но это оставляет человека без защиты от вражеских агентов — бактериальных инфекций, вирусов и прочих патогенов. Поэтому предпочтительнее сохранить активность иммунной системы в целом, избавив человека от аутоагрессии определенных ее компонентов. Именно так работают новые препараты — моноклональные антитела.
Биологические агенты воздействуют на отдельные «винтики» механизма иммунной защиты. Их мишенями могут быть цитокины и их рецепторы, мембранные молекулы лимфоцитов. В зависимости от точки приложения препарата моноклональные антитела делятся на группы (рис. 4):
- Ингибиторы ФНО (фактора некроза опухолей) — инфликсимаб, этанерцепт, цертолизумаб, голимумаб, адалимумаб.
- Блокаторы интерлейкиновых рецепторов — тоцилизумаб (ИЛ-6R), канакинумаб (ИЛ-1R), секукинумаб (ИЛ-17R).
- Анти-В-клеточные антитела (антитела к мембранным молекулам CD20) — ритуксимаб, белимумаб [17].
- Анти-Т-клеточные антитела (антитела к молекулам CD80 и CD86) — абатацепт [18].
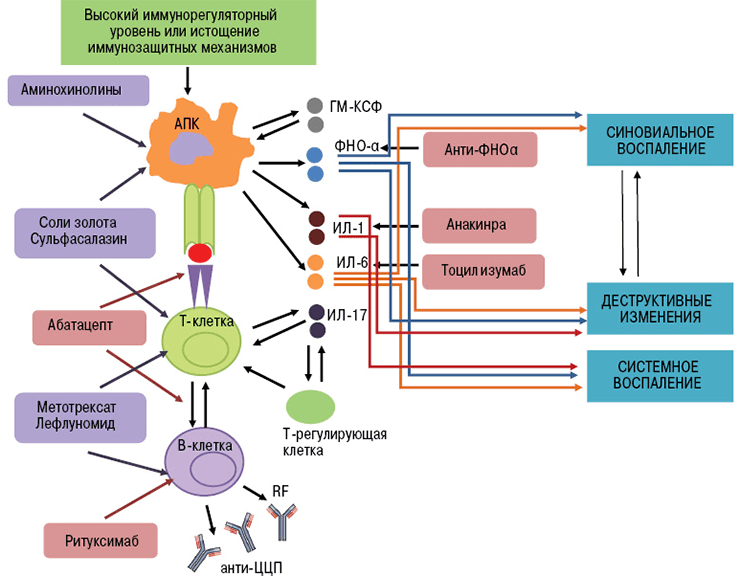
Рисунок 4. Патофизиологические «жертвы» моноклональных антител — интерлейкины, ФНО, поверхностные белки лимфоцитов.
Ингибиторы ФНО
Ингибиторы фактора некроза опухолей — это первые моноклональные антитела, внедренные в ревматологическую практику. В эту группу входят инфликсимаб, этанерцепт, цертолизумаб, голимумаб, адалимумаб.
Фактор некроза опухолей (ФНО) — это провоспалительный цитокин (вещество, которое стимулирует развитие воспалительной реакции). В норме при его выделении происходит пролиферация клеток сосудов, активация макрофагов, лизис опухолевых агентов. Эти эффекты играют важную роль в защите организма от патогенов. Воспаление можно считать ответной реакцией на воздействие повреждающих факторов.
Однако влияние ФНО на суставы при ревматических заболеваниях нельзя назвать положительным. Так, при ревматоидном артрите цитокин стимулирует размножение синовиальных фибробластов — клеток оболочки сустава. Это приводит к формированию паннусов — разрастаний агрессивной ткани. С течением заболевания процесс воспаления и деструкции распространяется на суставный хрящ и подлежащие кости (рис. 5). Ткани сустава заполняются иммунными клетками — макрофагами, Т- и В-лимфоцитами, нейтрофилами. Эти механизмы лежат в основе развития хронического воспаления. Освежить знания о патогенезе ревматоидного артрита можно в статье «Ревматоидный артрит: изменить состав суставов» [3].
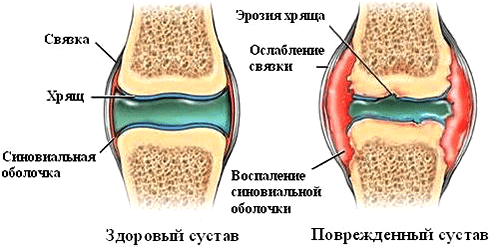
Рисунок 5. Патологические изменения в суставе при ревматоидном артрите. Аутоиммунный процесс вызывает появление эрозий, синовит (воспаление синовиальной оболочки), разрушение суставного хряща.
Одним из ингибиторов ФНО является препарат инфликсимаб. Он имеет «человеческую» и «мышиную» области. Примерно 25% всех аминокислот в составе моноклонального антитела получены из организма мышей. Это Fab-фрагмент — специфический участок, отвечающий за связывание с ФНО. Fc-фрагмент белка образуется из IgG1 — антитела человека.
Такое строение связано с механизмом получения препарата. Первоначально синтезируют антитело к фактору некроза опухолей в организме мыши. Полученный иммуноглобулин специфичен к ФНО и уже может его обезвреживать, но полностью чужеродные белки вводить в организм пациентов, конечно, нельзя. Это вызовет активную иммунную реакцию — выработку антител уже против терапевтических агентов. Поэтому домены мышиного иммуноглобулина заменяют сходными участками человеческих белков. Антитела, имеющие фрагменты разного происхождения, называются химерными. Фактически, они берут лучшие качества своих предшественников. Мышиная часть обеспечивает высокую чувствительность к ФНО, а человеческие фрагменты снижают иммуногенность — вероятность развития иммунного ответа.
Механизм действия инфликсимаба понятен из его строения. Fab-фрагмент молекулы связывает фактор некроза опухолей, образуя с ним устойчивый комплекс. Такое взаимодействие полностью блокирует активность цитокина, препятствуя его соединению с мембранными рецепторами p55 и p57. Инфликсимаб «обезвреживает» как растворимую, так и мембраноассоциированную формы ФНО (рис. 6). В клетках суставов снижается содержание и других провоспалительных факторов — ИЛ-1, ИЛ-6, монооксида азота.
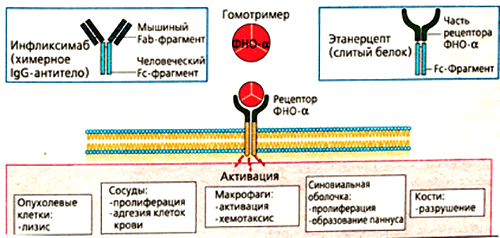
Рисунок 6. Основные эффекты ФНО и блокирующие его моноклональные антитела (инфликсимаб и этанерцепт). Мишенями для моноклональных антител являются свободная и мембраноассоциированная формы фактора некроза опухолей. Лекарства препятствуют связыванию цитокина с рецептором, благодаря чему снижается активность ревматоидного артрита.
Немного другую структуру имеет еще один эффективный препарат из группы ингибиторов ФНО — этанерцепт. В его состав входит внеклеточная часть рецептора к фактору некроза опухолей. Она «подсоединяется» к человеческому IgG1. Гибридная молекула вступает в жесткую конкуренцию за свободный ФНО и обезвреживает его до того, как цитокин успевает связаться с рецепторами и запустить воспалительную реакцию. Дополнительное действие этанерцепта, которого нет у других ингибиторов ФНО, — это нейтрализация лимфотоксина. Это вещество тоже относится к провоспалительным цитокинам. Выработка лимфотоксина стимулирует пролиферативные процессы в суставах. Соответственно, блокировка его действия снижает активность воспаления при ревматологических заболеваниях [18].
Ингибиторы ФНО хорошо показали себя не только при лечении ревматоидного артрита, но и при других аутоиммунных патологиях. Например, у пациентов с болезнью Бехтерева широко используют новые препараты. Замедление прогрессирования патологии в этом случае очень важно, так как аутоагрессия направлена на суставные и костные образования позвоночника. С течением времени болезнь превращает позвоночный столб в «бамбуковую палку» — монолитное негнущееся образование. Анкилоз развивается постепенно, но неотвратимо. С каждым годом двигательные возможности больных становятся все более ограниченными. Применение биологических препаратов позволяет снизить активность воспаления в позвоночнике. Это замедляет процесс формирования анкилоза [19].
Блокаторы интерлейкиновых рецепторов
В развитии аутоиммунного воспаления важную роль играют интерлейкины, которые, как и ФНО, относятся к провоспалительным цитокинам (рис. 7). Основными представителями этой группы являются ИЛ-6, ИЛ-1, ИЛ-17. Функция интерлейкинов — это контроль процессов дифференцировки, пролиферации и гибели (апоптоза) иммунных клеток, который осуществляется через соответствующие гены-мишени [20].
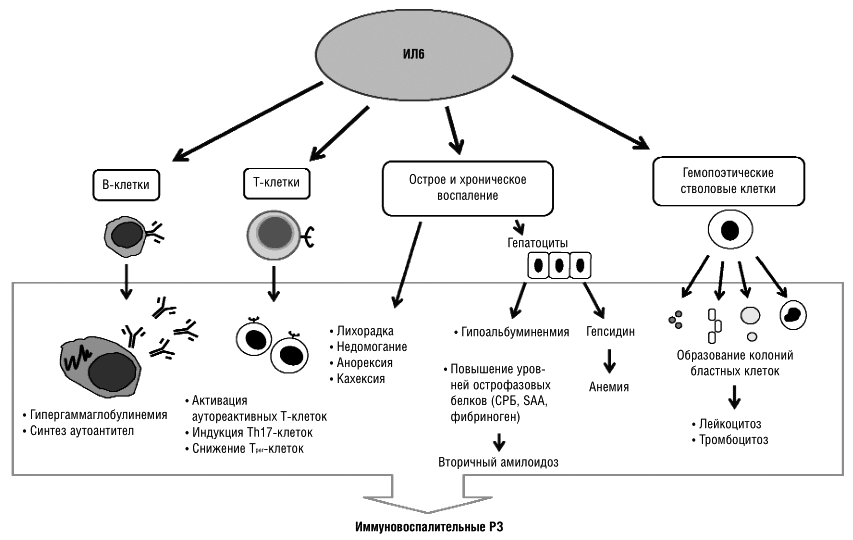
Рисунок 7. Механизм действия интерлейкинов при аутоиммунном воспалении (на примере ИЛ-6). Цитокин влияет на T- и B-лимфоциты, гемопоэтические клетки, гепатоциты. Он стимулирует выработку аутоантител В-клетками, а также формирование аутореактивных Т-клонов, которые непосредственно участвуют в аутоиммунном процессе. Влияние на костный мозг заключается в стимуляции выработки новых клеток крови — повышается число лейкоцитов и тромбоцитов. Воспаление сопровождается ответной реакцией клеток печени, появлением характерных симптомов аутоиммунного заболевания.
Влияние интерлейкинов — один из «спусковых крючков» воспалительного процесса. Поэтому блокировка их активности улучшает состояние пациентов с аутоиммунными заболеваниями. Приостановить работу интерлейкинов можно, если связать их рецепторы — молекулы, передающие сигнал иммунным клеткам. На этом основан механизм действия моноклональных антител из группы ингибиторов интерлейкиновых рецепторов.
Тоцилизумаб — это препарат, который блокирует работу ИЛ-6. Рецептор этого вещества состоит из двух компонентов — мембранного ИЛ-6R (α-цепь) и гликопротеина g130 (β-цепь). Мембранная часть рецептора связывается с ИЛ-6, образуя устойчивый комплекс. Вместе они активируют компонент g130, вызывая изменение его структуры (гомодимеризацию). Образуется рецепторный комплекс из двух молекул g130, который в свою очередь активирует JAK1-киназу. Этот фермент запускает каскад реакций в клетке, который приводит к появлению биологического эффекта цитокина — развитию воспаления. В некоторых случаях ИЛ-6 связывает не мембранная, а растворимая форма α-цепи (рис. 8). Механизм действия рецептора при этом не меняется [21].
В основе работы тоцилизумаба лежит конкуретное ингибирование. Сигнальные молекулы активно связываются с моноклональным антителом. Вакантное место занято — интерлейкин не может образовать комплекс с рецептором, а значит, он не способен активировать процесс воспаления.
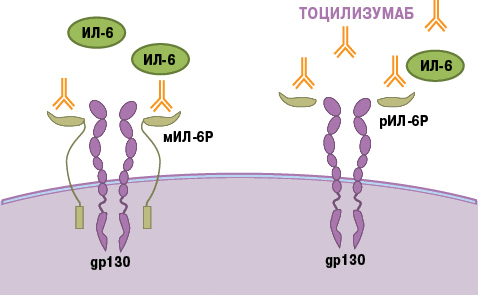
Рисунок 8. Механизм действия тоцилизумаба. Препарат связывает растворимые и мембранные рецепторы ИЛ-6, блокируя передачу сигналов.
Тоцилизумаб считается одним из самых безопасных препаратов, входящих в группу моноклональных антител. Это позволяет применять его при ювенильном идиопатическом артрите, который возникает в возрасте до 16 лет. Дети особенно остро реагируют на токсические воздействия, поэтому препараты, которые используют при их лечении, должны иметь минимальное число побочных реакций. Применение тоцилизумаба позволяет достигнуть необходимого эффекта лечения, не вызвав тяжелых осложнений.
Анти-B-клеточная терапия
Одними из главных элементов, участвующих в аутоиммунном воспалении, являются В-лимфоциты. Именно они вырабатывают аутоантитела, которые связываются со здоровыми клетками организма. Образовавшийся комплекс антитела и аутоантигена атакует система комплемента или цитотоксические лимфоциты. Этот процесс лежит в основе воспалительной реакции при таком ревматическом заболевании, как системная красная волчанка. Ей на «Биомолекуле» посвящена отдельная статья: «Системная красная волчанка: болезнь с тысячью лиц» [2].
Препараты из группы анти-B-клеточной терапии (ритуксимаб и белимумаб) блокируют активность В-лимфоцитов путем связывания их мембранных молекул CD20. Эти вещества есть только у определенных категорий В-клеток. Они специфичны для пре-В-лимфоцитов и зрелых В-лимфоцитов. CD20 нет у стволовых элементов и про-В-клеток, из которых будут образовываться новые лимфоцитарные элементы. Мембранные молекулы данного типа не содержатся и у плазматических клеток, которые вырабатывают иммуноглобулины [22].
Благодаря этой особенности белок CD20 является идеальной «жертвой» для биологических препаратов. При «выключении» его активности не нарушается ни образование новых лимфоцитов, ни выработка нормальных антител. Одним из лекарств с таким механизмом действия является ритуксимаб. Моноклональное антитело связывается с молекулой CD20. Это приводит к запуску иммунологических реакций по отношению к B-лимфоцитам, которые обеспечивают разрушение (лизис) этих клеток (рис. 9).
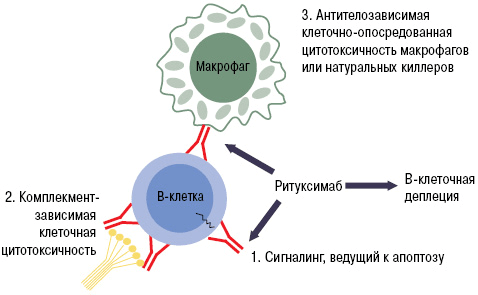
Рисунок 9. Механизм работы ритуксимаба. Fab-фрагмент моноклонального антитела связывается с CD20 на поверхности B-лимфоцита. Это запускает лизис клетки, который может осуществляться несколькими путями: через систему комплемента, программу апоптоза или агрессию натуральных киллеров и макрофагов.
Анти-Т-клеточная терапия
Блокировка действия Т-лимфоцитов возможна благодаря особенностям их активации. Чтобы Т-лимфоцит вступил в аутоиммунный процесс и связался с антигеном, он должен получить два сигнала от антигенпрезентирующих клеток (АПК). Первый сигнал обеспечивает распознавание специфического аутоантигена Т-клеточными рецепторами. Второй сигнал — это неспецифический процесс связывания мембранных молекул CD80 и CD86 на поверхности АПК с рецептором CD28 лимфоцита. Сочетание этих взаимодействий вызывает активацию Т-клеток, которые в свою очередь стимулируют выработку провоспалительных цитокинов. Это и есть основной вклад Т-лимфоцитов в аутоиммунный процесс.
Знания о механизме активации Т-клеток использовали при разработке моноклональных антител. Основной представитель анти-Т-клеточных агентов — это абатацепт. Препарат представляет собой белок, состоящий из двух частей. Специфическая часть образована молекулой CTLA-4 (антиген 4 цитотоксических лимфоцитов). Неспецифическая область — это Fc-фрагмент человеческого иммуноглобулина G1 [23].
Воздействие абатацепта направлено как раз на неспецифический (костимулирующий) сигнал. Компонент CTLA-4 связывает белки CD80 и CD86 на поверхности антигенпрезентирующих клеток. Рецептор лимфоцита CD28 уже не может взаимодействовать с ними, из-за чего активация Т-клетки не завершается (рис. 10).
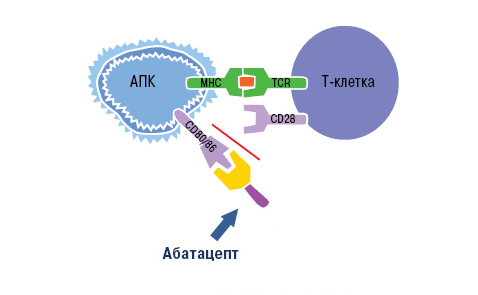
Рисунок 10. Механизм действия абатацепта. Абатацепт модулирует иммунный ответ через связывание с CD80/CD86 на антигенпрезентирующих клетках. Это препятствует связыванию CD80/CD86 с CD28 T-клеток, то есть активация Т-клеток отменяется через блокировку костимуляции.
Не всё так просто: возможные проблемы при использовании моноклональных антител
Препараты моноклональных антител уже довольно долго используют в ревматологической практике. Однако назначают их далеко не всем — не каждому первому и даже не каждому второму пациенту. Главным ограничением, с которым сталкиваются врачи и больные, является действительно «заоблачная» стоимость препаратов этой группы. Ревматические заболевания нельзя вылечить за неделю или месяц — они требуют многолетнего (или даже пожизненного) использования терапии. Поэтому при подборе лекарственного средства важна не только его эффективность, но и цена.
Например, одна пачка метотрексата стоит примерно 200 рублей. Цена упаковки инфликсимаба — около 43 тыс. рублей. Разница очевидна. За год лечения метотрексатом даже в максимальной дозировке пациент потратит на лекарство 1–2 тыс. рублей (в зависимости от фирмы-производителя, схемы лечения и стоимости препарата в местных аптеках). Цена годовой терапии инфликсимабом составляет примерно 700 тыс. рублей. Понятно, что самостоятельно обеспечить себя этим лекарством сможет только очень ограниченная группа пациентов.
Поэтому лечение ревматических заболеваний проводят по строгим алгоритмам. При выявлении патологии пациенту назначают базисный препарат. К примеру, при ревматоидном артрите основным лекарством, вероятнее всего, станет метотрексат. Добавлять моноклональные антитела к стандартной схеме лечения врачи будут только в исключительных случаях. В России их считают препаратами резерва — дополнительными средствами, которые стоит «оставить на потом», даже несмотря на высокую эффективность. Так, если выраженность симптомов не снижается долгое время (как минимум 6 месяцев!), к метотрексату могут добавить биологический препарат. Базисная терапия при этом не отменяется.
Если заболевание изначально имеет высокую активность, быстро прогрессирует и сопровождается внесуставными осложнениями, то больному сразу могут назначить комбинированное лечение базисными средствами и моноклональными антителами. Это связано с тем, что лучше всего биологические препараты работают именно в «остром периоде», когда выраженность симптомов максимальная. Кроме того, эффект от их использования наблюдается быстрее. Лечение инфликсимабом дает результаты уже через 2–4 недели, тогда как метотрексат «включается в работу» только через несколько месяцев.
Использование биологических препаратов допустимо в тех случаях, когда к базисным средствам у пациента развивается непереносимость. Больные испытывают тяжелое побочное воздействие лекарства, которое еще сильнее ухудшает их состояние. Применение препаратов с другим механизмом действия, в том числе и моноклональных антител, позволяет минимизировать побочные эффекты [18].
Назначение и реализация биологических препаратов контролируется государством. Многие средства из группы моноклональных антител (инфликсимаб, этанерцепт, тоцилизумаб, голимумаб) входят в «Перечень жизненно необходимых и важнейших лекарственных средств». В соответствии с ним формируется список лекарств, которые поступают в стационары по всей России. Конечно, биологические препараты сегодня есть далеко не в каждой больнице. Обычно их используют в региональных центрах или специализированных стационарах.
При неспособности обеспечить себя лекарствами пациенты получают инвалидность и проходят терапию за счет государства. Это право закреплено в действующей «Программе государственных гарантий оказания бесплатной медицинской помощи». Лечение биологическими препаратами предоставляется при ревматоидном артрите, болезни Бехтерева, СКВ, дерматополимиозите, ювенильном артрите и других заболеваниях. При этом врачи должны определить четкие показания к назначению того или иного средства. Получить дорогостоящее лечение довольно сложно — нужно пройти полное обследование, собрать документы. Однако предоставление государственной квоты для многих пациентов является последним шансом на полноценную жизнь.
Другая сложность, с которой можно столкнуться при использовании биологических препаратов, — это побочные реакции. Параллельно с накоплением данных об эффективности использования лекарств выявляют все новые нежелательные эффекты от их применения. Большая часть таких реакций связана с процессом иммуносупрессии. Подавляя активность иммунных клеток, моноклональные антитела снижают защитную функцию организма. В первую очередь страдают противоинфекционный и противоопухолевый иммунитеты [18], [24].
Парадоксально, но применение новых лекарств против аутоиммунитета может вызвать острые аутоиммунные реакции. Все биологические препараты представляют собой белковые молекулы, которые в той или иной степени чужеродны для организма. Поэтому при проникновении терапевтических агентов в тело больного иммунитет может распознать их как антигены. Появляется активный иммунный ответ — вырабатываются антитела уже против компонентов препарата.
Аутоиммунные синдромы, спровоцированные введением лекарства, обычно представлены васкулитами, СКВ, антифосфолипидным синдромом, псориазом [25]. Высокой иммуногенностью обладает инфликсимаб, в составе которого есть чужеродные мышиные фрагменты. Менее активно провоцируют иммунитет полностью «человеческие» препараты. Но даже при их применении есть высокий риск развития побочных аутоиммунных реакций. Чтобы устранить эти нарушения, необходимо скорректировать схему лечения больного. В нее включают дополнительные иммуносупрессоры, которые будут подавлять осложнения. Возможно, поэтому комбинации биологических препаратов с базисными лекарствами часто более эффективны, чем изолированная терапия, пусть даже и самыми новыми средствами [24].
Несмотря на все возможные сложности, моноклональные антитела прочно вошли в регистр лекарств, применяющихся в ревматологии. Перспектива использования биологических препаратов и их место в ревматологии будет зависеть от результатов многолетних исследований, которые еще предстоит провести. Но даже сейчас можно сказать, что разработка терапевтических моноклональных антител является важным шагом на пути к победе над аутоиммунным воспалением.
- Иммунитет: борьба с чужими и… своими;
- Системная красная волчанка: болезнь с тысячью лиц;
- Ревматоидный артрит: изменить состав суставов;
- Насонов Е.Л., Александрова Е.Н., Новиков А.А. (2015). Аутоиммунные ревматические заболевания — проблемы иммунопатологии и персонифицированной терапии. Вестник РАМН. 2, 169–182;
- Бабаева А.Р., Калинина Е.В., Звоноренко М.С. (2016). Новые возможности повышения эффективности и безопасности лечения ревматоидного артрита. Медицинский алфавит. 22, 5–12;
- Josef S Smolen, Robert Landewé, Ferdinand C Breedveld, Maya Buch, Gerd Burmester, et. al.. (2014). EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological disease-modifying antirheumatic drugs: 2013 update. Ann Rheum Dis. 73, 492-509;
- Насонов Е.Л. (2015). Метотрексат при ревматоидном артрите — 2015: новые факты и идеи. Научно-практическая ревматология. 4, 421–433;
- Каневская М.З. и Гурская С.В. (2013). Метотрексат в лечении ревматических заболеваний. Современная ревматология. 4, 47–53;
- D. T. Felson, J. S. Smolen, G. Wells, B. Zhang, L. H. D. van Tuyl, et. al.. (2011). American College of Rheumatology/European League Against Rheumatism Provisional Definition of Remission in Rheumatoid Arthritis for Clinical Trials. Annals of the Rheumatic Diseases. 70, 404-413;
- Patrick Durez, Jacques Malghem, Adrien Nzeusseu Toukap, Geneviève Depresseux, Bernard R. Lauwerys, et. al.. (2007). Treatment of early rheumatoid arthritis: A randomized magnetic resonance imaging study comparing the effects of methotrexate alone, methotrexate in combination with infliximab, and methotrexate in combination with intravenous pulse methylprednisolone. Arthritis Rheum. 56, 3919-3927;
- Моноклональные антитела;
- 12 методов в картинках: иммунологические технологии;
- Аутофагия, протофагия и остальные;
- Нобелевская премия по медицине и физиологии 2016: за самоедство;
- Зайчик А.М., Полетаев А.Б., Чурилов Л.П. (2013). Распознавание «Своего» и взаимодействие со «Своим» как основная форма активности адаптивной иммунной системы. Вестник СПбГУ. Серия 11. Медицина. 1;
- Аутоиммунитет. Современные взгляды на физиологические и патологические аспекты аутоиммунитета. Электронный архив НГУ;
- Впервые за полвека появилось новое лекарство от волчанки;
- Насонов Е.Л. и Каратеев Д.Е. (2013). Применение генно-инженерных биологических препаратов для лечения ревматоидного артрита: общая характеристика (лекция). Научно-практическая ревматология. 2, 163–169;
- Логвиненко С.И., Щербань Э.А., Придачина Л.С., Придачина А.Н., Маслова Ю.Ю., Кашичкина А.А. (2016). Генная инженерия в лечении анкилозирующего спондилита (болезни Бехтерева). Научные ведомости БелГУ. Серия: Медицина. Фармация. 19, 179–182;
- Masahiko Mihara, Misato Hashizume, Hiroto Yoshida, Miho Suzuki, Masashi Shiina. (2012). IL-6/IL-6 receptor system and its role in physiological and pathological conditions. Clin. Sci.. 122, 143-159;
- Насонов Е.Л., Александрова Е.Н., Авдеева А.С., Панасюк Е.Ю. (2013). Ингибиция интерлейкина 6 — новые возможности фармакотерапии иммуновоспалительных ревматических заболеваний. Научно-практическая ревматология. 4, 416–427;
- Супоницкая Е.В., Александрова Е.Н., Алексанкин А.П., Насонов Е.Л. (2015). Влияние терапии генно-инженерными биологическими препаратами на субпопуляции В-лимфоцитов при ревматических заболеваниях: новые данные. Научно-практическая ревматология. 1, 78–83;
- Бабаева А.Р., Черевкова Е.В., Гальченко О.Е., Солоденкова К.С. (2012). Биологические агенты в базисной терапии ревматоидного артрита. Лекарственный вестник. 7, 3–9;
- Муравьев Ю.В. и Муравьева Л.А. (2016). Несвоевременные мысли о применении генно-инженерных биологических препаратов при ревматических болезнях. Научно-практическая ревматология. 3, 361–366;
- Псориаз: на войне с собственной кожей.
Содержание
- Как остановить ревматоидный артрит?
- Препараты нового поколения для лечения СКС, ревматоидного артрита и анкилозирующего спондилита
- Показания
- Когда наступает улучшение?
- Побочные эффекты генно-инженерных препаратов
- Россия и Запад: где лечиться препаратами нового поколения?
- Вовремя начатое лечение — лучший результат
- Генно-инженерные препараты — на всю жизнь
- О клинике
- Стоимость лечения
- Как найти хорошего ревматолога?
- Мифы о лечении биологическими препаратами
- Как найти врача и клинику?
Правильно поставить диагноз и быстро начать лечение очень важно всегда, но особенно важно вовремя попасть к грамотному специалисту, если у вас — быстро прогрессирующее заболевание. В лечении таких болезней, как ревматоидный артрит, болезнь Бехтерева, системная красная волчанка, медлить нельзя. Если вас что-то беспокоит, а врачи в поликлинике разводят руками, действуйте — ищите грамотного ревматолога, ведь без адекватного лечения можно всего за 3-5 лет превратиться в инвалида. Само такое заболевание не пройдет.
Как остановить ревматоидный артрит?
Грамотный ревматолог поможет затормозить развитие недуга и максимально сохранить качество жизни. О современных генно-инженерных препаратах нового поколения, которые используются для лечения ревматологических болезней, мы поговорили с ревматологом Сизиковым Алексеем Эдуардовичем.
— Алексей Эдуардович, расскажите, пожалуйста, о том, чем вы занимаетесь и о сфере своих научных интересов.
— Здравствуйте! Меня зовут Алексей Эдуардович Сизиков, я ревматолог. Мы занимаемся ревматическими заболеваниями во всем их разнообразии.
Наиболее частые заболевания — это ревматоидный артрит, анкилозирующий спондилит, или болезнь Бехтерева, системная красная волчанка, системная склеродермия, дерматомиозит и многие другие, потому что спектр ревматических заболеваний очень разнообразен.
— Если мы говорим о трех заболеваниях — ревматоидном артрите, системной красной волчанке и болезни Бехтерева, то какое стандартное лечение обычно назначают на местах, и чем отличается лечение, которое назначают в вашем учреждении?
— Для каждого заболевания есть свое стандартное лечение. Все ревматологи, независимо от того, где они работают, опираются на клинические рекомендации. В них четко прописаны первый и второй этапы врачебной помощи, препараты первого, второго ряда и так далее.
Чем отличается конкретно наше учреждение? Наверное тем, что поскольку мы являемся федеральным учреждением, мы оказываем медицинскую помощь третьего уровня, то есть самую сложную, берем самые сложные случаи и используем самые последние достижения и новые препараты, которые применяются в нашей специальности.
— Какой из трех диагнозов, которые мы сегодня обсуждаем, хуже всего поддается лечению?
— Все эти болезни являются тяжелыми системными ревматологическими заболеваниями. Но нужно помнить о том, что каждое конкретное заболевание, будь то ревматоидный артрит, системная красная волчанка, болезнь Бехтерева, может течь по-разному у разных людей. У кого-то ревматоидный артрит очень тяжелый, человек обездвижен. У другого он течет более мягко. То же самое относится и к двум другим заболеваниям. Поэтому это неправильный подход — какое заболевание тяжелее, а какое — легче, нужно идти от человека.
— Сколько времени есть у человека с момента начала болезни до инвалидности, если нет лечения?
— Если говорить в среднем, то это 5-7 лет. В медицине это называется естественное течение заболевания. Хотя бывает, что люди без лечения становятся инвалидами за 1-2 года, а бывает, что люди, не получая должного лечения, сохраняют свою функциональную активность намного дольше. Все индивидуально.
— Действительно ли ревматоидный артрит часто приводит к инфаркту, инсульту или атеросклерозу?
— Есть статистические данные, что все сердечно-сосудистые патологии (инфаркты, инсульты, атеросклероз) у пациентов с ревматоидным артритом встречаются чаще, чем в популяции здоровых людей. Однако это не значит, что если у человека ревматоидный артрит, то 100% у него через три года разовьется инсульт.
Препараты нового поколения для лечения СКС, ревматоидного артрита и анкилозирующего спондилита
— Как работают генно-инженерные биологические препараты?
— Само название этой группы препаратов связано с механизмом их получения, то есть они получаются путем генной инженерии.
По механизму действия, как правило, эти препараты блокируют те или иные молекулы, которые участвуют в развитии заболевания и в развитии воспаления. Классов препаратов много и отношение к классу зависит конкретно от точки приложения — от того, какую молекулу они блокируют.

— Каким образом эти препараты могут улучшить качество жизни пациента?
— Это самое передовое лечение, которое есть на сегодняшний день.
Задача лечения любого заболевания, по крайней мере, в ревматологии, — это достижение либо стойкой ремиссии, то есть неактивного заболевания, либо низкой активности заболевания. Если переводить это на простой и понятный всеми нами язык — это возвращение человека в строй. И самая главная цель — это улучшение и нормализация качества его жизни.
Показания
— Есть ли при анкилозирующем спондилите стадии, когда применять биологические препараты невозможно?
— Для применения любых препаратов, в том числе биологических, должны быть показания. Сейчас считается, что какая бы стадия заболевания ни была, если у человека полыхает воспаление, а как раз это есть точка приложения генно-инженерных препаратов, тогда пациента на любой стадии анкилозирующего спондилита нужно лечить именно ими.
Самая простая ситуация, когда лечение этими препаратами не нужно: у человека все отболело, то есть у него было активное воспаление, образовались изменения в позвоночнике, но сейчас воспаления нет, то есть воспалительный процесс остановлен. Генно-инженерные препараты можно назначить, но они ни на что не подействуют.
Когда наступает улучшение?
— Если у человека острое воспаление, через какое время после начала приема биологических препаратов можно ожидать улучшения?
— Если говорить о том, через сколько развивается эффект от генно-инженерных препаратов, то бывает по-разному. Вообще временной промежуток для оценки эффективности данного лекарства — три месяца: у нас есть три месяца на то, чтобы понять, действует этот препарат или нет.
Есть определенные критерии, по которым мы оцениваем эффективность препарата. Если за три месяца мы не добиваемся того, чего изначально хотели, например, достижения низкой активности заболевания, значит что-то мы делаем не так, и препарат надо менять.
Что касается быстроты наступления эффекта, то есть пример из жизни, который относится к ревматоидному артриту. В 2001-м году, когда генно-инженерные препараты только появились в России и наша клиника была одной из первых трех, которым фирма дала этот препарат на испытания, у нас была очень тяжелая пациентка, обездвиженная, наша коллега, к сожалению. Она практически не могла встать с кровати. Мы первый раз прокапали первый препарат, появившийся в России, и на следующее утро пришли в палату на обход, она встала и показывала, как она может присесть, хотя накануне она лежала на кровати и не могла подняться. Бывает и так. То же самое бывает и при анкилозирующем спондилите.
Побочные эффекты генно-инженерных препаратов
— Опасны ли эти препараты, могут ли быть осложнения?
— Побочные эффекты у генно-инженерных биологических препаратов, конечно, есть. Следует помнить, что полезных лекарств не бывает, все лекарства вредные. Здоровому человеку ничего не нужно, в том числе не нужны и пищевые добавки, витамины.
Чем препарат новее, эффективнее, чем он «сильнее» действует, тем больше спектр вероятных побочных эффектов. Но этого не нужно пугаться, потому что если мы, например, прочитаем инструкцию к препарату «парацетамол», который мы все принимаем при простуде, она занимает несколько страниц мелкого текста. Нужно помнить о том, что эти побочные эффекты развиваются очень редко.
Почему эти списки побочных эффектов такие длинные? При испытаниях препарата, которые проводятся на многих десятках, иногда даже сотнях тысяч людей, если хоть у одного человека в мире во время испытания было зарегистрировано побочное действие, фирма обязана включить его в инструкцию. Встречаются они достаточно редко и с ними можно справиться. Необходимо помнить о том, что они есть.
Еще один момент, который я хотел бы отметить: именно с этим связано то, что каждый препарат, особенно сильнодействующий генно-инженерный препарат, назначается по строгим показаниям, а не просто так. Поэтому назначать его должны люди, которые знают, что это за препарат, умеют с ним работать и в идеале имеют достаточно большой опыт.
— Можно ли заводить детей, если вы принимаете биологические препараты? Как это сказывается на беременности?
— На фоне лечения, в том числе и генно-инженерный препаратами, возможность иметь детей никуда не девается. На фоне лечения некоторыми классами препаратов, беременеть, безусловно, нежелательно, поскольку вопрос деторождения, пожалуй, самый важный для женщины. Беременность и так должна быть планируемая, а у людей с хроническими заболеваниями она должна быть планируемая вдвойне. Поэтому если пациент лечится препаратами нового поколения и планирует забеременеть, то сначала нужно добиться ремиссии заболевания или хотя бы низкой активности, потом прекратить лечение, спокойно забеременеть и родить ребенка, и, если понадобится, после этого возобновить лечение.
Есть некоторые препараты, которые можно принимать во время беременности, то есть на их фоне можно забеременеть, можно вынашивать беременность, не прерывая лечения, можно спокойно рожать здоровых детей. У нас есть опыт работы с такими препаратами.

Россия и Запад: где лечиться препаратами нового поколения?
— Насколько в России разработка препаратов и их применение отличаются от того, что делают в западных странах?
— Впервые генно-инженерные препараты появились за границей. В последние годы появилось и сейчас работает несколько российских компаний, которые разрабатывают свои биологические препараты, локализуют препараты импортного производства.
Мне доводилось бывать на нескольких заводах российских компаний, и я вам могу сказать, что уровень разработки препаратов и их производства у нас нисколько не хуже, чем в странах западной Европы, Америки, а зачастую даже лучше. Это особенно важно, потому что в силу времени, в котором мы живем, мы можем оказаться отрезаны от западных лекарств, и очень здорово, что российские компании повторяют, производят эти самые передовые, самые эффективные препараты.
— Наши российские ингибиторы янус-киназы не уступают ли зарубежным?
— Строго говоря, ингибиторы янус-киназы — это другой класс препаратов, это таргетные синтетические препараты. Уровень их производства в России не уступает импортным аналогам.
Вовремя начатое лечение — лучший результат
— Если лечение начато поздно, будут ли биологические препараты также эффективны?
— Окно возможности означает тот промежуток, в который все наши терапевтические воздействия могут привести к какому-то конкретному результату. Моделируем ситуацию: человек только заболел, ему сразу поставлен диагноз, сразу начато адекватное лечение. Если мы попали в это окно возможностей, мы можем сохранить функциональный статус человека практически неизменным.
Если мы начинаем лечение на более позднем этапе, мы можем лишь остановить прогрессию заболевания, подавить воспалительную активность, добиться, чтобы у человека были нормальные анализы. Но если в суставах или позвоночнике что-то уже разрушилось или наоборот что-то выросло, никакие препараты, в том числе и генно-инженерные, не смогут вернуть суставы или позвоночник в то состояние, которое было изначально.
Поэтому чем раньше поставлен правильный диагноз, чем раньше начато адекватное лечение, не обязательно генно-инженерное, тем лучше конечный результат. Чем позже поставлен диагноз, а такие ситуации, к сожалению, бывают, тем хуже результат, и мы можем только остановить процесс на том месте, когда мы начали работать.
— Если генно-инженерные препараты такие эффективные, почему их не используют как препараты первой линии, чтобы предотвратить инвалидизацию?
— Был такой подход у наших западных коллег. Были знаменитые европейские ревматологи, которые считали, что всех, кто только заболел, нужно лечить генно-инженерными препаратами. Но это не получило такого большого развития в силу определенных причин.
Во-первых, если мы сразу начнем применять генно-инженерные препараты, то нам дальше будет некуда отступать. Кроме того, есть люди, которым все эти препараты не помогают. Поэтому сначала надо пройти все этапы.
Человеку может помочь более простой препарат, и таких людей много: по статистике, один из препаратов, метотрексат, который является золотым стандартом в лечении ревматоидного артрита, помогает 70% пациентов, если он правильно назначается.
Во-вторых, как я уже говорил, — чем препарат сильнее, тем он опаснее.
Есть еще один аспект, о котором я не случайно говорю в последнюю очередь. Эти препараты имеют несравнимо большую стоимость, чем препараты первого ряда. И не надо думать, что это проблема исключительно нашей страны. Они имеют такую стоимость, которая является высокой для всех стран, какими бы богатыми они ни были. Поэтому, если назначать генно-инженерные препараты направо и налево, то, во-первых, мы получим очень много побочных эффектов, а во-вторых, ни у одного государства не хватит на это денег. Это просто и не нужно.
Генно-инженерные препараты — на всю жизнь
— Предположим, мы лечим пациента биологическими препаратами, ему стало лучше, мы добились ремиссии. Можно ли при каких-то диагнозах эти медикаменты отменить и больше на них не тратиться? Или сделать периоды между приемами больше?
— У большинства людей, которым по тем или иным причинам отменили эти препараты, через некоторое время заболевание возвращается.
Сейчас считается, что эти препараты работают ровно тогда, пока мы продолжаем их использовать. Поэтому нужно четко понимать, что в нашей специальности на сегодняшний день нет такого препарата, чтобы был какой-то конечный промежуток времени — например, год-два пролечиться и все будет хорошо, мы его отменим, человек выздоровел.
Сделать периоды между приемами длиннее можно, это стандартная практика. Если мы видим у пациента четкую, стойкую ремиссию, то есть отсутствие лабораторных, клинических симптомов заболевания, то можно рассматривать вопрос об урежении введения.
— Насколько человек привязан к тем препаратам, которые он принимает? Может ли он их заменить на аналогичные? Или тот набор, который ему назначают, он должен принимать пожизненно?
— Бывает по-разному. Я предпочитаю оригинальные препараты, не дженерики.
Второй момент: если человек идет на препарате, то менять его на другой, пусть даже с таким же действующим веществом, но другого производства, опасно, потому что препараты одинаковые, но ситуации бывают разные. Другое дело, что в силу разных, не всегда медицинских причин, нам приходится это делать. Например, какой-то препарат взял и пропал с российского рынка, тогда мы работаем с аналогом.
У нас есть большой опыт переключении с западных препаратов на их российские аналоги, и никакого отрицательного результата об этом переключении мы не получили. Наши препараты работают не хуже, чем их зарубежные аналоги, на которых пациенты шли изначально, а в некоторых ситуациях — даже лучше.

О клинике
— Если там, где живет пациент, нет ревматолога, а врачи-неспециалисты не могут поставить диагноз, как вы можете помочь?
— Ревматолог может поставить правильный диагноз и начать правильное адекватное лечение ровно на том моменте, когда пациент к нему попал. Мы можем госпитализировать человека из любого региона. Если человек хочет, он может приехать и получить специализированную ревматологическую помощь на самом высоком уровне.
— Каким образом пациент может приехать к вам, и какую часть работы можно сделать удаленно?
— Для того, чтобы понять, нужно человеку приезжать или нет, сначала хочется посмотреть на его медицинские документы. Причем очень часто присылают снимки, описания рентгенограммы. Это все здорово, но этого недостаточно. Нужна выписка, составленная врачом-терапевтом, где будет медицинским языком четко написано, чем человек болеет, какие результаты обследований и так далее. Если говорить о ревматологических больных, то эти документы смотрю я. Если мы понимаем, что можем помочь, человек может к нам приехать.
— Как проходит лечение пациента, который приехал из другого региона, сколько времени это занимает, к чему нужно быть готовым?
— Человек приезжает, предварительно оплачивает определенную сумму, потом мы с ним работаем. Как правило, средний срок госпитализации —10-12 дней. После чего менеджеры клиники считают, какая сумма была потрачена на лечение. Мы получаем разницу между оплаченной и итоговой суммой, и человек ее доплачивает.
В процессе работы все траты согласовываются с пациентом. Не может быть такой ситуации, что он пролечился, ему озвучили сумму, а денег не хватило. Мы заранее все с пациентом согласовываем, лечение проводится только по обоюдному согласию. Диагностические возможности у нас большие, мы можем сделать практически все. А чего сделать не можем, сделаем в другом месте.
— Как получают генно-инженерные препараты? Например, пациент приехал к вам на госпитализацию, получил лечение, назначения от вас, где он потом берет препараты?
— Лечение генно-инженерными препаратами входит в программу госгарантий, то есть государство берет на себя бремя финансирования лечения этими дорогостоящими препаратами. Подавляющее большинство пациентов, которые лечатся у нас и в других ревматологических центрах, получают лечение этими препаратами в рамках ОМС.
Моделируя ситуацию с пациентом из другого региона, получаем следующее: пациент приезжает, мы его обследуем, смотрим и решаем, что ему показаны генно-инженерные препараты. Варианты следующие: мы пишем рекомендации, он приезжает домой, а там уже через свою поликлинику, через свой Минздрав добивается того, чтобы ему этот медикамент, согласно рекомендациям федерального учреждения, давали по месту жительства. Есть небольшое количество пациентов из других регионов, которых мы взяли на себя, которые раз в месяц приезжают к нам на очередное введение препарата. Но стоит понимать, что возможности федеральных учреждений не беспредельны. Если к нам завтра приедет 300 человек из других регионов, мы всем можем начать давать медпрепараты, потом квоты закончатся и все, все эти люди вместе с нами останутся ни с чем.
Поэтому механизм следующий: мы даем рекомендации, пациент приезжает к себе домой, добивается получения этого препарата от государства или просто покупает его сам. Второй вариант встречается несравнимо реже, чем помощь государства.
Стоимость лечения
— Какой в среднем порядок цен при лечении этих трех заболеваний?
— Порядок цен может быть самый разный. Если говорить о средней стоимости обычной госпитализации (здесь выносим за скобки генно-инженерные препараты, потому что это совершенно отдельные суммы), то обычно госпитализация стоит в районе 40-50 тыс. руб .
Если говорить о генно-инженерных препаратах, то там разброс цен достаточно большой. Годовой курс таких лекарств в среднем стоит от 400 тыс. до 1,5 млн руб., в зависимости от используемого препарата.
— Какие из ряда этих препаратов самые дорогостоящие и от чего зависит цена?
— Стоимость препарата зависит от политики компании-производителя, стоимости затрат и т.д. Мы работаем с препаратами, которые есть на рынке, и мы никаким образом не можем влиять на их стоимость. Могу сказать, что напрямую от механизма действия цена не зависит. Конечно, есть супердорогие препараты, но это, опять же, связано не столько с механизмом действия, сколько с особенностями их производства.
Как найти хорошего ревматолога?
— Ревматологи специализируются на лечении какой-то конкретной ревматической болезни или это более универсальные специалисты?
— Любой из ревматологов по своему профессиональному стандарту обязан уметь лечить все ревматические заболевания.
В крупных ревматологических центрах, таких как Научно-исследовательский институт ревматологии им. В. А. Насоновой в Москве, есть отделения, занимающиеся ревматоидным артритом. Естественно, у докторов, которые там работают, больший опыт в лечении конкретного заболевания, хотя все остальное они тоже знают, просто с одним заболеванием больше работают.
Что касается нас, мы работаем со всем спектром заболеваний. Любой грамотный ревматолог обязан уметь лечить все эти заболевания.
Мифы о лечении биологическими препаратами
— С какими распространенными страхами пациентов вам приходилось сталкиваться?
— Один из распространенных страхов — это то, что люди начинают читать аннотации к лекарственным препаратам, видят там раздел побочных эффектов, который обычно занимает несколько страниц мелким шрифтом, и пугаются.
Сейчас этого гораздо меньше, но когда эра генно-инженерных препаратов в России только начиналась, были люди, которые отказывались от лечения именно из соображений, что препараты сильнодействующие и, мягко говоря, не полезны для здоровья. На это я всегда пациентам отвечаю только одно: вы считаете, что с заболеванием жить лучше? Это, возможно, звучит жестко, но когда перед тобой сидит молодой мужчина или молодая женщина, не хочется, чтобы они въехали к тебе через 3-4 года на инвалидной коляске. А так, к сожалению, бывает.
Поэтому не надо бояться адекватного лечения, потому что все препараты, которые мы используем, назначаются только по показаниям и вероятность развития побочных значительно ниже, чем вероятность развития хорошего эффекта.
Еще одна точка зрения пациента, с которой мне приходится каждый день встречаться, когда он приходит, спрашиваешь: «Болит?», он говорит: «Болит». Мы предлагаем ему для снижения боли что-то попринимать, но он говорит: «Нет, мне не нужно обезболивания, мне нужно лечение». Я всегда задаю следующий вопрос: «А если бы у вас ничего не болело, вы бы ко мне пришли?». 99% отвечают, что нет, не пришли бы. Поэтому лечение боли и использование обезболивающих препаратов — это очень важная часть лечения. Вообще, когда у человека что-то болит, первое и главное, что должен сделать доктор любой специальности — это помочь человеку, а уже дальше — его обследовать, думать о том, какие препараты надо использовать.
— Представьте, что вы обращаетесь к пациенту, у которого болезнь по вашему профилю и он раздумывает о поездке к грамотному ревматологу, в хорошее учреждение. Что бы вы могли ему пожелать?
— Этому пациенту я бы мог пожелает все-таки собрать волю в кулак и дойти до хорошего ревматолога, потому что чем раньше и чем правильнее будет поставлен диагноз, тем лучше конечный результат лечения. Не нужно думать, что все пройдет само. К сожалению, заболевания, которыми мы занимаемся, сами не проходят. Чтобы человеку помочь как можно лучше, нужно это сделать как можно раньше и как можно правильнее.
Как найти врача и клинику?
Для того, чтобы найти клинику и доктора, кто возьмется и поможет при системных ревматологических заболеваниях, если вы готовы ехать за назначениями и на терапевтический курс в столицу или другой город, запишитесь по телефону: +7-967-077-5750 или заполните форму обращения выше. Фотографии и имеющиеся обследования направьте на russianhospitals@yandex.com. Портал сотрудничает с ведущими центрами и отделениями ревматологии в РФ.
Интервью записано 27 апреля 2023 года.
Беседовал наш коллега Максим Троянский специально для национального портала медицинского туризма RussianHospitals.

Содержание
1
Генно-инженерные препараты (ГИП) – это лекарственные средства, полученные с помощью биотехнологии, то есть изменения генетического материала живых организмов. Они имеют множество преимуществ перед традиционными лекарствами, так как они способны более точно и эффективно воздействовать на конкретные молекулы, ответственные за развитие заболеваний. ГИП широко используются в различных областях медицины, таких как онкология, иммунология, ревматология, эндокринология и другие.
Как создаются генно-инженерные препараты?
Для создания ГИП необходимо сначала выделить ген, кодирующий интересующий нас белок, например, антитело или гормон. Затем этот ген вставляют в клетку-продуцент, которая может быть бактерией, дрожжами, животной или растительной клеткой. Клетка-продуцент начинает синтезировать желаемый белок, который затем очищают и подготавливают к применению. Таким образом, получаются высокочистые и высокоактивные препараты, которые могут быть введены в организм человека.
Какие их виды существуют?
Существует несколько классов ГИП, в зависимости от их структуры и механизма действия. Самые распространенные из них – это:
- Моноклональные антитела – это белки, специфически связывающиеся с определенными антигенами, то есть веществами, вызывающими иммунный ответ. Они могут блокировать активность антигенов, усиливать иммунный ответ, доставлять лекарства или радиоактивные изотопы в опухоль и т.д. Примеры моноклональных антител: адалимумаб, этанерцепт, трастузумаб, ритуксимаб и другие.
- Рекомбинантные белки – это белки, полученные путем введения гена человека в геном другого организма. Они могут заменять недостающие или дефектные белки в организме человека, регулировать обмен веществ, стимулировать рост и регенерацию тканей и т.д. Примеры рекомбинантных белков: инсулин, эритропоэтин, интерфероны, факторы свертывания крови и другие.
- Генная терапия – это введение искусственных или модифицированных генов в клетки человека с целью исправления генетических дефектов, усиления иммунитета, борьбы с инфекциями или опухолями. Она может быть проведена с помощью вирусных или не вирусных векторов, то есть переносчиков генетического материала. Примеры генной терапии: лечение наследственных иммунодефицитов, гемофилии, слепоты и других заболеваний.
Преимущества и риски
ГИП имеют ряд преимуществ перед обычными лекарствами, такие как:
- Высокая специфичность – ГИП могут целенаправленно воздействовать на причину заболевания, не затрагивая другие системы и органы. Это позволяет уменьшить побочные эффекты и повысить эффективность лечения.
- Высокая активность – ГИП могут иметь более сильное и длительное действие, чем обычные лекарства, так как они не разрушаются в желудочно-кишечном тракте и не подвергаются метаболизму в печени. Это позволяет снизить дозировку и частоту введения препаратов.
- Высокая безопасность – ГИП могут быть более совместимы с организмом человека, так как они созданы на основе человеческих или похожих на них белков. Это позволяет снизить риск аллергических реакций и иммунного отторжения.
Однако, ГИП также имеют ряд рисков и ограничений, такие как:
- Высокая стоимость – ГИП требуют сложных и дорогостоящих технологий для их создания, контроля и хранения. Это делает их недоступными для многих пациентов и стран.
- Недостаточная изученность – ГИП являются относительно новыми препаратами, поэтому их долгосрочные эффекты и взаимодействие с другими лекарствами могут быть не полностью известны. Это требует постоянного мониторинга и наблюдения за пациентами, получающими ГИП.
- Возможные осложнения – ГИП могут вызывать нежелательные реакции, такие как инфекции, воспаления, анемия, тромбоцитопения, антифосфолипидный синдром, аутоиммунные заболевания и другие. Это требует индивидуального подбора препаратов и доз, а также профилактики и лечения осложнений.
Новые препараты генной инженерии
Карт-терапия – это вид генной терапии, при котором извлекаются иммунные клетки пациента (Т-лимфоциты), модифицируются генетически так, чтобы они вырабатывали специальные рецепторы, способные распознавать и уничтожать опухолевые клетки, и возвращаются обратно в организм пациента. Примеры карт-терапии: тисагенлеклеуцел, аксикабтаген цилолеуцел, брентуксимаб ведотин и другие.
РНК-препараты – это препараты, содержащие молекулы РНК, которые могут влиять на экспрессию генов в клетках. РНК-препараты могут быть разных типов, таких как малые вмешивающиеся РНК (siRNA), микро-РНК (miRNA), мессенджер-РНК (mRNA) и другие. РНК-препараты могут подавлять или активировать синтез белков, необходимых для развития или лечения заболеваний. Примеры РНК-препаратов: патисиран, инклисиран, вакцины против COVID-19 на основе mRNA и другие.
Еще 61 статья о веществах препаратов смотрите тут 👈
Криспр-препараты – это препараты, использующие систему кластеризованных коротких повторов и ассоциированных белков (CRISPR-Cas), которая позволяет точно и быстро редактировать геном в любом месте. Криспр-препараты могут исправлять мутации, вставлять или удалять гены, регулировать экспрессию генов и т.д. Примеры криспр-препаратов: лечение наследственных анемий, цистического фиброза, генетических заболеваний печени и других заболеваний.
Фоллистим: Гормон, стимулирующий рост и созревание яйцеклеток в яичниках и используемый для лечения бесплодия у женщин. Фоллистим производится по технологии рекомбинантной ДНК с использованием клеток яичников китайского хомячка.
Zolgensma: Генная терапия, которая лечит спинальную мышечную атрофию, редкое и смертельное генетическое заболевание, поражающее нервные клетки и функции мышц. Zolgensma доставляет функциональную копию гена SMN1 в клетки, восстанавливая их способность вырабатывать жизненно важный протеин.
Препараты ГИП в ревматологии
Генно-инженерные препараты в ревматологии – это лекарственные средства, которые воздействуют на иммунную систему, участвующую в развитии воспалительных и аутоиммунных заболеваний суставов, костей, мышц и других тканей. Применяются чаще всего для лечения ревматоидного артрита. Они могут быть разных типов, в зависимости от их цели и механизма действия. Среди них можно выделить следующие группы:
- Ингибиторы фактора некроза опухоли (иФНО) – это препараты, которые блокируют действие цитокина ФНО, который играет ключевую роль в запуске и поддержании воспаления. ИФНО могут быть человеческими, гуманизированными или химерными антителами к рецепторам или солубльным формам ФНО. Примеры иФНО: инфликсимаб, адалимумаб, этанерцепт, голимумаб, цертолизумаб пегол и другие. ИФНО применяются для лечения ревматоидного артрита, псориатического артрита, анкилозирующего спондилита, ювенильного идиопатического артрита и других заболеваний.
- Ингибиторы интерлейкина 6 (иИЛ6) – это препараты, которые блокируют действие цитокина ИЛ6, который стимулирует продукцию воспалительных медиаторов, активацию Т- и В-лимфоцитов, синтез антител и факторов роста. ИИЛ6 могут быть антителами к рецепторам или солубльным формам ИЛ6. Примеры иИЛ6: тоцилизумаб, сарилимумаб, клазакинумаб и другие. ИИЛ6 применяются для лечения ревматоидного артрита, системной красной волчанки, васкулитов и других заболеваний.
- Ингибиторы интерлейкина 1 (иИЛ1) – это препараты, которые блокируют действие цитокина ИЛ1, который участвует в регуляции иммунного ответа, температуры тела, аппетита, сна и других функций. ИИЛ1 могут быть антителами к рецепторам или солубльным формам ИЛ1. Примеры иИЛ1: анакинра, канакинумаб, рилонакепт и другие. ИИЛ1 применяются для лечения семейной средиземноморской лихорадки, криопирин-ассоциированных периодических синдромов, ювенильного идиопатического артрита и других заболеваний.
- Ингибиторы интерлейкина 17 (иИЛ17) – это препараты, которые блокируют действие цитокина ИЛ17, который способствует развитию хронического воспаления, ангиогенеза, фиброза и остеокластогенеза. ИИЛ17 могут быть антителами к рецепторам или солубльным формам ИЛ17. Примеры иИЛ17: секукинумаб, иксекизумаб, бродалумаб и другие. ИИЛ17 применяются для лечения псориатического артрита, анкилозирующего спондилита, псориаза и других заболеваний.
- Ингибиторы интерлейкина 23 (иИЛ23) – это препараты, которые блокируют действие цитокина ИЛ23, который регулирует дифференциацию и функцию Т-хелперов 17, которые вырабатывают ИЛ17. ИИЛ23 могут быть антителами к солубльным формам ИЛ23. Примеры иИЛ23: гуселкумаб, тилдракизумаб, ризанкизумаб и другие. ИИЛ23 применяются для лечения псориатического артрита, псориаза и других заболеваний.
- Ингибиторы Янус-киназ (иЯК) – это препараты, которые блокируют действие ферментов Янус-киназ, которые передают сигналы от рецепторов цитокинов в ядро клетки, активируя транскрипционные факторы. ИЯК могут быть малыми молекулами, проникающими в клетку и связывающимися с активными центрами Янус-киназ. Примеры иЯК: тофацитиниб, барицитиниб, упадацитиниб и другие. ИЯК применяются для лечения ревматоидного артрита, псориатического артрита, артрита при болезни Крона и других заболеваний.
Генно-инженерные препараты в ревматологии позволяют достичь высокой эффективности и ремиссии заболеваний, которые ранее считались неизлечимыми или трудно поддающимися терапии. Однако, они также имеют ряд побочных эффектов и противопоказаний. ГИП – это современное и перспективное направление в ревматологии, которое открывает новые возможности для улучшения качества жизни и здоровья многих пациентов.
Выводы
Генно инженерные препараты – это современные лекарственные средства, которые имеют большой потенциал в лечении различных заболеваний. Они основаны на использовании биотехнологии, то есть изменении генетического материала живых организмов. Они могут быть разных видов, в зависимости от их структуры и механизма действия. ГИП имеют ряд преимуществ, таких как высокая специфичность, активность и безопасность, но также имеют ряд рисков и ограничений, таких как высокая стоимость, недостаточная изученность и возможные осложнения. Они требуют ответственного и компетентного подхода к их применению, контролю и развитию. ГИП – это перспективное направление в медицине, которое может значительно улучшить качество жизни и здоровье многих людей.
Задайте вопрос и получите мгновенный ответ
от искусственного интеллекта
Еще 134 статьи смотрите тут
Использование материалов сайта означает принятие пользовательского соглашения. Информация предоставлена исключительно в ознакомительных целях и не является рекламой. Имеются противопоказания, обратитесь к врачу.
15824
09.02.2024
Вещества препаратов;
