Оригинальный отечественный препарат Димефосфон (диметилоксобутилфосфонилдиметилат) был синтезирован в 1952 г. А. Н. Пудовиком в Институте органической и физической химии им. А. Е. Арбузова[1]. Он относится к группе метаболиков и представляет собой диметиловый эфир 1,1-диметил-3-оксобутилфосфоновой кислоты, обладающий антиацидотическим и антиоксидантным действием. Димефосфон выпускается с 1983 г., в ходе клинического применения обнаружилась также вазо- и нейротропная активность препарата.
Антиоксидантное действие реализуется за счет предотвращения активации перекисного окисления липидов и повышения активности антиоксидантных ферментов в тканях головного мозга[8].
Димефосфон усиливает энергетические процессы в мозге как напрямую — воздействуя непосредственно на митохондрии, — так и косвенно — стимулируя и повышая потребление тканями тиреоидных гормонов, что сопровождается активизацией энергетических и катаболических процессов в митохондриях клеток. Он проявляет также свойства некоторых нейротрансмиттеров: обладает ГАМК-ергической, Н-холино- и дофаминергической активностью.
Антиацидотическое действие препарата реализуется за счет интенсификации почечного и легочного механизмов регуляции кислотно-щелочного состояния, усиления внутриорганного кровотока и тканевого метаболизма. Кроме того, при применении Димефосфона уменьшается содержание молочной и пировиноградной кислот в тканях головного мозга. В отличие от известных антиацидотических средств, непосредственно влияющих на кислотность крови путем введения соответствующего щелочного раствора, препарат производит свой эффект за счет вмешательства в метаболические процессы.
Одним из наиболее ценных свойств Димефосфона является его способность воздействовать на механизмы регуляции мозгового кровообращения и функции нервной системы. Экспериментально установлено, что препарат уменьшает явления циркуляторной гипоксии, улучшает регуляцию мозгового кровообращения, нормализует реактивность церебральных сосудов и кровенаполнение мозга и улучшает венозный отток. Кроме этого, Димефосфон нормализует нейромедиацию, благоприятно влияет на электрическую активность головного мозга, восстанавливает цикл «сон — бодрствование»[1].
Недавно в электрофизиологических исследованиях на нервно-мышечном синапсе было продемонстрировано, что Димефосфон обладает свойством блокировать ионные каналы. Это объясняет, почему он, подобно фенитоину, проявляет противосудорожную и антиаритмическую активность. Каналоблокирующее свойство Димефосфона, возможно, имеет прямое отношение к кальцийзависимым эффектам этого препарата[2].
Лекарственное средство выпускается в форме 15%-го раствора для приема внутрь во флаконах по 100 и 200 мл.
Наличие вазоактивного, нейропротективного, антиоксидантного, антигипоксантного и нейротропного эффектов Димефосфона обосновывает возможность его применения при различных формах церебральной патологии. За более чем 30-летний период использования Димефосфона в практической медицине проведены многочисленные клинические исследования, продемонстрировавшие его эффективность при различных формах патологии нервной системы.
Многолетнее экспериментально-клиническое исследование по оценке эффективности Димефосфона в лечении пострадавших с ЧМТ проводилось в Казани[6]. За 7 лет в отделении реанимации были пролечены 2324 пациента с тяжелой ЧМТ, в схему лечения которых входил Димефосфон. При сравнении процессов восстановления сознания и рефлексов на фоне применения препарата и без него отмечена более быстрая положительная динамика в отношении появления сознания, восстановления адекватности поведения и рефлексов у больных, получавших Димефосфон. При применении Димефосфона ускорялась нормализация дыхания и системной гемодинамики, препарат способствовал быстрому регрессу очаговой стволовой и полушарной симптоматики. В результате было зарегистрировано снижение среднего показателя летальности у пациентов с тяжелой ЧМТ до 27% против 38,6% в предыдущий период, когда Димефосфон не входил в курс лечения. Таким образом, включение Димефосфона в комплексное лечение больных с тяжелой ЧМТ привело к снижению летальности на 30%.
В 1994 г. были опубликованы результаты исследования по оценке влияния Димефосфона на систему регуляции церебрального кровообращения у больных с новообразованиями головного мозга[5]. Наблюдались 53 пациента в возрасте от 5 до 66 лет с опухолями различной гистологической структуры супра- и субтенториальной локализации, получавшие монотерапию Димефосфоном. Было показано, что пятидневный курс лечения Димефосфоном (30 мг/кг внутрь 3 раза в день) в дооперационном периоде улучшает регуляцию мозгового кровообращения у больных с церебральными опухолями. Препарат восстанавливал линейную скорость кровотока во внутренних яремных венах и нарушенные реакции пульсового кровенаполнения на унифицированную антиортостатическую нагрузку. Одновременно нормализовались реакции внутренних сонных артерий и основной артерии на нагрузку с ингаляцией карбогена. В условиях высокого внутричерепного давления, обусловленного дополнительным объемным опухолевым процессом, ликворной гипертензией и отеком головного мозга, применение препарата приводило к восстановлению деятельности регуляторных механизмов циркуляторного обеспечения как химического, так и физического гомеостаза и повышало их толерантность к операционной травме. В процессе лечения отмечались уменьшение двигательных и речевых расстройств, ослабление головной боли, улучшение сна, стабилизация гемодинамики и дыхания.
У больных, получавших Димефосфон до операции, уже к концу первых суток рядом с областью хирургического вмешательства регистрировалась нормальная реактивность мозговых сосудов, в отличие от пациентов, не получавших Димефосфон в качестве предоперационной фармакологической коррекции[5].
Димефосфон также продемонстрировал хороший эффект при лечении 49 больных с нарушениями мозгового кровообращения, обусловленными операционной травмой и тромбозом внутренних сонных артерий[12]. Больные принимали по 15 мл препарата 3 раза в день в течение 14 дней. При нарушениях мозгового кровообращения, обусловленных операционной травмой, на фоне курсового применения препарата происходил быстрый регресс неврологических нарушений. Димефосфон хорошо купировал головную боль, обусловленную спазмом сосудов. При выраженном спазме периферических отделов средней мозговой артерии с помощью транскраниальной доплерографии обнаруживали снижение повышенных значений систолической и средней скорости кровотока и нормализацию систоло-диастолического коэффициента. Методом водородного клиренса было выявлено нормализующее влияние Димефосфона на исходно низкую реактивность церебральных сосудов.
У больных с последствиями тромбоза внутренних сонных артерий на фоне курсового применения Димефосфона уменьшались двигательные и речевые нарушения. При этом препарат эффективно устранял мигренеподобную головную боль. Длительность анальгетического действия при разовом приеме составляла до трех часов. Димефосфон хорошо переносился пациентами: побочных явлений со стороны ЖКТ не отмечалось, местные и аллергические реакции отсутствовали[12].
На базе НИИ нейрохирургии им. Н. Н. Бурденко была проведена оценка влияния Димефосфона на функциональное состояние стволовых структур у нейрохирургических больных в раннем послеоперационном периоде[15]. У пациентов после удаления опухолей гипоталамо-гипофизарной и понтобульбарной локализации с клиникой транзиторного ишемического поражения мозга, нарушением сознания при сохранных центральных механизмах висцерально-вегетативной регуляции применение Димефосфона в суточной дозе 40–60 мг/кг обеспечивало регресс общемозговой и очаговой симптоматики начиная со 2–3-х суток от начала терапии. При этом наблюдалась тенденция к нормализации паттерна ЭЭГ.
У больных с опухолями гипоталамо-гипофизарной локализации, получавших Димефосфон, в сравнении с контрольной группой, где этот препарат не применялся, наблюдалась тенденция к более быстрому восстановлению объема циркулирующей крови после оперативного вмешательства, что, вероятно, было обусловлено нормализацией функций паравентрикулярных ядер гипоталамуса. При опухолях IV желудочка применение Димефосфона позволяло предотвратить развитие сердечной недостаточности центрального генеза. Аналогичный стресспротективный эффект Димефосфона отмечался у больных в остром периоде ЧМТ, при этом наиболее выраженным он был при симптомах поражения срединно-базилярных структур мозга. У пациентов, получавших Димефосфон, отмечалась тенденция к уменьшению глубины нарушения сознания[15].
В 1996 г. были опубликованы результаты применения Димефосфона при лечении синдрома Меньера[16]. В условиях стационара 30 пациентов в возрасте от 26 до 70 лет получали монотерапию препаратом в суточной дозе 45 мл в течение 2–3 недель. Длительность наблюдения пролеченных больных составляла 1,5 года. Стабильный положительный эффект отмечался у 67% пациентов. При этом наилучшие результаты прослеживались при сравнительно небольшой продолжительности заболевания (до 5 лет), одностороннем поражении лабиринта, вестибулярных расстройствах в дебюте болезни. При «кохлеарном» начале заболевания эффективность лечения составляла 50%. Полученные данные о положительном влиянии Димефосфона у больных с поражением периферического звена кохлеовестибулярного анализатора вследствие гидропса лабиринта, вероятнее всего, связаны с антиацидотическим эффектом препарата, а также с его благоприятным воздействием на микроциркуляцию в сосудах вертебробазилярной системы.
По результатам клинического испытания препарата Димефосфон[11], у пациентов с синдромом вегетативной дистонии его трехнедельный курс приводил к улучшению субъективного статуса: у больных уменьшались головная боль и головокружение, улучшался сон, сглаживались явления ипохондрии и раздражительности. Уменьшались проявления ангиодистонии, стабилизировались пульс и уровень АД. Тенденция к нивелированию дистонии сосудов мозга прослеживалась на результатах реоэнцефалографии. Среди пациентов, страдавших мигренью, купирования приступов головной боли под действием Димефосфона отмечено не было, частота приступов оставалась неизменной в течение всего времени приема препарата. В то же время в межприступном периоде большинство пациентов отмечали субъективное улучшение состояния: исчезали неврозоподобные наслоения, улучшался сон, уменьшались сенестопатические проявления.
Изучено влияние Димефосфона на динамику неврологического дефицита у больных с заболеваниями спинного мозга и его корешков[7]. Димефосфон назначался внутрь по 15 мл (2,25 мг) 3–4 раза в день в течение 2–3 недель. У 14 пациентов с радикулопатией после удаления грыжи межпозвоночного диска на 3–4-е сутки лечения препаратом исчезали корешковые боли и онемение в проекции дерматомов пораженных корешков. При нарушениях спинального кровообращения, обусловленных дисциркуляторной миелопатией, под воздействием Димефосфона значительно уменьшались органические нарушения: регрессировал парапарез и восстанавливались функции органов малого таза.
Авторы приводят также результаты лечения больной с нижней параплегией после тотального удаления экстрамедуллярной опухоли спинного мозга. На фоне лечения Димефосфоном отмечались быстрый регресс двигательных нарушений, потепление ниже верхнего уровня проводниковых расстройств и уменьшение болей в ногах[7].
Проанализированы результаты лечения больных с хроническим нарушением мозгового кровообращения в вертебробазилярном бассейне в возрасте от 26 до 60 лет, принимавших Димефосфон в течение 3 недель[10]. При вертебробазилярной сосудистой недостаточности Димефосфон уменьшал головные боли, головокружение, шум в ушах, неустойчивость походки, а также улучшал память и концентрацию внимания. Корригирующее действие Димефосфона в вертебробазилярном бассейне было связано с торможением развития отека ткани и улучшением реологии циркулирующих эритроцитов. Препарат сглаживает сдвиги микрокровенаполнения спинного и продолговатого мозга и оказывает антигипоксическое действие на мозговые структуры.
В исследованиях, проведенных в Казанской государственной медицинской академии, установлено, что Димефосфон может благоприятно влиять на клиническое течение рассеянного склероза[9]. Исследователи наблюдали 21 больного с церебральной формой рассеянного склероза, чей средний возраст составил 32,6 года. Димефосфон назначался перорально по 15 мл (2,25 мг) 3 раза в день в течение 10 дней. Клиническое улучшение наблюдалось у 16 больных (76,2%). Субъективно оно выражалось в улучшении самочувствия и повышении настроения. Объективно наблюдалось уменьшение тремора и шаткости при ходьбе. В ряде случаев исчезал нистагм, нарастала сила в ногах. Улучшались проприоцептивные рефлексы, в части наблюдений уменьшалась спастичность. Побочных явлений и ухудшения течения заболевания во время приема препарата отмечено не было.
Эффективность Димефосфона у пациентов с ишемическим инсультом и дисциркуляторной энцефалопатией (ДЭ) исследовалась в работе коллектива Центрального военного клинического госпиталя им. П. В. Мандрыка (г. Москва)[4]. В течение 20–25 дней 50 пациентов в возрасте 64–80 лет с этой формой церебральной патологии принимали Димефосфон внутрь в суточной дозе 45 мл. На фоне приема препарата уменьшались или полностью прекращались головная боль, головокружение, а также происходило улучшение памяти. В ряде случаев исчезали клинические проявления острого вестибулярного синдрома. При проведении ультразвуковой эхопульсографии основной артерии отмечалось увеличение ее просвета на фоне приема Димефосфона. При этом препарат, не обладая выраженным сосудорасширяющим эффектом, оказывал положительное влияние на метаболизм ишемизированной ткани мозга. Лечение хорошо переносилось больными.
На базе Института клинической и экспериментальной неврологии им. П. М. Сараджишвили (Грузия) было выполнено исследование эффективности препарата Димефосфон при острых и хронических сосудистых заболеваниях головного мозга в сравнении с циннаризином[13]. Под наблюдением находились 54 пациента с острыми нарушениями мозгового кровообращения (ишемический и геморрагический инсульты) и 102 — с хроническими.
Димефосфон оказался более эффективным в отношении проявлений вестибулярной дисфункции и при острых, и при хронических нарушениях мозгового кровообращения. У пациентов с мозговым инсультом на фоне терапии Димефосфоном через 3–4 дня улучшалось общее состояние, уменьшались очаговые симптомы. Положительная динамика чаще отмечалась при локализации очага в вертебробазилярном бассейне. В 42,6% случаев ишемического инсульта регистрировалось полное выздоровление. При хронических нарушениях мозгового кровообращения уже на 2–3-и сутки приема Димефосфона наблюдалось уменьшение как субъективных вестибулярных нарушений, так и объективных: нистагма, вестибулярной гипо- или гиперрефлексии, нарушения равновесия в простой и сенсибилизированной позах Ромберга. По сравнению с применением циннаризина регресс вестибуло-атактического синдрома при приеме Димефосфона наступал в более короткие сроки и был более стойким[13].
С целью оценки возможности, эффективности и безопасности применения препарата Димефосфон у больных ДЭ в 2013 г. на кафедре нервных болезней Института профессионального образования Первого Московского государственного медицинского университета им. И. М. Сеченова было проведено открытое сравнительное исследование по изучению эффективности трех методов лечения немоторных проявлений ДЭ: монотерапии Димефосфоном, использования Димефосфона в комбинации с винпоцетином, а также изолированного применения винпоцетина[14].
МАТЕРИАЛЫ И МЕТОДЫ
В исследовании приняли участие 58 пациентов с разными стадиями ДЭ. Средний возраст больных составил 70,4 ± 7,0 года (от 60 до 83 лет); мужчин было 13, женщин — 45. Первая стадия ДЭ имелась у 8,6%, вторая — у 84,5%, третья — у 6,9% больных.
В зависимости от метода лечения были сформированы три группы пациентов: монотерапии винпоцетином (n = 20), монотерапии Димефосфоном (n = 20) и комбинированного лечения Димефосфоном и винпоцетином (n = 18). Группы не имели статистически значимых различий по возрастному и половому составу, а также по степени тяжести ДЭ.
Димефосфон назначался в дозе 45 мл/сут, винпоцетин — в дозе 15 мг/сут. При комбинированном приеме больные принимали Димефосфон вместе с винпоцетином. Курс приема препаратов составлял 21 день.
У всех пациентов перед началом лечения оценивали когнитивные возможности при помощи шкалы краткой оценки психического статуса (Mini-Mental State Examination — MMSE), эмоциональный статус посредством госпитальной шкалы тревоги и депрессии, а также качество сна при помощи анкеты балльной оценки субъективных характеристик сна. Повторное тестирование по тем же шкалам выполняли на 21-й день лечения, результаты вносили в амбулаторные карты пациентов.
При статистическом анализе использовали критерий Хи-квадрат Пирсона с поправкой Бонферрони для множественных сравнений. Различия показателей в группах считали статистически значимыми при значениях p < 0,05.
РЕЗУЛЬТАТЫ
В таблице приведены сравнительные данные групп исследования по количеству пациентов, которые получили улучшение по какому-либо из оценивавшихся немоторных показателей. Респондеры были определены по суммарным баллам соответствующих опросников — улучшением считали их изменение более чем на 0%.
Таблица
Количество пациентов с улучшением немоторных проявлений дисциркуляторной энцефалопатии на фоне лечения, n (%)
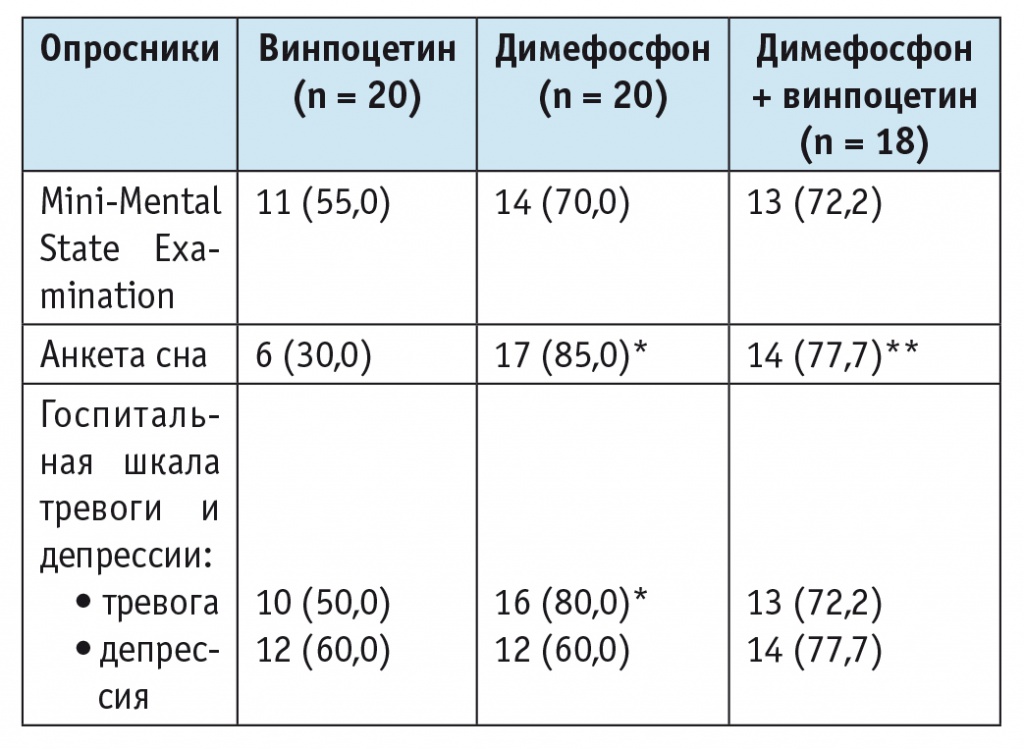
* Отличия группы больных, принимавших только Димефосфон, от группы монотерапии винпоцетином статистически значимы (p < 0,05).
** Отличие группы больных, принимавших Димефосфон с винпоцетином, от группы монотерапии винпоцетином статистически значимо (p < 0,05).
Примечание. Респондеров по отдельно взятым немоторным показателям определяли по изменению суммарных баллов соответствующих опросников более чем на 0%.
Как видно из этой таблицы, в группах пациентов, получавших Димефосфон в виде монотерапии и Димефосфон вместе с винпоцетином, наблюдалось большее число респондеров по всем шкалам. Монотерапия Димефосфоном в наибольшей степени способствовала улучшению субъективной оценки сна и снижению уровня тревоги. Комбинированное применение Димефосфона и винпоцетина сопровождалось наиболее выраженной позитивной динамикой показателей по шкале MMSE и уровня депрессии по госпитальной шкале.
В период лечения некоторые больные, получавшие только Димефосфон, жаловались на боль в желудке и изжогу, однако эти ощущения не потребовали отмены препарата. При приеме Димефосфона с винпоцетином в течение курса лечения отмечались однократный подъем АД до 160 мм рт. ст. (у одного пациента), боль в желудке (у двух пациентов), изжога и пошатывание при ходьбе (у одного пациента). На фоне изолированного приема винпоцетина побочных эффектов не наблюдалось.
ОБСУЖДЕНИЕ
Полученные в настоящем исследовании результаты подтвердили эффективность Димефосфона в лечении немоторных проявлений ДЭ. Эффект Димефосфона — препарата, относящегося к группе антиацидотических средств, — оказался сопоставимым с эффектом винпоцетина — «классического» сосудорасширяющего средства, улучшающего мозговое кровообращение. Известно, что главным механизмом действия винпоцетина на мозговой кровоток является его антивазоконстрикторное влияние[17]. Данный эффект реализуется за счет блокирования сосудистых норадренергических реакций. Клинический эффект Димефосфона определяется нормализацией кислотно-щелочного состояния при ацидозах различной этиологии, благодаря чему препарат оказывает вазоактивное, антиоксидантное и мембраностабилизирующее действие. В нашем исследовании применение Димефосфона у пациентов с хронической сосудистой мозговой недостаточностью в течение 21 дня сопровождалось статистически значимым (p < 0,05) улучшением когнитивных функций и показателей сна, а также снижением уровня тревоги.
Среди оценивавшихся немоторных нарушений на фоне применения Димефосфона в наибольшей степени улучшались субъективные характеристики сна. Это наблюдение представляется нам очень важным, поскольку для пациентов пожилого и старческого возраста характерна высокая распространенность нарушений сна[3]. Повышение качества сна при приеме Димефосфона может способствовать снижению дозы уже принимаемых снотворных препаратов, использование которых среди пациентов старших возрастных групп должно быть ограниченным в связи с нежелательными побочными эффектами.
Наибольшая степень снижения немоторных расстройств при хронической сосудистой мозговой недостаточности наблюдалась при проведении комбинированного лечения Димефосфоном в сочетании с винпоцетином. Наряду с улучшением показателей сна, когнитивного функционирования и снижением уровня тревоги на фоне комбинированной терапии отмечалось и снижение уровня депрессии.
Исследование показало хорошую переносимость препарата Димефосфон. Побочные явления были отмечены только в 12% случаев. Наблюдались симптомы раздражения верхних отделов ЖКТ — боль в желудке и изжога. Все побочные реакции имели легкую степень выраженности и не требовали отмены препарата или назначения корригирующей терапии. В целом данные по переносимости Димефосфона, полученные в нашей работе, сопоставимы с результатами упомянутых исследований и данными обзора Л. З. Подорожанской и соавт. (1996)[4, 7, 9, 11–13].
ЗАКЛЮЧЕНИЕ
Приведенные результаты применения Димефосфона, включая данные, полученные в нашем собственном исследовании, демонстрируют наличие клинически значимого эффекта препарата при различных формах патологии ЦНС. Более чем 30-летняя история применения Димефосфона в отечественной неврологии и нейрохирургии позволяет констатировать наличие многообразных лекарственных эффектов препарата и высокий уровень безопасности его использования.
Введение
Диметилоксобутилфосфонилдиметилат (диметиловый эфир 1,1-диметил-3-оксобутилфосфоновой кислоты, молекулярная масса — 208,20 г/моль, брутто-формула С8Н17О4Р) относится к группе синтетических малотоксичных неантихолинэстеразных фосфорорганических соединений. Впервые был синтезирован в 1952 г. в Институте органической и физической химии им. А.Е. Арбузова Казанского филиала АН СССР [1] и на кафедре фармакологии Казанского государственного медицинского университета [2].
В 1983 г. диметилоксобутилфосфонилдиметилат был разрешен для клинического использования в лекарственной форме 15% водного раствора для приема внутрь и наружного применения, а с 1993 г. одобрен для парентерального введения [3]. Как было показано многими исследователями, диметилоксобутилфосфонилдиметилат обладает низкой токсичностью: его LD50 (доза, вызывающая гибель 50% животных) для мышей при внутрибрюшинном способе введения составила 2500±150 мг/кг, для крыс и морских свинок — 2200–2500 мг/кг [4–7].
В настоящее время диметилоксобутилфосфонилдиметилат (Димефосфон®) зарегистрирован для медицинского применения; он принадлежит к фармакотерапевтической группе «антиацидотическое средство». Препарат имеет высокую биодоступность и проникает через гистогематические барьеры; наибольшая его концентрация создается в головном мозге, селезенке и эритроцитах [8]. Диметилоксобутилфосфонилдиметилат оказывает антиацидотическое, мембраностабилизирующее, противовоспалительное и антиоксидантное действие, нормализует кровоток и метаболизм мозга, улучшает регуляцию кровообращения, в т. ч. мозгового, что подтверждается результатами многочисленных клинических исследований [9–19].
Механизмы действия диметилоксобутилфосфонилдиметилата
Гипотермическое действие при введении больших доздиметилоксобу тилфосфонилдиметилата выявлено на мышах, крысах и кроликах. Температура тела животных в эксперименте понижалась в течение 1 ч после введения дозы 2000 мг/кг (максимально переносимая доза), эффект сохранялся до 9 ч [20]. Важно отметить, что данный эффект был получен на животных при использовании доз значительно более высоких, чем терапевтическая (для терапевтических доз данный эффект не отмечался), но экспериментальные данные подчеркивают безопасность диметилоксобутилфосфонилдиметилата. Параллельно со снижением температуры тела данное лекарственное средство снижает потребление кислорода, но не повышает устойчивость организма к гипоксии. Препарат подавляет метаболические процессы в печени, о чем свидетельствует его способность продлевать наркотическое действие гексенала [20]. После введения диметилоксобутилфосфонилдиметилата выявлено усиление потребления кислорода митохондриями печени подопытных крыс во всех метаболических состояниях. При этом индекс дыхательного контроля по Чансу и Ларди и коэффициент фосфорилирования не изменялись, таким образом, усиление скоростей дыхания митохондрий печени подопытных крыс не обусловлено нарушением сопряженности дыхания и фосфорилирования митохондрий [21].
Противосудорожное действие диметилоксобутилфосфонилдиметилата было изучено при отравлении мышей стимуляторами центральной нервной системы (ЦНС): коразолом, стрихнином и камфорой. Для каждого судорожного агента были определены параметры токсичности на интактных животных и на животных, получивших диметилоксобутилфосфонилдиметилат в дозе 1000 мг/кг. Оценивали также способность уменьшать судороги и длительность латентного периода [22]. Результаты исследований показали, что наиболее сильный противосудорожный и антидотный эффект диметилоксобутилфосфонилдиметилата был проявлен в отношении коразола (антагонист ГАМК-рецепторов). Токсичность камфоры и стрихнина на фоне диметилоксобутилфосфонилдиметилата, наоборот, повышалась при одновременном снижении судорожной активности. Мишенью воздействия стрихнина являются глициновые рецепторы спинного мозга. Таким образом, исследователи делают вывод о том, что данное лекарственное средство, по-видимому, оказывает основное действие на головной мозг, и действие это носит мозаичный характер [22].
Диметилоксобутилфосфонилдиметилат является антидотом обратимых (прозерин, эзерин) и необратимых ингибиторов (октаметил и фосфакол) холинэстеразы [4]. Терапевтические эффекты диметилоксобутилфосфонилдиметилата у некоторых исследователей вызывают скептическое отношение, поскольку принято считать, что большинство синтетических фосфорорганических соединений угнетают ацетилхолинэстеразу (АХЭ) с последующим ингибированием ацетилхолина, что приводит к нарушению нейрогуморальной регуляции. Для изучения механизма антидотного действия диметилоксобутилфосфонилдиметилата проводились исследования по влиянию на активность холинэстеразы in vitro и in vivo. Было установлено, что in vitro диметилоксобутилфосфонилдиметилат не оказывал ни защитного, ни реактивирующего действия на холинэстеразу, в то время как in vivo повышал активность ингибированной холинэстеразы (ХЭ) мозга мышей [23]. Эти факты подтверждены нейрогистологическими и гистохимическими исследованиями. Установлено, что препарат не только не угнетает АХЭ, но даже повышает активность этого фермента [24]. При отравлении нибуфином наряду с повышением активности ХЭ в мозге, кишечнике и сыворотке, печени наблюдается снижение уровня указанного фермента [25]. Доказан антидотный эффект диметилоксобутилфосфонилдиметилата в отношении антихолинэстеразного хлорофоса. Диметилоксобутилфосфонилдиметилат также предупреждает развитие судорог, фасцикуляций и снижает токсичность при отравлении животных этим ингибитором ХЭ [26].
В работах А.У. Зиганшина и Р.С. Гараева изучена кинетика гидролиза ацетилхолина на фоне диметилоксобутилфосфонилдиметилата. Результаты экспериментов позволили предположить, что препарат взаимодействует с холинэстеразой (скорее по типу неспецифической сорбции), меняя конформационные свойства энзима [27].
Антиацидотическое действие диметилоксобутилфосфонилдиметилата реализуется за счет легочного и почечного механизмов регуляции кислотно-щелочного состояния; препарат ускоряет реабсорбцию бикарбонатов и активирует процессы ацидо- и аммониогенеза в почках, а также усиливает вентиляцию легких, повышает сниженные показатели рН, уменьшает дефицит оснований, понижает парциальное давление углекислоты и увеличивает количество стандартных и истинных бикарбонатов крови [3, 28, 29]. Кроме этого, диметилоксобутилфосфонилдиметилат повышает содержание цитохромов с, с1, а, а3 в митохондриальной мембране и активирует адаптогенный внешний путь свободного окисления НАДН*Н в митохондриях печени. В отличие от гидрокарбоната натрия, действие которого связано с химической нейтрализацией кислых продуктов крови, диметилоксобутилфосфонилдиметилат оказывает антиацидотическое действие, участвуя в метаболических процессах, в частности, нормализуя углеводный обмен в цикле Кребса и интенсифицируя распад глюкозы по пентозному циклу [28].
Вазоактивные свойства диметилоксобутилфосфонилдиметилата обусловлены влиянием на эндотелий микрососудов, что приводит к повышению синтеза NO и проявлению вазодилатирующего действия. На активацию и высвобождение NO из эндотелия сосудов также оказывают изменения концентрации Са2+ [30].
Вазодилатирующие свойства диметилоксобутилфосфонилдиметилата также обусловлены предупреждением высвобождения норадреналина из симпатических терминалей при ишемии [31] и блокированием сосудистых адренергических реакций [32].
Е. Н. Чуя и соавт. показали, что диметилоксобутилфосфонилдиметилат влияет на осцилляции концентрации внутриклеточного свободного Са2+ через мембраны гладкомышечных клеток (увеличение амплитуды пиогенных ритмов), что отражает активность локальных пейсмекеров внутри этих клеток сосудистой стенки [30].
Мембраностабилизирующий эффект диметилоксобутилфосфонилдиметилата, по всей видимости, также обусловлен Са2+--зависимой вазодилатацией и сопровождается снижением уровня внутриклеточного Са2+ [19]. Л.Е. Зиганшина (1988) изучала влияние препарата на стабильность мембран эритроцитов в гипотоничной среде в сравнении с эталонными противовоспалительными препаратами (ацетилсалициловая кислота и диклофенак). По результатам проведенного исследования было показано, что диметилоксобутилфосфонилдиметилат ослабляет осмотический гемолиз эритроцитов в более широком диапазоне концентраций, чем препараты сравнения [33].
Антигипоксическое действие. В основе любого типа гипоксии лежит дефицит АТФ, приводящий к однотипным метаболическим и структурным сдвигам в органах и тканях. Низкое содержание АТФ в клетках ингибирует ключевой фермент гликолиза — фосфофруктокиназу, тем самым способствуя активации анаэробного гликолиза и частично компенсируя дефицит АТФ, но приводит к повышению концентрации лактата и развитию ацидоза. Последний нарушает течение многих биохимических реакций и вместе с тем повышает активность некоторых фосфолипаз и протеаз, что в свою очередь ведет к увеличению распада фосфолипидов и белков, разрушению клеточных структур. Распад фосфолипидов и ингибирование их ресинтеза приводят к увеличению концентрации ненасыщенных жирных кислот и активизации их перекисного окисления. Активация перекисного окиследния липидов (ПОЛ) в итоге приводит к подавлению и истощению антиоксидантной системы (супероксиддисмутазы, каталазы и др.) вследствие активации распада и ингибирования ресинтеза белковых составляющих данной системы. Продукты ПОЛ, в свою очередь, усугубляют нарушение как структуры, так и функции мембран. Антигипоксический эффект диметилоксобутилфосфонилдиметилата связан с уменьшением продукции лактата в структурах головного мозга одновременно с повышением активности ключевых ферментов энергообеспечения клеток: НАДФ (диафораза, сукцинатдегидрогеназа и глицеро-6-фосфат-дегидрогеназа), что сопровождается увеличением АТФ и креатинфосфата [3].
Антиоксидантные свойства. Супероксиддисмутаза (СОД), каталаза (КТ), так же как и ферменты системы глутатиона, служат основными высокоспецифичными ферментами, оказывающими антиоксидантное действие и нейтрализующими такие активные формы кислорода, как супероксидный анион-радикал и перекись водорода. Система глутатиона нейтрализует перекиси липидов и, поддерживая в восстановленном состоянии SH-группу белков, обеспечивает их функциональную активность. Глутатионпероксидаза (ГП) — фермент, восстанавливающий перекись водорода и липоперекиси с одновременным окислением глутатиона (GSH). Антиоксидантные свойства диметилоксобутилфосфонилдиметилата связаны с повышением активности СОД, ГП и КТ, что приводит к блокированию ПОЛ, уменьшению степени повреждения тканей и ускорению процессов репарации [34].
Антиишемическое действие диметилоксобутилфосфонилдиметилата обусловлено его антигипоксическими и антиоксидантными свойствами [35].
Антиагрегантное действие связано с частичной блокадой трансмембранного транспорта кальция, что приводит к понижению скорости экспрессии высокоаффинных рецепторов к фибриногену [36, 37].
Диметилоксобутилфосфонилдиметилат подавляет спонтанную, АДФ- и адреналин-индуцированную агрегацию тромбоцитов, а также ингибирует ПОЛ [26, 38–40].
Противовоспалительные свойства диметилоксобутилфосфонилдиметилата при резорбтивном действии обусловлены снижением уровня гистамина в крови и тканях, стимулированием гистаминопексии сыворотки и повышением активности гистидазы кожи. На моделях воспаления с экссудативным компонентом диметилоксобутилфосфонилдиметилат проявляет антигистаминное и антисеротониновое действие, превосходящее по силе таковое димедрола [41].
В работах Е.Н. Шуваловой с соавт. (2003), Л.И. Анчиковой с соавт. [12, 13, 36, 42], В.Г. Малышева с соавт. [3] безопасность диметилоксобутилфосфонилдиметилата в опытах на животных доказана и к настоящему времени подтверждена на практике. В ходе исследований влияния диметилоксобутилфосфонилдиметилата на морфологию большинства органов и систем (сердца, печени, легких, гонад, почек, нервной и эндокринной систем, селезенки, лимфатических узлов) было установлено, что единственными органами с выявленными структурными изменениями были щитовидная железа, тимус и тимусзависимые зоны селезенки и лимфатических узлов, а также надпочечники. При анализе микропрепаратов в тканях щитовидной железы выявлены вакуолизация клеток фолликулярного эпителия, что характерно для гиперфункции щитовидной железы. Из биохимических показателей установлено достоверное снижение уровня пировиноградной кислоты (на 20%) и аскорбиновой кислоты в гомогенате надпочечников. Однако при длительном применении диметилоксобутилфосфонилдиметилата признаков атипичного роста клеток в этих органах выявлено не было, и при отмене препарата гистологическая структура возвращалась к исходным показателям.
В доклинических исследованиях на животных моделях Р.Ф. Тумакаевым было показано, что диметилоксобутилфосфонилдиметилат способствует репарации и восстановлению функций поврежденных отделов спинного мозга, действуя на сосудистое русло и нейрональную активность спинного мозга. Применение данного лекарственного средства облегчает восстановление нейронов в зоне контузии, приводит к уменьшению пула реагирующих мотонейронов и подпороговой каймы [43].
Согласно исследованиям, проведенным Д.В. Бурнашевой с соавт. [32, 44], диметилоксобутилфосфонилдиметилат не вызывает структурных изменений в нервных волокнах, нейронах внутри- и внеорганных ганглиев пищеварительной, дыхательной и мочеполовой систем. В работе Р.Х. Хафизьяновой [8], выполненной на беременных крысах, было установлено, что диметилоксобутилфосфонилдиметилат не обладает эмбриотоксическим эффектом (не вызывает аномалий закладки, роста костной системы, органо- и гистогенеза внутренних органов, не влияет на дифференцировку гладкомышечных клеток в ходе пренатального онтогенеза).
Клиническое применение диметилоксобутилфосфонилдиметилата
Разнообразие фармакологических эффектов диметил оксобутилфосфонилдиметилата и низкая токсичность препарата являются основой его широкого применения в клинической практике.
Диметилоксобутилфосфонилдиметилат известен в России [1, 36, 45], Великобритании [46, 47], Германии [48], Швейцарии [49], Японии [50]; подтверждены его оригинальность и высокая клиническая эффективность.
Р.Х. Хафизьяновой (1991) изучено действие диметилоксобутилфосфонилдиметилата на энергетический обмен в тканях мозга при ишемическом и геморрагическом инсультах [18]. Л.Е. Зиганшиной (1988) изучены противовоспалительные свойства диметилоксобутилфосфонилдиметилата. На основании полученных данных препарат стали широко использовать в качестве противовоспалительного средства с антисептической активностью для местного применения [16, 17, 33, 51, 52].
В исследованиях К.А. Святкиной, В.П. Булатова, С.В. Мальцевой, Т.П. Варгиной, М.П. Флоринских, Т.М. Егоровой и др. было показано, что диметилоксобутилфосфонилдиметилат участвует в обмене фосфатов и кальция, снижает уровни пировиноградной кислоты и щелочной фосфатазы, что лежит в основе его противорахитного действия [53–56]. Л.Е. Зиганшина и соавт. изучали антиостеопоретический эффект диметилоксобутилфосфонилдиметилата, который обусловлен снижением экскреции оксипролина, кальция и неорганического фосфата с мочой на фоне экспериментального остеопороза, вызванного введением преднизолона [57].
В исследованиях, проведенных группой ученых в НИИ педиатрии и детской хирургии МЗ РСФСР (г. Москва), было показано иммуномодулирующее свойство диметилоксобутилфосфонилдиметилата [56]. На основании этих данных диметилоксобутилфосфонилдиметилат был рекомендован для нормализации иммунного гомеостаза [58].
В.П. Панковой (1978) впервые выявлена церебральная вазоактивность диметилоксобутилфосфонилдиметилата [59]. В.И. Даниловым и соавт. было изучено сравнительное влияние диметилоксобутилфосфонилдиметилата, ницерголина и пирацетама на реактивность мозговых сосудов и локальный мозговой кровоток у пациентов, оперированных по поводу опухолей (глиомы и менингиомы) больших полушарий головного мозга. Доказано преимущество диметилоксобутилфосфонилдиметилата как по продолжительности действия (по сравнению с ницерголином), так и по продолжительности и силе эффекта (по сравнению с пирацетамом). В других работах автора показаны уникальная церебральная вазоактивность и эффективность диметилоксобутилфосфонилдиметилата в комплексном лечении пациентов с тяжелой черепно-мозговой травмой [13, 14].
Также проведена оценка диметилоксобутилфосфонилдиметилата как средства коррекции нарушенной реактивности церебральных сосудов у пациентов в остром периоде черепно-мозговой травмы легкой и средней степени тяжести. Диметилоксобутилфосфонилдиметилат наряду с другими церебропротективными эффектами обладает выраженной способностью восстанавливать реактивность мозговых сосудов после травмы мозга, объективизированной с помощью рентгеновской компьютерной томографии. У пациентов, получавших диметилоксобутилфосфонилдиметилат в составе комплексной терапии в дозе 15 мл 15% раствора 3 р./сут, существенно быстрее купировались симптомы общемозгового синдрома — показатели реактивности мозговых сосудов (индекс вазомоторной реактивности, коэффициент овершута) восстанавливались достоверно быстрее [60].
В настоящее время накоплен большой клинический опыт применения диметилоксобутилфосфонилдиметилата при острых нарушениях мозгового кровообращения, послеоперационных и посттравматических церебральных нарушениях, болезни Меньера и вегетативной дисфункции, а также при спинномозговой травме (рис. 1) [16, 23, 43, 61].
![Рис. 1. Клиническое применение препарата Димефосфон® [31] Рис. 1. Клиническое применение препарата Димефосфон® [31]](https://www.rmj.ru/upload/medialibrary/f58/71-1.png)
Нейропротективные эффекты диметилоксобутилфосфонилдиметилата при хронической ишемии головного мозга представлены в наблюдениях Д.Р. Закировой с соавт. (2018). Отмечено влияние диметилоксобутилфосфонилдиметилата на степень выраженности краниалгического синдрома, координаторных нарушений, астенических и когнитивных расстройств при включении препарата в комплексную терапию пациентов с дисциркуляторной энцефалопатией 2–3-й степени. Было обследовано 87 пациентов в возрасте от 47 до 73 лет с дисциркуляторной энцефалопатией 2–3-й степени с ведущими краниалгическим и вестибулоатактическим синдромами и МР-верифицированными многоочаговыми дисциркуляторными изменениями головного мозга. Показано, что включение в схему комплексной стационарной терапии диметилоксобутилфосфонилдиметилата по 2 мл в/в капельно на 200 мл 0,9%-ного раствора NaCl 2 р./сут в течение 10 дней повышает эффективность терапии пациентов с дисциркуляторной энцефалопатией 2–3-й степени в части полного регресса головной боли, нормализации сна, коррекции координаторных функций, степени тревожности, депрессии и когнитивных нарушений. Весь комплекс полученных в настоящем исследовании положительных эффектов терапии с включением диметилоксобутилфосфонилдиметилата указывает на значимость такого комбинированного воздействия на качество жизни пациентов. Кроме того, полученные эффекты стимулирования активности когнитивных процессов и регуляторно-компенсаторных механизмов функции ходьбы и стояния у больных с данными коморбидными взаимопотенцирующими заболеваниями имеют большое прогностическое значение для активизации механизмов нейропластичности и повышения нейрореабилитационного потенциала, это можно объяснить выраженными антиоксидантными свойствами диметилоксобутилфосфонилдиметилата, которые в сочетании с адекватной энергетической поддержкой нейронов обеспечивают выраженный нейропротективный и нейрогенный эффект. Максимально выраженная эффективность в отношении краниалгического синдрома, безусловно, подтверждает вазоактивные свойства диметилоксобутилфосфонилдиметилата, обеспечивающие нормализацию реактивности церебральных сосудов, активизацию мозгового кровообращения и улучшение венозного оттока из полости черепа, что имеет особое значение для пациентов с извитостью сосудов вертебрально-базилярного бассейна и развитием хронической ишемии головного мозга [62].
Диметилоксобутилфосфонилдиметилат также нашел широкое применение в пульмонологии и фтизиатрии. Препарат рекомендован в комплексной терапии у больных ОРВИ с бронхообструктивным синдромом, рецидивирующим бронхитом и бронхиальной астмой, хроническими неспецифическими заболеваниями легких, а также пневмонии у новорожденных [59, 63, 64].
В результате проведенных клинических исследований у диметилоксобутилфосфонилдиметилата были обнаружены антиаритмический эффект [65] и способность предупреждать развитие склеротизации миокарда [66].
Перспективным остается применение диметилоксобутилфосфонилдиметилата в кардиологии и онкологии. В настоящее время диметилоксобутилфосфонилдиметилат используется в онкологии как корректор иммуносупрессивных свойств противоопухолевых средств [67] и в качестве радиопротектора [68].
Заключение
Таким образом, в данном обзоре показан полный круг фармакологического действия, механизмы и аспекты клинического применения оригинального отечественного препарата Димефосфон®. Рассмотрены вазоактивный и антигипоксический, нейропротекторный и церебропротекторный, а также антиоксидантный эффекты указанного препарата. Отмечена способность данного неантихолинэстеразного фосфорорганического соединения нормализовать цереброваскулярную реактивность, оптимизировать сосудистый тонус, нормализовать регионарный кровоток и кислородзависимый энергетический метаболизм в структурах ЦНС. Подчеркнута способность диметилоксобутилфосфонилдиметилата оптимизировать внутриклеточный метаболизм и нормализовывать обменно-энергетические процессы головного мозга, предотвращать ПОЛ и реализовывать антиацидотический эффект за счет интенсификации почечного и легочного механизмов регуляции кислотно-основного состояния организма как одного из важнейших и наиболее строго стабилизируемых параметров гомеостаза. Многолетние клинические исследования в практической медицине показали высокую терапевтическую эффективность и безопасность использования диметилоксобутилфосфонилдиметилата в нейрохирургии и неврологии, эндокринологии, кардиологии, хирургии, нефрологии, педиатрии, дерматологии, пульмонологии и других областях медицины.
Благодарность
Редакция благодарит компанию АО «Татхимфармпрепараты» за оказанную помощь в технической редактуре настоящей публикации.
ФГБОУ ВО «Казанский государственный медицинский университет» Минздрава России;
ГАУЗ «Межрегиональный клинико-диагностический центр»
Кнни К.С.
ФГБОУ ВО «Казанский государственный медицинский университет» Минздрава России;
ГАУЗ «Межрегиональный клинико-диагностический центр»
Магсумова Р.Л.
ГАУЗ «Межрегиональный клинико-диагностический центр»
Баранова Е.А.
ФГБУ «Федеральный центр мозга и нейротехнологий» Федерального медико-биологического агентства России;
Казанская государственная медицинская академия ― филиал ФГБОУ ДПО «Российская медицинская академия непрерывного последипломного образования» Минздрава России
- ORCID:
0000-0002-9200-9234
Хасанова Д.Р.
ГАУЗ «Межрегиональный клинико-диагностический центр»;
ФГБОУ ВО «Казанский государственный медицинский университет» Минздрава России
- ORCID:
0000-0002-8825-2346

Эффективность применения антиацидемического средства Димефосфон на первом этапе реабилитации у пациентов в остром периоде ишемического инсульта в каротидной системе
Авторы:
Данилова Т.В., Кнни К.С., Магсумова Р.Л., Баранова Е.А., Хасанова Д.Р.
Как цитировать:
Данилова Т.В., Кнни К.С., Магсумова Р.Л., Баранова Е.А., Хасанова Д.Р. Эффективность применения антиацидемического средства Димефосфон на первом этапе реабилитации у пациентов в остром периоде ишемического инсульта в каротидной системе. Журнал неврологии и психиатрии им. С.С. Корсакова.
2021;121(3):44‑51.
Danilova TV, Knni KS, Magsumova RL, Baranova EA, Khasanova DR. The efficacy of the anti-acidemic agent dimephosphone at the first rehabilitation stage in patients in the acute period of carotid-related ischemic stroke. S.S. Korsakov Journal of Neurology and Psychiatry. 2021;121(3):44‑51. (In Russ.)
https://doi.org/10.17116/jnevro202112103144
Острые нарушения мозгового кровообращения (ОНМК) занимают одну из лидирующих позиций в структуре заболеваемости, смертности и инвалидизации взрослого населения, нанося значимый ущерб экономике страны с учетом расходов на лечение, реабилитацию, потери в сфере производства [1]. По данным официальной статистики, в структуре церебральных инсультов в РФ 75—80% составляют пациенты с ишемическим инсультом (ИИ) [2].
Большая социальная значимость данной проблемы определяет необходимость поиска путей совершенствования системы оказания помощи больным инсультом на разных этапах, а также уточнения наиболее значимых мишеней лечебного воздействия на сам патологический процесс на базе оценки механизмов его развития, состояния функциональных систем и преморбидного статуса больного. Важная роль отводится изучению острого периода ИИ как наиболее значимого для уточнения патогенеза, выбора соответствующей тактики лечения с целью определения прогноза и течения заболевания [3].
У значительного числа пациентов в результате инсульта длительно сохраняются различные функциональные нарушения, негативно влияющие на качество их жизни. По данным регистра ФГБУ «Научный центр неврологии», к концу острого периода среди классических неврологических синдромов двигательные нарушения наблюдаются у 81,2% больных (гемиплегия — у 11,2%, грубый парез — у 11,1%, легкий парез — у 58,9%), афазии — у 35,9%, дизартрия — у 13,4% [4].
Важной задачей острого периода инсульта является максимально возможное восстановление или компенсация поврежденных в результате ОНМК функций. Это определяет актуальность поиска факторов, которые могут влиять на этот процесс.
Во многих экспериментальных исследованиях на модели ОНМК использовались препараты с мультимодальным действием, показавшие свою эффективность в отношении восстановления функциональных нарушений. Однако, несмотря на значительное количество изучаемых препаратов, нейропротективной программы, продемонстрировавшей в клинических исследованиях достоверное улучшение исхода заболевания, не создано [5]. В то же время известные патобиохимические процессы ишемического повреждения структур головного мозга в теории позволяют обосновать рациональность поиска эффективной нейропротекции. Однако разделить три базовых биологических процесса — нейропротекцию, нейротрофику и нейропластичность — не представляется возможным, и изучение эффективности препаратов осуществляется в контексте данного представления [6]. При этом для клинической практики важно иметь лекарственные средства, способствующие стимуляции репаративных процессов и ремоделированию отделов мозга (активации ранее незадействованных отделов мозга) для оптимизации функционирования головного мозга в изменившихся в результате инсульта условиях. Известно, что механизмы компенсации нарушенных функций развиваются на основе механизмов нейропластичности [7].
Вместе с тем большое прогностическое значение для функционального восстановления пациентов имеет состояние регуляторных механизмов. В ранее опубликованных клинических исследованиях показано, что в острой стадии ИИ у 100% пациентов с неврологическим дефицитом, превышающим 4 балла по шкале NIHSS, развиваются расстройства центральной вегетативной регуляции. Эти нарушения связаны как со структурным поражением головного мозга, так и с реакцией вегетативной системы на стресс, которым является острый инсульт [8].
По данным экспериментальных и клинических исследований, представляется вероятным и значимым, влияющим на темпы восстановления после перенесенного инсульта функциональное состояние вегетативной нервной системы, включающей в структуре многомерности влияний и регуляторные механизмы мозгового кровообращения [9]. Так, показатели цереброваскулярной реактивности отражают адаптационные возможности системы мозгового кровообращения в обеспечении постоянства кровоснабжения мозга, а также способность сосудов мозга адекватно реагировать на изменяющиеся условия функционирования и оптимизировать кровоток соответственно этим условиям. От длительности и выраженности нарушений ауторегуляции мозгового кровотока напрямую зависит течение ИИ [10].
Одной из задач применения препаратов с мультимодальными метаболическими свойствами у пациентов с инсультом, является медикаментозная поддержка реабилитационного процесса и увеличение реабилитационного потенциала [11]. Оценка эффективности препаратов метаболической защиты головного мозга, стимулирующих его нейропластичность, нормализующих регуляторные механизмы, поиск новых возможностей их применения в постинсультном периоде остаются важнейшими задачами экспериментальных и клинических исследований.
Оригинальный отечественный препарат Димефосфон (диметилоксобутилфосфонилдиметилат) синтезирован в 1952 г. А.Н. Пудовиком в Институте органической и физической химии им. А.Е. Арбузова [12]. Он относится к группе препаратов с метаболическими свойствами и представляет собой диметиловый эфир 1,1-диметил-3-оксобутилфосфоновой кислоты, обладающий антиацидотическим и антиоксидантным действием. Димефосфон производится с 1983 г., в ходе его клинического применения обнаружилась также вазо- и нейротропная активность препарата [13]. Димефосфон улучшает энергетические процессы в мозге как напрямую, воздействуя непосредственно на митохондрии, так и косвенно, стимулируя потребление тканями тиреоидных гормонов, в результате чего активирует энергетические и катаболические процессы в митохондриях клеток. Препарат также обладает ГАМКергической, Н-холино- и дофаминергической активностью. В результате применения препарата было доказано уменьшение содержания молочной и пировиноградной кислот в тканях головного мозга. В ряде экспериментальных исследований Димефосфон продемонстрировал свое влияние на механизмы регуляции мозгового кровообращения и функции нервной системы: уменьшал явления циркуляторной гипоксии, нормализовал реактивность церебральных сосудов и кровенаполнение мозга и улучшал венозный отток [12].
Наличие вазоактивного, нейропротективного, антиоксидантного, антигипоксантного и нейротропного эффектов Димефосфона обосновывает возможность его применения при различных формах церебральной патологии, что было подтверждено за более чем 30-летний период его использования в практической медицине.
Результаты клинических испытаний Димефосфона в качестве препарата, регулирующего мозговое кровообращение, позволяют назначать его пациентам с ОНМК (ишемическим и геморрагическим инсультом) сразу же после мозговой катастрофы, не опасаясь осложнений, характерных при использовании других вазоактивных препаратов. Это связано с тем, что Димефосфон уменьшает потребление кислорода мозговой тканью и не вызывает синдрома обкрадывания [14]. В то же время многие клинические исследования показали положительное действие данного препарата на систему вегетативной регуляции [15].
В связи с вышеизложенным нами было проведено пилотное рандомизированное сравнительное в параллельных группах клиническое исследование с целью оценки влияния внутривенной формы препарата Димефосфон на цереброваскулярную реактивность, вегетативную регуляцию, динамику регресса неврологического дефицита и функциональное восстановление в остром периоде ИИ в каротидном бассейне.
Материал и методы
Комплексно обследованы 60 пациентов (26 женщин и 34 мужчины) в возрасте от 54 до 85 лет (средний — 69,25±8,85 года) в остром периоде ИИ в каротидном бассейне, подтвержденного данными МРТ (24±4,6 ч от появления первых клинических симптомов), с величиной очага 1/3—1/2 зоны васкуляризации, находящихся в ясном сознании и понимающих обращенную речь, стабильных по гемодинамическим показателям, вне декомпенсации текущих соматических заболеваний. Все пациенты до заболевания имели по шкале Рэнкина оценку не более 2 баллов.
Обследование проводилось в условиях регионального головного сосудистого центра на базе Межрегионального клинико-диагностического центра (Казань). Диагноз «инсульт», патогенетический подтип инсульта, локализация острого сосудистого поражения устанавливались согласно критериям регистра инсульта Национальной ассоциации по борьбе с инсультом и классификации патогенетических подтипов ИИ TOAST (Trial of Org 10172 in Acute Stroke Treatment) [16]. Неврологический осмотр проводился по общепринятой методике. Для объективизации выраженности неврологических нарушений и динамики неврологического статуса у пациентов с ИИ использовалась шкала NIHSS (шкала тяжести инсульта Национальных институтов здоровья США). Для уточнения силы различных мышечных групп применялась шкала оценки мышечной силы Британского совета медицинских исследований. Уровень функциональной независимости пациентов, а также эффективность реабилитационных мероприятий оценивали по модифицированной шкале Рэнкина. Оценка состояния проводилась в первые 24 ч от момента госпитализации и на 10-е сутки стационарного лечения.
Всем пациентам на диагностическом этапе проводились визуализация структур головного мозга с помощью рентгеновской КТ и МРТ, исследование артерий каротидной и вертебрально-базилярной систем при помощи дуплексного исследования экстракраниальных и транскраниальных сосудов головного мозга, кардиологическое обследование с обязательным проведением электрокардиографии и эхокардиоскопии.
Всем пациентам при условии стабилизации основных показателей гомеостаза в первые 24 ч от госпитализации и на 10-е сутки была выполнена оценка цереброваскулярной реактивности (ЦВР) в бассейне средней мозговой артерии по стандартной методике на аппарате для транскраниальной допплерографии SONARA с проведением функциональных проб с оценкой индексов на гиперкапническую (Кр+) и гипокапническую (Кр–) нагрузку, индекса вазомоторной реактивности (ИВМР), коэффициента овершута (КО), который оценивался при компрессионном тесте. Для определения реактивности церебральных сосудов на гиперкапнию проводили пробу с произвольной задержкой дыхания, сосудистую реакцию оценивали через 20 с. Гипокапнический тест выполняли с помощью форсированных дыхательных движений, реакцию церебральных сосудов также оценивали через 20 с. Церебральная ауторегуляция изучалась посредством компрессионного теста: в покое проводилась фоновая запись средней линейной скорости кровотока (ЛСКср) в средней мозговой артерии, затем на протяжении 3 с (5 сердечных циклов) выполнялась компрессия ипсилатеральной общей сонной артерии, после чего регистрировались изменения ЛСКср. [17]. Диапазон нормальных значений для Кр+ и Кр– составляет 25—50%, для ИВМР — >70%, для КО — 1,21—1,52.
В основе изучения вегетативной нервной системы лежит функционально-динамический принцип с оценкой исходного вегетативного тонуса, вегетативной реактивности и вегетативного обеспечения деятельности с применением нагрузочных проб. Информативной пробой, отражающей важную составляющую вегетативного реагирования, является проба с ортостазом, позволяющая дать оценку вегетативной реактивности (симпатикотоническая, гиперсимпатикотоническая или асимпатикотоническая). Учитывая, что изменение частоты сердечных сокращений является универсальной реакцией на любые изменения внешнего и внутреннего воздействия, инструментальная оценка вариабельности сердечного ритма (ВСР) стала наиболее стандартизированной и применяемой методикой оценки типа вегетативной реактивности [18]. Таким образом, для оценки вегетативного гомеостаза всем пациентам на 2-е и 10-е сутки от момента начала заболевания было проведено исследование ВСР. Показатели ВСР регистрировались в состоянии относительного покоя в горизонтальном положении и в пассивной ортостатической пробе (вертикализация на трехсекционной кровати с возвышенным изголовьем до 60°) с помощью аппаратно-программного комплекса Кардиовар. Система предусматривает автоматическую обработку 200 кардиоциклов электрокардиограммы с расчетом показателей ВСР в соответствии с рекомендациями отечественных и зарубежных авторов [19, 20]. Перед началом записи ВСР исследуемые находились в покое в положении лежа в течение 5—10 мин. Исследование ВСР проводилось не ранее, чем через 1,5—2 ч после еды, в условиях палаты интенсивной терапии при первом исследовании и в условиях стандартной больничной палаты при втором исследовании. В помещении поддерживалась постоянная температура 20—22 °C. Оценивались следующие спектральные показатели ВСР: суммарная мощность спектра во всех диапазонах (Тр, мс2), отражающая напряженность деятельности вегетативной нервной системы, мощность спектра в области высоких частот (0,15—0,40 ГЦ, High Frequency (HF) %), отражающего вклад парасимпатического влияния, мощность спектра в области низких частот (0,04—0,15 ГЦ, Law Frequency (LF)%), определяющего вклад супрасегментарных, преимущественно симпатических влияний.
Всем пациентам проводилась стандартная медикаментозная терапия, включавшая базисную и антитромботическую терапию, и ранняя нейрореабилитация согласно действующему федеральному стандарту оказания медицинской помощи больным с инсультом. Применение препаратов ноотропного свойства, вазоактивные препараты или препараты нейропротективного ряда были исключены. В зависимости от получаемой терапии пациенты в остром периоде ИИ в каротидном бассейне были разделены на две группы. Основную группу составили 30 пациентов в возрасте от 58 до 85 лет (69,3±7,5), госпитализированные в среднем через 20,8±3,6 ч от появления первых клинических симптомов, которым вводился препарат Димефосфон внутривенно струйно 1,0 мл в дозе 1 г 3 раза в сутки на протяжении 10 дней. Первая инъекция препарата выполнялась в течение 1-го часа от момента госпитализации пациента в стационар. Группа сравнения также включала 30 пациентов в возрасте от 54 до 78 лет (63,1±12,5), поступивших в стационар в среднем через 20,3±4,3 ч от развития инсульта.
Протокол проведения рандомизированного сравнительного в параллельных группах клинического исследования был одобрен этическим комитетом. Исследование выполняли после получения письменного согласия пациентов и проведения врачебной комиссии.
Статистическая обработка полученных результатов проводилась с применением программ Microsoft Excel, Statistica (v 11.0), пакетов ANOVA. Достоверность различий оценивали на уровне значимости, равной p<0,05.
Результаты
Атеротромботический патогенетический подтип инсульта со стенозированием магистральных артерий головы в среднем 60,1±11,3% был диагностирован у 60% пациентов основной группы и 65% — группы сравнения со стенозом каротидных артерий в среднем 61,5±11,8% (p>0,05). Кардиоэмболический подтип инсульта в основной группе был установлен в 40% наблюдений, в группе сравнения — в 35% (p>0,05). Пациенты обеих исследуемых групп с кардиоэмболическим подтипом инсульта страдали постоянной формой фибрилляции предсердий, при этом среди пациентов в сравниваемых группах фибрилляция предсердий была неклапанной в 100% наблюдений.
Исходный неврологический дефицит по шкале NIHSS в первые 24 ч от момента госпитализации в основной группе составил 5,5±2,1 балла, а в группе сравнения — 5,2±2,2 балла. Таким образом, статистически достоверных отличий между группами в дебюте инсульта выявлено не было (p>0,05). Оценка в динамике неврологического статуса на 10-е сутки госпитализации продемонстрировала уменьшение баллов по шкале NIHSS в основной группе до 2,2±1,6 (в среднем на 60% от исходного уровня), в группе сравнения также зафиксировано снижение баллов по шкале NIHSS до 3,5±3,1 (в среднем на 33% от исходных баллов), но статистически менее значимое по сравнению с основной группой (p<0,05).
По данным транскраниальной допплерографии с применением функциональных проб в основной группе средние значения показателей ЦВР в 1-е сутки в правой каротидной системе составили Кр+ 31±13,7%, Кр– 21,3±9,2%, ИВМР 52,6±18,8%, КО 1,27±0,1; в левой каротидной системе — Кр+ 30,5±13,2%, Кр– 23,45±8,9%, ИВМР 57,8±13,8%, КО 1,26±0,12. В группе сравнения были зарегистрированы следующие средние исходные показатели ЦВР: в правой каротидной системе Кр+ 28±10,7%, Кр– 21,3±7,2%, ИВМР 45,8±19,3%, КО 1,4±0,1; в левой каротидной системе Кр+ 27±10,2%, Кр– 21,6±9,9%, ИВМР 52,4±11,8%, КО 1,46±0,1. Следовательно, в дебюте инсульта группы были сопоставимы по показателям ЦВР и не имели статистически достоверных отличий.
В динамике на 10-е сутки оценка ЦВР выявила увеличение показателей реактивности сосудов на гиперкапнию на 12±4,7% в основной группе и на 4±1,9% в группе сравнения в правой каротидной системе и на 9,1±3,7% и 5,14±2,1% соответственно в левой каротидной системе (средний показатель Кр+ в основной группе в правой каротидной системе составил 43±12,2%, в левой — 39,6±11,7%, в группе сравнения — 32,4±15,6% и 32,14±12,8% соответственно, p<0,05). При проведении в динамике пробы на гипокапническую нагрузку (Кр–) было выявлено достоверное увеличение показателя сосудистой реактивности в основной группе в правой каротидной системе на 6,7±3,1% и на 7,1±1,9% в левой (средние значения Кр– на 10-е сутки в каротидной системе справа 28±11,2%, слева 30,6±10,7%), в то время как в группе сравнения данный показатель увеличился лишь на 4±2,1% в правой каротидной системе и на 4,4±1,78% в левой (средние значения Кр– на 10-е сутки в каротидной системе справа 25±13,5%, слева 26±14,3%, p<0,05).
ИВМР, оцененный в динамике, позволяет судить о степени компенсаторных возможностей гемодинамики головного мозга. В обеих группах в динамике зарегистрировано повышение ИВМР. При этом более выраженная динамика средних значений ИВМР в сторону его нормализации зарегистрирована на 10-е сутки у пациентов, получавших Димефосфон (в правой каротидной системе 69,4±2%, в левой — 68±3%), что статистически значимо отличается от средних показателей ИВМР группы сравнения (в правой каротидной системе 48,8±8%, в левой — 56,6±3%) (p<0,05).
Состояние ауторегуляции мозгового кровотока оценивалось по выраженности гиперемических изменений после периода региональной гипотензии, вызванной временной компрессией общей сонной артерии, приводящей к снижению перфузионного давления во внутренней сонной и средней мозговой артериях. По прекращению компрессии отмечается преходящее повышение ЛСКср в результате компенсаторной вазодилатации, которое использовано в качестве индикатора ауторегуляции. Для оценки ауторегуляции использовали КО. В 1-е сутки в группе больных, получавших лечение Димефосфоном, данный показатель в среднем составил в правой каротидной системе 1,27±0,1, в левой — 1,26±0,12, в группе сравнения — справа 1,4±0,1, слева 1,46±0,1, что входит в диапазон нормальных значений ауторегуляции. Но при этом к 10-м суткам исследования средние значения КО в основной группе повысились в правой каротидной системе до 1,3±0,11, в левом — до 1,31±0,08, а в группе сравнения — справа 1,42±0,1, слева 1,47±0,1. Таким образом, увеличение показателя ауторегуляции было достоверно выше в группе пациентов, которым вводился Димефосфон, по сравнению с группой, где препарат не применялся, разница КО в основной группе и группе сравнения составила справа 0,13±0,03 и 0,02±0,005, слева 0,14±0,02 и 0,01±0,004 соответственно (p>0,05).
Проведен субанализ сравнительной оценки показателей перфузионного резерва у пациентов с атеротромботическим подтипом инсульта с гемодинамически значимыми стенозами каротидных артерий (>70%) на фоне лечения Димефосфоном и без применения препарата. Группы пациентов были сопоставимы по стороне и степени стеноза. Исходные средние показатели ЦВР на стороне симптомного гемодинамически значимого стеноза в основной группе (Кр+ 25,12±10,43%, Кр– 24,6±10,73%, ИВМР 52,12±7,8%) и группе сравнения (Кр+ 17,6±9,3%, Кр– 21,6±11,6%, ИВМР 39,3±9,5%) не были статистически различны. На 10-е сутки выявлены изменения ЦВР в сторону увеличения и в группе с применением препарата Димефосфон (средние значения Кр+ 32,7±11,3%, Кр– 28,6±8,67%, ИВМР 68,6±4,1%), и в группе сравнения (Кр+ 18,3±4,1%, Кр– 26,3±10,4%, ИВМР 43,3±13,3%). При этом обнаружено достоверно значимое увеличение показателей ЦВР на стороне стеноза к 10-м суткам заболевания у пациентов, которым вводился Димефосфон (средние значения повысились: Кр+ на 8,9±2,3%, Кр– на 8,5±3,4%, ИВМР на 16,5±6,4%) относительно группы больных, не получавших препарат (средние показатели повысились: Кр+ на 0,7±0,5%, Кр– на 4,6±2,5%, ИВМР на 4±3,4%) (p>0,05).
Таким образом, на основании проведенного анализа можно констатировать, что Димефосфон способствует улучшению показателей реактивности мозговых сосудов.
При исследовании исходных данных спектрального анализа ВСР показателей Тр в покое и на 1-й минуте ортостаза в оценке вегетативной реактивности в основной группе и в группе сравнения не было установлено статистически значимых различий (p=0,584 и p=0,631 соответственно), что подтверждает сопоставимость изучаемых групп. Однако на 10-й день госпитализации в группе, получавшей препарат Димефосфон, отмечается достоверное снижение Тр как в покое, так и после выполнения нагрузки (p<0,05) (рис. 1). Полученные данные свидетельствуют о состоянии напряженности системы вегетативной регуляции как в группе сравнения, так и в основной группе. На 10-й день госпитализации отмечено уменьшение значений суммарной мощности в группе, получавшей лечение Димефосфоном, достоверно отличающееся от сохраняющихся высоких значений в группе сравнения (p<0,05). Реакция на ортостаз с большей амплитудой по нарастанию общей мощности в основной группе (ΔТр на 10-й день 924±111 мс2 в основной группе и ΔТр на 10-й день в группе сравнения 501±183 мс2, p<0,05) в соответствии с «законом исходного уровня», согласно которому чем выше уровень, тем в более деятельном и напряженном состоянии находится система и тем меньший ответ возможен при действии возмущающих стимулов [21], также отражает уменьшение потенциала напряженности вегетативной функциональной системы.

Рис. 1. Динамика показателей Тр у обследуемых больных в покое и на фоне ортостаза.
Δ Тр — разница показателей общей мощности, * — p<0,05.
При первом исследовании анализ представленности HF и LF в спектре ВСР как в состоянии покоя, так и при ортостазе в основной группе и в группе сравнения не выявил достоверных различий. Сравнительная оценка показателей спектрального анализа ВСР на 10-й день от момента начала лечения относительно исходных данных выявила в покое в основной группе уменьшение представленности HF, в то время как в группе сравнения этот показатель увеличился (p=0,005), при этом зарегистрировано повышение LF в основной группе высоких и низких частот при уменьшении его в группе сравнения (p=0,005). Анализ динамики изучаемых показателей на ортостатическую пробу выявил, что в основной группе уровень HF существенно не изменился относительно исходных данных, в то время как в группе сравнения достоверно увеличился (p=0,005). Уровень LF в динамике на фоне ортостаза в основной группе увеличился (p=0,018), в то время как в группе сравнения уменьшился (рис. 2).

Рис. 2. Динамика показателей HF и LF в основной группе и группе сравнения в покое и на фоне ортостаза.
* — p<0,05.
В зависимости от характера медленноволновой составляющей на ортостатическую пробу были выделены следующие варианты вегетативной реактивности: симпатикотоническая (50% пациентов в основной группе и 60% — в группе сравнения), гиперсимпатикотоническая (20 и 20% соответственно), асимпатикотоническая (30 и 20% соответственно) (последние 2 варианта были отнесены к дезадаптивным) [22]. При сопоставлении данных соотношения типов вегетативной реактивности на 10-й день госпитализации относительно исходных значений в основной группе было выявлено статистически значимое увеличение числа пациентов с адаптивным симпатикотоническим типом на 30% (p=0,008) с уменьшением числа пациентов с гиперсимпатическим и асимпатическим типами вегетативной реактивности на 10 и 20% соответственно, в то время как в группе сравнения представленность дезадаптивных вариантов вегетативной реактивности сохранялось (рис. 3). В то же время на 10-й день в основной группе отмечалось наряду с увеличением LF на ортостаз одновременное умеренное повышение HF, что указывает на синергизм симпатических и парасимпатических влияний, также отражая тенденцию к нормализации вегетативных реакций. Таким образом, преобладание адаптивного типа вегетативной реактивности на 10-й день госпитализации в группе, получавшей Димефосфон, еще раз подтверждает вегетотропные эффекты препарата.

Рис 3. Типы вегетативной реактивности пациентов исходно и на 10-е сутки госпитализации.
* — уровень достоверности p<0,05 по сравнению с исходным уровнем.
На момент госпитализации в стационар все пациенты имели 4 балла по модифицированной шкале Рэнкин. На 10-й день госпитализации 1 балл по шкале Рэнкин был у 33% пациентов, получавших лечение Димефосфоном, и у 20% — из группы сравнения, 2 балла по шкале Рэнкин имели 50% пациентов в основной группе и 40% — в группе сравнения. Три балла по шкале Рэнкин к 10-му дню терапии зафиксированы у 14% пациентов, получавших Димефосфон, и у 25% — группы сравнения. Без изменений 4 балла по шкале Рэнкин сохранялись лишь у 3% больных из основной группы и 15% — группы сравнения. Таким образом, к 10-му дню госпитализации пациентов с отсутствием или наличием легких признаков инвалидности было достоверно больше среди получавших лечение Димефосфоном (83%), чем среди пациентов группы сравнения (60%) (p<0,05).
Обсуждение
По данным литературы, при оценке спектрального анализа ВСР низкий удельный вес LF, отражающих симпатические влияния, является информативным критерием, который позволяет определить прогноз течения и исход ИИ. Чем ниже активность симпатического отдела вегетативной нервной системы, особенно на функциональную нагрузку, тем тяжелее проходят адаптационные процессы в организме, обусловливая неблагоприятное течение заболевания в виде либо летального исхода, либо более длительного реабилитационного периода [23, 24]. Проведенное исследование еще раз демонстрирует связь функциональных исходов с улучшением вегетативного статуса.
Одновременно с этим препарат Димефосфон продемонстрировал достоверно значимое положительное влияние на показатели ЦВР, улучшая значения ИВМР, в том числе, что немаловажно, достоверно нормализуя ЦВР сосудов поврежденного полушария головного мозга в условиях гемодинамически значимого стеноза. Возможности препарата в регулировании мозгового кровотока ранее уже изучались в экспериментальных исследованиях [25], в которых была доказана его способность уменьшать циркуляторную гипоксию, потребление кислорода мозговой тканью, нормализовать мозговой кровоток, в том числе улучшать венозный отток. В клинических работах на примере травмы головного мозга [26], а также при опухолях головного мозга было выявлено, что при использовании пероральной формы Димефосфона характеристики реактивности мозговых сосудов (ИВМР, КО) восстанавливались быстрее, чем в группе сравнения [14, 27]. При этом, несмотря на полученные экспериментальные и клинические результаты, свидетельствующие о способности препарата улучшать адаптационные возможности системы мозгового кровообращения, работы, посвященные изучению действия препарата в острый период ИИ, в частности на ЦВР и состояние системы вегетативной регуляции, не выполнялись.
В нашем исследовании в группе пациентов с применением препарата Димефосфон зафиксировано достоверное уменьшение баллов по шкале NIHSS на фоне терапии по сравнению с группой без применения нейрометаболической поддержки. Кроме того, при равном исходном уровне баллов по шкале Рэнкин к 10-му дню госпитализации на фоне лечения Димефосфоном достоверно больше было пациентов с лучшим восстановлением функций самообслуживания и передвижения. Это дает основание предположить, что, улучшая регуляторные механизмы мозгового кровообращения, положительно влияя на показатели вегетативной регуляции, препарат способствует нормализации вегетативного гомеостаза в целом и, как следствие, восстановлению утраченных функций.
Была отмечена хорошая переносимость препарата, на фоне терапии не было зарегистрировано побочных эффектов. Кроме того, не выявлено лекарственных взаимодействий с другими применяемыми в данном исследовании для лечения пациентов лекарственными средствами. Возможно, это может быть обусловлено небольшой выборкой пациентов и требует дальнейшего изучения.
Заключение
Динамика состояния ЦВР в остром периоде ИИ в каротидном бассейне влияет на функциональное восстановление пациентов. Применение ВСР в оценке вегетативной реактивности с использованием простых нагрузочных проб может быть эффективно для определения показателей вегетативного гомеостаза в раннем постинсультном периоде, влияющих на процессы восстановления и определяющих прогноз заболевания. Улучшение показателей неврологического статуса и функциональная независимость в самообслуживании у пациентов в остром периоде ИИ значимо зависят от состояния системы вегетативной регуляции, в том числе ЦВР. Препарат Димефосфон может быть использован как средство для нормализации вегетативного гомеостаза с целью улучшения функционального восстановления пациентов начиная с острого периода ИИ.
Таким образом, использование препарата мультимодального действия Димефосфон в комплексной терапии у пациентов в остром периоде ИИ в каротидном бассейне способствует нормализации регуляторных механизмов мозгового кровообращения, состояния центральной вегетативной регуляции, тем самым содействуя улучшению функционального восстановления и повышению реабилитационного потенциала пациентов. Целесообразно дальнейшее изучение эффективности и безопасности препарата для оптимизации его применения.
Авторы заявляют об отсутствии конфликта интересов.
The authors declare no conflicts of interest.
Димефосфон: инструкция по применению
Подойницына Алёна Андреевна
29 сентября 2023

ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ. ВОЗМОЖНЫ ПОБОЧНЫЕ ЭФФЕКТЫ. НЕОБХОДИМА КОНСУЛЬТАЦИЯ СПЕЦИАЛИСТА.
Автор статьи
Подойницына Алёна Андреевна
,
Профессия: провизор
Название вуза: Пермская государственная фармацевтическая академия (ПГФА)
Специальность: фармация
Стаж работы: 5 лет
Диплом о фармацевтическом образовании: 105924 3510722 рег. номер 31917
Места работы: провизор в аптеке, преподаватель ПГФА на кафедре Управления и экономики фармации, провизор сервиса Мегаптека
Все авторы
Содержание
- РЛС
- Состав препарата
- От чего помогает
- Противопоказания
- Побочные действия
- Димефосфон: как хранить
- Краткое содержание
Инсульт – преобладающая причина утраты трудоспособности населения. Согласно сведениям Национального регистра, только 8% пациентов, перенесших инсульт, могут вернуться к прежней жизни. При этом 31% людей нуждается в постоянном присмотре и помощи в уходе за собой, а еще 20% не могут самостоятельно передвигаться.
Восстановление после инсульта – продолжительный и трудный процесс. Для ускорения выздоровления на фармацевтическом рынке ежегодно появляются новые препараты. Однако сегодня рассмотрим средство, разработанное еще в середине прошлого века.
Провизор расскажет о препарате Димефосфон: ознакомит с его составом, показаниями к применению, противопоказаниями, побочными действиями и правилами хранения.
РЛС
Димефосфон – препарат, зарегистрированный в Государственном реестре лекарственных средств России (ГРЛС). Медикамент принадлежит российской фармацевтической компании «Татхимфармпрепараты», которая выпускает две лекарственные формы:
- раствор для приема внутрь и наружного применения;
- ампулы с концентратом для приготовления раствора для внутривенного введения.
Важно отметить, что Димефосфон – лекарство без доказанной эффективности. Это означает, что препарат не имеет достоверных исследований, которые подтверждали бы положительный эффект от приема медикамента. Международные исследования отсутствуют.
Состав препарата
Димефосфон – лекарство на основе вещества под сложным названием диметилоксобутилфосфонилдиметилат. Активное соединение проявляет ряд полезных свойств:
- поддерживает кислотно-основное равновесие организма;
- стабилизирует мембраны клеток, уменьшая интенсивность пирамидных, мозжечковых, вестибулярных, зрительных и слуховых нарушений (например, один из симптомов, который облегчает препарат – шум в ушах);
- замедляет окисление клеток организма, ускоренное некоторыми заболеваниями;
- усиливает энергетические процессы в головном мозге;
- уменьшает сердечную и легочную недостаточность;
- регулирует мозговое кровообращение.
Вспомогательный состав рассматриваемого средства фармакологически нейтрален: в качестве дополнительного компонента в раствор Димефосфон добавлена вода очищенная.
От чего помогает
Список показания к применению Димефосфон обширный и отличается в зависимости от лекарственной формы и способа применения. Поможет ознакомиться с полным списком показаний взрослым – «Димефосфон: инструкция по применению». Наиболее распространенные назначения:
- при нарушении мозгового кровообращения: препарат выписывается для облегчения последствий инсульта, черепно-мозговых и нейрохирургических травм;
- от головной боли: препарат облегчает болевые ощущения мигренозного характера, за счет положительного влияния на метаболизм тканей мозга и улучшение мозгового кровообращения;
- от мигрени: фармакологические эффекты препарата позволяют облегчить проявления мигрени;
- от аллергии: препарат назначается внутрь для лечения поллиноза (сенной лихорадки) – сезонной аллергии на пыльцу растений;
- при остеохондрозе: прием раствора облегчает некоторые из симптомов болезни.
- от прыщей: лекарство проявляет противовоспалительное и антисептическое действие при наружном нанесении, за счет чего назначается для лечения угревой сыпи, жирной себореи и других заболеваний кожи.
Важно отметить, что Димефосфон назначается исключительно в качестве дополнения к основному лечению по решению врача. Препарат не может заменить базисную терапию. Ниже приведен список «популярных» запросов, при которых рассматриваемое лекарство не применяется или его использование ограничено:
- при кашле;
- при подагре;
- при ревматоидном артрите;
- при вегетативных кризах;
- при сахарном диабете первого типа.
Противопоказания
Разобрали показания Димефосфон, теперь перейдем к ограничениям. Согласно инструкции, в список противопоказаний для применения лекарственного средства входят следующие состояния:
- повышенная чувствительность к компонентам препарата;
- эпилепсия;
- хроническая почечная недостаточность.
Распространен вопрос пациентов о том, для чего назначают препарат детям. Однако лекарство противопоказано для пациентов младше 18 лет, за исключением выраженных случаев вегетососудистой дистонии по парасимпатическому типу. Тогда возрастной порог снижается до 12 лет.
Запрещено делать ингаляции с Димефосфоном. Раствор рассчитан на дозированный прием внутрь или наружное нанесение. Нельзя вводить внутримышечные и подкожные уколы Димефосфон. Концентрат нужен для изготовления раствора для внутривенного капельного или струйного введения. Ознакомит с особенностями приема препарата внутрь взрослым – «Димефосфон: инструкция по применению».
Побочные действия
- нарушения со стороны желудочно-кишечного тракта;
- сонливость;
- ухудшение концентрации внимания.
Димефосфон: как хранить
Для сохранения терапевтических свойств препарата требуется соблюдение правил хранения. К ним относится температурный режим не более 25 градусов, отсутствие прямых солнечных лучей и соблюдение срока годности. Капельница применяется медицинскими работниками сразу после изготовления и не хранится.
Краткое содержание
- Димефосфон – препарат, зарегистрированный в Государственном реестре лекарственных средств России (ГРЛС).
- Лекарство на основе вещества под сложным названием диметилоксобутилфосфонилдиметилат.
- Список показания к применению обширный и отличается в зависимости от лекарственной формы и способа применения.
- Имеет противопоказания и побочные действия.
- Для сохранения терапевтических свойств препарата требуется соблюдение правил хранения.
Задайте вопрос эксперту по теме статьи
Остались вопросы? Задайте их в комментариях ниже – наши эксперты ответят вам. Там же вы можете поделиться своим опытом с другими читателями Мегасоветов.
от 443 ₽
Full Text
Ацидотический сдвиг кислотно-основного состояния является важным патогенетическим звеном многих заболеваний. Его срочная коррекция у ургентных больных проводится обычно внутривенным введением натрия гидрокарбоната или трисамина, химически нейтрализующих избыток кислых метаболитов крови. Однако эти препараты не устраняют внутриклеточные сдвиги pH, не влияют на метаболитические процессы в тканях, вызвавшие ацидоз. Они могут быть применены только в условиях стационара под постоянным контролем кислотно-основного состояния, требующим использования специальной аппаратуры.
Нормализация кислотно-основного состояния в неэкстремальных ситуациях, основанная на изменении обменных процессов, облегчает течение многих заболеваний и ускоряет выздоровление. Известен эффект применения комплекса витаминных препаратов. В результате многолетних исследований и разработок химиков, технологов, фармакологов, клиницистов создан, освоен промышленностью и внедрен в медицинскую практику димефосфон — новый оригинальный отечественный препарат для борьбы с ацидозом, который принципиально отличается от известных антиацидотических средств. Его действие связано не с химической нейтрализацией избытка кислых метаболитов, а с активированием метаболических механизмов регуляции кислотно-основного состояния крови. В качестве антиацидотического средства димефосфон можно эффективно использовать как при острых, так и при хронических заболеваниях. Он отличается быстротой действия, отсутствием побочных эффектов и возможностью длительного применения вне стационара.
Его внедрение в клиническую практику следует рассматривать первым итогом в аспекте нового научного направления — поиска лекарственных препаратов среди синтетических фосфорорганических соединений с низкой токсичностью, не проявляющих антихолинэстеразной активности, оказывающих многогранное влияние на метаболические процессы.
Димефосфон — диметиловый эфир 1,1-диметил-3-оксобутилфосфоновой кислоты — синтезирован в ИОФХ имени А. Е. Арбузова Казанского филиала АН СССР (Б. А. Арбузов, А. О. Визель, А. А. Муслинкин и др.). Экспериментальное изучение (И. А. Студенцова, P. С. Гараев, И. В. Заиконникова, И. С. Мокринская, P. X. Хафизьянова, В. Ш. Исмагилов и др.) выявило низкую его токсичность. Он хорошо всасывается из желудочно-кишечного тракта, не накапливается в организме, хорошо переносится онтогенетически незрелыми животными.
Способность димефосфона оказывать нормализующее действие на кислотно-основное состояние была выявлена в условиях моделирования рахита (В. П. Булатов), глюкозоаминофосфатного (С. В. Мальцев) и аллоксанового диабета. Экспериментально показана способность димефосфона активировать ключевой фермент пентозного цикла — глюкозоб-фосфатдегидрогеназу (И. А. Студенцова, Л. А. Ашаева), снижать уровень пировиноградной кислоты крови (В. П. Булатов), усиливать эндогенное дыхание и внешний путь окисления в митохондриях (Л. И. Анчикова и соавт.). При клиническом его изучении было установлено, что препарат вызывает интенсификацию функционирования почечного и легочного механизмов регуляции кислотно-основного состояния, ускорение внутриорганного кровотока и тканевого метаболизма. Он усиливает реабсорбцию бикарбонатов, процессы ацидо- и аммониогенеза в почках, вентиляционную функцию легких (С. В. Мальцев).
Терапевтическая активность димефосфона установлена клиническими испытаниями, проведенными в различных медицинских учреждениях Советского Союза. Его включение в комплексную терапию пневмонии (исследования коллективов, руководимых профессорами А. В. Мазуриным, Ю. Е. Вельтищевым, К. А. Святкиной, Л. А. Исаевой и др.) ускоряет нормализацию кислотноосновного состояния, улучшает общее самочувствие больных, уменьшает одышку. Антиацидотическое действие препарата проявляется через 2—3 ч после первого приема и выражается в повышении pH крови, увеличении АВ и SB, уменьшении рСО2. Длительность курса лечения — 3—10 дней в зависимости от тяжести процесса.
При лечении детей с тяжелыми формами ОРВИ, осложненной пневмонией, было установлено (проф. А. Д. Царегородцев и сотр.), что однократный прием димефосфона вызывает достоверный сдвиг в сторону нормализации pH, BE, SB. Через сутки все параметры, характеризующие кислотно-основное состояние не отличались от показателей здоровых детей; исключение составил лишь BE, который нормализовался после пятидневного курса лечения. У детей контрольной группы нормализация кислотно-основного состояния происходила значительно медленнее. Включение в комплексную терапию препарата сокращало лихорадочный период, продолжительность интоксикации и физикальных изменений в легких, ускоряло клиническое выздоровление.
В процессе лечения димефосфоном детей с инфекционными болезнями (проф. Д. Ш. Еналеева и сотр.), в частности гриппом и ОРВИ, было выявлено повышение pH, уменьшение дефицита оснований и снижение рСО2 уже через 3 ч после однократного его приема. Введение димефосфона в комплексное лечение инфекционных заболеваний, в том числе вирусных гепатитов, способствовало нормализации кислотно-основного состояния, облегчало их клиническое течение, сокращало сроки стационарного лечения.
При хронических неспецифических заболеваниях легких с функциональными нарушениями сердечно-сосудистой системы у детей (проф. М. Р. Рокицкий, проф. В. Ф. Жаворонков, В. П. Панкова, акад. АМН СССР Г. А. Баиров и corp.) прием димефосфона приводил к улучшению состояния больных, уменьшению одышки, повышению толерантности к физической нагрузке. После 2—3-недельного курса лечения pH и рСО2 достоверно смещались в сторону нормализации.
При сахарном диабете (проф. В. В. Талантов, Т. В. Булатова, проф. А. М. Грановская-Цветкова) двухнедельный курс приема димефосфона способствовал нормализации кислотно-основного состояния, содержания в крови пировиноградной и молочной кислот независимо от тяжести заболевания и от вида базисной антидиабетической терапии. Больные, принимавшие димефосфон, отмечали улучшение общего состояния, нормализацию сна, уменьшение неприятных ощущений в ногах.
При витамин-D-дефицитном рахите (проф. К. А. Святкина, В. П. Булатов) выявили нормализующее влияние препарата на pH, SB, BE и рСО2, содержание в крови кальция и фосфора, а также улучшение состояния детей.
При рахитоподобных заболеваниях, сопровождавшихся ацидозом (проф. С В. Мальцев и сотр.), курс лечения в течение 1— 2 мес улучшал состояние больных: уменьшал утомляемость и мышечную слабость, способствовал исчезновению болей в ногах при ходьбе. Объективно регистрировалось нормализующее действие на pH, SB и BE.
В послеоперационном периоде (акад. АМН СССР Г. А. Баиров, проф. М. Р. Рокицкий, проф. В. Ф. Жаворонков, В. П. Панкова, А. А. Визель и др.) под действием димефосфона ускорялась нормализация pH и рСО2.
Обычно димефосфон не вызывает побочных эффектов. Лишь при повышенной индивидуальной чувствительности наблюдаются диспептические расстройства, которые быстро проходят при отмене препарата. Его не рекомендуется назначать для коррекции кислотно-основного состояния при тяжелой недостаточности функции почек — органа, участвующего в реализации антиаци- дотической активности препарата.
В лекарственной форме для приема внутрь (15% водный раствор во флаконах по 100 мл) димефосфон выпускается заводами «Санитас» и «Татхимфармпрепараты», постоянно поступает в аптечную сеть.
Препарат широко применяется в клиниках различного профиля, раскрываются его новые терапевтические возможности.
