Преждевременная эякуляция (ПЭ) – функциональное половое расстройство у мужчин, которое проявляется коротким половым актом, продолжительность которого недостаточна для сексуального удовлетворения обоих партнеров.
Согласно современным клиническим рекомендациям Международной ассоциации по сексуальной медицине (ISSM), выделяют первичную и вторичную формы преждевременной эякуляции. При этом к первому варианту описанного сексуального расстройства относят эякуляцию, возникающую приблизительно менее чем через 1 мин после начала коитуса или до интроекции и характеризующуюся возникновением с начала половой жизни, отсутствием контроля над эякуляторным процессом и негативным психологическим фоном у обоих партнеров. Вторичная форма ПЭ отличается приобретенным характером и временем интравагинальной задержки семяизвержения (ВИЗС) менее 3 мин.
По статистике ВОЗ с проблемой, когда половой акт длится менее 1 минуты, встречаются 40% мужчин. Преждевременная эякуляция не является заболеванием, но она порождает у мужчин комплексы и снижает самооценку. Это расстройство может нарушить отношения в паре и привести к разводу. Холостые мужчины избегают общения с женщинами и не решаются создать семью. Самое неприятное, что переживания мужчины по поводу преждевременной эякуляции могут повлечь за собой снижение потенции и половую дисфункцию (импотенцию).
Преждевременную эякуляцию разделяют на психогенную и органическую. В 80% случаев преждевременная эякуляция имеет психологическую природу. При психогенной форме причины расстройства исключительно психологические. Это могут быть пережитые психотравмы или внутренние конфликты. При органической форме у мужчин присутствуют заболевания или нарушения работы половых органов, эндокринной или нервной системы.
Абсолютная преждевременная эякуляция диагностируется в 2-х случаях:
- Семяизвержение во время предварительных ласк до введения полового члена во влагалище;
- Сразу после введения полового члена во влагалище;
Относительная преждевременная эякуляция – семяизвержение происходит до того, как оба партнера испытают сексуальное удовлетворение или в 50% случаев половой партнер не успевает получить оргазм по причине слишком короткого полового акта. Ранее критерии расстройства были более четкими. Преждевременной эякуляцией считалось состояние, когда семяизвержение наступало ранее, чем через 2 минуты после введения полового члена во влагалище или половой акт менее 8-15 фрикций.
Нарушением сексуальной функции не считается преждевременное семяизвержение в ситуациях, когда мужчина испытывает сильное сексуальное возбуждение: секс после длительного воздержания, чрезмерной стимуляции полового члена, близость с новой партнершей или женщиной к которой мужчина испытывает сильные чувства.
В начале лечения уролог определяет форму преждевременной эякуляции. Для того, чтобы исключить органические причины проводят ряд исследований:
- Пальцевое ректальное исследование предстательной железы. При этом определяют ее размер и эластичность.
- Микроскопия урологического мазка показывает наличие инфекций и воспалений.
- Бактериологический посев урологического мазка и определение чувствительности к антибиотикам.
- УЗИ предстательной железы, мошонки, полового члена.
- Определение вибрационной чувствительности головки полового члена.
- Определения кровоснабжения полового члена.
- При психогенной форме при обследовании не обнаруживается признаков болезни мочеполовой системы и позвоночника.
Признаки того, что у мужчины психогенная форма преждевременной эякуляции:
- Молодой возраст
- Отсутствие сексуального опыта и регулярной половой жизни
- При повторных половых актах их продолжительность может значительно возрастать
- Длительность зависит от того с какой партнершей и в каких обстоятельствах происходит половой акт
- Эякуляцию удается отсрочить при неприятных или отвлеченных мыслях
В психологической помощи нуждаются мужчины старше 30 лет с психогенной формой преждевременной эякуляции, если 50% и более половых актов заканчиваются преждевременной эякуляцией. Диагностикой и лечением преждевременного семяизвержения занимаются сексологи и урологи-андрологи, сексологи, а также психотерапевты и психологи. После тщательного сбора информации и обследования на основе жалоб пациента на преждевременную эякуляцию врач ставит диагноз.
Медикаментозное лечение ПЭ
Современная фармакотерапия обладает широкими возможностями в отношении коррекции ПЭ. Она включает использование таких групп препаратов как местные анестетики, селективные ингибиторы обратного захвата серотонина (СИОЗС), ингибиторы фосфодиэстеразы 5-го типа (иФДЭ-5) и а-адреноблокаторы.
В настоящее время препаратом выбора для лечения ПЭ является Дапоксетин-СЗ. Препарат из группы селективные ингибиторы обратного захвата серотонина. Действие препарата основано на блокировке рецепторов головного мозга и поглощении серотонина. Эякуляция контролируется напрямую из специальных центров в спинном мозге. Те, в свою очередь, подчиняются определенным ядрам головного мозга. Дапоксетин-СЗ приводит к увеличению тормозящего влияния ядер головного мозга на центры в спинном, что приводит к увеличению продолжительности полового акта.
Основное действующее вещество – дапоксетина гидрохлорид. Действие активного вещества имеет ряд доказанных преимуществ: эффективно продлевает половой акт, (при этом не снижая чувствительность), сохраняется интенсивность наслаждения, снижает стресс и страх неудачи, благодаря чему половой акт становится более насыщенным, комфортным, сексуальная близость приносит удовольствие обоим партнерам, а также заметно улучшает качество взаимоотношений между партнерами.
Дапоксетин- СЗ одобрен к применению в клинической практике для лечения ПС в 50 странах. Он рекомендован пациентам с ПС в возрасте от 18 до 64 лет. Применять таблетки необходимо перорально, запивайте их достаточным количеством жидкости. Но при этом использовать только безалкогольные напитки. Применять его следует в начальной дозировке 30 мг за 1–3 ч до полового акта при максимальной регулярности применения 1 раз в сутки. Препарат начинает действовать через 15-30 минут после приема, а продолжительность его воздействия на организм от 2 до 3 часов. Оптимальный эффект от применения препарата наступает в течение от 30 минут до 2 часов. Как правило, курс лечения назначается на 4 недели или 6-разовый прием. Если пациент принимает препарат в первый раз, используются таблетки, которые содержит 30 мг активного вещества. Но если необходимый эффект не был достигнут, можно увеличить дозировку – на 60 мг в сутки. Превышать эту дозу не стоит, так как это может негативно сказаться на здоровье пациента. Препарат следует принимать не чаще 1 раза в сутки. Максимальная суточная доза при хорошей переносимости составляет 60 мг. Врач назначающий препарат Дапоксетин-СЗ для лечения преждевременной эякуляции должен оценить риск и пользу применения препарата после первых 4 недель лечения или как минимум после приема первых 6 доз и определить соотношение риск-польза для принятия решения о целесообразности дальнейшего лечения препаратом Дапоксетин-СЗ .
Дапоксетин- СЗ обладает быстрым фармакологическим действием и относительно коротким периодом полувыведения. В исследованиях E. Jannini и соавт. C. McMahon и соавт. отмечена его эффективность у мужчин с первичной и вторичной формой ПЭ. Пациенты после назначения дапоксетина 30-60 мг/сут отмечали увеличение показателя ВИЗС в 3 раза. Кроме того, препарат хорошо переносится лицами, страдающими ПЭ в сочетании с эректильной дисфункцией (ЭД). Если у мужчины при приеме препарата нарушается эрекция, то можно комбинировать Дапоксетин- СЗ и Силденафила- СЗ или Тадалафил-СЗ (дозы препаратов подбирает врач-уролог), устраняющая данный нежелательный эффект.
Клиницисты выделяют два основных преимущества Дапоксетина-СЗ перед другими, более ранними, представителями ингибиторов обратного захвата серотонина. В отличие от остальных препаратов данной группы, имеющих галогенированные молекулы, в его молекулярной структуре содержится нафтильный фрагмент. Именно он обусловливает быструю абсорбцию препарата в желудочно-кишечном тракте и короткий период полувыведения, что обеспечивает значительно меньшее число побочных эффектов по сравнению с другими СИОЗС. Первое преимущество -это скорость достижения клинического эффекта от препарата. За счет быстрой реабсорбции препарата, максимальная его концентрация в организме достигается уже через 1-2 часа после приема. Благодаря этому свойству дапоксетин можно принимать «по требованию» и нет необходимости в длительном курсовом приеме. Второе преимущество кроется в быстрой экскреции препарата. Дапоксетин СЗ, в отличие от вышеописанных препаратов, не обладает накопительным эффектом. Это обусловлено быстрым выведением препарата из Таким образом, специалисты могут назначать Дапоксетин- СЗ своим пациентам без риска получить тяжелые побочные реакции.
Следует понимать, что при назначении данного лекарственного препарата и кратности его приема врач-уролог должен руководствоваться предпочтениями самого пациента и образом его жизни. Так, например, молодым мужчинам, которые ведут активную половую жизнь справедливо назначать СИОЗС в режиме ежедневного приема; в то время как прием «по-требованию» хорошо подойдет лицам редко или эпизодически вступающим в интимную близость со своим партнером.
Дапоксетин- СЗ выпускается в форме таблеток, принимать препарат рекомендуется один раз в сутки и только после консультации с лечащим врачом. Перед приемом препарата, рекомендуется проверить кровяное давление. Если показатели низкие, то принимать Дапоксетин запрещено.
Побочные эффекты
В результате исследования в США в 2009 году урологи определили, что чаще всего после приёма дапоксетина у мужчин появлялись: головокружение, головная боль, тошнота, бессонница, диарея. Однако эти побочные явления не оказывают серьёзного вреда для здоровья. Нежелательные побочные явления составляют не более 10%.
Препарат противопоказан при выраженной сердечной недостаточности, нарушениях проводимости, наличии искусственного водителя ритма, тяжелой ишемической болезни сердца и заболеваниях его клапанов, а также тяжелой почечной недостаточности. Кроме того, дапоксетин не следует назначать при среднетяжелых и тяжелых формах печеночной недостаточности и пациентам, которым проводится параллельное лечение лекарствами, ингибирующими активность цитохромов-P450 и любыми психотропными препаратами. Следует также избегать его совместного применения с алкоголем.
Дапоксетин- СЗ нельзя принимать одновременно с такими препаратами как : аспирин, варфарин, кетоконазол, ипрониазид, линезолид, бефол, ритонавир, антидепрессанты, саквинавир, а так же лекарства, произведённые на основе лития.
Таким образом, в настоящий момент доказана хорошая эффективность и достаточная безопасность Дапоксетина- СЗ при терапии всех форм ПЭ. Появление его на российском рынке открывает новые перспективы в консервативном лечении многочисленных пациентов с ускоренной эякуляцией в нашей стране.
Дапоксетин-СЗ (Dapoxetine-SZ) инструкция по применению
📜 Инструкция по применению Дапоксетин-СЗ
💊 Состав препарата Дапоксетин-СЗ
✅ Применение препарата Дапоксетин-СЗ
📅 Условия хранения Дапоксетин-СЗ
⏳ Срок годности Дапоксетин-СЗ
Актуальная урология от НАО «Северная звезда»
Терапия преждевременной эякуляции
Это видео содержит информацию, доступ к
которой могут иметь только специалисты в области медицины и фармации
Вы являетесь специалистом?
Да
Нет


Препарат Дапоксетин-СЗ
Это видео содержит информацию, доступ к
которой могут иметь только специалисты в области медицины и фармации
Вы являетесь специалистом?
Да
Нет


Производство жидких лекарственных форм
В Ленобласти открылся новый корпус фармацевтического завода «Северная звезда»
Фармзавод «Северная Звезда» в Ленобласти запустил производство спреев, глазных капель и инъекционных растворов
Препарат отпускается по рецепту
Температура хранения: от 2 до 25 °С

Описание лекарственного препарата
Дапоксетин-СЗ
(Dapoxetine-SZ)
Основано на общей характеристике лекарственного препарата (ОХЛП), утверждено
компанией-производителем и подготовлено для электронного справочника Видаль 2025 года.
Дата обновления: 2025.01.31
Код ATX:
G04BX14
(Дапоксетин)
Лекарственные формы
|
Препарат отпускается по рецепту |
Дапоксетин-СЗ |
Таблетки, покрытые пленочной оболочкой, 30 мг: 4, 6, 8, 10, 12, 20 или 30 шт. рег. №: ЛП-(007595)-(РГ-RU) |
|
Таблетки, покрытые пленочной оболочкой, 60 мг: 4, 6, 8, 10, 12, 20 или 30 шт. рег. №: ЛП-(007595)-(РГ-RU) |
Форма выпуска, упаковка и состав
препарата Дапоксетин-СЗ
Таблетки, покрытые пленочной оболочкой от светло-желтого до желтого цвета, круглые, двояковыпуклые; на поперечном разрезе ядро таблетки белого или почти белого цвета.
Вспомогательные вещества: лактозы моногидрат (сахар молочный), кроскармеллоза натрия (примеллоза), целлюлоза микрокристаллическая 102, кремния диоксид коллоидный (аэросил), магния стеарат.
Состав оболочки: гипромеллоза, полисорбат-80 (твин-80), тальк, титана диоксид (E171), краситель железа оксид желтый (E172).
4 шт. — упаковки ячейковые контурные (1) — пачки картонные.
6 шт. — упаковки ячейковые контурные (1) — пачки картонные.
6 шт. — упаковки ячейковые контурные (2) — пачки картонные.
8 шт. — упаковки ячейковые контурные (1) — пачки картонные.
10 шт. — упаковки ячейковые контурные (1) — пачки картонные.
10 шт. — упаковки ячейковые контурные (2) — пачки картонные.
10 шт. — упаковки ячейковые контурные (3) — пачки картонные.
20 шт. — банки полимерные (1) — пачки картонные.
20 шт. — флаконы полимерные (1) — пачки картонные.
Таблетки, покрытые пленочной оболочкой от светло-желтого до желтого цвета, круглые, двояковыпуклые; на поперечном разрезе ядро белого или почти белого цвета.
Вспомогательные вещества: лактозы моногидрат (сахар молочный), кроскармеллоза натрия (примеллоза), целлюлоза микрокристаллическая 102, кремния диоксид коллоидный (аэросил), магния стеарат.
Состав оболочки: гипромеллоза, полисорбат-80 (твин-80), тальк, титана диоксид (E171), краситель железа оксид желтый (E172).
4 шт. — упаковки ячейковые контурные (1) — пачки картонные.
6 шт. — упаковки ячейковые контурные (1) — пачки картонные.
6 шт. — упаковки ячейковые контурные (2) — пачки картонные.
8 шт. — упаковки ячейковые контурные (1) — пачки картонные.
10 шт. — упаковки ячейковые контурные (1) — пачки картонные.
10 шт. — упаковки ячейковые контурные (2) — пачки картонные.
10 шт. — упаковки ячейковые контурные (3) — пачки картонные.
20 шт. — банки полимерные (1) — пачки картонные.
20 шт. — флаконы полимерные (1) — пачки картонные.
Фармакологическое действие
Дапоксетин представляет собой мощный селективный ингибитор обратного захвата серотонина (СИОЗС) с концентрацией полумаксимального ингибирования (IC50) 1.12 нМ, метаболизирующийся в организме до основных метаболитов — дезметилдапоксетина (IC50<1.0 нМ) и дидезметилдапоксетина (IC50=2.0 нМ), в равной степени или менее активных (дапоксетин-N-оксид (IC50=282 нМ)).
Механизм действия дапоксетина при преждевременной эякуляции (ПЭ) связан с торможением обратного захвата серотонина нейронами с последующим усилением действия нейромедиатора на пре- и постсинаптические рецепторы.
У крыс дапоксетин ингибирует рефлекторный механизм наступления эякуляции с помощью воздействия на латеральное парагигантоклеточное ядро на супраспинальном уровне. Постганглионарные симпатические волокна, иннервирующие семенные пузырьки, семявыносящий проток, предстательную железу, мышцы, охватывающие бульбоуретральные железы и шейку мочевого пузыря, вызывают их координированные сокращения, необходимые для возникновения эякуляции. У крыс дапоксетин изменяет данный рефлекторный механизм наступления эякуляции.
Клиническая безопасность и эффективность
Эффективность дапоксетина при лечении по поводу ПЭ была установлена при проведении пяти двойных слепых клинических исследований с контролем плацебо, в рамках которых был рандомизирован, в общей сложности, 6081 пациент. Возраст пациентов был 18 лет и старше, и в течение 6 месяцев до включения данных лиц в исследование у них в большинстве половых актов имела место ПЭ. ПЭ определялась в соответствии с диагностическими критериями DSM-IV (Руководство по диагностике и статистике психических расстройств): короткое время наступления эякуляции (интравагинальное латентное время эякуляции [IELT; время от вагинальной пенетрации до интравагинальной эякуляции] составляет менее, чем 2 минуты, что измерялось с использованием секундомера в четырех исследованиях), слабый контроль над эякуляцией, а также обусловленные данным состоянием значительный стресс или сложности в межличностных отношениях.
Лица с другими видами половой дисфункции, включая эректильную дисфункцию (ЭД), а также лица, принимающие другие лекарственные препараты для лечения по поводу ПЭ, были исключены из всех исследований.
Результаты всех рандомизированных исследований являлись сопоставимыми. Эффективность демонстрировалась после 12 недель лечения. В одно исследование были включены пациенты как из стран ЕС, так и из других стран, а продолжительность лечения составляла 24 недели. В данном исследовании были рандомизированы 1162 пациента: 385 принимали плацебо, 388 принимали дапоксетин в дозе 30 мг по мере необходимости и 389 принимали дапоксетин в дозе 60 мг по мере необходимости. Среднее значение и медиана показателя среднего IELT в конце исследования представлены в таблице 1 ниже, а совокупное распределение субъектов, достигших, по меньшей мере, характерного уровня среднего IELT в конце исследования, представлено в таблице 3 ниже. Другие исследования и объединенный анализ данных на 12 неделе показали сходные результаты.
Таблица 1. Среднее значение и медиана показателя IELT в конце лечения, вычисленные методом наименьших квадратов*
*Исходное значение, перенесенное на пациентов с отсутствием исходных данных.
**Различие было статистически значимым (значение р ≤ 0.001).
Таблица 2. Субъекты, достигшие, по меньшей мере, характерного уровня среднего IELT в конце исследования*
* Исходное значение, перенесенное на пациентов с отсутствием исходных данных.
Значение удлинения IELT было соотнесено с исходным уровнем IELT и было различным у отдельных пациентов. Клиническая значимость эффекта от приема дапоксетина была также продемонстрирована при помощи анализа исхода лечения, о котором сообщали различные пациенты, у которых проявлялся терапевтический эффект. Пациент с терапевтическим эффектом был определен как субъект, у которого имело место повышение контроля за эякуляцией как минимум на 2 категории, а также снижение уровня стресса в связи с эякуляцией как минимум на 1 категорию. У большего процента субъектов в каждой из групп, принимавших дапоксетин, по сравнению с плацебо, терапевтический эффект развился в конце 12 или 24 недели исследования, что являлось статистически достоверным. В группах участников, принимавших дапоксетин в дозах 30 мг (11% – 95% ДИ [7.24; 14.87]) и 60 мг (16.4% – 95% ДИ [13.01; 19.75]), на 12 неделе имел место больший процент пациентов с терапевтическим эффектом по сравнению с группой участников, принимавших плацебо (объединенный анализ).
Клиническое значение эффекта от лечения дапоксетином было показано на примере терапевтической группы для измерения результата. Оценки общего клинического впечатления (CGIC), где пациентов просили сравнить ПЭ у себя с момента начала лечения, с градацией ответов от «гораздо лучше» до «гораздо хуже». В конце исследования (24 неделя) 28.4% (дапоксетин в дозе 30 мг) и 35.5% (дапоксетин в дозе 60 мг) субъектов, принимавших дапоксетин, сообщили, что их состояние стало «лучше» или «гораздо лучше», по сравнению с 14% в группе участников, принимавших плацебо, а 53.4% и 65.6% субъектов, принимавших дапоксетин в дозе 30 мг и 60 мг, соответственно, сообщили, что их состояние стало как минимум «немного лучше», по сравнению с 28.8% в группе плацебо.
Фармакокинетика
Всасывание
Дапоксетин быстро всасывается, Cmax в плазме крови достигается через 1-2 ч после приема препарата. Абсолютная биодоступность равна 42% (диапазон 15-76%) и экспозиция (AUC и Cmax) увеличивается пропорционально дозе в интервале от 30 мг до 60 мг. После многократного перорального приема AUC дапоксетина и его активного метаболита дезметилдапоксетина увеличивается примерно на 50% по сравнению со значениями AUC после однократного приема.
Прием жирной пищи умеренно уменьшает Cmax дапоксетина (на 10%) и на 12% увеличивает AUC и время достижения Cmax в плазме крови. Эти изменения клинически не значимы. Препарат Дапоксетин-СЗ можно принимать независимо от приема пищи.
Распределение
Более 99% дапоксетина связывается с белками плазмы in vitro. Активный метаболит — дезметилдапоксетин — связывается с белками плазмы крови на 98.5%. Дапоксетин распределяется по организму со средним равновесным Vd 162 л.
Метаболизм
Исследования in vitro позволяют предположить, что дапоксетин метаболизируется многими ферментами печени и почек, особенно CYP2D6, CYP3A4 и флавинсодержащей монооксигеназой (ФМ01) почек. В клиническом исследовании, в ходе которого изучался метаболизм 14C-дапоксетина, дапоксетин после перорального приема активно метаболизировался в основном путем N-окисления, N-деметилирования, гидроксилирования нафтогруппы, глюкуронизации и присоединения сульфогруппы. После перорального приема обнаружены признаки пресистемного метаболизма в печени. Основными компонентами, циркулирующими в плазме крови, были интактный дапоксетин и дапоксетин-N-оксид. В исследованиях in vitro обнаружено, что дапоксетин-N-оксид неактивен. Кроме того, обнаруживались дезметилдапоксетин и дидезметилдапоксетин в количестве менее 3% от общего количества циркулирующих метаболитов дапоксетина. В исследовании in vitro установлено, что дезметилдапоксетин по активности сопоставим с дапоксетином, а дидезметилдапоксетин примерно в 2 раза менее активен, чем дапоксетин. Экспозиция (AUC и Cmax) несвязанного дезметилдапоксетина составляла 50% и 23% от несвязанного дапоксетина соответственно.
Выведение
Метаболиты дапоксетина выводятся в основном почками в виде конъюгатов. Дапоксетин в неизменном виде в моче не обнаруживается. После перорального приема начальный (диспозиционный) Т1/2 дапоксетина составляет приблизительно 1.5 ч, уровень в плазме составляет менее 5% от Cmax через 24 ч после приема, а конечный Т1/2 составляет около 19 ч. При ежедневном приеме конечный Т1/2 составляет примерно 19 ч.
Фармакокинетика у особых групп пациентов
Метаболит дезметилдапоксетин усиливает фармакологический эффект дапоксетина, особенно, если концентрация его повышена. Ниже продемонстрировано повышение параметров активной фракции в некоторых группах пациентов. Она представляет собой сумму концентраций свободного дапоксетина и дезметилдапоксетина. Дезметилдапоксетин и дапоксетин обладают одинаковой эффективностью. Предварительные расчеты позволяют предполагать такое же распределение дезметилдапоксетина в ЦНС, однако неизвестно, так ли это.
Раса. Однократный прием дапоксетина в дозе 60 мг не выявил статистически достоверного различия показателей у представителей европеоидной расы, негроидной расы, латиноамериканцев и представителей монголоидной расы. Сравнение фармакокинетики дапоксетина у представителей европеоидной расы и японцев показало более высокие значения Cmax и AUC у последних (на 10-20%) из-за меньшей массы тела. Более высокий уровень системного воздействия вряд ли вызывает значимое различие клинического эффекта.
Пожилые пациенты (65 лет и старше). Анализ исследования клинической фармакологии с однократным приемом дапоксетина в дозе 60 мг не выявил существенного различия показателей фармакокинетики (Cmax, AUC0-∞, Тmax) у здоровых пожилых мужчин и здоровых мужчин более молодого возраста.
Почечная недостаточность. Клиническое фармакологическое исследование однократного применения дапоксетина в дозе 60 мг было проведено у пациентов с нарушением функции почек легкой (КК от 50 до 80 мл/мин), средней (КК от 30 до < 50 мл/мин) и тяжелой (КК < 30 мл/мин) степени, а также у субъектов с нормальной функцией почек (КК > 80 мл/мин). Явной тенденции к повышению AUC дапоксетина при нарушении функции почек не выявлено. У субъектов с нарушением функции почек тяжелой степени AUC было приблизительно в 2 раза выше, чем у субъектов с нормальной функцией почек, хотя у пациентов с нарушением функции почек тяжелой степени данные ограничены. У пациентов, находящихся на почечном диализе, оценка фармакокинетики дапоксетина не проводилась.
Печеночная недостаточность. У пациентов с печеночной недостаточностью легкой степени Cmax несвязанного дапоксетина снижалась на 28%, AUC не изменялась. Cmax и AUC активной фракции (сумма несвязанных фракций дапоксетина и дезметилдапоксетина) снижались на 30% и 5% соответственно. У пациентов с печеночной недостаточностью средней степени тяжести Cmax несвязанного дапоксетина обычно не изменяется (снижается в пределах 3%), AUC увеличивается на 66%. Cmax несвязанной активной фракции дапоксетина была неизменна, a AUC увеличена в 2 раза. У пациентов с печеночной недостаточностью тяжелой степени Cmax несвязанного дапоксетина была снижена на 42%, a AUC несвязанного дапоксетина была увеличена примерно на 223%. Cmax и AUC активной фракции изменялись подобным образом.
Полиморфизм CYP2D6. В клиническом фармакологическом исследовании однократного применения концентрация дапоксетина в дозе 60 мг, концентрация в плазме крови была выше у слабых метаболизаторов CYP2D6, чем у активных метаболизаторов CYP2D6 (приблизительно Cmax – на 31%, AUC0-∞ дапоксетина – на 36%, Cmax – на 98%, AUC0-∞ дезметилдапоксетина – на 161%). Значение Сmax активной фракции препарата Дапоксетин-СЗ может быть повышено приблизительно на 46%, a AUC – приблизительно на 90%. Данное повышение может увеличить частоту и усугубить тяжесть нежелательных реакций, зависящих от дозы. При приеме препарата Дапоксетин-СЗ у пациентов с низкой активностью CYP2D6 особое внимание следует обратить на безопасность при совместном приеме других лекарственных препаратов, которые могут ингибировать биотрансформацию дапоксетина, таких как ингибиторы CYP3A4 средней выраженности действия и сильные ингибиторы CYP3A4.
Показания препарата
Дапоксетин-СЗ
Препарат Дапоксетин-СЗ показан для лечения преждевременной эякуляции у мужчин в возрасте от 18 до 64 лет.
Препарат Дапоксетин-СЗ можно применять только у пациентов, удовлетворяющих все нижеперечисленные критерии:
- интравагинальное время задержки эякуляции (ИВВЗЭ) <2 мин;
- постоянно или регулярно возникающая эякуляция после минимальной сексуальной стимуляции перед, во время или вскоре после полового проникновения, и наступающая раньше желаемого пациентом момента;
- выраженный личностный дистресс или затруднения в межличностных отношениях вследствие преждевременной эякуляции;
- слабый контроль эякуляции;
- наступление преждевременной эякуляции в большинстве попыток осуществления полового акта за последние 6 месяцев.
Препарат Дапоксетин-СЗ следует применять только в режиме приема по потребности перед предполагаемой сексуальной активностью. Препарат Дапоксетин-СЗ не следует применять для задержки эякуляции у мужчин, не имеющих подтвержденного диагноза преждевременной эякуляции.
Режим дозирования
Внутрь. Таблетку следует проглатывать целиком, запивая, по крайней мере, одним полным стаканом воды. Препарат Дапоксетин-СЗ можно принимать независимо от времени приема пищи.
Взрослые мужчины от 18 до 64 лет
Рекомендуемая начальная доза для всех пациентов составляет 30 мг; эту дозу принимают за 1-3 ч до предполагаемого полового акта. Лечение препаратом Дапоксетин-СЗ не следует начинать с дозы 60 мг.
Препарат Дапоксетин-СЗ не предназначен для постоянного ежедневного применения. Его следует принимать только в случае предполагаемого полового акта. Препарат Дапоксетин-СЗ не следует принимать чаще, чем каждые 24 ч.
При недостаточном эффекте и хорошей переносимости дозы 30 мг (пациент не отмечает умеренных или тяжелых нежелательных реакций или явлений, которые могут предшествовать синкопальному состоянию), дозу можно увеличить до максимально рекомендуемой – 60 мг, с приемом по потребности за 1-3 ч до сексуальной активности. Частота и тяжесть нежелательных реакций выше при приеме препарата в дозе 60 мг.
Если у пациента отмечались ортостатические реакции при приеме начальной дозы, не следует повышать дозу до 60 мг (см. раздел «Особые указания»).
После первых 4 недель терапии (или, по меньшей мере, после приема 6 доз препарата) врач должен провести тщательную оценку соотношения пользы и риска препарата Дапоксетин-СЗ в каждом конкретном случае для решения вопроса о целесообразности продолжения лечения данным препаратом.
Данные об эффективности и безопасности применения дапоксетина в течение более 24 недель ограничены. Клиническую необходимость продолжения терапии и соотношения польза/риск от применения препарата Дапоксетин-СЗ следует оценивать, как минимум, каждые 6 месяцев.
Особые группы пациентов
Пациенты пожилого возраста (≥ 65 лет)
Эффективность и безопасность препарата Дапоксетин-СЗ у пациентов ≥ 65 лет не установлены.
Пациенты с нарушением функции почек
При приеме препарата пациентами с нарушениями функции почек легкой и средней степени тяжести следует соблюдать осторожность. Препарат Дапоксетин-СЗ противопоказан пациентам с почечной недостаточностью тяжелой степени .
Пациенты с нарушением функции печени
Препарат Дапоксетин-СЗ противопоказан пациентам с умеренно выраженным и тяжелым нарушениями функции печени (классы В и С по классификации Чайлд-Пью).
Пациенты с низкой активностью CYP2D6 и пациенты, одновременно принимающие сильные ингибиторы CYP2D6
Следует проявлять осторожность при увеличении дозы препарата Дапоксетин-СЗ до 60 мг у пациентов с низкой активностью CYP2D6 или у пациентов, принимающих препарат Дапоксетин-СЗ одновременно с сильными ингибиторами CYP2D6. Рекомендуется соблюдать осторожность при повышении дозы до 60 мг у пациентов, у которых диагностирован низкий метаболизм CYP2D6, и у пациентов, одновременно принимающих сильные ингибиторы CYP2D6.
Пациенты, получающие сильные ингибиторы CYP3A4 или ингибиторы CYP3A4 средней выраженности действия
Одновременный прием дапоксетина с сильными ингибиторами CYP3A4 противопоказан. Пациентам, одновременно принимающим ингибиторы CYP3A4 средней выраженности действия, необходимо соблюдать осторожность и не превышать дозу равную 30 мг.
Дети
Препарат Дапоксетин-СЗ противопоказан у детей и подростков в возрасте до 18 лет.
Побочное действие
В клинических исследованиях были зарегистрированы синкопе и ортостатическая гипотензия/
В клинических исследованиях фазы 3 зарегистрированы следующие нежелательные реакции, которые наблюдались часто и были дозозависимыми: тошнота (11.0% и 22.2% при приеме 30 мг и 60 мг дапоксетина соответственно), головокружение (5.8% и 10.9%), головная боль (5.6% и 8.8%), диарея (3.5% и 6.9%), бессонница (2.1% и 3.9%), усталость (2.0% и 4.1%). Самыми частыми реакциями, требовавшими отмены лечения, были тошнота (у 2.2% пациентов) и головокружение (1.2% пациентов).
Безопасность дапоксетина оценивалась у 4224 пациентов с ПЭ, принимавших участие в 5 двойных слепых плацебо-контролируемых клинических исследованиях. Из 4224 пациентов 1616 пациентов принимали дапоксетин в дозе 30 мг по мере необходимости, а 2608 – в дозе 60 мг либо по мере необходимости, либо 1 раз/сут.
Нежелательные реакции, наблюдавшиеся в ходе клинических исследований дапоксетина, распределены по системно-органным классам с указанием частоты их возникновения согласно рекомендациям ВОЗ: очень часто (≥1/10), часто (≥1/100-<1/10), нечасто (≥1/1000-<1/100), редко (≥1/10000-<1/1000).
Нежелательные реакции, о которых сообщалось при проведении 9-месячного долгосрочного расширенного открытого исследования, были аналогичны тем, о которых сообщалось при проведении двойных слепых исследований. О дополнительных нежелательных реакциях не сообщалось.
Описание отдельных нежелательных реакций
Обмороки с потерей сознания, с брадикардией или остановкой синусового узла наблюдались у пациентов при холтеровском мониторировании и были зарегистрированы в клинических исследованиях. Данные нежелательные реакции расценены как связанные с применением дапоксетина. Большинство случаев наблюдались в течение первых 3 часов после приема дапоксетина, после приема первой дозы или ассоциированы с медицинскими процедурами (забор крови, изменения положения тела, измерение артериального давления). Продромальные симптомы часто предшествовали обмороку.
Возникновение обморока и, возможно, продромальных симптомов зависит, по всей видимости, от дозы, что было продемонстрировано более высокой частотой их возникновения среди пациентов, принимавших дапоксетин в клинических исследованиях 3 фазы в дозах, превышающих рекомендуемые.
При проведении клинических исследований имели место сообщения о возникновении ортостатической гипотензии. Частота возникновения синкопе, характеризующегося потерей сознания, в программе клинической разработки дапоксетина варьировалась в зависимости от исследуемой популяции и находилась в диапазоне от 0.06% (30 мг) до 0.23% (60 мг) у лиц, включенных в фазу 3 клинических плацебо-контролируемых исследований, и до 0.64% (все дозы вместе) для фазы 1 исследования с участием здоровых добровольцев без наличия ПЭ.
Другие особые группы пациентов
Следует соблюдать осторожность при повышении дозы до 60 мг у пациентов, принимающих сильнодействующие ингибиторы CYP2D6, или при повышении дозы до 60 мг у пациентов, имеющих генотип слабых метаболизаторов CYP2D6.
Эффекты при отмене препарата
При внезапной отмене СИОЗС, длительно применяемых для лечения хронических депрессивных расстройств, отмечались следующие симптомы: дисфорическое состояние, раздражительность, возбуждение, головокружение, сенсорные нарушения (например, парестезия в виде ощущения удара электротоком), тревожность, спутанность сознания, головная боль, летаргия, эмоциональная лабильность, бессонница и гипомания.
Результаты исследования безопасности показали более высокую частоту симптомов отмены в виде бессонницы и головокружения легкой и умеренной степени после отмены препарата через 62 дня применения.
Сообщение о подозреваемых нежелательных реакциях
Важно сообщать о подозреваемых нежелательных реакциях после регистрации лекарственного препарата с целью обеспечения непрерывного мониторинга соотношения «польза – риск» лекарственного препарата. Медицинским работникам рекомендуется сообщать о любых подозреваемых нежелательных реакциях лекарственного препарата через национальную систему сообщения о нежелательных реакциях государств – членов Евразийского экономического союза.
Противопоказания к применению
- повышенная чувствительность к дапоксетину и/или к любому вспомогательному веществу, входящему в состав препарата;
- выраженная патология со стороны сердца, такая как:
- сердечная недостаточность (II-IV класса по NYHA);
- нарушения проводимости, такие как атриовентрикулярная блокада (AV-блокада) или СССУ;
- выраженная ИБС;
- выраженный клапанный порок;
- наличие обмороков в анамнезе;
- наличие мании или тяжелой депрессии в анамнезе;
- одновременный прием ингибиторов МАО, или если после прекращения их приема прошло менее 14 дней. Подобным образом, ингибиторы МАО не следует принимать в течение 7 дней после окончания приема препарата Дапоксетин-СЗ;
- одновременный прием тиоридазина, или период в течение 14 дней после окончания приема тиоридазина. Соответственно, тиоридазин не следует принимать в течение 7 дней после окончания приема препарата Дапоксетин-СЗ;
- одновременный прием ингибиторов обратного захвата серотонина (СИОЗС, СИОЗСН, трициклические антидепрессанты) или других лекарственных препаратов/препаратов растительного происхождения с серотонинергическим действием (например, L-триптофан, триптаны, трамадол, линезолид, литий, зверобой продырявленный (Нypericum perforatum)), или в течение 14 дней после отмены данных лекарственных препаратов/препаратов растительного происхождения. Соответственно, данные лекарственные препараты/препараты растительного происхождения не следует принимать в течение 7 дней после окончания приема препарата Дапоксетин-СЗ;
- одновременный прием сильнодействующих ингибиторов CYP3A4, таких как кетоконазол, итраконазол, ритонавир, саквинавир, телитромицин, нефазодон, атазанавир и т.д.;
- умеренно выраженные и тяжелые нарушения функции печени;
- тяжелые нарушения функции почек;
- возраст до 18 лет.
С осторожностью
- у пациентов с почечной недостаточностью легкой степени или средней степени тяжести;
- одновременное применение с сильными ингибиторами изофермента CYP2D6 и ингибиторами CYP3A4 средней выраженности действия у пациентов с генотипически низкой активностью изофермента CYP2D6 и пациентов с высокой активностью изофермента CYP2D6 (в комбинации с ингибиторами изофермента CYP3A4 средней выраженности действия);
- одновременное применение с препаратами, которые влияют на агрегацию тромбоцитов, и с антикоагулянтами из-за риска развития кровотечений, а также у пациентов, имеющих в анамнезе кровотечения или нарушения свертывания.
Применение при беременности и кормлении грудью
Препарат Дапоксетин-СЗ не предназначен для применения у женщин.
Исследования на животных не выявили прямого или косвенного негативного влияния в отношении фертильности, беременности или развития эмбриона/плода.
Неизвестно, проникают ли дапоксетин и его метаболиты в грудное молоко.
Применение при нарушениях функции печени
Противопоказано применение препарата при печеночной недостаточности средней и тяжелой степени.
Применение при нарушениях функции почек
Противопоказано применение препарата при почечной недостаточности тяжелой степени.
Для пациентов с почечной недостаточностью легкой или средней степени коррекции дозы не требуется, но рекомендуется проявлять осторожность.
Применение у детей
Применение дапоксетина у пациентов моложе 18 лет противопоказано, т.к. отсутствуют клинические данные по эффективности и безопасности применения дапоксетина у этой популяции пациентов.
Применение у пожилых пациентов
Применение дапоксетина у пациентов старше 65 лет противопоказано, т.к. отсутствуют клинические данные по эффективности и безопасности применения дапоксетина у этой популяции пациентов.
Особые указания
Общие рекомендации
Дапоксетин предназначен только для мужчин с ПЭ, удовлетворяющих всем критериям, перечисленным в разделах «Показания» и «Фармакологическое действие». Дапоксетин нельзя применять мужчинам, которым не был поставлен диагноз ПЭ. Безопасность применения дапоксетина у мужчин без ПЭ не установлена, данных о задержке эякуляции нет.
Другие виды сексуальной дисфункции
Перед началом лечения пациентам с другими видами половых расстройств, включая ЭД, необходимо проведение тщательного врачебного обследования. Дапоксетин нельзя применять у мужчин с ЭД, принимающих ингибиторы ФДЭ5.
Ортостатическая гипотензия
Перед началом терапии врач должен провести тщательное медицинское обследование, включая выяснение анамнеза ортостатических событий, а также ортостатическую пробу (измерение АД и ЧСС в положении сидя и стоя). В случае подтвержденных или предполагаемых ортостатических реакций в анамнезе следует избегать терапии дапоксетином.
В клинических исследованиях описаны случаи ортостатической гипотензии. Врач должен заранее проинформировать пациента о том, что при появлении возможных продромальных симптомов, например, головокружения сразу после вставания, следует немедленно лечь так, чтобы голова оказалась ниже туловища или сесть, опустив голову между колен, и оставаться в этой позе до исчезновения симптомов. Врач, выписывающий дапоксетин, должен проинформировать пациента о необходимости избегать резкого вставания после длительного лежания или сидения.
Самоубийство/суицидальные мысли
В краткосрочных исследованиях антидепрессанты, включая СИОЗС, по сравнению с плацебо, сильнее повышали риск возникновения суицидальных мыслей и суицидальность у детей и подростков с большим депрессивным расстройством и другими психическими расстройствами. При проведении краткосрочных исследований повышение риска суицидальности при приеме антидепрессантов, по сравнению с плацебо, у взрослых старше 24 лет выявлено не было. В клинических исследованиях дапоксетина для лечения ПЭ четких данных о появлении суицидальных мыслей на фоне лечения, оцененных по Колумбийскому алгоритму классификации для оценки суицида (C-CASA), шкале оценки депрессии Монтгомери-Асберга или опроснику депрессии Бека, выявлено не было.
Обморок
Пациентам следует избегать потенциально травмоопасных ситуаций, в частности, управления транспортными средствами или механизмами, в случае возникновения обморока или его продромальных симптомов, таких как головокружение или предобморочное состояние (см. раздел «Побочное действие»). У пациентов, получавших дапоксетин, по сравнению с пациентами, получавшими плацебо, чаще отмечались продромальные симптомы, в т.ч. тошнота, головокружение/предобморочное состояние и повышенное потоотделение.
Наблюдавшиеся в клинических исследованиях случаи обморока, охарактеризованные как потеря сознания, с брадикардией или остановкой синусового узла у пациентов при холтеровском мониторировании, были отнесены на счет вазовагального происхождения, и большинство их имело место в течение первых 3 ч после приема, после первой дозы, или же были ассоциированы с медицинскими обследованиями в условиях клиники (забор крови, изменения положения тела, измерение АД). Возможные продромальные симптомы, например, тошнота, головокружение, предобморочное состояние, сердцебиение, астения, спутанность сознания и повышенное потоотделение обычно также наблюдались в первые 3 ч после приема дапоксетина и часто предшествовали обмороку. Пациенты должны быть проинформированы о том, что в период лечения дапоксетином в любое время возможно развитие обморока с продромальными симптомами или без них. Врач должен проинформировать пациента о важности достаточной водной нагрузки и о распознавании продромальных признаков и симптомов для снижения риска серьезной травмы при возможном падении из-за потери сознания. При появлении возможных продромальных симптомов пациент сразу должен лечь так, чтобы голова оказалась ниже туловища, или сесть, опустив голову между колен, и оставаться в этой позе до исчезновения симптомов. При обмороке или других нежелательных реакциях со стороны ЦНС пациента следует предупредить о необходимости избегать потенциально травмоопасных ситуаций, включая управление автомобилем и другими механизмами.
Пациенты с риском сердечно-сосудистых заболеваний
В клинических исследованиях дапоксетина не участвовали пациенты с сердечно-сосудистыми заболеваниями. У пациентов с органическими заболеваниями сердца и сосудов (например, обструкцией выброса крови из сердца, поражением клапанного аппарата, стенозом сонной артерии, атеросклерозом коронарной артерии) повышен риск нежелательных сердечно-сосудистых последствий обмороков (сердечного и другого происхождения). Однако в настоящее время недостаточно данных для определения, распространяется ли этот риск на вазовагальный обморок у пациентов с сердечно-сосудистыми заболеваниями.
Применение с наркотическими средствами
Пациентам не следует принимать дапоксетин вместе с наркотическими средствами. Одновременный прием дапоксетина с наркотическими средствами, обладающими серотонинергической активностью, например, кетамином, метилендиоксиметамфетамином (МДМА) и диэтиламидом лизергиновой кислоты (ЛСД) может приводить к потенциально серьезным реакциям, включая, но не ограничиваясь аритмией, гипертермией и серотониновым синдромом. Применение дапоксетина одновременно с седативными средствами, например, опиатами или бензодиазепинами, может усиливать сонливость и головокружение.
Применение с этанолом
Пациентам должно быть рекомендовано не принимать дапоксетин вместе с алкоголем. Совместное применение дапоксетина с алкоголем может усиливать его действие на ЦНС, а также может усилить такие нейрокардиогенные нежелательные реакции, как синкопе, повышая, таким образом, риск случайной травмы. Поэтому пациентам следует рекомендовать воздержаться от приема алкоголя в период приема дапоксетина.
Лекарственные средства с вазодилатирующими свойствами
Дапоксетин следует применять с осторожностью пациентам, принимающим лекарственные препараты с вазодилатирующими свойствами (такие как альфа-адреноблокаторы и нитраты), в связи с возможным снижением ортостатической толерантности.
Ингибиторы CYP3A4 средней выраженности действия
Следует соблюдать осторожность при назначении дапоксетина пациентам, принимающим ингибиторы CYP3A4 средней выраженности действия; доза не должна превышать 30 мг.
Сильные ингибиторы CYP2D6
Рекомендуется проявлять осторожность при повышении дозы дапоксетина до 60 мг у пациентов, получающих сильные ингибиторы CYP2D6, или при повышении дозы до 60 мг у пациентов, имеющих генотип слабого метаболизатора CYP2D6, так как при этом может повышаться уровень системного воздействия дапоксетина с соответствующим увеличением частоты и тяжести дозозависимых нежелательных реакций.
Мания
Дапоксетин нельзя принимать пациентам, имеющим в анамнезе манию/гипоманию или биполярное расстройство, при появлении симптомов этих заболеваний прием дапоксетина следует прекратить.
Судороги
Из-за способности СИОЗС снижать судорожный порог следует избегать назначения дапоксетина пациентам с нестабильной эпилепсией, при появлении судорог препарат следует отменить. За пациентами с контролируемой эпилепсией требуется тщательное наблюдение.
Сопутствующая депрессия и/или психические расстройства
Перед началом терапии дапоксетином мужчинам с наличием признаков и симптомов депрессии следует провести обследование для исключения наличия недиагностированных депрессивных расстройств. Совместный прием дапоксетина и антидепрессантов, включая СИОЗС и СИОЗСН, противопоказан. Прерывание лечения по поводу имеющейся депрессии или чувства тревоги для того, чтобы начать прием дапоксетина для терапии по поводу ПЭ, не рекомендуется. Прием дапоксетина не показан при психических нарушениях и не должен использоваться у мужчин с такими заболеваниями, как шизофрения, или у пациентов с сопутствующей депрессией, т.к. нельзя исключить усугубление симптомов, связанных с депрессией. Это может быть следствием фонового психического расстройства или следствием приема лекарственного препарата. Врач должен рекомендовать пациентам в любое время сообщать о любых депрессивных мыслях или чувствах, и, если явления и симптомы депрессии развились во время лечения, прием дапоксетина следует прекратить.
Кровотечение
При применении СИОЗС описаны случаи кровотечения. Рекомендуется проявлять осторожность при применении дапоксетина одновременно с препаратами, влияющими на функцию тромбоцитов (например, атипичными нейролептиками, фенотиазинами, ацетилсалициловой кислотой, НПВП, антикоагулянтами (например, варфарином)), а также у пациентов с кровотечениями или нарушением свертываемости крови в анамнезе.
Нарушение функции почек
Дапоксетин не рекомендуется принимать пациентам с тяжелым нарушением функции почек, пациентам с умеренно выраженным и легким нарушением функции почек следует проявлять осторожность.
Синдром отмены
Имеются данные о том, что резкая отмена СИОЗС, длительно применявшихся для лечения хронических депрессивных расстройств, приводит к следующим симптомам: снижение настроения, раздражительность, возбуждение, головокружение, нарушения чувствительности (например, парестезия в виде ощущения удара электротоком), тревожность, спутанность сознания, головная боль, сонливость, эмоциональная нестабильность, бессонница, гипомания.
В двойном слепом клиническом исследовании у лиц с ПЭ, проведенном для оценки синдрома отмены после приема дапоксетина в дозе 60 мг в течение 62 дней ежедневно или по потребности, у лиц, переведенных на плацебо после ежедневного приема дапоксетина, проявились умеренные симптомы в виде небольшого повышения частоты бессонницы и головокружения.
Нарушения со стороны органа зрения
На фоне применения дапоксетина отмечались такие нежелательные реакции со стороны органа зрения, как мидриаз и боль в глазах. Дапоксетин следует применять с осторожностью у пациентов с повышенным внутриглазным давлением или с риском развития закрытоугольной глаукомы.
Вспомогательные вещества
Препарат Дапоксетин-СЗ содержит лактозы моногидрат. Пациентам с редко встречающейся наследственной непереносимостью галактозы, дефицитом лактазы или глюкозо-галактозной мальабсорбцией не следует принимать данный препарат.
Влияние на способность к управлению транспортными средствами и механизмами
Дапоксетин оказывает незначительное или умеренное влияние на способность к управлению транспортными средствами и обслуживанию механизмов. При проведении клинических испытаний у лиц, получавших дапоксетин, имели место сообщения о случаях головокружения, нарушения внимания, обморока, нечеткости зрения, сонливости. Следует предупредить пациента о необходимости избегать ситуаций, при которых возможно получение травмы, включая управление транспортными средствами и обслуживание механизмов. Одновременное употребление алкоголя и дапоксетина может усиливать связанные с алкоголем нейрокогнитивные эффекты и может также повышать риск развития нейрокардиогенных нежелательных реакций, таких как обморок, что, в свою очередь, увеличивает травмоопасность. Таким образом, пациентам следует рекомендовать избегать одновременного употребления алкоголя при применении препарата Дапоксетин-СЗ.
Передозировка
Случаев передозировки не описано.
Симптомы: прием дапоксетина в дозе до 240 мг (2 дозы по 120 мг с интервалом в 3 ч) не вызывал непредвиденных нежелательных реакций. В целом, симптомы передозировки СИОЗС включают серотонинергические реакции, в т.ч. сонливость, желудочно-кишечные расстройства (тошнота, рвота), тахикардию, тремор, возбуждение и головокружение.
Лечение: при передозировке следует, в случае необходимости, проводить стандартную поддерживающую терапию. Из-за значительного связывания препарата с белками плазмы крови и большого объема распределения дапоксетина форсированный диурез, диализ, гемоперфузия и переливание крови вряд ли будут эффективны. Специфический антидот неизвестен.
Лекарственное взаимодействие
Фармакодинамическое взаимодействие
Взаимодействие с ингибиторами МАО
У пациентов, получавших одновременно СИОЗС и ингибитор МАО, регистрировались серьезные нежелательные реакции, иногда с летальным исходом, в т.ч. гипертермия, ригидность, миоклонус, расстройства вегетативной нервной системы с возможным быстрым колебанием показателей жизненных функций, а также изменение психического состояния, в т.ч. сильное возбуждение, прогрессирующее до делирия и комы. Эти реакции также наблюдались у пациентов, недавно прекративших прием СИОЗС и начавших лечение ингибиторами МАО. В некоторых случаях симптомы напоминали злокачественный нейролептический синдром. Данные о совместном применении СИОЗС и ингибиторов МАО у животных позволяют предположить, что эти препараты могут синергически повышать АД и вызывать поведенческое возбуждение. Поэтому дапоксетин нельзя принимать одновременно с ингибиторами МАО и в течение 14 дней после прекращения их приема. Аналогично, ингибиторы МАО нельзя принимать в течение 7 дней после прекращения приема дапоксетина.
Взаимодействие с тиоридазином
Тиоридазин удлиняет интервал QTc, что сопровождается желудочковой аритмией. Препараты типа дапоксетина, которые ингибируют изофермент CYP2D6, по всей видимости, ингибируют метаболизм тиоридазина. Ожидается, что вызываемое этим повышение уровня тиоридазина будет усиливать удлинение интервала QTc. Дапоксетин нельзя принимать одновременно с тиоридазином и в течение 14 дней после прекращения его приема. Аналогично, тиоридазин нельзя принимать в течение 7 дней после прекращения приема дапоксетина.
Лекарственные препараты/препараты растительного происхождения с серотонинергическим действием
Как и в случае одновременного применения с другими СИОЗС, применение дапоксетина одновременно с серотонинергическими препаратами (включая ингибиторы МАО, L-триптофан, триптаны, трамадол, линезолид, СИОЗС, ингибиторы захвата серотонина и норэпинефрина, литий и препараты зверобоя продырявленного [Hypericum perforatum]) может повышать частоту серотонинергических нежелательных реакций. Дапоксетин нельзя принимать одновременно с другими СИОЗС, ингибиторами МАО и другими серотонинергическими препаратами и в течение 14 дней после прекращения применения этих препаратов. Аналогично, эти препараты нельзя принимать в течение 7 дней после прекращения применения дапоксетина.
Препараты, действующие на ЦНС
Применение дапоксетина одновременно с препаратами, действующими на ЦНС (например, противоэпилептические препараты, антидепрессанты, нейролептики, анксиолитики, снотворные препараты с седативным действием) у пациентов с преждевременной эякуляцией не изучалось. Поэтому рекомендуется проявлять осторожность при необходимости одновременного применения этих препаратов.
Фармакокинетическое взаимодействие
Влияние совместно принимаемых лекарственных препаратов на фармакокинетику дапоксетина
Исследования с использованием микросом печени, почек и кишечника человека in vitro показали, что дапоксетин метаболизируется преимущественно CYP2D6, CYP3A4 и флавинмонооксигеназой 1 (ФМО1). Следовательно, ингибиторы этих ферментов могут уменьшать клиренс дапоксетина.
Ингибиторы CYP3A4
Сильные ингибиторы CYP3A4. Прием кетоконазола в дозе 200 мг 2 раза/сут в течение 7 дней увеличивал Cmax и AUC0-∞ дапоксетина (60 мг однократно) на 35% и 99% соответственно. С учетом доли несвязанного дапоксетина и дезметилдапоксетина, Cmax активной фракции (сумма несвязанного дапоксетина и дезметилдапоксетина) в присутствии сильных ингибиторов CYP3A4 может увеличиваться примерно на 25%, a AUC может удваиваться. Это увеличение Cmax и AUC активной фракции может быть значительно более выражено в субпопуляции пациентов, не имеющих функционально активного фермента CYP2D6, например, у слабых метаболизаторов CYP2D6, а также при одновременном приеме сильных ингибиторов CYP2D6. Таким образом, применение дапоксетина одновременно с сильными ингибиторами CYP3A4, например, кетоконазолом, итраконазолом, ритонавиром, саквинавиром, телитромицином, нефазодоном, нелфинавиром и атазанавиром противопоказано. Грейпфрутовый сок также является мощным ингибитором CYP3A4, поэтому следует избегать его приема в течение 24 часов, предшествующих приему дапоксетина/
Ингибиторы CYP3A4 средней выраженности действия. Одновременное применение с ингибиторами CYP3A4 средней выраженности действия, например, эритромицином, кларитромицином, флуконазолом, ампренавиром, фосампренавиром, апрепитантом, верапамилом или дилтиаземом, может значительно увеличить степень системного воздействия дапоксетина и дезметилдапоксетина, особенно у пациентов с низкой активностью CYP2D6. Эти две меры относятся ко всем пациентам, кроме тех, которые по результатам гено- или фенотипирования были отнесены к группе активных метаболизаторов CYP2D6. Пациентам, которые относятся к группе активных метаболизаторов CYP2D6, при одновременном применении дапоксетина и сильного ингибитора CYP3A4 рекомендуется максимальная доза 30 мг. Им следует соблюдать осторожность при одновременном применении дапоксетина в дозе 60 мг и ингибитора CYP3A4 средней выраженности действия.
Сильные ингибиторы CYP2D6
Прием флуоксетина в дозе 60 мг/сут в течение 7 дней увеличивал Cmax и AUC0-∞ дапоксетина (60 мг однократно) на 50% и 88% соответственно. С учетом доли несвязанного дапоксетина и дезметилдапоксетина, Cmax активной фракции (сумма несвязанного дапоксетина и дезметилдапоксетина) в присутствии сильных ингибиторов CYP2D6 может увеличиваться примерно на 50%, a AUC может удваиваться. Это увеличение Cmax и AUC активной фракции близко к ожидаемому у пациентов с низкой активностью CYP2D6 и может приводить к повышению частоты и тяжести дозозависимых нежелательных реакций. Поэтому рекомендуется проявлять осторожность при повышении дозы дапоксетина до 60 мг у пациентов, получающих активные ингибиторы CYP2D6, и у пациентов с низкой активностью CYP2D6.
Ингибиторы фосфодиэстеразы 5 (ФДЭ5)
Пациентам, принимающим ингибиторы ФДЭ5, не следует принимать дапоксетин в связи с возможным снижением ортостатической устойчивости/
В перекрестном исследовании однократной дозы была изучена фармакокинетика дапоксетина, принимаемого в дозе 60 мг одновременно с тадалафилом (20 мг) или силденафилом (100 мг). Тадалафил не влиял на фармакокинетику дапоксетина. Силденафил вызвал небольшие изменения фармакокинетики дапоксетина: увеличение AUC0-∞ и Cmax (соответственно на 22% и 4%), что считается клинически незначимым. Дапоксетин следует с осторожностью назначать пациентам, принимающим ингибиторы ФДЭ5, из-за потенциально сниженной переносимости ортостатической гипотензии. Одновременное применение дапоксетина с ингибиторами ФДЭ5 может приводить к ортостатической гипотензии. Эффективность и безопасность дапоксетина у пациентов с преждевременной эякуляцией и эректильной дисфункцией, одновременно принимающих дапоксетин и ингибиторы ФДЭ5, не изучались.
Влияние дапоксетина на одновременно принимаемые лекарственные препараты
Тамсулозин
Однократный и многократный прием дапоксетина в дозах 30 мг и 60 мг у пациентов, ежедневно получающих тамсулозин, не приводил к изменению фармакокинетики последнего. При этом также не изменялась частота ортостатической гипотензии, которая была одинакова при приеме только тамсулозина и в комбинации тамсулозина с дапоксетином 30 мг или 60 мг. Дапоксетин следует с осторожностью назначать пациентам, принимающим альфа-адреноблокаторы, из-за потенциально сниженной у них переносимости ортостатической гипотензии.
Препараты, метаболизируемые CYP2D6
Многократный прием дапоксетина (60 мг/сут в течение 6 дней) увеличивал Cmax и AUC0-∞ дезипрамина (50 мг однократно) на 11% и 19% соответственно, по сравнению с приемом одного дезипрамина. Дапоксетин может аналогично повышать концентрацию в плазме крови и других препаратов, метаболизируемых CYP2D6. Клиническая значимость этого, скорее всего, невелика.
Препараты, метаболизируемые CYP3A4
Многократный прием дапоксетина (60 мг/сут в течение 6 дней) уменьшал AUC0-∞ мидазолама (8 мг однократно) примерно на 20% (диапазон от -60% до +18%). Клиническая значимость этого явления у большинства пациентов, скорее всего, невелика. Однако повышение активности CYP3A может иметь клиническое значение у некоторых пациентов, одновременно принимающих препараты, метаболизируемые в основном CYP3A и имеющие узкий терапевтический индекс.
Препараты, метаболизируемые CYP2C19
Многократный прием дапоксетина (60 мг/сут в течение 6 дней) не приводил к ингибированию метаболизма омепразола (40 мг однократно). Дапоксетин вряд ли влияет на фармакокинетику других субстратов CYP2C19.
Препараты, метаболизируемые CYP2C9
Многократный прием дапоксетина (60 мг/сут в течение 6 дней) не влиял на фармакокинетику и фармакодинамику глибенкламида (5 мг однократно). Дапоксетин предположительно не влияет на фармакокинетику и других субстратов CYP2C9.
Варфарин и лекарственные средства, ингибирующие свертываемость крови и/или тромбоцитарную функцию
Данных об эффектах длительного приема варфарина одновременно с дапоксетином нет. Рекомендуется соблюдать осторожность при назначении дапоксетина пациентам, длительно принимающим варфарин. В исследовании фармакокинетики многократный прием дапоксетина (60 мг/сут в течение 6 дней) не влиял на фармакокинетику и фармакодинамику (ПВ и МНО) варфарина (25 мг однократно). Отмечались случаи патологических кровотечений при одновременном применении с СИОЗС.
Этанол
Однократный прием этанола (0.5 г/кг или примерно 2 дозы) не влиял на фармакокинетику дапоксетина (60 мг однократно) и наоборот. Однако одновременный прием дапоксетина и этанола усиливает сонливость и значительно ослабляет бдительность по собственной оценке пациентов. Фармакодинамические измерения нарушений когнитивной функции (тест на скорость цифрового внимания, тест замены цифровых символов) также выявили наличие аддитивного эффекта при одновременном применении дапоксетина и этанола. Одновременный прием этанола и дапоксетина увеличивает частоту и тяжесть таких нежелательных реакций как головокружение, сонливость, замедление рефлексов, изменение суждений. Комбинация алкоголя и дапоксетина может усиливать связанные с приемом алкоголя нейрокардиогенные нежелательные реакции, в частности, частоту обморока, что повышает риск случайной травмы. Поэтому пациентам следует рекомендовать воздержаться от приема алкоголя в период лечения дапоксетином.
Условия хранения препарата Дапоксетин-СЗ
Препарат следует хранить в недоступном для детей, защищенном от света месте при температуре не выше 25°С.
Срок годности препарата Дапоксетин-СЗ
Срок годности — 3 года. Не применять по истечении срока годности, указанного на упаковке.
Условия реализации
Препарат отпускают по рецепту.
СЕВЕРНАЯ ЗВЕЗДА НАО
(Россия)
|
111524 Москва, |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
03.03.2025
Описание препарата Дапоксетин-СЗ (таблетки, покрытые пленочной оболочкой, 30 мг) основано на официальной инструкции, утверждено компанией-производителем в 2025 году
Дата согласования: 03.03.2025
Особые отметки:
Содержание
- Действующее вещество
- ATX
- Фармакологическая группа
- Нозологическая классификация (МКБ-10)
- Состав
- Описание лекарственной формы
- Фармакологическое действие
- Фармакодинамика
- Фармакокинетика
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью. Влияние на фертильность
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Производитель
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Заказ в аптеках Москвы
Действующее вещество
ATX
Фармакологическая группа
Состав
| Таблетки, покрытые пленочной оболочкой | 1 табл. |
| действующее вещество: | |
| дапоксетин (в виде гидрохлорида) | 30/60 мг |
| вспомогательные вещества, наличие которых надо учитывать в составе лекарственного препарата: лактоза (см. «Особые указания») | |
| вспомогательные вещества (полный перечень) ядро: лактозы моногидрат (сахар молочный); кроскармеллоза натрия (примеллоза); МКЦ 102; кремния диоксид коллоидный (аэросил); магния стеарат |
|
| оболочка пленочная: гипромеллоза; полисорбат 80 (твин 80); тальк; титана диоксид (Е171); краситель железа оксид желтый (Е172) |
Описание лекарственной формы
Таблетки, покрытые пленочной оболочкой: от светло-желтого до желтого цвета, круглые, двояковыпуклые.
На поперечном разрезе ядро таблетки белого или почти белого цвета.
Фармакологическое действие
Фармакодинамика
Механизм действия
Дапоксетин представляет собой сильный СИОЗС с IC50 1,12 нМ, биотрансформирующийся в организме до основных метаболитов — дезметилдапоксетина (IC50 <1,0 нМ) и дидезметилдапоксетина (IC50=2,0 нМ), в равной степени или менее активных (дапоксетин-N-оксид (IC50= 282 нМ).
Эякуляция у человека регулируется в основном симпатической нервной системой. Эякуляцию запускает спинальный рефлекторный центр при участии ствола мозга, на который оказывает первоначальное влияние ряд ядер мозга (медиальные преоптические и паравентрикулярные ядра).
Механизм действия дапоксетина при преждевременной эякуляции (ПЭ) связан с торможением обратного захвата серотонина нейронами с последующим усилением действия нейромедиатора на пре- и постсинаптические рецепторы.
У крыс дапоксетин ингибирует рефлекторный механизм наступления эякуляции с помощью воздействия на латеральное парагигантоклеточное ядро на супраспинальном уровне. Постганглионарные симпатические волокна, иннервирующие семенные пузырьки, семявыносящий проток, предстательную железу, мышцы, охватывающие бульбоуретральные железы и шейку мочевого пузыря, вызывают их координированные сокращения, необходимые для возникновения эякуляции. У крыс дапоксетин изменяет данный рефлекторный механизм наступления эякуляции.
Клиническая безопасность и эффективность
Эффективность дапоксетина при лечении по поводу ПЭ была установлена при проведении пяти двойных слепых клинических исследований с контролем плацебо, в рамках которых был рандомизирован в общей сложности 6081 пациент. Возраст пациентов был от 18 лет и старше, и в течение 6 месяцев до включения данных лиц в исследование у них в большинстве половых актов имела место ПЭ. ПЭ определялась в соответствии с диагностическими критериями DSM-IV (Руководство по диагностике и статистике психических расстройств): короткое время наступления эякуляции (интравагинальное латентное время эякуляции (IELT; время от вагинальной пенетрации до интравагинальной эякуляции) составляет менее чем 2 минуты, что измерялось с использованием секундомера в четырех исследованиях), слабый контроль над эякуляцией, а также обусловленные данным состоянием значительный стресс или сложности в межличностных отношениях.
Лица с другими видами половой дисфункции, включая эректильную дисфункцию (ЭД), а также лица, принимающие другие лекарственные препараты для лечения по поводу ПЭ, были исключены из всех исследований.
Результаты всех рандомизированных исследований являлись сопоставимыми. Эффективность демонстрировалась после 12 недель лечения. В одно исследование были включены пациенты как из стран ЕС, так и из других стран, а продолжительность лечения составляла 24 недели. В данном исследовании были рандомизированы 1162 пациента: 385 принимали плацебо, 388 принимали дапоксетин в дозе 30 мг по мере необходимости и 389 принимали дапоксетин в дозе 60 мг по мере необходимости. Среднее значение и медиана показателя среднего IELT в конце исследования представлены в таблице 1 ниже, а совокупное распределение субъектов, достигших по меньшей мере характерного уровня среднего IELT в конце исследования, представлено в таблице 2 ниже. Другие исследования и объединенный анализ данных на 12-й неделе показали сходные результаты.
Таблица 1
Среднее значение и медиана показателя IELT в конце лечения, вычисленные методом наименьших квадратов*
| Среднее значение IELT | Плацебо | Дапоксетин, 30 мг | Дапоксетин, 60 мг |
| Медианное значение, мин | 1,05 | 1,72 | 1,91 |
| Различие по сравнению с плацебо (95% ДИ) | 0,6 мин** (0,37, 0,72) | 0,9 мин** (0,66, 1,06) | |
| Среднее значение, вычисленное методом наименьших квадратов, мин | 1,7 | 2,9 | 3,3 |
| Различие по сравнению с плацебо (95% ДИ) | 1,2 мин** (0,59, 1,72) | 1,6 мин** (1,02, 2,16) |
*Исходное значение, перенесенное на пациентов с отсутствием исходных данных.
**Различие было статистически значимым (значение р ≤0,001).
Таблица 2
Субъекты, достигшие по меньшей мере характерного уровня среднего IELT в конце исследования*
| IELT, мин | Плацебо, % | Дапоксетин, 30 мг, % | Дапоксетин, 60 мг, % |
| ≥1,0 | 51,6 | 68,8 | 77,6 |
| ≥2,0 | 23,2 | 44,4 | 47,9 |
| ≥3,0 | 14,3 | 26,0 | 37,4 |
| ≥4,0 | 10,4 | 18,4 | 27,6 |
| ≥5,0 | 7,6 | 14,3 | 19,6 |
| ≥6,0 | 5,0 | 11,7 | 14,4 |
| ≥7,0 | 3,9 | 9,1 | 9,8 |
| ≥8,0 | 2,9 | 6,5 | 8,3 |
*Исходное значение, перенесенное на пациентов с отсутствием исходных данных.
Значение удлинения IELT было соотнесено с исходным уровнем IELT и было различным у отдельных пациентов. Клиническая значимость эффекта от приема дапоксетина была также продемонстрирована при помощи анализа исхода лечения, о котором сообщали различные пациенты, у которых проявлялся терапевтический эффект. Пациент с терапевтическим эффектом был определен как субъект, у которого имело место повышение контроля за эякуляцией как минимум на 2 категории, а также снижение уровня стресса в связи с эякуляцией как минимум на 1 категорию. У большего процента субъектов в каждой из групп, принимавших дапоксетин, по сравнению с плацебо, терапевтический эффект развился в конце 12-й или 24-й недели исследования, что являлось статистически достоверным. В группах участников, принимавших дапоксетин в дозах 30 мг (11%; 95% ДИ: 7,24; 14,87) и 60 мг (16,4%; 95% ДИ:13,01; 19,75), на 12-й неделе имел место больший процент пациентов с терапевтическим эффектом по сравнению с группой участников, принимавших плацебо (объединенный анализ).
Клиническое значение эффекта от лечения дапоксетином было показано на примере терапевтической группы для измерения результата. Оценки общего клинического впечатления (CGIC), где пациентов просили сравнить ПЭ у себя с момента начала лечения, с градацией ответов от «гораздо лучше» до «гораздо хуже». В конце исследования (24-я неделя) 28,4% (дапоксетин в дозе 30 мг) и 35,5% (дапоксетин в дозе 60 мг) субъектов, принимавших дапоксетин, сообщили, что их состояние стало «лучше» или «гораздо лучше» по сравнению с 14% в группе участников, принимавших плацебо, а 53,4 и 65,6% субъектов, принимавших дапоксетин в дозе 30 и 60 мг соответственно, сообщили, что их состояние стало как минимум «немного лучше» по сравнению с 28,8% в группе плацебо.
Фармакокинетика
Абсорбция. Дапоксетин быстро всасывается, и Сmах достигается через 1–2 ч после приема препарата. Абсолютная биодоступность равна 42% (диапазон 15–76%) и экспозиция (AUC и Сmах) увеличивается пропорционально дозе в интервале от 30 до 60 мг. После многократного перорального приема AUC дапоксетина и его активного метаболита дезметилдапоксетина увеличивается примерно на 50% по сравнению со значениями AUC после однократного приема.
Прием жирной пищи умеренно уменьшал Сmах дапоксетина (на 10%) и незначительно увеличивал (на 12%) AUC, а также слегка удлинял Tmax в плазме крови. Эти изменения клинически не значимы. Препарат Дапоксетин-СЗ можно принимать независимо от приема пищи.
Распределение. Более 99% дапоксетина связывается с белками плазмы in vitro. Активный метаболит — дезметилдапоксетин — связывается с белками плазмы крови на 98,5%. Дапоксетин распределяется по организму со средним Vss 162 л.
Биотрансформация. Исследования in vitro позволяют предположить, что дапоксетин биотрансформируется многими ферментами печени и почек, особенно CYP2D6, CYP3A4 и флавинсодержащей монооксигеназой (ФМО1) почек. После перорального приема 14С-дапоксетина последний активно биотрансформировался с образованием множества метаболитов, с вовлечением, прежде всего, следующих путей биотрансформации: N-окисление, N-деметилирование, гидроксилирование нафтила, глюкуронирование и сульфатирование. Имеется свидетельство о наличии пресистемного эффекта первого прохождения после приема внутрь. Исследования связывания и переноса in vitro подтверждают, что N-оксид дапоксетина неактивен. Дополнительные метаболиты, включая дезметилдапоксетин и дидезметилдапоксетин, составляли менее 3% от общего количества веществ в плазме, связанных с действующим веществом. Данные исследований связывания, проведенные in vitro, показали, что дезметилдапоксетин и дапоксетин обладают одинаковой эффективностью, а активность дидезметилдапоксетина составляет приблизительно 50% от активности дапоксетина (см. «Фармакодинамика»). Концентрация свободного дезметилдапоксетина (AUC и Сmax) составляет соответственно 50 и 23% от концентрации свободного дапоксетина.
Элиминация. Метаболиты дапоксетина выводятся в основном почками в виде конъюгатов. Дапоксетин в неизмененном виде в моче не обнаруживается. После перорального приема начальный T1/2 дапоксетина составляет приблизительно 1,5 ч, уровень в плазме — менее 5% от пиковой концентрации через 24 ч после приема, а конечный T1/2 составляет около 19 ч. Конечный Т1/2 дезметилдапоксетина составляет примерно 19 ч.
Фармакокинетика у особых категорий пациентов
Метаболит дезметилдапоксетин усиливает фармакологический эффект дапоксетина, особенно если концентрация его повышена. Ниже продемонстрировано повышение параметров активной фракции в некоторых группах пациентов. Она представляет собой сумму концентраций свободного дапоксетина и дезметилдапоксетина. Дезметилдапоксетин и дапоксетин обладают одинаковой эффективностью. Предварительные расчеты позволяют предполагать такое же распределение дезметилдапоксетина в ЦНС, однако неизвестно, так ли это.
Раса. Однократный прием дапоксетина в дозе 60 мг не выявил статистически достоверного различия показателей у представителей европеоидной расы, негроидной расы, латиноамериканцев и представителей монголоидной расы. Клинические исследования, проведенные для сравнения фармакокинетики дапоксетина у японцев и европейцев, выявили, что у японцев имеет место более высокий уровень дапоксетина в плазме (на 10–20%) (AUC и пиковая концентрация) из-за меньшей массы тела. Значимого клинического эффекта, если концентрация немного выше, не ожидается.
Пожилой возраст (≥65 лет). Анализ исследования клинической фармакологии с однократным приемом дапоксетина в дозе 60 мг не выявил существенного различия показателей фармакокинетики (Сmax, AUC0–∞, Тmax) у здоровых пожилых мужчин и здоровых мужчин более молодого возраста (см. «Способ применения и дозы»).
Почечная недостаточность. Клиническое фармакологическое исследование однократного применения дапоксетина в дозе 60 мг было проведено у пациентов с нарушением функции почек легкой (Cl креатинина от 50 до 80 мл/мин), средней (Cl креатинина от 30 до <50 мл/мин) и тяжелой (Cl креатинина <30 мл/мин) степени, а также у субъектов с нормальной функцией почек (Cl креатинина >80 мл/мин). Явной тенденции к повышению AUC дапоксетина при нарушении функции почек не выявлено. У субъектов с нарушением функции почек тяжелой степени AUC было приблизительно в 2 раза выше, чем у субъектов с нормальной функцией почек, хотя у пациентов с нарушением функции почек тяжелой степени данные ограничены. У пациентов, находящихся на почечном диализе, оценка фармакокинетики дапоксетина не проводилась (см. «Способ применения и дозы» и «Противопоказания»).
Печеночная недостаточность. У пациентов с печеночной недостаточностью легкой степени тяжести Сmax несвязанного дапоксетина снижалась на 28%, AUC не изменялась. Сmax и AUC активной фракции (сумма несвязанных фракций дапоксетина и дезметилдапоксетина) снижались на 30 и 5% соответственно. У пациентов с печеночной недостаточностью средней степени тяжести Сmax несвязанного дапоксетина обычно не изменяется (снижается в пределах 3%), AUC увеличивается на 66%. Сmax несвязанной активной фракции дапоксетина была неизменна, a AUC — увеличена в 2 раза. У пациентов с печеночной недостаточностью тяжелой степени Сmax несвязанного дапоксетина была снижена на 42%, a AUC несвязанного дапоксетина была увеличена примерно на 223%. Сmax и AUC активной фракции изменялись подобным образом (см. «Способ применения и дозы» и «Противопоказания»).
Полиморфизм CYP2D6. В клиническом фармакологическом исследовании однократного применения концентрация дапоксетина в дозе 60 мг, концентрация в плазме крови была выше у слабых метаболизаторов CYP2D6, чем у активных метаболизаторов CYP2D6 (приблизительно Сmax — на 31%, AUC0–∞ дапоксетина — на 36%, Сmax — на 98%, AUC0–∞ дезметилдапоксетина — на 161%). Значение Сmax активной фракции препарата Дапоксетин-СЗ может быть повышено приблизительно на 46%, a AUC — приблизительно на 90%. Данное повышение может увеличить частоту и усугубить тяжесть нежелательных реакций, зависящих от дозы (см. «Способ применения и дозы»). При приеме препарата Дапоксетин-СЗ у пациентов с низкой активностью CYP2D6 особое внимание следует обратить на безопасность при совместном приеме других лекарственных препаратов, которые могут ингибировать биотрансформацию дапоксетина, таких как ингибиторы CYP3A4 средней выраженности действия и сильные ингибиторы CYP3A4 (см. «Способ применения и дозы» и «Противопоказания»).
Показания
Препарат Дапоксетин-СЗ предназначен для лечения преждевременной эякуляции у мужчин от 18 до 64 лет.
Препарат Дапоксетин-СЗ можно применять только у пациентов, соответствующих следующим критериям:
— интравагинальное время задержки эякуляции (ИВВЗЭ) <2 мин;
— постоянно или регулярно возникающая эякуляция после минимальной сексуальной стимуляции перед, во время или вскоре после полового проникновения и наступающая раньше желаемого пациентом момента;
— выраженный личностный дистресс или затруднения в межличностных отношениях вследствие преждевременной эякуляции;
— слабый контроль эякуляции;
— наступление преждевременной эякуляции в большинстве попыток осуществления полового акта за последние 6 мес.
Препарат Дапоксетин-СЗ следует применять только в режиме приема по потребности перед предполагаемой сексуальной активностью. Препарат Дапоксетин-СЗ не должен применяться для задержки эякуляции у мужчин, не имеющих подтвержденного диагноза «преждевременная эякуляция».
Противопоказания
- гиперчувствительность к дапоксетину и/или к любому вспомогательному веществу в составе препарата (см. «Состав»);
- выраженная патология со стороны сердца (такая как сердечная недостаточность (II–IV класс по NYHA), нарушения проводимости, такие как атриовентрикулярная блокада (AV-блокада) или синдром слабости синусного узла, выраженная ишемическая болезнь сердца (ИБС), выраженный клапанный порок;
- наличие обмороков в анамнезе;
- наличие мании или тяжелой депрессии в анамнезе;
- одновременный прием ингибиторов моноаминоксидазы (МАО), или если после прекращения их приема прошло менее 14 дней. Подобным образом, ингибиторы МАО не следует принимать в течение 7 дней после окончания приема препарата Дапоксетин-СЗ (см. «Взаимодействие»);
- одновременный прием тиоридазина, или период в течение 14 дней после окончания приема тиоридазина. Соответственно, тиоридазин не следует принимать в течение 7 дней после окончания приема препарата Дапоксетин-СЗ (см. «Взаимодействие»);
- одновременный прием ингибиторов обратного захвата серотонина селективных ингибиторов обратного захвата серотонина (СИОЗС), селективных ингибиторов обратного захвата серотонина и норадреналина (СИОЗСН), трициклических антидепрессантов (ТЦА) или других лекарственных препаратов, в т.ч. препаратов растительного происхождения с серотонинергическим действием (например, L-триптофан, триптаны, трамадол, линезолид, литий, зверобой продырявленный (Нypericum perforatum), или в течение 14 дней после отмены данных лекарственных препаратов, в т.ч. препаратов растительного происхождения. Соответственно, данные лекарственные препараты/препараты растительного происхождения не следует принимать в течение 7 дней после окончания приема препарата Дапоксетин-СЗ (см. «Взаимодействие»);
- одновременный прием сильнодействующих ингибиторов CYP3A4, таких как кетоконазол, итраконазол, ритонавир, саквинавир, телитромицин, нефазодон, атазанавир (см. «Взаимодействие»);
- умеренно выраженные и тяжелые нарушения функции печени;
- тяжелые нарушения функции почек;
- возраст до 18 лет.
С осторожностью: пациенты с почечной недостаточностью легкой или средней степени тяжести; одновременное применение с сильными ингибиторами изофермента CYP2D6 и ингибиторами CYP3A4 средней выраженности действия у пациентов с генотипически низкой активностью изофермента CYP2D6 и пациентов с высокой активностью изофермента CYP2D6 в комбинации с ингибиторами изофермента CYP3A4 средней выраженности действия; одновременное применение с препаратами, которые влияют на агрегацию тромбоцитов, и с антикоагулянтами из-за риска развития кровотечений, а также пациенты, имеющие в анамнезе кровотечения или нарушения свертывания.
Применение при беременности и кормлении грудью. Влияние на фертильность
Препарат Дапоксетин-СЗ не предназначен для применения у женщин. Исследования на животных не выявили прямого или косвенного негативного влияния в отношении фертильности, беременности или развития эмбриона/плода.
Способ применения и дозы
Внутрь. Таблетку следует проглатывать целиком, запивая по крайней мере одним полным стаканом воды. Препарат Дапоксетин-СЗ можно принимать независимо от приема пищи.
Мужчины от 18 до 64 лет. Рекомендуемая начальная доза для всех мужчин составляет 30 мг, эту дозу принимают за 1–3 ч до предполагаемого полового акта. Лечение препаратом не следует начинать с дозы 60 мг.
Препарат Дапоксетин-СЗ не предназначен для постоянного ежедневного применения. Его следует принимать только в случае предполагаемого полового акта. Препарат Дапоксетин-СЗ не следует принимать чаще чем каждые 24 ч.
При недостаточном эффекте и хорошей переносимости дозы 30 мг (пациент не отмечает умеренных или тяжелых нежелательных реакций или явлений, которые могут предшествовать синкопальному состоянию), дозу можно увеличить до максимально рекомендуемой — 60 мг, с приемом по потребности за 1–3 ч до сексуальной активности. Частота и тяжесть нежелательных реакций выше при приеме препарата в дозе 60 мг.
Если у пациента отмечались ортостатические реакции при приеме начальной дозы, не следует повышать дозу до 60 мг (см. «Особые указания»). После первых 4 нед терапии (или после приема по меньшей мере 6 доз препарата) врач должен провести тщательную оценку соотношения пользы и риска препарата Дапоксетин-СЗ в каждом конкретном случае для решения вопроса о целесообразности продолжения лечения данным препаратом.
Данные об эффективности и безопасности применения дапоксетина в течение более 24 нед ограничены. Клиническую необходимость продолжения терапии и соотношения польза/риск от применения препарата Дапоксетин-СЗ следует оценивать как минимум каждые 6 мес.
Особые группы пациентов
Пожилой возраст (65 лет и старше). Эффективность и безопасность дапоксетина у пациентов ≥65 лет и старше не установлены (см. «Фармакокинетика»).
Нарушение функции почек. При приеме препарата пациентами с нарушениями функции почек легкой и средней степени тяжести следует соблюдать осторожность. Препарат Дапоксетин-СЗ противопоказан пациентам с почечной недостаточностью тяжелой степени (см. «Противопоказания»).
Нарушение функции печени. Препарат Дапоксетин-СЗ противопоказан пациентам с умеренно выраженными и тяжелыми нарушениями функции печени (классы В и С по классификации Чайлд-Пью) (см. «Противопоказания»).
Пациенты с низкой активностью изофермента CYP2D6 и пациенты, одновременно принимающие сильные ингибиторы CYP2D6. Следует проявлять осторожность при увеличении дозы препарата Дапоксетин-СЗ до 60 мг у пациентов с низкой активностью изофермента CYP2D6 или принимающих препарат Дапоксетин-СЗ одновременно с сильными ингибиторами изофермента CYP2D6. Рекомендуется соблюдать осторожность при повышении дозы до 60 мг у пациентов, у которых диагностирован низкий метаболизм CYP2D6, и у пациентов, одновременно принимающих сильные ингибиторы CYP2D6 (см. «Особые указания», «Взаимодействие», «Фармакокинетика»).
Пациенты, получающие сильные или умеренно активные ингибиторы изофермента CYP3A4. Одновременное применение препарата Дапоксетин-СЗ с сильными ингибиторами изофермента CYP3A4 противопоказано. Пациентам, одновременно принимающим ингибиторы CYP3A4 средней выраженности действия, необходимо соблюдать осторожность и не превышать дозу равную 30 мг (см. «Противопоказания»., «Особые указания» и «Взаимодействие»).
Дети. Препарат Дапоксетин-СЗ противопоказан у детей и подростков в возрасте до 18 лет (см. «Противопоказания»).
Побочные действия
Реклама: ООО «РЛС-Патент», ИНН 5044031277
Резюме профиля безопасности
В клинических исследованиях были зарегистрированы синкопе и ортостатическая гипотензия (см. «Особые указания»). В клинических исследованиях III фазы зарегистрированы следующие нежелательные реакции дапоксетина, которые были дозозависимыми: тошнота (11,0 и 22,2% при приеме 30 и 60 мг дапоксетина соответственно), головокружение (5,8 и 10,9%), головная боль (5,6 и 8,8%), диарея (3,5 и 6,9%), бессонница (2,1 и 3,9%), усталость (2,0 и 4,1%). Самыми частыми реакциями, требовавшими отмены лечения, были тошнота (у 2,2% пациентов) и головокружение (1,2% пациентов).
Табличное резюме нежелательных реакций
Безопасность дапоксетина оценивалась у 4224 пациентов с ПЭ, принимавших участие в 5 двойных слепых плацебо-контролируемых клинических исследованиях. Из 4224 пациентов 1616 пациентов принимали дапоксетин в дозе 30 мг по мере необходимости, а 2608 — в дозе 60 мг либо по мере необходимости, либо 1 раз в сутки.
Нежелательные реакции, наблюдавшиеся в ходе клинических исследований дапоксетина, распределены по системно-органным классам с указанием частоты их возникновения: очень часто (≥1/10); часто (≥1/100, <1/10); нечасто (≥1/1000, <1/100); редко (≥1/10000, <1/1000); очень редко (<1/10000); частота неизвестна (на основании имеющихся данных оценить невозможно).
Таблица 3
Нежелательные реакции дапоксетина
| Системно-органный класс | Частота | Нежелательные реакции |
| Нарушения психики | Часто | Чувство тревоги, возбуждение, беспокойство, необычные сновидения, снижение либидо |
| Нечасто | Депрессия, депрессивное настроение, состояние эйфории, перемены настроения, нервозность, безразличие, апатия, спутанность сознания, дезориентация, патологическое мышление, соматосенсорная амплификация, нарушения сна, инициальная инсомния, интрасомническое расстройство, ночные кошмары, бруксизм, потеря либидо, аноргазмия | |
| Со стороны нервной системы | Очень часто | Головокружение, головная боль |
| Часто | Сонливость, нарушение концентрации внимания, тремор, парестезия | |
| Нечасто | Обморок, в т.ч. вазовагальный, постуральное головокружение, акатизия, расстройство вкусового восприятия, гиперсомния, сонливость, седативный эффект, угнетение сознания | |
| Редко | Головокружение при физической нагрузке, внезапное засыпание | |
| Со стороны органа зрения | Часто | Нечеткость зрения |
| Нечасто | Мидриаз, боль в глазах, нарушение зрения | |
| Со стороны органа слуха и лабиринта | Часто | Звон в ушах |
| Нечасто | Вертиго | |
| Со стороны сердца | Нечасто | Прекращение активности синусного узла, синусовая брадикардия, тахикардия |
| Со стороны сосудов | Часто | Приливы крови |
| Нечасто | Снижение АД, систолическая гипертензия, приливы жара | |
| Со стороны дыхательной системы, органов грудной клетки и средостения | Часто | Заложенность носа, зевота |
| Со стороны ЖКТ | Очень часто | Тошнота |
| Часто | Диарея, рвота, запор, боли в области живота, боли в верхней части живота, диспепсия, метеоризм, дискомфорт в области желудка, вздутие живота, сухость во рту | |
| Нечасто | Дискомфорт в животе, дискомфорт в эпигастральной области | |
| Редко | Неотложные позывы к дефекации | |
| Со стороны кожи и подкожных тканей | Часто | Гипергидроз |
| Нечасто | Зуд, холодный пот | |
| Со стороны половых органов | Часто | Эректильная дисфункция |
| Нечасто | Отсутствие эякуляции, нарушение оргазма у мужчин, мужская генитальная парестезия | |
| Общие расстройства | Часто | Слабость, раздражительность |
| Нечасто | Астения, чувство жара, ощущение тревоги, ощущение недомогания, чувство опьянения |
Описание отдельных нежелательных реакций
Обмороки с потерей сознания, с брадикардией или остановкой синусного узла наблюдались у пациентов при холтеровском мониторировании и были зарегистрированы в клинических исследованиях. Данные нежелательные реакции расценены как связанные с применением дапоксетина. Большинство случаев наблюдались в течение первых 3 ч после приема дапоксетина, после приема первой дозы или ассоциировались с медицинскими процедурами (забор крови, изменения положения тела, измерение АД). Продромальные симптомы часто предшествовали обмороку (см. «Особые указания»).
Возникновение обморока, и возможно, продромальных симптомов зависит, по всей видимости, от дозы, что было продемонстрировано более высокой частотой их возникновения среди пациентов, принимавших дапоксетин в клинических исследованиях фазы 3 в дозах, превышающих рекомендуемые.
При проведении клинических исследований имели место сообщения о возникновении ортостатической гипотензии (см. «Особые указания»). Частота возникновения синкопе, характеризующегося потерей сознания, в программе клинической разработки дапоксетина варьировалась в зависимости от исследуемой популяции и находилась в диапазоне от 0,06% (30 мг) до 0,23% (60 мг) у лиц, включенных в III фазу клинических плацебо-контролируемых исследований, и до 0,64% (все дозы вместе) для I фазы исследования с участием здоровых добровольцев без наличия ПЭ.
Другие особые группы пациентов. Следует соблюдать осторожность при повышении дозы до 60 мг у пациентов, принимающих сильнодействующие ингибиторы CYP2D6, или при повышении дозы до 60 мг у пациентов, имеющих генотип слабых метаболизаторов CYP2D6 (см. «Особые указания», «Взаимодействие» и «Фармакокинетика»).
Эффекты при отмене препарата
При внезапной отмене СИОЗС, длительно применяемых для лечения хронических депрессивных расстройств, отмечались следующие симптомы: дисфорическое состояние, раздражительность, возбуждение, головокружение, сенсорные нарушения (например, парестезия в виде ощущения удара электротоком), тревожность, спутанность сознания, головная боль, летаргия, эмоциональная лабильность, бессонница и гипомания.
Результаты исследования безопасности показали более высокую частоту симптомов отмены в виде бессонницы и головокружения легкой и умеренной степени после отмены препарата через 62 дня применения.
Сообщение о подозреваемых нежелательных реакциях
Важно сообщать о подозреваемых нежелательных реакциях после регистрации лекарственного препарата с целью обеспечения непрерывного мониторинга соотношения польза/риск лекарственного препарата. Медицинским работникам рекомендуется сообщать о любых подозреваемых нежелательных реакциях лекарственного препарата через национальную систему сообщения о нежелательных реакциях государств — членов Евразийского экономического союза.
Российская Федерация. Федеральная служба по надзору в сфере здравоохранения. 109012, Москва, Славянская пл., 4, стр. 1.
Тел.: +7 800 550-99-03.
e-mail: pharm@roszdravnadzor.gov.ru
www.roszdravnadzor.gov.ru
Взаимодействие
Фармакодинамическое взаимодействие (ФДВ)
Ингибиторы МАО
У пациентов, получавших одновременно СИОЗС и ингибитор МАО, регистрировались серьезные нежелательные реакции, иногда с летальным исходом, в т.ч. гипертермия, ригидность, миоклонус, расстройства вегетативной нервной системы с возможным возникновением быстрых изменений показателей жизненно важных функций организма, а также изменение психического состояния, в т.ч. сильное возбуждение, прогрессирующее до делирия и комы. Эти реакции также наблюдались у пациентов, недавно прекративших прием СИОЗС и начавших лечение ингибиторами МАО. В некоторых случаях симптомы напоминали злокачественный нейролептический синдром. Данные о совместном применении СИОЗС и ингибиторов МАО у животных позволяют предположить, что эти препараты могут синергически повышать АД и вызывать поведенческое возбуждение. Поэтому дапоксетин нельзя принимать одновременно с ингибиторами МАО и в течение 14 дней после прекращения их приема. Аналогично ингибиторы МАО нельзя принимать в течение 7 дней после прекращения приема дапоксетина (см. «Противопоказания»).
Тиоридазин
Тиоридазин удлиняет интервал QTc, что сопровождается желудочковой аритмией. Препараты типа дапоксетина, которые ингибируют изофермент CYP2D6, по всей видимости, ингибируют метаболизм тиоридазина. Ожидается, что вызываемое этим повышение уровня тиоридазина будет усиливать удлинение интервала QTc. Дапоксетин нельзя принимать одновременно с тиоридазином и в течение 14 дней после прекращения его приема. Аналогично тиоридазин нельзя принимать в течение 7 дней после прекращения приема дапоксетина (см. «Противопоказания»).
Лекарственные препараты/препараты растительного происхождения с серотонинергическим действием
Как и в случае одновременного применения с другими СИОЗС, совместное применение с лекарственными препаратами, в т.ч. препаратами растительного происхождения с серотонинергическим действием (включая ингибиторы МАО, L-триптофан, триптаны, трамадол, линезолид, СИОЗС, СИОЗСН, литий и препараты зверобоя продырявленного (Hypericum perforatum) может повышать частоту серотонинергических нежелательных реакций. Дапоксетин нельзя принимать одновременно с другими СИОЗС, ингибиторами МАО и другими серотонинергическими препаратами и в течение 14 дней после прекращения применения этих препаратов. Аналогично эти препараты/препараты растительного происхождения нельзя принимать в течение 7 дней после прекращения применения дапоксетина (см. «Противопоказания»).
Препараты, действующие на ЦНС
Применение дапоксетина одновременно с препаратами, действующими на ЦНС (например, противоэпилептические препараты, антидепрессанты, нейролептики, анксиолитики, снотворные препараты с седативным действием), у пациентов с ПЭ не изучалось. Поэтому рекомендуется проявлять осторожность при необходимости одновременного применения этих препаратов.
Фармакокинетическое взаимодействие (ФКВ)
Влияние совместно принимаемых лекарственных препаратов на фармакокинетику дапоксетина
Исследования с использованием микросом печени, почек и кишечника человека in vitro показали, что дапоксетин биотрансформируется преимущественно с участием CYP2D6, CYP3A4 и ФМО1. Поэтому ингибиторы этих ферментов могут уменьшать клиренс дапоксетина.
Ингибиторы CYP3A4
Сильные ингибиторы CYP3A4. Прием кетоконазола в дозе 200 мг 2 раза в день в течение 7 дней увеличивал Сmах и AUC0–∞ дапоксетина (60 мг однократно) на 35 и 99% соответственно. С учетом доли несвязанного дапоксетина и дезметилдапоксетина, Сmах активной фракции в присутствии сильных ингибиторов CYP3A4 может увеличиваться примерно на 25%, a AUC может удваиваться. Это увеличение Сmах и AUC активной фракции может быть значительно более выражено в субпопуляции пациентов, не имеющих функционально активного фермента CYP2D6, например у слабых метаболизаторов CYP2D6, а также при одновременном приеме сильных ингибиторов CYP2D6.
Таким образом, применение дапоксетина одновременно с сильными ингибиторами CYP3A4, например кетоконазолом, итраконазолом, ритонавиром, саквинавиром, телитромицином, нефазодоном, нелфинавиром и атазанавиром, противопоказано. Грейпфрутовый сок также является сильным ингибитором CYP3A4, поэтому следует избегать его приема в течение 24 ч, предшествующих приему дапоксетина (см. «Противопоказания»).
Ингибиторы CYP3A4 средней выраженности действия. Одновременное применение с ингибиторами CYP3A4 средней выраженности действия, например эритромицином, кларитромицином, флуконазолом, ампренавиром, фосампренавиром, апрепитантом, верапамилом или дилтиаземом, может значительно увеличить степень системного воздействия дапоксетина и дезметилдапоксетина, особенно у пациентов с низкой активностью CYP2D6. Это относится ко всем пациентам, кроме тех, которые по результатам гено- или фенотипирования были отнесены к группе активных метаболизаторов CYP2D6. Пациентам, которые относятся к группе активных метаболизаторов CYP2D6, при одновременном применении дапоксетина и сильного ингибитора CYP3A4 рекомендуется максимальная доза 30 мг. Им следует соблюдать осторожность при одновременном применении дапоксетина в дозе 60 мг и ингибитора CYP3A4 средней выраженности действия.
Сильные ингибиторы CYP2D6
Прием флуоксетина в дозе 60 мг/сут в течение 7 дней увеличивал Сmах и AUC0–∞ дапоксетина (60 мг однократно) на 50 и 88% соответственно. С учетом доли несвязанного дапоксетина и дезметилдапоксетина, Сmах активной фракции в присутствии сильных ингибиторов CYP2D6 может увеличиваться примерно на 50%, a AUC может удваиваться. Это увеличение Сmах и AUC активной фракции близко к ожидаемому у пациентов с низкой активностью CYP2D6 и может приводить к повышению частоты и тяжести дозозависимых нежелательных реакций (см. «Особые указания»).
Ингибиторы ФДЭ-5
Пациентам, принимающим ингибиторы ФДЭ-5, не следует принимать дапоксетин в связи с возможным снижением ортостатической устойчивости (см. «Особые указания»).
В перекрестном исследовании однократной дозы была изучена фармакокинетика дапоксетина, принимаемого в дозе 60 мг одновременно с тадалафилом (20 мг) или силденафилом (100 мг). Тадалафил не влиял на фармакокинетику дапоксетина. Силденафил вызвал небольшие изменения фармакокинетики дапоксетина: увеличение AUC0–∞ и Сmах (соответственно на 22 и 4%), что считается клинически незначимым. Одновременное применение дапоксетина с ингибиторами ФДЭ-5 может приводить к ортостатической гипотензии (см. «Особые указания»). Эффективность и безопасность дапоксетина у пациентов с ПЭ и ЭД, одновременно принимающих дапоксетин и ингибиторы ФДЭ-5, не изучались.
Влияние дапоксетина на одновременно принимаемые ЛС
Тамсулозин
Однократный и многократный прием дапоксетина в дозах 30 и 60 мг пациентами, ежедневно получающими тамсулозин, не приводил к изменению фармакокинетики последнего. При этом также не изменялась частота ортостатической гипотонии, которая была одинакова при приеме только тамсулозина и в комбинации тамсулозина с дапоксетином 30 или 60 мг. Дапоксетин следует с осторожностью назначать пациентам, принимающим альфа-адреноблокаторы из-за потенциально сниженной у них переносимости ортостатической гипотонии (см. «Особые указания»).
Препараты, биотрансформируемые CYP2D6
Многократный прием дапоксетина (60 мг/сут в течение 6 дней) увеличивал Сmах и AUC0–∞ дезипрамина (50 мг однократно) на 11 и 19% соответственно по сравнению с приемом одного дезипрамина. Дапоксетин может аналогично повышать концентрацию в плазме крови и других препаратов, метаболизируемых CYP2D6. Клиническая значимость этого, скорее всего, невелика.
Препараты, биотрансформируемые CYP3A
Многократный прием дапоксетина (60 мг/сут в течение 6 дней) уменьшал AUC0–∞ мидазолама (8 мг однократно) примерно на 20% (диапазон от −60 до +18 %). Клиническая значимость этого явления у большинства пациентов, скорее всего, невелика. Однако повышение активности CYP3A может иметь клиническое значение у некоторых пациентов, одновременно принимающих препараты, метаболизируемые в основном CYP3A и имеющие узкий терапевтический индекс.
Препараты, биотрансформируемые CYP2C19
Многократный прием дапоксетина (60 мг/сут в течение 6 дней) не приводил к ингибированию метаболизма омепразола (40 мг однократно). Дапоксетин вряд ли влияет на фармакокинетику других субстратов CYP2C19.
Препараты, биотрансформируемые CYP2C9
Многократный прием дапоксетина (60 мг/сут в течение 6 дней) не влиял на фармакокинетику и фармакодинамику глибенкламида (5 мг однократно). Дапоксетин, предположительно, не влияет на фармакокинетику и других субстратов CYP2C9.
Варфарин и ЛС, ингибирующие свертываемость крови и/или тромбоцитарную функцию
Сведений в отношении взаимодействия при регулярном длительном одновременном применении варфарина и дапоксетина нет. Рекомендуется соблюдать осторожность при назначении дапоксетина пациентам, длительно принимающим варфарин (см. «Особые указания»). В исследовании фармакокинетики многократный прием дапоксетина (60 мг/сут в течение 6 дней) не влиял на фармакокинетику и фармакодинамику (ПВ и МНО) варфарина (25 мг однократно). Отмечались случаи патологических кровотечений при одновременном применении с СИОЗС (см. «Особые указания»).
Этанол
Однократный прием этанола (0,5 г/кг или примерно 2 дозы) не влиял на фармакокинетику дапоксетина (60 мг однократно) и наоборот. Однако одновременный прием дапоксетина и этанола усиливает сонливость и значительно ослабляет бдительность, по собственной оценке пациентов. Фармакодинамические измерения нарушений когнитивной функции (тест на скорость цифрового внимания, тест замены цифровых символов) также выявили наличие аддитивного эффекта при одновременном применении дапоксетина и этанола. Одновременный прием этанола и дапоксетина увеличивает частоту и тяжесть таких нежелательных реакций, как головокружение, сонливость, замедление рефлексов, изменение суждений. Это также может усиливать нейрокардиогенные нежелательные реакции, в частности частоту обморока, что повышает риск случайной травмы. Поэтому пациентам следует рекомендовать воздержаться от приема алкоголя в период лечения дапоксетином.
Передозировка
Случаев передозировки не описано. Прием дапоксетина в дозе до 240 мг (2 дозы по 120 мг с интервалом в 3 ч) не вызывал непредвиденных нежелательных реакций.
Симптомы: в целом симптомы передозировки СИОЗС включают серотонинергические реакции, в т.ч. сонливость, желудочно-кишечные расстройства (тошнота, рвота), тахикардия, тремор, возбуждение и головокружение.
Лечение: при передозировке следует в случае необходимости проводить стандартную поддерживающую терапию. Из-за значительного связывания препарата с белками плазмы крови и большого Vd дапоксетина форсированный диурез, диализ, гемоперфузия и переливание крови вряд ли будут эффективны. Специфический антидот неизвестен.
Особые указания
Общие рекомендации
Дапоксетин можно применять только у пациентов с ПЭ, соответствующих критериям, указанным в разделе «Показания». Дапоксетин нельзя применять мужчинам, которым не был поставлен диагноз ПЭ. Безопасность применения препарата у мужчин без ПЭ не установлена, данных о задержке эякуляции нет.
Другие виды сексуальной дисфункции
До начала лечения пациенты с другими видами сексуальных расстройств, включая ЭД, должны быть тщательно обследованы врачом. Дапоксетин не следует применять пациентам с ЭД, получающим ингибиторы ФДЭ-5 (см. «Взаимодействие»).
Ортостатическая гипотония
Перед началом терапии врач должен провести тщательное медицинское обследование, включая выяснение анамнеза ортостатических событий, а также ортостатическую пробу (измерение АД и ЧСС в положении сидя и стоя). В случае подтвержденных или предполагаемых ортостатических реакций в анамнезе следует избегать терапии дапоксетином.
В клинических исследованиях описаны случаи ортостатической гипотонии. Врач должен заранее проинформировать пациента о том, что при появлении возможных продромальных симптомов, например головокружения сразу после вставания, следует немедленно лечь так, чтобы голова оказалась ниже туловища, или сесть, опустив голову между колен, и оставаться в этой позе до исчезновения симптомов. Кроме того, нужно проинформировать пациента о необходимости избегать резкого вставания после длительного лежания или сидения.
Самоубийство/суицидальные мысли
В краткосрочных исследованиях антидепрессанты, включая СИОЗС, по сравнению с плацебо сильнее повышали риск возникновения суицидальных мыслей и суицидальность у детей и подростков с большим депрессивным расстройством и другими психическими расстройствами. При проведении краткосрочных исследований повышение риска суицидальности при приеме антидепрессантов по сравнению с плацебо у взрослых старше 24 лет выявлено не было. В клинических исследованиях дапоксетина для лечения ПЭ четких данных о появлении суицидальных мыслей на фоне лечения, оцененных по Колумбийскому алгоритму классификации для оценки суицида (C-CASA), шкале оценки депрессии Монтгомери-Асберга или опроснику депрессии Бека, выявлено не было.
Обморок
Пациентам следует избегать потенциально травмоопасных ситуаций, в частности управления транспортными средствами или механизмами, в случае возникновения обморока или его продромальных симптомов, таких как головокружение или предобморочное состояние (см. «Побочные действия»). У пациентов, получавших дапоксетин, по сравнению с пациентами, получавшими плацебо, чаще отмечались продромальные симптомы, в т.ч. тошнота, головокружение/предобморочное состояние и повышенное потоотделение.
Наблюдавшиеся в клинических исследованиях случаи обморока, охарактеризованные как потеря сознания, с брадикардией или остановкой синусного узла у пациентов при холтеровском мониторировании, были отнесены на счет вазовагального происхождения, и большинство их имели место в течение первых 3 ч после приема, после первой дозы, или же были ассоциированы с медицинскими процедурами (забор крови, изменения положения тела, измерение АД). Возможные продромальные симптомы, например тошнота, головокружение, предобморочное состояние, сердцебиение, астения, спутанность сознания и повышенное потоотделение, обычно также наблюдались в первые 3 ч после приема препарата и часто предшествовали обмороку. Пациенты должны быть проинформированы о том, что в период лечения дапоксетином в любое время возможно развитие обморока с продромальными симптомами или без них. Врач должен проинформировать пациента о важности достаточной водной нагрузки и о распознавании продромальных признаков и симптомов для снижения риска серьезной травмы при возможном падении из-за потери сознания. При появлении возможных продромальных симптомов пациент сразу должен лечь так, чтобы голова оказалась ниже туловища, или сесть, опустив голову между колен, и оставаться в этой позе до исчезновения симптомов. При обмороке или других нежелательных реакциях со стороны ЦНС пациента следует предупредить о необходимости избегать потенциально травмоопасных ситуаций, включая управление автомобилем и другими механизмами (см. «Взаимодействие»).
Пациенты с риском сердечно-сосудистых заболеваний
В клинических исследованиях дапоксетина не участвовали пациенты с сердечно-сосудистыми заболеваниями. У пациентов с органическими заболеваниями сердца и сосудов (например, обструкция при выбросе крови из сердца, поражение клапанного аппарата, стеноз сонной артерии, атеросклероз коронарной артерии) повышен риск нежелательных сердечно-сосудистых последствий обмороков сердечного и другого происхождения. Однако в настоящее время недостаточно данных для определения, распространяется ли этот риск на вазовагальный обморок у пациентов с сердечно-сосудистыми заболеваниями.
Прием вместе с наркотическими средствами
Пациентам не следует принимать дапоксетин вместе с наркотическими средствами. Одновременный прием дапоксетина с наркотическими средствами, обладающими серотонинергической активностью, например кетамином, метилендиоксиметамфетамином (МДМА) и диэтиламидом лизергиновой кислоты (ЛСД), может приводить к потенциально серьезным реакциям, включая, но не ограничиваясь, аритмию, гипертермию и серотониновый синдром. Применение дапоксетина одновременно с седативными средствами, например опиатами или бензодиазепинами, может усиливать сонливость и головокружение.
Применение с этанолом
Совместное применение дапоксетина с алкоголем может усиливать его действие на ЦНС, а также усилить такие нейрокардиогенные нежелательные реакции, как обморок, повышая таким образом риск случайной травмы. Поэтому пациентам следует рекомендовать воздержаться от приема алкоголя в период приема дапоксетина (см. «Взаимодействие»).
ЛС с вазодилатирующими свойствами
Дапоксетин следует применять с осторожностью пациентам, принимающим лекарственные препараты с вазодилатирующими свойствами (такие как альфа-адреноблокаторы и нитраты) в связи с возможным снижением ортостатической толерантности.
Ингибиторы CYP3A4 средней выраженности действия
Следует соблюдать осторожность при применении дапоксетина одновременно с ингибиторами CYP3A4 средней выраженности действия (эритромицин, кларитромицин, флуконазол, ампренавир, фосампренавир, апрепитант, верапамил, дилтиазем), а дозу препарата следует снизить до 30 мг (см. «Способ применения и дозы», «Взаимодействие»).
Сильные ингибиторы CYP2D6
Рекомендуется проявлять осторожность при повышении дозы дапоксетина до 60 мг у пациентов, получающих сильные ингибиторы CYP2D6, и у пациентов с низкой активностью CYP2D6, т.к. при этом может повышаться уровень системного воздействия препарата с соответствующим увеличением частоты и тяжести дозозависимых нежелательных реакций (см. «Способ применения и дозы», «Взаимодействие», «Фармакокинетика»).
Мания
Дапоксетин нельзя принимать пациентам, имеющим в анамнезе манию/гипоманию или биполярное расстройство, при появлении симптомов этих заболеваний прием препарата следует прекратить.
Судороги
Из-за способности СИОЗС снижать судорожный порог следует избегать назначения дапоксетина пациентам с нестабильной эпилепсией, при появлении судорог препарат следует отменить. За пациентами с контролируемой эпилепсией требуется тщательное наблюдение.
Сопутствующая депрессия и/или психические расстройства
Перед началом терапии дапоксетином мужчинам с наличием признаков и симптомов депрессии следует провести обследование для исключения наличия недиагностированных депрессивных расстройств. Совместный прием дапоксетина и антидепрессантов, включая СИОЗС и СИОЗСН, противопоказан (см. «Противопоказания»). Прерывание лечения по поводу имеющейся депрессии или чувства тревоги для того, чтобы начать прием дапоксетина для терапии по поводу ПЭ, не рекомендуется. Прием дапоксетина не показан при психических нарушениях и не должен использоваться у мужчин с такими заболеваниями, как шизофрения, или у пациентов с сопутствующей депрессией, т.к. нельзя исключить усугубление симптомов, связанных с депрессией. Это может быть следствием фонового психического расстройства или приема лекарственного препарата. Врач должен рекомендовать пациентам в любое время сообщать о любых депрессивных мыслях или чувствах, и если явления и симптомы депрессии развились во время лечения, прием дапоксетина следует прекратить.
Кровотечение
При применении СИОЗС описаны случаи развития кровотечения. Рекомендуется проявлять осторожность при приеме дапоксетина одновременно с препаратами, влияющими на функцию тромбоцитов (например, атипичные нейролептики, фенотиазины, ацетилсалициловая кислота, НПВП, антикоагулянты (например, варфарин), а также у пациентов с кровотечениями или нарушением свертываемости крови в анамнезе (см. «Взаимодействие»).
Нарушение функции почек
Дапоксетин не рекомендуется принимать пациентам с почечной недостаточностью тяжелой степени, пациентам с почечной недостаточностью легкой степени или средней степени тяжести следует проявлять осторожность (см. «Способ применения и дозы», «Фармакокинетика»).
Синдром отмены
Имеются данные о том, что резкая отмена СИОЗС, длительно применявшихся для лечения хронических депрессивных расстройств, приводит к следующим симптомам: снижение настроения, раздражительность, возбуждение, головокружение, нарушения чувствительности (например, парестезия в виде ощущения удара электротоком), тревожность, спутанность сознания, головная боль, сонливость, эмоциональная нестабильность, бессонница, гипомания.
В двойном слепом клиническом исследовании у лиц с ПЭ, проведенном для оценки синдрома отмены после приема дапоксетина в дозе 60 мг в течение 62 дней ежедневно или по потребности, у лиц, переведенных на плацебо после ежедневного приема дапоксетина, проявились умеренные симптомы в виде небольшого повышения частоты бессонницы и головокружения.
Нарушения со стороны органа зрения
На фоне применения дапоксетина отмечались такие нежелательные реакции со стороны органа зрения, как мидриаз и боль в глазах. Дапоксетин следует применять с осторожностью у пациентов с повышенным ВГД или риском развития закрытоугольной глаукомы.
Вспомогательные вещества
Препарат Дапоксетин-СЗ содержит лактозы моногидрат (сахар молочный). Пациентам с редко встречающейся наследственной непереносимостью галактозы, дефицитом лактазы или глюкозо-галактозной мальабсорбцией не следует принимать данный препарат.
Влияние на способность к управлению транспортными средствами и механизмами. Дапоксетин оказывает влияние на способность к управлению транспортными средствами и обслуживанию механизмов. При приеме дапоксетина описаны случаи головокружения, нарушения внимания, обморока, нечеткости зрения, сонливости. Следует предупредить пациента о необходимости избегать ситуаций, при которых возможно получение травмы, включая управление транспортными средствами и обслуживание механизмов. Одновременное употребление алкоголя и дапоксетина может усиливать связанные с алкоголем нейрокогнитивные эффекты и также повышать риск развития нейрокардиогенных нежелательных реакций, таких как обморок, что, в свою очередь, увеличивает травмоопасность. Таким образом, пациентам следует рекомендовать избегать одновременного употребления алкоголя при применении препарата Дапоксетин-СЗ (см. «Особые указания», «Взаимодействие»).
Форма выпуска
Таблетки, покрытые пленочной оболочкой, 30 и 60 мг. По 4, 6, 8, 10 табл. в упаковке ячейковой контурной из пленки ПВХ и фольги алюминиевой.
По 20 табл. в банке полимерной типа БП из ПЭНД с крышкой из ПЭВД или во флаконе полимерном из ПЭНД с крышкой из ПЭВД.
Каждую банку, флакон, 1 упаковку ячейковую контурную по 4, 6, 8, 10 табл., или 2 упаковки ячейковые контурные по 6 табл., или 2, 3 упаковки ячейковые контурные по 10 табл. вместе с листком-вкладышем помещают в пачку картонную.
Производитель
Держатель регистрационного удостоверения. Российская Федерация. НАО «Северная звезда». Юридический адрес: 111524, Москва, ул. Электродная, 2, стр. 34, эт. 2, помещ. 47.
Тел./факс: +7 (495) 137-80-22.
e-mail: electro@ns03.ru
Представитель держателя регистрационного удостоверения/претензии потребителей направлять по адресу. Российская Федерация. НАО «Северная звезда». Ленинградская обл., муниципальный р-н Всеволожский, г.п. Кузьмоловское, гп. Кузьмоловский, ул. Заводская, 4, к. 1.
Тел./факс: +7 (812) 309-21-77.
e-mail: safety@ns03.ru
Условия отпуска из аптек
По рецепту.
Условия хранения
В защищенном от света месте, при температуре не выше 25 °C.
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не применять по истечении срока годности, указанного на упаковке.
Описание проверено
-
Лобанова Елена Георгиевна
(фармаколог, доктор медицинских наук, профессор)
Опыт работы: более 30 лет
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.
-
Архив журнала
/ -
2017
/ - №5
Доказательность эффективности и безопасности дапоксетина при лечении преждевременного семяизвержения
DOI: https://dx.doi.org/10.18565/urology.2017.5.106-110
Н.Д. Ахвледиани, И.П. Матюхов
ФГАОУ ВО «Первый МГМУ им. И. М. Сеченова» Минздрава России (Сеченовский Университет), Москва, Россия
Цель работы – изучить доказательные сведения по эффективности и профилю безопасности дапоксетина при преждевременном семяизвержении (ПС). Рассмотрены результаты рандомизированных плацебо-контролируемых исследований, интегративных обзоров и одного мета-анализа по клинической эффективности и безопасности дапоксетина. Во всех работах показана высокая эффективность дапоксетина при ПС по сравнению с плацебо. Его прием в дозировке 30 и 60 мг позволяет увеличивать продолжительность коитуса приблизительно до 3,0 и 3,5 мин соответственно. Профиль безопасности дапоксетина позволяет применять его в клинической практике. Дапоксетин является новым на российском рынке эффективным и безопасным лекарственным препаратом для лечения ПС.
Ключевые слова: преждевременное семяизвержение, дапоксетин, примаксетин, эффективность, безопасность
Согласно современным клиническим рекомендациям Международной ассоциации по сексуальной медицине (ISSM), выделяют первичную и вторичную формы преждевременного семяизвержения (ПС). При этом к первому варианту описанного сексуального расстройства относят эякуляцию, возникающую приблизительно менее чем через 1 мин после начала коитуса или до интроекции и характеризующуюся возникновением с начала половой жизни, отсутствием контроля над эякуляторным процессом и негативным психологическим фоном у обоих партнеров. Вторичная форма ПС отличается приобретенным характером и временем интравагинальной задержки семяизвержения (ВИЗС) менее 3 мин [1].
Общепризнанно, что ПС относится к распространенным сексуальным нарушениям, так как, по разным данным, оно встречается у 20–40% мужской популяции. Вместе с тем, согласно клиническим рекомендациям Европейской ассоциации урологов, с учетом имевших в недавнем прошлом несоответствий между существующими дефинициями и диагностическим критериям описанного полового расстройства, нельзя исключить его гипердиагностику [2].
Одной из основных причин первичного ПС считают дисрегуляцию церебрального 5-гидрокситриптамина (5-ГТ) или серотонина, описанную авторами нейробиологической теории возникновения ускоренной эякуляции. Имеются доказательства генетической обусловленности недостатка данного нейромедиатора у обсуждаемой категории пациентов в синаптических щелях серотонинэргических нейронов головного мозга [3]. Описанная особенность связана с генотипом гена транспортера серотонина. Имеются доказательства того, что к ПС наиболее предрасположены мужчины с S-аллельсодержащими вариантами строения данного белка [4].
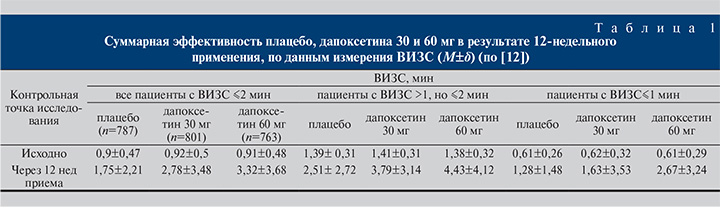
Состоятельность нейробиологической теории еще до ее официального возникновения доказал в 1973 г. H. Eaton, впервые успешно применивший при ускоренной эякуляции трициклический антидепрессант кломипрамин, обладающий мощной способностью блокировать обратный нейрональный захват 5-ГТ. Впоследствии в начале 1990-х гг. были синтезированы антидепрессанты группы селективных ингибиторов обратного захвата серотонина (СИОЗС), которые прицельно воздействовали на серотонинэргические нейроны. Руководствуясь имевшимися в то время данными о роли церебрального серотонина в регуляции эякуляторной функции, в зарубежных странах их стали активно применять не по показаниям при первичноим ПС [5]. Примечательно, что принадлежность СИОЗС к психотропным лекарствам группы антидепрессантов в ряде стран не позволяет назначать их по поводу ПС, так как это не оговорено в зарегистрированных инструкциях. В Российской Федерации возможность использования любого препарата определяется врачом в рамках, ограниченных официальными показаниями, заявленными производителем. В США и в ряде государств Западной Европы назначение лекарств не по зарегистрированным основаниям допустимая практика, при этом ответственность за жизнь и здоровье пациента целиком ложится на доктора, что предусмотрено в юридических полномочиях врачебной лицензии [6, 7].
В отношении СИОЗС следует учитывать, что на сегодняшний день подтверждена повышенная вероятность суицидальных тенденций при их отмене. Это дополнительно обосновывает нежелательность их назначения пациентам без депрессии, которая должна быть диагностирована психиатром [8].

С учетом указанных обстоятельств специально для лечения преждевременного семяизвержения был разработан СИОЗС дапоксетин. В отличие от остальных препаратов данной группы, имеющих галогенированные молекулы, в его молекулярной структуре содержится нафтильный фрагмент [9]. Именно он обусловливает быструю абсорбцию препарата в желудочно-кишечном тракте и короткий период полувыведения, что обеспечивает значительно меньшее число побочных эффектов по сравнению с другими СИОЗС. Максимальная концентрация в плазме крови достигается через 1,5 ч после приема [10]. Быстрое снижение плазменного содержания препарата не позволяет обнаруживать более 4% данного препарата спустя 24 ч.
После продолжительных ежедневных приемов обсуждаемого СИОЗС доказано отсутствие его значимого накопления [11].
Впервые эффективность дапоксетина в рамках рандомизированного двойного слепого плацебо-контролируемого исследования изучили J. Pryor и соавт. в 2006 г. [12]. Участие в нем принял 2351 пациент, который был разделен на 3 группы по 787, 801 и 763 человека, получавших в течение 12 нед соответственно плацебо, дапоксетин 30 и 60 мг. Препарат назначался по требованию за 1–3 ч до предполагаемой сексуальной активности. К концу исследования обе дозы дапоксетина были достоверно более эффективны по сравнению с плацебо (p<0,0001), при этом 60 мг значимо превышали по эффекту 30 мг лекарства (p=0,0007). К 12-й неделе 109 (14%), 232 (29%) и 261 (34%) пациент 1-й, 2-й и 3-й групп соответственно имели показатель ВИЗС, превысивший 3 мин. Прием первой дозы дапоксетина по эффективности достоверно превосходил плацебо. В группах, получавших плацебо, дапоксетин 30 и 60 мг, ВИЗС от базового уровня увеличилось на 1,38; 2,05 и 2,41 мин соответственно (табл. 1).
При оценке профиля безопасности лечения обсуждаемым СИОЗС (в дозировке 30 и 60 мг) были соответственно отмечены тошнота (8,7 и 20,1%), диарея (3,9 и 6,8%), головная боль (5,9 и 6,8%) а также головокружение (3,0 и 6,2%) [12].
В 2009 г. J. Kaufman и соавт. [13] провели двойное слепое плацебо-контролируемое исследование эффективности дапоксетина при ПС, в котором завершили участие 652 пациента. Основная оценка эффективности лечения проведена по анкете Профиля преждевременного семяизвержения (ППС; табл. 2). В результате лечения пациенты, получавшие дапоскетин, отметили статистически значимое снижение обеспокоенности по поводу состояния эякуляторной функции, уменьшение выраженности межличностных конфликтов в паре, а также улучшение контроля над семяизвержением и удовлетворение от полового акта.
Дополнительно всем пациентам, участвовавшим в данном исследовании, проведено анкетирование по шкале общего впечатления об изменении эякуляторной функции в результате лечения. Наивысшую степень удовлетворения от проведенной терапии отметили 41,3 и 20,8% больных, получавших дапоксетин и плацебо соответственно (p<0,001). Кроме того, оценен клинический профиль безопасности указанного СИОЗС (табл. 3). Было отмечено, что частые побочные эффекты, имевшие место более чем в 5% наблюдений, среди которых тошнота, головокружение, головная боль, диарея и бессонница, чаще возникали при приеме 60 мг дапоксетина. Отказ от продолжения лечения по причине нежелательных явлений был констатирован у 10 и 2% пациентов, принимавших указанное лекарство и плацебо соответственно. При этом наиболее часто причиной отмены дапоксетина служили тошнота и бессонница [13].
J. Buvat и соавт. [14] провели 24-недельное плацебо-контролируемое исследование эффективности дапоксетина при ПС, которое завершили 618 пациентов. Среднее ВИЗС возросло при применении плацебо, а также дапоксетина 30 и 60 мг с 0,9 до 1,9; 3,2 и 3,5 мин соответственно. Таким образом, применение данного СИОЗС в обеих дозах позволило статистически значимо увеличить продолжительность полового акта (p<0,001). Наиболее частыми нежелательными явлениями при приеме дапоксетина были тошнота, головокружение, диарея и головная боль. Отказ от лечения по причине тяжелых побочных эффектов в группах, получавших плацебо, а также обсуждаемый СИОЗС в дозировках 30 и 60 мг отмечены в 1,3, 3,9 и 8,2% наблюдений соответственно [14].
В 2010 г. С. McMahon и соавт. [15] провели двойное слепое рандомизированное плацебо-контролируемое исследование эффективности дапоксетина при ПС в Азиатско-Тихоокеанском регионе. Участие в нем завершили 858 пациентов. Среднее ВИЗС при применении плацебо, а также дапоксетина 30 и 60 мг увеличилось с 1,1 мин до 2,4; 3,9 и 4,2 мин соответственно. Удовлетворенность произошедшими в результате лечения дапоксетином изменениями эякуляторной функции была статистически значимо выше (p<0,005) по сравнению с группой пациентов, принимавших плацебо [15].
H. Porst и соавт. [16] провели обобщенный анализ 3 рандомизированных плацебо-контролируемых исследований эффективности обсуждаемого СИОЗС, включивший 2228 наблюдений. При этом авторы акцентировали усилия на сравнении существующих дозировок дапоксетина и плацебо при первичном и вторичном ПС в зависимости от наличия эректильной дисфункции (ЭД; см. рисунок). Авторами показано статистически значимое увеличение ВИЗС по сравнению с плацебо при применении указанного лекарства в дозировке 30 мг пациентами с обеими формами эякуляторного нарушения только в отсутствие нарушений эрекции. Вместе с тем еще более значимое возрастание продолжительности коитуса было отмечено у больных ПС при приеме 60 мг дапоксетина вне зависимости от формы ускоренной эякуляции и наличия ЭД [16].
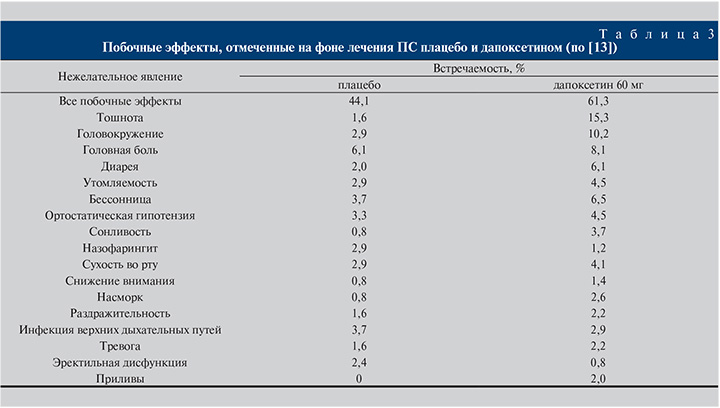
В 2011 г. С. McMahon и соавт. [17] представили результаты анализа крупнейших рандомизированных плацебо-контролируемых исследований III фазы, проведенных в 25 странах и включивших 6081 пациента. Через 12 и 24 нед приема 30 мг дапоксетина было отмечено достоверное возрастание ВИЗС с 0,9 до 3,1 и 2,0 мин соответственно. При лечении препаратом в дозировке 60 мг продолжительность полового акта в указанные контрольные сроки возросла с 0,8 до 3,6 и 2,3 мин соответственно. Применение обеих дозировок дапоксетина позволило достигать положительной динамики по показателю ВИЗС, особенно через 12 нед от начала терапии (p<0,0001) [17].
В работе [18] проведена оценка эффективности 12-недельного комбинированного назначения дапоксетина пациентам с ПС и сопутствующей ЭД, получавших ингибиторы фосфодиэстеразы 5-го типа (ИФДЭ-5). Исследование завершили 429 пациентов. Авторы отметили, что продолжительность полового акта одинаково статистически значимо возросла при комбинированной терапии с СИОЗС по сравнению с группой пациентов, получавших плацебо+ИФДЭ-5 (5,2 против 3,4 мин; p<0,01). Общая удовлетворенность лечением при анкетировании также достоверно различалась в основной и контрольной группах (56,6 против 35,4%; p<0,001).
Авторы не отметили каких-либо лекарственных взаимодействий при совместном назначении с коротко- (силденафил) и длительнодействующим (тадалафил) ИФДЭ-5.
Частота побочных явлений при применении плацебо и дапоксетина в составе комбинированной терапии с эректогенными препаратами первой линии составила 20,9 и 29,6% соответственно. Отказ от лечения по причине нежелательных эффектов был отмечен в 1,6% наблюдений в основной и контрольной группах. Наиболее частыми побочными явлениями, ассоциированными с СИОЗС, были тошнота (9,2%), головная боль (4,4%), диарея (3,6%), головокружение (2,4%) и постуральная гипотензия (2,4%) [18].
Единственный на данный момент мета-анализ 5 рандомизированных плацебо-контролируемых клинических исследований эффективности дапоксетина был проведен F. Yue и соавт. в 2015 г. [19]. Установлено, что данный препарат значимо эффективней плацебо по показателю ВИЗС – в 1,47 раза (95% доверительный интервал [ДИ] – 1,22–1,71; p<0,00001). По данным анкетирований, оценивавших диагностические критерии ПС, дапоксетин лучше плацебо в 3,19 раза (95% ДИ – 2,47–4,11; p<0,00001). Преимущества указанного СИОЗС по сравнению с плацебо отмечены в отношении удовлетворения от полового акта (в 1,89 раза; 95% ДИ – 1,68–2,12; p<0,00001) и снижения обеспокоенности сексуальной пары в 0,72 раза (95% ДИ – 0,57–0,9; p<0,00001). Авторы пришли к выводу, что дапоксетин является достаточно эффективным и хорошо переносимым препаратом для лечения первичного и вторичного ПС. Вместе с тем было указано, что отдаленные результаты терапии и переносимости требуют дополнительной оценки [19].
В настоящий момент дапоксетин одобрен к применению в клинической практике для лечения ПС в 50 странах. Он рекомендован пациентам с ПС в возрасте от 18 до 64 лет. Применять его следует в начальной дозировке 30 мг за 1–3 ч до полового акта при максимальной регулярности применения 1 раз в сутки. В случае необходимости дозировка дапоксетина может быть увеличена до 60 мг.
Препарат противопоказан при выраженной сердечной недостаточности, нарушениях проводимости, наличии искусственного водителя ритма, тяжелой ишемической болезни сердца и заболеваниях его клапанов, а также тяжелой почечной недостаточности. Кроме того, дапоксетин не следует назначать при среднетяжелых и тяжелых формах печеночной недостаточности и пациентам, которым проводится параллельное лечение лекарствами, ингибирующими активность цитохромов-P450 и любыми психотропными препаратами. Следует также избегать его совместного применения с алкоголем [20].
В сентябре 2016 г. в России был зарегистрирован официальный генерик дапоксетина – Примаксетин®, выпускаемый в традиционных дозировках 30 и 60 мг. Осенью 2017 г., он поступил в продажу в отечественные аптечные сети, что позволяет применять его в клинической практике российским врачам-урологам [21, 22]. Препарат отпускается по рецепту врача. Оригинальный препарат дапоксетина Прилиджи® так и не успел выйти на российский рынок до окончания действия патентной защиты, при этом регистрация его состоялась в 2013 г. и действует по настоящее время.
Таким образом, в настоящий момент доказана хорошая эффективность и достаточная безопасность дапоксетина при терапии всех форм ПС. Появление его на российском рынке открывает новые перспективы в консервативном лечении многочисленных пациентов с ускоренной эякуляцией в нашей стране.
Литература
1. Althof S.E., McMahon C.G., Waldinger M.D., Serefoglu E.C., Shindel A.W., Adaikan P.G., Becher E., Dean J., Giuliano F., Hellstrom W.J., Giraldi A., Glina S., Incrocci L., Jannini E., McCabe M., Parish S., Rowland D., Segraves R.T., Sharlip I., Torres L.O. An update of the International Society of Sexual Medicine’s guidelines for thediagnosis and treatment of premature ejaculation (PE). J Sex Med. 2014;11(6):1392–422. Doi: 10.1111/jsm.12504.
2. Porst H., Montorsi F., Rosen R.C., Gaynor L., Grupe S., Alexander J. The Premature Ejaculation Prevalence and Attitudes (PEPA) survey: prevalence, comorbidities, and professional help-seeking. Eur Urol. 2007;51(3):816–23; discussion 824. Doi: 10.1016/j.eururo.2006.07.004.
3. Waldinger M.D. The neurobiological approach to premature ejaculation. J Urol 2002;168:2359–2367. Doi: 10.1097/01.ju.0000035599.35887.8f.
4. Zhu L., Mi Y., You X., Wu S., Shao H., Dai F., Peng T., Qin F., Feng N. A meta-analysis of the effects of the 5-hydroxytryptamine transporter gene-linked promoter region polymorphism on susceptibility to lifelong premature ejaculation. PLoS One. 2013;8(1):e54994. Doi: 10.1371/journal.pone.0054994.
5. Waldinger M.D. Pharmacotherapy for premature ejaculation. Expert Opin Pharmacother. 2015;16(17):2615–2624. Doi: 10.1517/14656566.2015.1096928.
6. Mendelevich V.D., Zalmunin K.Y. Paradoxes of evidence in Russian addiction medicine. Int J Risk Saf Med. 2015;27(Suppl. 10:S102–103. Doi: 10.3233/JRS-150708.
7. The Federal Law «On the fundamentals of protecting the health of citizens in the Russian Federation». M.: Normatika. 2017. 72 p. (Федеральный закон «Об основах охраны здоровья граждан в Российской Федерации». М., 2017;72 с.)
8. Sadeghi-Nejad H., Watson R. Premature ejaculation: current medical treatment and new directions (CME). J Sex Med. 2008;5(5):1037–1050; quiz 1051-2. Doi:10.1111/j.1743-6109.2008.00831.x.
9. Kendirci M., Salem E., Hellstrom W.J. Dapoxetine, a novel selective serotonin transport inhibitor for the treatment of premature ejaculation. Ther Clin Risk Manag. 2007;3:277–289. PMCID: PMC1936309.
10. Modi N.B., Dresser M.J., Simon M. et al. Single- and multiple-dose pharmacokinetics of dapoxetine hydrochloride, a novel agent for the treatment of premature ejaculation. J Clin Pharmacol. 2006;46:301–309. Doi: 10.1177/0091270005284850.
11. Andersson K.E., Mulhall J.P., Wyllie M.G. Pharmacokinetic and pharmacodynamic features of dapox-etine, a novel drug for ‘on-demand’ treatment of premature ejaculation. BJU Int 2006;97:311–315. Doi: 10.1111/j.1464-410X.2006.05911.x.
12. Pryor J.L., Althof S.E., Steidle C., Rosen R.C., Hellstrom W.J., Shabsigh R., Miloslavsky M., Kell S. Dapoxetine Study Group. Efficacy and tolerability of dapoxetine in treatment of premature ejaculation: an integrated analysis of two double-blind, randomised controlled trials. Lancet. 2006;368(9539):929–937. Doi:10.1016/S0140-6736(06)69373-2.
13. Kaufman J.M., Rosen R.C., Mudumbi R.V., Tesfaye F., Hashmonay R., Rivas D. Treatment benefit of dapoxetine for premature ejaculation: results from a placebo-controlled phase III trial. BJU Int. 2009;103(5):651–658. Doi:10.1111/j.1464-410X.2008.08165.x.
14. Buvat J., Tesfaye F., Rothman M., Rivas D.A., Giuliano F. Dapoxetine for the treatment of premature ejaculation: results from a randomized, double-blind, placebo-controlled phase 3 trial in 22 countries. Eur Urol. 2009;55(4):957–967. Doi: 10.1016/j.eururo.2009.01.025.
15. McMahon C., Kim S.W., Park N.C., Chang C.P., Rivas D., Tesfaye F., Rothman M., Aquilina J.Dapoxetine 3003 Study Investigators. Treatment of premature ejaculation in the Asia-Pacific region: results from a phase III double-blind, parallel-group study of dapoxetine. J Sex Med. 2010;7(1 Pt 1):256–268. Doi: 10.1111/j.1743-6109.2009.01560.x.
16. Porst H., McMahon C.G., Althof S.E., Sharlip I., Bull S., Aquilina J.W., Tesfaye F., Rivas D.A. Baseline characteristics and treatment outcomes for men with acquired or lifelong premature ejaculation with mild or no erectile dysfunction: integrated analyses of two phase 3 dapoxetine trials. J Sex Med. 2010;7(6):2231–2242. Doi: 10.1111/j.1743-6109.2010.01820.x.
17. McMahon C.G., Althof S.E., Kaufman J.M., Buvat J., Levine S.B., Aquilina J.W., Tesfaye F., Rothman M., Rivas D.A., Porst H. Efficacy and safety of dapoxetine for the treatment of premature ejaculation: integrated analysis of results from five phase 3 trials. J Sex Med. 2011;8(2):524–539. Doi: 10.1111/j.1743-6109.2010.02097.x.
18. McMahon C.G., Giuliano F., Dean J., Hellstrom W.J., Bull S., Tesfaye F., Sharma O., Rivas D.A., Aquilina J.W. Efficacy and safety of dapoxetine in men with premature ejaculation and concomitant erectile dysfunction treated with a phosphodiesterase type 5 inhibitor: randomized, placebo-controlled, phase III study. J Sex Med. 2013;10(9):2312–2325. Doi: 10.1111/jsm.12236.
19. Yue F.G., Dong L., Hu T.T., Qu X.Y. Efficacy of Dapoxetine for the treatment of premature ejaculation: a meta-analysis of randomized clinical trials on intravaginal ejaculatory latency time, patient-reported outcomes, and adverse events. Urology. 2015;85(4):856–861. Doi: 10.1016/j.urology.2015.01.009.
20. McCarty E., Dinsmore W. Dapoxetine: an evidence-based review of its effectiveness in treatment of premature ejaculation. Core Evid. 2012;7:1–14. Doi: 10.2147/CE.S13841.
21. http://www.grls.rosminzdrav.ru/Grls_View_v2.aspx?routingGuid=ac041539-bb30-4409-ba29-5a90153d358a&t=68af6333-bb61-42df-8df3-048b8d88dedf
22. http://www.grls.rosminzdrav.ru/Grls_View_v2.aspx?routingGuid=597584d2-765f-413b-986e-486f107d7219&t
Об авторах / Для корреспонденции
А в т о р д л я с в я з и: Н. Д. Ахвледиани – д.м.н., профессор кафедры урологии ФГАОУ ВО «Первый МГМУ им. И. М. Сеченова» Минздрава России (Сеченовский Университет), Москва, Россия; e-mail: nikandro@mail.ru
