Статьи
Опубликовано в журнале:
«Русский медицинский журнал», 2008, Том 16, №20, с. 3-11
В. Вуттке1, К. Горков2, Д. Сейдлова–Вуттке1
1 Университет в Геттингене, Германия 2 «Бионорика», Ноймаркт, Германия
Из–за повышенного риска рака молочной железы и сердечно–сосудистых заболеваний, таких как инфаркт миокарда или инсульт [7–11], перевешивающих доказанную эффективность гормональной терапии (ГТ) в отношении проявлений климакса, ее положительное влияние на метаболизм в костной ткани и состояние слизистой оболочки влагалища [1–6], пациентки все реже соглашаются на этот вид лечения. Поэтому и врачи, и больные стараются найти альтернативные эстрогенам препараты, прием которых позволил бы купировать симптомы менопаузы и поддерживать прочность костной ткани. Такой альтернативой мог бы быть селективный модулятор рецептора эстрогенов, который подавлял бы проявления климакса и оказывал бы положительное влияние на костную ткань; при этом он был бы лишен неблагоприятных эффектов в отношении ткани молочной железы и матки, характерных для эстрогенов [12,13].
В этом плане весьма перспективны препараты растительного происхождения, поскольку есть убедительные данные в пользу того, что использование некоторых травяных экстрактов облегчает симптоматику климактерического синдрома и улучшает метаболизм в костной ткани у женщин постменопаузального возраста. Одним из таких растительных препаратов является вытяжка из корневищ цимицифуги (Cimicifuga racemosa, клопогон кистевидный). Его эффективность доказана результатами нескольких клинических испытаний; их отрицательна сторона – открытый дизайн или отсутствие плацебо–контроля [14–16]. Лишь однажды проводилось двойное слепое плацебо–контролируемое исследование, в ходе которого удалось продемонстрировать эффективность цимицифуги в отношении проявлений климакса по сравнению с плацебо [17]. При этом, однако, удваивали рекомендуемую суточную дозу (что соответствовало 80 мг растительного препарата вместо стандартных 40 мг). В дальнейшем была предпринята попытка сопоставить эффекты лечения экстрактом цимицифуги BNO 1055 (Климадинон® Бионорика АГ, Германия), с одной стороны, и конъюгированными эстрогенами и плацебо, с другой [18]. Эффективность экстракта цимицифуги BNO 1055 и конъюгированных эстрогенов оказалась сравнимой и значительно превосходила таковую плацебо в отношении проявлений климактерического синдрома. Но в отличие от конъюгированных эстрогенов, плацебо и экстракт цимицифуги BNO 1055 не вызывали утолщения эндометрия.
Исследования на доклиническом этапе, проведенные за последние 10 лет, позволили больше узнать об эффектах экстракта цимицифуги. В опытах in vitro по связыванию экстракта цимицифуги с рекомбинантными рецепторами эстрогенов (ЭРα и ЭРβ) было установлено, что экстракт не связывает ни один из двух эстрогеновых рецепторов. Согласно результатам экспериментов на грызунах экстракт цимицифуги не имеет утеротропного действия [19,20]. На основании этих данных был сделан вывод о том, что экстракты цимицифуги не содержат эстрогеноподобных компонентов, хотя экстракт цимицифуги BNO 1055 замещает радиоактивно меченный 17β–эстрадиол (Е2) в цитозольных препаратах матки свиньи и эндометрия человека [21]. Следовательно, можно предполагать, что пока неизвестные составляющие экстракта цимицифуги BNO 1055 способны взаимодействовать с пока не выявленным эстроген–связывающим белком.
У крыс экстракт цимицифуги BNO 1055 оказывает благоприятное воздействие на гипоталамус, подавляя пульсирующее высвобождение лютеинизирующего гормона (ЛГ), а возможно – и приливы [22]. Экстракты цимицифуги содержат компоненты, связывающие серотониновые рецепторы, и не исключено, что это и есть механизм, благодаря которому приливы ослабевают [23]. Однако Е2 и экстракт цимицифуги BNO 1055 одинаковым образом модулируют экспрессию в костной ткани двух генов, регулируемых эстрогенами. Эффекты экстракта цимицифуги BNO 1055 и Е2 наблюдали в костной ткани у крыс после удаления яичников, недостаточность которых восполняли обоими препаратами на протяжении 12 недель [19]. Оба препарата тормозили экспрессию генов IGF1 и TRAP [19,22]. Все это указывает на то, что на фоне такого лечения активность остеобластов и остеокластов, повышенная вследствие овариэктомии, восстанавливается до нормальных значений, как у интактных животных. У грызунов, которым вводили Е2 и экстракт цимицифуги BNO 1055, Е2 практически полностью предотвращал более чем 50%–ю потерю минеральной плотности костной ткани метафиза большеберцовой кости, в то время как у крыс, получавших экстракт цимицифуги BNO 1055, этот эффект оказался частичным, но все же значимым при сравнении с контрольной группой [19,24]. Также продемонстрировано положительное влияние экстракта цимицифуги на уровень маркеров метаболизма костной ткани и минеральную плотность бедренной кости [25].
Во влагалище Е2 обусловливает пролиферацию эпителия, что способствует выработке бактериями лактата с закислением среды, не допуская тем самым восходящего бактериального инфицирования матки. Тот же самый эффект, хотя и слабовыраженный, можно наблюдать у женщин, принимающих экстракт цимицифуги. В опытах на крысах с удаленными яичниками показано наличие умеренного вагинотропного действия у экстракта цимицифу-ги BNO 1055 [22]. Эстрогены повышают активность системы свертывания крови, что может спровоцировать тромбоэмболию. О наличии таких побочных эффектов у цимицифуги информации нет.
С учетом благоприятного влияния экстракта цимицифуги BNO 1055, а также отсутствия у него эстрогеноподобного действия в отношении матки и эндометрия можно предположить, что этот экстракт обладает органной селективностью [19,22], хотя ее механизмы пока не изучены. Эта активность не опосредована ни одним из двух описанных эстрогеновых рецепторов, но, возможно, связана со стимуляцией их активизирующих и/или подавляющих посредников.
Определенные опасения вызывает предполагаемая гепатотоксичность препаратов цимицифуги, поскольку сообщается о развитии острой печеночной недостаточности, ассоциированной с применением этой растительной добавки [26]. Вопрос о гепатотоксичности интенсивно обсуждался на последнем симпозиуме Националь ного центра нетрадиционной и альтернативной медицины/Национальных институтов здоровья (http://nccam.nih.gov/news/pastmeetings/blackcohosh_mtn gsumm.htm), и было выдвинуто предложение соблюдать необходимые параметры безопасности в ходе проведения клинических исследований. Таким образом, анализируя влияние спиртового экстракта цимицифуги BNO 1055 на проявления климактерического синдрома, также необходимо обращать внимание на параметры анализа крови, которые могли бы указывать на гепатотоксичность. Учитывая скудность информации, касающейся эффектов цимицифуги в отношении остеопороза и состояния слизистой влагалища, а также недостаточность сведений по действию цимицифуги на содержание липидов в крови или факторов гемостаза, ниже будут представлены и эти данные по пациенткам.
Методы
Первичные конечные точки этого двойного слепого плацебо–контролируемого исследования описаны ранее [18]. Вторичной задачей приводимой работы являлось сравнительное изучение влияния экстракта цимицифуги BNO 1055 на уровень маркеров метаболизма костной ткани, менопаузального гормона, связывающего половые гормоны глобулина (ГСПГ) и липидов, а также на цитологию эпителия влагалища и результаты стандартных лабораторных анализов относительно конъюгированных эстрогенов и плацебо.
Дизайн исследования
Описание методов рандомизированного двойного слепого сравнения экстракта цимицифуги BNO 1055 с конъюгированными эстрогенами и плацебо приведено в ранних работах [18]. Ниже представлены сокращенные методы, а основной акцент сделан на специфических показателях, которые упоминались выше.
Исследование проводилось в период с 1998 по 2000 г. в 13 исследовательских центрах Чехии в соот ветствии с положениями Хельсинкской Декларации и Правилами надлежащей клинической практики ICH–GCP. Объем выборки (по 30 женщин в постменопаузе на каждую группу лечения) формировали в зависимости от показателя клинически достоверных различий по первичной конечной точке – ослаблению симптоматики климактерического синдрома, которую определяли по первой версии рейтинговой шкалы постменопаузы [27].
Сбалансированность всех трех групп лечения обеспечивалась перестановочной блоковой рандомизацией [28]. Продолжительность лечения составила 12 недель. Медицинские осмотры и лабораторные анализы крови проводили за 2 недели до начала основных испытаний (в момент старта подготовительной фазы), на 0 неделе (исходно), а затем через 4, 8 и 12 недель.
Перед проведением всех медицинских измерений, связанных с исследованием, всех пациенток информировали в устной или печатной форме о целях исследования, его особенностях, сопряженном риске и преимуществах, длительности лечения и его альтернативах, после чего испытуемые давали добровольное информирование согласие в письменном виде.
Критерии включения и исключения
Критериями включения являлись: наличие менопаузы; возраст от 40 до 60 лет; срок с момента последних менструаций не менее 6 месяцев; индекс массы тела ≤30 кг/м2; концентрация постменопаузального уровня гормонов (Е2) ≤40 пг/мл и уровень фолликулостимулирующего гормона (ФСГ) ≥25 мМЕ/мл в начале подготовительного периода (неделя –2) и на исходном этапе (неделя 0); по меньшей мере, 3 эпизода приливов в сутки в ходе подготовительного периода (согласно записям в дневниках); сумма баллов по первым шести пунктам рейтинговой шкалы менопаузы (MRS) ≥1,7 на неделе –2 и 0, количество баллов по первому пункту шкалы MRS (приливы) ≥0,3 на неделе –2 и 0. Критерии исключения перечислены в таблице 1.
Таблица 1. Критерии исключения
- Овуляторные или ановуляторные циклы в течение подготовительного этапа исследования (признаком которых являются влагалищные кровотечения, уровень Е2>40 пг/мл и ФСГИндекс массы тела >30 кг/м2 (изначально не рассматривался как критерий исключения, но затем такие женщины были исключены из испытаний вследствие повышенного риска гипертрофии эндометрия и меньшей вероятности развития остеопороза по причине выработки эстрогенов в жировой ткани; все это объединяло таких пациенток в отдельную подгруппу, и их распределение между когортами лечения было бы неравномерным)
- Гистерэктомия в анамнезе
- Отсутствие ответа на терапию эстрогенами в прошлом
- Любые противопоказания к лечению эстрогенами или про-гестинами
- Генитальные кровотечения неясного генеза
- Подозрение на эстроген–зависимую карциному молочной железы и/или эндометрия (или верифицированный диагноз)
- Толщина эндометрия >5 мм
- Эндометриоз
- Тромбоэмболии в анамнезе и на момент обследования
- Флебиты
- Острая или хроническая печеночная недостаточность
- Нарушение метаболизма желчных пигментов
- Сахарный диабет
- Серповидно–клеточная анемия
- Клинически значимая гипертриглицеридемия или гиперхолестеринемия
- Перенесенный инфаркт миокарда
- Опухоли половых органов
- Выраженная варикозная болезнь вен
- Доказанная гиперчувствительность к изучаемым препаратам или их компонентам
- Сопутствующее лечение эстрогенами
- Сопутствующее лечение психотропными препаратами, антидепрессантами и успокоительными средствами, прием снотворных
- Неудовлетворительное общее состояние, алкогольная и/или наркотическая зависимость
Изучаемые препараты
Изучаемые препараты представляли собой твердые желатиновые капсулы со стеаратом магния и лактозой в качестве наполнителя. Все капсулы имели одинаковый размер, форму, вес, внешний вид и вкус. Суточная доза равнялась двум капсулам. Женщины из первой группы получали препарат с лиофилизированной водно–спиртовой (58% объема) вытяжкой BNO 1055 из корневищ Cimicifuga racemosa (цимицифуга; Климадинон, Bionorica AG, Ноймаркт, Германия). Каждая капсула (серийный номер 805005) содержала 1,66–2,86 мг нативного экстракта, что соответствовало 20 мг растительного препарата.
Пациентки второй группы принимали суточную дозу из двух капсул, в состав которых входило по 0,3 мг конъюгированных эстрогенов. Эти капсулы (серийный номер 71011210) представляли собой эстрофеминал (Heinrich Mack Nachf., иллертиссен, Германия), включающий эстрон (75–85%), эквилин (6–15%), эквиленин (до 4%), эстрадиол–17α, 17α–дигидроэквилин и 17α–дигидроэквиленин (2–8%). В третьей группе использовали капсулы с плацебо (серийный номер 805001).
После завершения подготовительного этапа длительностью 2 недели испытуемые начинали принимать изучаемый препарат (день 0). Их подвергали рандомизации, а затем выдавали первую упаковку лекарственного средства. Запакованные и помеченные индивидуальные контейнеры с 70 капсулами распределяли на неделе 0 (на недели 1–4), 4 (на недели 5–8) и 8 (на недели 9–12).
Изучаемые препараты изготавливали в соответствии со стандартами качественного производства GMP. Сертификаты анализов, проводимых до и в процессе исследования, а также описания изучаемых препаратов были подшиты к остальной документации.
Исследуемые параметры
Для определения уровня маркеров метаболизма костной ткани – щелочной фосфатазы костной ткани, (ЩФКТ) как критерия остеогенеза, и С–концевых телопептидов коллагена I типа (CrossLaps), как критерия резорбции костной ткани – эстрадиола 17β (иммунореактивного), Л Г, ФСГ и SHBG, а также параметров жирового обмена (общий холестерин, липопротеиды высокой плотности/ЛВП, липопротеиды низкой плотности/ЛНП, триглицериды) исходно и на 4, 8 и 12–й неделях утром натощак у испытуемых брали анализы крови. Поскольку концентрации Е2 и ФСГ являлись основными критерием включения, их дополнительно измеряли за 2 недели до начала основной фазы (неделя –2). Содержание гормонов и CrossLaps анализировали на приборе ELECSYS System (Roche–Diagnostics, Мангейм, Германия), уровень ЩФКТ – с помощью ферментного метода (Hitachi/Roche–Diagnostics, Мангейм, Германия), а показатели жирового обмена – с помощью цветных ферментных тестов. Спецификации исследований представлены в таблице 2.
Таблица 2. Параметры анализов крови
| Параметр анализа/ переменная |
Е2 (пг/мл) |
ФСГ (мМЕ/мл) | ЛГ (мМЕ/мл) | ГСПГ (нмоль/л) | ЩФКТ (Ед/л) | CrossLaps (нг/мл) | Холестерин (мг/дл) | ЛПВП (мг/дл) | ЛПНП (мг/дл) | Триглице-риды (мг/дл) |
| Чувствительность | <5 | <0,1 | 0,3 | 0,35 | 0,01 | 0,01 | 3 | 3 | 3 | 4 |
| Коэффициент вариации | <5% | <5% | <5% | <4% | <1% | <7% | <3% | <2% | <2% | <3% |
Исходно (неделя 0) и через 12 недель устанавливали степень зрелости эпителия влагалища (как меру влияния эстрогенов) с использованием т.н. индекса зрелости [29]. Для этого специальной щеточкой делали соскоб клеток эпителия влагалища, наносили их мазком на предметное стекло микроскопа, сразу же фиксировали и окрашивали по Папаниколау. Для определения индекса зрелости подсчитывали процентное соотношение парабазальных, промежуточных и поверхностных клеток (на 500 клеток).
Исходно и после завершения лечения оценивали стандартные лабораторные показатели безопасности (креатинин, мочевина, мочевая кислота, общий белок, натрий, калий, кальций, железо, общий билирубин, АСТ, АЛТ, γ–ГТ, ЩФ, глюкоза) и проводили развернутый анализ крови (эритроциты, лейкоциты, тромбоциты, формула крови, гемоглобин, гематокрит). В эти же сроки проверяли состояние свертывающей системы крови по активированному тромбопластиновому времени (в секундах) и тромбопластиновому времени (в виде международного нормализованного отношения – INR). В ходе каждого медицинского осмотра определяли уровень АД, частоту сердечных сокращений (в положении сидя/стоя) и массу тела.
Методы статистики
Переменные вычисляли как разницу между исходными и конечными значениями. Множественное сравнение каждой переменной между группами лечения осуществляли путем анализа ковариации (ANCOVA). Исходные показатели и центральная разность были включены в модель ANCOVA в качестве ковариации. Изменение численности пула поверхностных клеток (по результатам цитологии эпителия влагалища) оценивали с помощью обобщенного рангового критерия Вилкоксона. Статистически значимой считалась величина коэффициента р, меньше или равная 0,05. Статистическую обработку результатов выполняли в программе SAS (версия 8.2).
Результаты
Пациенты
Рандомизации подверглись 97 пациенток. Анализ в этой группе проводили в соответствии с принципом назначенного лечения (ITT). Двое испытуемых были преждевременно исключены из исследования вследствие отказа подписывать на исходном этапе бланк добровольного информированного согласия, их дальнейшая судьба не прослеживалась. Всего в результате нарушений протокола исследования из анализа по ITT выбыло 33 женщины: у 5 эпизоды приливов возникали в процессе подготовительного периода реже, чем 3 раза в сутки; в 16 случаях отсутствовали явные проявления постменопаузы (продолжение овуляторных или ановуляторных циклов на протяжении подготовительного периода, признаком которых являлись влагалищные кровотечения, уровень Е2>40 пг/мл и/или ФСГ30 кг/м2). В протокольный анализ включили 62 пациентки (экстракт цимицифуги BNO 1055, n=20; конъюгированные эстрогены, n=22; плацебо, n=20). Исходные характеристики эти испытуемых – возраст, рост, вес, концентрации гормонов, содержание маркеров остеогенеза и резорбции костной ткани – оказались сопоставимы во всех трех группах (табл. 3). Подсчет использованных капсул показал, что степень комплаентности больных (compliance) была высока во всех трех группах.
Таблица 3. Демографические характеристики
| Экстракт цимицифуги BNO 1055 | Конъюгированные эстрогены | Плацебо | ||||
| Возраст, лет | ||||||
| Среднее ± СО | 52,25 | ±3,19 | 52,32 | ±3,03 | 54,05 | ±4,36 |
| Медиана (n) | 52,50 | 20 | 52,00 | 22 | 54,00 | 20 |
| Масса, кг | ||||||
| Среднее ± СО | 67,00 | ±8,05 | 67,86 | ±9,3 | 65,15 | ±7,72 |
| Медиана (n) | 67,50 | 69,00 | 65,00 | |||
| Рост, см | ||||||
| Среднее ± СО | 164,20 | ±6,57 | 167,00 | ±5,27 | 164,05 | ±5,6 |
| Медиана (n) | 165,50 | 167,00 | 164,00 | |||
| Е2, пг/мл | ||||||
| Среднее ± СО | 19,45 | ±10,05 | 17,04 | ±9,23 | 14,57 | ±9,52 |
| Медиана (n) | 20,00 | 19,07 | 12,81 | |||
| ФСГ, мМЕ/мл | ||||||
| Среднее ± СО | 83,92 | ±33,47 | 80,97 | ±25,64 | 30,45 | ±19,6 |
| Медиана (n) | 79,90 | 82,79 | 69,92 | |||
| ЩФКТ, Ед/л | ||||||
| Среднее ± СО | 54,8 | ±14,34 | 52,85 | ±21,48 | 56,06 | ±23,31 |
| Медиана (n) | 56,00 | 20 | 54,50 | 20 | 55,00 | 18 |
| CrossLaps, нг/мл | ||||||
| Среднее ± СО | 0,25 | ±0,20 | 0,24 | ±0,12 | 0,25 | ±1,6 |
| Медиана (n) | 0,22 | 17 | 0,24 | 19 | 0,23 | 17 |
| ЩФ – щелочная фосфатаза |
Гормоны и ГСПГ
В группе получавших конъюгированные эстрогены содержание иммунореактивного Е2 через 4, 8 и 12 не дель заметно превышает аналогичные показатели по сравнению с группой плацебо. В отношении экстракта цимицифуги BNO 1055 такой эффект отсутствовал (рис. 1). Разница в содержании иммунореактивного Е2 между группой плацебо и группой экстракта цимицифуги BNO 1055 была статистически незначимой. Влияние проводимого лечения на концентрацию ФСГ в крови проиллюстрировано на рисунке 2. Во все три момента времени конъюгированные эстрогены ощутимо снижали уровень ФСГ, но не ЛГ (данные не представлены). Экстракт цимицифуги не оказывал заметного воздействия на титры обоих гормонов. Из–за небольшого количества предоставленной сыворотки измерить содержание ГСПГ удалось только у 16 женщин I группы, 20 женщин II группы и 15 женщин III группы, получавших в конце основного периода лечение экстрактом цимицифуги BNO 1055, конъюгированными эстрогенами и плацебо, соответственно. На фоне терапии экстрактом цимицифуги BNO 1055 и плацебо наблюдалось уменьшение этого показателя, в то время как конъюгированные эстрогены значительно повышали концентрацию ГСПГ (рис. 3).
Рис. 1. Анализ гормонального профиля: эстрадиол
*p
На фоне лечения конъюгированными эстрогенами в трех моментах времени наблюдается повышение титров Е2 по сравнению с плацебо и экстракт цимицифуги BNO 1055. Представлены средние значения величин с поправкой на исходные, центральная разность и стандартные ошибки среднего
Рис. 2. Анализ гормонального профиля: ФСГ
*p
На фоне лечения конъюгированными эстрогенами в трех моментах времени наблюдается снижение сывороточных титров ФСГ по сравнению с плацебо и экстракт цимицифуги BNO 1055. Представлены средние значения величин с поправкой на исходные, центральная разность и стандартные ошибки среднего
Рис. 3. Анализ содержания глобулина, связывающего половые гормоны (ГСПГ)
*p
По сравнению с плацебо и экстракт цимицифуги BNO 1055 сывороточная концентрация ГСПГ у женщин, получавших конъюгированные эстрогены, достоверно выше. Представлены средние значения величин с поправкой на исходные, центральная разность и стандартные ошибки среднего
Маркеры метаболизма костной ткани
Анализ сывороточных маркеров метаболизма костной ткани у женщин в постменопаузе выявил терапевтическую выгоду экстракта цимицифуги BNO 1055 и конъюгирован-ных эстрогенов. В случае плацебо уровень достоверного маркера резорбции костной ткани – продукта С–концевой деградации коллагена–1α1 костной ткани (т.е. CrossLaps) – нарастает незначительно, но статистически недостоверно. На фоне лечения экстрактом цимицифуги BNO 1055 содержание CrossLaps остается стабильным, а применение конъюгированных эстрогенов приводит к резкому снижению его концентрации через 4 и 12 недель (рис. 4).
Рис. 4. Метаболизм костной ткани: CrossLaps
*p
На фоне лечения конъюгированными эстрогенами наблюдается достоверное снижение сывороточных титров CrossLaps. Представлены средние значения величин с поправкой на исходные, центральная разность и стандартные ошибки среднего
Через 4 недели титр ЩФКТ, представляющей собой метаболический маркер остеогенеза, заметно увеличивается в группе получавших конъюгированные эстрогены по сравнению с плацебо, но через 8 и 12 недель этот эффект исчезает. Терапия экстрактом цимицифуги BNO 1055 обусловливает достоверный рост уровня ЩФКТ через 12 недель относительно плацебо (рис. 5).
Рис. 5. Метаболизм костной ткани: щелочная фосфатаза костной ткани
*p
На фоне приема плацебо сывороточные титры ЩФКТ остаются стабильными, в то время как лечение экстрактом цимицифуги BNO 1055 обусловливает достоверное повышение значения этого показателя через 12 недель по сравнению с плацебо и конъюгированными эстрогенами. Представлены средние значения величин с поправкой на исходные, центральная разность и стандартные ошибки среднего
Цитология эпителия влагалища
Если на фоне приема конъюгированных эстрогенов численность пула поверхностных клеток значительно увеличивается по сравнению с плацебо (рРис. 6. Цитология эпителия влагалища
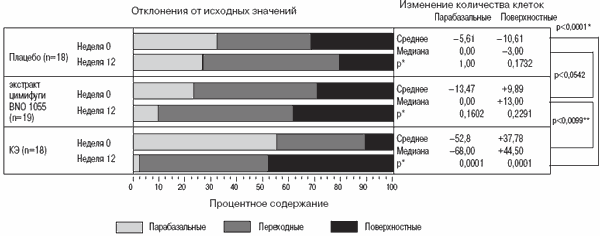
На фоне лечения конъюгированными эстрогенами происходит достоверное увеличение численности пула поверхностных клеток по сравнению с плацебо и экстрактом цимицифуги BNO 1055. Через 12 недель от начала приема экстракта цимицифуги BNO 1055 численность этого пула клеток несколько возрастает до почти достоверной разницы по сравнению с плацебо. В случае плацебо количество поверхностных клеток через 12 недель продолжало сокращаться. Представлены значения Р (обобщенного рангового критерия Вилкоксона) в сравнении с плацебо (*) и экстрактом цимицифуги BNO 1055 (**). КЭ – конъюгированные эстрогены
Метаболизм липидов
Экстракт цимицифуги BNO 1055 и конъюгированные эстрогены не оказывали заметного влияния на концентрацию холестерина в сыворотке крови (общий холестерин, ЛПВП, ЛПНП).
В отличие от плацебо у женщин, получавших конъюгированные эстрогены и экстракт цимицифуги BNO 1055, уровень триглицеридов в сыворотке крови был резко повышен (рис. 7).
Рис. 7. Метаболизм липидов: триглицериды
*p
Через 4 недели от начала лечения конъюгированными эстрогенами и экстрактом цимицифуги BNO 1055 наблюдается достоверное повышение сывороточных титров триглицеридов. Представлены средние значения величин с поправкой на исходные, центральная разность и стандартные ошибки среднего
Подробные результаты клинического и биохимического анализов крови приводятся в таблице 4. Согласно полученным данным, проводимое лечение не имело выраженного системного действия. В частности, ни один из трех препаратов не повлиял на состояние свертывающей системы крови (т.е. на значения показателей активированного тромбопластинового времени в секундах и тромбо-пластинового времени в виде INR). Уровень печеночных ферментов (АСТ, АЛТ, γ–ГТ) также оставался стабильным, в случае применения экстракта цимицифуги BNO 1055 имела место тенденция к понижению их концентрации.
Таблица 4. Изменения параметров общего и биохимического анализов крови в ходе исследования (неделя 0 – неделя 12)
| Параметры | Плацебо | Экстракт цимицифуги BNO 1055 | Конъюгированные эстрогены |
| Общий анализ крови | |||
| Тромбоциты, 1010/л | 29,50±118,16 | -3,60±41,32 | 3,27±44,48 |
| Лейкоциты, 1010/л | 0,13±2,10 | 0,16±1,29 | -0,44±1,39 |
| Эритроциты, 107л | -0,11±0,31 | -0,12±0,35 | -0,08±0,31 |
| Гемоглобин, г/л | -5,40±12,21 | -3,92±6,26 | -3,00±6,70 |
| Гематокрит, % | -1,20±3,05 | -1,18±2,71 | -0,85±2,29 |
| Базофилы, % | -0,07±0,37 | 0,04±0,61 | 0,03±0,50 |
| Эозинофилы, % | -0,48±1,84 | -0,36±1,74 | 0,42±1,86 |
| Палочкоядерные нейтрофилы, % | 0,07±0,75 | 0,03±2,04 | -0,58±1,73 |
| Сегментоядерные нейтрофилы, % | 0,47±13,45 | 0,48±10,69 | 3,00±6,54 |
| Лимфоциты, % | 1,27±12,07 | 0,14±11,08 | -1,84±8,37 |
| Моноциты, % | -0,11±3,38 | 0,00±2,28 | -0,21±2,53 |
| Биохимический анализ крови | |||
| Глюкоза, моль/л | 0,32±1,21 | 0,15±0,94 | 0,07±0,70 |
| Мочевина, ммоль/л | -0,14±1,12 | -0,19±1,43 | 0,12±1,07 |
| Креатинин, мкмоль/л | 1,46±11,23 | 0,89±11,88 | 0,88±10,59 |
| Мочевая кислота, мкмоль/л | -41,71±63,94 | 4,00±38,12 | 9,32±67,98 |
| Общий билирубин, мкмоль/дл | -0,11±0,5 | 0,10±0,36 | -0,15±0,39 |
| Общий белок, г/л | 0,71±4,71 | -2,38±4,38 | -0,15±3,88 |
| Железо, мкмоль/л | 0,34±5,75 | 0,37±6,05 | -4,37±9,66 |
| АСТ, nkat/л | -52,00±131,29 | 135,00±259,73 | 0,91±115,118 |
| АЛТ, nkat/л | -83,00±174,06 | -165,50±240,67 | -23,18±301,05 |
| у–ГТ, nkat/л | -58,42±309,47 | -65,50±170,52 | 34,29±290,44 |
| ЩФ, nkat/л | 53,16±444,12 | 19,50±225,12 | 30,00±188,30 |
| Натрий, ммоль/л | 1,34±4,39 | 1,64±3,46 | 0,16±3,17 |
| Калий, моль/л | -0,03±0,33 | 0,25±0,50 | -0,05±0,44 |
| Кальций, нмоль/л | -0,01±0,17 | 0,02±0,17 | -0,03±0,18 |
| Тромбопластиновое время, сек | -0,29±3,24 | -0,58±5,25 | -1,53±7,61 |
| Тромбопластиновое время, INR | -0,01±0,15 | -0,02±0,08 | -0,4±0,20 |
| Данные представлены как среднее ± стандартное отклонение |
Артериальное давление и частота сердечных сокращений
Клинически значимых эффектов проводимой терапии в отношении артериального давления и частоты сердечных сокращений в положении сидя и стоя выявлено не было. В группе плацебо у 1 пациентки возникло головокружение. Головокружение, головные боли и гипертензия, появившиеся у одной из испытуемых группы принимавших экстракт цимицифуги BNO 1055, были отнесены за счет побочного действия лекарственного препарата. И в том, и в другом случае артериальное давление и частота сердечных сокращений оставались постоянными.
По прошествии 12 недель лечения средняя масса тела достоверно не изменялась.
Обсуждение
В ходе проведения этого исследования, дизайн которого был разработан с целью изучить терапевтическую эффективность препарата экстракта цимицифуги BNO 1055 в отношении проявлений климакса, оценивали вторичные параметры. Благоприятные исходы по первичному параметру оказались сопоставимы с эффектами конъюгированных эстрогенов и лучше результатов в группе плацебо [18]. Тем более удивительным стал факт явной эффективности лечения несмотря на то, что проводимое исследование было небольшим и достаточно краткосрочным. По результатам более ранних экспериментов по использованию другого экстракта цимицифуги [30] и опытов на животных с применением препарата экстракта цимицифуги BNO 1055 [22] выявлено статистически достоверное снижение концентрации ЛГ на фоне проводимой терапии. Следовательно, регрессия симптоматики климактерического синдрома может быть опосредована на уровне гипоталамуса, в частности, серотонинергическим действием вытяжек экстракта цимицифуги [23]. В ходе настоящего исследования не удалось пронаблюдать супрессивный эффект экстракта цимицифуги BNO 1055 в отношении ЛГ, однако и конъюгированные эстрогены были лишены способности тормозить высвобождение ЛГ из гипофиза в течение всего периода проведения испытаний. У женщин в постменопаузе эстрогены уменьшают сывороточную концентрацию ФСГ во все три момента времени, а для экстракта цимицифуги BNO 1055 этот эффект не характерен. Известно, что пульсирующий выброс гонадотропин–рилизинг–гормона – один из факторов патогенеза приливов [31], причем активность этого гормона селективно модулируют гипофизарные ЛГ или ФСГ [32]. Не исключено, что именно это лежит в основе механизма, благодаря которому эстрогены способствуют снижению частоты приливов, а серотонинергические [23] и допаминергические [21] эффекты цимицифуги могут опосредовать другие, еще не описанные механизмы.
Повышение титров иммунореактивного Е2 на фоне приема конъюгированных эстрогенов в процессе их метаболизма вполне прогнозируемо, поскольку антисыворотка, используемая для определения Е2, дает перекрестные реакции с эквин–конъюгированными эстрогенами или их метаболитами. В случае экстракта цимицифуги BNO 1055 уровень иммунореактивного Е2 остается постоянным, свидетельствуя тем самым о том, что этот растительный препарат не содержит эстрогеноподобных соединений с иммуносупрессивными свойствами. В опытах in vitro продемонстрировано, что компоненты этой вытяжки цимицифуги не взаимодействуют с рекомбинантными человеческими белками рецепторов эстрогенов α и β [21]. Однако умеренное снижение концентрации ФСГ, зарегистрированное на начальном этапе лечения и сходное с эффектом конъюгированных эстрогенов, позволяет предположить, что экстракт цимицифуги BNO 1055 может действовать аналогично эстрогенам, но через Е2-связывающие белки (а не ЭРа и ЭР(5), обнаруживаемые в эндометрии свиней и человека [21].
Как и ожидалось, содержание ГСПГ значительно повышается на фоне лечения конъюгированными эстрогенами по сравнению с плацебо, а у женщин, принимавших экстракт цимицифуги BNO 1055, этот эффект отсутствует. Кроме того, в группе получавших растительный препарат прослеживается отчетливая тенденция к уменьшению сывороточного уровня печеночных ферментов (АСТ, АЛТ, у–ГТ), а лечение конъюгированными эстрогенами не вызывает таких последствий. В совокупности эти данные указывают на то, что в процессе лечения экстрактом цимицифуги BNO 1055 функции печени и, в частности, обменные процессы, имеющие место в ее паренхиме, не страдают.
Влияние экстракта цимицифуги BNO 1055 в отношении маркеров метаболизма костной ткани характеризуется анаболическим действием. Остеобласты и остеокласты, отвечающие за образование и резорбцию костной ткани, чувствительны к эстрогенам [33-35]. У женщин, находящихся в ре про дуктивной фазе цикла или получающих заместительную гормональную терапию эстрогенами, активность клеток обоих типов сбалансирована: остеокласты разрушают костную ткань, а остеобласты способствуют остеогенезу Механизмы, лежащие в основе метаболизма костной ткани и развития остеопороза из-за недостатка эстрогенов, изучались весьма активно, причем установлено, что у животных после овариэктомии и женщин в постменопаузе активность как остеобластов, так и остеокластов возрастает, однако превалируют функции резорбтивных остеокластов, а это влечет за собой снижение минеральной плотности костей и остеопороз [36]. Таким образом, содержание маркеров активности остеобластов и остеокластов у женщин в постменопаузе и у крыс после удаления яичников увеличивается. Эстрогены способны компенсировать этот дефект и уменьшить тем самым значения суррогатных показателей. Ранее доказана терапевтическая выгода применения экстрактов цимицифуги в отношении маркеров костной ткани в крови и моче, а также минеральной плотности костей у крыс после овариэктомии [19,25], а результаты настоящего исследования подтверждают наличие аналогичного эффекта у женщин в постменопаузе. Препарат цимицифуги BNO 1055 оказывает явное положительное влияние на суррогатные показатели метаболизма костной ткани. Так, критерием остеогенеза (т.е. активности остеобластов) служит ЩФКТ. По сравнению с плацебо и конъюгирован-ными эстрогенами экстракта цимицифуги BNO 1055 резко повышает концентрацию ЩФКТ, отражая тем самым усиление активности остеобластов, которое происходит в первые 4 недели от начала терапии и становится статистически значимым к 12–й неделе. Насколько нам известно, это первое свидетельство в пользу существования у растительных препаратов способности индуцировать остеогенез. Степень резорбции костной ткани, опосредованной остеокластами, оценивают по сывороточной концентрации С–концевых продуктов метаболизма коллагена 1 α 1, специфичного для костной ткани (т.н. CrossLaps). В группе плацебо содержание CrossLaps незначительно нарастает, в то время как прием конъюгированных эстрогенов ассоциируется с заметным уменьшением содержания CrossLaps по сравнению с плацебо, иллюстрируя тем самым хорошо известное антирезорбтивное действие эстрогенов в отношении костной ткани. В группе получавших экстракт цимицифуги BNO 1055 уровень CrossLaps оказался промежуточным (т.е. между значениями показателя в группе плацебо и в группе принимавших эстрогены), что также может указывать на незначительное снижение активности остеокластов с возможным положительным влиянием на минеральную плотность костей. Непродолжительный период лечения (12 недель) недостаточен для того, чтобы анализировать минеральную плотность костей, но из опытов на крысах известно, что эффекты в отношении суррогатных показателей метаболизма костной ткани отражают и состояние минеральной плотности костей [19,25]. Чтобы окончательно подтвердить эти предположения, необходимо провести более длительные исследования в объемной выборке больных с вычислением минеральной плотности костей.
У женщин в постменопаузе, которые не принимают конъюгированных эстрогенов, в эпителии влагалища преобладают парабазальные клетки, а у пациенток, получающих эстрогены – поверхностные клетки [29]. Поскольку в процессе настоящего исследования не были использованы никакие другие эстрогены, скорее всего, сдвиг «индекса зрелости» в пользу промежуточных и поверхностных клеток обусловливает именно изучаемый препарат. Активируя слизистую оболочку влагалища, эстрогены вызывают увеличение численности пула поверхностных клеток. Этот эффект эстрогенов хорошо известен, благодаря ему происходит снижение pH, что препятствует восходящему бактериальному инфицированию. При половом возбуждении эстрогены улучшают смазку. Влияние экстракта цимицифуги BNO 1055 выражено в меньшей степени относительно конъюгированных эстрогенов, тем не менее на фоне его применения численность пула поверхностных клеток также нарастала в масштабах, близких к статистически достоверным по сравнению с плацебо. Описанный эффект ассоциирован с явным уменьшением ощущения сухости во влагалище и сообщался ранее [18]. Аналогичные результаты были получены и в ходе некоторых (но не во всех) более ранних клинических исследованиях других препаратов цимицифуги [14,17]. Их можно наблюдать только у женщин в постменопаузе длительностью, по меньшей мере, 6 месяцев, не принимавших ранее никаких эстрогенов. Это может объяснить, почему в процессе некоторых клинических испытаний экстрактов цимицифуги с привлечением женщин в перименопаузальном периоде (когда уровень эндогенного эстрадиола еще продолжает колебаться) такое благоприятное влияние на цитологию эпителия влагалища отмечено не было [16].
У крыс с удаленными яичниками эстрогены резко снижают титры холестерина, ЛПВП и ЛПНП [37]. То же са мое происходит у женщин, находящихся на гормональной терапии [38]. Однако по результатам настоящего исследования такой эффект не выявлен. Ни конъюгированные эстрогены, ни экстракт цимицифуги BNO 1055 не затрагивали концентрацию холестерина, ЛПВП или ЛПНП. На фоне приема конъюгированных эстрогенов в некоторых случаях повышается содержание триглицеридов, что также было продемонстрировано в настоящем исследовании. Это не было связано, например, с поступлением триглицеридов с пищей, поскольку все анализы крови брались натощак. Нарастание уровня триглицеридов, по всей вероятности, отражает подъем титров липопротеинов очень низкой плотности, ассоциированных с риском атеросклероза. Но эстрогены обладают липолитическим и антилипотропным действием [39], и то же самое может быть справедливо в отношении экстрактов цимицифуги [19].
Терапия конъюгированными эстрогенами и экстрактом цимицифуги BNO 1055 не имела системного эффекта, что проявлялось в стабильном уровне показателей гемограммы, клинического и биохимического анализов крови, факторов свертывающей системы, а также постоянной величиной артериального давления и частоты сердечных сокращений, массой тела. Следует подчеркнуть, что оба вида лечения никак не повлияли на гемостаз. Ранее сообщалось о случае возникновения острой печеночной недостаточности на фоне применения цимицифуги, поэтому при проведении настоящего исследования отдельное внимание уделялось определению концентрации печеночных ферментов. Заре гистрировано незначительное снижение титров АСТ, АЛТ и γ–ГТ, что не доказывает наличия у экстракта цимицифуги BNO 1055 гепатотоксических свойств. Препарат хорошо переносился и не вызывал значимых (по сравнению с плацебо) побочных эффектов.
Некоторые аспекты клинического действия экстракта цимицифуги BNO 1055 аналогичны таковым конъюгированных эстрогенов, в то время как другие отличаются качественно и/или количественно. Ранее было показано, что проводимое лечение купирует многие проявления климакса [18], а по своей эффективности оно сопоставимо с приемом конъюгированных эстрогенов. Оба препарата имели преимущества перед плацебо [18]. Данные, полученные нами в опытах in vitro, свидетельствуют о том, что экстракт цимицифуги BNO 1055 способен взаимодействовать с цитозольными местами (сайтами) связывания эстрогенов человека, крыс и свиней, но не с рекомбинантными белками α– и β–рецепторов эстрогенов (ЭРα и ЭРβ) человека [21]. Механизмы действия препаратов экстракта цимицифуги пока остаются неразгаданными, но, возможно, они опосредованы органоспецифическими эстроген-рецепторными стимулирующими или подавляющими генами. Это может открыть принципиально иные возможности в создании лекарственных препаратов, обладающих органоспецифическим эстрогеноподобным (а следовательно – благоприятным) селективным модулирующим влиянием на Э Р.
Непонятно, одинаковые ли свойства имеют препараты цимицифуги, предлагаемые разными производителями. Есть данные, что водно–спиртовой экстракт отличается от изопропанолового (при тонкослойной хроматографии этих экстрактов получается разное количество полос) [40]. Из–за того, что активные действующие компоненты цимицифуги не определены, остается неизвестным, различаются ли свойства у разных препаратов. В любом случае, назначать следует лишь тот конкретный препарат, эффективность которого доказана клиническими испытаниями.
Заключение
Таким образом, ранее уже сообщалось о благоприятном воздействии экстракта цимицифуги BNO 1055 и конъюгированных эстрогенов на симптоматику климактерического синдрома [18]. Нами же было впервые продемонстрировано, что экстракт цимицифуги BNO 1055 может препятствовать развитию остеопороза, о чем свидетельствуют значения суррогатных сывороточных маркеров метаболизма костной ткани. Кроме того, для этого растительного препарата характерно эстрогеноподобное влияние на слизистую оболочку влагалища. Стабильная концентрация печеночных ферментов и содержание факторов свертывающей системы крови указывают на отсутствие у экстракта цимицифуги BNO 1055 гепатотоксического действия.
Реферат подготовлен Е.Б. Третьяк по материалам статьи W. Wuttke, C. Gorkow, D. Seidlova–Wuttke «Effects of black cohosh (Cimicifuga racemosa) on bone turnover, vaginal mucosa, and various blood parameters in postmenopausal women: a double–blind, placebo–controlled, and conjugated estrogens–controlled study» Menopause: The Journal of The North American Menopause Society 2006, Vol. 13, No 2: 185–196
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
микрокристаллическая целлюлоза (носитель), экстракт соевых бобов, экстракт корневищ цимицифуги, холекальциферол, магниевая соль стеариновой кислоты (агент антисле-живающий), оболочка таблетки: гидроксипропилметилцеллюлоза (загуститель), полиэтиленгликоль (стабилизатор), диоксид титана (краситель), оксид железа красный (краситель), оксид железа желтый (краситель).
(1 таблетка) содержит, мг
Изофлавоны 10 мг (±20%)
Витамин D3 5 мкг/200 МЕ (±20 %)
Цимицифуга — это травянистое растение, ценность которого люди обнаружили уже много лет назад. Цимицифугу использовали для нормализации менструального цикла, а также облегчения климактерических симптомов, которые преподносят неприятные сюрпризы в новый для женщины период. В современном мире области применения цимицифуги только расширились — благодаря научным исследованиям стало известно, что это растение оказывает положительное влияние не только на женское здоровье, но и на нервную и сердечно-сосудистую системы.
«Цимицифуга комплекс» — биологически активная добавка к пище, которая способствует нормализации менструального цикла, а также облегчению симптомов проявления климакса.
Суточная доза содержит Рекоменд.1/ адекватный уровень сут-ого потр-ния Верхний допуст. уровень потр-ния2 % рекоменд./ 2 уровня
Изофлавоны 10 мг (±20%) 50 мг2 150 мг 202 (162 — 242)
Витамин D3 5 мкг/200 МЕ (±20 %) 5 мкг (200 МЕ)1 15 мкг (600 МЕ) 1001 (801 — 1201*)
Информация о биологически активных веществах и их свойствах:
Соя — богатый источник высококачественных белков, в состав которых входят все незаменимые аминокислоты, без холестерина и с меньшим по сравнению с продуктами животного происхождения содержанием насыщенных жиров.
Другими важными биологически активными соединениями соевых бобов являются изофлавоны — фитохимические вещества, часто называемые фитоэстрогенами. По своей структуре они схожи (но не идентичны) с одним из основных половых гормонов женского организма — эстрогеном. Фитоэстрогены способны связываться с теми же рецепторами, что и эстрогены, с той лишь разницей, что действие фитоэстрогенов значительно слабее.
Изофлавоны благоприятно влияют на уровень сахара и холестерина в крови, тем самым способствуя поддержке сердечно-сосудистой системы. Их прием способствует поддержанию плотности костей у женщин в период менопаузы.
Экстракт цимицифуги содержит различные полезные соединения, такие как тритер-пеновые гликозиды, фенолы, алкалоиды, органические кислоты. Экстракт оказывает положительное влияние на организм: способствует снижению проявления симптомов климакса, «приливов», повышенного потоотделения, эмоционального напряжения.
Холекальциферол (витамин D3) — это жирорастворимый витамин, играющий важную роль в физиологии человека, особенно — в период менопаузы у женщин, когда происходит изменение уровня определенных половых гормонов, следствием чего может стать значительное снижение уровня витамина D3 в организме. Холекальциферол положительно влияет на сердечно-сосудистую, нервную и костную системы, способствует повышению иммунитета и нормализации работы щитовидной железы.
Повышенная чувствительность к цимицифуге; эстрогензависимые опухоли; беременность, период грудного вскармливания; возраст до 18 лет; алкоголизм (для лекарственных форм, в состав которых входит этанол).
С осторожностью: нарушения функции печени, эпилепсия, черепно-мозговая травма, заболевания головного мозга
При гастритах с повышенной секрецией применять с осторожностью.
Продолжительность лечения не должна превышать 3 месяцев без консультации врача.
При наступлении беременности необходимо прекратить прием средства и обратиться к врачу.
При изменении характера менструального цикла (нарушение или возобновление менструаций) необходимо проконсультироваться с врачом.
Биологически активная добавка к пище.
Не является лекарственным средством.
Перед применением рекомендуется проконсультироваться с врачом.
Средство растительного происхождения. Циклоартановые тритерпеноиды, в т.ч. шенгманол, ацетилшенгманол, оказывают гипотензивное и седативное действие, повышают сократимость миокарда, не влияя на ЧСС. В сочетании с сапонинами и фитостерином они проявляют гиполипидемическую, антиоксидантную и ангиопротекторную активность.
Внешний вид упаковки может отличаться от фотографии
Средняя цена в аптеках
449 ₽
Среди
2914
аптек,
подключенных к Ютеке в вашем регионе
Оплата и способы получения
в Москве
Самовывоз
Сегодня бесплатно
из 125 аптек
Завтра или позже бесплатно
из 2914 аптек
Оплата картой или наличными в аптеке
Доставка
Конкретный срок и стоимость доставки зависят от вашего адреса
Информация о товаре
Форма выпуска:
таблетки, покрытые оболочкой
Первичная упаковка:
блистер
Количество в упаковке:
30 шт.
Страна:
Россия
Страна производства может отличаться, проверяйте при получении заказа
Инструкция на Цимицифуга Комплекс таблетки, покрытые оболочкой, 30 шт.
Состав
Микрокристаллическая целлюлоза (носитель), экстракт соевых бобов, экстракт корневищ цимицифуги, холекальциферол, магниевая соль стеариновой кислоты (агент антисле-живающий), оболочка таблетки: гидроксипропилметилцеллюлоза (загуститель), полиэтиленгликоль (стабилизатор), диоксид титана (краситель), оксид железа красный (краситель), оксид железа желтый (краситель).
(1 таблетка) содержит, мг:
- Изофлавоны 10 мг (±20%)
- Витамин D3 5 мкг/200 МЕ (±20 %)
Описание
Цимицифуга — это травянистое растение, ценность которого люди обнаружили уже много лет назад. Цимицифугу использовали для нормализации менструального цикла, а также облегчения климактерических симптомов, которые преподносят неприятные сюрпризы в новый для женщины период.
В современном мире области применения цимицифуги только расширились — благодаря научным исследованиям стало известно, что это растение оказывает положительное влияние не только на женское здоровье, но и на нервную и сердечно-сосудистую системы.
Информация о биологически активных веществах и их свойствах:
Соя — богатый источник высококачественных белков, в состав которых входят все незаменимые аминокислоты, без холестерина и с меньшим по сравнению с продуктами животного происхождения содержанием насыщенных жиров.
Другими важными биологически активными соединениями соевых бобов являются изофлавоны — фитохимические вещества, часто называемые фитоэстрогенами. По своей структуре они схожи (но не идентичны) с одним из основных половых гормонов женского организма — эстрогеном. Фитоэстрогены способны связываться с теми же рецепторами, что и эстрогены, с той лишь разницей, что действие фитоэстрогенов значительно слабее.
Изофлавоны благоприятно влияют на уровень сахара и холестерина в крови, тем самым способствуя поддержке сердечно-сосудистой системы. Их прием способствует поддержанию плотности костей у женщин в период менопаузы.
Экстракт цимицифуги содержит различные полезные соединения, такие как тритер-пеновые гликозиды, фенолы, алкалоиды, органические кислоты. Экстракт оказывает положительное влияние на организм: способствует снижению проявления симптомов климакса, «приливов», повышенного потоотделения, эмоционального напряжения.
Холекальциферол (витамин D3) — это жирорастворимый витамин, играющий важную роль в физиологии человека, особенно — в период менопаузы у женщин, когда происходит изменение уровня определенных половых гормонов, следствием чего может стать значительное снижение уровня витамина D3 в организме. Холекальциферол положительно влияет на сердечно-сосудистую, нервную и костную системы, способствует повышению иммунитета и нормализации работы щитовидной железы.
Цимицифуга Комплекс: Показания
В качестве биологически активной добавки к пище — источника изофлавонов, дополнительного источника витамина D3 (в 1 таблетке 200 МЕ).
Способ применения и дозы
Взрослым по 1 таблетке в день во время еды.
Продолжительность приема — 1 месяц. При необходимости прием можно повторить.
Цимицифуга Комплекс: Противопоказания
Индивидуальная непереносимость компонентов, беременность, кормление грудью.
Особые указания
Биологически активная добавка (БАД) к пище
Не является лекарственным средством.
Перед применением рекомендуется проконсультироваться с врачом.
Характеристики
Торговое название
Цимицифуга Комплекс
Форма выпуска
таблетки, покрытые оболочкой
Первичная упаковка
блистер
Противопоказания БАД
БАД. НЕ ЯВЛЯЕТСЯ ЛЕКАРСТВЕННЫМ СРЕДСТВОМ
Представлено описание активных веществ лекарственного препарата. Описание препарата основано на официально утвержденной инструкции по применению от компании-производителя. Приведенное описание носит исключительно информационный характер и не может быть использовано для принятия решения о возможности применения конкретного лекарственного препарата.
Цены в аптеках на Цимицифуга Комплекс таблетки, покрытые оболочкой, 30 шт.
История стоимости Цимицифуга Комплекс таблетки, покрытые оболочкой, 30 шт.
минимальнаясредняямаксимальная
Указана средняя стоимость товара в аптеках региона Москва и МО за период и разница по сравнению с предыдущим периодом
Цены Цимицифуга Комплекс и наличие в аптеках в Москве
таблетки, покрытые оболочкой, 30 шт.
Достоинства: рекомендую!!! не одни таблетки климаксные не давали какого эффекта. я начала вставать , заниматься делами домашними без потения. советую. приливы можно сказать пропали. третья упаковка пошла. Полет нормальный. пробуйте
Недостатки: нет
Достоинства: Я так поняла, имеют накопительный эффект. Приливы стали меньше , после недельного приема!
Недостатки: Чтоб купить, нужно еще поискать. Проехать полгорода)
Комментарий: Рекомендую. Цена приятная.
Достоинства: Хорошо помогает от приливов.Заметила это после того,как пропила один курс. Через какое то время, приливы начались с удвоенной силой, побежала за новой «дозой», в течении недели всё нормализовалось, теперь без них уже не могу) По другим критериям(настроение, вес, сон и тд) судить не могу, не увидела взаимосвязи.
Смотреть все отзывы
Популярные товары в категории
Популярные товары в Ютеке
Купить Цимицифуга Комплекс, таблетки, покрытые оболочкой, 30 шт. в Москве с доставкой в аптеку или домой, сделав заказ через Ютеку
Цена Цимицифуга Комплекс, таблетки, покрытые оболочкой, 30 шт. в Москве от 245 руб. на сайте и в приложении
Подробная инструкция по применению Цимицифуга Комплекс, таблетки, покрытые оболочкой, 30 шт.
Информация на сайте не является призывом или рекомендацией к самолечению и не заменяет консультацию специалиста (врача), которая обязательна перед назначением и/или применением любого лекарственного препарата.
Дистанционная торговля лекарственными препаратами осуществляется исключительно аптечными организациями, имеющими действующую лицензию на фармацевтическую деятельность, а также разрешение на дистанционную торговлю лекарственными препаратами. Дистанционная торговля рецептурными лекарственными препаратами, наркотическими и психотропными, а также спиртосодержащими лекарственными препаратами запрещена действующим законодательством РФ и не осуществляется.
На информационном ресурсе применяются
рекомендательные технологии
.
Ежегодно в мире регистрируется около 11 млн новых случаев заболевания раком, более 850 тыс. из них приходится на поражение органов женской половой сферы. Сложные хирургические вмешательства, специальные методы лечения онкологических больных влекут за собой тяжелые изменения в организме. И если успехи, достигнутые в лечении злокачественных новообразований, способствуют увеличению числа излеченных больных, то перед онкологами встает очередная серьезная задача — улучшение качества жизни таких пациенток.
Следствием проводимого лечения онкологических больных является проявление у них посткастрационного синдрома.
Посткастрационный синдром — комплекс соматопсихических проявлений, возникающих у женщин репродуктивного возраста вследствие проведения у них оперативной (удаление яичников), лучевой или лекарственной кастрации. Вегетососудистые нарушения возникают практически у каждой 3-й женщины после надвлагалищной ампутации матки без придатков и в 2 раза чаще — при экстирпации матки с придатками. Если естественный климактерий — процесс, как правило, плавный, когда включаются механизмы адаптации организма, то искусственный — это всегда стресс [1].
Особенно остро он протекает в молодом возрасте, когда женщина ни физиологически, ни психологически не подготовлена к наступлению менопаузы.
Выпадение гормональной функции яичников вызывает сложные реакции адаптации в нейроэндокринной системе. Внезапное снижение уровня половых гормонов приводит к нарушению секреции нейротрансмиттеров в подкорковых структурах мозга, обеспечивающих координацию кардиоваскулярных, респираторных, температурных реакций. Это вызывает патологические симптомы, весьма сходные с симптомами, возникающими при климактерическом синдроме. Нарушения секреции нейропептидов гипоталамуса (люлиберин, тиролиберин, кортиколиберин и др.) изменяют функцию эндокринных желез, особенно надпочечников, в корковом веществе которых усиливается образование глюкокортикоидов.
После кастрации андрогены коры надпочечников являются единственным источником синтеза эстрогенов. Уменьшение образования андрогенов приводит к снижению синтеза эстрогенов и затрудняет процессы адаптации организма. В щитовидной железе нарушается синтез Т3 и Т4.
Посткастрационный синдром у оперированных женщин репродуктивного возраста развивается в 80% наблюдений, часто он протекает тяжело, с утратой трудоспособности. Основными клиническими проявлениями его служат вегетативно-сосудистые симптомы — «приливы жара». Они могут сопровождаться усиленным потоотделением, учащением пульса, ощущением нехватки воздуха, чувством страха, иногда полуобморочным состоянием, судорогами. Эти симптомы усиливаются ночью, в жаркое время года, особенно при нервном возбуждении. Частоту и интенсивность приливов считают показателем тяжести посткастрационного синдрома. Они развиваются уже через 2—3 нед. после операции и достигают пика своего развития через 2—3 мес. [2].
К числу обменно-эндокринных нарушений, связанных с посткастрационным синдромом, относят также ожирение, гиперхолестеринемию. Изменения гормонального баланса обусловливают нарушения липидного обмена и развитие атеросклероза. С метаболическими нарушениями связывают также трофические изменения в наружных и внутренних половых органах, мочевом пузыре, уретре. У таких больных очень часто развиваются кольпиты, появляются трещины, лейкоплакии, крауроз вульвы. Наступают атрофические изменения в молочных железах, происходит замещение железистой ткани соединительной и жировой.
Частым спутником вегетативно-сосудистых нарушений посткастрационного синдрома является остеопороз. Остеопороз — это системное заболевание скелета, характеризующееся снижением плотности костной массы и ухудшением архитектоники костной ткани, вследствие чего повышается хрупкость костей и подверженность переломам.
Ф. Элбрайт в серии клинических очерков среди различных причин развития остеопороза выдвигал недостаточность половых гормонов.
В своих наблюдениях он показал, что среди пациентов с остеопорозом было значительно больше женщин с овариэктомией, чем ожидалось. Операции у них почти всегда были выполнены в более молодом возрасте, чем возраст наступления естественной менопаузы. Резкое снижение синтеза эстрогенов у женщин после удаления яичников — одна из основных причин развития остеопороза.
Эстрогены оказывают как прямое, так и опосредованное влияние на метаболизм костной ткани. Они имеют высокоспецифичные рецепторы на остеокластах. Эти клетки являются органом-мишенью для эстрогенов. Опосредованное действие заключается в стимулировании образования в организме ряда высокоактивных биологических веществ, участвующих в процессе ремоделирования.
Под влиянием эстрогенов активность остеокластов снижается, воздействие на остеобласты носит опосредованный характер.
Эстрогены оказывают на костную ткань защитное действие против резорбции. Защитное действие может быть также опосредовано кальцитонином, секреция которого стимулируется эстрогенами. Снижение продукции половых гормонов делает кости более чувствительными к паратиреоидному гормону. Эстрогены являются его физиологическим антагонистом и сдерживают вызываемую им резорбцию костной ткани.
Эстрогены поддерживают баланс между активностью остеобластов и остеокластов в процессе ремоделирования за счет снижения резорбции и вторичного понижения образования костной ткани. При дефиците эстрогенов одновременно утрачиваются как органические, так и минеральные элементы костной ткани, что типично для остеопороза.
Остеопороз у женщин после удаления яичников развивается постепенно и поэтому долгое время может оставаться незамеченным. Характерными симптомами являются боли в поясничном и грудном отделах позвоночника, медленное уменьшение роста с соответствующими изменениями осанки, переломы при минимальных травмах. При этом риск возникновения перелома позвоночника возрастает в 9 раз, а шейки бедренной кости — в 3 раза по сравнению с таковыми у здоровых женщин того же возраста. И если у большинства больных в течение первого года после операции наблюдается обратное развитие патологических симптомов, то у 25% пациенток они сохраняются в течение 5 лет и более, а остеопороз продолжает прогрессировать даже после исчезновения других клинических проявлений.
Исходя из этого, становится ясным, какое неблагоприятное воздействие оказывает кастрация на практически все системы организма молодой женщины.
Длительное время заместительная гормональная терапия (ГТ) являлась стандартным лечением проявлений посткастрационного синдрома и остеопороза. Однако из-за повышенного риска развития рака молочной железы (РМЖ) и сердечно-сосудистых заболеваний, таких как инфаркт миокарда или инсульт, перевешивающих доказанную эффективность ГТ в отношении проявлений симптомов климакса, пациентки все реже соглашаются на этот вид лечения. Особенно это касается пациенток с отягощенной онкологической наследственностью, так как риск возникновения индукции опухолевого заболевания часто не позволяет проводить заместительную ГТ продолжительное время, необходимое для достижения полного клинического эффекта. В связи с этим и врачи, и больные стараются найти альтернативные эстрогенам препараты, прием которых позволил бы купировать симптомы менопаузы и поддерживать прочность костной ткани. Такой альтернативой мог бы быть селективный модулятор рецептора эстрогенов (РЭ), который подавлял бы проявление климакса и оказывал бы положительное влияние на костную ткань. При этом он был бы лишен неблагоприятных эффектов в отношении ткани молочной железы и матки, характерных для эстрогенов.
В этом отношении представляются весьма перспективными препараты, созданные на основе корневищ растения цимицифуга кистевидная (Cimicifuga racemosa, клопогон кистевидный), поскольку есть убедительные данные о том, что использование специальных экстрактов из корневищ этого растения облегчает симптоматику посткастрационного синдрома и улучшает метаболизм в костной ткани.
Исследования на доклиническом этапе, проведенные за последние 10 лет, позволили больше узнать об эффектах, оказываемых цимицифугой.
Первоначально предполагалось, что цимицифуга содержит вещества, структурно сходные со стероидными гормонами и обладающие эстрогенными свойствами, т.е. цимицифуга была отнесена к числу «фитоэстрогенных» растений. Однако далее в опытах in vitro по связыванию экстракта цимицифуги с рекомбинантными ЭР (ЭРα и ЭРβ) было установлено, что экстракт не связывается ни с одним из двух подтипов ЭР, но замещает радиоактивно меченный 17β-эстрадиол (Е2) в цитозольных препаратах матки свиньи и эндометрия человека. Такая активность цимицифуги объясняется, возможно, тем, что какие-то компоненты экстракта цимицифуги способны взаимодействовать с невыявленным эстроген-связывающим белком.
Согласно результатам экспериментов на грызунах, экстракт цимицифуги не оказывает уретеротропного действия. На основании этих данных был сделан вывод о том, что экстракты цимицифуги не содержат эстрогеноподобных компонентов [1].
Особое место у исследователей занимает вопрос о безопасности использования препаратов цимицифуги у больных с эстрогенозависимыми опухолями, в первую очередь РМЖ. К настоящему времени опубликованы многие исследования, посвященные выявлению стимулирующего влияния цимицифуги на линии клеток эстрогенозависимых опухолей (например, РМЖ MCF-7) и в различных тест-моделях на животных. С учетом совокупности полученных результатов принято считать, что цимицифуга не демонстрирует эстрогенной активности или пролиферативных эффектов в отношении возникновения или роста эстрогенозависимых опухолей. Это же подтверждается и исследованиями по безопасности применения цимицифуги [3—5]. В современных монографиях по цимицифуге кистевидной (ESCOP, ВОЗ) не указаны риски применения ее в отношении эстрогенозависимых опухолей и эстрогенозависимые опухоли не приводятся в качестве противопоказаний [6, 7]. Тем не менее инструкции по применению практически всех препаратов цимицифуги содержат противопоказания по этому пункту.
В соответствии с современной установкой на то, что каждый растительный препарат обладает уникальным «качеством», включающим в себя и стандартизованность препарата, и его фармакологические эффекты, считается, что среди растительных препаратов принципиально не может быть генериков, поэтому при обсуждении тех или иных эффектов препаратов цимицифуги внимание стали обращать на свойства конкретных экстрактов, содержащихся в них. Среди многих экстрактов цимицифуги одним из наиболее изученных является экстракт цимицифуги BNO 1055*. Установлено, что у крыс экстракт цимицифуги BNO 1055 оказывает благоприятное воздействие на гипоталамус, подавляя пульсирующее высвобождение лютеинизирующего гормона (ЛГ), а возможно — и приливы. Экстракты цимицифуги BNO 1055 содержат компоненты, связывающие серотониновые рецепторы, и не исключено, что это и есть механизм, благодаря которому приливы ослабевают. Однако Е2 и экстракт цимицифуги BNO 1055 одинаковым образом модулируют экспрессию в костной ткани двух генов, регулируемых эстрогенами. Эффекты экстракта цимицифуги BNO 1055 и Е2 наблюдали в костной ткани у крыс после удаления яичников, недостаточность которых восполняли обоими препаратами на протяжении 12 нед. Оба препарата тормозили экспрессию генов IGF1 и TRAP. Все это указывает на то, что на фоне такого лечения активность остеобластов и остеокластов, повышенная вследствие выполнения овариэктомии, восстанавливается до нормальных значений. У грызунов, которым вводили Е2 и экстракт цимицифуги BNO 1055, Е2 практически полностью предотвращал более чем 50% потерю минеральной плотности костной ткани, в то время как у крыс, получавших экстракт цимицифуги BNO 1055, этот эффект оказался частичным, но все же значимым при сравнении с таковым в контрольной группе. Также продемонстрировано положительное влияние экстракта цимицифуги BNO 1055 на уровень маркеров метаболизма костной ткани и минеральную плотность бедренной кости.
Во влагалище Е2 обусловливает пролиферацию эпителия, что способствует выработке бактериями лактата с закислением среды, не допуская тем самым восходящего бактериального инфицирования матки. Тот же самый эффект, хотя и слабовыраженный, можно наблюдать у женщин, принимающих экстракт цимицифуги BNO 1055.
В опытах на крысах с удаленными яичниками показано наличие умеренного вагинотропного действия у экстракта цимицифуги BNO 1055. Эстрогены повышают активность системы свертывания крови, что может спровоцировать развитие тромбоэмболии. О наличии таких побочных эффектов у цимицифуги информации нет.
С учетом благоприятного влияния экстракта цимицифуги BNO 1055, а также отсутствия у него эстрогеноподобного действия в отношении молочных желез и эндометрия можно предположить, что этот препарат обладает органной селективностью, хотя ее механизмы пока не изучены. Эта активность не опосредована ни одним из двух описанных ЭР, но, возможно, связана со стимуляцией их активизирующих и/или подавляющих посредников.
Клиническая эффективность экстракта цимицифуги BNO 1055 в отношении психовегетативных симптомов менопаузального синдрома доказана результатами нескольких клинических исследований [1, 8]. Одно из них, проведенное В. Вуттке и соавт. [1], показало не только благоприятное воздействие препарата на симптоматику менопаузального синдрома, но и впервые продемонстрировало, что экстракт цимицифуги BNO 1055 может препятствовать развитию остеопороза.
Кроме того, было найдено лишь незначительное эстрогеноподобное влияние экстракта на слизистую оболочку влагалища. При этом во всех наблюдениях отмечалась стабильная концентрация печеночных ферментов и факторов свертывающей системы крови, что свидетельствовало об отсутст вии у препарата гепатотоксического действия.
Первое исследование безопасности для эндометрия длительного применения цимицифуги у женщин было проведено с экстрактом BNO 1055, срок лечения составил 12 мес [8]. Результаты исследования показали, что длительное лечение экстрактом BNO 1055 является безопасным для эндометрия по данным биопсий: не выявило гиперплазии эндометрия, характерной для применения эстрогенов. Плотность молочных желез в ходе лечения не изменилась, следовательно, риск развития РМЖ не увеличился. Кроме того, отсутствие существенных изменений содержания печеночных ферментов и гемостатических факторов свидетельствовало в пользу того, что данный экстракт не имеет подобных побочных эффектов. На основании изучения показателей, связанных с обменом костной ткани, можно определенно утверждать, что экстракт BNO 1055 обладает антирезорбтивной активностью. Наконец, снижение числа приливов на 80% отражает существенное субъективное улучшение, наступившее благодаря использованию экстракта ВNO 1055.
Имеется опыт применения цимицифуги и при посткастрационном синдроме. Так, А.А. Осипова и соавт. [9] изучили действие экстракта BNO 1055 в сочетании с препаратами кальция, использовавшихся в течение 3 мес. для лечения женщин репродуктивного возраста, перенесших гистерэктомию без придатков, на симптомы климактерического синдрома и маркеры костного ремоделирования. Оперативное лечение пациенткам было проведено в среднем за 1,5 года до исследования по поводу миомы матки или аденомиоза.
По результатам повторного обследования, проведенного через 3 мес., установлено, что только у 2 из 24 женщин прием цимицифуги не сопровождался снижением числа симптомов климактерического синдрома. Установлены достоверное уменьшение интенсивности жалоб на симптомы посткастрационного синдрома (индекс Куппермана), достоверное повышение уровня остеокальцина. Лечение хорошо переносилось и не имело побочных эффектов.
Особый интерес для онкологов-клиницистов представляют работы Т.Н. Коломойцевой и соавт. [2] и Л.В. Покуль и соавт. [10], в которых продемонстрирован опыт применения экстракта цимицифуги BNO 1055 у пациентов, перенесших специальное лечение по поводу онкогинекологической патологии в комплексной терапии с целью реабилитации и облегчения психовегетативной симптоматики.
Личный опыт применения препарата этими авторами продемонстрировал позитивные результаты, требующие, однако, в дальнейшем проведения дополнительных углубленных исследований.
В заключение следует отметить, что на сегодняшний день критерием эффективности лечения /онкологической патологии должно быть не только полное излечение больных, но и их полноценная реабилитация. Таким образом, каждый новый препарат дает шанс пациенту и врачу для достижения этой цели. Попытки использовать препараты цимицифуги для устранения симптомов посткастрационного синдрома продемонстрировали обнадеживающие результаты. Хотелось бы, чтобы сходные исследования были бы спланированы и проведены на большем количестве онкологических пациентов, нуждающихся в помощи. В случае достижения воспроизводимых положительных результатов и при благоприятном профиле безопасности вполне возможно, что цимицифуга займет свое место среди лекарств для лечения посткастрационного синдрома не только у пациентов с доброкачественными заболеваниями, но и при онкологической патологии.
ГУ РОНЦ им. Н.Н. Блохина РАМН, Москва.
Ю.Г. Паяниди, К.И. Жорданиа.
Познакомиться со всеми статьями и новостями по разделу «Фитониринг» вы можете по ссылке http://medicalexpress.ru/news/cat=6
Познакомиться со всеми статьями и новостями по разделу «Фитотека» вы можете по ссылке http://medicalexpress.ru/news/cat=10
Л И Т Е Р А Т У Р А
1. Вуттке В., Горков К., Сайдлова-Вуттке Д. Влияние цимицифуги (Cimicifuga racemosa) на метаболизм в костной ткани, состояние слизистой оболочки влагалища и различные параметры анализа крови у женщин в постменопаузе: двойное слепое плацебо-контролируемое и контролируемое конъюгированными эстрогенами исследование. Рус мед журн 2008;16(20):3—11.
2. Коломойцева Т.Н., Орлов О.А., Козлова Г.А. Опыт использования препарата из экстракта цимицифуги (Климадинон) в комплексной реабилитации больных раком шейки матки. ОЖРС 2008;(3):57—61.
3. Huntley A., Ernst E. A systematic review of the safety of black cohosh. Menopause 2003;10(1):58—64.
4. Low Dog T.L., Powell K.L., Weisman S.M. Critical evaluation of the safety of cimicifuga racemosa in menopausal symptom relief. Menopause 2003;10(4):299—313.
5. Mahady G.B. Is black cohosh estrogenic? Nutr Rev 2003;61(5):183—6.
6. European Scientific Cooperative on Phytotherapie (ESCOP). Cimicifuga racemosa. In: ESCOP Monographs, 2nd ed. 2003. p. 79—91.
7. World Health Organisation (WHO). Rhizoma cimicifugae racemosae. In: WHO Monographs on selected medicinal plants, 2002. Vol. 2. p. 55—65.
8. Рауш К., Брюкер К., Горков К., Вуттке В. Первые доказательства безопасности для эндометрия экстракта клопогона кистевидного (Actaea и Cimicifuga racemosa) CR BNO 1055. Рус мед журн2008;16(9);1—8.
9. Осипова А.А., Казначеева Т.В. Фитоэстрогены в реабилитации женщин, перенесших гистерэктомию без придатков. Пробл репрод 2007;(5):1—4.
10. Покуль Л.П., Порханова Н.В. Клиническая оценка применения препарата «Климадинон» у онкологических больных (анализ результатов экспериментального наблюдения). Врач 2007;(8):67—71.

ГБОУ ВПО Первый Московский государственный медицинский университет им. И.М.Сеченова; ФГБОУ ВПО Российский университет дружбы народов, Москва.
Резюме
В данном обзоре рассматриваются вопросы эффективности и безопасности фитогормонов в лечении климактерического синдрома.Особое внимание уделяется экстракту цимицифуги как лекарственному препарату, обладающему отличным от других средств этой группы спектром действия. Рассматриваются результаты современных исследований, согласно которым экстракт цимицифуги является не столько фитогормоном, сколько растительным вегетотропным средством, опосредующим свое действие через серотонинергические рецепторы. Высокая эффективность экстракта цимицифуги в купировании вазомоторных симптомов подтверждается сравнительными и плацебо-контролируемыми исследованиями. Вместе с тем отсутствие прямого взаимодействия с рецепторами эстрогенов определяет безопасность экстракта цимицифуги. Длительное применение лекарственных средств на основе экстракта цимицифуги не влияет на пролиферативные процессы в эндометрии и молочных железах. Препараты экстракта цимицифуги можно считать достойной альтернативой гормональной терапии в случаях, когда она невозможна или нежелательна.
Ключевые слова: постменопауза, фитогормоны, экстракт цимицифуги, приливы жара, эндометрий, молочная железа, безопасность.
Summary
The review deals with the effectiveness and safety of plant hormones in the treatment of menopausal syndrome. Particular attention is given to black cohosh extract as a drug with distinction from other drugs in this group thanks to its action spectrum. The results of modern studies show that black cohosh extract is not so much phytohormonal as a natural vegetotropic agent that mediates its effect through serotonergic receptors. High-performance of black cohosh extract in relieving vasomotor symptoms is confirmed by comparative, placebo-controlled trials. However, no direct interaction with estrogen receptors defines security of black cohosh extract use. Long-term use of drugs based on black cohosh extract has no effect on the endometrium proliferative processes and mammary glands. Use of black cohosh extract can be considered a viable alternative to hormone replacement therapy in cases where it is impossible or undesirable.
Key words: postmenopause, plant hormones, an extract of black cohosh, hot flushes, endometrial, breast, security.
Сведения об авторах
Кузнецова Ирина Всеволодовна – д-р мед. наук, проф., гл. науч. сотр. НИО женского здоровья НОК Центр женского здоровья ГБОУ ВПО Первый МГМУ им. И.М.Сеченова; проф. каф. акушерства и гинекологии ФГБОУ ВПО РУДН. E-mail: ms_smith@list.ru
Обзор размещен в издании “ГИНЕКОЛОГИЯ” | ТОМ 16 | №4
В периоде менопаузального перехода и постменопаузе большинство женщин испытывают негативные симптомы, значительно снижающие качество жизни [1–3]. К наиболее ранним признакам, которые могут появляться даже при регулярном менструальном цикле, относятся вазомоторные и психосоматические симптомы климактерического синдрома, в постменопаузе к ним присоединяются урогенитальные расстройства и трофические изменения кожи, а к 60 годам и в более позднем возрасте манифестируют метаболические последствия эстрогенного дефицита (остеопороз, атеросклероз) и болезнь Альцгеймера.
Основным проявлением климактерического синдрома [4] и одной из наиболее частых причин обращения к врачу в период перименопаузы [5] становятся приливы жара. Прилив представляет собой внезапное ощущение жара в области лица и шеи, распространяющееся по телу, часто сопровождающееся потливостью или ознобом и длящееся, как правило, несколько минут. Приливы ухудшают сон [6], настроение [7, 8], снижают качество жизни [9] и могут сигнализировать о начале эпизода тяжелого депрессивного расстройства или его рецидиве [10, 11].
Около 25% женщин не ощущают приливов жара в климактерическом периоде, примерно столько же испытывают изнуряющие приливы, неблагоприятно отражающиеся на профессиональной деятельности и повседневной жизни, у 50% женщин приливы отмечаются нечасто и выражены не столь значительно. Распространенность вазомоторных симптомов зависит от стадии менопаузального перехода, и ее пик приходится на раннюю менопаузу [12], со временем выраженность приливов уменьшается. Долгое время бытовала точка зрения, что приливы длятся в течение 0,5–2 лет [13], но Мельбурнское исследование здоровья женщин определило большую, до 5 лет, продолжительность приливов [14], а в метаанализе, включившем 10 исследований приливов жара, медиана продолжительности равнялась 4 годам [12]. В том же метаанализе было установлено, что у 10% женщин приливы сохраняются по истечении 12 лет после менопаузы. Наконец, недавно завершившееся 13-летнее проспективное когортное исследование [15] уточнило медиану продолжительности умеренно тяжелых и тяжелых приливов, которая составила 10,2 года, причем при включении в анализ женщин, испытывающих легкие приливы, медиана возросла до 11,6 года.
Механизм появления приливов до конца не понят. Доминирующая концепция полагает, что они обусловлены дефицитом эстрогенов, аргументируется данное положение частой ассоциацией вазомоторных симптомов со снижением уровня эстрогенов, а также успехами менопаузальной гормональной терапии (МГТ). Но существуют и контраргументы, среди которых такие факты, как частое отсутствие корреляции между уровнем эстрогенов и наличием приливов, возникновение вазомоторных жалоб при нормальной секреции эстрогенов даже на фоне овуляторного менструального цикла [16, 17]. Наилучшие предикторы вазомоторных симптомов в периоде менопаузального перехода не гормональные маркеры, а предшествующая история приливов жара и ночной потливости в репродуктивном периоде [17]. Эти данные позволяют предположить, что одного снижения эстрогенов для развития вазомоторных симптомов недостаточно, и иначе взглянуть на происхождение вазомоторных симптомов, в котором становится очевидной роль гипоталамуса и/или других компонентов центральной нервной системы, постепенно утрачивающих чувствительность к эстрогенам в результате физиологического старения или пережитых стрессов [18, 19].
Патофизиология прилива жара малоизучена [20], но ясно, что он возникает в результате нарушения процессов терморегуляции, которые обеспечивают центральная и вегетативная нервная система, и действие эстрогенов является не прямым, а опосредуется нейромедиаторами. Поэтому не удивляет связь приливов с нарушениями психической сферы. Так, предиктором приливов жара считается тревожность, и большинство женщин, обладающих повышенной тревожностью, склонны к более тяжелым приливам [21]. В одном из исследований, в котором сравнивали шкалу тревоги у женщин с приливами и без приливов жара, существенное повышение тревожности было обнаружено только у пациенток в пери- и постменопаузе, но не в пременопаузе [22]. Это обосновывает успешное применение с целью коррекции вазомоторных симптомов нейротропных препаратов, таких как антидепрессанты (преимущественно селективные ингибиторы обратного захвата серотонина) и противосудорожные средства (габапентин), не уступающие по эффективности эстрогенам [23].
Отражая интенсивность сосудистой реакции и эндотелиальной дисфункции в ответ на нейрогормональный дисбаланс, приливы жара становятся своеобразными предикторами сердечно-сосудистого риска [24], ассоциированными с субклиническими кардиоваскулярными заболеваниями [25, 26], повышением кальцификации стенки аорты [27], увеличением частоты ишемической болезни сердца [28]. Следует заметить, что с увеличением возраста растет частота других классических факторов риска сердечно-сосудистых заболеваний, в том числе распространенность артериальной гипертензии повышается от 30% среди женщин 45–55 лет до 50–70% у женщин старше 55 лет. Но менопаузальный переход также вносит вклад в формирование артериальной гипертензии, причем повышение артериального давления первично диагностируется у 20% женщин в перименопаузе и 37% женщин в постменопаузе [29], а степень повышения систолического артериального давления прямо зависит от выраженности и частоты приливов.
Таким образом, патологическое течение менопаузального перехода связано не только со снижением качества жизни, но и с повышением кардиоваскулярного риска, следовательно, лечение вазомоторных и психовегетативных симптомов надо рассматривать не только как средство улучшения общего самочувствия и социального функционирования, но и как залог снижения смертности от сердечно-сосудистых заболеваний.
Терапевтические возможности
Самым эффективным средством облегчения менопаузальных симптомов по праву считается гормональная терапия [30], но ряд противопоказаний и побочных реакций ограничивает ее назначение и продолжительность применения [31, 32]. В свете представлений о возможном появлении приливов жара на фоне нормальной эстрогенной секреции становится непонятным и даже вызывает законные опасения слишком раннее начало приема МГТ в пременопаузе [16]. Результаты исследований Heart and Estrogen/ Progestin Replacement Study (HERS), Women`s Health Initiative (WHI), Million Women Study (MWS) и Women’s International Study of Long Duration Oestrogen after Menopause (WISDOM) показали, что у некоторых групп женщин МГТ повышает риск рака молочной железы (РМЖ), острых кардиоваскулярных эксцессов, венозной тромбоэмболии и деменции [33]. Эти результаты напугали не только врачей, но и женщин. Публикация их в средствах массовой информации привела к тому, что многие женщины по всему миру самостоятельно отказались от приема МГТ и стали искать иные способы облегчения приливов жара [34, 35]. В результате потребность в эффективной и безопасной негормональной альтернативе лечения менопаузальных симптомов возросла и остается актуальной.
Средства растительного происхождения
Исследования растительных средств в практике лечения климактерических симптомов появились в результате наблюдений меньшего числа приливов жара и их интенсивности у жительниц Японии и Юго-Восточной Азии по сравнению с коренными представительницами Европы и их потомками в Северной Америке. Анализ этих данных позволил сделать вывод, что лучшее самочувствие азиаток в пери- и постменопаузе было связано с особенностями питания [36]. В результате начались многочисленные исследования соединений растительного происхождения, способных уменьшить выраженность симптомов, связанных с менопаузой. Восприятие приливов как результата дефицита эстрогенов, положительное влияние препаратов эстрадиола на вазомоторные симптомы стало предпосылкой для ошибочной интерпретации действия всех растительных средств, облегчающих приливы, как эстрогеноподобного. В результате все эти соединения стали обозначать единым термином «фитоэстрогены», что с биохимической точки зрения некорректно.
На самом деле способностью связываться с эстрогеновыми рецепторами и вызывать эффекты, сходные с эффектами эндогенных эстрогенов, т.е. свойствами, позволяющими отнести биологически активное вещество к фитоэстрогенам [37], обладают только две группы соединений: изофлавоны, соответствующие по структуре гетероциклическим фенолам, и лигнаны, структурно относящиеся к классу дифенолов. На сегодняшний день лучше изучены изофлавоны, содержащиеся в больших количествах в соевых бобах, других стручковых растениях, чечевице, гранатах, финиках, семенах подсолнечника, капусте, красном клевере.
Однако список биологически активных веществ, применяемых для купирования симптомов климакса, не исчерпывается классическими фитоэстрогенами, и особое место в нем занимает цимицифуга кистевидная (Cimicifuga racemosa, Actaea racemosa, клопогон кистевидный, Black Cohosh) [38]. Компоненты экстрактов цимицифуги включают тритерпеновые моногликозиды с циклоартановым скелетом, фитостерин, флавоноиды, салициловую кислоту и горечи [39]. Наиболее важными составляющими являются терпеноиды – органические соединения, производные терпенов. Строение молекул терпеноидов заметно отличает их от других органических субстанций повышенной лабильностью, склонностью к изомеризации, циклизации и полимеризации, которые нередко проходят в мягких условиях, под действием света, кислорода воздуха, паров воды и т.п. Терпеноиды активно участвуют в обменных процессах, протекающих в растениях, регулируют активность генов, включаются в фотохимические реакции. Углеродные цепи ряда терпеноидов являются ключевыми промежуточными продуктами биосинтеза холестерина, стероидных гормонов, ферментов, витаминов D, Е, К, желчных кислот. Широкий спектр биологического действия растительных терпеноидов представляет интерес для поиска новых лекарственных средств.
Действие изофлавонов и тритерпенгликозидов принципиально различается. Изофлавоны связываются с эстрогеновыми рецепторами и являются классическими фитоэстрогенами, точнее, растительными селективными модуляторами эстрогеновых рецепторов, обеспечивающими в зависимости от эстрогенной насыщенности слабый антиэстрогенный или эстрогенный эффект [40]. Преимущественно взаимодействуя с β-рецепторами, широко представленными в лимбико-ретикулярном комплексе и гипоталамусе, фитоэстрогены нормализуют синтез и обмен катехоламинов мозга (серотонин, дофамин, норадреналин), повышают уровень β-эндорфина, нейротензина, нормализуют активность центра терморегуляции и тонус вегетативной нервной системы. Одновременно достигаются незначительное гипотензивное действие, стабилизация сердечного ритма, легкий седативный эффект и улучшение качества сна.
Экстракт цимицифуги
Аналогичные эффекты оказывает экстракт цимицифуги, но в исследованиях с применением метода связывания «лиганд–рецептор эстрогенов» было подтверждено отсутствие взаимодействия компонентов экстракта цимицифуги кистевидной (используется в производстве отечественного лекарственного препарата Ци-Клим) с рецепторами эстрогенов типа α или β, основными проводниками сигнала эстрогенов. С другой стороны, доказано, что экстракты цимицифуги кистевидной связываются с рецепторами серотонина [41], и это может объяснить их достоверное положительное влияние (обнаруженное в плацебо-контролируемых исследованиях [42, 43]) на психосоматические и вазомоторные жалобы. Тем не менее спектр влияний экстракта цимицифуги, например ее эффект в отношении минеральной плотности кости, заставляет продолжить поиски механизма эстрогеноподобного действия, так как объяснить подобное влияние серотонинергическими свойствами нельзя. Существует предположение о возможной стимуляции компонентами экстракта цимицифуги неких протеинов, опосредованно подавляющих и/или стимулирующих эстрогенные рецепторы. Другая гипотеза предполагает вероятность связывания с иными (не α или β) подтипами эстрогеновых рецепторов, например, G-протеин-ассоциированными или другими, еще не идентифицированными вариациями. Как бы то ни было, но в экспериментальных исследованиях тритерпен-гликозиды оказывали ингибирующее воздействие на остеокласты [44], что смещает процесс ремоделирования кости в сторону костеобразования.
Можно бесконечно рассуждать о том, какой эффект – эстрогенный или нейротропный – предпочтителен в купировании вазомоторных и психовегетативных симптомов климакса. Но при этом не следует забывать о многообразии эстрогенных воздействий, среди которых есть и нежелательные в постменопаузе утеротропный и маммотропный эффекты [45, 46]. Экстракту цимицифуги данные эффекты несвойственны. Утеротропное действие проверялось на модели крыс с удаленными яичниками: ни в одном случае экстракты цимицифуги не стимулировали рост матки или экспрессию инсулиноподобного фактора роста 1, гены которого up-регулируются эстрадиолом [47]. Применение экстракта цимицифуги не вызывает увеличения числа трубчатых и альвеолярных долек молочной железы в отличие от аналогичного по длительности курса орального приема эстрадиола [48]. В ходе клинического исследования с экстрактом цимицифуги было показано, что в полученной с помощью биопсии ткани молочной железы не обнаруживается пролиферативных изменений [49]. Более того, пролиферация клеточной линии MCF-7 (Michigan Cancer Foundation-7) РМЖ, стимулируемая эстрадиолом, в присутствии экстракта цимицифуги существенно и дозозависимо ингибируется [50]. Данный эффект не является антиэстрогенным и характеризует не только ответ клеток РМЖ, но и клеток карциномы простаты, пролиферация которых ингибируется под действием экстракта цимицифуги [51]. Предполагается, что противоопухолевый эффект реализуется посредством активации арилуглеводородных рецепторов [51]. В исследованиях in vitro также показано, что гликозидциклоартантритерпен и его агликоны из экстракта корня цимицифуги индуцируют антипролиферативные и проапоптические гены [52]. Долговременные клинические исследования подтверждают, что применение экстракта цимицифуги в течение 2 лет и более не сопровождается изменениями тканей эндометрия и молочных желез [43].
За последние 20 лет были проведены десятки клинических исследований, оценивающих эффективность растительных средств лечения менопаузальных симптомов, опубликовано несколько систематических обзоров и мета-анализов, но результаты их оказались неоднозначны и противоречивы [53, 54], что ставит закономерный вопрос о возможных причинах расхождений полученных данных и выводов.
Эффект растительных экстрактов дозозависим. Но содержание активных веществ в лекарственных препаратах и особенно в биологически активных добавках к пище, оцененное в разных исследованиях, отличалось весьма существенно. Таким образом, не все препараты были способны обеспечить поступление достаточного для облегчения приливов количества активной субстанции [55]. Это определяет преимущество стандартизированных экстрактов цимицифуги в лекарственных препаратах, в числе которых лекарственное средство Ци-Клим.
Необходимо принимать во внимание и отличия в действии самих активных субстанций, по поводу чего неоднократно проводились сравнительные и плацебо-контролируемые исследования. В нескольких исследованиях не было обнаружено преимуществ растительных лекарственных средств как перед друг другом, так и по сравнению с плацебо [55–57]. Однако как изофлавоны представлены группой веществ разной степени активности, так и цимицифуга представлена несколькими видами, существенно различающимися по действию.
Несколько клинических исследований этанолового экстракта цимицифуги кистевидной, включивших более 500 пациентов [42, 43], подтвердили его положительное влияние на вазомоторные симптомы, которое выразилось в снижении числа приливов на 50–80% от исходного уровня, сравнимое с эффектом конъюгированных эстрогенов. Одновременно было зафиксировано положительное действие препарата на костный обмен. Через 12 недель лечения в значительной степени повышался плазменный уровень костной специфической щелочной фосфатазы при отсутствии изменений концентрации С-терминальных телопептидов, и индекс ремоделирования костной ткани возрастал.
Вместе с тем клинические исследования экстракта цимицифуги продемонстрировали его хорошую переносимость и безопасность [43] как для эндометрия, так и для молочных желез. Биопсия эндометрия, проведенная через 12 месяцев лечения, не выявила ни одного случая гиперпластических изменений, а при проведении маммографии не было выявлено ни одного случая повышения плотности молочных желез. Помимо того, было установлено отсутствие действия экстракта цимицифуги на маркеры функции печени и параметры гемостаза.
В России стандартизированный экстракт цимицифуги входит в состав препарата Ци-Клим, производство которого отвечает мировым стандартам – GMP (Good Manufacturing Practice – Надлежащая производственная практика).
Таким образом, лекарственный препарат Ци-Клим, содержащий в 1 таблетке 20 мг сухого стандартизированного экстракта корневища цимицифуги, может применяться в практике лечения климактерических расстройств в суточной дозе 40 мг (1 таблетка 2 раза в день). Показаниями к применению лекарственного средства Ци-Клим являются вазомоторные (приливы жара) и психосоматические (головокружение, головная боль, боли в костях и суставах, сердцебиение, дыхательные расстройства, нарушения настроения депрессивного или тревожного характера и др.) симптомы климактерического синдрома. В постменопаузе Ци-Клим можно назначать как альтернативу МГТ, когда гормональное лечение противопоказано или нежелательно. В ранней пременопаузе Ци-Клим имеет преимущества перед гормональной терапией, поскольку устойчивый дефицит эстрогенов еще не сформировался и применение МГТ чревато формированием эстрогенного избытка с возможными побочными эффектами [17]. Отсутствие связывания компонентов экстракта цимицифуги с эстрогеновыми рецепторами определяет безопасность назначения лекарственного средства Ци-Клим с целью купирования психовегетативных жалоб при любом уровне эстрогенной секреции. Более того, учитывая серотонинергическое действие экстракта цимицифуги, Ци-Клим можно рассматривать как средство выбора при появлении вазомоторных симптомов не только в климактерическом периоде, но и у женщин репродуктивного возраста. В отличие от назначения МГТ при рекомендации препарата Ци-Клим молодым женщинам нет необходимости подтверждать у них наличие эстрогенного дефицита, следовательно, нижнего возрастного порога его применения не существует. Аналогично, не существует и верхнего возрастного порога назначения экстрактов цимицифуги, поскольку им несвойственны риски гормональной терапии. Фактически препараты цимицифуги выступают как альтернатива селективным ингибиторам обратного захвата серотонина в лечении вазомоторных симптомов вне зависимости от возраста и репродуктивного статуса женщины. В то же время Ци-Клим имеет преимущества перед данной группой психотропных препаратов, которые могут назначаться только при наличии депрессивных расстройств. Кроме того, психотропные препараты для лечения психовегетативных пароксизмов рекомендуются относительно коротким курсом, в то время как экстракты цимицифуги не вызывают побочных реакций и могут назначаться длительно.
Процессы старения многолики, и вазомоторные/психосоматические симптомы являются только частью расстройств, нарушающих качество жизни женщины. Полноценная профилактика болезней, обычно манифестирующих в периоде менопаузального перехода, невозможна без всесторонней поддержки метаболических процессов и, следовательно, без назначения витаминов [59]. Ци-Клим витамины для женщин 45+, в составе которых экстракт цимицифуги (20 мг), также представлены компанией «Эвалар». Среди компонентов этого комплекса – витамины-антиоксиданты С и Е, важнейшие тканевые адаптогены, группа витаминов В (В1, В2, В6, фолиевая кислота), обладающие особой тропностью к нервной системе, пантотенат, L-карнитин и рутин, улучшающие трофику тканей и укрепляющие сосудистые стенки микроциркуляторного русла. Магний и селен в составе комплекса чрезвычайно значимы не только в силу своей вовлеченности в жизненно важные процессы организма (магний – кофактор около 300 энзимов, мощный адаптоген; селен – замыкающее звено антиоксидантной системы), но и по причине высокой распространенности их дефицита, особенно в стареющей популяции. Экстракт пустырника дополняет положительное действие витаминов В, магния и экстракта цимицифуги на центральную и вегетативную нервную систему, а витамин А обеспечивает регенеративные способности слизистых оболочек и кожи, которые снижаются в результате дефицита эстрогенов.
Дополнительный бонус от линейки Ци-Клим женщины могут получить, используя кремы, в состав которых, помимо экстракта цимицифуги, входят гиалуроновая кислота, магний и другие биологически активные компоненты, позволяющие сохранить эластичность кожи, предотвратить ее обезвоживание и образование морщин. Нутриентная поддержка изнутри и уход за кожей в совокупности с вероятным положительным влиянием экстракта цимицифуги на структуры кожи по аналогии с действием в отношении костной ткани позволяют надеяться на косметический эффект комплексной терапии, что, несомненно, отразится на качестве жизни женщин.
Общая продолжительность курса лекарственными средствами, содержащими экстракт цимицифуги, в климактерическом периоде не должна ограничиваться рамками нескольких месяцев. Постоянное применение под контролем врача можно рекомендовать столь долго, сколь долго женщина нуждается в негормональной коррекции менопаузальных расстройств и их профилактике. В связи с планированием длительного приема лекарственного средства становится очевидным преимущество отечественного препарата Ци-Клим, являющегося доступным по цене средством для всех категорий населения.
Литература
- Клинические рекомендации. Акушерство и гинекология. Вып. 2. Под ред. В.И.Кулакова. М.: ГЭОТАР-Медиа, 2008.
- Nelson HD, Haney E, Humphrey L et al. Management of menopause-related symptoms. Summary, Evidence Report/Technology Assessment No. 120 (Prepared by the Oregon Evidence-based Practice Center, under contract No. 290-02-0024). AHRQ Pub. No. 05-E016-1. Rockville, MD: Agency for Health Research Quality, 2005.
- Maclennan AH, Broadbent JL, Lester S et al. Oral oestrogen and combined oestrogen/progestogen therapy versus placebo for hot flashes. Cochrane Database Syst Rev 2004; 4: CD002978.
- Williams RE, Kalilani L, Di Benedetti DB et al. Frequency and severity of vasomotor symptoms among peri- and postmenopausal women in the United States. Climacteric 2008; 11: 32–43.
- Owens GM. Gender differences in health care expenditures, resource utilization, and quality of care. J Manag Care Pharm 2008; 14 (Suppl.): 2–6.
- Joffe H, Massler A, Sharkey KM. Evaluation and management of sleep disturbance during the menopause transition. Semin Reprod Biol 2010; 28: 404–21.
- Bromberger JT, Kravitz HM, Matthews K et al. Predictors of first lifetime episodes of major depression in midlife women. Psychol Med 2009; 39: 55–64.
- Woods NF, Smith-DiJulio K, Percival DB et al. Depressed mood during the menopausal transition and early postmenopause: observation from the Seattle Midlife Women’s Health Study. Menopause 2008; 15: 223–32.
- Nappi RE, Lachowsky M. Menopause and sexuality: prevalence of symptoms and impact on quality of life. Maturitas 2009; 63: 138–41.
- Reed SD, Ludman EJ, Newton KM et al. Depressive symptoms and menopausal burden in the midlife. Maturitas 2009; 62: 306–10.
- Stahl SM. Vasomotor symptoms and depression in women, part I. Role of vasomotor symptoms in sighaling the onset or relapse of a major depressive episode. J Clin Psychiatry 2009; 70: 11–2.
- Politi MC, Schleinitz MD, Col NF. Revisting the duration of vasomotor symptoms of menopause: a meta-analysis. J Gen Intern Med 2008; 23: 1513–97.
- North American Menopause Society. Treatment of menopause-associated vasomotor symptoms: position statement of The Notrth American Menopause Society. Menopause 2004; 11: 11–33.
- Col NF, Guthrie JR, Politi M, Dennerstein L. Duration of vasomotor symptoms in middle-aged women: a longitudinal study. Menopause 2009; 16: 453–7.
- Freeman EW, Sammel MD, Lin H et al. Duration of menopausal hot flushes and associated risk factors. Obstet Gynecol 2011; 117 (5): 1095–104.
- Santoro N, Lasley B, McConnell D et al. Body size and ethnicity are associated with menstrual cycle alterations in women in the early menopausal transition: the Study of Women’s Health across the Nation (SWAN) Daily Hormone Study. J Clin Endocrinol Metab 2004; 89: 2622–31.
- Skurnick JH, Weiss G, Goldsmith LT et al. Longitudinal changes in hypothalamic and ovarian function in perimenopausal women with anovulatory cycles: relationship with vasomotor symptoms. Fertil Steril 2009; 91 (4): 1127–34.
- Rapkin AJ. Vasomotor symptoms in menopause: physiologic condition and central nervous system approaches to treatment. Am J Obstet Gynecol 2007; 196: 97–106.
- Freedman RR, Benton MD, Genic RJ, Graydon FX. Cortical activation during menopausal hot flashes. Fertil Steril 2006; 85: 674–8.
- Loprinzi CL, Barton DL. Oh hot flash mechanism, measurement, and treatment. Menopause 2009; 16: 621–3.
- Freeman EW, Sammel MD, Lin H et al. The role of anxiety and hormonal changes in menopausal hot flashes. Menopause 2005; 12: 258–66.
- Juang KD, Wang SJ, Lu SR et al. Hot flashes are associated with psychological symptoms of anxiety and depression in peri- and post- but not premenopausal women. Maturitas 2005; 52: 119–26.
- Reddy SY, Warner H, Gutusso T et al. Gabapentin, estrogen and placebo for treating hot flashes. Obstet Gynecol 2006; 108: 41–8.
- Gast GC, Pop VJ, Samsioe GN et al. Vasomotor menopausal symptoms are associated with increased risk of coronary heart disease. Menopause 2011; 18 (2): 146–51.
- Thurston RC, Sutton-Tyrrell K, Everson-Rose SA et al. Hot flashes and subclinical cardiovascular disease: findings from the Nation Heart Study. Circulation 2008; 118: 1234–40.
- Thurston RC, Christie IC, Matthews KA. Hot flashes and cardiac vagal control: a link to cardiovascular risk? Menopause 2010; 17: 456–61.
- Thurston RC, Kuller LH, Edmundowicz D, Matthews KA. History of hot flashes and aortic calcification among postmenopausal women. Menopause 2010; 17: 256–61.
- Rossouw JE, Prentice RL, Manson JE et al. Postmenopausal hormone therapy and risk of cardiovascular disease by age and years since menopause. JAMA 2007; 297: 1465–77.
- Кириллова М.Ю. Влияние эстроген-прогестиновой терапии на кардиометаболические риски у женщин в перименопаузе. Автореф. дис. … канд. мед. наук. М., 2012.
- Sturdee DW et al. Updated IMS recommendations on postmenopausal hormone therapy and preventive strategies for midlife health. Climacteric 2011; 14: 302–20.
- Gompel A, Rozenberg S, Barlow DH. The EMAS 2008 update on clinical recommendations on postmenopausal hormone replacement therapy. Maturitas 2008; 61: 227–32.
- Hill DA, Hill SR. Counseling patients about hormone therapy and alternatives for menopausal symptoms. Am Fam Physician 2010; 82: 801–7.
- Anderson GL, Limacher M, Assaf AR et al. Effects of conjugated equine estrogen in postmenopausal women with hysterectomy: the Women’s Health Initiative randomized controlled trial. J Am Med Ass 2004; 291 (14): 1701–12.
- Tsai SA, Stefanick ML, Stafford RS. Trends in menopausal hormone therapy use of US office-based physicians, 2000–2009. Menopause 2011; 18: 385–92.
- Kronenberg F, Cushman LF, Wade CM et al. Race/ethnicity and women`s use of complementary and alternative medicine in the United States: results of national survey. Am J Public Health 2006; 96: 1236–42.
- Melby MK. Chilliness: a vasomotor symptom in Japan. Menopause 2007; 14: 752–9.
- Rimbach G, Boesch-Saadatmandi C, Frank J et al. Dietary isoflavones in the prevention of cardiovascular disease – a molecular perspective. Food Chem Toxicol 2008; 46: 1308–19.
- EMA European Medicine Agency. Committee on Herbal Medicinal Products (HMPC). Community herbal mono-graph on Cimicifuga racemosa (L.) Nutt., rhizome. EMA/HMPC/ 600717/2007 Corr., 2011.
- ESCOP Monographs. CIMICIFUGAE RHIZOMA – Black Cohosh. European Scientific Cooperative on Phytotherapy, Exeter, UK, 2011, http://www.escop.com/
- Oseni T, Patel R, Pyle J, Jordan VC. Selective estrogen receptor modulators and phytoestrogens. Planta Med 2008; 74: 1656–65.
- Powell SL, Gödecke T, Nirolic D et al. In vitro serotonergic activity of Black Cohosh and identification of Nω-Methylserotonin as a potential active constituen. J Agric Food Chem 2008; 56 (24): 11718–26.
- Wuttke W, Rauš K, Gorkow C. Efficacy and tolerability of the Black cohosh (Actaea racemosa) ethanolic extract BNO 1055 on climacteric complaints: a double-blind, placebo- and conjugated estrogens-controlled study. Maturitas 2006; 55 (1): S83–S91.
- Rauš K, Brucker C, Gorkow C, Wuttke W. First-time proof of endometrial safety of the special black cohosh extract (Actaea or Cimicifuga racemosa extract) CR BNO 1055. Menopause 2006; 13 (4): 678–91.
- Li JX, Liu J, He CC et al. Triterpenoids from Cimicifuga rhizoma, a novel class of inhibitors on bone resorption and ovariectomy-induced bone loss. Maturitas 2007; 58: 59–69.
- Bolton JL, Thatcher GR. Potential mechanisms of estrogen quinone carcinogenesis. Chem Res Toxicol 2008; 21: 93–101.
- Yeh IT. Postmenopausal hormone replacement therapy: endometrial and breast effects. Adv Anat Pathol 2007; 14: 17–24.
- Kretzschmar G, Nisslein T, Zierau O, Vollmer G. No estrogenlike effects of an isopropanolic extract of Rhizoma Cimicifuga racemosa on uterus and vena cava of rats after 17 day treatment. J Steroid Biochem Mol Biol 2005; 97: 271–7.
- Зайдлова-Вуттке Д., Вуттке В. Краткий обзор применения цимицифуги (Cimicifuga racemosa) в гинекологии. Рос. вестн. акуш.-гинекол. 2009; 3: 47–52.
- Hirschberg AL, Edlund M, Svane G et al. An isopropanolis extract of black cohosh does not increase mammographic breast density or breast cell proliferation in postmenopausal women. Menopause 2007; 14 (1): 89–96.
- Bodinet C, Freudenstein J. Influence of marketed herbal menopause preparation on MCF-7 cell proliferation. Menopause 2004; 11: 281–9.
- Jarry H, Thelen P, Christoffer V et al. Cimicifuga racemosa extract BNO 1055 inhibits proliferation of the human prostate cancer cell line LNCaP. Phytomedicine 2005; 12: 178–82.
- Gaube F, Wolfl S, Pusch L et al. Gene expression profiling reveals effects of Cimicifuga racemosa (L.). NUTT (black cohosh) on the estrogen receptor positive human breast cancer cell line MCF-7. BMC Pharmacol 2007; 7: 11.
- Nelson HD, Vesco KK, Haney E et al. Nonhormonal therapies for menopausal hot flashes: systematic review and meta-analysis. JAMA 2006; 295: 2057–71.
- Nedrow A, Miller J, Walker M et al. Complementary and alternative therapies for the management of menopause-related symptoms: a systematic evidence review. Arch Intern Med 2006; 166: 1453–65.
- Newton KM, Reed SD, LaCroix AZ et al. Treatment of vasomotor symptoms of menopause with black cohosh, multibotanicals, soy, hormone therapy, or placebo: a randomized trial. Ann Intern Med 2006; 145: 869–79.
- Geller SE, Shulman LP, van Breemen RB et al. Safety and efficacy of black cohosh and red clover for the management of vasomotor symptoms: a randomized controlled trial. Menopause 2009; 16: 1156–66.
- Grady D. Clinical practice. Management of menopausal symptoms. N Engl J Med 2006; 355: 2338–47.
- Beer A-M, Neff A. Differentiated Evaluation of Extract-Specific Evidence on Cimicifuga racemosa’s Efficacy and Safety for Climacteric Complaints. Hindawi Publishing Corporation Evidence-Based Complementary and Alternative Medicine 2013, Article ID 860602.
- Ребров В.Г., Громова О.А. Витамины, макро- и микроэлементы. М.: ГЭОТАР-МЕД, 2008.
