Исторически сложилось, что нарушением развития речи у детей занимаются логопеды, психологи, дефектологи, неврологи. Поэтому для достижения максимального результата необходимы преемственность и согласованность в работе всех специалистов. Эпидемиологические исследования в регионах, которые позволили бы представить реальную распространенность речевой патологии, не проводились, вследствие чего в литературе имеется разброс показателей по этой проблеме. Так, по данным Л. Н. Зуевой и Е. Е. Шевцовой, среди дошкольников доля страдающих нарушениями речи достигает 20–25%[7]. Л. С. Чутко указывает, что частота речевых расстройств среди детей дошкольного возраста составляет 5–10%[6].
Дети с нарушением развития речи в дошкольном периоде при переходе в общеобразовательную школу имеют проблемы с письменной речью, чтением (дислексия, дисграфия). Для многих из них школьная программа становится непосильной. Дети тяжело переживают социальную дезадаптацию, становятся раздражительными, агрессивными, замыкаются в себе, теряют уверенность. Очень важно вовремя распознать эту патологию и оказать необходимую помощь, пока существуют компенсаторные возможности головного мозга и не успели сформироваться патологические поведенческие реакции.
ВВЕДЕНИЕ
Жалобы родителей на нарушение речи у ребенка чаще всего предъявляются по достижении им трехлетнего возраста и в 5–7 лет. Это происходит потому, что до 3 лет родители ждут, когда ребенок заговорит самостоятельно, а в 5–7 лет дети с нарушением речи с трудом проходят предшкольную подготовку. Для овладения письменной речью и чтением требуется много времени, приобретенные навыки не закрепляются, что и является главным мотивом обращения к специалистам.
Этиологию специфического расстройства речевого развития в настоящее время связывают с наследственными факторами и гипоксически-ишемическим повреждением ЦНС в перинатальном периоде в виде формирования церебральной атрофии, сочетающимся с темповой задержкой развития на первом году жизни[5].
Специфические расстройства речевого развития в детском возрасте характеризуются первичными нарушениями развития речи, при которых ребенок имеет соответствующий возрасту интеллект, нормальный слух и нормальные условия для овладения речью, расстройствам речи не предшествует период нормального ее развития[5, 10, 14]. Данные расстройства характеризуются постоянным течением без ремиссий или рецидивов. В эту категорию не входят ринолалия, речевые нарушения, обусловленные нарушением слуха, умственной отсталостью, аутизмом, эпилепсией. Речевые звуки, используемые этими детьми, ниже уровня их интеллектуального развития, хотя понимание речи находится в пределах нормы. При этом могут отмечаться (или не отмечаться) расстройства артикуляции. Двигательные расстройства речевого акта у этих пациентов носят разноплановый характер, наблюдаются псевдобульбарная дизартрия, мозжечковая дизартрия, корковая дизартрия, экстрапирамидная мезенцефально-диэнцефальная дизартрия по типу гипо-, гипер- и дистонии[2]. Данные синдромы могут сочетаться у детей в различных вариациях.
Речевые нарушения в детском возрасте сопровождаются неврологической симптоматикой: двигательными нарушениями (нарушение равновесия, координации движений, мелкой моторики), синдромом дефицита внимания и гиперактивности (СДВГ), церебрастенией, эмоциональной лабильностью, неврозоподобными нарушениями (ночные страхи, энурез, тики, заикание), вегетососудистыми нарушениями, головными болями.
У детей применение Церебролизина описано с 1970-х годов как отечественными (Е. В. Шмидт, 1975), так и зарубежными авторами (W. Englert, D. Schlich, 1977). Этот препарат наиболее изучен при лечении СДВГ у детей и подростков (Н. Н. Заваденко, 1990; О. Л. Бадалян, 1993; Н. Ю. Сотникова, 2003) и на различных этапах лечения ЧМТ (Е. В. Изнак и соавт., 2010; Z. Fei, Y. I. Shenyui, 1992; D. Zhou, S. Yang, 1993; M. Wang et al., 1998). При СДВГ эффективность применения Церебролизина имеет уровень доказательности В[12].
Церебролизин представляет собой комплекс нейропептидов с молекулярной массой не более 10 000 Да (15%), свободных аминокислот (85%) и микроэлементов. Углубленные исследования безопасности препарата с использованием иммуноблоттинга и электронной микроскопии не выявили в Церебролизине функционально активных проонкогенов, нуклеиновых кислот и белковых соединений класса амилоидов, в том числе прионов[13].
Механизм действия Церебролизина связан со способностью активировать эндогенные защитные механизмы, основными составляющими которых являются нейротрофичность, нейропротекция, нейропластичность и нейрогенез[23, 24]. Нейротрофическое действие обеспечивает координацию процессов нейропротекции, нейропластичности и нейрогенеза на оптимальном уровне[23, 24]. В различных исследованиях показана структурная и функциональная эквивалентность нейропептидов Церебролизина и нейротрофических факторов. По имеющимся данным, препарат способен увеличивать связывание собственного нейротрофического фактора мозга (brain-derived neurotrophic factor — BDNF) к TrkB-рецепторам[18], активировать секрецию собственного BDNF[15], а также модулировать соотношение про- и зрелых собственных нейротрофинов, что прямо свидетельствует о нейротрофической модуляции[33]. Нейропротективное действие Церебролизина проявляется в снижении глутаматной эксайтотоксичности[19, 20], инактивации образования свободных радикалов[17, 31], подавлении воспалительного ответа[16, 22], уменьшении отека[30] и торможении процессов апоптоза и некроза[19–21, 29, 35, 36]. Церебролизин способен модулировать нейропластичность, оптимизировать нейрональные соединения в мозге, способствуя отрастанию поврежденных отростков нейронов и увеличению плотности синапсов и поддерживая тем самым способность мозга адаптироваться к изменениям среды[23, 25, 26, 28, 34].
Свой вклад в активацию процессов нейропротекции и нейрорегенерации также вносят входящие в состав Церебролизина аминокислоты. Они обладают детоксицирующим действием, способны активировать белковый синтез, восстанавливать медиаторный баланс с нормализацией синтеза аденозина, таурина, глицина[4]. Присутствие аденозина обеспечивает пул пуриновых и пиримидиновых оснований, необходимых для синтеза антиапоптозных белков. Микроэлементы, содержащиеся в препарате, являются каталитическими центрами синтеза всех нейропептидов головного мозга[3]. Под воздействием Церебролизина происходит активация нейрогенеза — процесса формирования нейронов и клеток глии из клеток-предшественников. Показано, что препарат способен стимулировать нейро- и ангиогенез в субвентрикулярной зоне боковых желудочков и в зубчатой извилине гиппокампа как у здоровых животных, так и на моделях патологии[23, 27, 32, 36, 37].
Цель работы:
исследование эффективности применения полипептидного препарата Церебролизин в амбулаторных условиях у детей 3–7 лет, страдающих речевыми нарушениями, и анализ изменений церебральной гемодинамики на фоне лечения.
МАТЕРИАЛЫ И МЕТОДЫ
Для проведения исследования за период 2013–2014 годов из осмотренных 578 детей от 3 до 7 лет были отобраны 84 ребенка с речевыми нарушениями, что составило 14,5% от общего числа детей, прошедших осмотр.
Согласно логопедической классификации общее недоразвитие речи второго уровня выявлено у 10 из 84 человек (11,9%). У этих пациентов имеют место выраженные нарушения звукопроизношения, грубые нарушения грамматической и лексической сторон речи. Речевые расстройства сочетаются с неврологическими и психопатологическими симптомами и синдромами. Часто выявляются синдромы ликворно-венозной дистензии, синдромы двигательных расстройств. В психических процессах отмечается снижение познавательной деятельности — ослабление внимания, памяти, праксиса, гнозиса. Дети этой группы испытывают затруднения при обучении[7].
Общее недоразвитие речи третьего уровня было выявлено у 74 детей (88,1%). Для пациентов данной категории характерны менее выраженные нарушения звукопроизношения, незначительные аграмматизмы, бедность словарного запаса. В психическом облике этих детей имеет место эмоционально-волевая незрелость[7].
Среди обследованных детей преобладали мальчики: мальчиков было 53 (63%), девочек — 31 (37%); соотношение мальчиков и девочек — 1 : 1,7. У 65 детей (77%) имелись СДВГ, астенический синдром, эмоционально-волевые нарушения, недифференцированность движений пальцев рук и артикуляционных движений. Пациентов рандомизировали и относили к контрольной (первой) или основной (второй) группе методом случайных чисел, численность детей в первой и второй группах составила 41 и 43 ребенка соответственно. В первой группе проводили занятия с логопедом. Пациенты второй группы, помимо занятий с логопедом, получали внутримышечно инъекции Церебролизина. Стандартный курс препарата составлял 15 инъекций в утренние часы через день с постепенным наращиванием дозы от 0,1 мл/сут до 0,1–0,2 мл/кг/сут за 5 инъекций.
Контроль эффективности лечения осуществлялся путем изучения динамики неврологического и логопедического статусов, оценки тонкой моторики с помощью теста Лесны на диспраксию-дисгнозию[8]. Всем детям было проведено транскраниальное дуплексное сканирование (ТДС) на аппаратах Philips HD3 (датчики C 4–2, C 5–2) и «Унисон-2-03» (датчики СА 621, PA 230) до назначения лечения и спустя один месяц (по окончании курса). При интерпретации данных использованы оценочные таблицы Национального руководства по лучевой диагностике и терапии[9].
Проверка статистических гипотез о равенстве частот улучшения показателей речевого развития, а также патологических ультразвуковых паттернов, оцененных с помощью ТДС, в выделенных группах проводилась с использованием двустороннего точного критерия Фишера (F-критерий) и критерия Хи-квадрат (χ2) с поправкой Йетса. Достоверность различия по критерию Фишера и χ2 применяли для анализа различий частот выявления бинарного признака в группе контроля и опытной группе после лечения.
РЕЗУЛЬТАТЫ
В результате лечения показатели речевого развития улучшились у детей обеих групп: по окончании курса были отмечены коррекция звукопроизношения и автоматизация звуков, расширился словарный запас, улучшились лексика и грамматика, повысилось речевое внимание. На фоне лечения Церебролизином показатели речевого развития улучшились у 39 детей из 43, или у 90,7%, тогда как в группе сравнения аналогичный показатель составил 46,3% — 19 пациентов из 41 (χ2 = 17,302; р < 0,01).
Помимо этого, на фоне применения Церебролизина компенсировались неврологические нарушения. В группе детей, которые получали Церебролизин, количество выполненных заданий по мелкой моторике увеличилось на 23%, а в группе сравнения — на 11%. Редукция клинических признаков СДВГ у детей, получавших Церебролизин, также происходила более быстрыми темпами. Пациенты без медикаментозного лечения сохраняли неврологическую симптоматику.
Таким образом, характеризуя динамику неврологического и логопедического статусов у детей двух групп во время исследования, необходимо отметить, что пациенты, в план лечения которых входил Церебролизин, показывали более высокие результаты в отношении восстановления речевой функции (звукопроизношение, лексика, грамматика) и компенсации неврологической симптоматики.
С помощью метода ТДС пациенты исследовались на наличие патологических ультразвуковых признаков: мозаичной асимметрии индекса резистентности (resistance index — RI); внутрибассейновой асимметрии; диффузного повышения RI; снижения линейных скоростей кровотока в каротидном бассейне; снижения линейных скоростей кровотока в вертебробазилярном бассейне; асимметрии кровотока; измененной цереброваскулярной реактивности (вазодилататорный и вазоконстрикторный тесты); повышения скорости венозного оттока по базальным венам, вене Галена; увеличения ширины третьего желудочка, глубины залегания затылочных рогов боковых желудочков. При повторном обследовании в основной группе было выявлено значительное снижение количества больных, у которых встречались данные признаки (табл.). Все выявленные ультразвуковые характеристики нозологически неспецифичны, т. е. не позволяют поставить диагноз, но они дают возможность выявить детей, у которых отклонения в развитии речевой функции возникли на фоне морфологических нарушений головного мозга, нарушений кровотока.
Таблица
Динамика частоты выявления патологических ультразвуковых паттернов у детей 3–7 лет с речевыми расстройствами в исследуемых группах
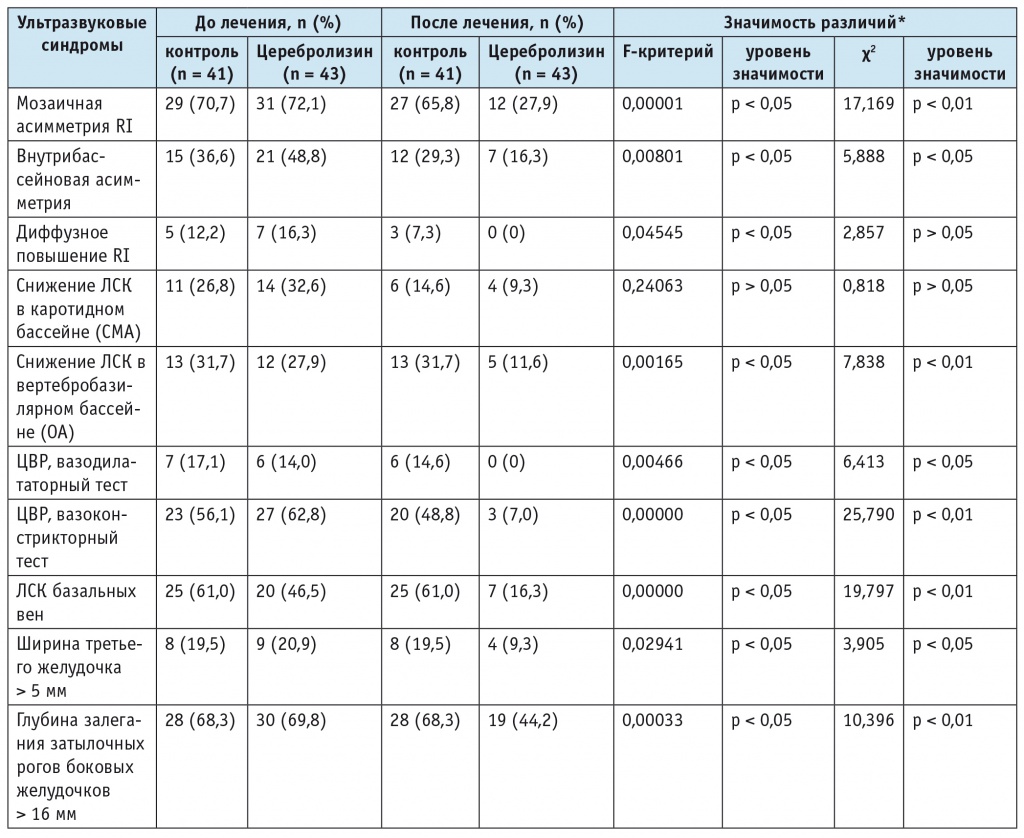
Примечание. ЛСК — линейная скорость кровотока; ОА — основная артерия; СМА — средняя мозговая артерия; ЦВР — цереброваскулярная реактивность; RI — индекс резистентности.
* Показана значимость различий между частотами выявления признаков в группе контроля и опытной группе после лечения.
Кроме того, одним из универсальных факторов, лимитирующих диапазон возможных реакций организма на любой предъявляемый раздражитель, является способность потреблять и утилизировать кислород. В целом возможность организма изменять уровень потребления кислорода в зависимости от меняющихся условий — это основной фактор, определяющий реабилитационный потенциал пациента. Клиническая оценка эффективности обмена кислорода проводится с помощью пробы на цереброваскулярную реактивность. Значимое улучшение неврологического и логопедического статусов в группе пациентов, получавших Церебролизин, сочеталось с восстановлением цереброваскулярной реактивности, а также с нормализацией индексов сосудистого сопротивления, симметрии кровотока и оттока крови по системе глубоких вен мозга. Нейротрофический эффект Церебролизина проявлялся в ослаблении признаков церебральной атрофии в виде уменьшения ширины увеличенного третьего желудочка и уменьшения глубины залегания затылочных рогов боковых желудочков.
Проведение инструментального обследование до и после лечения наглядно демонстрирует, что улучшение неврологического и логопедического статуса проходит на фоне положительной динамики церебральной гемодинамики. Применение Церебролизина приводит к нормализации сосудистого сопротивления, цереброваскулярной реактивности и восстановлению внутрибассейновой симметрии кровотока. Значимого влияния на линейные скорости кровотока Церебролизин не оказывал. Вклад в улучшение церебральной гемодинамики может вносить ранее показанная способность Церебролизина влиять на гемореологические и морфоденсиметрические показатели крови: снижение агрегации тромбоцитов (на 20–25%) и эритроцитов (более чем на 25–30%); нормализация размеров агрегатов тромбоцитов, эритроцитов; повышение деформируемости эритроцитов; сдвиг субпопуляционного состава эритроцитов в сторону нормальных форм; нормализация интегрального показателя кривизны мембраны и индекса спикулярности эритроцитов[1].
ЗАКЛЮЧЕНИЕ
В проведенном исследовании показана возможность эффективного амбулаторного лечения пациентов с нарушением речевой функции за счет добавления к комплексу логопедических упражнений курса препарата Церебролизин. Применение Церебролизина способствует регрессу неврологической симптоматики, ускоряет темпы речевого развития и повышает качество речи. Положительная динамика неврологических и логопедических нарушений повышает мотивацию и способствует росту приверженности к лечению пациентов и их родителей. Компенсация неврологических нарушений и улучшение показателей речевого развития коррелируют с улучшением гемодинамических показателей мозгового кровообращения. Исследование динамики патологических ультразвуковых паттернов с помощью метода транскраниального дуплексного сканирования может быть использовано в целях инструментального контроля ведения пациентов с нарушением речевой функции.
Церебролизин широко применяется в терапии различных неврологических заболеваний. Основными механизмами действия Церебролизина являются регуляция энергетического метаболизма мозга, собственное нейротрофическое влияние и модуляция активности эндогенных факторов роста, а также взаимодействие с системами нейропептидов и нейромедиаторов [2]. Установлено, что Церебролизин обладает антиоксидантными свойствами, заключающимися в торможении процессов свободнорадикального окисления и ПОЛ, а кроме того, обладает положительным влиянием на гомеостаз микроэлементов (магния, калия, селена, марганца, ванадия), являющихся антиоксидантами. Приводятся данные о тормозящем влиянии Церебролизина на апоптоз–зависимые процессы в нервной клетке, вызванные стрессом [1,2]. Это связано с тем, что Церебролизин обладает способностью предотвращать гиперактивацию микроглии и снижать продукцию интерлейкинов и других противовоспалительных цитокинов, что влияет на выраженность местной воспалительной реакции и процессы оксидантного стресса [1]. Препятствуя активации микроглиальных клеток мозга, Церебролизин оказывает нейроиммунотронный эффект, защищающий церебральные структуры от апоптоза. На культуре кортикальных нейронов цыпленка было показано тормозящее влияние Церебролизина на процессы нейроапоптоза, вызванные стрессорными факторами [7].
Тики и синдром Туретта относятся к распространенной неврологической патологии, встречающейся в детском возрасте. Провоцирующими факторами в возникновении тиков являются стресс и инфекции верхних дыхательных путей. Патогенетическая концепция тиков у детей заключается в нарушении антиоксидантного статуса и во вторичных изменениях нейромедиаторной рецепции генетического и приобретенного характера [4]. Определенный интерес представляет также предположение о возможном участии аутоиммунных процессов в патогенезе тиков и синдрома Туретта в тех случаях, когда развитию заболевания предшествовала инфекция [8,9]. Данные об антиоксидантных свойствах Церебролизина, о его нейроиммунотронном влиянии позволили предположить, что использование данного препарата в лечении тиков и синдрома Туретта может оказаться эффективным.
Целью данной работы явилось изучение эффективности использования Церебролизина в терапии тикозных гиперкинезов.
Материалы и методы
В исследование были включены 30 больных тиком и синдромом Туретта. Диагноз заболевания устанавливался в соответствии с МКБ 10 (Международная классификация болезней 10 пересмотра) и систематизацией тиков у детей, разработанной на кафедре неврологии детского возраста РМАПО (утверждена МЗ РФ, 2000, зав. кафедрой – профессор, д.м.н., В.П. Зыков). Основными критериями включения больных в исследование являлись зависимость дебюта или обострения тикозных гиперкинезов от инфекции верхних дыхательных путей, отягощенный аллергоанамнез, а также резистентность к проводимой ранее терапии. Выделено 3 группы, каждая из которых включала 10 пациентов: 1 группу составили больные распростаненным тиком (6 пациентов) и синдромом Туретта (4 пациента). На момент госпитализации отмечалось возобновление или усиление тиков. Церебролизин назначался в качестве монотерапии. Вторая группа включала пациентов с распространенным тиком, которые получали комплексную терапию Церебролизином и клоназепамом. Третью группу составили больные синдромом Туретта, Церебролизин назначался в сочетании с тиапридом. Имелись также 2 группы сравнения: в одну вошли пациенты, получавшие монотерапию клоназепамом, а в другую – тиапридом. Церебролизин вводился внутримышечно, в разовой дозе 1,0 мл на 10 кг веса, на курс 10–15 инъекций. Для оценки эффективности терапии использовался подсчет тиков за 20 минут до и после лечения. Осуществлялось катамнестическое наблюдение больных – спустя 6 месяцев после введения Церебролизина.
Результаты лечения
В первой группе больных (монотерапия Церебролизином) были получены следующие результаты: у больных синдромом Туретта – у 2 пациентов эффекта от проводимой терапии не получено и у 2 пациентов отмечалось усиление тиков; у больных распространенным тиком – у 1 пациента наблюдалось усиление тиков и у 5 пациентов отмечалась положительная динамика (уменьшение тиков на 15, 66, 75, 88% и в одном случае – полное прекращение тиков). Результаты монотерапии Церебролизином представлены на рисунках 1 и 2.
Во второй группе больных (Церебролизин в сочетании с клоназепамом) лишь в одном случае не было отмечено улучшения, у 9 больных количество тиков уменьшилось на 80, 60, 66, 64, 46, 40% , в том числе у 2 пациентов наблюдалось полное прекращение тиков. Эффект от проводимой терапии сохранялся в течение 6 месяцев. Результаты представлены на рисунке 3.
В группе сравнения (10 больных, которые принимали клоназепам в качестве монотерапии) – у 5 больных эффекта от проводимой терапии не получено, в остальных случаях уменьшение тиков отмечалось на 33, 40, 44, 41 и 71%. Терапевтический эффект сохранялся у 2 пациентов в течение 6 месяцев и у 3 больных – в течение 4 мес. Результаты представлены на рисунке 4.
Таким образом, сравнительный анализ эффективности лечения распространенного тика клоназепамом и клоназепамом в сочетании с Церебролизином, выявил более высокие результаты при включении в терапию Церебролизина (рис. 5).
В третьей группе больных (назначение Церебролизина совместно с тиапридом) эффекта от проводимой терапии не наблюдалось в 2 случаях, у 8 пациентов отмечалось значительное улучшение (уменьшение тиков на 66, 82, 58 и 80%, а в 4 случаях – полное прекращение тиков). Результаты представлены на рисунке 6.
В группе сравнения (10 больных, которые принимали тиаприд в качестве монотерапии) положительный терапевтический эффект был достигнут лишь у 5 больных (уменьшение тиков на 60, 41, 44, 83, 61%). Ремиссия сохранялась в течение 5 месяцев. Результаты представлены на рисунке 7.
Таким образом, использование Церебролизина в комплексном лечении синдрома Туретта значительно повысило эффективность терапии (рис. 8). В таблице 1 приведена оценка достоверности результатов проводимой терапии.
Обсуждение
Полученные результаты свидетельствуют об эффективности использования Церебролизина в лечении распространенного тика, особенно при комплексной терапии, в сочетании с клоназепамом. При синдроме Туретта в некоторых случаях также отмечалась отчетливая положительная динамика, когда препарат назначался пациентам, принимавшим нейролептики в течение продолжительного времени, но без эффекта. По нашим наблюдениям, это относится не только к длительному приему тиаприда, но и галоперидола. Можно предположить, что это связано с антигипоксическим и антиоксидантным действием Церебролизина. Существенным представляется тот факт, что Церебролизин влияет на процессы перекисного окисления липидов и свободнорадикального окисления, играющих важную роль в обмене дофамина и определяющих активность его рецепторов [1,2]. Нарушение антиоксидантной среды на уровне дофаминовых рецепторов изменяет метаболизм нейромедиаторов и удлиняет его инактивацию, что, в свою очередь, приводит к перевозбуждению корковых отделов и снижению тормозного влияния на подкорково–стволовые структуры [4]. Перекисное окисление липидов также выполняет универсальные гомеостатические функции, регулирует состояние эндокринных, нейрорефлекторных, иммунологических механизмов, участвует в адаптации организма к неблагоприятным факторам среды.
Использование Церебролизина в комплексной терапии синдрома Туретта представляется целесообразным в тех случаях, когда тикозная симптоматика сочетается с синдромом гиперактивности с дефицитом внимания. Исследования, проведенные Н.Н. Заваденко и соавт. (2002), выявили существенное улучшение показателей, характеризующих гиперактивность, тревожность, учебные и психосоматические проблемы, а также поведение в целом.
Неэффективность Церебролизина в качестве монотерапии синдрома Туретта можно объяснить сложным, многокомпонентным патогенезом данного заболевания, что требует комплексного подхода к лечению. Это не только не исключает использования Церебролизина в сочетании с нейролептиками, но и позволяет снизить дозы галоперидола и тиаприда. Длительный прием галоперидола в высоких дозах (именно они часто используются в терапии синдрома Туретта) создает опасность развития в качестве осложнения симптомов паркинсонизма и дискинезий. Проведенные в 90–х годах XX века исследования [Balenty, Grassmugg, 1991; В.А. Концевой с соавт. 1997] выявили достоверное снижение экстрапирамидных симптомов у пациентов с паркинсонизмом и поздней дискинезией. Таким образом, Церебролизин не только патогенетически участвует в терапии синдрома Туретта, но и позволяет снизить риск возникновения осложнений, связанных с приемом нейролептиков, а также влияет на сопутствующие тикам состояния, такие как гиперактивность и дефицит внимания.
Доза Церебролизина в данном исследовании (1,0 мл на 10 кг веса) в среднем составляла 5,0 мл в сутки, введение однократное. Переносимость такой дозы была удовлетворительной, побочных эффектов не отмечено. Таким образом, можно рекомендовать указанную дозу в качестве терапевтической.
Следовательно, полученные данные позволяют сделать выводы об эффективности Церебролизина в лечении распространенного тика, а также в комплексной терапии синдрома Туретта.

Литература
1. Гомазков О.А. Апоптоз нейрональных структур и роль нейротрофических ростовых факторов. Биохимические механизмы эффективности пептидных препаратов мозга. //Журн. Неврол. и психиатр., 2002, №7, приложение, с.17–21.
2. Гусев Е.И., Скворцова В.И. Нейропротективная терапия ишемического инсульта. Вторичная нейропротекция. //Журн. Неврол. и психиатр., 2002, №6, с. 3–18.
3. Заваденко Н.Н., Суворинова Н.Ю., Румянцева М.В., Петрухин А.С. Церебролизин в лечении минимальных мозговых дисфункций у детей IV . Международный Симпозиум «Церебролизин: фармакологические эффекты и место в клинической практике». Москва, 2002. С, 66–79,
4. Зыков В.П. Тики детского возраста М.: Научно–медицинская фирма МБН, 2002. 163 с.
5. Концевой В.А., Медведев А.В., Андрусенко М.П., Звенигородская Ю.В., Шешенин В.С. Использование церебролизина для лечения затяжных экстрапирамидных осложнений. //Журн. Неврол. и психиатр. Корсакова 1997., 97 (6): 39–44.
6. Balenty E., Grasmugg B. Erste Ergebnisse der Anwendung von Cerebrolysin an Patienten mit Morbus Parkinson. //Neuropsychiatrie 1987; (1/2): 94–97.
7. Hartbauer M., Hutter–Paier B., Skofitsch G. Windisch Antiapoptotic effects of the peptidergic drug cerebrolysin on primary cultures of embryonic chick cortical neurons. //J Neural Transm 2001; 108(4):459–473.
8. Leonard H.L., Swedo S.E. Paediatric autoimmune neuropsychiatric disorders associated with streptococcal infection (PANDAS) //Int–J–Neuropsychopharmacol. 2001. Jun; 4(2): 191–8.
9. Visvanathan K., Trifiletti R.R., Altemus M., Zabriskie J.B. Autoimmune mechanisms in movement disorders . Semin–Pediatr–Neurol. 2000 Jun; 7(2): 103–7.
Институт мозга человека РАН им. Н.П. Бехтеревой, Санкт-Петербург;
Санкт-Петербургская государственная педиатрическая медицинская академия
- SPIN РИНЦ: 8414-1893
- Scopus AuthorID:
6507009385 - ORCID:
0000-0002-1065-9859
Яковенко Е.А.
Институт мозга человека РАН им. Н.П. Бехтеревой, Санкт-Петербург
Сурушкина С.Ю.
Институт мозга человека РАН им. Н.П. Бехтеревой, Санкт-Петербург;
Санкт-Петербургская государственная педиатрическая медицинская академия
- РИНЦ AuthorID: 179853
- Scopus AuthorID:
35771705500 - ORCID:
0000-0001-9510-7182
Крюкова Е.М.
Оренбургская областная клиническая психиатрическая больница №1, Оренбург, Россия
Паляева С.В.
Оренбургская областная клиническая психиатрическая больница №1, Оренбург, Россия

Эффективность церебролизина при расстройствах аутистического спектра
Авторы:
Чутко Л.С., Яковенко Е.А., Сурушкина С.Ю., Крюкова Е.М., Паляева С.В.
Как цитировать:
Чутко Л.С., Яковенко Е.А., Сурушкина С.Ю., Крюкова Е.М., Паляева С.В. Эффективность церебролизина при расстройствах аутистического спектра. Журнал неврологии и психиатрии им. С.С. Корсакова.
2017;117(9):71‑75.
Chutko LS, Iakovenko EA, Surushkina SYu, Kryukova EM, Palaieva SV. The efficacy of cerebrolysin in the treatment of autism spectrum disorders. S.S. Korsakov Journal of Neurology and Psychiatry. 2017;117(9):71‑75. (In Russ.)
https://doi.org/10.17116/jnevro20171179171-75
Расстройства аутистического спектра (РАС) представляют собой группу дезинтегративных нарушений психического развития, характеризующихся отсутствием способности к социальному взаимодействию, коммуникации, стереотипностью поведения, приводящих к социальной дезадаптации. По современным эпидемиологическим данным, распространенность РАС составляет около 1% в детской популяции [1—3]. Соотношение частоты аутистических расстройств у мальчиков и девочек составляет 4:1 [4].
На сегодняшний день общепризнанной концепции этиологии РАС в мире не существует, но предполагают, что в этиологии и патогенезе этого расстройства большую роль играют генетические факторы. Так, L. Kanner еще в 1943 г. [5] заявил о наследственной природе аутизма на основе наблюдений членов семей детей с аутизом, которые также имели аутистические черты. S. Sandin и соавт. [6] показали, что наличие родного брата или сестры с РАС увеличивает риск возникновения этого расстройства более чем в 10 раз; единокровного или единоутробного брата или сестры с аутизмом — более чем в 3 раза; двоюродного брата или сестры — в 2 раза.
В соответствии с генетическими гипотезами РАС рассматриваются как результат структурных изменений генома на различных уровнях: нуклеотидные замены в генах, изменение числа копий генов, изменение количества хромосом в отдельных клетках [4]. Предполагают также, что важным фактором, увеличивающим риск развития аутизма, является возраст родителей. Популяционный анализ, проведенный А. Reichenberg и соавт. [7], показал, что немолодой возраст отца оказывает значительное влияние на вероятность развития РАС у детей: риск рождения ребенка с РАС у отцов старше 40 лет в 5,75 раза больше, чем у отцов младше 30 лет. Существенное влияние на развитие РАС оказывает и перинатальная патология. Так, низкое значение оценки состояния новорожденного по шкале Апгар (менее 7 баллов) может являться предиктором возникновением РАС [8]. Кроме того, повышенный риск развития РАС связан с преждевременным рождением (раньше 35-й недели) и гипоксией плода [9, 10]. По данным В.Е. Кагана [11], частота выявления органической неврологической симптоматики у детей с аутизмом колеблется от 50 до 84%.
Аутизм характеризуется наличием «триады» нарушений: 1) недостатком социального взаимодействия (отрешенность, отторжение, скудность зрительного контакта, отсутствие адекватных реакций на эмоции других людей); 2) недостатком взаимной коммуникации; 3) стереотипными регрессивными формами поведения [4]. К этому расстройству может быть применима теория «понимание чужого сознания» (theory of mind) [12], подразумевающая способность делать выводы о психическом состоянии другого индивидуума, которое является причиной его действий.
Рецептивная и экспрессивная речь при РАС развивается с задержкой [4]. В раннем детстве отсутствует жестикуляция, гуление и лепет бедные. В экспрессивной речи первые слова (в форме эхолалий, повторов последних и первых слогов слов) появляются на 2—4-м году жизни. Больные произносят их напевно, то четко, то смазано. Словарный запас пополняется медленно, после 3—5 лет отмечаются короткие фразы-штампы, преобладает эгоцентрическая речь.
Характерным симптомом аутизма является также нарушение координации движений. Так, S. Berkeley и соавт. [13] и S. Cassidy и соавт. [14] отметили частые проявления при данной патологии диспраксии. Ч. Ньокиктьен [15] писал, что многие аутисты испытывают трудности при обращении с предметами и инструментами. C. Gillberg [16] предложил концепцию DAMP (дефицит внимания, моторного контроля, восприятия), соединяющую патогенетические звенья, играющие роль в развитии ряда расстройств, в том числе и РАС. Дефицит внимания в таких случаях сочетается с нарушениями координации движений.
Комплексное использование медикаментозных и немедикаментозных методов лечения (дефектологическая, психологическая, педагогическая, нейропсихологическая коррекция, психотерапевтическая, социальная работа с пациентом и его семьей) является одним из основополагающих принципов курации аутистических расстройств у детей [4].
Наличие когнитивных нарушений при РАС приводит к необходимости использования ноотропных препаратов. В исследованиях, выполненных М.Г. Радзивилл и В.М. Башиной [17], был показан положительный эффект применения церебролизина в коррекции поведенческих расстройств и когнитивной дисфункции у детей с аутизмом.
Цель настоящего исследования — оценка клинических и нейрофизиологических изменений, возникающих у детей с разными вариантами РАС на фоне приема препарата церебролизин.
Материал и методы
Под наблюдением находились 43 ребенка с РАС в возрасте 4—6 лет (средний — 4,10±1,6 года): 36 мальчиков и 7 девочек.
Диагностику РАС осуществляли на основании критериев МКБ-10, в соответствии с которыми состояние пациента можно было расценить как детский аутизм (F84.0.)
Из исследования исключались дети с синдромом Аспергера, синдромом Ретта, психотическими расстройствами, наследственными синдромальными формами умственной отсталости, эпилепсией, тяжелой соматической патологией, снижением слуха.
В период исследования и за 3 мес до включения в него пациенты не получали лекарственных препаратов, действующих на ЦНС.
Во время первого визита (день 0) для оценки и объективизации степени выраженности аутизма была использована количественная шкала оценки выраженности детского аутизма (Childhood Autism Rating Scale — CARS).
Всем детям проводилось электроэнцефалографическое исследование (ЭЭГ). Регистрация ЭЭГ производилась с 19 электродов, расположенных на поверхности головы в соответствии с международной системой 10—20, в состоянии покоя с закрытыми и с открытыми глазами (по 3 мин). С целью контроля над движениями глаз выполнялась запись электроокулограммы (ЭОГ). Рутинный анализ кривой состоял в оценке общего функционального состояния головного мозга, региональных изменений ЭЭГ и локализации патологических изменений, наличия/отсутствия эпилептиформных и пароксизмальных изменений, оценке соответствия уровня созревания электрогенеза возрастной норме.
Абсолютная мощность ЭЭГ рассчитывалась до и после проведенного лечения в θ- (4—7 Гц), α1— (7—14 Гц), β1— (14—20 Гц), β2-диапазонах (20—30 Гц) при закрытых глазах. Для анализа количественной ЭЭГ брали отрезки длительностью не менее 15 с.
Перед вычислением спектров ЭЭГ производили предварительную обработку кривой с помощью пакета программ WinEEG, в ходе которой устранялись артефакты. Участки кривой, которые отклонялись от изолинии больше чем 150 мкВ, интервал перед/после 200 мс, медленные волны частотой 0—1 кол/с и амплитудой более 50 мкВ не анализировались. Спектры ЭЭГ вычислялись следующим образом: весь интервал записи ЭЭГ разбивали на отрезки равной длины. Длина отрезка, представляющего собой длительность эпохи анализа, равнялась 4 с. Было установлено 50% перекрывание, каждая следующая эпоха (начиная со второй) выделяла отрезок записи ЭЭГ, сдвинутый относительно предыдущей эпохи на половину ее длины. После разделения интервала записи ЭЭГ на отрезки (эпохи анализа), вычисления для каждого канала выполнялись отдельно.
Всем детям вводили препарат церебролизин (15 инъекций по 2,0 мл через день внутримышечно). Другой терапии за этот период пациенты не получали.
Оценку эффективности лечения с помощью шкалы CARS проводили после окончания курса (на 30-е сутки от начала лечения — 2-й визит) и спустя 30 сут после окончания курса (60-е сутки от начала терапии — 3-й визит). Кроме того, во время 3-го визита проводилась повторная запись ЭЭГ.
Статистическую обработку результатов осуществляли с применением пакета программ Statistica 8.0. Достоверность различий оценивали методами вариационной статистики с использованием критерия Манна—Уитни для независимых выборок и критерия Вилкоксона для парных случаев непараметрических распределений. Данные представлены в виде среднего и стандартного отклонения. Статистический анализ данных ЭЭГ проводили с помощью двухфакторного дисперсионного анализа для повторных измерений с факторами: номер пробы (до и после лечения; число уровней 2) и локализация электродов (число уровней 19). Различия считались достоверными при значениях p<0,05.
Результаты
По анализу анамнестических данных (наличие патологии перинатального периода) пациенты по классификации аутистических расстройств А.С. Тиганова и В.М. Башиной (цит. по [4]) были условно разделены на две группы. В 1-ю группу вошли 23 (53,5%) ребенка, 19 мальчиков и 4 девочки, с детским аутизмом эндогенным, во 2-ю группу — 20 (46,5%) детей, 17 мальчиков и 3 девочки, с детским аутизмом экзогенным, связанным с органическим поражением ЦНС. Оценка выраженности расстройства по шкале CARS свидетельствовала о большей величине этого показателя в 1-й группе (табл. 1).

При визуальном анализе ЭЭГ у всех детей в исследуемых группах не регистрировалось эпилептиформной активности, пароксизмальных изменений, а также грубых очаговых изменений биопотенциалов.
У 15 (65,2%) детей в 1-й группе при закрытых глазах регистрировался нерегулярный α-ритм в затылочных отведениях, у 7 (30,4%) пациентов — группы α-волн в затылочных отведениях, у 1 пациента — легкие признаки задержки электрогенеза. Доминирующим ритмом являлась α-подобная θ-активность, регистрировались одиночные α-волны. В затылочных отведениях у 20 (87%) пациентов наблюдалось наличие полифазных потенциалов, заостренных волн.
Во 2-й группе при закрытых глазах у 9 (45,0%) детей наблюдался нерегулярный α-ритм в затылочных отведениях обоих полушарий, у 5 (25%) детей основной ритм представлен нерегулярными группами α-волн в затылочных отведениях обоих полушарий, еще у 5 (25%) пациентов отмечалась задержка электрогенеза, доминирующей являлась θ-активность. У 17 (85,0%) пациентов в фоновой ЭЭГ в затылочных отведениях обоих полушарий субдоминировала θ-активность. У 7 (35,0%) детей регистрировалось наличие полифазных потенциалов, заостренных волн.
При повторном обследовании после окончания курса лечения признаки улучшения были зарегистрированы у 27 (62,8%) детей. Положительной динамики не выявили у 16 (37,2%) пациентов. После курса лечения родители отмечали увеличение речевой активности. По их словам, дети стали лучше понимать обращенную речь, чаще прибегать к жестам, улучшился зрительный контакт.
Клиническое улучшение (по словам родителей) отмечено у 13 (56,5%) детей в 1-й группе и у 14 (70,0%) детей во 2-й группе. Оценка состояния с помощью шкалы CARS показала снижение данного показателя в обеих группах, более выраженное во 2-й группе (см. табл. 1).
Катамнестическое обследование (на 60-е сутки) показало, что полученные клинические результаты не ухудшались у абсолютного большинства детей с зарегистрированным ранее улучшением, при этом следует отметить достоверное улучшение показателей СARS (табл. 2). Часть детей стали чаще использовать речь для общения. Большая степень улучшения также была достигнута во 2-й группе.

У 16 (37,8%) пациентов в середине курса терапии наблюдалось умеренное увеличение гиперактивности. Подобная симптоматика была отмечена родителями при 2-м визите (30-е сутки). Данные изменения отмечались у 7 (30,4%) детей в 1-й группе и 9 (45,0%) детей во 2-й группе. Вскоре после окончания курса проявления гиперактивности уменьшились, и на 3-м визите (60-е сутки) этот побочный эффект был зарегистрирован только у 10 (23,3%) пациентов: 4 (17,3%) пациента в 1-й группе и 6 (30,0%) — во 2-й группе. Проявления гиперактивности на фоне лечения были отмечены у детей с более выраженным улучшением речевого развития.
При повторной ЭЭГ в 1-й группе после лечения визуальный анализ показал, что у 13 (56,5%) пациентов увеличилось количество сгруппированных α-волн, уменьшилось количество θ-волн в затылочных отведениях обоих полушарий.
Проведенный статистический анализ данных абсолютной мощности ЭЭГ при закрытых глазах до и после лечения выявил, что в 1-й группе увеличение мощности волн α-диапазона в затылочно-теменных отведениях левого полушария (O1, Р3) и уменьшение этого диапазона в лобном отведении правого полушария (F4) различались статистически достоверно (p<0,05 и p<0,05 соответственно). В θ-диапазоне статистически достоверное уменьшение мощности наблюдали в лобном отведении правого полушария (F4) и в теменном отведении правого полушария (Р4) (p<0,03 и p<0,05 соответственно) (см. табл. 2).
После лечения во 2-й группе при визуальном анализе на фоне закрытых глаз у 13 (65,0%) детей наблюдали увеличение мощности α-ритма в затылочных отведениях обоих полушарий, уменьшение представленности волн α-диапазона в лобных отведениях (больше справа) и в центральных отведениях обоих полушарий. У 12 (60,0%) детей уменьшилось количество диффузных θ-волн в лобно-центрально-височных отведениях (больше справа), в затылочно-теменных отведениях уменьшилось количество одиночных θ-волн и групп θ-волн.
Согласно данным сравнительного анализа абсолютной мощности до и после лечения, во 2-й группе в α-диапазоне статистически значимые результаты наблюдались в затылочных отведениях обоих полушарий после проведенного лечения, отмечалось увеличение спектральной мощности (p<0,03), тогда как в теменно-центральных отведениях обоих полушарий отмечалось статистически значимое уменьшение мощности волн α-диапазона (p<0,05), в лобных отведениях статистически значимое уменьшение отмечалось в отведении F4 и Fz (p<0,05). В θ-диапазоне в затылочно-теменных отведениях обоих полушарий и в лобных отведениях (F4, Fz) наблюдалось статистически значимое уменьшение мощности, p<0,05 и p<0,03 соответственно (см. табл. 2, рисунок).

Обсуждение
По мнению В.М. Башиной [18], в случаях коморбидности аутизма с органическим поражением ЦНС следует определять их как аутистическиподобные расстройства (синдромы) до тех пор, пока в этих состояниях не будут представлены все феномены аутизма, предполагая возможность не только эндогенной, но и иной этиологии. Согласно ее наблюдениям, у таких детей присутствуют торпидность, дисфории, неврологические симптомы, более выражена тотальность умственного недоразвития, стереотипная деятельность сводится к примитивным, привычным патологическим действиям, отсутствуют позитивные психопатологические расстройства. С.С. Мнухин и соавт. (цит по [18]) в свое время выдвинули концепцию органического происхождения аутизма у детей, согласно которой имело место частичное или полное фенокопирование синдрома Каннера. В.Е. Каган [11] органическим аутизмом обозначал случаи, не удовлетворяющие всем основным диагностическим требованиям раннего детского аутизма и обнаруживающие признаки органической патологии головного мозга.
Результаты настоящего исследования показывают нейрофизиологические особенности преимущественно эндогенного и экзогенного (органического) вариантов аутизма. Так, у детей с органическим вариантом оказались более выражены признаки несформированности корково-подкорковых взаимоотношений, тогда как у детей в 1-й группе эти признаки менее выражены. Таким образом, у детей с органическим аутизмом, характеризующимся меньшей степенью аутистической симптоматики по шкале CARS, по данным ЭЭГ наблюдалась большая степень функциональной незрелости коры головного мозга, отмечались небольшие патологические изменения биопотенциалов. Следует отметить, что выделение данных вариантов носит все же условный характер, и они могут являться частями одного континуума РАС, а именно детского аутизма (F.84.00).
При лечении органических заболеваний нервной системы у детей, сопровождающихся когнитивными нарушениями, традиционно применяются нейропротективные средства, одно из ведущих мест среди которых занимает препарат церебролизин.
Проведенное исследование выявило позитивные клинические изменения после курса церебролизина, при этом более выраженный эффект достигнут при лечении органического аутизма. Катамнестическое наблюдение показало, что полученные в ходе лечения положительные результаты не только не уменьшились в течение месяца после окончания терапии, но, наоборот, наблюдалась тенденция к дальнейшему улучшению. Данный факт можно объяснить позитивным влиянием церебролизина на нейропластичность. Интересно отметить, что побочный эффект в виде гиперактивности часто встречался у детей с более выраженным улучшением по шкале CARS и уменьшением степени речевых нарушений. Таким образом, можно предположить, что появление гиперактивности является прогностически благоприятным признаком.
При повторной ЭЭГ после лечения (60-й день, 3-й визит) в обеих группах наблюдали положительные сдвиги в снижении выраженности проявлений функциональной незрелости структур головного мозга пациентов, таких как увеличение мощности волн α-диапазона в затылочных отведениях обоих полушарий и уменьшение мощности этого диапазона в лобных отведениях. Таким образом, стал лучше выражен градиент распределения мощности α-диапазона «лобные отведения — затылочные отведения», один из признаков созревания электрогенеза. Также отмечалось уменьшение мощности волн медленноволнового спектра (θ-волны) в затылочно-теменных отделах и в лобных отделах обоих полушарий. Однако у детей с органическим аутизмом эти положительные изменения были более выражены по сравнению с детьми с эндогенным аутизмом. Ни в одном случае применение церебролизина не привело к появлению эпилептиформной активности на ЭЭГ.
Механизм действия церебролизина подобен естественным нейротрофическим факторам. Церебролизин является препаратом с доказанной нейронспецифической, нейротрофической активностью, аналогичной естественным факторам нейронального роста, но проявляющейся, в отличие от них, в условиях периферического введения.
В связи со сказанным интересно отметить, что в литературе имеются исследования [19—21], показавшие, что у детей с РАС нарушена работа системы зеркальных нейронов (MNS), влияющая на восприятие других людей. Дисфункция MNS-систем, возникшая, возможно, в результате комбинации генетических факторов и неблагоприятных факторов окружающей среды, может приводить к нарушению представления «я—другие» и быть причиной социального и коммуникативного дефицита у больных с РАС [22]. Можно предположить, что в результате нейротрофической активности церебролизина улучшается активность системы зеркальных нейронов.
Результаты настоящего исследования позволяют рекомендовать препарат церебролизин в комплексной терапии аутизма.
Авторы заявляют об отсутствии конфликта интересов.
Мы используем файлы cооkies для улучшения работы сайта. Оставаясь на нашем сайте, вы соглашаетесь с условиями
использования файлов cооkies. Чтобы ознакомиться с нашими Положениями о конфиденциальности и об использовании
файлов cookie, нажмите здесь.
ЭТОТ СТРАШНЫЙ ЦЕРЕБРОЛИЗИН, НУЖЕН ЛИ?
Неврология
Дорогие мамочки! Поделитесь опытом, пожалуйста: кому детям кололи церебролизин. Как перенесли дети, не было ли побочных эффектов серьезных. Наш невролог усиленно советует нам эти уколы, считает, что доча отстает в развитии. С рождения был гипотонус, лечили массажами, физиотерапией, каждый день в ванне купаемся (тоже говорят хорошее средство). Раньше много на фитболе занимались, сейчас дочке не нравится уже почему-то. Большая стала-1 год исполнился. Развивалась более-менее сначала: в 2 мес. голову держала норм, в 4 месяца переворачивалась, в 5 встала на четвереньки и раскачивалась, в 6 поползла на животе, а потом мы как-то затормозили: села сама, встала на ноги и поползла на четвереньках она только в 10,5 мес. Массажист сказала: слабая спина. Сейчас нам годик, доча немного ходит приставным шагом держась за мебель,сидит со сгорбленной спиной, не может видно прямо держать, сама не ходит, немного водим за ручки, но она быстро устает.Еще мы оч. мало лепечем, раньше гулили тоже мало, говорим только одно слово «мама», когда жалуемся или просим есть. Ребенок спокойный, беспокоит, что много спит иногда, хотелось чтобы была поактивнее. Сама может долго заниматься игрушками, книжками. Но бывают и «припадки» двигательной активности-ползает она уже шустро. Возможно, темперамент такой, мама с папой тоже не электровеники:) Стоит диагноз-ППЦНС, гипотонус, ЗРР. Все в раздумьях насчет церебролизина: ноотропный препарат все-таки и ставить нам его придется не в стационаре, а скорее всего дома. С др. стороны, можно упустить момент, когда этот курс уколов может действительно помочь. Всем откликнувшимся огромное спасибо!
Описание препарата Церебролизин® (раствор для инъекций) основано на официальной инструкции, утверждено компанией-производителем в 2022 году
Дата согласования: 25.08.2022
Особые отметки:
Содержание
- Фотографии упаковок
- ATX
- Фармакологическая группа
- Нозологическая классификация (МКБ-10)
- Состав
- Описание лекарственной формы
- Фармакологическое действие
- Характеристика
- Фармакодинамика
- Фармакокинетика
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Производитель
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Заказ в аптеках Москвы
Фотографии упаковок

25.08.2022

25.08.2022

25.08.2022
ATX
Фармакологическая группа
Состав
| Раствор для инъекций | 1 мл |
| действующее вещество: | |
| Церебролизин® концентрат (комплекс пептидов, полученных из головного мозга свиньи) | 215,2 мг |
| вспомогательные вещества: натрия гидроксид; вода для инъекций |
Описание лекарственной формы
Раствор для инъекций: прозрачный, желтовато-коричневого цвета.
Фармакологическое действие
Характеристика
Активная фракция препарата Церебролизин® представлена пептидами, молекулярная масса которых не превышает 10000 Да.
Фармакодинамика
Церебролизин® содержит низкомолекулярные биологически активные нейропептиды, которые проникают через ГЭБ и непосредственно поступают к нервным клеткам. Препарат обладает органоспецифическим мультимодальным действием на головной мозг, т.е. обеспечивает метаболическую регуляцию, нейропротекцию, функциональную нейромодуляцию и нейротрофическую активность.
Метаболическая регуляция. Церебролизин® повышает эффективность аэробного энергетического метаболизма головного мозга, улучшает внутриклеточный синтез белка в развивающемся и стареющем головном мозге.
Нейропротекция. Церебролизин® защищает нейроны от повреждающего действия лактат-ацидоза, предотвращает образование свободных радикалов, повышает выживаемость и предотвращает гибель нейронов в условиях гипоксии и ишемии, снижает повреждающее нейротоксическое действие возбуждающих аминокислот (глутамат).
Нейротрофическая активность. Церебролизин® — единственный ноотропный пептидергический препарат с доказанной нейротрофической активностью, аналогичной действию естественных факторов нейронального роста (NGF), но проявляющейся в условиях периферического введения.
Функциональная нейромодуляция. Церебролизин® оказывает положительное влияние при нарушениях когнитивных функций, улучшает процессы запоминания.
Фармакокинетика
Сложный состав препарата Церебролизин®, активная фракция которого состоит из сбалансированной и стабильной смеси биологически активных олигопептидов, обладающих суммарным полифункциональным действием, не позволяет провести обычный фармакокинетический анализ отдельных компонентов.
Показания
- болезнь Альцгеймера;
- синдром когнитивных нарушений различного генеза, включая деменцию;
- хроническая цереброваскулярная недостаточность (хроническая ишемия мозга, дисциркуляторная энцефалопатия);
- ишемический инсульт;
- черепно-мозговая травма;
- задержка умственного развития у детей;
- синдром дефицита внимания и гиперактивность у детей;
- при эндогенной депрессии, резистентной к антидепрессантам, — в комплексной терапии.
Противопоказания
- индивидуальная непереносимость препарата;
- тяжелая почечная недостаточность;
- эпилептический статус.
С осторожностью: аллергические диатезы; заболевания эпилептического характера, в т.ч. при генерализованной эпилепсии (ввиду возможного увеличения частоты приступов).
Применение при беременности и кормлении грудью
В период беременности и во время грудного вскармливания препарат Церебролизин® следует применять только после тщательного анализа соотношения положительного эффекта лечения и риска, связанного с его проведением.
Результаты экспериментальных исследований не дают оснований полагать, что препарат Церебролизин® обладает тератогенным действием или оказывает токсическое влияние на плод. Однако аналогичные клинические исследования не проводились.
Способ применения и дозы
В/м (до 5 мл), в/в (до 10 мл), в/в путем медленной инфузии (от 10 до 50 мл).
Дозы и продолжительность лечения зависят от характера и тяжести заболевания, а также от возраста больного. Возможно назначение однократных доз, величина которых может достигать 50 мл, однако более предпочтительно проведение курса лечения. Рекомендуемый оптимальный курс лечения — ежедневные инъекции в течение 10–20 дней.
Болезнь Альцгеймера — 10–30 мл.
Синдром когнитивных нарушений различного генеза, включая деменцию, — 5–30 мл.
Хроническая цереброваскулярная недостаточность (хроническая ишемия мозга, дисциркуляторная энцефалопатия) — 5–20 мл.
Ишемический инсульт: острый период — 10–50 мл; восстановительный период — 5–30 мл.
Черепно-мозговая травма — 5–50 мл.
Задержка умственного развития у детей — 0,1–0,2 мл/кг.
Гиперактивность и дефицит внимания у детей — 0,1–0,2 мл/кг.
При эндогенной депрессии, резистентной к антидепрессантам (в комплексной терапии), — 5–30 мл.
Для повышения эффективности лечения могут проводиться повторные курсы, до тех пор пока наблюдается улучшение состояния пациента вследствие лечения. После проведения первого курса периодичность назначения доз может быть снижена до 2 или 3 раз в нед.
Дозы от 10 до 50 мл рекомендуется вводить только посредством медленных в/в инфузий после разведения предложенными стандартными растворами для инфузий. Продолжительность инфузий составляет от 15 до 60 мин.
Побочные действия
Реклама: ООО «РЛС-Патент», ИНН 5044031277
Частота проявлений побочных действий определялась в соответствии с рекомендациями ВОЗ: очень часто (≥1/10); часто ( от ≥1/100 до <1/10); нечасто (от ≥1/1000 до <1/100); редко (от ≥1/10000 до <1/1000); очень редко, включая отдельные сообщения (<1/10000).
Со стороны иммунной системы: очень редко — повышенная индивидуальная чувствительность, аллергические реакции, кожные реакции, боли в шее, голове и конечностях, лихорадка, легкие боли в спине, одышка, озноб, коллаптоидное состояние.
Со стороны обмена веществ и питания: редко — потеря аппетита.
Co стороны психики: редко — предполагаемый эффект активации сопровождается возбуждением, проявляющимся агрессивным поведением, спутанностью сознания, бессонницей.
Со стороны нервной системы: редко — слишком быстрое введение препарата может привести к головокружению; очень редко — отдельные случаи генерализованной эпилепсии и один случай развития судорог был связан с применением препарата Церебролизин®.
Со стороны сердца: очень редко — слишком быстрое введение препарата может привести к учащению сердцебиения и аритмии.
Со стороны ЖКТ: очень редко — диспепсия, диарея, запор, тошнота, рвота.
Со стороны кожи и подкожных тканей: редко — при чрезмерно быстром введении возможно ощущение жара, потливость, зуд.
Общие расстройства и нарушения в месте введения: очень редко — покраснение, зуд, жжение в месте введения.
По результатам одного исследования сообщалось о связи между применением препарата в редких случаях (от ≥1/10000 до <1/1000) с гипервентиляцией, артериальной гипертонией, гипотонией, усталостью, тремором, возможным развитием депрессии, апатии и/или сонливости, гриппоподобных симптомах (простуда, кашель, инфекции дыхательных путей).
Поскольку препарат Церебролизин® применяют в основном у пожилых пациентов, вышеперечисленные симптомы заболеваний являются типичными для этой возрастной группы и часто возникают также без применения препарата. Следует учесть, что некоторые нежелательные эффекты (возбуждение, артериальная гипертония, артериальная гипотония, вялость, тремор, депрессия, апатия, головокружение, головная боль, одышка, диарея, тошнота) были выявлены в ходе клинических испытаний и возникали в равной мере как у пациентов, получавших препарат Церебролизин®, так и у пациентов группы плацебо.
Если любые из указанных в инструкции побочных эффектов усугубляются или пациент заметил любые другие побочные эффекты, не указанные в инструкции, следует сообщить об этом лечащему врачу.
Уведомление в случае подозрения на побочные эффекты
Важно сообщать о побочных эффектах после регистрации лекарственного препарата с целью обеспечения непрерывного мониторинга отношения риска и пользы препарата.
Медицинских работников просят сообщать обо всех случаях побочных эффектов, наблюдаемых при использовании препарата, через национальные системы сообщения о нежелательных реакциях и/или по адресу организации, принимающей претензии потребителей.
Взаимодействие
С учетом фармакологического профиля препарата Церебролизин® следует уделить особое внимание возможным аддитивным эффектам при совместном назначении с антидепрессантами, в т.ч. ингибиторами МАО. В таких случаях рекомендуется снизить дозу антидепрессанта.
Применение высоких доз препарата Церебролизин® (30–40 мл) в сочетании с высокими дозами ингибиторов МАО может вызвать повышение АД.
Не следует смешивать в одном растворе для инфузий препарат Церебролизин® и сбалансированные растворы аминокислот.
Препарат Церебролизин® несовместим с растворами, в состав которых входят липиды, и с растворами, изменяющими рН среды (5,0–8,0).
Передозировка
Не выявлено.
Особые указания
При чрезмерно быстром выполнении инъекций возможно ощущение жара, потливость, головокружение, поэтому препарат следует вводить медленно.
Проверена и подтверждена совместимость препарата (в течение 24 ч при комнатной температуре и наличии освещения) со следующими стандартными растворами для инфузий:
— 0,9% раствор натрия хлорида (9 мг NaCl/мл);
— раствор Рингера (Na+ — 153,98 ммоль/л; Са2+ — 2,74 ммоль/л; К+ — 4,02 ммоль/л; Cl− — 163,48 ммоль/л);
— 5% раствор глюкозы.
Допускается одновременное назначение препарата Церебролизин® с витаминами и препаратами, улучшающими коронарное кровообращение, однако эти препараты не следует смешивать в одном шприце с препаратом Церебролизин®.
Использовать следует только прозрачный раствор и только однократно.
Влияние на способность к управлению транспортными средствами. Клинические испытания показали, что препарат Церебролизин® не оказывает влияние на способность к управлению транспортными средствами и использованию механизмов.
Форма выпуска
Раствор для инъекций.
При производстве на производственных площадках ЭВЕР Фарма Йена ГмбХ, Германия
Ампулы 1, 2 мл. По 1 или 2 мл в стеклянных ампулах коричневого цвета. По 10 ампул помещают в контурную ячейковую упаковку из ПВХ, покрытую вощеной бумагой. 1 контурную ячейковую упаковку с инструкцией по применению помещают в картонную пачку, на которую дополнительно могут быть нанесены защитные наклейки.
Ампулы 5, 10, 20 мл. По 5, 10, 20 мл в стеклянных ампулах коричневого цвета. По 5 ампул в контурной ячейковой упаковке из ПВХ, покрытой вощеной бумагой. 1 контурную ячейковую упаковку с инструкцией по применению помещают в картонную пачку, на которую дополнительно могут быть нанесены защитные наклейки.
При производстве на производственных площадках ЗАО «ФармФирма «Сотекс», Россия
Ампулы 2 мл. По 2 мл в стеклянных ампулах коричневого цвета с желтой точкой. По 5 ампул помещают в контурную ячейковую упаковку из ПВХ, покрытую пленкой из ПЭТ. 2 контурные ячейковые упаковки с инструкцией по применению помещают в картонную пачку, на которую дополнительно могут быть нанесены защитные наклейки.
Ампулы 5, 10, 20 мл. По 5, 10, 20 мл в стеклянных ампулах коричневого цвета с желтой точкой. По 5 ампул помещают в контурную ячейковую упаковку из ПВХ, покрытую пленкой из ПЭТ.
Одну контурную ячейковую упаковку с инструкцией по применению помещают в картонную пачку, на которую дополнительно могут быть нанесены защитные наклейки.
Производитель
Производитель готовой лекарственной формы, фасовщик (первичная упаковка). ЭВЕР Фарма Йена ГмбХ, Отто-Шотт-штрассе 15, 07745 Йена, Германия; ЗАО «ФармФирма «Сотекс», Россия, Московская обл., Сергиево-Посадский муниципальный р-н, сельское поселение Березняковское, пос. Беликово, 10, 11, 12.
Вторичная (потребительская) упаковка. ЭВЕР Фарма Йена ГмбХ, Брюсселер штрассе 18, 07747 Йена, Германия; ЗАО «ФармФирма «Сотекс», Россия, Московская обл., Сергиево-Посадский муниципальный р-н, сельское поселение Березняковское, пос. Беликово, 10, 11, 12.
Выпускающий контроль качества. ЭВЕР Нейро Фарма ГмбХ, Обербургау 3, 4866 Унтерах-ам-Аттерзее, Австрия; ЗАО «ФармФирма «Сотекс», Россия, Московская обл., Сергиево-Посадский муниципальный р-н, сельское поселение Березняковское, пос. Беликово, 10, 11, 12.
Наименование держателя (владельца) регистрационного удостоверения. ЭВЕР Нейро Фарма ГмбХ, Обербургау 3, 4866 Унтерах-ам-Аттерзее, Австрия.
Организация, принимающая претензии потребителей. ООО «ЭВЕР Нейро Фарма». 107061, Россия, Москва, Преображенская пл., 8.
Тел.: (495) 933-87-02.
info.ru@everpharma.com
Условия отпуска из аптек
По рецепту.
Условия хранения
В защищенном от света месте, при температуре не выше 25 °C.
Хранить в недоступном для детей месте.
Срок годности
5 лет.
Не применять по истечении срока годности, указанного на упаковке.
Описание проверено
-
Крылов Юрий Федорович
(фармаколог, доктор медицинских наук, профессор, академик Международной академии информатизации)
Опыт работы: более 34 лет
Аналоги по действующему веществу не найдены.
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.
