Признание атеротромбоза основой патогенеза большинства сердечно-сосудистых заболеваний (ССЗ), успехи в изучении молекулярных механизмов тромбообразования оказали влияние на развитие антитромбоцитарной терапии и способствовали появлению новых препаратов [1]. Наиболее изученными и широко применяемыми в клинической практике антитромбоцитарными препаратами в настоящее время являются ацетилсалициловая кислота (АСК) и клопидогрел.
В качестве лекарственного средства АСК известна с 1899 г. Несмотря на более чем 100-летний опыт использования и появление в последние годы новых антиагрегантов, АСК удалось сохранить за собой позиции «золотого» стандарта антитромбоцитарной терапии. В основе антитромбоцитарного действия АСК лежит ее способность необратимо ингибировать фермент циклооксигеназу (ЦОГ) тромбоцитов, вследствие чего снижается образование тромбоксана А2 — мощного стимулятора агрегации тромбоцитов и вазоконстриктора. Циклооксигеназа имеет две изоформы: ЦОГ-1 и ЦОГ-2. Притом, что АСК блокирует обе изоформы, ее активность в отношении ЦОГ-1 в тромбоцитах в 50–100 раз выше, чем влияние на ЦОГ-2 в моноцитах и других клетках воспаления. Поскольку тромбоциты не имеют ядра и поэтому не способны синтезировать белки, необратимое ингибирование ЦОГ-1 приводит к тому, что блокада синтеза тромбоксана А2 под действием АСК сохраняется на протяжении всего периода жизни тромбоцитов (в течение 7–10 дней). Именно способность необратимо блокировать ЦОГ-1 обусловливает стабильный и длительный антитромбоцитарный эффект АСК [2].
Клопидогрел по химической структуре относится к тиенопиридинам. Механизм антитромбоцитарного действия клопидогрела отличается от такового АСК и заключается в селективном и необратимом ингибировании P2Y12-рецепторов тромбоцитов, что, в свою очередь, приводит к угнетению стимуляции аденилатциклазного механизма и блокированию связанного с ним сигнала, направленного на усиление агрегации тромбоцитов [3]. Клопидогрел является пролекарством и метаболизируется в печени в активный метаболит с помощью нескольких изоферментов цитохрома Р450 (CYP). Исследования последних лет показали, что существуют полиморфизмы генов, носительство которых ассоциируется со снижением активности ферментов, участвующих в превращении клопидогрела в активный метаболит [4]. Так, носительство аллеля CYP2C19*1 обеспечивает полностью функционирующий метаболизм, тогда как носительство аллелей CYP2C19*2 и CYP2C19*3 уменьшает функциональную активность ферментов, метаболизирующих клопидогрел. Установлено, что носительство различных аллелей CYP2C19 определяет не только фармакокинетику активного метаболита клопидогрела, но и антитромбоцитарный эффект. По данным ряда исследований [5–10], носительство аллелей CYP2C19*2 и CYP2C19*3 соотносится с меньшим подавлением агрегации тромбоцитов и более высокой частотой неблагоприятных сердечно-сосудистых событий (включая тромбозы внутрикоронарных стентов) у больных, получающих клопидогрел в стандартной дозировке (75 мг/сут).
Важно отметить, что при одновременном применении АСК и клопидогрела антитромбоцитарный эффект усиливается. Предполагают, что это обусловлено синергизмом между двумя препаратами в подавлении агрегации тромбоцитов, индуцированной коллагеном [3, 11].
Ацетилсалициловая кислота, безусловно, является более изученным препаратом, чем клопидогрел, поэтому неудивительно, что спектр ее применения в кардиологии значительно шире. Назначение АСК позволяет уменьшить частоту неблагоприятных исходов у больных стабильной и нестабильной стенокардией, инфарктом миокарда с наличием зубца Q на ЭКГ и без такового, после чрескожных коронарных вмешательств и операции аортокоронарного шунтирования, при цереброваскулярной болезни, а также у пациентов с перемежающейся хромотой атеросклеротического происхождения. Согласно рекомендациям европейских, американских и российских медицинских сообществ при всех вышеперечисленных заболеваниях и состояниях рекомендован неограниченно долгий (пожизненный) прием АСК. В разных рекомендациях при одном и том же заболевании предписано использовать различные дозы АСК (так, например, в Европе поддерживающая доза АСК обычно составляет 75–100 мг/сут, а в США — 81 мг/сут), но предпочтительны все-таки низкие дозы АСК как минимально эффективные.
Клопидогрел рекомендуется использовать в основном в комбинации с АСК (так называемая двойная антитромбоцитарная терапия) при инфаркте миокарда и нестабильной стенокардии, а также у больных, подвергнутых чрескожным коронарным вмешательствам, поскольку, как было показано в многочисленных крупных исследованиях, добавление клопидогрела к АСК в этих ситуациях превосходит по эффективности монотерапию АСК. Монотерапия клопидогрелом как альтернатива монотерапии АСК может быть рекомендована только при атеросклеротическом поражении артерий нижних конечностей [12–14] и в качестве средства вторичной профилактики у больных, перенесших острое нарушение мозгового кровообращения [15–17]. Во всех остальных случаях монотерапия клопидогрелом возможна лишь при непереносимости АСК.
Рассмотрим более подробно некоторые аспекты применения АСК и клопидогрела в кардиологической практике.
Первичная профилактика ССЗ
Ацетилсалициловая кислота — единственный антитромбоцитарный препарат, рекомендованный для первичной профилактики ССЗ. В разное время были выполнены рандомизированные контролируемые исследования по первичной профилактике ССЗ: British Doctors’ Study (BDT), US Physicians’ Health Study (PHS), Thrombosis Prevention Trial (TPT), Hypertension Optimal Treatment Trial (HOT), Primary Prevention Project (PPP) и Women’s Health Study (WHS). В 2009 году опубликованы результаты метаанализа [18], объединившего все 6 исследований, который включил 95 000 человек, 660 000 пациенто-лет, 3 554 неблагоприятных сердечно-сосудистых события (табл.). В целом снижение риска неблагоприятных сердечно-сосудистых событий у принимавших АСК составило 12% (p = 0,0001) и было достигнуто, главным образом, за счет уменьшения риска нефатального инфаркта миокарда. Терапия АСК практически не влияла на общее количество инсультов, но снижала риск ишемического инсульта на 14% (р = 0,05). Сердечно-сосудистая смертность у получавших АСК и плацебо не различалась, причем как у мужчин, так и у женщин. Частота больших (главным образом, желудочно-кишечных) кровотечений оказалась выше у получавших АСК (0,1% в год для АСК против 0,07% в год для плацебо, p < 0,0001). Метаанализ показал, что прием АСК позволяет предотвратить около 8 случаев инфаркта миокарда на каждую 1 000 мужчин и примерно 2 ишемических инсульта на каждую 1 000 женщин. Также было отмечено, что назначение АСК с целью первичной профилактики способно предупредить развитие 5 нефатальных неблагоприятных сердечно-сосудистых событий при риске возникновения 3 желудочно-кишечных и 1 внутричерепного кровотечения на 10 000 пациентов в год.

Кроме того, в исследовании НОТ [19] была продемонстрирована польза назначения низких доз АСК (75 мг/сут) больным артериальной гипертонией с хорошо подобранной гипотензивной терапией. Так, на фоне приема АСК снижение риска развития инфаркта миокарда составило 36% (р = 0,002), любых сердечно-сосудистых осложнений — 15% (р = 0,003). Анализ подгрупп показал, что у некоторых категорий пациентов польза от применения АСК превышала риск геморрагических осложнений. Риск любых неблагоприятных сердечно-сосудистых событий был ниже на 45% у больных артериальной гипертензией с уровнем сывороточного креатинина ≥ 115 мкмоль/л, на 20% — при исходном систолическом АД ≥ 180 мм рт. ст., на 29% — при исходном диастолическом АД ≥ 107 мм рт. ст., на 22% — у пациентов с уровнем риска ССЗ ≥ 10% по шкале SCORE. При этом наибольший эффект терапии АСК был отмечен у больных с высоким и очень высоким уровнем риска ССЗ. Полученные результаты позволили экспертам рекомендовать низкие дозы АСК (75–150 мг/сут) больным артериальной гипертензией с умеренным повышением уровня сывороточного креатинина или при очень высоком риске сердечно-сосудистых осложнений даже при отсутствии других ССЗ [20, 21].
В настоящее время нет данных об эффективности и безопасности монотерапии клопидогрелом в первичной профилактике ССЗ.
Использование комбинации АСК и клопидогрела с целью первичной профилактики ССЗ у лиц с высоким риском также нецелесообразно. Это продемонстрировал анализ подгрупп в исследовании CHARISMA [22]. Целью этого многоцентрового рандомизированного плацебо-контролируемого клинического испытания являлось сравнение терапии клопидогрелом (75 мг/сут) и плацебо у пациентов, получающих низкие дозы АСК (75–162 мг/сут) с целью как первичной, так и вторичной профилактики сердечно-сосудистых осложнений. В него включили 15 603 пациента в возрасте 45 лет и старше (средний возраст 64 года; 70% мужчин) с документированными симптомными ССЗ (ишемическую болезнь сердца имели около 50% участников; цереброваскулярную болезнь — около 35%; атеросклеротическое поражение артерий нижних конечностей — около 23%), а также с множественными факторами риска атеротромбоза. Половина пациентов (n = 7 802) получали клопидогрел и АСК (группа вмешательства), остальные участники (n = 7 801) — плацебо и АСК (группа контроля), однако прием препаратов досрочно прекратили 20,4% и 18,2% больных соответственно (p < 0,001), в том числе 4,8% и 4,9% — из-за развития побочных эффектов. Средний срок наблюдения составил 28 месяцев. Частота возникновения первичной конечной точки (инфаркт миокарда + инсульт + сердечно-сосудистая смерть) в группах клопидогрела и плацебо составила 6,8% и 7,3% соответственно (относительный риск (ОР) 0,93; 95% доверительный интервал (ДИ) 0,83–1,05; р = 0,22). По частоте серьезных кровотечений статистически значимых различий между группами клопидогрела и плацебо обнаружено не было (1,7% против 1,3% соответственно; ОР 1,25; 95% ДИ 0,97–1,61; р = 0,09), хотя имел место тренд в пользу плацебо. Таким образом, в целом для изученной выборки пациентов комбинированная терапия клопидогрелом и АСК не обнаружила преимуществ перед монотерапией АСК.
Анализ подгрупп показал, что среди 3 284 обследуемых с множественными факторами риска ССЗ частота первичной конечной точки в группе клопидогрела оказалась выше, чем в группе плацебо (6,6% против 5,5% соответственно), что сопровождалось увеличением риска неблагоприятных сосудистых событий на 20% (ОР 1,20; 95% ДИ 0,91–1,59; р = 0,20), которое, тем не менее, не достигало уровня статистической значимости. Однако при этом значительно возрастала смертность как от любых причин (5,4% против 3,8% в группе плацебо; р = 0,04), так и сердечно-сосудистая (3,9% против 2,2% в группе плацебо; р = 0,01). Результаты именно этого фрагмента исследования позволили сделать вывод о нецелесообразности использования монотерапии клопидогрелом с целью первичной профилактики ССЗ.
Напротив, использование клопидогрела с целью вторичной профилактики ССЗ в этом же исследовании оказалось более эффективным. На это указывает анализ подгрупп, включивший 12 153 симптомных больных с подтвержденными ССЗ. У этой категории пациентов частота первичной конечной точки в группе клопидогрела была ниже, чем в группе плацебо (6,9% против 7,9% соответственно), что сопровождалось снижением риска неблагоприятных событий на 12% (ОР 0,88; 95% ДИ 0,77–0,998; р = 0,046) без какого-либо влияния на риск сердечно-сосудистой смерти. По частоте больших кровотечений различий между принимавшими клопидогрел и плацебо выявлено не было, а частота малых геморрагий была значительно выше в группе клопидогрела (2,1% против 1,3% в группе плацебо; р < 0,001).
Антитромбоцитарная терапия у больных со стабильными проявлениями атеротромбоза
Прямое сопоставление монотерапии АСК с монотерапией клопидогрелом у больных высокого риска, недавно перенесших инфаркт миокарда, инсульт или имеющих клинические проявления атеросклероза артерий нижних конечностей, выполнено в рандомизированном контролируемом исследовании CAPRIE [23], результаты которого были опубликованы в 1996 году. Исследование было многоцентровым (384 лечебных учреждения из 16 стран) и включило 19 185 пациентов. Поводом для включения послужило наличие у больного одного из клинических проявлений атеросклероза: 1) инфаркта миокарда с формированием патологических зубцов Q на ЭКГ и/или повышением уровня кардиоспецифических ферментов более чем в 2 раза от верхней границы нормы давностью от нескольких дней до 35 суток; 2) ишемического инсульта (в том числе лакунарного) давностью от 1 недели до 6 месяцев; 3) симптомов атеросклероза периферических артерий (перемежающаяся хромота предположительно атеросклеротического генеза в сочетании со сниженным лодыжечно-плечевым индексом или хирургические вмешательства в связи с перемежающейся хромотой в анамнезе). Наличие одного из данных заболеваний — основной критерий для включения в исследование, в соответствии с которым пациентов распределили на три подгруппы. Однако у многих больных проявления атеросклероза не ограничивались одним сосудистым бассейном, нередко имело место сочетанное поражение (например, часть пациентов с ишемическим инсультом ранее перенесли инфаркт миокарда или имели сопутствующую перемежающуюся хромоту), поэтому распределение на подгруппы по основному критерию включения достаточно условно. Все пациенты были рандомизированы к приему либо АСК (325 мг/сут), либо клопидогрела (75 мг/сут) на протяжении 1–3 лет (средняя продолжительность антитромбоцитарной терапии составила 1,91 года).
Суммарная частота неблагоприятных событий (инфаркт миокарда, ишемический инсульт и сердечно-сосудистая смерть) оказалась несколько ниже в группе клопидогрела (5,32% в год для клопидогрела против 5,83% в год для АСК), что соответствовало снижению ОР на 8,7% (95% ДИ 0,3–16,5; р = 0,043). В целом использование клопидогрела позволяло дополнительно предотвратить 5 неблагоприятных исходов на каждую 1 000 пролеченных больных в год. На основании полученных результатов сформировалась точка зрения, что если клопидогрел и имеет некоторое преимущество перед АСК, оно не является столь выраженным и очевидным, чтобы оправдать масштабную замену повсеместно доступной и дешевой АСК на более дорогой клопидогрел.
При анализе подгрупп оказалось, что если основанием для включения в исследование были недавно перенесенные инфаркт миокарда или ишемический инсульт, то эффективность АСК и клопидогрела была практически одинаковой. Если же больных включили в связи с клинически выраженным атеросклерозом артерий нижних конечностей, преимущество клопидогрела было более существенным, чем в исследовании в целом. Среди 6 452 пациентов с атеросклерозом артерий нижних конечностей 3 198 были рандомизированы в группу АСК, 3 233 — в группу клопидогрела. Частота неблагоприятных сердечно-сосудистых событий у данных больных представлена на рис. 1. Снижение риска любых неблагоприятных событий на фоне приема клопидогрела составило 23,8% в год, что соответствовало предотвращению 11 неблагоприятных исходов на 1 000 пролеченных пациентов.

Клопидогрел также превосходил АСК в способности предотвратить достаточно обширный инфаркт миокарда (с формированием патологических зубцов Q на ЭКГ и/или повышением уровня кардиоспецифических ферментов более чем в 2 раза от верхней границы нормы). У принимавших клопидогрел ОР этого осложнения за весь период наблюдения (1–3 года) был ниже на 19,2% (р = 0,008) [24].
Дальнейший ретроспективный анализ базы данных исследования CARPIE обнаружил, что эффективность клопидогрела была выше у больных, ранее перенесших операцию аортокоронарного шунтирования, имевших несколько осложнений атеросклероза в анамнезе и страдающих сахарным диабетом, особенно инсулинзависимым.
Таким образом, результаты исследования CAPRIE свидетельствуют о том, что в целом монотерапия клопидогрелом как минимум не уступает по эффективности монотерапии АСК в профилактике сердечно-сосудистых осложнений у больных с клинически выраженными проявлениями атеросклероза. Нельзя исключить, что при наличии атеросклеротического заболевания клопидогрел может лучше АСК предотвращать инфаркт миокарда, особенно у больных с исходно высоким риском именно этого неблагоприятного исхода. Однако, поскольку эти данные были получены при анализе подгрупп (в основном ретроспективном), с уверенностью утверждать о наличии подобных закономерностей и, соответственно, делать вывод о преимуществе клопидогрела перед АСК у данных категорий пациентов не представляется возможным.
В уже упоминавшемся ранее исследовании CHARISMA было показано, что у больных со стабильными проявлениями атеросклероза (ишемической болезнью сердца, цереброваскулярной болезнью и атеросклерозом артерий нижних конечностей) использование комбинации АСК и клопидогрела способно значительно снизить риск неблагоприятных исходов без существенного увеличения частоты больших кровотечений. Однако данная закономерность была выявлена при ретроспективном анализе подгрупп в исследовании, продемонстрировавшем в целом отрицательный результат, поэтому полученные данные нуждаются в подтверждении в проспективных исследованиях и не могут служить основанием для уверенного суждения о предпочтительности подобной стратегии лечения.
Безопасность антитромбоцитарной терапии
Основным побочным эффектом антитромбоцитарной терапии считается неблагоприятное воздействие на слизистую оболочку желудочно-кишечного тракта (ЖКТ), начиная от симптомов диспепсии и заканчивая желудочно-кишечными кровотечениями, в ряде случаев оказывающихся фатальными. Несмотря на различия в механизмах антитромбоцитарного действия, неблагоприятное влияние на ЖКТ свойственно и АСК, и клопидогрелу. При этом нельзя сказать, что последний более безопасен в этом отношении, нежели АСК. Клопидогрел не оказывает существенного влияния на слизистую оболочку желудка лишь при кратковременном применении [25]. Однако поскольку тромбоциты являются источником ростовых факторов, стимулирующих ангиогенез в стенке желудка, то, необратимо подавляя функцию тромбоцитов, клопидогрел препятствует заживлению язв и эрозий [26]. По мнению экспертов, применение клопидогрела вместо АСК с целью профилактики желудочных кровотечений является нецелесообразным [26, 27].
Результаты многих исследований указывают на то, что, несмотря на отсутствие прямого раздражающего действия на слизистую оболочку, риск кровотечения из верхних отделов ЖКТ на фоне монотерапии клопидогрелом достаточно высок. В исследовании же CAPRIE [28], напротив, частота желудочно-кишечных кровотечений в группе клопидогрела была ниже, чем в группе АСК (0,52% против 0,72% соответственно). Однако в этой работе использовали слишком высокую по современным представлениям дозу АСК (325 мг/сут). Рекомендуемые в настоящее время для длительного применения дозы АСК значительно ниже и в большинстве случае составляют 75–150 мг/сут. Также известно, что неблагоприятное воздействие АСК на слизистую ЖКТ и риск кровотечения зависят от дозы (рис. 2) и являются наименьшими при использовании в дозах до 100 мг/сут [29–31]. Как показали результаты крупного метаанализа [31], включившего 338 191 пациента, риск желудочно-кишечного кровотечения на фоне приема АСК в дозах, превышающих 325 мг/сут, и клопидогрела значительно выше, чем при терапии низкими дозами АСК и дипиридамолом (рис. 2). Еще в одном эпидемиологическом исследовании, выполненном методом «случай-контроль» с участием 8 309 пациентов, риск желудочно-кишечного кровотечения на фоне терапии клопидогрелом и АСК (100 мг/сут) возрастал в равной степени [32].

Пациентам с высоким риском развития желудочно-кишечных кровотечений для повышения безопасности длительного лечения клопидогрелом рекомендовано назначение ингибиторов протонной помпы (ИПП), например, омепразола [1]. Однако в последние годы появились сомнения относительно целесообразности совместного использования ИПП и клопидогрела. Результаты некоторых исследований дали основание предполагать наличие взаимодействия между клопидогрелом и ИПП, которое снижает антитромбоцитарный эффект клопидогрела при одновременном применении с ИПП. Существует несколько возможных объяснений данного феномена. Во-первых, некоторые ИПП могут препятствовать превращению клопидогрела в биологически активную форму, уменьшая тем самым его эффективность и увеличивая риск неблагоприятных исходов, обусловленных активацией свертывания крови. Во-вторых, метаболизм ИПП и клопидогрела контролирует один и тот же ген CYP2C19. Допускается существование и других механизмов влияния ИПП на эффективность клопидогрела. Вместе с тем данные о наличии взаимодействия между клопидогрелом и ИПП противоречивы и относятся преимущественно к одному представителю этой группы — омепразолу. В отдельных исследованиях показано, что клопидогрел не взаимодействует с другими ИПП, в частности, с пантопразолом. Клиническое значение взаимодействия клопидогрела и ИПП окончательно не определено. Эксперты сходятся на том, что врачам следует соблюдать осторожность и назначать ИПП только при наличии у пациента очевидных проблем со стороны ЖКТ, которые не контролируются приемом Н2-блокаторов. Если использование ИПП все же необходимо и оправдано, то, вероятно, следует избегать назначения омепразола и отдавать предпочтение другим ИПП, например, пантопразолу.
С целью улучшения переносимости лечения, защиты слизистой оболочки желудка и уменьшения вероятности развития побочных эффектов со стороны ЖКТ при длительном применении следует использовать «защищенные» лекарственные формы АСК — кишечнорастворимые или буферные. Имеются данные [33, 34], что субъективная переносимость и профиль безопасности буферных форм АСК лучше, чем кишечнорастворимых. Примером буферной формы АСК является препарат Кардиомагнил, содержащий наряду с АСК кислотный буфер — невсасывающийся антацид гидроксид магния. Добавление гидроксида магния позволяет защитить слизистую оболочку желудка от неблагоприятного воздействия АСК, не снижая при этом ее антитромбоцитарный эффект [35].
Таким образом, и АСК, и клопидогрел являются эффективными антитромбоцитарными препаратами, давно и успешно применяемыми в кардиологической практике. Несмотря на появление в последние годы новых антиагрегантов, АСК по-прежнему остается наиболее востребованным антитромбоцитарным препаратом и удерживает свои позиции «золотого» стандарта. Клопидогрел хотя и продемонстрировал несколько большую, чем АСК, эффективность в отношении снижения частоты сердечно-сосудистых эпизодов у больных высокого риска в исследовании CAPRIE, тем не менее, редко используется в качестве монотерапии.
Литература
- Антитромботическая терапия у больных со стабильными проявлениями атеротромбоза // Кардиоваскулярная терапия и профилактика. 2009; 8 (6): Приложение 6.
- Панченко Е. П., Добровольский А. Б. Тромбозы в кардиологии. Механизмы развития и возможности терапии. М.: Спорт и культура, 1999. 464 с.
- Coulell A. J., Markham A. Clopidogrel // Drugs. 1997; 54: 745–750.
- Hulot J.-S., Bura A., Azizi M. et al. Cytochrome P450 2 C19 loss-of-function polymorphism is a major determinant of clopidogrel responsiveness in healthy subjects // Blood. 2006; 108: 2244–2247.
- Trenk D., Hochholzer W., Fromm M. F. et al. Cytochrome P450 2 C19681G>A polymorphism and high on clopidogrel platelet reactivity associated with adverse 1-year clinical outcome of elective percutaneous coronary intervention with drug-eluting or bare-metal stents // J Am Coll Cardiol. 2008; 51: 1925–1934.
- Mega J. L., Close S. L., Wiviott S. D. et al. Cytochrome P-450 Polymorphisms and Response to Clopidogrel // N Engl J Med. 2009; 360: 354–362.
- Collet J.-P., Hulot J.-S., Pena A. et al. Cytochrome P450 2 C19 polymorphism in young patients treated with clopidogrel after myocardial infarction: a cohort study // Lancet. 2009; 373: 309–317.
- Sibbing D., Stegherr J., Latz W. et al. Cytochrome P450 2 C19 loss-of-function polymorphism and stent thrombosis following percutaneous coronary intervention // Eur Heart J. 2009; 30: 916–922.
- Giusti B., Gori A. M., Marcucci R. et al. Relation of cytochrome P450 2 C19 loss-of-function polymorphism to occurrence of drug-eluting coronary stent thrombosis // Am J Cardiol. 2009; 103: 806–811.
- Shuldiner A. R., O’Connell J. R., Bliden K. P. et al. Association of cytochrome P450 2 C19 genotype with the antiplatelet effect and clinical efficacy of clopidogrel therapy // JAMA. 2009; 302: 849–857.
- Plosker G. L., Lyseng-Williamson K. A. Clopidogrel. A review of its use in the prevention of thrombosis // Drugs. 2000; 64: 613–646.
- Antithrombotic Therapy in Peripheral Artery Disease Antithrombotic Therapy and Prevention of Thrombosis, 9 th ed.: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines // Chest. 2012; 141 (2) (Suppl): 669–690.
- ACC/AHA 2005 Practice Guidelines for the Management of Patients With Peripheral Arterial Disease (Lower Extremity, Renal, Mesenteric, and Abdominal Aortic): Executive Summary // Circulation. 2006; 113: 1474–1547.
- ESC Guidelines on the diagnosis and treatment of peripheral artery diseases // Eur Heart J. 2011; 32: 2851–2906.
- Национальные рекомендации по кардиоваскулярной профилактике // Кардиоваскулярная терапия и профилактика. 2011; 10 (6): приложение 2.
- The European Stroke Organization (ESO) Executive Committee and the ESO Writing Committee. Guidelines for Management of Ischaemic Stroke and Transient Ischaemic Attack 2008 // Cerebrovasc Dis. 2008; 25 (5): 457–507.
- Adams R., Albers G., Alberts M. et al. Update to the AHA/ASA Recommendations for the Prevention of Stroke in Patients With Stroke and Transient Ischemic Attack // Stroke. 2008; 39: 1647–1652.
- Antithrombotic Trialists’ (ATT) Collaboration; Baigent C., Blackwell L., Collins R. et al. Aspirin in the primary and secondary prevention of vascular disease: collaborative meta-analysis of individual participant data from randomised trials // Lancet. 2009; 373: 1849–1860.
- Zanchetti A., Hansson L., Dahlof B. et al., on behalf of the HOT Study Group. Benefit and harm of low-dose aspirin in well-treated hypertensives at different baseline cardiovascular risk // J Hypertens. 2002; 20: 2301–2307.
- Диагностика и лечение артериальной гипертензии (третий пересмотр) //Кардиоваскулярная терапия и профилактика. 2008; 7 (6): приложение 2.
- 2013 ESH/ESC Guidelines for the management of arterial hypertension. The Task Force for the management of arterial hypertension of the European Society of Hypertension (ESH) and of the European Society of Cardiology (ESC) // Eur Heart J. 2013; 34: 2159–2219.
- Bhatt D. L., Fox K. A. A., Hacke W. et al., for the CHARISMA Investigators. Clopidogrel and Aspirin versus Aspirin Alone for the Prevention of Atherothrombotic Events // N Engl J Med. 2006; 354: 1706–1717.
- CAPRIE Steering Committee. A randomised, blinded, trial of clopidogrel versus aspirin in patients at risk of ischaemic events (CAPRIE) // Lancet. 1996; 348: 1329–1339.
- Cannon C. P., on behalf of the CAPRIE Investigators. Effectiveness of Clopidogrel Versus Aspirin in Preventing Acute Myocardial Infarction in Patients With Symptomatic Atherothrombosis (CAPRIE Trial) // Am J Cardiol. 2002; 90: 760–762.
- Fork F. T., Lafolie P., Toth E., Lindgarde F. Gastroduodenal tolerance of 75 mg clopidogrel versus 325 mg aspirin in healthy volunteers. A gastroscopic study // Scand J Gastroenterol. 2000; 35 (5): 464–469.
- ACCF/ACG/AHA 2008 Expert Consensus Document on Reducing the Gastrointestinal Risks of Antiplatelet Therapy and NSAID Use. A Report of the American College of Cardiology Foundation Task Force on Clinical Expert Consensus Documents // Circulation. 2008; 118: 1894–1909.
- Lai K. C., Chu K. M., Hui W. M. et al. Esomeprazole with aspirin versus clopidogrel for prevention of recurrent gastrointestinal ulcer complications // Clin Gastroenterol Hepatol. 2006; 4 (7): 860–865.
- Bhatt D. L., Hirsch A. T., Ringleb P. A. et al., on behalf of the CAPRIE investigators. Reduction in the need for hospitalization for recurrent ischemic events and bleeding with clopidogrel instead of aspirin // Am Heart J. 2000; 140: 67–73.
- Serebruany V. L., Steinhubl S. R., Berger P. B. et al. Analysis of Risk of Bleeding Complications After Different Doses of Aspirin in 192,036 Patients Enrolled in 31 Randomized Controlled Trials // Am J Cardiol. 2005; 95: 1218–1222.
- Patrono C., Baigent C., Hirsh J., Roth G. Antiplatelet Drugs. American College of Chest Physicians Evidence-Based Clinical Practice Guidelines (8 th Edition) // Chest. 2008; 133: 199S–233S.
- Serebruany V. L., Malinin A. I., Eisert R. M., Sane D. C. Risk of Bleeding Complications With Antiplatelet Agents: Meta-Analysis of 338,191 Patients Enrolled in 50 Randomized Controlled Trials // Am J Hematol. 2004; 75: 40–47.
- Lanas A., Garcia-Rodriguez L. A., Arroyo M. T. et al. Risk of upper gastrointestinal ulcer bleeding associated with selective cyclooxygenase-2 inhibitors, traditional non-aspirin non-steroidal anti-inflammatory drugs, aspirin and combinations // Gut. 2006; 55: 1731–1738.
- Баркаган З. С., Котовщикова Е. Ф. Сравнительный анализ основных и побочных эффектов различных форм ацетилсалициловой кислоты // Клиническая фармакология и терапия. 2004; 13 (3): 1–4.
- Верткин А. Л., Аристархова О. Ю., Адонина Е. В. и др. Безопасность и фармакоэкономическая эффективность применения различных препаратов ацетилсалициловой кислоты у пациентов с ИБС // РМЖ. 2009; 17 (9): 570–575.
- Яковенко Э. П., Краснолобова Л. П., Яковенко А. В. и др. Влияние препаратов ацетилсалициловой кислоты на морфофункциональное состояние слизистой оболочки желудка у кардиологических пациентов пожилого возраста // Сердце. 2013; 12 (3): 145–150.
Н. М. Воробьёва, доктор медицинских наук
ФГБУ РКНПК МЗ РФ, Москва
Контактная информация: natalyavorobjeva@mail.ru
00:00
Владимир Трофимович Ивашкин, академик РАМН, доктор медицинских наук:
— Следующее сообщение. Оксана Михайловна Драпкина. «Ингибиторы протонной помпы (ИПП) и «Клопидогрель» («Clopidogrel»).
Оксана Михайловна Драпкина, исполнительный директор интернет-сессии, секретарь межведомственного совета по терапии РАМН:
— Уважаемые коллеги, лекция будет посвящена возможным связям. Есть ли эти связи. Насколько правильно говорить о том, что ИПП влияют на активность «Клопидогреля». Остается или не остается вопрос в этой области.
ИПП – это препараты, которые блокируют Н-калиевую АТФазу, всасываясь в париетальных клетках и накапливаясь в тубуло-визикулярной системе, снижают синтез соляной кислоты. Это приводит к тому, что рН у пациента повышается и происходит снижение кислотности. Снижается рефлюкс эзофагит и другие неприятные последствия повышенной кислотности.
Спектр применения ИПП огромен. Это гастроэзофагеальная рефлюксная болезнь (ГЭРБ). Сегодня была лекция Александра Сергеевича. Язвенная болезнь желудка двенадцатиперстной кишки, эрадикация Н. pylori. Различные варианты диспепсии.
Сегодня мне больше хотелось бы поговорить о возможном снижении риска кровотечений на фоне применения антитромботических средств. На этот вопрос мы отвечаем, безусловно, да. ИПП остаются средством профилактики для лечения кровотечений на фоне применения антитромботических средств.
В связи с тем, что так велико влияние и велики различные эффекты ИПП, возникают вопросы о возможных нежелательных реакциях, которые связаны с ИПП. Подобно статинам в кардиологии, ИПП в гастроэнтерологии, на мой взгляд, являются одним из самых безопасных препаратов. Но и здесь не обошлось без ложки дегтя в бочке меда.
Какое-то время говорили о возможной компенсаторной гипергастринемии, что не подтвердилось статистически и клинически значимо. О полипах фундальных желез, о повышении риска переломов шейки бедра. Последние мета-анализы также не показали статистически достоверной значимости.
Повышение внегоспитальной пневмонии за счет снижения кислотности, повышения рН и колонизации глотки различными бактериями. Последние годы очень активно муссируется вопрос о снижении эффективности антиагрегантов. В частности, «Клопидогреля».
Где здесь правда, где ложь, мы попробуем разобраться. Прежде чем разобраться в этой проблеме, нам надо поговорить и вспомнить курс фармакологии, который рассказывал о лекарственных взаимодействиях. Согласно этому курсу мы можем сказать, что лекарственные взаимодействия – это изменение фармакологического эффекта одного или нескольких лекарственных препаратов при одновременном или последовательном их применении.
03:33
Как могут взаимодействовать лекарственные препараты. По нескольким механизмам. Это могут быть два механизма: либо они «за», либо «против». Либо это синергизм, либо антагонисты. В синергизме есть «за» с двумя, тремя плюсами и так далее. «За» с последующими плюсами, которые нарастают: сенситизирующее, аддитивное действие, суммация действия и потенцирование действие.
Все виды лекарственных взаимодействий можно разделить на три большие группы. Фармацевтическое – взаимодействие лекарств вне организма. Сегодня оно нас интересует в меньшей степени. Фармакокинетическое – изменение фармакокинетических характеристик лекарственных веществ. Фармакодинамическое – изменение эффектов препаратов.
Если мы говорим о фармакокинетических взаимодействиях ИПП, то понимаем, что в связи с повышением рН желудочного сока, снижения уровня соляной кислоты может снижаться абсорбция некоторых лекарственных препаратов:
o солей железа;
o витамина В12;
o «Аспирина» («Acetylsalicylic acid»);
o «Итраконазола» («Itraconazole») и так далее.
Если мы подходим к вопросу фармакодинамики, то здесь следует осветить пути или фазы метаболизма лекарств. Первая фаза чрезвычайно важна. Это фаза окисления. На ней сегодня мы и остановимся более подробно. Эта фаза чрезвычайно важна потому, что в ней участвует очень мощная система цитохрома Р450.
Вторая фаза, в которой проходит ряд стадий:
o глюкуронирование;
o сульфатирование;
o ацетилирование;
o метилирование;
o коньюгация.
05:30
Все вещества, все лекарственные средства попадают в организм в нерастворимой форме. Для того чтобы вывести, их надо сделать растворимыми. Именно для этого нужна слаженная работа системы цитохрома Р450. Если бы этой работы не было, то эти вещества, оставаясь нерастворимыми, долгое время, практически всю жизнь, циркулировали бы по кровотоку, не оказывая никакого фармакологического действия.
Очень многие реакции изучены на примере «Омепразола» («Omeprazole»). Я имею в виду ИПП в печени. Метаболизм «Омепразола» происходит с помощью активации изоформы Р450, особенной изоформы CYP2C19. Сегодня CYP2C19 будет служить объектом пристального внимания, потому что именно он по многим публикациям некоторых исследователей повинен в том, что при совместном применении ИПП и «Клопидогреля» возможны взаимодействия, которые снижают активность последнего.
Цитохром Р450 – это сложноустроенная система микросомального окисления (фосфолипид-флавопротеид, который содержит гем). Основная цель и основная работа цитохрома Р450 – сделать вещества более растворимыми, а, следовательно, менее токсичными путем внедрения гидроксильного радикала. Это делает различные изоформы цитохрома Р450. Основная локализация печень. Биотрансформация, которая проходит в печени.
Как работает цитохром Р450. Это чрезвычайно мощная система. Для работы цитохрома Р450 необходим кислород воздуха, плохорастворимый (ксенобиотик или ИПП) агент. Нужен универсальный донатор протона и электрона. В качестве универсального донатора, восстановителя выступает НАДФН + Н+.
Работа и система настолько мощная, что она способна оторвать один атом кислорода и присоединить его к вымышленному ИПП (ксенобиотику), сделав его растворимым и не столь опасным. Он начинает оказывать свое фармацевтическое действие. Затем это растворимое вещество выводится почками. Дополнительными продуктами образования служит Н2О (вода).
08:36
Что делает основную работу или каково участие различных изоформ цитохрома Р450 в окислении лекарств. Основную работу принимает на себя CYP3A4. Очень многие препараты (статины, ингибиторы ангиотензин-превращающего фермента, антигипертензивные препараты) метаболизируются с помощью CYP3A4.
Нас интересует изоформа CYP2C19, потому что именно она ответственна за метаболизм «Клопидогреля» и большинства ИПП.
Особенности этой изофомы заключаются в следующем. Во-первых, это высокоэффективный цитохром. Он метаболизирует порядка 8% всех лекарственных средств. Для него характерен генетический полиморфизм (что тоже важно знать) в предсказании какого-либо эффекта, который мы ожидаем от препарата, который будет метаболизироваться этой изоформой CYP2C19.
Маркерный субстрат наиболее хорошо изучен. «Омепразол». Есть работы с другими субстратами. ИПП. Такие хорошо известные препараты, как «Варфарин» («Warfarin»), «Индометацин» («Indometacin»), «Прогестерон» («Progesterone») и так далее.
Цитохрому CYP2C19 свойственны генетические полиморфизмы. В основном все мы (европейцы) являемся интенсивными метаболизаторами. Метаболизаторы, у которых отсутствуют мутации в гене кодирующих работ CYP2C19.
Есть промежуточные метаболизаторы, где происходят изменения в одной аллели гена. Есть медленные метаболизаторы, где мутации подверглись оба аллеля.
Если сравнить расу европеоидов и монголоидов, мы понимаем, что в лечении, в предсказании эффекта ИПП очень большое значение будет играть, кто перед нами. Кто наш пациент, к какой расе он относится и в какой из долевых пирогов он попадает.
11:13
Что же больше всего из ингибиторов протонной помпы влияет на цитохром CYP2C19. Наибольшее ингибирующее влияние описано в отношении «Лансопразола» («Lansoprazole»). В меньшей степени это делают «Омепразол» и «Эзомепразол» («Еsomeprazole»). Еще ниже эффект ««Рабепразола» («Rabeprazole»). Самый менее ингибирующий «Пантопразол» («Pantoprazole»).
Мы сейчас рассмотрим, каким образом происходит межлекарственное взаимодействие.
(Демонстрация слайда).
Первая схема выделена прямоугольником. Поступает лекарство в организм. Оно встречается с каким-то индуктором цитохрома. Например, фенобарбиталом. Все это метаболизируется цитохромом Р450 и опосредуется в ускорении метаболизма, уменьшении времени жизни в плазме крови.
Другая ситуация. Лекарство повстречалось на своем пути с ингибитором цитохрома. Например, это будут фторхинолоны. Здесь будет замедление метаболизма и увеличение времени жизни в плазме крови. Эффект будет несколько меньше.
Ситуация, которую мы сейчас рассматриваем. Мы рассматриваем взаимодействие «Клопидогреля» и ИПП. (Это схематичное изображение 3). Лекарство 1 + лекарство 2 (которое метаболизируется той же изоформой CYP2C19). Это приводит к тому, что замедляется метаболизм обоих лекарственных форм.
Что такое «Клопидогрель». Хорошо нам известный агрегант. Он метаболизируется этой системой. С одной стороны, для того чтобы он превратился в активный метаболит, требуется напряжение системы цитохрома Р450. С другой стороны, такого же напряжения требует трансформация «Омепразола». Чем больше доза ИПП, тем меньше активного метаболита в «Клопидогреле» есть.
«Клопидогрель», как и «Аспирин» очень прочно вошел в нашу жизнь. Показания для применения «Клопидогреля» только увеличиваются. Практически ничего не уменьшается. Это, как минимум, 75 мг раз в сутки у стабильных пациентов. Нагрузочная доза составляет 300 мг. Некоторые исследования говорят и о 600 мг.
13:52
Фармакокинетика «Клопидогреля» хорошо известно. Работа цитохрома CYP2C19. Неактивный «Клопидогрель» должен подвергнуться биотрансформации в печени с помощью этой системы и превратиться в 2-оксо-клопидогрель. Он посредством повторного прохождения через эту систему превращается в активное тиольное производное «Клопидогреля». Оказывает свои эффекты, а именно, необратимо связывается с рецепторами к АДФ тромбоцитов.
Этот препарат зарекомендовал себя довольно хорошо. Есть масса исследований. Сегодня нам наиболее интересно исследование, в которое вошли более 20-ти тысяч пациентов. Сравнивали эффективность «Аспирина», которая доказана уже временем, и «Клопидогреля» как нового антиагреганта в профилактике инфаркта миокарда, инсульта и сосудистой смерти.
Исследование «Caprie». Согласно этому исследованию оказалось, что «Клопидогрель», как минимум, также эффективен (эффективность даже была выше, но она не достигла статистически достоверной разницы). Как максимум, он более безопасен, чем «Аспирин».
Желудочно-кишечные кровотечения и язвы желудочно-кишечного тракта в меньшей степени отмечались у тех пациентов, которые принимали «Клопидогрель» 75 мг в сутки. Процент был существенный. Минус 25% и 41%, соответственно.
Можем ли мы отказаться от антиагрегантов? Нет, не можем. Нарастает число пациентов после аорто-коронарного шунтирования, после стентирования. В то же время риск желудочно-кишечных кровотечений на фоне применения двойной антитромбоцитарной терапии растет. Двойная антитромбоцитарная терапия (год после наличия стента) любой локализации. Желудочно-кишечные кровотечения составляют 50% всех кровотечений при дебюте острого коронарного синдрома (ОКС).
Как сориентироваться в клинической ситуации. Как понять, что этому пациенту мы профилактически назначили ИПП, а другому пациенту не назначили. Для этого есть определенные шкалы, рекомендации.
16:31
Представлена таблица, по которой мы можем распределить пациентов по степени риска. В высокий риск войдут пациенты со множественными факторами риска (если их больше двух) и если в анамнезе осложненная язва, особенно недавняя.
В умеренный риск – наличие одного или двух факторов:
o пожилой возраст > 65-ти лет;
o высокая доза нестероидных противовоспалительных препаратов;
o неосложненная язва в анамнезе;
o одновременный прием нестероидных противовоспалительных препаратов, кортикостероидов и антикоагулянтов.
Низкий риск – нет факторов риска.
Ревматологи отмечают, что наличие H. Pylori – независимый и дополнительный фактор риска, который нужно рассматривать отдельно.
Давайте проанализируем или составим портрет воображаемого пациента, которому мы бы обязательно профилактически назначили ИПП, причем в довольно высокой дозе. Это чаще женщины хрупкого телосложения, старше 65-ти лет, которые имеют в анамнезе язвенную болезнь и кровотечения. Анамнез, отягощенный по сердечно-сосудистым заболеваниям (ССЗ). Те, кто имеет явления сердечной недостаточности, низкую скорость клубочковой фильтрации, очень высокое и очень низкое артериальное давление (АД).
Что делать? До 2008-го года все было нормально. Все спокойно жили: и врачи, и пациенты. Как только пациент попадал в группу риска, ему назначался ИПП при сохранении назначения «Клопидогреля». Но вдруг в 2008-м году на 32-м ежегодном собрании Общества сердечно-сосудистой ангиографии было сделано заявление. Оно говорило о том, что совместный прием ИПП и «Клопидогреля» значительно повышает риск возникновения больших неблагоприятных сердечно-сосудистых событий.
Начался шум.FDA принялось расследовать эти случаи. Были спланированы очень большие репрезентативные мета-анализы, которые показали несколько разные результаты.
19:07
У нас есть план тактики ведения пациента с ОКС, за чем надо следить. Надо следить за интенсивностью кровотечения, мониторировать уровень эритроцитов, гематокрита, крови в моче и стуле. Необходимо осуществлять инфузионно-трансфузионную терапию. В рекомендациях черным по белому написано, что это применяется при гематокрите < 25% или гемаглобине < 7 г/дл. Наша цель – добиться гемаглобина 9 – 10 г/дл (а не 120, который считается нормой).
Некоторые исследования показывают, что при более высоких показателях гемотрансфузии способны ухудшить прогноз. «Эритропоэтин» («Еrythropoietin») таким пациентам не показан. Рука не поднимается применять тромболитики и «Гепарин» («Heparin») пациентам с кровотечением.
Как будто в этих рекомендациях написано, что предпочтительнее терапия ИПП плюс блокаторы Н2-рецепторов внутривенно. Хотя последние рекомендации говорят о том, что данные по клинической значимости взаимодействия «Клопидогреля» и ИПП неоднозначны.
Эффект «Празугрела» (новый антитромбоцитарный препарат) не зависит от ИПП.
ИПП все равно показаны пациентам с ОКС совместно с двойной антитромботической терапией, с язвенной болезнью желудка или желудочно-кишечным кровотечением.
Тяжелые кровотечения: остановка антитромботической терапией. В тех случаях, когда местное гемостатическое пособие высокоэффективно, терапию можно продолжать.
Таким образом, на сегодняшний день различные исследования показали неоднозначную оценку ситуации совместного применения ИПП и «Клопидогреля». В частности, ретроспективное исследование с участием более 20-ти тысяч пациентов не показало значимого влияния ни одного из используемых ИПП на увеличение частоты сердечно-сосудистых событий.
21:34
Тем не менее, компании-производители каждых из ИПП начинают исследования, которые порой подтверждают, порой не подтверждают возможное взаимодействие. В частности, одно из последних исследований касается «Рабепразола». Это препарат, который в меньшей степени влияет на активность цитохрома Р450.
Влияние «Рабепразола» на антиагрегантные свойства «Клопидогреля». Оценивался индекс реактивности тромбоцитов. Он определяется как PRI. Пациенты, которые принимают плацебо, «Рабепразол» 20 мг и «Омепразол» 20 мг.
Что получается. Группа пациентов, которые принимают «Рабепразол» и «Омепразол», не имеют статистически достоверной разницы по этому показателю (по индексу реактивности тромбоцитов). С другой стороны, если сравниваются эти два препарата с плацебо, то ответ «Рабепразола» на изменение значения индекса абсолютно сравним с плацебо. Этого нет у «Омепразола».
С небольшой долей достоверности мы можем сказать, что у пациента с двойной антитромбоцитарной терапией применение «Рабепразола» 20 мг будет более предпочтительно. Чем применение «Омепразола».
Таким образом, мы все еще остаемся на некоторых дискутабельных позициях. Но можем сказать, что ИПП могут влиять на фармакокинетику «Клопидогреля».
Я возвращаю вас к началу лекции, где говорила о формах цитохрома Р450 и особенно CYP2C19.
Имеющиеся данные позволяют говорить о потенциально клинически значимом лекарственном взаимодействии между ИПП и «Клопидогрелем». Мета-анализы не подтвердили выраженного взаимодействия. «Рабепразол» в определенных ситуациях может быть препаратом выбора.
Решать, какой ИПП применить, применить ли его вообще и в какой дозе, что перевешивает: риск кровотечения или риск тромбоза, придется нам в каждой конкретной клинической ситуации.
Спасибо за внимание.

Содержание
1
Сердечно-сосудистые заболевания стоят на первом месте среди причин смерти во всем мире. Они могут вызывать опасные осложнения, такие, как инфаркт миокарда, инсульт, тромбоз и другие. Для предупреждения и лечения этих заболеваний часто используются лекарства, которые делают кровь менее вязкой и не допускают образования тромбов. Среди таких лекарств – кардиомагнил и клопидогрел. Что они из себя представляют, чем отличаются и какой из них выбрать? В этой статье мы попытаемся ответить на эти вопросы.
Состав
Лекарства имеют различный состав и форму выпуска. Кардиомагнил выпускается в виде таблеток, покрытых оболочкой, которая растворяется только в кишечнике. Каждая таблетка содержит 75 мг или 150 мг ацетилсалициловой кислоты и 15,2 мг гидроксида магния. Кроме того, в состав входят помогающие вещества, такие, как: крахмал, целлюлоза, тальк, титановый диоксид и другие.
Клопидогрел выпускается в виде таблеток, покрытых пленкой, которая растворяется в желудке. Каждая таблетка содержит 75 мг действующего вещества в виде бисульфата. Также в состав входят помогающие вещества, такие, как: лактоза, целлюлоза, кросповидон, стеарат магния и другие.
Воздействие на организм
Лекарства принадлежат к группе антиагрегантов, то есть тех, которые препятствуют слипанию тромбоцитов – кровяных пластинок, которые отвечают за свертывание крови. Тромбоциты могут агрегироваться между собой и с поврежденными участками сосудов, формируя тромбы, которые могут забивать сосуды и нарушать кровоток. Это может приводить к ишемии – недостатку кислорода и питания для тканей, в особенности для сердца и мозга. Антиагреганты помогают избежать этого, улучшая свойства крови и уменьшая риск тромбоза. Оба препарата воздействуют на тромбоциты по-своему.
Кардиомагнил ингибирует фермент циклооксигеназу, который участвует в производстве тромбоксана – вещества, которое стимулирует агрегацию тромбоцитов. Клопидогрел ингибирует рецепторы тромбоцитов, которые активизируются при контакте с аденозиндифосфатом – посредником, который также способствует слипанию тромбоцитов. Таким образом, оба препарата подавляют активацию тромбоцитов, но разным образом влияют на их реакции.
Еще 80 статей о здоровье сосудов и сердца смотрите тут 👈
Действующие вещества в Кардиомагниле
Кардиомагнил состоит из двух составляющих: ацетилсалициловой кислоты (АСК) и гидроксида магния. АСК – это средство, которое обладает противовоспалительным, жаропонижающим и обезболивающим действием, а также антиагрегантным эффектом. Она была открыта в 1897 году немецким химиком Феликсом Гофманом, который получил ее из салициловой кислоты – вещества, которое находится в коре ивы и имеет целебные свойства. Также стала одним из самых известных и широко применяемых лекарств в мире.
Гидроксид магния – это средство, которое нейтрализует излишек кислоты в желудке и защищает его слизистую оболочку. Он был открыт в 1755 году шотландским химиком Джозефом Блэком, который изучал свойства магния и его соединений. Гидроксид магния добавляется для того, чтобы уменьшить раздражение АСК на желудок и предотвратить возможные побочные явления, такие, как: язвы, гастриты и кровотечения.
Вещество Клопидогрел
Клопидогрел – это средство, которое ингибирует рецепторы тромбоцитов, которые активизируются при контакте с аденозиндифосфатом. Он был открыт в 1982 году французскими учеными из компании Санофи-Авентис, которые искали новые средства для предупреждения тромбоза. Данная субстанция является пролекарством, то есть тем, которое превращается в активную форму в организме под действием ферментов печени. Клопидогрел эффективен при предупреждении и лечении сердечно-сосудистых заболеваний, в особенности после ангиопластики и стентирования сосудов сердца.
Исследования эффективности
Данные препараты эффективны в профилактике и терапии сердечно-сосудистых патологий, как показали многочисленные исследования. Например, в исследовании CAPRIE (Сравнение клопидогрела и ацетилсалициловой кислоты у пациентов с риском ишемических осложнений) было установлено, что клопидогрел лучше АСК в предотвращении ишемических осложнений у пациентов с атеротромбозом. Он уменьшал риск на 8,7% в сравнении с АСК. В исследовании CURE (Клопидогрел при нестабильной стенокардии для профилактики рецидивов) было доказано, что присоединение данного препарата к АСК у пациентов с нестабильной стенокардией или острым коронарным синдромом без подъема сегмента ST снижало риск летальности.
Кардиомагнил также проявлял эффективность в профилактике и лечении сердечно-сосудистых заболеваний. В исследовании ISIS-2 (Второе международное исследование выживаемости при инфаркте) было выявлено, что АСК уменьшал риск смерти от инфаркта миокарда на 23% по сравнению с плацебо. В исследовании HOT (Оптимальное лечение гипертонии) было обнаружено, что средство уменьшало риск сердечно-сосудистых осложнений на 15% по сравнению с плацебо у пациентов с гипертонией).
Сравнительная таблица
| Наименование товара | Наименование производителя и страна | Полный состав | Стоимость | Дозировка |
| Кардиомагнил | Астра Зенека, Швеция | АСК 75 мг или 150 мг, гидроксид магния 15,2 мг, вспомогательные вещества | От 200 до 400 рублей за 30 таблеток | 1 таблетка в день |
| Клопидогрел | Различные производители, в том числе Россия, Индия, Франция и другие | Клопидогрел бисульфат 75 мг, вспомогательные вещества | От 100 до 1000 рублей за 28 таблеток | 1 таблетка в день |
Главные отличия
Препараты отличаются по способу воздействия, показаниям, противопоказаниям, нежелательным реакциям и совместимости с другими лекарствами. Давайте рассмотрим некоторые из них:
- Кардиомагнил не рекомендуется применять при наличии аллергии на АСК или другие нестероидные противовоспалительные средства, язвенном поражении желудка и двенадцатиперстной кишки, геморрагическом диатезе, тяжелом нарушении функции почек или печени, беременности и лактации.
- Кардиомагнил может спровоцировать нежелательные реакции, такие, как: расстройство пищеварения, воспаление слизистой желудка, язвы и кровопотери из желудочно-кишечного канала, аллергию, нарушение свертываемости крови, повышение трансаминаз, воспаление печени, воспаление почек, бронхиальную астму, анафилактический шок и другие. Препарат может спровоцировать нежелательные реакции, такие, как: понос, диспепсия, боли в брюшной полости, вздутие, язвы и кровопотери из желудочно-кишечного канала, гематомы, кровоизлияния, снижение тромбоцитов, снижение лейкоцитов, агранулоцитоз, аллергию, сыпь, зуд, отек Квинке и другие.
- Клопидогрел может влиять на действие других лекарств, усиливая или ослабляя их эффект. Например, он может усилить эффект антикоагулянтов, сахароснижающих средств, метотрексата, дигоксина, вальпроевой кислоты и других. Также может ослабить эффект мочегонных, антигипертензивных и уратоуретических средств и т.д.
Мнение врачей
Врачи отмечают, что кардиомагнил — это недорогой и доступный препарат, который хорошо себя зарекомендовал в профилактике и терапии сердечно-сосудистых заболеваний. Однако они также обращают внимание на высокий риск развития желудочно-кишечных кровотечений и других нежелательных реакций, особенно при длительном использовании и при наличии сопутствующих заболеваний ЖКТ. Советуют контролировать состояние желудка и крови при использовании кардиомагнила, а также придерживаться диеты и режима питья.
Врачи отмечают, что клопидогрел — это более новый и эффективный препарат, который предпочтительнее в уменьшении риска тромбоза и ишемии, особенно у пациентов с высоким атеротромботическим риском и после стентирования сосудов сердца. Однако они также обращают внимание на высокую цену лекарства, необходимость индивидуального выбора дозы и длительности терапии. Врачи советуют проводить генетическое тестирование на CYP2C19 перед назначением клопидогрела, а также контролировать состояние крови и избегать одновременного использования с другими антиагрегантами и средствами, влияющими на его метаболизм.
Отзывы потребителей
Пациенты, которые используют кардиомагнил, отмечают, что он помогает им понизить давление, улучшить самочувствие, предупредить приступы стенокардии и инсульта. Однако они также сталкиваются с постоянной болью в желудке, тошнотой, рвотой, изжогой, кровяными выделениями из ЖКТ, аллергией, головной болью и другими неприятными симптомами. Покупатели говорят, что им приходится использовать дополнительные средства для защиты желудка и крови, а также придерживаться строгой диеты.
Пациенты, использующие клопидогрел, отмечают, что он эффективно защищает их от тромбоза и ишемии, особенно после операций на сердце. Однако они также сталкиваются с высокой ценой препарата и сложностью его приобретения в аптеках. Покупатели говорят, что им приходится искать дешевые аналоги или заказывать лекарство через интернет. Отмечают, что у них возникают кровотечения из носа, десен, гематомы, синяки, диарея, сыпь и другие побочные эффекты. Также говорят о том, что им приходится регулярно сдавать анализы крови и консультироваться с врачом о дозировке и совместимости с другими лекарствами.
Вывод
В этой статье мы подробно изучили основные характеристики этих препаратов и установили, чем они отличаются друг от друга. Давайте сделаем выводы, основываясь на написанном материале. Кардиомагнил и клопидогрел – это два различных лекарства, которые имеют свои достоинства и недостатки в профилактике и лечении сердечно-сосудистых заболеваний. Кардиомагнил – это недорогое и легкодоступное средство, которое хорошо проверено и изучено, но может спровоцировать серьезные побочные эффекты на желудок и кровь. Клопидогрел – это более новый и действенный препарат, который превышает противовоспалительные, жаропонижающие и обезболивающие средства в уменьшении риска тромбоза и ишемии, но который имеет высокую цену и требует индивидуального выбора дозы и длительности лечения. Выбор между ними должен быть сделан врачом с учетом состояния пациента, наличия сопутствующих заболеваний, генетических особенностей, а также возможных взаимодействий с другими препаратами. Пациенту необходимо следовать рекомендациям врача, регулярно проверять состояние желудка и крови, а также не заниматься самолечением.
Задайте вопрос и получите мгновенный ответ
от искусственного интеллекта
Еще 133 статьи смотрите тут
Использование материалов сайта означает принятие пользовательского соглашения. Информация предоставлена исключительно в ознакомительных целях и не является рекламой. Имеются противопоказания, обратитесь к врачу.
40764
15.01.2024
Сосуды и сердце;
Роль клопидогреля в лечении и профилактике сердечно-сосудистых заболеваний
Статьи
Опубликовано в журнале:
«CONSILIUM MEDICUM»; ТОМ 11; № 10; стр. 130-137.
Г.А.Барышникова
Кафедра семейной медицины
ФГХ Учебно-научный медицинский центр, Москва
Ежегодно в России от сердечно-сосудистых заболеваний (ССЗ) умирают более 1 млн человек, т.е. примерно 700 человек на 100 тыс. населения. Хорошо известно, что причиной развития тяжелых сердечно-сосудистых осложнений, прежде всего инфаркта миокарда (ИМ) и инсульта, является повреждение поверхности атеросклеротической бляшки с формированием внутрисосудистого тромбоза (атеротромбоз) [1]. Именно клинические проявления атеротромбоза — ведущая причина смертности населения в экономически развитых странах, в том числе в России. В 2000 г. в мире в структуре общей смертности 52% составила смертность от осложнений атеротромбоза, существенно опередив онкологическую патологию (24%) [2]. Первыми на разрыв атеросклеротической бляшки реагируют тромбоциты, «прилипая» к открывающимся субэндотелиальным структурам (адгезия). Происходящая при этом активация тромбоцитов ведет к вовлечению в адгезивный процесс все новые кровяные пластинки и экспрессии на их поверхности IIb/IIIa гликопротеиновых (ГП) рецепторов, которые на завершающем этапе агрегации тромбоцитов играют ключевую роль в процессе тромбообразования, образуя «мостики» между тромбоцитами и адгезивными белками, прежде всего фибриногеном. Активация тромбоцитов может происходить под влиянием нескольких веществ, важнейшим из которых является аденозиндифосфат (АДФ). АДФ в высоких концентрациях содержится в плотных внутритромбоцитарных гранулах и, высвобождаясь из них, способен инициировать и усиливать процесс агрегации [3]. Активация АДФ-рецепторов ведет к изменению формы тромбоцитов, возрастанию внутриклеточной концентрации кальция, экспрессии ГП IIb/IIIa рецепторов и высвобождению β-селектина -мембранного гликопротеина, способствующего взаимодействию тромбоцитов с другими клетками [4].
Ведущая роль в профилактике осложнений атеросклероза принадлежит антитромбоцитарным препаратам (антиагрегантам), ингибирующим функцию тромбоцитов. Классификация антитромбоцитарных средств (антиагрегантов) представлена в табл. 1. Перечисленные антиагреганты блокируют агрегацию тромбоцитов посредством разных механизмов действия. Аспирин блокирует циклооксигеназу, предотвращая образование тромбоксана А2; дипиридамол увеличивает концентрацию циклических нуклеотидов и влияет на концентрацию АДФ, тромбина, арахидоновой кислоты; производные тиенопиридина (тиклопидин, клопидогрель) необратимо ингибируют АДФ-индуцированную агрегацию тромбоцитов, блокируя аденозиновые рецепторы тромбоцитов; антагонисты ГП рецепторов тромбоцитов GP IIb/IIIa предотвращают образование межтромбоцитарных фибриногеновых мостиков.
Таблица 1.
Основные классы антиагрегантных препаратов
Аспирин
Курантил
Тиклопидин (Тиклид)
Клопидогрель (Плавикс, Лопирел)
Абсиксимаб (Рео Про)
Эптифибатид
Тирофибан
Поскольку в первую очередь, вызывается и усиливается агрегация тромбоцитов тромбоксан А2 и АДФ, неудивительно, что с целью профилактики атеротромботических осложнений стали широко применять антиагреганты, влияющие на образование ТхА2 (аспирин) или блокирующие АДФ-рецепторы тромбоцитов (тиенопиридины). Дипиридамол используется преимущественно после перенесенного ишемического инсульта в комбинации с аспирином. Ингибиторы IIβ/IIIα ГП-рецепторов (прежде всего абсиксимаб) с успехом применяются (парентерально!) при проведении ангиопластики, однако попытка использовать эти препараты длительно перорально не увенчалась успехом.
В течение многих лет «золотым стандартом» антиагрегантной терапии оставалась ацетилсалициловая кислота (аспирин), имеющая очень хорошую доказательную базу. Доказана эффективность аспирина при всех формах ишемической болезни сердца (остром коронарном синдроме — ОКС, остром ИМ, после перенесенного инфаркта, стабильной стенокардии, после аортокоронарного шунтирования и ангиопластики), при ишемическом инсульте и после перенесенного ишемического инсульта, при поражении периферических артерий. По данным метаанализа 287 исследований, включивших более 200 тыс. пациентов высокого риска сердечно-сосудистых осложнений, проведенного группой экспертов Antithrombotic Trialists’ Collaboration, 2002 г. [5], длительный прием аспирина (75-325 мг/сут) снижает суммарную частоту ИМ, инсульта и сердечно-сосудистой смерти на 23%. При остром ишемическом инсульте аспирин вообще является единственным (безальтернативным) антиагрегантом, эффективность которого доказана. Кроме того, только аспирин рекомендован для первичной профилактики сердечно-сосудистых осложнений. Во многом благодаря именно аспирину показания к применению антиагрегантов после 2-го метаанализа, проведенного группой экспертов Antithrombotic Trialists’ Collaboration, значительно расширились (табл. 2). К середине 1990-х годов аспирин вошел в качестве обязательного препарата практически во все рекомендации по лечению и профилактике клинических проявлений атеротромбоза.
Таблица 2.
Расширение показаний к применению антитромбоцитарных препаратов по итогам метаанализа 2002 г. [5]
| Показания к применению антитромбоцитарных препаратов | 1994 г. | 2002 г. |
| Острый ИМ | + | + |
| Нестабильная стенокардия | + | + |
| Перенесенный ИМ | + | + |
| Перенесенный ишемический инсульт | + | + |
| Острый ишемический инсульт | + | |
| Перемежающаяся хромота | + | |
| Стабильная стенокардия | + |
Но при всех его достоинствах аспирин не лишен ряда недостатков. Хорошо известны его побочные эффекты: диспепсия (в 20-30% случаев при длительном применении), эрозивно-язвенные поражения желудочно-кишечного тракта (ЖКТ), бронхоспазм, острый приступ подагры (из-за нарушения экскреции мочевой кислоты); аллергические реакции. Развитие аспирининдуцированных осложнений со стороны слизистой оболочки ЖКТ требует отмены аспирина и назначения наиболее эффективных в данной ситуации ингибиторов протонной помпы. Снизить риск неблагоприятного воздействия аспирина на ЖКТ можно, используя таблетки с кишечнорастворимой оболочкой, например Аспирин Кардио [6]. При непереносимости аспирина альтернативой ему согласно большинству европейских и отечественных рекомендаций является клопидогрель.
Следует также указать, что в последние годы привлечено внимание клиницистов к возможности резистентности больных к аспирину (неспособность аспирина угнетать синтез тромбоксана А2 и подавлять агрегацию тромбоцитов). По данным разных исследований, частота резистентности к аспирину колеблется в широких пределах от 1 до 61% [7-9], однако надежных тестов для выявления аспиринорезистентности нет [10]. Сложилось мнение, что у пациентов с высоким риском тромботических осложнений целесообразно сочетать аспирин с другими антитромбоцитарными средствами (клопидогрелем — у больных ишемической болезнью сердца — ИБС, с синдромом перемежающейся хромоты, цереброваскулярной недостаточностью; дипиридамолом — после перенесенного ишемического инсульта).
В связи с этим понятен интерес клиницистов к сравнительно новому классу антиагрегантов — тиенопиридинам (тиклопидин, клопидогрель), уменьшающим агрегацию, блокируя АДФ-рецепторы тромбоцитов. После аспирина клопидогрель является одним из наиболее изученных антитромбоцитарных препаратов, эффективность и безопасность которого подтверждены в крупных рандомизированных контролируемых плацебо исследованиях.
Одним из первых исследований, в которых сравнивалась эффективность клопидогреля и аспирина, было исследование CAPRIE (Clopidogrel versus Aspirin in Patients at Risk of Ischaemic Events). В него были включены 19 185 больных с поражением одного из сосудистых бассейнов: больные, недавно перенесшие ИМ или ишемический инсульт либо страдающие атеросклерозом сосудов нижних конечностей и, соответственно, имеющие высокий риск развития повторной сердечно-сосудистой катастрофы. Половина больных в течение 1-3 лет (средняя длительность наблюдения 1,9 года) получали аспирин 325 мг/сут, половина — клопидогрель 75 мг/сут.
Частота регистрируемых ишемических событий (ИМ, ишемический инсульт, ампутация конечностей, сердечно-сосудистая смерть) составила 5,32% в группе рандомизированных к приему клопидогреля и 5,83% — в группе рандомизированных к приему аспирина (рис. 1). Относительное снижение риска возникновения этих событий при использовании клопидогреля составило 8,7% (р=0,043) [11]. Мнение экспертов, по результатам исследования, заключалось в том, что появился новый антиагрегант с отличающимся от аспирина механизмом действия, который не менее эффективен, чем аспирин, а у больных, перенесших ИМ, инсульт и страдающих перемежающейся хромотой, даже более эффективен. При сравнении эффективности клопидогреля и аспирина отдельно по подгруппам больных были обнаружены его наибольшие преимущества у лиц, страдающих перемежающейся хромотой. Возможно, это связано с тем, что у больных с перемежающейся хромотой АДФ как индуктор агрегации имеет большее значение, чем тромбоксан А2, на содержание которого преимущественно влияет аспирин. Кроме того, в исследовании CAPRIE в группе клопидогреля отмечено меньшее число осложнений со стороны ЖКТ (рис.2).
Рис. 1. Сравнительная эффективность аспирина и клопидогреля в исследовании CAPRIE [11].
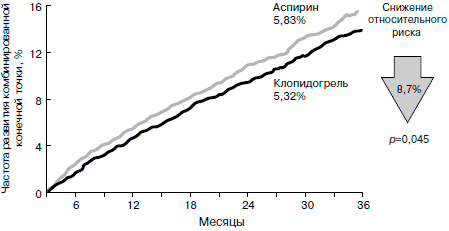
Рис. 2. Риск осложнений со стороны ЖКТ в исследовании CAPRIE [12].
Клопидогрель по сравнению с аспирином вызывает меньше осложнений со стороны ЖКТ

*Пациенты, имеющие непереносимость или толерантность к аспирину, и пациенты с рецидивирующей язвенной болезнью желудка или язвенной болезнью в анамнезе были исключены из исследования.
После подведения итогов исследования CAPRIE возникла идея оценить эффективность одновременного назначения аспирина и клопидогреля у больных с показаниями к антитромбоцитарной терапии, тем более что имелись экспериментальные данные, указывающие на синергизм антитромботического действия аспирина и клопидогреля. В дальнейшем клопидогрель уже не противопоставляется аспирину, а используется в комбинации с аспирином. Так, в исследовании CURE (Clopidogrel in Unstable Angina to Prevent Recurrent Events) оценивается эффективность комбинации клопидогреля с аспирином и монотерапии аспирином при ОКС без стойких подъемов сегмента ST [13]. В исследование были включены 12 562 больных, 61% — с нестабильной стенокардией, а 39% — с мелкоочаговым ИМ. Подавляющее большинство больных получали гепарин (96% больных) и β-блокаторы (78% больных), около 50% больных получали ингибиторы ангиотензинпревращающего фермента (ИАПФ) и статины.
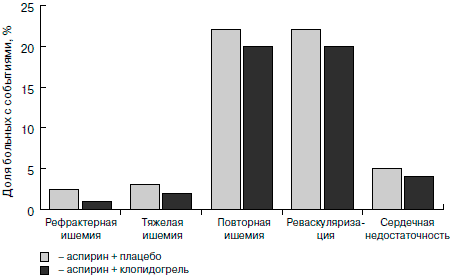
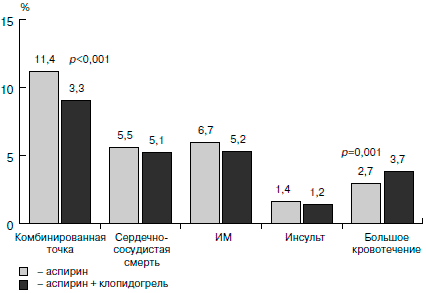
Все больные были рандомизированы в группу монотерапии аспирином (75-325 мг/сут; 6303 человека) или в группу терапии аспирином в комбинации с клопидогрелем (в 1-е сутки нагрузочная доза 300 мг, в дальнейшем — 75 мг/сут; 6259 больных). Нагрузочная доза клопидогреля (300 мг) позволила ускорить действие препарата: различия в сравниваемых группах начали проявляться уже через 2 ч. Через 12 мес количество главных конечных точек (смерть от сердечных причин, ИМ и инсульт) в группе больных, получавших комбинацию клопидогреля и аспирина, оказалось на 20% меньше, чем в группе аспирина (9,3 и 11,4% в группах соответственно, p=0,001; рис. 3). Относительный риск развития ИМ с зубцом Q в группе комбинированной терапии снизился на 40%! Уже к концу 1-х суток лечения количество сердечно-сосудистых смертей, ИМ, инсультов и эпизодов рефрактерной ишемии в группе клопидогреля было на 34% меньше, чем в группе плацебо (1,4 и 2,1% соответственно, p<0,003) [14]. На рефрактерной ишемии следует остановиться особо, поскольку ее уменьшение означает уменьшение числа пациентов с выраженным болевым синдромом, требующим коронарной реваскуляризации, проведения тромболизиса и др. (рис. 4). Однако следует отметить достоверно более высокую частоту больших кровотечений в группе комбинированной антиагрегантной терапии.
Рис. 3. Эффективность комбинированной антиагрегантной терапии при ОКС без ST: исследование CURE [13, 14].
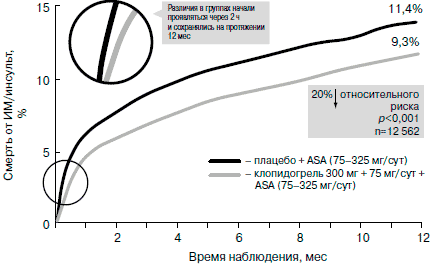
Рис. 4. Симптоматические эффекты комбинации аспирина с клопидогрелем в исследовании CURE [13].
Результаты исследования CURE оказались столь впечатляющими, что комбинация аспирина и клопидогреля была включена в рекомендации по лечению больных ОКС без ST на электрокардиограмме (ЭКГ). Клопидогрель следует назначать вместе с аспирином немедленно после установления диагноза ОКС без ST (в 1-й день нагрузочная доза составляет 300 мг, в дальнейшем — по 75 мг ежедневно в течение 9-12 мес). При возникновении потребности в проведении аортокоронарного шунтирования клопидогрель следует отменить за 5 дней до операции [15-17].
В исследовании CURE более чем у 20% больных было выполнено чрескожное внутрикоронарное вмешательство (ЧКВ), в большинстве случаев со стентированием коронарной артерии. В рамках субисследования CURE-PCI (Clopidogrel in Unstable angina to prevent Recurrent Events — Percutaneous Coronary Intervention) планировалось оценить роль раннего назначения клопидогреля больным, подвергнутым ЧКВ. Для этого половине больных (n=1313) назначили клопидогрель в день поступления в стационар (в среднем за 10 дней до ЧКВ). Остальным больным (n=1345) клопидогрель был назначен в день выполнения ЧКВ (до этого они получали плацебо). Затем обе группы больных в течение 28 дней получали комбинацию аспирин + клопидогрель в «открытом» режиме, после чего 1-я группа продолжила комбинированную антитромбоцитарную терапию, 2-я вернулась к приему аспирина с плацебо. Частота неблагоприятных исходов (сердечная смерть, ИМ и необходимость в экстренной реваскуляризации) в течение 30 дней после ЧКВ в группе больных, получавших клопидогрель до ЧКВ, была достоверно ниже, чем в группе больных, начавших прием клопидогреля в день выполнения ЧКВ (4,5 и 6,4% соответственно, p=0,03) [18]. У больных, получавших клопидогрель до ЧКВ и продолживших его прием по окончании 28дневного периода «открытого» использования клопидогреля после ЧКВ, частота неблагоприятных исходов (сумма смертей и ИМ) в период от ЧКВ до окончания наблюдения была достоверно ниже (6%), чем в группе плацебо (8%; p=0,047). Если же за точку отсчета взять не ЧКВ, а момент рандомизации, то различие между группами будет более выраженным (частота смерти и ИМ составит 8,8% в группе клопидогреля и 12,6% — в группе плацебо; p=0,002); относительное снижение риска смерти и/или ИМ составило 31%. Преимущество клопидогреля перед плацебо отмечено не только в случае стентирования, но и в случаях, когда вмешательство ограничивалось обычной баллонной ангиопластикой коронарных артерий. При этом снижение риска смерти, ИМ и инсульта было даже более выраженным (44%), чем при ангиопластике со стентированием (27%). По завершении исследования CURE-PCI стали очевидными преимущества назначения клопидогреля в нагрузочной дозе минимум за 6 ч до ЧКВ с длительным последующим приемом, но и целесообразность применения препарата по такой схеме не только при стентировании коронарных артерий, но и у больных, подвергнутых обычной баллонной ангиопластике.
Доказательства эффективности длительной (около 1 года) терапии клопидогрелем после ЧКВ, полученные у больных с ОКС в исследовании CURE-PCI, послужили основанием для организации нового крупномасштабного исследования CREDO (Clopidogrel for the Reduction of Events During Observation trial), целью которого было изучение эффективности 12-месячной терапии клопидогрелем в дозе 75 мг/сут на фоне стандартной терапии, включающей аспирин, в сравнении с плацебо [19].
В исследование включали больных ИБС с показаниями к ЧКВ (53% имели клиническую картину нестабильной стенокардии). Все больные с 1-го дня после выполнения ЧКВ получали клопидогрель по 75 мг ежедневно в течение 28 дней. Рандомизация осуществлялась в две группы: больные в 1-й группе получали нагрузочную дозу клопидогреля 300 мг за 3-24 ч до ЧКВ, а затем по 75 мг ежедневно в течение 12 мес, во 2-й — вместо нагрузочной дозы клопидогреля было плацебо, и после 28-го дня до окончания времени наблюдения (12 мес) назначалось плацебо. Больные обеих групп на протяжении всего исследования получали аспирин. Оказалось, что длительный прием клопидогреля больными после ЧКВ приводит к снижению риска развития смерти, ИМ и инсульта на 27% (рис. 5). В соответствии с результатами исследований PCI-CURE и CREDO рекомендуется прием клопидогреля начинать с нагрузочной дозы 300 мг за 6 ч до выполнения ЧКВ и продолжать прием 75 мг клопидогреля ежедневно в течение 3-12 мес. При необходимости сократить время, требующееся для максимального подавления агрегации тромбоцитов, до 2 ч рекомендуется увеличить ударную дозу клопидогреля до 600 мг [20-22].
Рис. 5. Эффективность монотерапии аспирином и комбинированной терапии аспирином и клопидогрелем при ОКС без подъема ST: данные исследования CURE [13].
В 2007 г. E.Eisenstein и соавт. [23] опубликовали сообщение о необходимости более продолжительного, чем было рекомендовано ранее, приема клопидогреля после ЧКВ с установкой стентов, высвобождающих антипролиферативные препараты. В течение 2 лет осуществлялось наблюдение за больными, перенесшими ЧКВ с установкой обычных металлических стентов (3165 больных) или стентов, обработанных сиролимусом или паклитакселем (1501 больной). В той и другой группе больных учитывались такие исходы, как смерть, развитие острого ИМ или необходимость повторной реваскуляризации в зависимости от типа стента и приема в дополнение к аспирину клопидогреля или плацебо. У пациентов с освобождающими лекарства стентами без перечисленных событий через 6 мес после стентирования использование клопидогреля ассоциировалось со значительным снижением риска осложнений (смерть, смерть + острый ИМ), в то время как у больных, которым были установлены обычные стенты, влияние клопидогреля на риск осложнений было недостоверным (рис. 6). В настоящее время тип установленного стента учитывается при определении продолжительности приема клопидогреля после ЧКВ (рис. 7).
Рис. 6. Эффект длительного (до 1 года) приема клопидогреля после ЧКВ: данные исследования CREDO [19].
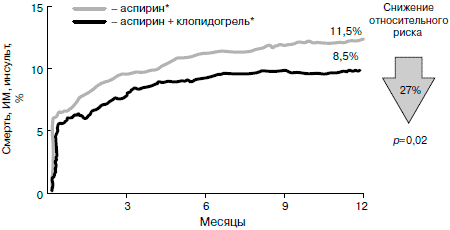
Рис. 7. Влияние длительной терапии клопидогрелем на частоту осложнений после ангиопластики со стентированием в зависимости от типа стента [23].
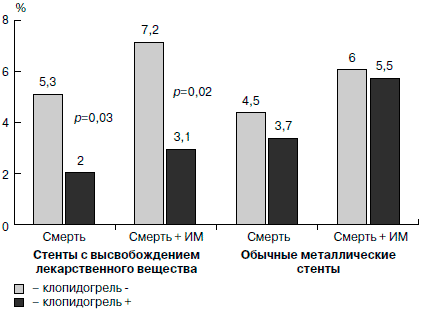
Исследование CLARITY (CLpidogrel as Adjunctive ReperfusIon TherapY) открыло новые возможности применения клопидогреля. Известно, что проводимый согласно стандартам лечения острого ИМ с подъемом сегмента ST тромболизис оказывается успешным немногим более чем у половины больных, причем у части больных даже после успешного тромболизиса развивается реокклюзия инфарктсвязанной коронарной артерии. Полагают, что это может быть связано с повышением активности тромбоцитов под действием тромболитиков. В исследование CLARITY были включены больные (n=3491), доставленные в стационар в течение 12 ч от появления симптомов со стойким подъемом сегмента ST. Половине больных в дополнение к аспирину и тромболитику назначался клопидогрель (нагрузочная доза 300 мг, затем — 75 мг/сут), половине — плацебо. Через несколько дней всем больным проводили коронарную ангиографию. Первичная комбинированная конечная точка включала в себя зарегистрированную при коронарографии окклюзию инфарктсвязанной артерии, смерть, рецидив ИМ. Частота достижения первичной конечной точки в группе плацебо составила 21,7%, в группе клопидогреля — 15%, т.е. в группе клопидогреля события, составляющие конечную точку, развивались на 36% реже (p<0,001). На 30-й день в группе клопидогреля такие неблагоприятные события, как сердечнососудистая смерть, повторный ИМ и повторная ишемия, потребовавшая реваскуляризации, развивались на 20% реже, чем в группе плацебо. Больные, получавшие клопидогрель, значительно реже подвергались экстренной коронарографии в первые 2 сут (15,4% против 18,6%, p=0,01) и неотложной реваскуляризации (19,5% против 23,3%, p=0,005). Частота крупных кровотечений и геморрагических инсультов в обеих группах достоверно не различалась [24].
Доказательства эффективности клопидогреля при остром ИМ также были получены в крупномасштабном исследовании COMMIT/CCS-2 (ClOpidogrel & Metoprolol in Myocardial Infarction Trial) [2]. В исследование COM-MIT/CCS-2 были включены 45 852 пациента с подозрением на острый ИМ. Больные были рандомизированы на две группы: получавших клопидогрель 75 мг/сут (без нагрузочной дозы) в течение 2-4 нед и получавших плацебо. Кроме того, все больные получали аспирин, и более чем половине больных была проведена тромболитическая терапия. Комбинированную конечную точку составили смерть, рецидив ИМ и инсульт; частота ее развития у больных, получавших клопидогрель, в течение 28 дней наблюдения оказалась на 9% ниже, чем у больных, получавших плацебо. Кроме того, отмечено достоверное (на 7%) снижение смертности. Было рассчитано, что клопидогрель, назначенный 1000 больных с подозрением на острый ИМ дополнительно к аспирину, предотвратит 3 рецидива ИМ (p=0,01), 1 инсульт (p=0,3) и 5 смертельных исходов (p=0,03). Следует отметить, что действие клопидогреля на конечную точку оказалось статистически значимым у больных, получивших тромболитик, но недостоверным у больных без тромболитического лечения.
Таким образом, в двух независимых друг от друга исследованиях, включавших почти 50 тыс. больных с ИМ, показана способность клопидогреля снижать риск осложнений преимущественно при проведении тромболитической терапии. Предполагается, что в основе благоприятного действия клопидогреля у этой категории больных лежит его способность предотвратить ретромбоз коронарной артерии после успешного тромболизиса.
В 2006 г. в США Управление по контролю за пищевыми продуктами и лекарственными средствами (Food and Drug Administration -FDA), основываясь на результатах исследований COMMIT и CLARITY (50 тыс. пациентов), одобрило использование клопидогреля (совместно с аспирином) в лечении пациентов с острым ИМ с подъемом сегмента ST на ЭКГ, которым не планируется выполнение ангиопластики.
Таким образом, комбинация аспирина и клопидогреля в острой ситуации (ОКС, острый ИМ, выполнение ЧКВ с последующим стентированием коронарных артерий) может обеспечить более высокую эффективность в предупреждении серьезных кардиоваскулярных событий, чем монотерапия аспирином. Однако большой интерес вызывали также перспективы комбинирования разных антитромбоцитарных препаратов, прежде всего аспирина и клопидогреля, для вторичной и первичной профилактики у пациентов с низким риском (при стабильном течении существующего ССЗ, при наличии факторов риска ССЗ). Попытка изучить эффективность комбинированной антитромбоцитарной терапии у таких пациентов была предпринята в международном контролируемом плацебо исследовании CHARISMA [26]. В этом исследовании, включавшем 15 603 пациента, изучали эффективность комбинированной антитромбоцитарной терапии клопидогрелем и аспирином в сравнении с монотерапией аспирином у лиц с уже имеющейся кардиоваскулярной патологией (документированные ИБС, цереброваскулярная патология и/или облитерирующий атеросклероз нижних конечностей) и у лиц без ССЗ, но с множественными факторами риска атеротромбоза. Первая подгруппа, соответственно, называлась симптомной, или группой вторичной профилактики атеротромботических событий, вторая — бессимптомной, или группой первичной профилактики. Средняя длительность наблюдения в этом исследовании составила 28 мес.
По результатам исследования, частота первичной конечной точки (сердечно-сосудистая смерть, нефатальные ИМ и инсульт) составила 7,3% в группе монотерапии аспирином и 6,8% в группе комбинированной антитромбоцитарной терапии (уменьшение относительного риска — 7,1%; p=0,22). Однако при оценке эффективности комбинированной терапии отдельно у больных с ССЗ (симптомная подгруппа) отмечены ее явные преимущества (6,9% в группе комбинированной терапии против 7,9% в группе монотерапии аспирином; относительное уменьшение риска составило 12,5%, p=0,046). Риск тяжелых геморрагических осложнений при этом возрос по сравнению с монотерапией аспирином недостоверно (1,7% против 1,3%, p=0,09). Однако у больных с множественными факторами риска ССЗ, но без диагностированного ССЗ, в случае комбинированной антитромбоцитарной терапии риск наступления сердечно-сосудистой смерти оказался достоверно выше, чем при монотерапии аспирином (3,9% против 2,2%, p=0,01). Таким образом, исследование CHARISMA продемонстрировало, что у больных с множественными факторами риска, но без установленных ССЗ, т.е. в качестве средства первичной профилактики, проведение комбинированной антитромбоцитарной терапии нецелесообразно, тогда как у больных с установленной кардиоваскулярной патологией риск сердечно-сосудистых осложнений снижается без значимого увеличения частоты тяжелых кровотечений. Результаты исследования CHARISMA явились «холодным душем» для приверженцев агрессивной антиагрегантной терапии [27]. Выводы из исследования CHARISMA представлены в табл. 3.
Таблица 3.
Антиагреганты при ангиопластике и стентировании коронарных артерий в зависимости от лекарственного покрытия стентов и использованного для покрытия препарата (Федеральное руководство по применению лекарственных препаратов, 2007)
|
|
|
|
| Продолжительность терапии после ЧКВ: 1) при использовании металлических стентов без покрытия — 2-4 нед; 2) при использовании стентов, покрытых сиролимусом, — не менее 3 мес; 3) при использовании стентов, покрытых пакликтакселом, — не менее 6 мес; 4) ОКС без подъема ST + покрытый стент — 1 год |
Рис. 8. Кривые концентрация-время при назначении здоровым добровольцам Лопирела и Плавикса.
Наиболее обоснованным представляется использование комбинации клопидогреля и аспирина в тех случаях, когда имеется выраженное атеросклеротическое поражение сонных и других мозговых артерий у пациентов, перенесших транзиторную ишемическую атаку или инсульт, при сочетанном поражении артерий, а также при возникновении повторных сердечнососудистых событий на фоне приема аспирина [28].
Таким образом, в крупных клинических исследованиях (CAPRIE, CURE, CREDO) почти у 35 тыс. больных получены доказательства того, что клопидогрель является эффективным и безопасным средством профилактики тромботических осложнений атеросклероза. Клопидогрель признан обязательным элементом антитромботического лечения при стентировании коронарных артерий. Причем данные исследований исследования PCI CURE, CREDO указывают на необходимость начала лечения клопидогрелем не менее чем за 6 ч до внутрикоронарного вмешательства.
Главным недостатком оригинального клопидогреля остается его высокая стоимость, поэтому появление его генериков может только приветствоваться при условии их биоэквивалентности оригинальному препарату. Одним из генериков клопидогреля является препарат Лопирел, (компания «Актавис») недавно появившийся в России, доказательства фармакокинетической биоэквивалентности которого были получены при проведении исследования в Канаде (рис. 8). Лопирел выпускается в таблетках по 75 мг. Препарат хорошо всасывается из ЖКТ независимо от приема пищи. Торможение агрегации тромбоцитов наблюдается через 2 ч после приема нагрузочной дозы (300 мг), максимальный эффект — через 4-7 дней постоянного приема в дозе 75 мг/сут. Применение Лопирела показано у больных с ОКС (в комбинации с аспирином) и у больных, перенесших ИМ, ишемический инсульт, с синдромом перемежающейся хромоты (дозы и режим применения представлены в табл. 4). Лопирел хорошо переносится. К числу его наиболее часто встречающихся побочных эффектов относятся диспепсия, диарея. Подобно другим антитромбоцитарным препаратам, Лопирел следует с осторожностью назначать больным с повышенным риском кровотечения. Его назначение противопоказано при остром кровотечении, язвенной болезни желудка и двенадцатиперстной кишки в стадии обострения, беременности, тяжелой печеночной недостаточности. Перед оперативным вмешательством прием Лопирела следует прекратить за 5-7 дней. В случае необходимости эффект Лопирела может быть устранен переливанием тромбоцитной массы. Более низкая по сравнению с оригинальным клопидогрелем стоимость Лопирела позволяет надеяться на более широкое применение этого высокоэффективного антиагреганта как у больных с непереносимостью аспирина, так и в составе комбинированной антиагрегантной терапии.
Таблица 4.
Показания к применению Лопирела
| Контингент больных | Профилактика атеротромбоза | |
| начальная доза | поддерживающая доза | |
| Больные, перенесшие ИМ, ишемический инсульт, с диагностированным заболеванием периферических артерий | 75 | 75 |
| Больные с ОКС без подъема сегмента ST (нестабильная стенокардия или ИМ без зубца Q на ЭКГ), в комбинации с аспирином | 300 | 75 |
ЛИТЕРАТУРА
1. Fuster V, Fallon JT, Badimon JJ, Nemerson Y. The unstable atherosclerotic plaque: clinical significance and therapeutic intervention. Thrombosis and Hemostasis 1997; 78 (1): 247-55.
2. The World Health Report 2001. Geneva: WHO; 2001.
3. George JN. Platelets. Lancet 2000; 355: 1531-9.
4. Daniel JL, Dangelmaier C, Jin J et al. Molecular basis for ADP-induced platelet activation: I. Evidence for three distinct ADP receptors on human platelets. J Biol Chem 1998; 273: 2024-9.
5. Collaborative meta-analysis of randomized trials of antiplatelet therapy for prevention of death, myocardial infarction, and stroke in high risk patients. BMJ 2002; 324: 71-86.
6. Kubler W, Darius HZ. Kardiol 2005; 94 (suppl. 3): 66-73.
7. Gum PA, Kottke-Marchant K, Welsh PA et al. A prospective, blinded determination of the natural history of aspirin resistance among stable patients with cardiovascular disease. J Am Coll Cardiol 2003; 41: 961-5.
8. Mueller MR, Salat A, Stangl P et al. Variable platelet response to low-dose ASA and the risk of limb deterioration in patients submitted to peripheral arterial angioplasty. Thromb Haemost 1997; 78: 1003-7.
9. Eikelboom JW, Hirsh J, Weitz JI et al. Aspirin resistance and the risk of myocardial infarction, stroke, or cardiovascular death in patients at high risk of cardiovascular outcomes. Circulation 2002; 105: 1650-5.
10. Ушкалова Е.А. Аспиринорезистентность: механизмы развития, методы определения и клиническое значение. Фарматека. 2006; 13: 35-41.
11. CAPRIE Steering Committee. Lancet 1996; 348: 1329-39.
12. Harker LA et al. Drug Safety 1999; 21: 325-35.
13. The Clopidogrel in Unstable Angina to Prevent Recurrent Events trial investigators. Effects of clopidogrel in addition to aspirin in patients with acute coronary syndromes without ST.segment elevation. New Engl J Med 2001; 345:494-502.
14. Yusuf S, Mehta SR, Zhao F et al on Behalf of the CURE (Clopidogrel in Unstable angina to prevent Recurrent Events) Trial Investigators. Early and Late Effects of Clopidogrel in Patients With Acute Coronary Syndromes. Circulation 2003; 107: 966-72.
15. Bertrand ME, Simoons ML, Fox KAA et al. Management of acute coronary syndromes in patients presenting without persistent ST.segment elevation. The Task Force on the Management of Acute Coronary Syndromes of the European Society of Cardiology. EurHeart J 2002; 23: 1809-40.
16. Braunwald E, Antman EM, Beasley JW et al. ACC/AHA guideline update for the management of patients with unstable angina and non-ST.segment elevation myocardial infarction: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Committee on the Management of Patients With Unstable Angina). J Am Coll Cardiol 2002; 40: 1366-74.
17. Всероссийское научное общество кардиологов. Рекомендации по лечению острого коронарного синдрома без стойкого подъема сегмента ST на ЭКГ. М., 2007.
18. Mehta S, Yusuf S, Peters R et al. Effects of pretreatment with clopidogrel and aspirin followed by longterm therapy in patients undergoing percutaneous coronary intervention: the PCI CURE study. Lancet 2001; 358: 527-33.
19. Beinart S, Kolm P, Veledar E et al. «Short and Long.Term Cost Effectiveness of Early and Sustained Dual Oral Antiplatelet Therapy with Clopidogrel following Percutaneous Coronary Intervention: Results from CREDO» Circulation 2003; 108 (Suppl. 4; 17): iv-775 (abstract) 3495.
20. Seyfarth Hf, Koksch M, Roethig G et al. Effect of 300- and 450-mg clopidogrel LDs on membrane soluble P-selectin in patients undergoing coronary stent implantation. Am Heart f 2002; 143: 118-23.
21. Muller I, Seufarth M, Rudiger S et al. Effect of high LD of clopidogrel on platelet function in patients undergoing coronary stent placement. Heart 2000; 85: 92-3.
22. Angiolillo Df, Fernandez-Ortiz A, Bernardo E et al. High clopidogrel loading dose during coronary stenting: effects on drug response and interindividual variability. Eur Heartf 2004; 25: 1903-10.
23. Eisenstein EL, Anstrom Kf, Kong DF et al. Clopidogrel use and long-term clinical out-comes after drug-eluting stent implantation. JAMA 2007; 297 (2): 159-68.
24. Sabatine MS, Cannon CP, Gibson CM et al. Addition of clopidogrel to aspirin and fibrinolytic therapy for myocardial infarction with ST-segment elevation N Engl J Med 2005; 352: 1179-89.
25. COMMIT collaborative group. Addition of clopidogrel to aspirin in 45852 patients with acute myocardial infarction: randomized placebo-controlled trial. Lancet 2005; 366: I607-21.
26. Bhatt DL, Fox K.A, Hacke W et al CHARISMA Investigators. Clopidogrel and aspirin versus aspirin alone for the prevention of atherothrombotic events. N Engl J Med 2006; 354 (16): 1706-17.
27. Serebruany VL. Aggressive antiplatelet strategies: time to reconsider. Eur Heart J 2007; 28: 2183-4.
28. Ушкалова Е.А. Добавление клопидогреля к аспирину может быть полезно больным с симптоматическим атеротромбозом, но не рекомендуется для пациентов с множественными факторами риска: результаты исследования CHARISMA Фарматека. 2006; 13: 16-9.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Лекарства для «разжижения» крови: частые вопросы кардиологу
Содержание:
- Когда начинать прием лекарств для разжижения крови
- Какие лекарства разжижают кровь
- Как понять, нужно ли принимать кроверазжижающие препараты
Препараты для профилактики и лечения заболеваний, связанных с образованием тромбов, прочно вошли в арсенал современной медицины, и, конечно, очень активно применяются в кардиологии и сердечно-сосудистой хирургии.
Интерес к этим лекарственным средствам подстегнула и недавняя пандемия коронавирусной инфекции, что привело к широкому, и часто необоснованному их применению.
Давайте попытаемся немного разобраться в вопросах назначения этой группы препаратов.
Когда начинать прием лекарств для разжижения крови
“Соседка говорит, что начинать принимать кроверазжижающие лекарства нужно всем после 40 лет — профилактически. Это так?”
На самом деле, нет.
Назначение препаратов не зависит от возраста, и строго определяется наличием показаний и противопоказаний у конкретного пациента. Если не учесть эти факторы, то можно нанести вред, значительно увеличив риск кровотечений и поражений желудочно-кишечного тракта. Поэтому, это как раз тот случай, когда самолечение — это плохо.
Какие лекарства разжижают кровь
“А эти препараты: они же все от тромбов — значит действуют, примерно, одинаково? А почему тогда моей сестре назначили препарат за 300 рублей, а мне за 3 тысячи рублей? Мне попался плохой врач? Можно мне принимать лекарство, как у сестры?”
Постараемся ответить подробно!
Препараты, влияющие на тромбообразование, относятся к разным группам:
- антиагреганты — не дают кровяным пластинкам — (тромбоцитам) склеиваться между собой, применяются в основном для профилактики и лечения заболеваний, связанных с артериальным тромбозом — например, ишемическая болезнь сердца.
Самый известный представитель этого класса — это ацетилсалициловая кислота (торговые марки: тромбо АСС, аспирин — кардио, кардиомагнил, кардиаск и т.д.), ещё есть клопидогрел (плавикс, зилт, плагрил, и т.д), тикагрелор (брилинта), прасугрель (эфиент), а также некогда популярный дипиридамол, больше известный, как «курантил».
Иногда, например, после хирургических вмешательств на артериях или после инфаркта миокарда два препарата этой группы назначаются совместно (например, аспирин + плавикс) - антикоагулянты — это лекарства, которые влияют на процессы тромбообразования за счёт изменения активности факторов свёртывания, находящихся в плазме (жидкой части крови).
Назначаются при тромбозах различных сосудов, тромбах в полостях сердца, наличии протезов клапанов сердца, при мерцательной аритмии (её ещё называют — фибрилляция предсердий), как профилактику тромбозов при некоторых хирургических вмешательствах и тяжёлых заболеваниях (в том числе онкологических), при осложнениях течения беременности.
Бывают в виде таблеток — варфарин (требует контроля специального показателя — МНО), более современные препараты — ксарелто, прадакса и эликвис; и в виде — инъекций — гепарин и его низкомолекулярные формы (клексан, фраксипарин и т.п.) - Тромболитики — очень серьёзные препараты! Применяются в первые часы (реже сутки) после острого эпизода тромбоза для растворения тромб — только в инъекциях, в условиях палаты интенсивной терапии или реанимации. Иногда бывает случаи, когда антитромботические препараты из разных групп назначаются одновременно — например, антикоагулянт + антиагреггант. Это всегда требует пристального врачебного контроля, так как такая схема увеличивает риск кровотечений
Как видите, все эти препараты очень разные, назначаются в разных ситуациях, и, далеко не всегда, взаимозаменяемы.
Доверяйте вашему доктору!
Как понять, нужно ли принимать кроверазжижающие препараты
“К врачу не всегда можно попасть быстро. А медсестра в процедурном кабинете, когда брала у меня кровь, сказала, что кровь « густая». Я могу как-то определить самостоятельно, что нужно принимать кроверазжижающие препараты? Есть ли какой-то анализ, который я могу сдать и по результатам начать пить эти лекарства в ожидании приема врача?”
Самостоятельно принимать никакие препараты из этой группы не надо! Все эти препараты могут иметь достаточно серьезные побочные эффекты, вплоть до очень тяжелых кровотечений. Никакого лабораторного анализа определяющего показания к назначению этих препаратов без учета состояния пациента не существует.
Правильный подбор и дозирование препарата с учетом всех показаний, противопоказаний и лекарственных взаимодействий возможен только после проведения подробной консультации квалифицированного специалиста.
Врачи нашей клиники всегда готовы приложить все наши знания, чтобы назначенное лечение стало для Вас максимально эффективным и безопасным!
Если у вас остались вопросы и вам нужна профессиональная консультация, вы всегда можете обратиться за помощью к нашим докторам!
Записаться на прием
Оставьте нам свои контакты, и мы обязательно Вам перезвоним.

Павлова Ольга
Борисовна
Врач-кардиолог, врач-терапевт
Стаж работы: c 1998 года
Подробнее
