Другой важный аспект снижения системного эффекта ИГКС — размер частиц ГКС, поступающих из ингалятора в дыхательные пути. К респирабельной фракции (т. е. поступающей к тканям-мишеням) относят мелкие частицы, которые оседают в бронхах всех калибров (средний аэродинамический диаметр для депозиции в легких составляет 2–4,7 µm). Так, недавно была разработана новая форма экстрамелкодисперсного беклометазона с использованием пропеллента гидрофторалкана 134а. Клинические исследования, проведенные у детей и взрослых, больных БА, показали высокую эффективность и безопасность препарата в половинной дозе (100 мкг экстрамелкодисперсного Беклометазона дипропионата клинически эквивалентны 250 мкг неэкстрамелкодисперсной форме Беклометазона дипропионата) и отсутствие у него системного побочного эффекта на метаболизм костей, рост и надпочечниковую функцию [16, 17].
Интересно отметить, что остеобласты экспрессируют на своей поверхности бета2-адренорецепторы. Пока нет отдельных научных исследований, посвященных влиянию на костную ткань монотерапии бета2-агонистами у больных БА. Но клиницисты уже давно получили доказательства преимущества применения комбинации ИГКС с бета2-агонистом длительного действия по сравнению с повышением дозы ГКС при лечении средней и тяжелой форм БА.
Логично предположить, что подобный подход будет полезным и в превенции развития ОП. Лишь недавно опубликованы результаты влияния на костный метаболизм комбинированной терапии (сальметерол + флутиказона пропионат) по сравнению с монотерапией флутиказоном [18]. Через год после терапии выраженное снижение МПКТ документировано в группе больных, принимавших только ИГКС, однако это различие было статистически недостоверным.
Возможно, более благоприятный эффект на костный метаболизм будет выявлен у другого нового комбинированного препарата — Фостер, состоящего из 100 мкг экстрамелкодисперсного беклометазона (клинически эквивалентного 250 мкг его неэкстрамелкодисперсной форме) и 6 мкг формотерола. Экстрамелкие частицы действующих веществ беклометазона и формотерола (1,4 и 1,5 µm соответственно) обеспечивают не только равномерное распределение, но и высокую легочную депозицию препарата (до 31% у Фостера, по сравнению с 10–20% у обычных ДАИ и 20–25% — у порошковых ингаляторов) [10]. Опубликованы исследования, указывающие на более выраженную клиническую эффективность Фостера у взрослых больных БА по сравнению с двумя другими комбинированными препаратами (Серетид, Симбикорт, Турбухалер) [20, 21].
Еще одной благоприятной возможностью для снижения доз ГКС (системных/ингаляционных) следует рассматривать анти-IgE-терапию. В GINA препарат омализумаб рекомендовано назначать пациентам с неконтролируемой IgE-опосредованной БА тяжелой формы. Однако, как показывает анализ научных публикаций, препарат с успехом может быть использован в лечении даже детей в возрасте старше 6 лет, имеющих обострение БА (ухудшение симптомов заболевания, которое требует увеличение дозы ингаляционных и/или системных ГКС) [22]. Перспективным направлением в превенции ГКС-индуцированного ОП может быть также использование теофиллина. Как известно, в GINA препараты этого ряда рассматриваются как альтернатива ГКС. In vitro исследования показали, что ингибиторы фосфодиэстеразы-4 подавляют образование подобных остеокластам клеток, повышают экспрессию мРНК RANKL и остеобластогенез. Установлено также, что ежедневный прием Ролипрама, ингибитора PDE4, предотвращает дальнейшую потерю костной массы у взрослых крыс и по данным денситометрии повышает плотность костей, подобно алендронату, т. е. обладает антирезорбтивным действием [23].
Недавно были получены экспериментальные данные о влиянии блокаторов аденозиновых рецепторов I типа на резорбцию кости и активность остеокластов, что позволяют рассматривать препараты этой группы в будущем полезными при лечении ОП.
Каковы современные подходы к терапии ГКС-индуцированного ОП?
В лечении этого вторичного ОП используют все те группы лекарственных средств, которых обычно назначают при ОП:
-
препараты, тормозящие резорбцию кости (эстрогены — Фемостон, Эстрофем и др); кальцитонины (Миакальцик); бисфосфонаты и др.);
-
препараты, стимулирующие костеобразование (анаболические гормоны, паратиреоидный гормон, стеогенон);
-
другие препараты (витамин D и его активные производные, комплексные соединения с кальцием и т. п.).
На сегодняшний день бисфосфонаты (алендроновая кислота, ризедронат, ибандронат, этидронат и др.) являются стандартом для профилактики переломов у больных с ГКС-индуцированным ОП (уровень А по критериям доказательной медицины). Этидронат был первым бисфосфонатом, эффективность которого была доказана в рандомизированных исследованиях у пациентов с ГКС-индуцированным ОП (как для первичной, так и вторичной профилактики) [3]. Считается, что именно прием бисфосфонатов позволяет сохранить костную массу на существующем уровне (или увеличить ее примерно до 10%), независимо от возраста и пола пациента. Бисфосфонаты влияют на прочность кости, уменьшая риск переломов, вследствие усиления апоптоза остеокластов и уменьшения, подобно кальцитонину, апоптоза остеоцитов. Однако бисфосфонаты контролируют течение ОП, но не излечивают его.
С целью профилактики развития ОП бисфосфонаты следует принимать регулярно, также как и в случае уже развившегося ГКС-индуцированного ОП. Плацебо-контролируемые исследования показали, что длительный прием оральных бисфосфонатов (до 10 лет и больше) способствует поддержанию костной массы до нормы и достоверно снижает риск переломов у больных ОП [24].
Побочные эффекты бисфосфонатов: диспепсия, стриктура пищевода, мышечная боль, гриппоподобный синдром, головокружение, гепатотоксичность, слуховые галлюцинации, крапивница, ангиоотек. Бисфосфонаты не вызывают остеонекроз челюсти, атипичные переломы или остеосаркому. До настоящего времени в литературе широко дискутируется вопрос о связи приема бисфосфонатов и риском развития фибрилляции предсердий. Причину тому ученые видят не в развившейся гипокальциемии, а в высвобождении провоспалительных цитокинов (таких как фактор некроза опухоли альфа, интерлейкин-1, 6), которые приводят к ремоделированию в предсердии, фиброзу ткани и т. п.
Недавно Isik А. впервые сообщил о клиническом случае, в котором у женщины 45 лет, страдающей контролируемой БА, алендроновая кислота была названа вероятной причиной развития приступа астмы вскоре после его приема пациентом [25]. Повторный прием бисфосфоната уже после купирования первого обострения БА вновь вызвал у пациентки одышку и свистящее дыхание, потребовавшее ее госпитализации. Автор признает, что не следует игнорировать возможность того, что вспомогательные вещества, входящие в состав коммерческой формы препарата (Fosamax), могли быть причиной астматической реакции. Хотя в литературе есть данные о том, что алендроновая кислота влияет на активность гистидин-декарбоксилазы в различных тканях (печень, легкие, селезенка), что приводит к увеличению уровня гистамина. Другое объяснение возникшего приступа БА — стимуляция блуждающего нерва пищевода, которая может привести к бронхоспазму.
После приема стронция ранелата описан так называемый DRESS-синдром (drug rash with eosinophilia and systemic symptoms): сыпь, отек лица, энантема, эозинофилия, нарушение функции печени, вовлечение легких, неврологические симптомы, повышение температуры. Безусловно, во всех таких случаях необходимо отменить препарат.
Побочные действия бисфосфонатов (чаще со стороны ЖКТ) и низкий комплаенс приводят к тому, что больные начинают прекращать их прием вскоре после начала терапии. В связи с этим ученые изучают эффективность интермиттирующих режимов терапии бисфосфонатами. Недавно было показано, например, что по терапевтической эффективности (влиянию на МПКТ и изменения биохимических маркеров) прием алендроната и ризедроната 1–2 раза в неделю не уступает их приему ежедневно. А такой мощный нитроген-содержащий бисфосфонат, как ибандронат (Boniva®, в России не зарегистрирован), назначают в/в каждые 2 или 3 месяца, что так же эффективно, как ежедневный прием препарата (исследование Monthly Oral iBandronate In LadiEs: MOBILE). Фосамакс (алендроновая кислота) и Актонель (ризедроновая кислота) предназначены для применения один раз в неделю. При передозировке бисфосфонатов больным дают выпить полный стакан молока.
Всем больным с ОП, а также в тех случаях, когда они уже получают бисфосфонаты, рекомендуют принимать сбалансированную пищу, обогащенную Са2+ и витамином D; важную роль играет также достаточная физическая активность пациента. Однако в исследовании Campbell и соавт. научного подтверждения о благоприятном эффекте сочетанного применения у больных БА бисфосфоната этидроната и кальция получено не было [26].
Другие антирезорбтивные препараты — эстрогены (Фемостон, Эстрофем и др.), а также кальцитонины (Миакальцик) не получили столь широкого применения для профилактики и лечения ГКС-индуцированного ОП. Так, исследования по влиянию на МПКТ ралоксифена — нестероидного селективного модулятора эстрогеновых рецепторов, который назначают для профилактики и лечения постменопаузального ОП, показали, что эстрогены обладают более эффективным антирезорбтивным действием, чем ралоксифен. Ралоксифен рекомендуют использовать в качестве дополнительного средства при лечении тяжелого ОП у женщин в постменопаузе (противопоказан при венозной тромбоэмболии в анамнезе).
В рандомизированном перекрестном исследовании по эффективности терапии тестостероном (его назначали ежемесячно в/м мужчинам с низким уровнем тестостерона в сыворотке (< 300 нг/мл), у 15 мужчин с БА, принимавших ГКС, к концу 12 месяца терапии было достигнуто увеличение плотности костной ткани поясничного отдела позвоночника на 4% [27].
Кальцитонин вводят подкожно или интраназально. Показано повышение МПКТ в поясничном отделе позвоночника, но не в шейке бедренной кости у больных, принимавших кальцитонин на фоне длительной терапии ГКС [28]. Кальцитонины рассматривают в качестве препаратов второй линии для лечения пациентов с низкой плотностью костной ткани, которые получают ГКС длительно и имеют противопоказания или побочные действия на прием бисфосфонатов.
Другим подходом лечения ОП рассматривают длительный прием активного витамина D3, хотя его эффект ниже, чем бисфосфонатов (уровень В). В недавно опубликованном метаанализе сказано о том, что препараты на основе активного и природного витамина D помогают поддерживать МПКТ по данным денситометрии поясничного отдела позвоночника у больных, принимающих низкие дозы ГКС. В другом двухлетнем рандомизированном клиническом исследовании изучали эффект активной формы витамина D — кальцитриола в дозе 0,5 мкг/сут на МПКТ у 41 мужчины (средний возраст 53,2 ± 1,7 года) и 67 женщин (средний возраст 49,1 ± 1 год), страдающих средней и тяжелой БА, которым для контроля над течением заболевания требовались > 800 мкг/сут беклометазона и периодически — пероральные ГКС [28]. По заключению авторов, потеря костной массы отмечалась у всех больных, независимо от того, принимали они кальцитриол или нет. Epstein S. подтвердил эффективность включения в схему терапии ОП комбинации алендроновой кислоты в дозе 70 мг и холекальциферола (витамин D3 в дозе 2800 IU (1 таблетка 1 раз в неделю)) [29]. Однако рандомизированные контролируемые исследования указывают, что оральные бисфосфонаты более эффективны в поддержании МПКТ, чем препараты на основе витамина D.
В последнее время в научной литературе активно обсуждается роль витамина D в регуляции иммунных функций (в дополнение к хорошо известным его таким свойствам, как участие в гомеостазе кальция и костном метаболизме): в создании иммунитета против вирусов, микобактерий, индукции экспрессии антимикробных генов кателицидина, бета2-дефензина и т. п. Недавно было установлено, что уже через неделю после приема стандартной дозы кальцитриола у больных БА, принимающих ГКС, восстанавливался ex vivo ответ CD4+ T-клеток и продукция ими интерлейкина-10 [30].
Учитывая тот факт, что дефицит витамина D отмечается у большинства проживающих в северных странах пожилых людей, особенно в зимнее время, и испытывающих ограничения в физической активности, им следует ежедневно назначать его в дозе 700–800 МЕ в день.
Также для профилактики и лечения ГКС-индуцированного ОП ученые рассматривают целесообразность применения рекомбинантного человеческого паратиреоидного гормона rhPTH — терипаратида — первого анаболического гормона для лечения ОП. Эффект препарата опосредован связыванием с G-протеин-зависимым рецептором-1 паратиреоидного гормона на клеточной мембране. Связывание лиганда с рецептором приводит к активации цАМФ и ряда фосфолипаз (A, C и D) и повышению внутриклеточного уровня цАМФ и Са.
Терипаратид увеличивает количество остеобластов и формирование кости посредством активации клеток-предшественников остеобластов и снижения их апоптоза. Учитывая разнонаправленность патофизиологических механизмов действия бисфосфонатов (ингибируют резорбцию) и терипаратида (ускоряет формирование костной ткани), такая комбинация может быть полезной в лечении и профилактике ОП. В сравнительном исследовании этих двух препаратов было установлено, что терипаратид оказывает более выраженное действие на плотность костной ткани, чем бисфосфонат алендроновая кислота [31]. Есть публикации также по результатам комбинированного применения терипаратида с эстрогенами у женщин с постменопаузальным ОП, больных вторичным ОП. Из-за анаболического действия терипаратид используют как альтернативу традиционной терапии ОП. Его наиболее выраженное побочное действие — гиперкальциурия.
Использование других анаболиков с целью увеличения костной массы — фторида натрия, простагландина Е2 (PGE2) и основного фактора роста фибробластов (bFGF) — при ОП ограничено из-за их побочных эффектов.
Наконец, несколько слов о том, что мы имеем на практике. Во-первых, как показывают опросы врачей общей практики, не только в России, но и США, Дании, Англии и др. странах большинство больных БА и ХОБЛ, принимающих ГКС, не получают препараты для профилактики и лечения ОП (бисфосфанаты + Са + витамин D). Лишь в последние годы (после 2003–2005 гг.) в зарубежных странах отмечается некоторый рост численности больных, которым была проведена денситометрия (в 3 раза, по сравнению с 1995–1998 гг.) и назначено лечение при ГКС-индуцированном ОП (количество таковых увеличилось вдвое). В свою очередь, более половины пациентов с ОП, которым назначили антирезорбтивный препарат ежедневно или один раз в неделю, прекращают его прием в течение первых 12 месяцев от начала терапии.
В России следует учитывать также социальный фактор — стоимость препаратов для профилактики и лечения ОП, требующих длительного применения, — в сочетании с терапией основного заболевания такое лечение довольно дорогостоящее. Кроме того, скрининг пациентов с ОП остается низким, врачами реально не учитываются факторы риска переломов, пациентам своевременно не проводится денситометрия в профилактических и даже в лечебных целях так, как этого требуют международные согласительные документы по ОП и их состояние, включая больных детей. Так, в статье Верткина А. Л. и соавт. (2006) сказано о том, что лишь 5% врачей из 19 городов России были осведомлены о распространенности ОП, о факторах риска ОП знают лишь 35% опрошенных; из 25 стационаров лишь один был оснащен денситометром DEXA, а из 30 поликлиник — только в трех использовали денситометрию, основанную на ультразвуковом сканировании; низкий уровень знаний о самом заболевании, его осложнениях и необходимости проведения профилактики продемонстрировали и сами опрошенные пациенты [32]. Неоценимую помощь врачам в диагностике и лечении больных ОП может оказать блестящее руководство «Клинические рекомендации. Остеопороз: диагностика, профилактика и лечение» под редакцией проф. Л. И. Беневоленской и проф. О. М. Лесняк, выпущенное в 2005 г.
Заключение
Альтернатива для уменьшения негативных последствий терапии ИГКС у детей:
-
используйте низкие дозы ИГКС, контролирующие БА;
-
используйте спейсеры для уменьшения локальных побочных действий ИГКС;
-
следует полоскать полость рта после ингалирования ИГКС;
-
проводить мониторирование роста у ребенка;
-
контроль за сопутствующими заболеваниями (аллергический ринит, синусит, ожирение, гастроэзофагеальнорефлюксная болезнь);
-
употребление достаточного количества Са2+ с пищей;
-
физические упражнения.
При необходимости повышения дозы ИГКС:
-
определить приверженность пациента к проводимому лечению;
-
оценить технику ингалирования препаратов;
-
оценить факторы окружающей среды (аллергены, триггеры), которые могут поддерживать тяжесть БА;
-
рассмотреть возможность добавления пролонгированных бета-агонистов или антагонистов лейкотриеновых рецепторов вместо повышения дозы ИГКС.
Литература
-
Pedersen S. Clinical Safety of IC for Asthma in Children // Drug Safety. 2006, 29: 7, 599.
-
Остеопороз. Современные представления. Под ред. Калдримидис Ф. Novartis Pharma, 2004, с. 112.
-
Richy F., Bousquet J., Ehrlich G. E., Meunier P. et al. Inhaled corticosteroids effects on bone in asthmatic and COPD patients: a quantitative systematic review // Osteoporos Int. 2003. May; 14 (3): 179–190.
-
Woolf F. An update on glucocorticoid-induced osteoporosis // Curr Opin Rheumatol. 2007; 19: 370–375.
-
Binkovitz L. A., Henwood M. J. Pediatric DXA technique and interpretation // Pediatr Radiol. 2007, 37: 21–31.
-
Luengo M., del Rio L., Pons et al. Bone mineral density in asthmatic patients treated with inhaled corticosteroids: a case-control study // Eur Respir J. 1997; 10: 2110–2113.
-
Baranova I. A., Gadzhiev K. Z., Toroptsova N. и др. [Bone mineral density and risk factors for developing Os in bronchial asthma patients // Ter Arkh. 2003; 75: 27–32.
-
Luengo M., Picado C., Del Rio L. Vertebral fractures in steroid dependent asthma and involutional Osteoporosis: a comparative study // Thorax. 1991; 46: 803–806.
-
De Vries F., van Staa T. P. et al. Severity of obstructive airway disease and risk of osteoporotic fracture // Eur Respir J. 2005; 25: 879–884.
-
Vestergaard P., Rejnmark L., Mosekilde L. Fracture risk in patients with chronic lung diseases treated with bronchodilator drugs and inhaled and oral corticosteroids // Chest. 2007; 132: 1599–1607.
-
Van Staa T., Leufkens H., Abenhaim L. et al. Use of oral corticosteroids and risk of fractures // J Bone Miner Res. 2000; 15: 993-10-00.
-
Boot A., de Jongste J., Verberne A. et al. Bone mineral density and bone metabolism of prepubertal children with asthma after long-term treatment with inhaled corticosteroids // Pediatr Pulmonol. 1997; 24: 379–384.
-
Agertoft L., Pedersen S. Bone mineral density in children with asthma receiving long-term treatment with inhaled budesonide // Am J Respir Crit Care Med. 1998; 157: 178–183.
-
Rossi G., Cerasoli F., Cazzola M. Safety of IC: room for improvement // Pulm Pharmacol Ther. 2007; 20: 23–35.
-
Van Schayck cp., Donnell D. The efficacy and safety of QVAR (hydrofluoroalkane-beclometasone diproprionate extrafine aerosol) in asthma (Part 2): Clinical experience in children // Int J Clin Pract. 2004; 58: 786–794.
-
Pedersen S., Warner J., Wahn U. Growth, Systemic Safety, and Efficacy During 1 Year of Asthma Treatment With Different Beclomethasone Dipropionate Formulations: An Open-Label, Randomized Comparison of Extrafine and Conventional Aerosols in Children // Pediatrics. 2002; 109: e92.
-
Pasaoglu G., Gok H., Mungan D. et al. Does the combination of inhaled steroids with long acting beta2 agonists decrease the risk for osteoporosis? A 1-year prospective follow-up study // Rheumatol Int. 2006; 27: 141–146.
-
Derom E.,Pauwels R.Pharmacokinetic and pharmacodynamic properties of inhaled beclometasone dipropionate delivered via hydrofluoroalkane-containing devices //Clin Pharmacokinet. 2005; 44: 815–836.
-
Papi A., Paggiaro P., Nicolini G. et al. Beclometha-sone/formoterol vs fluticasone / salmeterol inhaled combinationin moderate to se-vere asthma // Allergy. 2007; 62: 1182–1188.
-
Papi A., Paggiaro P. L., Nicolini G. et al. Bеclomethasone/formoterol versus budesonide /formoterol combination therapy in asthma // Eur Respir J. 2007; 29: 682–689.
-
Lanier B., Bridges T., Kulus M. Omalizumab for the treatment of exacerbations in children with inadequately controlled allergic (IgE-mediated) asthma // J Allergy Clin Immunol. 2009; 124: 1210–1216.
-
Tian X, Chen J. Rolipram, a phosphodiesterase 4 inhibitor, prevented cancellous and cortical bone loss by inhibiting endosteal bone resorption and maintaining the elevated periosteal bone formation in adult ovariectomized rats // J Asthma. 2008; 45: 519–522.
-
Liberman U. Long-term safety of bisphosphonate therapy for osteoporosis: a review of the evidence // Drugs Aging. 2006; 23: 289–298.
-
Isik A., Uras I., Uyar M. et al. Alendronate-induced asthma // Ann Pharmacother. 2009; 43: 547–548.
-
Campbell I., Douglas J., Francis R. et al. Five year study of etidronate and/or calcium as prevention and treatment for osteoporosis and fractures in patients with asthma receiving long term oral and/or inhaled glucocorticoids // Thorax. 2004; 59: 761–768.
-
Reid I., Wattie D., Evans M., Stapleton J. Testosterone therapy in glucocorticoid-treated men // Arch Intern Med. 1996; 156: 1173–1177.
-
McDonald C., Zebaze R., Seeman E. Calcitriol does not prevent bone loss in patients with asthma receiving corticosteroid therapy: a double-blind placebo-controlled trial//Osteoporos Int. 2006;17:1546–1551.
-
Epstein S. The problem of low levels of vitamin D and osteoporosis: use of combination therapy with alendronic acid and colecalciferol (vitamin D3) // Drugs Aging. 2006; 23: 617–625.
-
Xystrakis E. Reversing the defective induction of IL-10-secreting regulatory T cells in glucocorticoid-resistant asthma patients // J. Clin. Invest. 2006; 116: 146–155.
-
Curtis J. R, Saag K. Prevention and treatment of glucocorticoid-induced osteoporosis // Curr Osteoporos Rep. 2007, Mar; 5 (1): 14–21.
-
Верткин А. Л., Наумов А. В., Максименкова Е. В. и др. Распространенность факторов риска и клинических маркеров остеопороза в клинике внутренних болезней//Лечащий Врач. 2006, № 2, с. 69–72.
Д. Ш. Мачарадзе, доктор медицинских наук, профессор
РУДН, Москва
Контактная информация об авторе для переписки: dalim@mail.ru
Давайте разберемся с целями лечения и современнымарсеналом противоастматических препаратов. Итак, начнем с реальных целей терапии бронхиальной астмы. Кратко они сводятся к формуле: достижение контроля над астмой. И это справедливо для пациента любого возраста, с любой исходнойтяжестью состояния.
Контролируемая астма должна вести себя так, чтобы не напоминать о себеникакими симптомами как можно дольше. И опыт последних лет говорит о том, что этой высокой цели можно достичь у большинства пациентов. Только для этого необходимо всей семье поработать совместно (с лечащим врачом). А вот пассивное ожидание чудес (например, полного и окончательного исцеления или того, что ребенок «перерастет» свою болезнь) – не рекомендуется.
Итак, для сотрудничества нам понадобится общий язык и инструментысамоконтроля: дневник симптомов и пикфлоуметрии, регулярное заполнениеопросников АСТ и/или ACQ. Незнакомые слова? Обратитесь к статьям этого жераздела на нашем сайте или к своему лечащему врачу. А в рамках этоймаленькой статьи расскажу о двух группах противоастматичекихпрепаратов. Это – СРЕДСТВА БАЗИСНОЙ ТЕРАПИИ (1) и ПРЕПАРАТЫ СКОРОЙПОМОЩИ (2)*.
1. СРЕДСТВА БАЗИСНОЙ ТЕРАПИИ *
Врач назначает обычно сразу на длительный срок (месяцы!) с противовоспалительной целью, для ежедневного применения вне зависимостиот наличия/отсутствия проявлений астмы в данный момент, для профилактики, а не снятия бронхиальной обструкции. На эти лекарства и возлагаются главныенадежды по достижению контроля над астмой. Причем длительность ихприменения не ограничена, нет понятия «пройти курс лечения»: лекарственнаяподдержка может использоваться так долго, как будет в ней необходимость. Итак, к БАЗИСНЫМ относятся:
- Ингаляционные глюкокортикостероиды=ИГКС («гормоны» на языкеначинающих): Беклометазон (Беклазон, Бекотид, Кленил-джет), Будесонид(Пульмикорт, Буденит-Стеринеб, Тафен-новолайзер), Флутиказон (Фликсотид) и пришедшие в Россию в 2013 г.-Мометазон (Астманекс) и Циклесонид (Альвеско). Сегодня ИГКС — изученная и «заслуженная» группа препаратов. Их приход в практику около 40 лет назад стал подлинной революцией в подходах к лечениюастмы, ведь он сделал возможным избежать системного (внутрь или внутривенно) назначения стероидов, а лечить непосредственно воспаленныебронхи! Не будет преувеличением сказать, что ИГКС являются краеугольнымкамнем базисной, противовоспалительной терапии астмы у пациентов любоговозраста и степени тяжести от легкой до тяжелой. Эта группа – препаратыпервого выбора для лечения астмы во всем мире.
- Антилейкотриеновые препараты = АЛТР: Монтелукаст (Сингуляр, Монтелар) и Зафирлукаст (Аколат). В настоящее время очень активно изучаютсяих особенности, эффекты, накапливается опыт применения при различныхвариантах астмы (в том числе астма физического усилия у профессиональныхспортсменов – препараты разрешены антидопинговыми правилами WADA), снижен возрастной порог применения (Монтелукаст – в России с 2х лет). Самойлюбопытной чертой всей группы является таблеттированная форма, а неингалятор. Поэтому никаких технических сложностей с приемом лекарства невозникает ни у старых, ни у малых. Интересным эффектом этой группыпрепаратов является возможность и самостоятельного применения и комбинаций с ИГКС-терапией, особенно актуальная в периоды «всплеска» респираторных вирусных инфекций.
- Кромоны: Кромогликат натрия (Интал, Кромгексал), Недокромил натрия(Тайлед). Интерес к ним сохраняет отечественная педиатрическая школа — при легком течении астмы у детей раннего возраста, на этапе снижения терапии и для профилактики бронхоспазма при физических нагрузках, при так называемомкашлевом варианте астмы.
- Комбинации ИГКС с длительно действующими бронхорасширяющимисредствами (ИГКС+ДДБА): Серетид, Симбикорт, Тевакомб, Форадил-комби, Фостер. Фиксированные комбинации «2 в одном» для базисной терапии – сегодня основной инструмент достижения контроля над средне-тяжелой и тяжелой астмой, при наличии ночных симптомов, выраженнойгиперреактивности бронхов, невозможности полного исключения действияпровоцирующих факторов. Эти лекарства предназначены для планового приемаежедневно ровно два раза в день (утром и вечером), так как действуют как раз в течение 10-12 часов после ингаляции. Часто один препарат выпускается в разных дозировках и/или формах, что очень удобно при переходе на следующийуровень терапии (и поверьте, врач всегда мечтает о «ступени вниз», то естьснижении объемов лекарственной терапии).
2. ПРЕПАРАТЫ СКОРОЙ ПОМОЩИ *
Бронхорасширяющие, бронхолитики, бронхоспазмолитики, бронходилататоры. Они используются, напротив, для быстрого облегчения симптомов астмы в обострении/в приступе, то есть по мере надобности, а не в плановом порядке. В этой группе лекарств не так уж много: Сальбутамол (Вентолин, Саламол), Фенотерол (Беротек), Комбинированные препараты Беродуал и Ипрамол-Стеринеб, а также таблетки и уколы Эуфиллина. Эти лекарства через несколькоминут после приема расслабляют спазмированные гладкие мышцы бронхов, засчет чего и восстанавливается проходимость дыхательных путей, воздух вновьсвободно поступает в бронхи при вдохе и выдыхается при выдохе. Но на другиемеханизмы бронхиальной обструкции – отек слизистой оболочки, выделениеслизи, утолщение стенки бронхов вследствие воспаления и перестройки наклеточном уровне – бронхолитики влиять не умеют. Да и профилактическимдействием они не обладают, за исключением способности предотвращатьбронхоспазм, вызванный физической нагрузкой (астма физического усилия). Эффект – расширение бронхов под действием бронхолитиков — сохраняетсяоколо 3-6 часов. Таким образом, чем чаще больному приходится пользоватьсяпрепаратом скорой помощи, тем хуже контролируется его астма.
Правда, есть еще группа бронхолитиков для плановой терапии – они начинаютдействовать не так быстро, но зато работают не 3-6ч, а все 8-12, и поэтомуобычно врач назначает их 2 раза в день для приема в течение некотороговремени (от 5 дней до нескольких недель) и всегда в сочетании с ИГКС — это: Сальметерол (Серевент), Формотерол (Форадил, Оксис, Атимос), Кленбутерол, Ипратропиум (Атровент, Ипратропиум-Стеринеб), пролонгированныетеофиллины (таблетки Теопэк, Теотард и др.).
Как видите, универсального или идеального лекарства пока не обнаружено. Исследуются и внедряются в жизнь и новые группы средств. У каждогопрепарата, пусть даже отнесенного в одну группу, есть свои нюансыприменения, часто – свое устройство для ингаляции (дозированные аэрозольныеили порошковые ингаляторы, небулайзер), особенности действия, преимуществаи недостатки.
Рассказать обо всем сразу – просто нереально, да наверное и не нужно. Ведь мынаконец добрались до самого интересного. На чем же основан выборконкретного лекарства для конкретного пациента?
Клинические рекомендации по лечению астмы (международные – GINA, российские – Национальная программа) рекомендуют определенную ступеньтерапии в зависимости от того, достигнут ли контроль над астмой. Соответственно, на протяжении времени возможны и «шаги вниз» (то естьснижение доз, числа используемых препаратов) и «шаги вверх» по ступеням (тоесть наращивание терапии).
Необходимо учесть предыдущий индивидуальный опыт самого больного(переносимость, нежелательные явления, мнение об эффективности), правильность применения и удобство ингаляционного устройства, возможныевозрастные ограничения и ограничения по безопасности (у детей, у беременныхи кормящих мам), сопутствующие заболевания и их лечение медикаментами в данное время.
Так что выбор будет делать Ваш лечащий врач в процессе диалога с Вами. И чем активнее и честнее Ваша позиция – тем быстрее удастся найти по-настоящему Ваш препарат. Обязательно попросите доктора проверитьтехнику ингаляции (особенно при переходе на новый для Вас тип устройства или если этого никогда не делали раньше), захватите дневники опросник (проявите свою подкованность в самоконтроле!) и обсудитепоявившиеся вопросы .
Желаю всем астматикам полного контроля!
* При написании названий препаратов даю первым международноенепатентованное наименование, а в скобках – коммерческие наименования.
Юлия Артуровна Яснова, аллерголог-иммунолог Центра «Парацельс»
Среди болезней органов дыхания бронхиальная астма (БА) является одним из наиболее распространенных заболеваний, от нее почти 250 тыс. пациентов ежегодно умирают в результате тяжелого обострения[1]. Астмой страдают более 300 миллионов человек в мире, а в США ежегодно затраты на нее составляют 80 миллиардов долларов[2].
В Китае в период с 2013 по 2016 г. проанализированы 32 238 случаев БА и установлено, что риск развития БА растет вместе с глобальным изменением климата, распространением нехарактерной для регионов температуры, перепадами влажности и снижением чистоты вдыхаемого воздуха[3].
В 2014–2016 гг. в одном из крупных медицинских учреждений Москвы рассмотрены 849 случаев БА и выявлена тенденция к увеличению численности таких больных. За 3 года показатель распространенности заболевания вырос с 15,79 до 23,24, а атопической БА — с 9,22 до 15,12. Отмечена тенденция к омоложению больных атопической БА[4]. Эти данные делают анализ текущего лечения и обновления подходов к нему актуальным в настоящее время.
Целью нашего обзора стало изучение применения фиксированной комбинации будесонида-формотерола с доставкой через дозированный порошковый ингалятор (ДПИ) Турбухалер® в лечении БА и революционных изменений в режимах использования этой фиксированной комбинации, произошедших в 2019 г.
ПРОГРЕСС В ЛЕЧЕНИИ БРОНХИАЛЬНОЙ АСТМЫ ЗА ПОСЛЕДНИЕ 70 ЛЕТ
Лечение БА является объектом быстро продвигающихся исследований, создания новых препаратов, схем и режимов терапии. На глазах того поколения врачей, к коим относятся авторы данного обзора, произошли революционные изменения. Когда происходило наше становление как врачей, основой лечения БА были инъекции и ингаляции адреналина, эфедрина, атропина, внутривенные инфузии аминофиллина (Эуфиллина) и преднизолона[5, 6].
В терапии БА был период увлечения системными стероидами длительного действия, депо-препаратами, которые давали относительно стойкий противовоспалительный эффект с очень серьезными системными последствиями[7].
Появление первых ингаляционных бронхолитиков короткого действия — тогда еще недостаточно селективных — было для врачей и пациентов серьезным шагом, «снимающим» больных с иглы и капельницы и выручающих в неотложной ситуации.
Но уже тогда появились англоязычные работы, предупреждающие о риске учащения приступов и астматических статусов на фоне монотерапии этими бронхолитиками короткого действия, в частности при использовании фреонового ингалятора с изопреналином[8].
Внедрение в практику ингаляционных глюкокортикостероидов (ИГКС), повышение селективности бронхолитических препаратов в значительной степени завуалировали эту проблему, она ушла на второй план, и долгое время пациенты и врачи полагали, что использование ежемесячно по баллончику бронхолитика — это хорошая практика и гарантия для больного.
Эксперты Глобальной инициативы по изучению БА (Global Initiative for Asthma, GINA) до 2019 г. поддерживали рекомендацию о допустимости применения монотерапии бронхолитиком короткого действия на 1-й ступени терапии[9]. При отсутствии облигатного аллергена, вне сезона поллинации пара доз бронхолитика — β2-адреномиметика короткого действия (КДБА) — перед физической нагрузкой значительно облегчала жизнь больного БА, но в случае воздействия провоцирующего аллергена эти ингаляции снимали бронхоспазм, не оказывая влияния на прогрессирующее воспаление, являющееся основой патогенеза БА, что увеличивало вероятность последующего тяжелого обострения.
Появление бронхолитиков длительного действия в 1990 г. поначалу создало новую иллюзию о роли этих препаратов в лечении БА, однако одно из исследований салметерола (SNS trial, Великобритания)[10] повысило обеспокоенность, связанную с ростом смертности больных БА при применении салметерола в качестве монотерапии без ИГКС в сравнении с таковой при других режимах лечения.
После исследования SNS Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (Food and Drug Administration, FDA) попросило производителя провести постмаркетинговое исследование добавления салметерола к текущей терапии БА, которое было досрочно прекращено в 2003 г. в связи с неблагоприятными исходами и трудностями включения в исследование[11]. Эти данные поставили точку в монотерапии β2-адреномиметиками длительного действия при лечении БА. ИГКС стали облигатными спутниками длительно действующих β2-агонистов (ДДБА). Но в то же время в рекомендациях и руководствах сохранялась возможность лечении БА на 1-й ступени короткодействующими бронхолитиками.
После введения понятия контроля БА и оценки тяжести БА на основании объема проводимой терапии полностью изменилось понимание БА легкого течения, когда среди пациентов с легкой БА на 1–2-й ступени терапии по GINA каждый четвертый переносил в течение года тяжелые обострения[12]. Сопоставление частоты обострений БА с методом лечения показало, что применение трех и более ингаляторов КДБА в год увеличивает риск обострений БА[13], а применение 12 и более ингаляторов КДБА в год связано с повышенным риском смерти по причине БА[14].
Нельзя не отметить еще один этап в развитии фармакотерапии БА. С появлением комбинаций ИГКС/ДДБА стало правилом применять их регулярно каждые 12 часов (для некоторых 1 раз в сутки), а в течение суток по потребности использовать КДБА для купирования симптомов. По мере роста потребности в применении КДБА оценивали стабильность состояния пациента и, при необходимости, увеличивали дозу ИГКС, а в тяжелых случаях прибегали к системным стероидам. Пациент обращался к врачу, когда, несмотря на регулярное применение ИГКС/ДДБА, у него нарастала потребность в КДБА.
Накопленный опыт по безопасности использования ИГКС (например, высоких доз ИГКС при небулайзерной терапии БА) и по кардиобезопасности КДБА, а также практика наращивания дозы ИГКС при отсутствии контроля над БА логично привели к применению ИГКС/ДДБА на регулярной основе и по потребности. Такая тактика использования будесонида-формотерола, названная в клинических исследованиях SMART-терапией (Symbicort Maintenance and Reliever Therapy), дала сразу ряд преимуществ[15].
Во-первых, пациент получил возможность естественным образом регулировать (увеличивать или уменьшать) дополнительный объем своей противовоспалительной терапии в зависимости от текущей возрастающей или уменьшающейся потребности. Применяя ИГКС/ДДБА по потребности ради облегчения симптомов, приносимого формотеролом, он временно увеличивал дозу ИГКС, которая брала под контроль воспаление. По мере уменьшения воспаления в стенке бронхов на фоне дополнительных ингаляций будесонида-формотерола снижалась и потребность в дополнительных ингаляциях данной фиксированной комбинации. Это уменьшало вероятность перехода усиления бронхоспазма в тяжелый приступ и необходимость обращения за помощью к врачу[16]. Во-вторых, тактика «единого ингалятора» увеличила частоту правильного использования устройства доставки. Ранее регулярное лечение и терапия по требованию часто осуществлялись с помощью разных устройств, а переход на одно устройство снизил частоту ошибок.
Так, применение дозирующего аэрозольного ингалятора (ДАИ) требует координации с нажатием на устройство со спокойным глубоким вдохом, а дозированные порошковые ингаляторы (ДПИ) — энергичного начала вдоха, чтобы достичь необходимой энергии турбулентности, которая обеспечит движение сухих частиц из агломератов или с фрагментов лактозы. Пациент с БА — заболеванием, имеющим у некоторых больных и черты психосоматического, — не всегда правильно пользуется устройством в экстренной ситуации. Переход на одно устройство, одну технику ингаляции стал залогом повышения эффективности терапии.
В 2019 г. накопилось достаточно данных, чтобы пересмотреть 1-ю ступень лекарственной терапии БА, одновременно было введено новое понятие «предпочтительный препарат для купирования симптомов БА (preferred reliever)». В эту категорию эксперты Глобальной инициативы GINA на 1–5-й ступени терапии БА включили комбинацию ИГКС и формотерола с уточнением, что доказательства для 1–2-й ступени терапии получены только для фиксированной комбинации будесонида-формотерола. Монотерапия КДБА в этом документе и в рекомендациях Российского респираторного общества более не является предпочтительной для купирования симптомов БА[17, 18].
Следует отметить, что КДБА не исключены полностью — они перемещены в другую категорию средств для купирования симптомов БА, причем КДБА могут применяться только совместно с базисной терапией, содержащей ИГКС, но не в виде монотерапии.
При тяжелом приступе, при невозможности использовать портативные устройства средство доставки КДБА и ИГКС — небулайзер. Но это не относится к регулярной терапии пациента, это экстраординарная ситуация.
Начиная с 2019 г. применение низкой дозы ИГКС в фиксированной комбинации с формотеролом стало универсальным средством на всех ступенях лечения БА, при любой степени тяжести заболевания, у пациентов с 12 лет, хотя тактика применения данной комбинации может быть различной[17–19]. Теперь пациент может использовать фиксированную комбинацию будесонида-формотерола Турбухалер®: 1) в режиме по потребности при легкой БА в качестве предпочтительного препарата для купирования симптомов (160/4,5 мкг/доза); 2) в режиме по потребности (для купирования симптомов) с поддерживающей терапией (в виде единого ингалятора) на 3-й ступени и выше (80/4,5 и 160/4,5 мкг/доза; 3) в режиме регулярной терапии (если нет дополнительной потребности) на 3-й ступени и выше (см. инструкции к препарату Симбикорт® Турбухалер® 80/4,5 мкг, 160/4,5 мкг, 320/9 мкг).
МЕСТО ФИКСИРОВАННОЙ КОМБИНАЦИИ БУДЕСОНИДА-ФОРМОТЕРОЛА В ЛЕЧЕНИИ БРОНХИАЛЬНОЙ АСТМЫ
Интересен тот факт, что формотерол и будесонид были запатентованы в один год в 1972 г. — формотерол в Японии, а будесонид в Швеции. В виде комбинации два препарата разрешены к клиническому применению в 2000 г. в Швеции, в 2001 г. — в России, в 2006 г. — в США[20]. Первой фиксированной комбинацией будесонида-формотерола стал препарат Симбикорт® в многодозовом ДПИ Турбухалер®. Интересно и третье хронологическое совпадение — Турбухалер® был создан в том же 1972 г. сотрудником компании «Астра».
Существует история о том, что Кьелл Веттерлин, любящий отец, придумал это устройство для своей дочери, которая страдала БА.
В 2010 г. Симбикорт® Турбухалер® получил одну из самых престижных мировых наград — премию за лучший дизайн Good Design Award[21].
Опыт применения указанной комбинации в мире включает сотни тысяч наблюдений, о чем свидетельствует одна из последних публикаций из Северной Каролины, где на основании 15-летнего наблюдения более 100 000 случаев БА установлено, что применение комбинации ИГКС/ДДБА снижает частоту обострений в 1,76 раза[2].
Одним из ключевых исследований, положенных в основу изменений 1-й ступени терапии GINA в 2019 г., стало 52-недельное исследование SYGMA1 (NCT02149199), в котором приняли участие 3836 больных БА легкого течения. Пациенты были рандомизированы на три группы: 1277 больных 2 раза в день получали плацебо + тербуталин (0,5 мг) по потребности (группа тербуталина), 1277 больных — 2 раза в день плацебо + по потребности будесонид-формотерол (200 мкг будесонида и 6 мкг формотерола — дозы отмеренные, что соответствует 160/4,5 мкг доставленной) (группа будесонида-формотерола), 1282 пациента — 2 раза в день будесонид (200 мкг) + тербуталин по потребности (группа будесонида).
По среднему проценту недель, в течение которых больные хорошо контролировали БА, будесонид-формотерол превосходил тербуталин (34,4% против 31,1% недели; ОШ = 1,14; 95%-ный ДИ: 1,00–1,30; p = 0,046), но уступал поддерживающей терапии будесонидом (34,4% и 44,4% соответственно; ОШ = 0,64; 95%-ный ДИ: 0,57–0,73). Однако среднесуточная доза ИГКС в группе будесонида-формотерола (57 мкг) составляла 16,8% от дозы в группе будесонида (340 мкг).
Ежегодная частота тяжелых обострений в группе тербуталина составила 0,20, будесонида-формотерола — 0,07, поддерживающей терапии будесонидом — 0,09.
ОШ развития обострения при сравнении будесонида-формотерола с тербуталином составило 0,36 (95%-ный ДИ: 0,27–0,49), а при сравнении с поддерживающей терапией будесонидом — 0,83 (95%-ный ДИ: 0,59–1,16). Показатель приверженности лечению в группе будесонида — 78,9%.
Исследование наглядно показало, что у пациентов с легкой БА применение будесонида-формотерола по потребности обеспечивало лучший контроль над симптомами, чем использование тербуталина по потребности, но уступало поддерживающей терапии будесонидом. Однако это преимущество обеспечивалось более чем 4-кратным повышением дозы ИГКС. Иначе говоря, будесонид-формотерол, используемый по потребности, приводил к значительно более низкой стероидной нагрузке, чем поддерживающая терапия будесонидом[22].
В другом 52-недельном рандомизированном открытом контролируемом исследовании в параллельных группах с участием 668 взрослых больных легкой формой БА пациенты были рандомизированы на три группы: Альбутерола (сальбутамола) (100 мкг в дозе ДАИ по потребности); будесонида (200 мкг, одна ингаляция через ДПИ Турбухалер® 2 раза в день + сальбутамол по потребности); будесонида-формотерола (200 мкг будесонида и 6 мкг формотерола (отмеренные дозы), через ДПИ Турбухалер® по потребности). Точные данные о приверженности к лечению получены с помощью электронного мониторинга использования ингаляторов.
Частота обострений в течение года была ниже у получавших будесонид-формотерол, чем в группе сальбутамола (0,195 против 0,400), тогда как у получавших будесонид на регулярной основе она существенно не отличалась (0,175). Однако средняя суточная доза ИГКС была значимо ниже при использовании фиксированной комбинации по потребности в сравнении с таковой при регулярных ингаляциях будесонида (107 мкг против 222 мкг).
Частота тяжелых обострений была значимо ниже в группе будесонида-формотерола, чем в группе сальбутамола (9 против 23) и в группе поддерживающей терапии будесонидом (9 против 21). Это открытое исследование подтвердило, что применение по потребности будесонида-формотерола превосходит использование сальбутамола в отношении предотвращения обострений БА легкого течения[23].
Группа испанских ученых недавно сделала обобщение четырех рандомизированных контролируемых исследований, обосновывающих замену КДБА на будесонид-формотерол. Два из них — рандомизированные плацебо-контролируемые исследования, которые вошли в клиническую программу SYGMA, и два исследования реальной клинической практики — Novel START и PRACTICAL. Исследования SYGMA 1 и 2 показали, что фиксированная комбинация формотерола-будесонида Турбухалер® в режиме по потребности обеспечивала лучший контроль над астмой, чем применение β2-агониста короткого действия (тербуталина) у пациентов на 2-й ступени лечения по GINA.
Исследование SYGMA-2, в котором приняли участие 4176 пациентов (2089 в группе будесонида-формотерола и 2087 в группе поддерживающей терапии будесонидом), показало, что у пациентов с БА легкого течения комбинация формотерола-будесонида, применявшаяся по потребности, не уступала использованию будесонида дважды в день по влиянию на частоту тяжелых обострений в течение 52 недель лечения, но при этом стероидная нагрузка составила 25% от таковой у регулярно применявших будесонид.
Исследование Novel START подтвердило, что фиксированная комбинация будесонида-формотерола Турбухалер® по потребности превосходила КДБА сальбутамол по эффективности предотвращения обострений БА.
В исследовании PRACTICAL получены доказательства того, что фиксированная комбинация будесонида-формотерола Турбухалер®, используемая по потребности, более эффективно снижала частоту серьезных обострений, чем регулярное применение низких доза будесонида и тербуталина по потребности[24].
Опыт лечения пациентов с БА меняет подходы, делает терапию более надежной и удобной. Еще недавно четко дистанцированные друг от друга препараты и подходы постепенно приближались, слились воедино, и возник новый англоязычный термин anti-inflammatory reliever — противовоспалительный бронхолитик по потребности, — основанный на исследованиях будесонида-формотерола[25]. Все данные по возможностям противовоспалительного бронхолитика в режиме по потребности с поддерживающей терапией или без нее были получены при использовании ингалятора Турбухалер®, для других устройств данных клинических исследований в этом режиме нет (есть только данные об эквивалентности с будесонидом-формотеролом Турбухалер® в режиме регулярной терапии)[26, 27].
Комбинация беклометазона-формотерола в ДАИ, подобно будесониду-формотеролу, имеет доказательную базу для применения по потребности в сочетании с поддерживающей терапией (режим MART), но не в качестве самостоятельного противовоспалительного бронхолитика. Комбинация формотерола с флутиказоном в виде ДАИ не имеет данных по применению ни в качестве противовоспалительного бронхолитика, ни в режиме MART, а только для поддерживающей терапии с фиксированными дозами.
На сегодняшний день доказательства эффективного использования ИГКС/ДДБА в качестве противовоспалительного бронхолитика по потребности с поддерживающей терапией или без нее на всех ступенях терапии БА получены только для ДПИ Симбикорт® Турбухалер® в дозе 160/4,5 мкг для пациентов с 12-летнего возраста.
Мы уже отмечали ранее, что препарат Симбикорт® был зарегистрирован в США заметно позже, чем в Европе и России. Так и с концепцией противовоспалительного бронхолитика — в США FDA пока не одобрило применение препарата по потребности с поддерживающей терапией или без нее. Тем не менее даже в режиме регулярной терапии Симбикорт® Рапихалер, зарегистрированный в США с 2007 г., продемонстрировал клиническое преимущество в терапии БА перед другой комбинацией ИГКС/ДДБА[28].
В масштабном ретроспективном исследовании реальной клинической практики показано, что Симбикорт® Рапихалер в режиме регулярной терапии снижал частоту обострений БА в 2 раза эффективнее по сравнению с фиксированной комбинацией салметерола и флутиказона пропионата ДАИ (–0,15 vs –0,07, 95%-ный ДИ: 0,85–0,99; p = 0,0255)[28].
Очевидно, что высокие дозы КДБА, применяемые на фоне базисной терапии, могут вызывать системные эффекты, такие как тахикардия и гипокалиемия. Новая концепция предусматривает только одновременное применение формотерола с будесонидом, который восстанавливает чувствительность β2-адренорецепторов и поддерживает бронхолитический эффект формотерола[25].
ЗАКЛЮЧЕНИЕ
Анализ данных литературы позволяет сделать вывод о том, что использование фиксированной комбинации будесонида-формотерола Турбухалер® 160/4,5 мкг/доза у пациентов с бронхиальной астмой (БА) любой степени тяжести с 12 лет в качестве противовоспалительного бронхолитика с поддерживающей терапией или без нее является современным подходом к лечению БА, который упрощает его, обеспечивает оптимальный долгосрочный эффект, снижает частоту обострений и при этом помогает уменьшить дозу ингаляционных глюкокортикостероидов, которую получает пациент.
Поэтому вполне логично, что данный подход включен как в последнее издание Global Initiative for Asthma 2020 г., так и в клинические рекомендации Российского респираторного общества 2019 г.
Поступила: 24.04.2020
Принята к публикации: 03.07.2020
Введение
В последние годы среди врачей отмечался повышенный интерес к порошковым ингаляторам (ПИ), т. к. этот класс ингаляторов не требует от больного координации в процессе выполнения вдоха и очень часто обеспечивает лучший уровень депозиции препарата в легких по сравнению с другими типами ингаляторов [1]. В данном обзоре рассмотрены различные типы ингаляторов, обсуждаются особенности их применения в клинической практике.
Применение ПИ не требует координации с вдохом, поскольку они являются пассивными устройствами: препарат покидает ингалятор и перемещается в дыхательные пути больного за счет потока воздуха на вдохе. Таким образом, ПИ являются хорошей альтернативой для примерно четверти больных астмой, у которых не получается точно синхронизировать активацию дозирующего аэрозольного ингалятора (ДАИ) с вдохом через ингалятор [2]. С другой стороны, большинство ПИ требуют от больного относительно высокой объемной скорости потока на вдохе, обычно не менее 60 л/мин (т. е. 1 л/с), а в некоторых случаях и выше (табл. 1) [3, 4].

Размер частиц в современных ПИ составляет 2–3 мкм (что в 20–30 раз меньше толщины волоса и примерно соответствует размерам пневмококка). Требуется надежно защитить препарат от влаги, и, кроме того, ингалятор должен очень точно отмерять дозу препарата, поэтому из мелких частиц лекарственного средства и крупных частиц инертного носителя формируются агломераты, которые проще отмерить и сохранить, однако при этом поток воздуха на вдохе должен обеспечить энергию для распада агрегатов за счет соударения друг с другом. Установлено, что поток воздуха на вдохе должен обеспечить перепад давления между ингалятором и атмосферным воздухом на уровне 4 кПа. Благодаря этому перепаду большинство частиц препарата покидает ингалятор. Кроме того, при быстром потоке воздуха движение частиц становится турбулентным, благодаря чему крупные порошковые агрегаты распадаются на отдельные частицы за счет соударения друг с другом (рис. 1) [5].
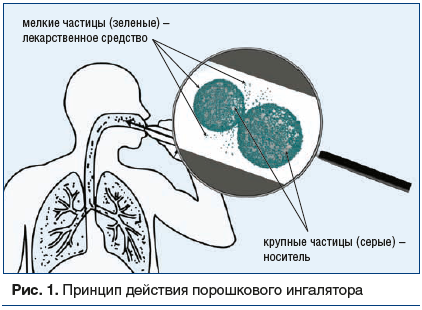
Если у пациента не получается обеспечить оптимальный поток воздуха на вдохе, ингалятор продуцирует относительно более крупные частицы. Важно отметить, что такие частицы (>5 мкм в диаметре) не способны поступать в дыхательные пути с потоком воздуха, они оседают в полости рта и потенциально способны вызывать нежелательные эффекты [6].
Достижение высокой скорости потока на вдохе может быть трудным для некоторых категорий больных. Например, у детей [7], пожилых пациентов [8], больных тяжелой хронической обструктивной болезнью легких (ХОБЛ) [9] скорость потока на вдохе нередко оказывается ниже 60 л/мин. Причем чем тяжелее заболевание и хуже функциональные показатели больного, тем меньше у него шансов обеспечить необходимое усилие в процессе ингаляции [8]. Например, среди больных, госпитализированных с обострением ХОБЛ, от 32% до 52% пациентов были не в состоянии на момент выписки вдохнуть через ПИ со скоростью ≥60 л/мин [10, 11]. Субоптимальная (менее 60 л/мин) пиковая скорость потока на вдохе чаще отмечается у больных с тяжелым течением ХОБЛ и лиц старше 70 лет (рис. 2) [12].
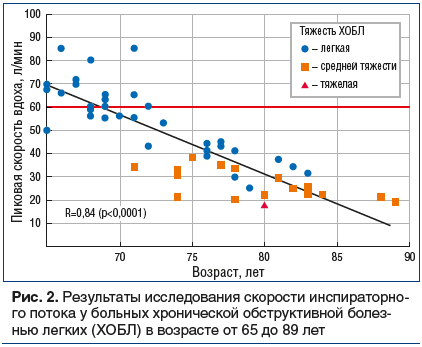
Типы порошковых ингаляторов и особенности их применения
ПИ различаются дизайном и требованиями к технике ингаляции. Так, у капсульных ингаляторов препарат находится в капсуле, которую надо поместить в ингалятор перед использованием. Резервуарные ПИ (Турбухалер®) содержат внутри резервуар, вмещающий от 30 до 120 доз. Применение капсульных ингаляторов по сравнению с резервуарными требует от больного выполнения вдоха большего объема и продолжительности [13], а также визуального контроля капсулы после ингаляции: если в капсуле остался порошок, больной должен повторить ингаляцию [14]. Напротив, резервуарные ингаляторы не требуют от больных столь значимых усилий при вдохе [15].
ПИ значительно отличаются друг от друга и по такому параметру, как поток воздуха на вдохе, который требуется для адекватной ингаляции. Чем ниже сопротивление ингалятора, тем больший поток воздуха требуется от больного во время выполнения ингаляции ( табл. 1). Для большинства ПИ пиковый поток на вдохе должен превышать 60 л/мин (или 1 л/с). Исключения составляют ингаляторы с высоким уровнем собственного сопротивления.
Например, Турбухалер® имеет относительно высокое сопротивление, кроме того, особенностью ингалятора является система спиральных каналов, двигаясь по которым порошок испытывает дополнительную турбулентность, необходимую для адекватного разделения частиц препарата и носителя. Благодаря этим конструктивным особенностям Турбухалер® обеспечивает приемлемые характеристики вдыхаемых частиц уже при вдохе со скоростью 30 л/мин [16]. Поэтому уровень в 30 л/мин является нижним лимитом пиковой скорости воздушного потока для ингалятора Турбухалер®. А при оптимальном вдохе со скоростью 60 л/мин ингалятор обеспечивает легочную диспозицию более 30% от дозы, что является хорошим показателем [17].
Проблема субоптимального воздушного потока при ингаляции через порошковые ингаляторы
По данным W. Azouz et al. (2015), среди пациентов с бронхиальной астмой (БА), применяющих Турбухалер®, все были способны выполнить вдох со скоростью >30 л/мин, а 44% больных вдыхали со скоростью >60 л/мин [7], однако среди пожилых больных ХОБЛ, которым был назначен Турбухалер®, примерно четверть пациентов оказалась не в состоянии выполнить вдох со скоростью ≥40 л/мин [18].
Таким образом, часть тяжелых пациентов с ХОБЛ и БА не способны выполнить вдох через ПИ с оптимальной скоростью. При этом, к сожалению, поток на вдохе невозможно измерить при помощи обычного спирографа, чтобы определить, подходит ли пациенту ПИ, поскольку спирограф не учитывает уровень сопротивления, которое отличается у различных моделей ПИ. С другой стороны, в клинических исследованиях было показано, что у больных ХОБЛ с субоптимальным потоком на вдохе снижается эффективность терапии и увеличивается риск обострений и госпитализаций [10].
В клинической практике мы не можем измерить инспираторный поток у каждого больного, но можно выделить типы больных, у которых чаще всего встречается недостаточный поток на вдохе и, как следствие, снижается эффективность ПИ: лица пожилого и старческого возраста, женщины, люди с низким ростом. К снижению потока на вдохе приводят снижение форсированной жизненной емкости легких и емкости вдоха в % от должного, слабость дыхательной мускулатуры, тяжелая степень ХОБЛ.
Таким образом, различные ПИ отличаются по своим характеристикам и требуют разного потока на вдохе
(см. табл. 1).
Но, кроме того, существует определенная часть пациентов, у которых назначение ПИ может оказаться нерациональным из-за неспособности правильно выполнить инспираторный маневр. Эффективной альтернативой для таких больных являются ингаляционные устройства, способные активно выделять препарат: ДАИ, небулайзеры и Респимат.
Существует несколько примеров, когда ПИ разрабатывались в дополнение к существующим ДАИ. Так, например, появились салметерол / флутиказона пропионат Мультидиск и беклометазона дипропионат / формотерол Некстхалер. Это позволило создать устройства, не требующие от больного координации вдоха. Однако практика показала возможность движения в обратную сторону: создание новых ДАИ, которые не требуют от пациентов усилия на вдохе, в дополнение к уже имеющимся ПИ. Так, был разработан и зарегистрирован в России Симбикорт® Рапихалер (рис. 3) — ДАИ, содержащий те же активные компоненты, что и давно известный в нашей стране Симбикорт® Турбухалер® [19–21].

Симбикорт® Рапихалер снабжен счетчиком доз и защитой от случайной активации [21]. Средний массовый диаметр аэрозольных частиц, которые продуцирует Симбикорт® Рапихалер, составляет 3,3–3,6 мкм [23]. Частицы жидкости по сравнению с частицами порошка лучше проникают в дыхательные пути: при столкновении со стенкой бронха капли жидкости разбиваются на мелкие фрагменты и продолжают движение в периферические отделы бронхов. Жидкие частицы размерами 3,3–3,6 мкм проникают в дыхательные пути так же хорошо, как частицы порошка размером около 2,1 мкм. Следовательно, Симбикорт® Рапихалер [21] по способности доставлять препарат в дыхательные пути эквивалентен ингалятору Симбикорт® Турбухалер® [19], и при переходе с использования одного устройства на другое не требуется пересчета дозы (табл. 2). Причем на долю мелких частиц (менее 4,7–5 мкм) как в ПИ Турбухалер®, так и в ДАИ Рапихалер приходится около 60% [23]. Таким образом, фракция респирабельных частиц в этих ингаляторах существенно выше, чем в большинстве ПИ (см. табл. 1).
![Таблица 2. Показания к применению и дозы препаратов Симбикорт® Турбухалер® и Симбикорт® Рапихалер. Информация из утвержденных инструкций по медицинскому применению препаратов [19–21] Таблица 2. Показания к применению и дозы препаратов Симбикорт® Турбухалер® и Симбикорт® Рапихалер. Информация из утвержденных инструкций по медицинскому применению препаратов [19–21]](https://www.rmj.ru/upload/medialibrary/142/46-5.png)
Возможности применения дозированных аэрозольных ингаляторов в терапии бронхиальной астмы и хронической обструктивной болезни легких
На рисунке 4 показаны результаты оценки средних значений пиковой скорости потока при вдохе через Турбухалер® у взрослых и детей, больных БА, и пациентов с ХОБЛ [7].
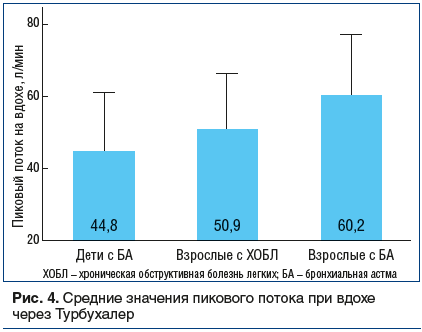
Средний инспираторный поток у больных БА, согласно результатам этого исследования, составляет 60,2 л/мин, что соответствует оптимальному уровню для ингаляции через Турбухалер®. Симбикорт® Турбухалер®, 160/4,5 мкг/доза, для терапии БА с 2019 г. одобрен в режиме применения «противовоспалительный бронхолитик» по потребности. Это позволяет больным использовать один и тот же препарат как для купирования симптомов воспаления (по потребности для пациентов с любой степенью тяжести БА с 12 лет), так и одновременно для базисной терапии при среднетяжелой и тяжелой БА [19]. Назначение препарата Симбикорт® Турбухалер®, 160/4,5 мкг/доза, для устранения симптомов не только удобно для больных, но и позволяет значимо сократить риск обострений БА, независимо от тяжести заболевания [24]. Кроме того, назначение препарата Симбикорт® Турбухалер®, 160/4,5 мкг/доза, в режиме противовоспалительного бронхолитика позволяет увеличить у больных приверженность терапии: если пациент пропускает применение препарата Симбикорт® Турбухалер®,160/4,5 мкг/доза, утром и вечером, то дополнительные ингаляции для купирования симптомов позволяют скомпенсировать пропущенную дозу глюкокортикостероидов [25, 26]. Наконец, назначение одного ингалятора вместо двух позволяет облегчить обучение больного технике ингаляции и упростить инструкции по амбулаторному лечению [27]. У больных тяжелой БА перевод на терапию Симбикорт® Турбухалер®, 160/4,5 мкг/доза, в качестве противовоспалительного бронхолитика является одним из этапов оптимизации терапии, который должен предшествовать назначению биологической терапии и/или назначению ГКС внутрь [28]. Симбикорт® Турбухалер®, 160/4,5 мкг/доза, — первый препарат с международным непатентованным наименованием (МНН) будесонид/формотерол, одобренный для применения по потребности у больных с легким течением БА с 12 лет [19].
С другой стороны, среди больных БА можно выделить категории, для которых назначение препарата Симбикорт® более целесообразно в форме ингалятора Рапихалер:
Дети 6–11 лет. Исследования показали, что у детей, больных БА, инспираторный поток при вдохе через Турбухалер® существенно ниже 60 л/мин (см. рис. 4). В этом случае лучший лечебный результат может быть достигнут при назначении препарата Симбикорт® Рапихалер, 80/4,5 мкг/доза, — ингалятора, который не требует усилия на вдохе.
Пожилые пациенты, больные с сочетанием БА и ХОБЛ и другими состояниями [8].
Пациенты, которые предпочитают использовать ДАИ в силу наличия интуитивной обратной связи (звук, ощущение ингаляции). Ингаляция через ДАИ сопровождается специфическими ощущениями в груди, связанными с тем, что быстрое испарение пропеллента вызывает эффект охлаждения. Ряд больных интуитивно воспринимают это ощущение как свидетельство того, что препарат попал в дыхательные пути. Такие пациенты могут быть не удовлетворены вдохом через ПИ, который не сопровождается специфическими ощущениями в груди.
В крупном ретроспективном исследовании реальной клинической практики было показано, что Симбикорт® Рапихалер в режиме регулярной терапии снижал частоту обострений БА в 2 раза эффективнее по сравнению с фиксированной комбинацией салметерол / флутиказона пропионат ДАИ (-0,15 против -0,07, 95% ДИ 0,85–0,99, p=0,0255) [30].
Важно отметить, что больные БА могут использовать Симбикорт® Турбухалер®, 160/4,5 мкг/доза, в качестве своего единственного ингалятора как для базисной терапии, так и для устранения симптомов Но для больного ХОБЛ помимо препарата Симбикорт® всегда необходим бронхолитик короткого действия в форме ДАИ. Если больной использует ингаляторы одного типа, это облегчает задачу обучения больного и снижает число потенциальных ошибок. D. Price et al. (2012) [27] показали, что, если для лечения ХОБЛ выбраны ингаляторы одного типа, это позволяет дополнительно на 18% снизить число тяжелых обострений и на 46% сократить использование средств для купирования симптомов. Поэтому для больного ХОБЛ более рациональным представляется назначение препарата Симбикорт® Рапихалер, 160/4,5 мкг/доза, в сочетании с короткодействующим бронхолитиком в форме ДАИ для купирования симптомов.
С другой стороны, назначая Симбикорт® Рапихалер, врач должен проверить способность больного точно синхронизировать начало вдоха с моментом нажатия на баллончик, при котором происходит активация ингалятора. Если больной из-за нарушений мелкой моторики не способен правильно синхронизировать ДАИ, то существует возможность применения препарата Симбикорт® Рапихалер через спейсер большого объема (≥750 мл). Ингаляции через спейсер позволяют значительно увеличить легочную депозицию будесонида и формотерола [31] и повысить контроль над БА [32].
Заключение
Таким образом, в настоящее время существуют различные устройства доставки в дыхательные пути препаратов для лечения БА и ХОБЛ, благодаря чему возможно дифференцированно подходить к выбору ингалятора в каждой конкретной клинической ситуации [33]. С учетом результатов клинических исследований можно заключить, что большинству больных БА старше 12 лет можно рекомендовать использование препарата Симбикорт® Турбухалер®, 160/4,5 мкг/доза, в режиме противовоспалительного бронхолитика (с поддерживающей терапией или без нее), в то время как пациентам с БА в возрасте 6–11 лет, пожилым пациентам с БА и ХОБЛ более рациональным представляется назначение ингалятора Симбикорт® Рапихалер.
Благодарность
Редакция благодарит ООО «АстраЗенека Фармасьютикалз» за оказанную помощь в технической редактуре настоящей публикации.
Состав
Одна доза препарата Симбикорт Турбухалер включает 320 мкг микронизированного будесонида и 9 мкг дигидрата фумарата формотерола либо 160 мкг микронизированного будесонида и 4,5 мкг дигидрата фумарата формотерола либо 80 мкг микронизированного будесонида и 4,5 мкг дигидрата фумарата формотерола.
Дополнительные компоненты: лактозы моногидрат.
Форма выпуска
Порошок, предназначенный для ингаляций в виде белых гранул округлой формы.
60 доз (для всех дозировок) такого порошка в пластиковом ингаляторе «турбухалер», один такой ингалятор в пачке из картона.
120 доз (для дозировок 80/4,5 мкг и 160/4,5 мкг) такого порошка в пластиковом ингаляторе «турбухалер», один такой ингалятор в пачке из картона.
Фармакологическое действие
Противовоспалительное, бронхолитическое.
Фармакодинамика и фармакокинетика
Фармакодинамика
Двухкомпонентное средство для терапии бронхиальной астмы. МНН отсутствует. Включает будесонид и формотерол, которые обладают разным действием и проявляют взаимостимулирующий эффект в отношении понижения частоты приступов бронхиальной астмы.
Будесонид — глюкокортикостероид, имеющий дозозависимое и быстрое противовоспалительное действие на респираторные пути, понижая выраженность признаков и частоту приступов бронхиальной астмы. При использовании ингаляций будесонида отмечается уменьшенная частота появления серьезных негативных эффектов, чем при использовании глюкокортикостероидов системного действия. Ослабляет отек слизистой бронхов, выделение слизи, мокроты.
Формотерол – второй компонент, избирательный стимулятор β2-адренорецепторов. Вызывает быстрое и долговременное расслабление гладких мышц бронхов у больных с обратимым сужением просвета дыхательных путей. Это действие дозозависимо и наступает через 2-3 минуты после ингаляции и продолжается минимум 12 часов.
При комбинированном использовании формотерола и будесонида снижается выраженность признаков бронхиальной астмы, стимулируется функция легких и снижается частота приступов заболевания. Препарат хорошо переносится больными.
Фармакокинетика
Исследования не выявили доказательств взаимодействия будесонида и формотерола. Ингалируемый будесонид активно абсорбируется и через 30 минут достигает максимальной концентрации. Биодоступность составляет 49%. Фармакокинетика у детей 6-16 лет и у взрослых пациентов не отличается.
Ингалируемый формотерол также активно абсорбируется после ингаляции и через 10 минут достигает максимальной концентрации. Системная биодоступность – 61%. Связывание с протеинами плазмы формотерола составляет 50%, будесонида – примерно 90%.
Будесонид подвергается активной биотрансформации при «первом прохождении» сквозь печень с синтезом метаболитов, обладающих слабой гормональной активностью.
Формотерол метаболизируется в печени конъюгационным способом с образованием активных метаболитов. Будесонид выводится почками в виде метаболитов и лишь в малом количестве – в первоначальном виде.
После применения до 13% доставленного количества формотерола выводится в первоначальном виде почками. Период полувыведения составляет 17 часов.
Показания к применению
- Хроническая обструктивная болезнь легких (симптоматическая терапия у лиц с тяжелой формой заболевания и с рецидивами обострений в анамнезе и с выраженными симптомами, несмотря на лечение бронходилататорами продленного действия).
- Бронхиальная астма (плохо контролируемая использованием ингаляционных глюкокортикостероидов и бета2-адреномиметиков кратковременного действия или хорошо контролируемая ингаляционными глюкокортикостероидами и бета2-адреномиметиками долговременного действия).
Противопоказания
- Возраст до 6 лет (для всех форм выпуска).
- Возраст до 12 лет (для форм выпуска 320/9 мкг).
- Сенсибилизация к формотеролу, будесониду или ингалируемой лактозе.
С осторожностью необходимо использовать у больных с туберкулезом легких; с вирусными, бактериальными или грибковыми инфекциями органов дыхания; с тиреотоксикозом, сахарным диабетом, феохромоцитомой, гипокалиемией, артериальной гипертензией тяжелой степени, аневризмой или сердечно-сосудистыми болезнями тяжелой степени.
Побочные действия
- Реакции со стороны ЦНС: тошнота, головная боль, беспокойство, психомоторное возбуждение, депрессия, нарушения сна, нарушения вкуса.
- Реакции со стороны системы кровообращения: фибрилляция предсердий, тахикардия, экстрасистолия, стенокардия, изменения давления.
- Реакции со стороны костно-мышечной системы: судороги, тремор.
- Реакции со стороны респираторной системы: легкое раздражение в горле, кандидоз слизистых рта и глотки, хрипота, кашель, бронхоспазм.
- Дерматологические реакции: экзантема, зуд, кровоподтеки, дерматиты.
- Аллергические реакции: отек Квинке, крапивница, анафилактические реакции.
- Метаболические нарушения: гипергликемия, гипокалиемия, симптомы генерализованного действия глюкокортикостероидов.
Инструкция по применению Симбикорт Турбухалер (Способ и дозировка)
Инструкция по применению Симбикорта Турбухалера указывает, что данный препарат не служит для первоначальной терапии бронхиальной астмы легкой степени тяжести.
Подбор дозы проводится индивидуально, учитывая тяжесть заболевания. Перед первым применением ингалятор необходимо подготовить, чтобы понять, как это делается и как пользоваться ингалятором необходимо посмотреть видео.
Видео как пользоваться Симбикортом Турбухалером:
Бронхиальная астма
Пациентам, принимающим препарат нужно регулярно проходить обследования у врача, назначившего препарат, чтобы дозировка оставалась оптимальной.
Рекомендуемые дозы. Взрослые (от 18 лет) могут производить до двух ингаляций дважды в день. Некоторым больным может понадобиться до четырех ингаляций дважды в день. Детям (12-17 лет) следует использовать также до двух ингаляций дважды в день.
После осуществления контроля над симптомами астмы дозу подбирают до наименьшей эффективной, вплоть до использования средства раз в день. У детей (6-12 лет) используется лекарственная форма с наименьшей дозировкой до двух ингаляций дважды в день.
Хроническая обструктивная болезнь легких
Рекомендуемая доза для взрослых – две ингаляции дважды день.
Передозировка
Симптомы: угнетение функции надпочечников, тремор, гиперкортицизм, учащенное сердцебиение, головная боль, гипергликемия, гипокалиемия, аритмия, тошнота.
Лечение – симптоматическое.
Взаимодействие
Бета-адреноблокаторы ослабляют действие формотерола.
При совместном применении с дизопирамидом, хинидином, прокаинамидом, антигистаминными препаратами, фенотиазинами, ингибиторами МАО и трициклическими антидепрессантами возрастает риск появления желудочковой аритмии.
L-тироксин, L-допа, окситоцин и этиловый спирт могут ухудшать сердечно-сосудистую переносимость бета-2-симпатомиметиков.
Совместное использование ингибиторов МАО, фуразолидона и прокарбазина способно вызвать аллергические реакции.
Условия продажи
По рецепту.
Условия хранения
Соблюдать температурный режим до 30 градусов. Беречь от детей.
Срок годности
Два года.
Особые указания
Не влияет на способность к вождению автомобиля.
Аналоги Симбикорт Турбухалер
Совпадения по коду АТХ 4-го уровня:
Существуют следующие аналоги Симбикорта: Форакорт 200 (полный аналог), Аиртрек, Беродуал, Серетид.
Детям
Запрещено принимать препарат детям до 6 лет, а лекарственную форму 320/9 мкг – детям до 12 лет.
При беременности (и лактации)
Возможно использование при наличии строгих показаний и по назначению врача.
Отзывы о Симбикорт Турбухалер
Отзывы о Симбикорте на форумах в интернете и отзывы врачей свидетельствуют, что данный препарат помогает многим людям справляться с приступами бронхиальной астмы и значительно улучшить качество жизни.
Что лучше Серетид или Симбикорт?
Выбор между препаратами Серетида и Симбикорта следует делать исходя из индивидуальных особенностей пациента. Нередки случаи, когда один из препаратов оказывается малоэффективным, тогда его заменяют аналогом.
Цена Симбикорт Турбухалер, где купить
Купить препарат, содержащий наименьшую дозировку, в России составит 1025-1910 рублей. А цена Симбикорта Турбухалера 80/4,5 мкг на Украине достигает 360 гривен.
- Интернет-аптеки РоссииРоссия
ЗдравСити
-
Симбикорт Турбухалер порошок для ин. дозир. 160мкг+4,5мкг/доза 120 дозAstraZeneca
-
Симбикорт Турбухалер ингалятор порошок для ингаляций дозированный 80/4,5мкг/доза 60дозAstraZeneca
-
Симбикорт Турбухалер порошок для ин. дозир. 80мкг+4,5мкг/доза 120 дозAstraZeneca
-
Симбикорт турбухалер пор. д/ингал. 320мкг+9мкг/доза 60дозAstraZeneca
-
Симбикорт Турбухалер порошок для ин. дозир. 160мкг+4,5мкг/доза 60 дозAstraZeneca
показать еще
