Full Text
Группа ингибиторов ароматазы (ИА) 3-го поколения включает два обратимых нестероидных ингибитора: летрозол (Фемара) и анастрозол (Аримидекс) – и необратимый стероидный инактиватор экземестан (Аромазин). Эти препараты убедительно продемонстрировали преимущества в эффективности и токсичности по сравнению с тамоксифеном при лечении диссеминированного гормонозависимого рака молочной железы (РМЖ) как в первой линии гормонотерапии, так и при резистентности к другим препаратам гормонотерапии. В настоящее время изучается их действие при лечении больных ранним РМЖ. В зависимости от дизайна исследования по адъювантной гормонотерапии РМЖ можно сгруппировать следующим образом. В данной статье мы рассмотрим результаты исследований, посвященных оценке эффективности Фемары в адъювантной гормонотерапии рецепторпозитивного РМЖ у больных в менопаузе. Стандартом адъювантной гормонотерапии до недавнего времени был тамоксифен, назначавшийся в дозе 20 мг/сут в течение 5 лет. Установлено, что именно такой режим является оптимальным и позволяет существенно снизить частоту рецидивов болезни (на 41%) и смертей (на 31%) от РМЖ у больных с гормонозависимыми опухолями [1]. Вместе с тем оказалось, что тамоксифен не способствует профилактике отдаленных метастазов, а является более эффективным средством профилактики развития местных рецидивов. В то же время более длительный его прием существенно повышает риск серьезных нежелательных явлений и не приводит к улучшению отсроченных результатов лечения, поскольку более 50% рецидивов болезни и смертей, обусловленных прогрессированием, происходит после окончания 5-летнего срока адъювантной гормонотерапии: частота рецидивов РМЖ составляет 15% в течение первых 5 лет после хирургического лечения и 33% по прошествии 15 лет, смертность от РМЖ за этот период увеличивается в 3 раза (8,3% через 5 лет и 26% через 15 лет после первичного лечения) [1, 2]. Эти факты выявили недостатки существующего стандарта адъювантной гормонотерапии тамоксифеном и послужили основанием для инициации ряда исследований, направленных на поиск более совершенных подходов к лечению раннего гормонозависимого РМЖ. Такая возможность появилась с внедрением в клиническую практику ИА 3-го поколения анастрозола, экземестана и Фемары. Фемара в различного рода сравнительных исследованиях продемонстрировала ряд преимуществ: • более эффективную по сравнению с анастрозолом супрессию эстрадиола [3, 4]; • большую непосредственную эффективность по сравнению с анастрозолом (р=0,013) во второй линии гормонотерапии у больных метастатическим РМЖ [5]; • большую эффективность по сравнению с тамоксифеном в первой линии гормонотерапии диссеминированного РМЖ [6]; • лучшие непосредственные результаты по сравнению с анастрозолом при непрямом сравнении ИА (летрозол и анастрозол) с тамоксифеном в неоадъювантной гормонотерапии [7–9]; • более эффективное угнетение пролиферации опухолевых клеток при сравнении с тамоксифеном и анастрозолом [4, 7, 10]. Эти факты породили чрезвычайно интересный вопрос: реализуются ли перечисленные преимущества Фемары при ее использовании в качестве адъювантной гормонотерапии. Для ответа на этот вопрос были инициированы два международных многоцентровых исследования с включением Фемары – BIG 1–98 и МА.17. Следует отметить, что дизайн этих исследований позволяет сравнить Фемару и тамоксифен при всех трех режимах использования (в качестве инициальной гормонотерапии сразу после хирургического вмешательства, в режиме переключения и в продленном режиме адъювантной гормонотерапии). Исследование Британской Международной Группы 1–98 (British International Group – BIG 1–98) представляет собой проспективное рандомизированное двойное слепое исследование III фазы, в котором сравниваются 4 варианта адъювантной гормонотерапии (см. рис. 1): • тамоксифен в течение 5 лет; • Фемара в течение 5 лет; • тамоксифен в течение 2 лет с переходом на Фемару в течение 3 лет; • Фемара в течение 2 лет с переходом на тамоксифен в течение 3 лет. Таким образом, исследование BIG 1–98 по сути состоит из двух частей, которые позволяют оценить Фемару в сравнении с тамоксифеном как в инициальной адъювантной гормонотерапии, так и в режиме переключения (Фемара→тамоксифен и тамоксифен→Фемара). Основной целью исследования BIG 1–98 была оценка безрецидивной выживаемости, второстепенными задачами являлись оценка выживаемости без отдаленных метастазов, общей выживаемости и безопасности лечения. C марта 1998 г. по март 2003 г. в исследование были включены 8028 женщин постменопаузального возраста после хирургических вмешательств по поводу раннего гормонозависимого РМЖ. У 41% больных имелись метастазы в подмышечных лимфатических узлах (N+), у 37% больных размер опухоли превышал 2 см; 25% больных получали адъювантную химиотерапию. В период с марта 1998 г. по март 2000 г. больных рандомизировали в группы монотерапии Фемарой 2,5 мг/сут или тамоксифеном 20 мг/сут. С апреля 1999 г. по май 2003 г. рандомизация осуществлялась во все 4 группы. В результате распределения по группам в общей сложности 2463 больных получали лечение Фемарой, 2459 больных – тамоксифеном, а с учетом подгрупп, в которых проводили смену препарата, 4003 пациентки на первом этапе получали Фемару и 4007 пациенток – тамоксифен (рис. 2). Результаты этой части исследования, т.е. сравнение эффективности летрозола и тамоксифена в качестве инициальной гормонотерапии, доступны для обсуждения. Промежуточный анализ, проведенный при медиане времени наблюдения 25,8 мес, показал увеличение безрецидивной выживаемости на 19% (р=0,003) в группе Фемары по сравнении с тамоксифеном, в том числе и в подгруппе неблагоприятного прогноза, в которую вошли больные с N1, а также получавшие адъювантную химиотерапию. Еще более важным с клинических позиций оказался тот факт, что Фемара снижала риск отдаленного метастазирования на 27%, что было намного эффективнее (р=0,0012), чем в группе тамоксифена. Отдаленные метастазы были основным видом прогрессирования болезни и ассоциировались с увеличением смертности. В группе Фемары метастазы были диагностированы у 4,4% больных (177/351 событие), а в группе тамоксифена – у 5,8% (232/428 событий) больных. Это влияние сохранялось в отношении любой локализации метастазирования (в мягкие ткани, кости, внутренние органы). Что касается летальных исходов, то в группе Фемары произошло в общей сложности несколько меньше смертей по сравнению с группой тамоксифена (166 против 192), в том числе летальных исходов, обусловленных раком, было на 43 меньше (111 против 154). Снижение смертности в группе Фемары на 14%, зафиксированное при данном промежуточном анализе, не достигло статистической значимости (р=0,16), возможно, ввиду небольшого срока наблюдения [11]. Второй промежуточный анализ в подгруппах монотерапии Фемарой или тамоксифеном был проведен при медиане времени наблюдения 51 мес [13]. К этому времени примерно 1/2 больных продолжала получать лечение, 1200 пациенток закончили 5-летний адъювантный прием Фемары или тамоксифена. В подгруппе Фемары досрочное прекращение гормонотерапии вследствие побочных реакций происходило чаще, чем в подгруппе тамоксифена (12,3% против 11,1% соответственно), в то время как прекращение лечения по причине прогрессирования, наоборот, чаще встречалось в подгруппе тамоксифена (7,9% против 11,5%). В целом данные второго промежуточного анализа подтвердили предыдущие результаты. Следует подчеркнуть, что статистически значимое преимущество в безрецидивной выживаемости сохранилось как во всей группе (р=0,07), так и для больных с N+ (р=0,004). В подгруппе с N0 имелась тенденция к снижению на 12% риска рецидива при приеме Фемары, однако разница не достигла статистической значимости (р=0,26). Эти данные свидетельствуют о том, что Фемара в качестве ранней адъювантной гормонотерапии приносит пользу в первую очередь больным с высоким риском раннего рецидива болезни. Крайне важным при оценке результативности любого вида лечения является его переносимость и безопасность. Данные исследования BIG 1–98 свидетельствуют о том, что в целом терапия Фемарой хорошо переносится пациентками. Прием тамоксифена ассоциировался с существенным увеличением частоты тромбоэмболий (3,5% по сравнению с 1,5%), рака эндометрия (0,3% по сравнению с 0,1%) и вагинальных кровотечений (6,6% по сравнению с 3,3%), в то время как прием Фемары не приводил к подобным осложнениям, а чаще наблюдались костно-мышечные осложнения: развитие остеопороза, костных переломов (5,7% по сравнению с 4,0%), артралгий (20,3% по сравнению с 12,3%). Общая частота кардиоваскулярных расстройств была сопоставимой (3,7% по сравнению с 4,2% для Фемары и тамоксифена соответственно) и подтвердилась в более позднем анализе (с медианой времени наблюдения 51 мес) [11, 13]. В группе Фемары частота кардиальных осложнений III–V степени была выше, хотя в целом эти явления встречались крайне редко (2,1% по сравнению с 1,1%). Таким образом, прямое сравнение эффективности Фемары и тамоксифена в качестве инициальной адъювантной гормонотерапии рецепторположительного РМЖ продемонстрировало возможность улучшения некоторых отдаленных результатов лечения (безрецидивной выживаемости и выживаемости без отдаленных метастазов), особенно для больных с высоким риском рецидива. Сегодня мы располагаем данными сходного исследования АТАС, в котором с тамоксифеном сравнивали эффективность другого ИА анастрозола. Несмотря на некоторые различия в дизайне, целях и задачах этих протоколов, в целом выявлено сопоставимое влияние обоих препаратов (летрозол и анастрозол) на показатели безрецидивной выживаемости: в исследовании АТАС анастрозол снижал риск рецидива болезни при рецепторположительных опухолях на 17% по сравнению с тамоксифеном (n=6241, медиана времени наблюдения 68 мес). В то же время при непрямом сравнении результатов были выявлены существенные различия в пользу Фемары в отношении риска возникновения отдаленных метастазов: Фемара в исследовании BIG 1–98 снижала риск раннего метастазирования на 30%, в то время как анастрозол в исследовании АТАС – только на 7% [14, 15]. Прямое сравнение Фемары и анастрозола в качестве начальной ранней адъювантной терапии проводится в настоящее время в исследовании FACE, которое, возможно, и даст ответ на вопрос, какой же из двух ИА – Фемара или Аримидекс – лучше [16]. Таким образом, ИА способны снизить риск раннего (в ближайшие 2–2,5 года после хирургического лечения) рецидивирования. Фемара при непрямом сравнении оказалась более эффективной, чем анастрозол, в отношении возникновения отдаленных метастазов. Другое исследование с участием Фемары МА.17 было построено по принципу сравнения эффективности стандартного 5-летнего приема тамоксифена и продленной адъювантной гормонотерапии, при которой 5-летний прием тамоксифена дополнялся 5 годами приема Фемары по 2,5 мг/сут (см. рис. 1) [17]. Цель данного исследования заключалась в том, чтобы выяснить, может ли продленная адъювантная гормонотерапия снизить количество рецидивов РМЖ, возникающих в поздние сроки, т.е. после завершения стандартной 5-летней адъювантной гормонотерапии тамоксифеном. МА.17 является рандомизированным двойным слепым плацебоконтролируемым исследованием, в котором в общей сложности приняли участие 5187 женщин постменопаузального возраста, закончивших стандартную адъювантную гормонотерапию тамоксифеном. С 1998 по 2002 г. участницы исследования были рандомизированы в группы приема Фемары (2,5 мг/сут) в течение 5 лет (n=2583) или плацебо (n=2587). Сравниваемые группы были сбалансированы по основным клинико-анамнестическим данным. У 97,4% больных опухоли были положительны по РЭ и/или РП, около 1/2 больных не имели метастазов в подмышечных лимфатических узлах (N0), чуть более половины (54,3 и 54,8%) получали адъювантную химиотерапию. В исследовании планировалось оценить безрецидивную выживаемость (основная цель), а также выживаемость без отдаленных метастазов, общую выживаемость, безопасность лечения и качество жизни (второстепенные цели). Промежуточный анализ, выполненный при медиане времени наблюдения 2,5 года, показал существенное (на 40%) снижение риска возникновения отдаленных метастазов в группе летрозола. Четырехлетняя безрецидивная выживаемость была также существенно выше в группе продленной адъювантной гормонотерапии: разница составила 42%. Влияние Фемары на безрецидивную выживаемость касалось всех вариантов прогрессирования болезни, т.е. локорегионарных рецидивов, отдаленных метастазов и контралатерального рака независимо от состояния подмышечных лимфатических узлов и наличия в анамнезе адъювантной химиотерапии. В подгруппе больных с метастазами в подмышечные лимфатические узлы, которые составили 46% всех участниц исследования, прием Фемары существенно (р=0,04) увеличил общую выживаемость по сравнению с плацебо. Следует особо подчеркнуть данное обстоятельство, поскольку это первое статистически значимое увеличение продолжительности жизни больных ранним РМЖ, достигнутое с помощью ИА. При ретроспективном анализе эффективности продленной адъювантной гормонотерапии в зависимости от рецепторного статуса опухоли оказалось, что в наибольшей степени от приема Фемары выигрывали больные с опухолями, положительными по обоим видам рецепторов (РЭ+/РП+): в этой подгруппе отмечено снижение частоты рецидивов болезни на 51% по сравнению с плацебо, в то время как при РЭ-/РП+ этот показатель равнялся 44%, а у больных с РЭ+/РП- вообще не отмечено преимущества от приема Фемары. Примерно такая же закономерность была выявлена и для выживаемости без отдаленных метастазов. Что касается общей выживаемости, то эффект от приема Фемары по этому показателю был статистически значим только для больных с РЭ+/РП+. Среди участниц исследования пациентки с таким вариантом рецепторного статуса составили 73% [18]. Поскольку роль РП в регуляции функционирования РЭ хорошо известна, становится понятным, почему потеря РП существенно снижала активность летрозола. Важной частью исследования МА.17 является оценка безопасности лечения, особенно учитывая общую длительность гормонотерапии, которая в экспериментальной группе должна составить 10 лет. Напомним также, что попытка увеличить продолжительность приема тамоксифена с адъювантной целью ассоциировалась с усугублением ряда побочных явлений. В исследовании МА.17 проявления токсичности были причиной прекращения лечения у 4,9% больных в группе Фемары и у 3,6% больных в группе плацебо (р=0,019). Частота приливов, анорексии, артралгий и миалгий, а также алопеции была выше в группе летрозола. В группе плацебо чаще встречались вагинальные кровотечения. Кроме того, в группе Фемары чаще наблюдались явления так называемой специфической токсичности, свойственной всей группе ИА и обусловленной нарушением метаболизма костной ткани. В частности, новые случаи остеопороза были зафиксированы в общей сложности у 364 пациенток, из которых 209 (8,1%) получали Фемару, а 155 (6,0%) – плацебо (р=0,003); медиана времени до развития остеопороза составила 0,70 года в группе Фемары и 0,52 года – в группе плацебо. В то же время учащение случаев остеопороза существенно не отразилось на частоте переломов: из 256 пациенток, у которых произошли переломы, 137 (5,3%) получали Фемару и 119 (4,6%) плацебо (р=0,25). Медиана времени от момента рандомизации до развития переломов составила 1,06 года в группе летрозола и 0,86 года в группе плацебо. Еще один вид токсичности, которая считается специфической для ИА, – кардиоваскулярные явления – отмечен у 149 (5,8%) и 144 (5,6%) больных в группах Фемары и плацебо соответственно (р=0,76). Была проанализирована также частота вторых опухолей: у 4 больных в группе Фемары и у 11 больных в группе плацебо развился рак эндометрия (р=0,12). Различий в частоте вторых опухолей других локализаций не выявлено. Таким образом, терапию Фемарой в целом больные переносили удовлетворительно. Исследование МА.17 показало, что прием Фемары в течение 5 лет после окончания стандартной адъювантной гормонотерапии тамоксифеном может существенно снизить риск прогрессирования РМЖ, в том числе риск возникновения отдаленных метастазов, а у больных с метастазами в подмышечные лимфатические узлы увеличить выживаемость. Продленный вариант адъювантной гормонотерапии Фемарой переносится больными удовлетворительно. Анализируя промежуточные результаты протоколов BIG 1–98 и МА.17 в контексте других исследований по адъювантной гормонотерапии с использованием ИА следует признать, что, несмотря на ряд преимуществ, о которых говорилось выше, вопрос об оптимальном препарате и режиме его использования пока остается открытым. Требуется углубленное изучение безопасности лечения, особенно отсроченных нежелательных явлений, поскольку речь идет о потенциально излечимых больных. Существенной проблемой при лечении ИА являются остеопороз и связанные с ним переломы костей. Коррекция этого осложнения возможна с помощью группы препаратов, которые называют бисфосфонатами. При обсуждении рекомендаций по адъювантной гормонотерапии на очередном Х консенсусном митинге по лечению раннего РМЖ, проходившем в марте этого года в Сен-Галлене, большинство экспертов сошлись во мнении, что прием тамоксифена в течение 5 лет остается одной из возможных опций адъювантной гормонотерапии РМЖ. Однако отмечено, что применение ИА 3-го поколения существенно расширяет возможности адъювантной гормонотерапии. Оптимальной стратегией является переход на прием ИА после 2–3 лет приема тамоксифена. В качестве ранней адъювантной гормонотерапии Фемара и другие ИА показаны больным с высокой экспрессией РЭ и РП группы высокого риска рецидива, в частности при гиперэкспрессии HER-2/neu [19], а также при противопоказаниях к приему тамоксифена (гиперпластические процессы в эндометрии, гиперкоагуляция, тромбоэмболии и тромбофлебит в анамнезе и др.). Что касается продленного варианта адъювантной гормонотерапии, то прием ИА по завершении 5 лет лечения тамоксифеном следует обсуждать у пациенток с метастазами в подмышечные лимфатические узлы. Несмотря на существующие пока разногласия, интеграция ИА, в том числе Фемары, в систему адъювантной гормонотерапии, безусловно, позволит с большим оптимизмом обсуждать прогноз при РМЖ, поскольку возможность снижения числа рецидивов болезни, а для некоторых категорий больных – увеличения продолжительности жизни, стала вполне реальной.
Наше сообщество ВКонтакте>ссылка>
На вопросы отвечает победитель Всероссийской премиии «Будем жить» в номинации»ЖЕМЧУЖИНЫ ПРОФЕССИИ» кмн, заведующий отделением ГКОД СПБ Скворцов Виталий Александрович
ВОПРОС: У меня в декабре 2014г обнаружили РМЖ 2 стадия без метостазов, мне удалили правую грудь и лимфоузлы,назначили пить 5 лет ЛЕТРОЗОЛ 2.5 мг. Я его продолжаю пить, может ужу бросить пить? У него в ПОБОЧНЫХ НАРУШЕНИЕ СНА, у меня почти постоянная бессонница, постоянный Зуд головы. Может мне перейти на АНАСТРОЗОЛ- Тева?
ОТВЕТ: Здравствуйте! В данном случае можно вообще уже отменить принимать препарат, так как согласно международным рекомендациям его прием назначают на 5 лет! Обратитесь к онкологу и он вам отменит этот препарат!
ВОПРОС: Добрый день. После РМЭ Т2М0N0 с сентября 2016 принимаю тамоксифен 20mg в день. После четвёртого выскабливания по поводу гиперплазии эндометрия в соскобе рак матки с переходом на верхнюю 1/3 цервикального канала Т2АМ0N0. 10 июня 2019 проведена экстирпация матки с придатками, лимфоузлами. Проводится послеоперационное обследование перед лучевой терапией. Месяц не принимала тамоксифен. Возможен ли приём тамоксифена на фоне лучевой терапии по поводу рака матки? Два месяца между операцией и началом лучевой терапии — это много? Онкомаммолог сказала продолжить приём тамоксифена, органы-мишени удалены. Онкогинеколог затруднилась с ответом. Подскажите, пожалуйста.
ОТВЕТ: Здравствуйте! Надо продолжить принимать Тамоксифен или же можно перейти так же на ингибиторы ароматазы!
ВОПРОС: Мне 41 год. в январе обнаружили РМЖ. 22/01/19 была проведена радикальная мастэктомия по Маддену с удалением лимфоузлов. Удалены 3 узла в груди: 1,3Х1Х0,8 ; 1Х1Х0,8 ; и 0,5 см. 10 из 13 лимфоузлов с метастазами. Мультицентричный протоковый инфильтрующий рак 2 степени злокачественности с метастазами в подмышечные лимфоулы до 2 см, в заключении стоит pT1mN3M0 G2 ИГХ: ER-6 б, Pr-7 б, Her2neu — 0 б, Ki67 — 10% Прошла ХТ АС 4шт, 25 лучей, удалили яичники, чтобы не назначать тамоксифен, Назначили анастразол. на него пошла очень сильная аллергия. Отменили и все- таки назначили тамоксифен. Хотя так упорно его избегали. Было КТ с контрастом — все чисто, кроме какого-то подкожного узла на уровне рукоятки грудины справа 0,7 Х 0,8. На УЗИ ничего не увидели кроме серомы примерно того же размера. Ходила на КТ с жуткими ожогами. Радиолог сказал они так могли засветится.Хочу уточнить. может что-то еще есть из антигормонального лечения и на счет подкожного узла на уровне рукоятки, может ли так отсветить серома или ожог от лучей?
ОТВЕТ: Здравствуйте! Анастрозол можно было заменить на другой препарат из этой группы: летрозол, экземестан. Но в принципе, если Вы хорошо переносите тамоксифен, то его можно продолжить принимать, это тоже хороший и эффективный препарат. Образование под кожей может быть просто липома, гранулема или же внутрикожный метастаз, надо обратиться к онкологу, и он решит что с ним делать, можно наблюдать, а можно сделать биопсию. В любом случае обсудите этот вопрос с онкологом.
ВОПРОС: Добрый день! Елена, 30 лет. Рак левой молочной железы I стадия рT1N0M0 G3 Люминальный А тип. Неспецифированный/протоковый рак II степени злокачественности. Размер узла 15Х12Х11. Иммуногистохимия ER PR положительная по 8 баллов, HER2 1 балл, ki67-9%. Генетических нарушений нет. Проведена подкожная мастэктомия с одномоментным протезированием. Расположение опухоли верхне-внутреннее, высоко от соска. Обещали, что при мастэктомии эстетический результат будет лучше, но в итоге сделали два шва, чтобы добраться. По поводу гормонотерапии консультировались уже у 4 специалистов. Мнения разделились: двое добавляют Золадекс к Тамоксифену (я так понимаю из-за G3), двое советуют оставить только тамоксифен стандартно на 5 лет. Учитывая все побочные эффекты Золадекса и длительность применения, что бы Вы назначили в данном случае? Спасибо за ответ!
ОТВЕТ: Здравствуйте! Я считаю, что Ваш возраст 30 лет и G3 — факторы риска, и я бы Вам назначил Золадекс пока на 2 года и тамоксифен. Вообще это лечение назначается комиссионно по месту жительства!
ВОПРОС: Какой препарат лучше после удаления груди тамоксифен или летрозол?
ОТВЕТ: Здравствуйте! Это разные препараты по своему механизму действия, и они назначаются в разных ситуациях. Врач онколог определяет, что именно назначить тамоксифен или ингибиторы ароматазы (летрозол).
ВОПРОС: Здравствуйте! Мне 37лет, рмж гормонозависимый, her2 позитивный, скажите, пожалуйста, через какое время после последней капельницы кадсилы я могу начать прием тамоксифена?
ОТВЕТ: Здравствуйте! Прием тамоксифена одновременно с таргетной терапией не противопоказан и принимать можно даже сейчас.
ВОПРОС: Виталий Александрович, Вы уже давали ответ на мой вопрос хотелось бы уточнить по правильности назначеного лечения. Напомню вопрос: маме 65 лет, ей 8 лет назад удалили матку и яичники (миома), раковых клеток не обнаружили на данный момент обратились на консультацию с грудью, ранее по снимках была установлена мастапатия , при обследовании биопсии до операции раковых клеток не обнаружили, но была большая опухоль и деформации кожного покрова. Было принято решении оперировать. После операции был поставлен диагноз Рак молочной железы pT2N3M0, G3, 3C ст. 2 кл.гр. Заключение: Инвазивная дольковая карциома G3, 4см в диаметре. Метастазы рака в 7 (из17) подмышечных л/у, в 2(4) подключичных л/у. ИГХ исследование показало Эстраген 6б, Прогестерон 7б, Her-2/Neu 0, Ki 67-10%. Пошли на прием к химиотерапевту был назначен АС (доксорубицин 60 мг/м в/в 1-й день +циклофосфамид 600 мг/м в/в в 1-й день раз в 3 нед. 4 цикла) далее лучевая и гормональная на 5 лет. Препарат горманальной не был назван. Какой лучше?
ОТВЕТ: Здравствуйте! Обычно назначают стандартную эффективную эндокринотерапию тамоксифеном или ингибиторами ароматазы — анастрозолом. Это определяет Ваш онколог по месту жительства.
ВОПРОС: Виталий Александрович, добрый день. Меня зовут Альбина, 20.01.2015 была вашей пациенткой, огромное спасибо, за профессионализм и человеческую заботу. Я была на консультации у онколога на Берёзовой, по поводу приёма Тамоксифена. Принимаю его с 23.02.15, почти 4,5 года, рассчитывала на то что скоро 5 лет и всё прием окончен! Но он меня не обрадовал, сказал, что на комиссии решили пить до 7 лет. Что делать продолжать пить?
ОТВЕТ: Здравствуйте! Я вам в WhatsApp ответил, что Вам надо продолжить принимать до 7 лет. Не всем пациентам это рекомендовано. Я вас помню и у вас есть факторы, которые говорят о продолжении тамоксифена до 7 лет.
ВОПРОС: Здравствуйте. Можете расшифровать результаты гистологии? Эр+ (260) Пр+ (30) онко — ; Кi67 15% Люминальный В Her2 отр (рТ2рN2М0). Мне рекомендовано ХТ, лучевая терапия и тамоксифен. Я прочитала, что люминальный тип В эффективно лечиться Трастузумабом. Можете прокомментировать?
ОТВЕТ: Здравствуйте! Вы понимаете неправильно. Во-первых, у Вас люминальный тип А, а не В! Трастузумаб назначают при HER2 позитивном раке, ,а в данном случае у Вас отрицательный. Он вам не показан! Вам показана химиотерапия, назначенная местной комиссией, а потом лучевая терапия и эндокринотерапия.
ВОПРОС: Здравствуйте, на время лучевой терапии отмена тамоксифена на 1.5 месяца грозит негативным влиянием?
ОТВЕТ: Здравствуйте! На самом деле это не страшно, у Вас же адъювантный прием Тамоксифена, просто можно вообще не отменять тамоксифен, некоторые радиологи отменяют антигормональную эндокринотрепию терапию, а некоторые продолжают облучать на фоне приема тамоксифена, это все зависит от Вашего радиолога.
ВОПРОС: Здравствуйте, я принимаю тамоксифен уже 6 лет, кто-то говорит из врачей , что можно до 10 лет, кто-то говорит, переходить на аримидекс. Кто-то говорит вообще не пить таблетки. У меня мастоктамия и опухоль гормональная , стадия 1 а в 52 года с активным циклом. Менопаузу сделали химическим путём- золодекс на протяжении 4 лет. Что дальше не пойму! Может есть у Вас какие-то методы профилактики?
ОТВЕТ: Здравствуйте! Тамоксифен на 10 лет назначается тем, кто находится в группе риска. Вы не относитесь к данной группе, поэтому вам можно прекратить прием эндокринотерапии, сейчас пока четких рекомендаций для тех кто не в группе риска.
ВОПРОС: Виталий Александрович, добрый день. Очередной раз обращаюсь к Вам за помощью. Во-первых огромное Вам спасибо за Ваш, труд, работу, терпимость к нам. Земной Вам поклон и крепкого здоровья Вам и Вашей семье. Виталий Александрович, подскажите, пожалуйста: начат прием Фарестона и несколько дней задержка месячных. Может ли, на Ваш взгляд, это быть связано с приемом препарата? Заранее огромное Вам спасибо.
ОТВЕТ: Здравствуйте! Это может быть на фоне приема Фарестона! Но Вы читали в аннотации к препарату ,что этот препарат назначается у женщин только в постменопаузе. Обсудите еще раз этот вопрос со своим лечащим врачом.
ВОПРОС: Виталий Александрович, 5 лет принимаю тамоксифен, молекулярный подтип опухоли люминальный В her позитивный. Продолжать дальше адъювантную антигормональную эндокринотерапию? Были 2 мтс в лимфоузлах, лучевой терапии не было, не считая интраоперационного облучения.
ОТВЕТ: Здравствуйте! На сегодня длительность приема тамоксифена более 5 лет, согласно последним данным, относится к женщинам, которые относятся к группе риска. Вы со своми пораженными лимфоузлами и her 2 раком относитесь к этой группе. Вам надо продолжить прием Тамоксифена пока до 7 лет.
ВОПРОС: Здравствуйте, Виталий Александрович! Спасибо за предоставленный ранее ответ. Прошу Вас еще помочь разобраться с важными вопросами. Хочу вкратце напомнить, мне 44 года, диагноз: pT1cpN1aM0, опухоль полностью гормонозависимая, HER2 -отр., Ki-67: 37,5%, Люминальный тип B, Her2- негативный, операция с сохранением МЖ. Лечение: 4 курса АПХТ по схеме AC+адьювантная фракционированная лучевая терапия, 1-4 группы лимфоузлов (подмышечные, подключичные, надключичные). На текущий момент принимаю Тамоксифен 20мг ежедневно + Золадекс. Учитывая мой диагноз и лечение очень прошу Вас ответить на мои вопросы:
1.От ТАМОКСИФЕНА сильно болят ног, а раньше не болели. Врач говорит, что это может быть побочное действие. Как вариант предлагает мне перейти на препарат второго поколения Таморифен (Фарестон) по 60 мг./сутки, от которого нет никаких побочных эффектов, а действие его равнозначно Тамоксифену. Как Вы считаете, это будет правильное решение? И насколько Фарестон лучше или хуже Тамоксифена? Есть ли у него побочные действия?
2. Имеет ли смысл для снижения последующих возможных рецидивов (даже через 10 лет) сделать операцию по удалению яичников и перейти на прием ингибиторов, например, Аримидекса? Мой врач говорит, что при приеме Тамоксифена и наличии яичников (даже не действующих) возможны более частые рецидивы и даже спустя много лет. Если удалять, то когда в 1-й год после операции?
3. Какими методами проверить себя на отсутствие рецидива в яичниках, и как часто это нужно делать?
4. Все ли можно есть и пить, или стоит что-то исключить?
Для меня очень важно Ваше мнение по этим вопросам.
ОТВЕТ: Здравствуйте! Прием Тамоксифена не вызывает рак яичников и не увеличивает риск возникновения. Ноги могут болеть, конечно, от тамоксифена, а Фарестон может снизить интенсивность этих побочных эффектов, но на самом деле, Фарестон лучше Тамоксифена, но в показаниях написано, что прием этого препарата только у женщин в постменопаузе, Вы сейчас еще пока с сохраненным циклом, Хотя фармакологическая группа одна и таже. Назначение ингибиторов ароматазы улучшит Ваше лечение, но надо выключить яичники лекарствами или операцией!
ВОПРОС: Здравствуйте, Виталий Александрович! Мне 42 года. Диагноз: pT1N1M0. Инвазивная умереннодифференцированная карцинома. Проведена секторальная резекция. Прошла 4 курса ХТ АС. Впереди лучевая терапия. Назначен курс гормонотерапии: тамоксифен — 20 мг- длительно и бусерелин 3,75 мг.- 1 раз в месяц. Скажите, пожалуйста, обязателен ли прием в моем случае бусерелина и на какой период времени его необходимо применять?
ОТВЕТ: Здравствуйте! Если у Вас люминальный тип А рака молочной железы, то одним из назначений, кроме эндокринотерапии, идет выключение функции яичников. Одним из существующих способов их выключить это введение Бусерелина, если Вам его назначила онкологическая комиссия, значит, он Вам показан и придется колоть минимум 2 года, а потом повторно будет подниматься вопрос о продлении или прекращении.
ВОПРОС: Добрый день, я уже обращалась к Вам с вопросом, спасибо за ответ. Мой диагноз : рмж 2 В стадия, экстрогены -8 баллов, прогестерон-4 балла, KI 67-30%, HER-2/neu 1+, 3 степень злокачественности. В январе 2018 г. мастэктомия по Маддену, 6 красных химий, летрозол на 5 лет. Принимаю летрозол с сентября 2018 г., на фоне его приема появились ноющие боли в мышцах и костях, в шейке бедра и одном позвонке остеопения. Скажите, пожалуйста, можно ли применять препарат АСД-2 на фоне приема летрозола? Читала много положительных отзывов об АСД-2. Заранее благодарна.
ОТВЕТ: Здравствуйте! В международных рекомендациях нет рекомендаций по назнаачению данного препарата и не понимаю для чего Вы можете его принимать в данном случае, обратиетсь к онкологу, и он Вас должен дообследовать, если есть в этом необходимость и нананчить адекватное проверенное лечение.
ВОПРОС: Здравствуйте доктор. У меня РМЖ, после двух капельниц АС менструация пропала; гормоны ФСГ. 72,7. Эстрадиол 41. Врач назначила ингибиторы ароматазы и контроль гормонов. Месячных нет 2;5 месяца. Правильно ли это? Другой врач тамоксифен назначает. Как быть? Очень надеюсь на Ваш ответю
ОТВЕТ: Здравствуйте. В данном случае нет месячных 2,5 месяца и это очень мало, поэтому нежелательно назначение ингибиторов ароматазы и лучше начать прием Тамоксифена, потому что нет полной уверенности, что наступила менопауза.
ВОПРОС: Виталий Александрович, что делать в такой ситуации — выпила аримидекс и через 50 минут началась рвота. Стоит ли в таком случае повторить прием аримидекса.
ОТВЕТ: Здравствуйте! Возникновение рвоты может быть и психологически, в данном случае это для вас этот препарат эффективный, его надо продолжить принимать, но только на следующий день!
ВОПРОС: Виталий Александрович, спасибо за ответ, а от ингибиторов побочка на кости? У меня в последнее время пошли проблемы с костями. А просто если прекратить все, есть риск рецидива?
ОТВЕТ: В данном случае конечно риск есть, Вы достаточно молоды, поэтому лучше начать прием ингибиторов ароматазы, хотя бы на 2,5 года, потому что тамоксифен уже 4 года, побочных явлений с костями у Вас не должны быть, я так думаю. Лучше не прекращать прием ингибиторов ароматазы.
ВОПРОС: Добрый день! Люминальный В, проведена операция. Адъювантная химиотерапия, ЛТ. 59 лет. Принимаю летрозол уже 4 месяца.. Прописан на 5 лет. Вопрос: А что дальше? После тамоксифена — ингибиторы ароматазы назначают, а после ИА что? Только наблюдение? Или 5 лет — это предел? Или надеяться на то, что наука что-нибудь изобретет? Спасибо.
ОТВЕТ: Здравствуйте! 5 лет ингибиторов ароматазы, а потом наблюдение, потому что вы не в группе риска, и для Вас достаточно принимать эндокринотерапию 5 лет.
ВОПРОС: РМЖ, pT1HOMO, 1 ст 3 кл гр, позитивная инвазивная карцинома, прогестерон 8 б, с отрицательным статусом HER2 /neu 1 +, что значат эти символы и мне назначили гормонотерапию. Пошли проблемы, отменили совсем, меня это беспокоит, гормоны принимала 6 мес 1год, 6 мес прошло с операции.
ОТВЕТ: Здравствуйте! В даном случае это гормонозависимая опухоль, но по каким-то причинам у Вас это лечение не пошло, надо разбираться. Удаленно по интернету это сложно сделать, надо менять одну линию эндокринотерапии на другую. Обратитесь к онкологу по месту жительства и вам лечение скорректируют.
ВОПРОС: Добрый день. Подскажите, пожалуйста, поставлен диагноз рак Левой молочной железы, т2nxm0, по иммуногистохимии ER 10% 3 балла, PR 0, Her2/neu-0, ki 67 5%. Один врач назначает тамоксифен, другой нет. Стоит ли принимать и какие прогнозы при таком диагнозе? Возраст 60 лет.
ОТВЕТ: При такой форме рака обычно при Вашей стадии назначается тамоксифен ежедневно, любое назначение делается врачом-онкологом, а иногда специальной онкологической комиссией. В данном случае я бы тоже назначил тамоксифен 20 мг.
ВОПРОС: Добрый день, Виталий Александрович! В очередной раз обращаюсь к Вам за помощью и советом. Напомню, 41 год, 1 ст., люминальный А, С.50.2, Т1N0M0, G2, HER2- отр., КI-67 — 15%, ЭР+8, ПР+7. Сейчас принимаю фарестон. Подскажите, пожалуйста, что можно принимать параллельно с фарестоном, чтобы снизить канцерагенность препарата для организма? И скажите, пожалуйста, что Вы советуете своим пациентам принимать в целях профилактики ОРЗ и ОРВИ в осенне-зимний период? Заранее Вам огромное спасибо и земной поклон.
ОТВЕТ: Здравствуйте! Я своим пацциентам не рекомендую принимать специальные препараты для снижения канцерогенности фарестона, я не считаю, что он канцерогенен, а в зимнее время для лечения ОРВИ использовать обычную терапию, запретов нет. Также вы можете использовать прививки для профилактики ГРИППА
ВОПРОС: Здравствуйте, Виталий Александрович. У меня в феврале 2019г .нашли образование в молочной железе 9.2мм с нервными контурами.Трепан- биопсия гистология инвазивный протоковый рак молочной железы. HER2-отрицательный. ER -7б, RP- 7б, Ki 67- 27% -люминальный тип В. Мне сделали операцию по удалению груди, потом 6 курсов химии красной и облучение. После облучения назначили фаристон, золадекс. Мне 42 года и толком при всем лечении мне врачи ничего не объясняли, надо и все. Сейчас у меня месячных нет и приливы страшные. Для чего эти лекарства и нужны ли они мне. Я знаю, что мне 5 лет принимать гормоны это фаристон, а укол в живот, зачем золадекс. Заранее спасибо.
ОТВЕТ: Здравствуйте! Предположительно возникновением Вашего рака стало воздействие гормонов эстрогенов, а они выделяются многими органами в нашем организме, надо это убрать, воздействуя на гипофиз уколом Золадекса, это я в кратце рассказал!!!! Все другие препараты — фаристон- он воздействует на рецепторы куда может оседать эстроген, и тем самым фаристон блокирует эти рецепторы. Принимайте препараты и слушайте своего доктора.
ВОПРОС: Меня интересует профилактика остеопороза при приеме фемары.
ОТВЕТ: Прием препаратов Кальция курсом 1 раз в год или введение других более глобальных препаратов, например, препаратов резорбции костной ткани, но все по согласованию с Вашим врачом.
ВОПРОС: Здравствуйте! Виталий Александрович, назначили тамоксифен. Можно ли его принимать при миоме матки. Не будет ли она расти?
ОТВЕТ: Здравствуйте! Принимать можно и миома матки не будет увеличиваться в размерах, а эндометрий может расти и поэтому в данном случае надо наблюдаться у гинеколога на фоне приема тамоксифена.
ВОПРОС: Принимала Анастрозол 3 года, перерыв полгода, можно начать прием препарата снова?
ОТВЕТ: Здравствуйте! При таком большом перерыве в приеме анастрозола нет смысла. И почему у Вас был перерыв?Возможно просто продолжить наблюдение, согласуйте это со своим онкологом.
ВОПРОС: Здравствуйте, 1,5 года назад удалили левую грудь. Была химиотерапия до и после операции, затем облучение, сейчас принимаю тамоксифен почти год. Диабет 2 типа (метформин 1500). За последние полгода сильно ушел вес, почти 20кг. В побочных действиях тамоксифена указан набор веса, а у меня наоборот. Эндокринолог говорит, что индивидуальная реакция организма.
ОТВЕТ: Здравствуйте! Это возможно и я думаю, что это лучше, чем набирать вес. Прием тамоксифена не должен сказываться на Вашем сахарном диабете, поэтому спокойно принимайте данный препарат — метформин.
ВОПРОС: Виталий Александрович, добрый день. В очередной раз обращаюсь к Вам с вопросом. Напомню, 42 года, рмж , 1 стадия, люминальный А. Четвертый месяц принимаю фарестон. Сдала очередные анализы: РЭА, Са 15-3, СА 125 — в норме. А эстрадиол (8 день цикла) при норме 46,00 — 607,00 пМоль, — у меня 3 289,00 — превышение больше, чем в пять раз. С чем, на Ваш взгляд, это связано? Фарестон не действует или имеет обратное действие. Заранее огромное спасибо.
ОТВЕТ: Здравствуйте! Причин может быть много, этот препарат, конечно, действует, другое дело возможно он может оказывать и другие эффекты, он же не исследовался у женщин с сохраненным циклом, в аннотации к препарату написано, что он должен использоваться у женщин в постменопаузе. В данном случае вам надо разбираться с Вашим лечащим врачом.
ВОПРОС: Здравствуйте. Что лучше тамоксифен или торемифен?
ОТВЕТ: Здравствуйте! В данном случае нельзя сравнивать два препарата, потому что они назначаются в разных линиях лечения. Но торемифен переносится наиболее мягче, но препарат дороже. Хотя я лично очень люблю тамоксифен и торемифен оставляю на исключительные случаи.
ВОПРОС: Здравствуйте! С 18 июля 2019 года начала принимать тамоксифен-гексал. Теперь в аптеке выдали веро-тамоксифен. Скажите, пожалуйста, может ли данная замена привести к каким-либо последствиям?
ОТВЕТ: Здравствуйте! Замена препарата в данном случае не скажется на Вашем здоровье, потому что это один и тот же препарат, просто разные производители.
ВОПРОС: Добрый день, Виталий Александрович. В очередной раз обращаюсь к Вам за помощью и советом. Напомню, 42 года, в 2018г. был поставлен диагноз рмж, 1 стадия, люминальный, тип А, С.50.2, Т1N0M0, G2, HER2- отр., КI-67 — 15%, ЭР+8, ПР+7. Проведена мастэктомия радикальная по Маддену справа, через месяц поставлен имплант. Назначена гормонотерапия — фарестон. Недавно сдала анализ на эстрадиол, и он высокий, выше нормы в 2 раза. Подскажите, не поздно ли (через год после операции) назначать золадекс к тамоксифену? Не ухудшит ли золадекс качество моей жизни ? И подскажите, пожалуйста, анализы на какие гормоны необходимо сдать, чтобы посмотреть на свой гормональный статус в свете гормонотерапии? Заранее Вам огромное спасибо и низкий поклон за Вашу работу.
ОТВЕТ: Здравствуйте! Отключение яичников актуально даже через год, в данном случае у вас функционируют яичники в обычном режиме и эти показатели говорят об этом. Пр выключении яичников у Вас наступит менопауза и будете себя чувствовать как в менопаузе с приливами, но это все во благо вашему здоровью, данное лечение назначается местной онкологической комиссией.
ВОПРОС: В 2015 г мастэктомия левой груди, химиотерапия, гормонозависимая опухоль, герцептин. В 2019 г началась cin3 шейки матки.Удалила матку и яичники. Гистология ds: cin 3 цервик канала.Менопауза с 2016г. ,принимаю тамоксифен. Вопрос: после удаления матки и придатков мне продолжать принимать тамоксифен?
ОТВЕТ: Здравствуйте! Этот вопрос обсудите с Вашим гинекологом, а вообще рак шейки матки не имеет отношения к РМЖ и к приему Тамоксифена, и продолжить прием возможно дальше, если есть сомнения, то можно перейти на анастрозол.
ВОПРОС: Добрый вечер. У меня рак молочной железы 8522\3 С50.4 рТ1сN0m0 1А ст.3 кл.гр. Эр(+), Пр(+) Her2 eu0. После резекции назначили лучевую терапию, после которой надо 5 лет принимать тамоксифен. У меня миома матки 44х40,5х42,3 мм субсерозный узел на широком основании. Можно мне при таком диагнозе принимать тамоксифен?
ОТВЕТ: Здравствуйте! Принимать можно, но лучше это обсудить с онкогинекологом, возможно, это потребует хирургического лечения или перевода на ингибиторы ароматазы.
ВОПРОС: Здравствуйте, у меня эстрогенозависимый РМЖ, прошла операцию и 6 химий, назначена антигормональная терапия, УЗИ показало эндометрий 6,5, что делать чтоб он он не увеличивался, мне 59 лет.
ОТВЕТ: Здравствуйте! В принципе ничего не сделать! Просто наблюдать, тем более это не критический уровень!Наблюдайтесь у гинеколога по месту жительства.
ВОПРОС: Здраствуйте, принимают ли тамоксифен между курсами химиотерапии?
ОТВЕТ: Здравствуйте! Во всех международных рекомендациях тамоксифен принимается после химиотерапии, в промежутках химиотерапии тамоксифен не принимают!
ВОПРОС: Виталий Александрович, добрый вечер. Моей маме поставлен диагноз Рак молочной железы с Т2NxMo, ст.2, гр2.. Г/А -инвазивная карцинома. ИГХ РЭ-100% РП-95% Кi67-20% Нer2 eu-1(+). Ей назначено принимать летрозол. Подскажите, пожалуйста, может быть вместо летрозола ей лучше принимать препарат Фемара ( швейцария). Может быть у него меньше побочных действий, и он будет легче переноситься? Маме 82 года. Заранее благодарю за ответ.
ОТВЕТ: Здравствуйте! Я не вижу смысла в смене летрозола на Фемару, потому что это одно и тоже, также ингибиторы ароматазы вообще обладают невыраженными побочными эффектами, поэтому продолжите принимать данный препарат в прежнем режиме.
ВОПРОС: Добрый день, Виталий Александрович. Огромнейшее Вам спасибо за Ваш труд и земной Вам поклон. В очередной раз обращаюсь к Вам за помощью и консультацией. Напомню: 42 года, в 2018г. — рмж,1 ст., люмин. А, С50.4, Т1N0M0, G2, HER2- отр., КI-67 — 15%, ЭР+8, ПР+7, радикальная мастэктомия, установлен имплант. Назначена гормонотерапия — 4 месяца на фарестоне. Два месяца назад прошла очередной осмотр у химиотерапевта. Сданы все анализы: общий анализ крови, биохимия крови, моча, УЗИ трех основных зон, онкомаркеры — всё в норме. Только эстрадиол — был превысил норму в пять раз при норме 46,00 — 607,00 пмоль/л — 3 289,00 пмоль/л). Пока химиотерапевт разбирался в ситуации, фарестон я не принимала и через месяц повторно сдала анализ на эстрадиолю. И без приема фарестона — эстрадиол был уже в норме. Виталий Александрович, какого Ваше мнение, — повышение уровня эстрадиола — это реакция организма на прием фарестона? И если начать его принимать снова и будет опять высокий уровень эстрадиола — справится ли препарат со своей прямой задачей? Что бы Вы порекомендовали своим пациентам в сложившейся ситуации? Заранее огромное Вам спасибо.
ОТВЕТ: Здравствуйте! В данном случае Вы принимаете антиэстроген и действие данного препарата не влияет на его выработку, а действие направлено на подавление специальных рецепторов от эстрогенов, что данные препараты и делают, поэтому я бы вообще не учитывал уровень эстрогенов, вы же не ингибиторы ароматазы принимаете. В аннотации к Фарестону сказано, что данный препарат показан у женщин в менопаузе, а у женщин с сохраненным циклом этот препарат не зарегистрирован. Возможно лучше перейти на тамоксифен. Обсудите данный вопрос со своим лечащим врачом.
ВОПРОС: Здравствуйте. Мне 35 лет. В октябре 2019г. проведена онкопластическая резекция левой молочной железы с подмышечной лимфаденэктомей слева. По результатам ихг: PR 7, ER 8, Her-2 отриц., Ki-67 менее 5%. Стадия Т1N1M0. Задет 1 лимфоузел. Показана лучевая терапия и гормонотерапия (золадекс+тамоксифен 0,2) на 5 лет. Как вы считаете, лечение правильное?
ОТВЕТ: Здравствуйте! С данной схемой лечения абсолютно согласен, так как основной вид лечения это ангтигормональная терапия, потому что это люминальный тип А рака молочной железы. В 35 лет необходимо выключение функции яичников при назначении тамоксифена.
ВОПРОС: После 25 дней приема тамоксифена увеличился эндометрий с нормы до 7-8 мм, болит низ живота и появились светлые выделения. Один гинеколог рекомендует пропить 10 дней норкалут, чем вызвать менструацию,которой нет уже 10 лет, сделать снова узи органов малого таза и посмотреть, уменьшился ли эндометрий, чтобы не делать выскабливание. Другой гинеколог против норкалута, утверждает, что эндометрий сам уменьшится после отмены тамоксифена. Кого слушать?
ОТВЕТ: Здравствуйте! Я согласен со вторым мнением, просто прием Тамоксифена и наблюдение, а 7-8 мм на фоне тамоксифена это совсем мало, наблюдайтесь у гинеколога и принимайте Тамоксифен 20 мг .
ВОПРОС: Здравствуйте, у меня РМЖ , пью таблетки тамоксифен 3 года, гиперплазия эндометрия 18,6. Стоит ли менять таблетки, если у всех такой побочный эффект. Спасибо.
ОТВЕТ: Здравствуйте! Данный вопрос надо обсуждать с гинекологом и решать вопрос о выскабливании эндометрия! Я считаю, что менять тамоксифен пока не надо, очень хороший препарат. Продолжайте прием препарата до последующего увеличения эндометрия. Наблюдайтесь у гинеколога.
ВОПРОС: Здравствуйте! ДИАГНОЗ: ИГХ инфильтрирующая карцинома Grade II молочной железы GATA 3 — положительно Synaptophisin — отрицательно, Chromogranin A — отрицательно, CD 56 отрицательно, ER -100 % слабой экспрессии в клетках опухоли, PR — 70% слабой экспрессии в клетках опухоли, HER2 — отрицательно, Ki67-10%. (43 года). Подкожная мастоэкомия с удалением подмышечных лимофузлов. Мутации генов BRCA1,2 отриц. Химиотерапию не назначали, только гормонотерапия. Местный онколог назначал уколы золадекс (28дн) и тамоксифен 20 мг, я еще проконсультировалась у Питерского онколога, он не видит смысла назначение золадекса при 2 стадии рака. Также я читала, что схема золадекс+тамоксифен в результате исследований не показала более эффективной, чем просто тамоксифен, и сейчас такая схема по международным нормам не назначается. Хотела услышать Ваше мнение, можно ли обойтись одним тамоксифеном, золадекс очень снижает качество жизни. Заранее Благодарю.
ОТВЕТ: Здравствуйте! Такая схема лечения существует (Золадекс и Тмоксифен ). Она эффективна, просто назначать сразу же Золадекс с ингибиторами ароматазы не совсем корректно, поэтому сначала Тамоксифен с Золадексом, а затем переходят на ингибитры с Золадексом , потому что менопауза наступает на фоне Золадекса. Также в Вашем случае можно и в монорежиме принимать Тамоксифен без уколов Золадекса. Многие клинические исследования все-таки показали преимущество выключения яичников и даже со второй стадией. Я бы все-таки оставил Вас на Золадексе хотя бы на два года.
ВОПРОС: Добрый день. Мне 64 года. В феврале 2014 была проведена двухсторонняя мастэктомия, диагноз: инфильтрирующая протоковая карцинома левой молочной железы T1N0M0 1ст. и инфильтрирующая дольковая карцинома 2а ст. правой молочной железы после комбинированного лечения в 2002 году. Рецидив: Метастаз в 1 подмышечный лимфоузел. После операции была проведена химиотерапия, затем в качестве гормонотерапии назначен прием анастрозола в течении 5 лет. Я пропила его уже 5 лет. Вопрос: надо ли мне продолжить лечение анастрозолом?
ОТВЕТ: Здравствуйте! Прием 5 лет Анасторозола достаточно, больше Вам не надо принимать этот препарат, но по всем правилам отмена препарата идет через маммологический консилиум, так как Вы должны пред этим быть обследованы для исключения метастазирования.
ВОПРОС: Здравствуйте, Виталий Александрович. Принимаю анастрозол вечером, можно ли перенести прием на утро и как лучше это сделать. Спасибо.
ОТВЕТ: Здравствуйте! Никаких сложностей !Просто начинаете принимать утром! Так можно.
ВОПРОС: Здравствуйте! У меня синхронный рак молочных желез. По левой 3а стадия, а по правой 1 стадия. Проведен курс химиотерапии (8 химий) которые прекратили регулярные месячные (мне 51 г). Сейчас проведена лучевая на левую грудь, через месяц будет на правую. При этом уже 3 раза через 28 дн. вводился Золодекс. А месяц назад начала принимать Анастразол. В настоящее время под Новый год не оказалось Золодекса в 2-х местах, где я принимаю лечение. Очень боюсь, что могут вернуться месячные. Можно ли в период отсутствия Золодекса принимать Анастразол не по 1 мг в день, а более, чтобы месячные не возобновились?
ОТВЕТ: От увеличения дозы Анастрозла месячные не прекратятся, а наоборот могут начаться!!! Вместо Золадекса можно колоть Диферелин или аналоги! В системе ОМС такого не бывает, чтобы для пациента не было Золадекса или Диферелина. На крайний случай, если вы все-таки лечитесь не в ОМС системе, то купите сами себе!
ВОПРОС: Здравствуйте! Мне 53 года. В 2010 году была операция по поводу РМЖ, Т2N3М0 гормонозависимая, химиотерапия 6 курсов FAC, лучевая терапия. Прием тамоксифена 8 месяцев, гистерэктомия, затем до сегодняшнего дня прием Фемара, по данным обследований без прогрессирования. Онколог в поликлиннике не рекомендует дальнейший прием Фемары, говорит что уже достаточно, т.к. стандартный срок приема 5 лет. Как вы считаете нужно ли продолжать дальнейший прием? В замен ничего не назначили.
ОТВЕТ: Здравствуйте! По международным стандартам Вам необходимо прекратить прием Фемары.
ВОПРОС: Доброго времени суток! Мне 43 года онкология 1 первой стадии. Подскажите, пожалуйста, можно ли поменять время приема анастрозола с вечера на утро и как лучше это сделать.
ОТВЕТ: Здравствуйте! Вы смело можете перейти на утренний прием — просто начните принимать анастрозол утром.
ВОПРОС: Здравствуйте, Виталий Алексеевич! Спасибо большое за ответ! У меня еще вопрос. Если остаться на золадексе, то через сколько надо заменить тамоксифен на ингибиторы ароматозы. Я уже уколола два укола золадекса, через две недели третий укол, пью пока томаксифен, нужно уже переходить на ингибиторы ароматазы? Или надо сдать какие-то анализы, чтобы проверить наступила ли менопауза. Менструация была после первого укола, ну очень скудная и раньше на две недели. Сейчас ничего нет. Посоветуйте, пожалуйста, какие препараты лучше принимать из ингибиторов ароматозы с дозировкой, и как переходить на томаксифен через два года после прекращение золадекса, (сейчас мне 43 года). Заранее благодарю за ответ. Еще хотела написать перед приемом гормонотерапии сдавала гормоны — эстрадиол и прогестерон был в норме.
ОТВЕТ: Здравствуйте! Не имеет значения какой препарат из ингибиторов ароматазы принимать! Чтобы перейти на ингибиторы надо сдать анализ на менопаузу, а в частности эстрадиол и ФСГ. Вы можете в принципе сейчас переходить на ингибитры! В любом случае надо согласовывать переход на ингибиторы с лечащим врачом по месту жительства.
ВОПРОС: День добрый, мне 38, хожу в спортзал, но масса не набирается совсем, ранее 15 лет назад была язва ДПК, также имеется синдром Жильбера о чем узнал после 30 лет, хотя на себе не испытаю не каких симптомов, хотя билирубин относительно высокий. Хотел узнать можно ли принять всего одну таблетку Тамоксифена, в целях повышения тестостерона и соответственно массы, будет ли хоть минимальный результат? К слову курсом не хочу принимать, опасаюсь.
ОТВЕТ: Здравствуйте! Прием одной таблеки Тамоксифена не вызовет подъем тестостерона, а длительный прием может Вас превратить в женщину. Делайте выводы. Это очень опасно для здоровья. Зачем вам это? Вам 38 лет и Вы здоровы! Наслаждайтесь жизнью.
ВОПРОС: Здравствуйте! У мамы РМЖ с метастазами, прошли первую химиотерапии и назначили тамоксифен по 20 мг в день, на днях сдали анализы для 2-ой химиотерапии, и она решила пока 3 дня не принимать тамоксифен, боясь за плохие показатели. Можно ли не принимать?
ОТВЕТ: Следуйте строго рекомендациям своего лечащего врача и только при условии всех рекомендаций вы сможете достичь хорошего результата в лечении.
На прочтение статьи –
3 хвилини
Летрозол — это препарат, используемый для лечения рака молочной железы у женщин в Израиле, переживших менопаузу.
Вы также можете услышать, что Letrozol называется Femara. Существует ряд других марок летрозола, все из которых содержат одну и ту же дозу препарата.
Мужчинам с раком молочной железы можно давать летрозол, хотя чаще используется другой препарат, называемый тамоксифен.
Как работает летрозол?
Летрозол работает, уменьшая количество эстрогена, вырабатываемого в организме.
Некоторые виды рака молочной железы стимулируются к росту гормоном эстрогеном. Они известны как положительные рецепторы эстрогена или ER+ рак молочной железы.
Летрозол относится к группе препаратов, называемых ингибиторами ароматазы.
Для кого он подходит
Летрозол подходит для женщин, которые прошли через менопаузу и у которых рак молочной железы является положительным рецептором эстрогена.
Иногда летрозол дают вместе с препаратом под названием гозерелин (Золадекс) женщинам, которые еще не прошли через менопаузу.
Если рак является отрицательным рецептором гормона, то летрозол не принесет никакой пользы.
Когда применяется летрозол
Фемара обычно дают после операции, чтобы снизить риск возвращения или распространения рака молочной железы.
Если пациентка проходит химиотерапию или лучевую терапию, ваш специалист скажет вам, когда лучше всего начать прием летрозола.
Иногда летрозол может быть использован в качестве первого средства лечения рака молочной железы, например, когда операция не подходит или должна быть отложена. В онкоцентре Ихилов (Израиль, Тель-Авив) летрозол иногда дают перед операцией, чтобы уменьшить крупную опухоль молочной железы.
Фемара также может быть использован для лечения рецидивирующего рака молочной железы. Его также можно давать для лечения рака молочной железы, который распространился на другую часть тела.
Как долго потребуется принимать летрозол?
Это будет зависеть от индивидуальных обстоятельств, но летрозол обычно принимают в течение 5-10 лет.
Некоторые люди начинают принимать летрозол после нескольких лет приема гормонотерапевтического препарата тамоксифен.
Если пациентка принимает летрозол для лечения рака молочной железы, который вернулся или распространился на другую часть тела, она обычно принимаете его до тех пор, пока он держит рак под контролем.
Остановка летрозола
Ваша медицинская команда в онкоцентре Ихилов скажет, когда прекратить прием летрозола. Вам не нужно будет прекращать принимать его постепенно.
Некоторые люди беспокоятся о прекращении лечения, но есть доказательства того, что летрозол продолжает снижать риск возвращения рака молочной железы в течение многих лет после того, как его перестают принимать.
Однако отказ от приема препарата в течение рекомендованного времени может увеличить риск возвращения рака молочной железы. Если вы думаете о прекращении приема летрозола по какой-либо причине, сначала поговорите со своим специалистом. Иногда можно перейти на другой гормональный препарат.
Гормональная терапия является очень распространенным методом лечения вторичного рака молочной железы, и многие люди принимают ее в течение длительного времени. Если летрозол перестает работать, ваш специалист может назначить другой гормональный препарат.
Пройти лечение рака молочной железы в Израиле
Как происходит прием препарата?
Летрозол принимают в виде таблетки один раз в день, с пищей или без нее. Лучше всего принимать его в одно и то же время каждый день.
Если пациентка пропустила дозу, не нужно принимать дополнительную дозу на следующий день. Уровень препарата в организме останется достаточно высоким со вчерашнего дня.
Прием летрозола с другими препаратами
Если вы принимаете какие-либо другие предписанные или безрецептурные лекарства, проконсультируйтесь с лечащей командой или фармацевтом, можете ли вы принимать их вместе с летрозолом.
Не принимайте другие препараты, содержащие эстроген, такие как заместительная гормональная терапия, во время приема летрозола, так как это может повлиять на его эффективность.
Первый шаг к выздоровлению вы можете сделать прямо сейчас. Для этого заполните заявку – и в течение 2 часов с вами свяжется один из наших врачей.
Либо позвоните по телефону:+972-3-376-03-58 в Израиле и +7-495-777-6953 в России.
Введение
Рак молочной железы (РМЖ) занимает первое место в структуре онкологической заболеваемости женского населения во всем мире. По данным IARC, в мире ежегодно регистрируют более 1 млн женщин с впервые выявленным РМЖ и каждый год более 600 тыс. больных погибают от РМЖ [15]. Аналогичная тенденция наблюдается в Европе: ежегодно регистрируется около 250 тыс. новых случаев РМЖ, от которого умирают около 60 тыс. больных [11].
Рак молочной железы (РМЖ) занимает первое место в структуре онкологической заболеваемости женского населения во всем мире. По данным IARC, в мире ежегодно регистрируют более 1 млн женщин с впервые выявленным РМЖ и каждый год более 600 тыс. больных погибают от РМЖ [15]. Аналогичная тенденция наблюдается в Европе: ежегодно регистрируется около 250 тыс. новых случаев РМЖ, от которого умирают около 60 тыс. больных [11].
В Российской Федерации, по данным Госкомстата, за последние годы также наблюдается рост заболеваемости РМЖ. Так, в 2005 году число женщин с впервые установленным диагнозом РМЖ составило 49500 (61,1 на 100 тыс. женского населения), причем пик заболеваемости приходится на наиболее социально активный возраст (40–60 лет) [21].
Среди женщин с впервые выявленным РМЖ более чем в 60% диагносцируют I–II стадии заболевания [22]. Преобладающее большинство этих больных после завершения хирургического этапа лечения нуждается в проведении адъювантной лекарственной терапии. Одними из основных критериев выбора метода лекарственной терапии (использование цитостатиков, средств гормонотерапии и трастузумаба) служит наличие или отсутствие экспрессии рецепторов эстрогенов, прогестерона и Her2–new в ткани опухоли, а также состояние менструальной функции у женщины. Перечисленные факторы являются не только прогностическими, но и предсказательными в отношении чувствительности опухолевых клеток к тому или иному виду лечения (и, в частности, гормонотерапии).
До настоящего времени ингибиторы ароматазы третьего поколения служат краеугольным камнем гормонотерапии метастатического рака молочной железы, а сегодня все шире используются для проведения адъювантной терапии у больных операбельным раком молочной железы в менопаузе. Последнее стало возможным после анализа результатов трех крупных рандомизированных исследований, показавших, что использование ингибиторов/инактиваторов ароматазы третьего поколения (анастрозола, летрозола, экзаместана в монорежиме или последовательно) после завершения 2–5 лет терапии тамоксифеном увеличивает длительность безрецидивного периода в сравнении с использованием тамоксифена [1,4,16].
Полученные данные кардинально изменили подходы к адъювантной гормонотерапии больных раком молочной железы в менопаузе.
Современные принципы адъювантной гормонотерапии больных РМЖ были сформулированы на совещании экспертов, состоявшемся в марте 2007 года в St. Gallen. А именно:
• адъювантная терапия тамоксифеном в течение 5 лет в настоящее время не является «золотым стандартом»;
• альтернатива тамоксифену – использование ингибиторов ароматазы;
• оптимальная длительность адъювантной терапии составляет 5–10 лет;
• назначение цитостатиков и гормонотерапии должно осуществляться последовательно [9].
Тем не менее в различных странах мира, в том числе Российской Федерации, в рекомендациях по проведению адъювантной гормонотерапии больным гормоночувствительным РМЖ в менопаузе по–прежнему присутствует тамоксифен [25].
Изменение ранее существовавшей клинической практики проведения адъювантной терапии у больных РМЖ в менопаузе вызвало целый ряд вопросов у клиницистов:
• Какому из препаратов отдать предпочтение?
• В каком режиме рекомендовать проведение адъювантной терапии:
– монотерапия ингибиторами ароматазы?
– последовательное назначение ингибиторов ароматазы после завершения 2–3 лет терапии тамоксифеном?
– или же назначение ингибиторов ароматазы последовательно после завершения 5 лет терапии тамоксифеном?
• И, наконец, отличаются ли различные ингибиторы ароматазы по показателям эффективности и безопасности? Имеется ли между ними сходство и различие?
Очевидно, что для окончательного суждения о преимуществах или недостатках того или иного препарата и режиме его назначения, эффективности и безопасности терапии, сходстве и различиях между ингибиторами/инактиваторами ароматазы необходимы дальнейшие, многолетние исследования. На основании информации, доступной сегодня, ответа на большинство из этих вопросов пока нет.
В сложившейся ситуации любое различие, в том числе по показателю «стоимость/эффективность», может оказаться существенным аргументом в пользу вы-бора того или иного лекарственного препарата и режима его назначения. Поскольку даже при условии сходной розничной цены ингибиторов/инактиваторов ароматазы и равной противоопухолевой эффективности, различные режимы терапии могут отличаться между собой по показателю «стоимость/эффективность».
Теоретически можно предположить, что любой из препаратов равно эффективен в режиме адъювантной терапии при гормоночувствительном РМЖ, любой режим терапии (моно или последовательно) в равной мере снижает абсолютный риск рецидива и риск смерти, и нет различий в побочных эффектах между лекарственными препаратами.
Если обратиться к результатам ранее завершенных исследований, нестероидные ингибиторы ароматазы третьего поколения (анастрозол и летрозол) и стероидный инактиватор (экзаместан) снижают уровень эстрогенов в сыворотке крови более чем на 98%, причем наибольшей активностью из них обладает летрозол [8,26].
Наиболее крупное клиническое исследование, в котором предпринята попытка ответить на вопрос, является ли использование летрозола (Фемара) в ранней адъювантной терапии у женщин с гормоночувствительным РМЖ в менопаузе эффективной альтернативой тамоксифену – исследование BIG 1–98 [16]. Это клиническое исследование проведено в соответствии с принципами доказательной медицины (рандомизированное, многоцентровое, с использованием двойного слепого метода и значительным числом клинических наблюдений). Характеристики пациенток, принявших участие в этом исследовании, репрезентативны примерно для 2/3 больных РМЖ, что позволяет рассматривать его результаты как доказательные.
Основной целью исследования BIG 1–98 являлась оценка безрецидивной выживаемости, определенной как время от момента рандомизации до возникновения любого из следующих событий: рецидив в той же молочной железе; рецидив в области послеоперационного рубца на грудной стенке; метастазы в региональные лимфатические узлы (внутримаммарные, аксилярные); отдаленные метастазы (включая ипсилатеральные надключичные); выявление инвазивного рака в другой молочной железе; развитие других злокачественных опухолей; смерти, без предшествующего события, обусловленного злокачественной опухолью.
Вторичными целями исследования являлись оценка: общей выживаемости; выживаемости без симптомов проявления болезни; выживаемости в группе больных с отдаленными метастазами (исключены больные с локальными и регионарными рецидивами, контрлатеральным РМЖ); времени до развития отдаленных метастазов (исключены больные с локальным рецидивом и другими злокачественными опухолями); безопасности терапии; выживаемости без отдаленных метастазов.
Сравнительный анализ результатов исследования BIG 1–98 (n=8010; медиана наблюдения – 51 месяц) свидетельствует о высокой эффективности летрозола (Фемара) в ранней адъювантной терапии ЭР–позитивного РМЖ у женщин в менопаузе [2]. У больных, получавших в ранней адъювантной терапии летрозол, снижение относительного риска рецидива составило 18% (hazard ratio: 0,82, 95% CI: 0,71–0,95, р=0,007). Безрецидивная (бессобытийная) выживаемость при терапии летрозолом была существенно выше (84,0%), чем при назначении тамоксифена (81,1%) (рис. 1). Отличалась и частота событий, обусловленных заболеванием, в лечебных группах. Так, число неудач терапии (352) при использовании летрозола было на 3,4% меньше, чем в группе тамоксифена (418) (р=0,0002). Лечение летрозолом позволило сохранить жизнь бо?льшему числу больных РМЖ: 194 (7,9%) летальных исхода в группе летрозола и 211 (8,6%) – в группе тамоксифена (различие – 17 летальных исходов) [2, 7].
В другом крупном исследовании ATAC в аналогичной группе больных соответствующие показатели были хуже (296 летальных исходов в группе анастрозола, 301 – в группе тамоксифена, различие – 5 летальных исходов) [1].
Если и далее сравнивать результаты исследования BIG 1–98 с результатами исследования ATAC (n=6241; медиана наблюдения 68 месяцев), в котором в ранней адъювантной терапии гормоночувствительного РМЖ у женщин в менопаузе использовали анастрозол, то становится очевидно, что летрозол (Фемара) превосходит анастрозол по нескольким показателям, особенно в отношении снижения риска развития отдаленных метастазов, которые, как известно, являются основной причиной смерти больных РМЖ.
При назначении в ранней адъювантной терапии у больных РМЖ летрозол (Фемара) превосходил тамоксифен по времени до развития отдаленных метастазов (hazard ratio: 0,81, р=0,03) и времени до развития рецидива (hazard ratio: 0,78). У больных, получавших в ранней адъювантной терапии летрозол, риск развития отдаленных метастазов снижался на 27%, по сравнению с тамоксифеном. В исследовании ATAC, при использовании анастрозола риск рецидива был ниже на 17%, а риск развития отдаленных метастазов на 16%. При оценке общей выживаемости в исследовании BIG 1–98 снижение риска смерти достигает 9% (Hazrad ratio = 0,91), что втрое превышает аналогичный показатель в исследовании ATAC (3%) [3,10,17].
Анализ в подгруппах (медиана наблюдения – 51 месяц) позволил также установить преимущество использования в ранней адъювантной терапии летрозола, поскольку его эффективность была выше эффективности тамоксифена (рис. 2).
Важно, что использование летрозола у больных РМЖ с метастазами в лимфатические узлы, относящихся к группе высокого риска развития рецидива заболевания, позволило существенно (на 29%) увеличить безрецидивную выживаемость (hazard ratio: 0,77, 95%CI: 0,64–0,92, р=0,004) в сравнении с группой пациенток, получавших тамоксифен. В то же время летрозол был эффективен и при отсутствии метастазов в лимфатические узлы: достигнуто снижение риска развития рецидива на 12% (hazard ratio: 0,88, 95%CI: 0,70–1,10, р=0,26). Кроме того, летрозол более эффективно предупреждал развитие рецидива у больных, ранее получавших химиотерапию (hazard ratio: 0,74, 95%CI: 0,56–0,97, р=0,03) (табл. 1).
Результаты исследования BIG 1–98 при использовании Фемары и тамоксифена в ранней адъювантной терапии РМЖ представлены в таблице 2 [2,3].
Таким образом, анализ результатов исследования BIG 1–98 свидетельствует о преимуществах назначения в ранней адъювантной терапии у больных РМЖ в менопаузе летрозола (Фемара) по показателям эффективности терапии: безрецидивной (бессобытийной) выживаемости, времени до развития отдаленных метастазов, особенно в группе больных с высоким риском развития рецидива (с метастазами в лимфатические узлы) и/или ранее получавших химиотерапию.
Экономическая целесообразность назначения летрозола у больных РМЖ в менопаузе в ранней адъювантной терапии вместо тамоксифена подтверждена в исследованиях, проведенных в различных странах. Однако исследований по фармакоэкономической целесообразности использования летрозола (Фемара) у больных РМЖ в менопаузе в ранней адъювантной терапии в Российской Федерации не проводилось.
Клинико–экономический анализ
Методика исследования. Настоящее сравнительное исследование предпринято для оценки фармакоэкономической целесообразности использования летрозола (Фемара) в ранней адъювантной терапии эстрогенпозитивного РМЖ в Российской Федерации. Для сравнительной оценки экономической целесообразности использования в ранней адъювантной терапии у больных раком молочной железы в менопаузе летрозола (Фемара) в исследовании была предусмотрена оценка коэффициента «стоимость–эффективность» (CER). Полученные данные анализировали в сравнении с аналогичным показателем, рассчитанным для тамоксифена в аналогичной группе больных. В Российской Федерации в качестве сравниваемой конечной оценочной стоимости коэффициента «стоимость–эффективность» используют трехкратную величину валового внутреннего продукта на душу населения Российской Федерации. В настоящей работе использована величина валового внутреннего продукта за предшествовавший исследованию 2006 год. Экономическую оценку затрат выражали в рублях. На момент выполнения расчетов в исследовании курс доллара США составил 25,7 рублей/$.
Для построения фармакоэкономической модели были использованы данные, полученные в многоцентровом рандомизированном клиническом исследовании BIG 1–98, обсуждавшиеся выше. Потребность в хирургическом лечении, лучевой и лекарственной терапии (цитостатики) при развитии рецидива или метастазов рассчитана на основании результатов упомянутого исследования (табл. 2) [2].
В исследовании BIG 1–98, и соответственно фармакологической модели настоящего исследования, медиана длительности адъювантной терапии летрозолом и тамоксифеном у больных РМЖ составила 51 месяц (4,25 года).
Для проведения клинико–экономического анализа разработана модель (алгоритм) принятия возможных решений при развитии рецидива заболевания (рис. 3).
Вероятность развития различных исходов у больных РМЖ во время адъювантной терапии (медиана наблюдения – 51 месяц) была линейно экстраполирована из исследования BIG 1–98 и предусматривала развитие любого из событий, оцениваемых в исследовании BIG 1–98 и обсужденных в настоящей работе выше.
Данные проанализированы для подсчета затрат. Расчет стоимости проводили в два этапа: идентификация ресурсов, используемых в исследовании; соотнесение ресурсов, используемых в исследовании к единице затрат в Российской Федерации.
Источники затрат линейно экстраполированы из исследования BIG 1–98 и, в национальной системе здравоохранения, рассчитаны с учетом «Стандарта медицинской помощи больным со злокачественным новообразованием молочной железы» [25]. Затраты на лечение РМЖ сгруппированы следующим образом: лечение оцениваемыми препаратами; лечение рецидива – хирургическое лечение; химиотерапия; лучевая терапия; гормонотерапия, летальный исход.
Фармакоэкономический анализ предусматривал учет прямых медицинских затрат на адъювантное лечение больных РМЖ и возможных прямых медицинских расходов на лечение рецидивов РМЖ, а дизайн исследования – использование статистических данных и модельных расчетов.
Результаты
После анализа данных исследования BIG 1–98, на основании усредненных розничных цен на лекарственные средства в аптеках города Москвы (по состоянию на 24.04.2007 г.) и прейскуранта на платные медицинские услуги в учреждениях здравоохранения Москвы и Санкт–Петербурга рассчитана средняя стоимость затрат на адъювантную терапию Фемарой или тамоксифеном и затрат на лечение РМЖ в случае развития рецидива [20,23,24].
Стоимость сравниваемых лекарственных средств. Стоимость летрозола (Фемара) рассчитана на основании данных о розничной цене препарата, полученных при анализе предложений в сети аптек в городе Москве (103 аптеки) по состоянию на 24.04.2007 г. Аналогично рассчитана стоимость тамоксифена (г. Москва, 164 аптеки, также по состоянию на 24.04.2007 г.) [20]. На основании усредненных розничных цен рассчитана средняя стоимость препаратов, стоимость лечения в сутки и стоимость 51 месяца адъювантной терапии (табл. 3).
Стоимость медицинских услуг в случае развития рецидива рассчитана с учетом «Стандартов медицинской помощи больным со злокачественным новообразованием молочной железы» (табл. 4).
Сравнительный анализ стоимости ранней адъювантной терапии тамоксифеном и летрозолом (Фемара) у больных раком молочной железы. Стоимость ранней адъювантной терапии летрозолом (Фемара) и тамоксифеном при медиане наблюдения 51 месяц и затрат на отдельные виды медицинских услуг у больных РМЖ при развитии рецидива представлены в таблице 5.
Из анализа данных таблицы 5 следует, что использование в ранней адъювантной терапии Фемары при медиане наблюдения 51 месяц (4,25 года) позволяет снизить прямые затраты на наиболее ресурсоемкие услуги здравоохранения, а именно: хирургическое лечение рака молочной железы на 34%; лекарственную терапию (цитостатики) на 18%; лучевую терапию на 13%.
Коэффициент
«стоимость–эффективность»
В исследовании BIG 1–98 в группе больных РМЖ в менопаузе, получавших в ранней адъювантной терапии Фемару, неудач терапии было на 3,4% меньше, чем при терапии тамоксифеном [7]. Что, с учетом этого показателя, позволяет рассчитать коэффициент «стоимость–эффективность» достижения клинического эффекта (CER) для Фемары по формуле:
4,25-летняя стоимость лечения Фемарой 1 больной 406 669 руб.
CER = ––––––––––––––––––––––––––––––––––––––––– = ––––––––– = 419 246 руб.
Кумулятивная частота неудач 1 – 0,034
Согласно рекомендациям Всемирной Организации Здравоохранения (ВОЗ) коэффициент «стоимость–эффективность» (CER) приемлем, если он не превышает величины валового внутреннего продукта, рассчитанной на душу населения более чем в 3 раза. Такой метод лечения признается затратно–эффективным и его внедрение и финансирование одобряется правительством. Напротив, внедрение нового метода лечения считается неоправданным с экономической точки зрения, даже при наличии убедительных данных о его клинической эффективности и безопасности, если величина CER превышает величину валового внутреннего продукта, рассчитанную на душу населения более чем в 3 раза [19].
По данным Госкомстата Российской Федерации, объем величины валового внутреннего продукта в 2006 году составил 26 781,1 млрд. рублей при численности населения РФ 142,8 млн. человек, в среднем – 187 542 рубля на 1 человека, то есть 187 542 руб. х 3 = 562 628 руб. [21].
Таким образом, на основании данных настоящего фармакоэкономического исследования применение летрозола в ранней адъювантной терапии у больных с эстрогенпозитивным РМЖ в Российской Федерации эффективно и экономически обосновано.
Обсуждение полученных результатов
Анализу фармакоэкономической целесообразности использования в ранней адъювантной терапии РМЖ летрозола (Фемара) посвящено несколько исследований.
Karnon et al. (2005) в сравнительном аспекте оценивали эффективность и экономическую целесообразность использования Фемары (исследование BIG 1–98) или анастрозола (АТАС) в ранней адъювантной терапии РМЖ у женщин в менопаузе в Великобритании [13]. Для оценки использована экономическая модель Маркова, предусматривающая оценку стоимости добавленного года жизни (QALY = quality–adjusted life year) при лечении оцениваемыми препаратами. В исследовании установлено, что стоимость добавленного года жизни для Фемары – ?10,379 (95% CI: ?6,705–?23,574), что ниже стоимости добавленного года жизни для анастрозола – ?11,428 (95% CI: ?6,211–?48,795).
Если сравнивать 5–летнюю эффективность лечения в отношении снижения риска рецидива, обусловленного РМЖ, расчетная стоимость QALY в сравнении с тамоксифеном составила ?6,253 для Фемары и ?7,015 – для анастрозола.
В Великобритании метод лечения признается затратно–эффективным и его внедрение и финансирование одобряется правительством, если стоимость добавленного года жизни составляет ?20,000. Авторы исследования полагают, что в Великобритании использование Фемары в ранней адъювантной терапии у женщин в менопаузе с гормоночувствительным РМЖ не только эффективно, но и экономически более оправдано, чем назначение анастрозола [13].
Delea et al. (2006) также оценивали экономическую эффективность использования тамоксифена, анастрозола и летрозола в ранней адъювантной терапии РМЖ. Для анализа эффективности авторы использовали данные популяционных исследований в США (тамоксифен в сравнении с плацебо) и результаты исследований ATAC (анастрозол в сравнении с тамоксифеном) и BIG 1–98 (летрозол в сравнении с тамоксифеном). Для расчета стоимости добавленного года жизни QALY, с учетом данных о вероятности развития рецидива и побочных эффектов, использована модель Маркова. Стоимость добавленного года жизни (QALY) для Фемары была ниже –$33,536 (95% CI: $20,409 – $70,566), чем для анастрозола – $38,967 (95% CI: $23,826 – $81,904). Авторы полагают, что в США использование Фемары в ранней адъювантной терапии у женщин в менопаузе с гормоночувствительным РМЖ эффективно и экономически более предпочтительно, чем анастрозола ($9647 и $10190 – соответственно 0,29 против 0,26) [6].
По данным канадских исследователей, стоимость QALY при адъювантной терапии Фемарой у больных РМЖ в менопаузе составила $36,807. В Канаде использование метода лечения считается экономически обоснованным, если стоимость QALY составляет $50,000 – $100,000.
Таким образом, по данным всех зарубежных исследователей, стоимость добавленного года жизни (QALY) для Фемары меньше, чем для анастрозола и составляет – $36,807(Канада), ?10,379 и ?11,428 для летрозола и анастрозола, соответственно (UK), в США для летрозола – $33,536 (95% CI: $20,409 – $70,566), для анастрозола – $38,967 (95% CI: $23,826 – $81,904). Причем согласно обзору (Early Adjuvant Breast cancer review, 2006, NICE) эффективность летрозола в сравнении с анастрозолом выше, и его использование экономически более выгодно [5,12].
В настоящем фармакоэкономическом исследовании в Российской Федерации применение летрозола в ранней адъювантной терапии у больных гормоночувствительным РМЖ экономически обосновано, что находится в соответствии с мнением исследователей различных стран, включая США, Великобританию, Канаду.
Заключение
Развитие отдаленных метастазов – наиболее частая причина смерти больных РМЖ, которая ассоциируется с существенным увеличением стоимости лечения заболевания. Как упоминалось выше, пик прогрессирования у больных раком молочной железы приходится на первые 2–3 года после хирургического лечения, причем относительный риск смерти достоверно возрастает при выявлении рака в другой молочной железе (р=0,01), регионарного рецидива (р<0,001), отдаленных метастазов (р<0,001). С экономической точки зрения развитие отдаленных метастазов влечет существенное увеличение затраты на лечение. Так, по данным зарубежных исследователей, стоимость добавленного года жизни при отсутствии рецидива составляет 39000$, при развитии контрлатерального РМЖ – 59000$, регионарных метастазов – 69000$, отдаленных метастазов – 90000$ [14].
Летрозол (Фемара) при использовании в режиме ранней адъювантной терапии у больных РМЖ в менопаузе превосходит эффективность тамоксифена по безрецидивной выживаемости, частоте развития рецидивов (3,4%), времени до развития отдаленных метастазов, особенно у больных, относящихся к группе высокого риска. Применение Фемары позволяет снизить экономические затраты на наиболее ресурсоемкие и экономически затратные методы лечения рецидивов и метастазов РМЖ, а именно:
• хирургическое лечение – на 34%;
• лекарственную терапию (цитостатики) – на 18%;
• лучевую терапию – на 13%.
Таким образом, использование Фемары в ранней адъювантной терапии гормоночувствительного РМЖ у женщин в менопаузе в Российской Федерации является высокоэффективным, безопасным и экономически оправданным методом лечения, поскольку коэффициент «стоимость–эффективность» при назначении Фемары на 25,5% меньше, чем трехкратное значение величины валового внутреннего продукта на душу населения.
В современной адъювантной терапии гормоночувствительного РМЖ летрозол (Фемара) – препарат предпочтительного выбора для проведения ранней адъювантной терапии, особенно у женщин с высоким риском развития рецидива (при наличии метастазов в лимфатические узлы и/или ранее получавших химиотерапию).
Включение летрозола (Фемары) в различные режимы адъювантной терапии РМЖ обосновано как с клинической, так и с экономической точек зрения. Превосходя тамоксифен по эффективности, Фемара позволяет снизить не только прямые расходы на лечение рецидивов (наиболее затратные и ресурсоемкие услуги здравоохранения) но и, кроме того, избежать существенных затрат на госпитализацию больных для проведения хирургического, цитостатического и/или лучевого лечения.
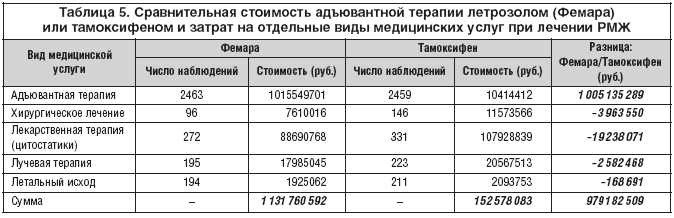
Литература
1. ATAC Trialists’ Group. Results of the ATAC (Arimidex, Tamoxifen, Alone or in Combination) trial after completion of 5 years’ adjuvant treatment for breast cancer. Lancet 2005, 365, 60–62.
2. Coates A.S., Keshavian A., Thurlimann B. et al. Five years of letrozole compared with tamoxifen as initial adjuvant therapy for postmenopausal women with endocrine–responsive early breast cancer: update of study BIG 1–98 // J Clin Oncol. 2007; 25:486–492.
3. Coates AS et al. Presented at: ESMO 2006, Istanbul, Turkey. Abstract 241O.
4. Coombes RC, Hall E, Snowdon CF, et al. The Intergroup Exemestane Study: a randomized trial in postmenopausal patients with early breast cancer who remain disease–free after two to three years of tamoxifen–updated survival analysis. Breast Cancer Res Treat 2004, 88(1), abstr 3.
5. Delea et al. Ann Oncol. 2006;17 (suppl 9):ix107. Abstract 296P.
6. Delea et al. J Clin Oncol. 2006;24(18S):574s. Abstract 10577.
7. Forbes J.F. Data Presented at the 2005 annual Meeting of the American Society of Clinical oncology (ASCO). Orlando, FL, USA, 2005.
8. Geisler et al. J Clin Oncol. 2002; 20:751–757.
9. Goldhirsch A et al. Progress and promise: highlights of the international expert consensus on the primary therapy of early breast cancer 2007. Annals of Oncology 18: 1133–1144, 2007.
10. Howell et al. Lancet. 2005;365:1225–1226.
11. Imai H., Kuroi K., Ohsumi S. et al. Economic evaluation of the prevention and treatment of breast cancer–present status and open issues // Brest Cancer. – 2007; 14 (1): 81–87.
12. Karnon et al. Ann Oncol. 2006;17(suppl 9):ix109. Abstract 295P.
13. Karnon et al. ECCO, 2005. Abstract 341.
14. Lamerato et al. Breast Cancer Res Treat. 2004;88(suppl 1):S104. Abstract 2084.
15. Stewart B., Klrihus P.(2003) World Health Organisation. World Cancer Report. International Agency on Research for Cancer/ IARC Press, Lion,p.p.188–190.
16. Thurlimann BJ, Keshaviah A, Mouridsen H, et al. Letrozole versus Tamoxifen as adjuvant endocrine therapy for postmenopausal women with receptor–positive breast cancer. BIG 1–98: a prospective randomised double–blind phase III study. Proc Am Soc Clin Oncol 2005, abstr 511.
17. Thurlimann et al. N Engl J Med. 2005;363:2747–2757.
18. Update of continuous therapy arms of BIG 1–98 из презентации Alan S. Coates MD for the BIG 1–98 Collaborative Group.
19. WHO Commission on Macroeconomics and Health. Macroeconomics and Health: investing in health for economic development. Report of the Commission on Macroeconomics and Health. Geneva: WHO, 2001.
20. www.medlux.ru, по состоянию на 24.04.2007.
21. Госкомстат РФ, 2006 г. www.gks.ru/wps/portal.
22. Злокачественные новообразования в России в 2005 году. Под ред. В.И. Чиссова. ФГУ МНИОИ им. П.А.Герцена Росздрава, 2007.
23. Прейскурант на медицинские услуги ГКБ им. Боткина, г. Москва, 2007.
24. Прейскурант на медицинские услуги ЦНИИРИ, г. Санкт–Петербург, 2007.
25. Стандарт медицинской помощи больным со злокачественным новообразованием молочной железы. Утв. приказом Министерства здравоохранения и социального развития РФ от 1 декабря 2005г. N 744.
26. Miller WR. Biological rationale for endocrine therapy in breast cancer. Best Pract and Res 2004, 18; 1:32.
Сравнительный фармакоэкономический анализ применения анастрозола, летрозола и экземестана при адъювантной терапии рака молочной железы
Источник: Белоусов Д.Ю., Афанасьева Е.В., Зырянов С.К. Сравнительный фармакоэкономический анализ применения анастрозола, летрозола и экземестана при адъювантной терапии рака молочной железы. // Качественная клиническая практика, №2, 2012 г., стр. 45-55
Скачать статью в pdf: http://www.clinvest.ru/images/parts/pdf/pdf-267.pdf
Введение
Рак молочной железы (РМЖ) – занимает первое место среди злокачественных новообразований у женщин и является одной из главных причин смертности женского населения во всём мире. Заболеваемость РМЖ увеличивается с возрастом. Как правило, опухоли возникают после 35-40 лет, пик заболеваемости регистрируют у женщин в возрасте 60-65 лет [14].
В России в структуре заболеваемости злокачественными новообразованиями РМЖ занимает 1-ое место (18,1%). Распространённость РМЖ в 2011 г. на 100 000 населения – 369,5 человек. В 2011 г. выявлено 57 379 больных РМЖ женщин, из них 55 184 поставлено на учёт. Удельный вес больных с диагнозом, подтверждённым морфологически, от числа больных с впервые в жизни установленным диагнозом РМЖ – 96,6%. Удельный вес больных с опухолевым процессом I стадии от числа больных с впервые в жизни установленным диагнозом РМЖ – 18,5%, II стадии – 46,5%, III стадии – 24,8%, IV стадии – 9,1% [19].
Радикальное лечение РМЖ получило 36 469 женщин [19], в том числе:
- с использованием только хирургического метода – 29,7% случаев,
- только лучевого – 0,4%,
- только лекарственного – 0,0%,
- комбинированного и/ или комплексного (кроме химиолучевого) – 69,5%,
- химиолучевого – 0,5% случаев.
Пятилетняя выживаемость в 2011 г. составила 57,6%. Индекс накопления контингентов больных с РМЖ – 9,5. Одногодичная летальность с момента установления РМЖ – 8,7% [19].
Как уже было сказано выше, среди женщин с впервые выявленным РМЖ в 65% случаев диагностируют I-II стадии заболевания [19]. Преобладающее большинство этих больных, после завершения хирургического этапа лечения, нуждается в проведении адъювантной лекарственной терапии. Одними из основных критериев выбора метода лекарственной терапии (использование цитостатиков, средств гормонотерапии) служит наличие или отсутствие экспрессии рецепторов эстрогенов, прогестерона и Her2-new в ткани опухоли, а так же состояние менструальной функции у женщины. Перечисленные факторы являются не только прогностическими, но и предсказательными в отношении чувствительности опухолевых клеток к тому или иному виду лечения и, в частности, гормонотерапии.
До настоящего времени ингибиторы/инактиваторы ароматазы третьего поколения служат краеугольным камнем гормонотерапии метастатического рака молочной железы, а сегодня всё шире используются для проведения адъювантной терапии у больных операбельным раком молочной железы в менопаузе. Последнее стало возможным после анализа результатов трёх крупных рандомизированных исследований, показавших, что использование ингибиторов/инактиваторов ароматазы III поколения: анастрозола, летрозола, экземестана в монорежиме или последовательно, после завершения 2-5 лет терапии тамоксифеном увеличивает длительность безрецидивного периода в сравнении с использованием тамоксифена [1, 2, 10-12].
Полученные данные кардинально изменили подходы к адъювантной гормонотерапии больных РМЖ в менопаузе.
Современные принципы адъювантной гормонотерапии больных РМЖ были сформулированы на совещании экспертов, состоявшемся в марте 2007 года в St. Gallen. А именно:
-
адъювантная терапия тамоксифеном в течение 5 лет в настоящее время не является «золотым стандартом»;
-
альтернатива тамоксифену – использование ингибиторов/инактиваторов ароматазы;
-
оптимальная длительность адъювантной терапии составляет 5-10 лет;
-
назначение цитостатиков и гормонотерапии должно осуществляться последовательно [4].
Изменение ранее существовавшей клинической практики проведения адъювантной терапии у больных РМЖ в менопаузе вызвало целый ряд вопросов у клиницистов:
-
Какому из препаратов отдать предпочтение?
-
В каком режиме рекомендовать проведение адъювантной терапии:
-
монотерапия ингибиторами/инактиваторами ароматазы?
-
последовательное назначение ингибиторов/инактиваторов ароматазы после завершения 2-3 лет терапии тамоксифеном?
-
или же назначение ингибиторов/инактиваторов ароматазы последовательно после завершения 5 лет терапии тамоксифеном?
-
-
Отличаются ли различные ингибиторы/инактиваторы ароматазы по показателям эффективности и безопасности? Имеется ли между ними сходство и различие?
Если обратиться к результатам ранее завершённых клинических исследований, нестероидные ингибиторы ароматазы III поколения (анастрозол и летрозол) и стероидный инактиватор (экземестан) снижают уровень эстрогенов в сыворотке крови более чем на 98%. Поэтому мы предположили, что любой из препаратов равно эффективен в режиме адъювантной терапии при гормоночувствительном РМЖ, любой режим терапии (моно или последовательно) в равной мере снижает абсолютный риск рецидива и риск смерти, и нет различий в побочных эффектах между лекарственными препаратами.
Очевидно, что для окончательного суждения о преимуществах или недостатках того или иного препарата и режиме его назначения, эффективности и безопасности терапии, сходстве и различиях между ингибиторами/инактиваторами ароматазы необходимы дальнейшие исследования. В современных условиях одним из основных критериев выбора схемы лечения, наряду с клинической эффективностью, переносимостью и безопасностью, является анализ эффективности затрат (cost effectiveness analysis / CEA). Любое различие по показателю «затраты-эффективность» (cost effectiveness ratio / CER) может оказаться существенным аргументом в пользу выбора того или иного лекарственного препарата и режима его назначения, поскольку даже при условиях схожей противоопухолевой эффективности ингибиторов/инактиваторов ароматазы, различные режимы терапии могут отличаться между собой по показателю CER.
В настоящее время в Российской Федерации требуется проведение оценки клинической и экономической эффективности медицинских технологий (ОМТ). Это является результатом осознания того, что решения, связанные с распределением ресурсов в стране с бюджетной системой финансирования здравоохранения, должны быть подкреплены информацией о стоимости лечения и об относительной эффективности медицинского вмешательства.
В данной статье отражены результаты анализа эффективности затрат, сравнивающего альтернативные схемы гормональной терапии рака молочной железы ингибиторами/инактиваторами ароматазы.
Цель исследования
Целью данной работы являлась сравнительная фармакоэкономическая оценка терапии анастрозолом, летрозолом и экземестаном пациенток с I-II стадиями РМЖ в условиях российской системы здравоохранения.
Задачи исследования
- Разработка методологии фармакоэкономического исследования
- Анализ литературных источников
- Разработка Марковской модели для оценки исходов лечения
- Разработка модели принятия решений
- Определение критериев исследуемой популяции пациентов
- Выбор препаратов сравнения по классу, МНН, торговому названию, и определение их стоимостной характеристики
- Расчёт прямых медицинских затрат на медицинскую помощь больным РМЖ:
- первичную диагностику
- дальнейшее наблюдение
- консервативную хирургическую помощь или мастэктомию
- химиотерапию
- лучевую терапию
- летальный исход
- Описание сравниваемых альтернативных стратегий лечения
- Сравнение 5-летней экономической эффективности альтернативных стратегий
Популяция больных
Женщины, находящиеся в менопаузе, с I-II стадией рака молочной железы, находящиеся на гормональной адъювантной терапии ингибиторами/инактиваторами ароматазы.
Методология исследования
При проведении фармакоэкономического анализа был использован применяемый в РФ Отраслевой стандарт «Клинико-экономического исследования» [17]. Были использованы следующие методы экономического анализа:
- Марковское моделирование
- Анализ принятия решения (построение «древа» решений)
- Расчёт прямых медицинских затрат на лечение и терапию препаратами сравнения
- Анализ эффективности затрат
- Дисконтирование
- Анализ экономической целесообразности
- Анализ чувствительности результатов
Марковское моделирование. Для прогнозирования вероятности развития событий при лечении РМЖ и ассоциированных с ними прямых медицинских затрат за определённый период времени при использовании различных терапевтических стратегий была разработана Марковская модель, которая выбрана из-за длительного течения РМЖ. Её структура позволяет следующее:
- изучить несколько альтернативных стратегий лечения;
- рассмотреть разные периоды времени;
- оценить риски развития событий;
- провести дисконтирование полученных результатов.
Модель представлена на рис. 1 и табл. 1, продолжительность цикла модели 1 год (всего 5 циклов), включает следующие состояния [5]:
- отсутствие прогрессирования заболевания;
- развитие местно-регионарных рецидивов;
- развитие рака контралатеральной молочной железы;
- ремиссия после лечения местно-регионарных рецидивов или рака контралатеральной молочной железы;
- появление отдалённых метастазов;
- смерть в результате прогрессирования заболевания;
- смерть от других причин.
При построении модели было сделано допущение о том, что при развитии местно-регионарного рецидива или рака контралатеральной молочной железы в этом состоянии пациентки находились на протяжении 1 года (т.е. 1 цикла в модели), после чего происходил переход в другие клинические состояния (стабилизация состояния на фоне лечения, развитие отдалённых метастазов или смерть от причин, не связанных с течением заболевания) [5].
Рис. 1
Марковская модель прогрессирования рака молочной железы
Таблица 1
Матрикс Марковской модели рака молочной железы с переходом из одного состояния в другое
Для проведения клинико-экономического анализа разработан алгоритм принятия возможных решений при развитии рецидива заболевания (рис. 2).
Рис. 2
Алгоритм принятия возможных решений при развитии рецидива РМЖ («древо» решений)
Стоимость прямых медицинских затрат. По Стандарту оказания медицинской помощи больным со злокачественными новообразованиями молочной железы [20] были рассчитаны прямые медицинские затраты на использование медицинских ресурсов при оказании медицинской помощи больным РМЖ на:
- первичную диагностику (допущение: мы не брали в расчёт, т.к. проводится у всех больных);
- наблюдение (допущение: мы не брали в расчёт, т.к. проводится у всех больных);
- консервативную хирургическую помощь или мастэктомию;
- химиотерапию;
- лучевую терапию;
- летальный исход.
Прямые медицинские затраты. Для расчётов ценовых показателей стоимости медицинских услуг мы использовали Прейскурант на оказание медицинских услуг клиник ПМГМУ им. И.М. Сеченова [18], ФГБУ «Российский научный центр рентгенорадиологии» за 2012 г. г. Москва [24]; цены на препараты сравнения были рассчитаны как средние розничные в аптеках г. Москвы [13].
Показатель эффективности затрат. Так как у сравниваемых стратегий разные показатели эффективности и затрат был проведён анализ показателя эффективности затрат (cost—effectiveness ratio – CER). Наиболее фармакоэкономически приемлемым считался наименьший показатель CER, который рассчитывался по следующей формуле:
CER = DC ÷ Ef, где
DC – прямые медицинские затраты (равно CoI – стоимости болезни);
Ef – эффективность (действенность), выраженная в показателях безрецидивной выживаемости (DFS – disease—free survival).
Вероятность перехода в состояние и эффективность препаратов. Вероятность перехода из одного состояния здоровья в другое и эффективность сравниваемых препаратов оценивалась по результатам контролируемых клинических исследований: ATAC [10, 11], ARNO 95 [6], BIG 1-98 [1, 2, 12], IES [3], на которых и обосновывался данный модельный фармакоэкономический анализ.
Вероятность перехода из одного состояния в другое
Исследование ATAC – оценка эффективности терапии анастрозолом по сравнению с тамоксифеном в качестве инициальной адъювантной терапии I-II стадии РМЖ (табл. 3) [10, 11].
Таблица 3
Вероятность перехода в исследовании ATAC из одного состояния в другое [10, 11]
|
Показатели |
% |
|
Местно-региональный рецидив |
2,14 |
|
Рак контралатеральной молочной железы |
5,05 |
|
Отдалённые метастазы |
0,45 |
|
Смерть, не связанная с РМЖ |
2,50 |
|
Смерть после отдалённых метастазов |
3,90 |
Исследование ARNO 95 – исследование клинической эффективности перевода пациенток на анастрозол после 2-х лет терапии тамоксифеном при условии отсутствия рецидива (табл. 4) [6
Таблица 4
Вероятность перехода в исследовании ARNO 95 из одного состояния в другое [6]
|
Показатели |
% |
|
Местно-региональный рецидив |
2,5 |
|
Рак контралатеральной молочной железы |
1,4 |
|
Отдалённые метастазы |
5,5 |
|
Смерть, не связанная с РМЖ |
2,5 |
|
Смерть после отдалённых метастазов |
0,9 |
Исследование BIG 1-98 – рандомизированное контролируемое клиническое исследование, в котором предпринята попытка ответить на вопрос, является ли использование летрозола в ранней адъювантной терапии у женщин с гормоночувствительным РМЖ в менопаузе эффективной альтернативой тамоксифену (табл. 5) [12].
Таблица 5
Вероятность перехода в исследовании BIG 1-98 из одного состояния в другое [12]
|
Показатели |
% |
|
Местно-региональный рецидив |
0,8 |
|
Рак контралатеральной молочной железы |
0,6 |
|
Отдалённые метастазы |
7,4 |
|
Смерть, не связанная с РМЖ |
1,4 |
|
Смерть после отдалённых метастазов |
2,7 |
Исследование IES – исследование клинической эффективности перевода пациенток на экземестана после 2-3-х лет терапии тамоксифеном при условии отсутствия рецидива (табл. 6) [3].
Таблица 6
Вероятность перехода в исследование IES из одного состояния в другое [3]
|
Показатели |
% |
|
Местно-региональный рецидив |
2,11 |
|
Рак контралатеральной молочной железы |
9,31 |
|
Отдалённые метастазы |
0,77 |
|
Смерть, не связанная с РМЖ |
6,12 |
|
Смерть после отдалённых метастазов |
3,45 |
Итоговые значения вероятности перехода из одного состояния в другое показаны в табл. 7.
Таблица 7
Итоговые значения вероятности перехода (%) из одного состояния в другое
|
Показатели |
Анастрозол |
Летрозол |
Экземестан |
|
Инициальная адъювантная терапия |
|||
|
Местно-региональный рецидив |
2,14 |
0,8 |
— |
|
Рак контралатеральной молочной железы |
5,05 |
0,4 |
— |
|
Отдалённые метастазы |
0,45 |
4,4 |
— |
|
Смерть, не связанная с РМЖ |
2,50 |
1,4 |
— |
|
Смерть после отдалённых метастазов |
3,90 |
2,7 |
— |
|
Исследование |
ATAC |
BIG-98 |
— |
|
Переключение с продолжением терапии тамоксифеном |
|||
|
Местно-региональный рецидив |
2,5 |
— |
2,11 |
|
Рак контралатеральной молочной железы |
1,4 |
— |
9,31 |
|
Отдалённые метастазы |
5,5 |
— |
0,77 |
|
Смерть, не связанная с РМЖ |
2,5 |
— |
6,12 |
|
Смерть после отдалённых метастазов |
0,9 |
— |
3,45 |
|
Исследование |
ARNO 95 |
— |
IES |
Показатели безрецидивной выживаемости
Эффективность сравниваемых вмешательств была выражена в показателях безрецидивной выживаемости (DFS). Безрецидивная выживаемость выражена в процентах, не связанна со смертью от других причин; была определена как отсутствие любого из нижеперечисленных событий, причинно-связанных с РМЖ:
- местно-регионального рецидива;
- отдалённых метастазов;
- нового рака контралатеральной молочной железы;
- смерти после отдалённых метастазов.
Таблица 8
Эффективность сравниваемых препаратов, выраженная в показателях безрецидивной выживаемости (DFS)
|
Препарат |
Эффективность (95% ДИ) |
Источник |
|
Инициальная адъювантная терапия |
||
|
Летрозол (Фемара 2,5 мг №30) |
91,70% |
BIG-98 |
|
Анастрозол (Аримидекс 1 мг №28) |
88,46% |
ATAC |
|
Переключение с продолжением терапии тамоксифеном |
||
|
Анастрозол (Аримидекс 1 мг №28) |
89,70% |
ARNO 95 |
|
Экземестан (Аромазин 25 мг №30) |
84,36% |
IES |
Примечание. ДИ – доверительный интервал.
Фармакоэкономическая целесообразность. Для определения экономической целесообразности применения сравниваемых стратегий лечения РМЖ был использован установленный «порог готовности общества платить» (wtR – willingness to pay ratio) [критерий фармакоэкономической целесообразности – cost-effectiveness threshold], рассчитанный как размер трёхкратного ВВП на душу населения РФ, который в 2011 г. составлял: 54 585,6 млрд. руб. ÷ 141,9 млн. человек = 384 676 руб./чел./год х 3 = 1 154 029 руб. [9, 16, 21, 22]. Применительно к данному фармакоэкономическому анализу wtR отражает ту сумму, которую общество готово потратить на достижение терапевтического эффекта от применения ингибиторов/инактиваторов ароматазы III поколения. Интерпретируется порог следующим образом: полученный показатель CER, выраженный в рублях, и не превосходящий wtR, экономически эффективен для системы лекарственного возмещения в РФ [15].
В результате wtR-анализа, можно сделать вывод о том, является ли та или иная альтернативная стратегия лечения РМЖ фармакоэкономически целесообразной при используемом нами пороге wtR.
Временной интервал. Модель охватывает временной интервал в 5 лет.
Экономические показатели. Все расчёты выполнены в рублёвых ценах 2012 года (условный кросс-курс руб./$ США = 30/1). Окончательные расчёты выражены в показателях CER.
Дисконтирование. Дисконтирование исходов и затрат проводилось по ставке 3,5% в год, принятой в РФ на данный момент для проведения фармакоэкономических анализов [23].
Вероятность переходов из одного состояния в другое не дисконтировалось.
Анализ чувствительности. Для проведения анализа чувствительности мы сделали допущение о равной эффективности, выраженной в показателях безрецидивной выживаемости (DFS) для анастрозола, летрозола и экземестана.
Результаты
Стоимость препаратов сравнения. Для фармакоэкономического анализа были отобраны оригинальные препараты: анастрозол (Аримидекс), экземестан (Аромазин) и летрозол (Фемара), цены на котрые были рассчитаны как средние розничные в аптеках г. Москвы (табл. 9) [13].
Таблица 9
Розничные цены препаратов сравнения [13]
|
Препарат |
Стоимость уп., руб., с учётом НДС |
Стоимость в сут., руб. |
Стоимость в год, руб. * |
Стоимость за 5 лет (дисконт), руб. ** |
|
Аримидекс 1 мг №28 (анастрозол) |
6 240,94 |
222,89 |
81 131,96 |
67 893,55 |
|
Аромазин 25 мг №30 (экземестан) |
2 082,33 |
69,41 |
25 265,24 |
21 142,68 |
|
Фемара 2,5 мг №30 (летрозол) |
6 279,79 |
209,33 |
76 196,12 |
63 763,10 |
|
Примечание. * – Условно принято, что в году 364 дня; ** – дисконтирование – 3,5% в год. |
Прямые медицинские затраты. Для расчётов ценовых показателей стоимости медицинских услуг мы использовали Прейскурант на оказание медицинских услуг клиник ПМГМУ им. И.М. Сеченова за 2012 г. [18], ФГБУ «Российский научный центр рентгенорадиологии» за 2012 г. [24].
В хирургическое лечение вошли: госпитализация, инструментальные и лабораторные методы исследования, приём врача (консультации специалистов), проведение операции.
В химиотерапию вошли: госпитализация, инструментальные и лабораторные методы исследования, приём врача (консультации специалистов), проведение химиотерапевтического лечения.
В лучевую терапию вошли: госпитализация, инструментальные и лабораторные методы исследования, приём врача (консультации специалистов), проведение лучевой терапии и другое.
Дисконтированные результаты расчётов показаны в табл. 10.
Таблица 10
Расчёт стоимости прямых медицинских затрат
|
Медицинские услуги |
Стоимость, руб. |
Стоимость (дисконт за 5 лет), руб. |
|
Хирургическое лечение |
||
|
Приём (консультация) |
27 000 |
22 594 |
|
Лабораторные методы исследования |
9 060 |
7 582 |
|
Инструментальные методы исследования |
12 492 |
10 454 |
|
Госпитализация |
30 000 |
25 105 |
|
Хирургия |
49 387 |
41 328 |
|
Итого хирургическое лечение |
127 939 |
107 063 |
|
Химиотерапия |
||
|
Приём (консультация) |
45 000 |
37 657 |
|
Лабораторные методы исследования |
18 820 |
15 749 |
|
Инструментальные методы исследования |
17 810 |
14 904 |
|
Госпитализация |
60 000 |
50 210 |
|
Химиотерапия |
154 424 |
129 226 |
|
Другое |
32 325 |
27 050 |
|
Итого химиотерапия |
328 379 |
274 797 |
|
Лучевая терапия |
||
|
Приём (консультация) |
45 000 |
37 657 |
|
Лабораторные методы исследования |
18 120 |
15 163 |
|
Инструментальные методы исследования |
17 810 |
14 904 |
|
Госпитализация |
60 000 |
50 210 |
|
Лучевая терапия |
73 670 |
61 649 |
|
Другое |
1 200 |
1 004 |
|
Итого лучевая терапия |
215 800 |
180 588 |
|
Летальный исход |
||
|
Аутопсия |
16 000 |
13 389 |
|
Морфометрия |
5 176 |
4 331 |
|
Итого летальный исход |
21 176 |
17 721 |
Расчёт стоимости исходов в группах сравнения при инициальной адъювантной терапии показан в табл. 11 и 12.
Таблица 11
Анастрозол: расчёт стоимости прямых медицинских затрат при инициальной адъювантной терапии и итоговые значения вероятности перехода (%) из одного состояния в другое (в расчёте на 100 пациенток в течение 5 лет)
|
Показатели |
Вероятность перехода, % |
Вмешательство, исход |
Стоимость вмешательства, исхода, руб. * |
Итого, руб. |
|
Анастрозол |
85,96 |
Аримидекс 1 мг №28 |
33 946 776 |
29 180 649 |
|
Местно-региональный рецидив |
2,14 |
хирургия |
10 706 303 |
229 115 |
|
химиотерапия |
27 479 697 |
588 066 |
||
|
Рак контралатеральной молочной железы |
5,05 |
хирургия |
10 706 303 |
540 668 |
|
химиотерапия |
27 479 697 |
1 387 725 |
||
|
Отдалённые метастазы |
0,45 |
химиотерапия |
27 479 697 |
123 659 |
|
лучевая терапия |
18 058 763 |
81 264 |
||
|
Смерть, не связанная с РМЖ |
2,50 |
судмедэкспертиза |
1 772 068 |
44 302 |
|
Смерть после отдалённых метастазов |
3,90 |
судмедэкспертиза |
1 772 068 |
69 111 |
|
ВСЕГО на 100 пациенток, руб. |
32 244 558 |
|||
|
В СРЕДНЕМ на 1 пациентку, руб. |
322 446 |
|||
|
Примечание. * – Дисконтированные. |
Таблица 12
Летрозол: расчёт стоимости прямых медицинских затрат при инициальной адъювантной терапии и итоговые значения вероятности перехода (%) из одного состояния в другое (в расчёте на 100 пациенток в течение 5 лет)
|
Показатели |
Вероятность перехода, % |
Вмешательство, исход |
Стоимость вмешательства, исхода, руб. * |
Итого, руб. |
|
Летрозол |
90,3 |
Фемара 2,5 мг №30 |
31 881 550 |
28 789 040 |
|
Местно-региональный рецидив |
0,8 |
хирургия |
10 706 303 |
85 650 |
|
химиотерапия |
27 479 697 |
219 838 |
||
|
Рак контралатеральной молочной железы |
0,4 |
хирургия |
10 706 303 |
42 825 |
|
химиотерапия |
27 479 697 |
109 919 |
||
|
Отдалённые метастазы |
4,4 |
химиотерапия |
27 479 697 |
1 209 107 |
|
лучевая терапия |
18 058 763 |
794 586 |
||
|
Смерть, не связанная с РМЖ |
1,4 |
судмедэкспертиза |
1 772 068 |
24 809 |
|
Смерть после отдалённых метастазов |
2,7 |
судмедэкспертиза |
1 772 068 |
47 846 |
|
ВСЕГО на 100 пациенток, руб. |
31 323 619 |
|||
|
В СРЕДНЕМ на 1 пациентку, руб. |
313 236 |
|||
|
Примечание. * – Дисконтированные. |
Расчёт стоимости исходов в группах сравнения при переключении с продолжением терапии тамоксифеном показан в табл. 13 и 14.
Таблица 13
Анастрозол: расчёт стоимости прямых медицинских затрат при переключении с продолжением терапии тамоксифеном и итоговые значения вероятности перехода (%) из одного состояния в другое (в расчёте на 100 пациенток в течение 5 лет)
|
Показатели |
Вероятность перехода, % |
Вмешательство, исход |
Стоимость вмешательства, исхода, руб. * |
Итого, руб. |
|
Анастрозол |
88,1 |
Аримидекс 1 мг №28 |
33 946 776 |
29 907 110 |
|
Местно-региональный рецидив |
2,5 |
хирургия |
10 706 303 |
267 658 |
|
химиотерапия |
27 479 697 |
686 992 |
||
|
Рак контралатеральной молочной железы |
1,4 |
хирургия |
10 706 303 |
149 888 |
|
химиотерапия |
27 479 697 |
384 716 |
||
|
Отдалённые метастазы |
5,5 |
химиотерапия |
27479697 |
1 511 383 |
|
лучевая терапия |
18 058 763 |
993 232 |
||
|
Смерть, не связанная с РМЖ |
2,5 |
судмедэкспертиза |
1 772 068 |
44 302 |
|
Смерть после отдалённых метастазов |
0,9 |
судмедэкспертиза |
1 772 068 |
15 949 |
|
ВСЕГО на 100 пациенток, руб. |
33 961 230 |
|||
|
В СРЕДНЕМ на 1 пациентку, руб. |
339 612 |
|||
|
Примечание. * – Дисконтированные. |
Таблица 14
Экземестан: расчёт стоимости прямых медицинских затрат при переключении с продолжением терапии тамоксифеном и итоговые значения вероятности перехода (%) из одного состояния в другое (в расчёте на 100 пациенток в течение 5 лет)
|
Показатели |
Вероятность перехода, % |
Вмешательство, исход |
Стоимость вмешательства, исхода, руб. * |
Итого, руб. |
|
Экземестан |
78,24 |
Аромазин 25 мг №30 |
10 571 339 |
8 271 016 |
|
Местно-региональный рецидив |
2,11 |
хирургия |
10 706 303 |
225 903 |
|
химиотерапия |
27 479 697 |
579 822 |
||
|
Рак контралатеральной молочной железы |
9,31 |
хирургия |
10 706 303 |
996 757 |
|
химиотерапия |
27 479 697 |
2 558 360 |
||
|
Отдалённые метастазы |
0,77 |
химиотерапия |
27 479 697 |
211 594 |
|
лучевая терапия |
18 058 763 |
139 052 |
||
|
Смерть, не связанная с РМЖ |
6,12 |
судмедэкспертиза |
1 772 068 |
108 451 |
|
Смерть после отдалённых метастазов |
3,45 |
судмедэкспертиза |
1 772 068 |
61 136 |
|
ВСЕГО на 100 пациенток, руб. |
13 152 090 |
|||
|
В СРЕДНЕМ на 1 пациентку, руб. |
131 521 |
|||
|
Примечание. * – Дисконтированные. |
Результаты анализов эффективности затрат (CEA) сравниваемых стратегий лечения и препаратов терапии показаны в табл. 15.
Таблица 15
Анализ эффективности затрат сравниваемых препаратов на 1 пациента
|
Препарат |
Затраты, руб. |
Эффективность (DFS), дисконтированная |
CER, руб. |
|
Инициальная адъювантная терапия |
|||
|
Анастрозол (Аримидекс 1 мг №28) |
322 446 |
0,7403 |
435 561 |
|
Летрозол (Фемара 2,5 мг №30) |
313 236 |
0,7674 |
408 178 |
|
Переключение с продолжением терапии тамоксифеном |
|||
|
Анастрозол (Аримидекс 1 мг №28) |
339 612 |
0,7506 |
452 454 |
|
Экземестан (Аромазин 25 мг №30) |
131 521 |
0,7059 |
186 317 |
Примечание. DFS – Показатель безрецидивной выживаемости; CER – показатель эффективности затрат.
Анализ фармакоэкономической целесообразности показал, что применение летрозола (Фемары), анастрозола (Аримидекса) и экземестана (Аромазина) более чем в 2 раза меньше «порога готовности общества платить» – wtR (табл. 16).
Таблица 17
Анализ экономической целесообразности сравниваемых препаратов
|
Препарат |
CER, руб. |
wtR, руб. |
% от wtR |
< wtR, разы |
|
Инициальная адъювантная терапия |
1 154 029 |
|||
|
Анастрозол (Аримидекс) |
435 561 |
38 |
2,65 |
|
|
Летрозол (Фемара) |
408 178 |
35 |
2,83 |
|
|
Переключение с продолжением терапии тамоксифеном |
||||
|
Анастрозол (Аримидекс) |
452 454 |
39 |
2,55 |
|
|
Экземестан (Аромазин) |
186 317 |
16 |
6,19 |
|
|
Примечание. wtR (willingness to pay ratio) – установленный «порог готовности общества платить» [критерий фармакоэкономической целесообразности – cost—effectiveness threshold]. |
Анализ чувствительности. Мы сделали допущение, что при адъювантной терапии и при переключении с продолжением терапии тамоксифеном при РМЖ препараты анастрозол, летрозол и экземестан имеют равную эффективность (DFS) = 0,7. Результаты анализа показаны в табл. 18.
Таблица 18
Анализ чувствительности сравниваемых препаратов на 1 пациента
|
Препарат |
Затраты, руб. |
Эффективность (DFS), дисконтированная |
CER, руб. |
|
Инициальная адъювантная терапия |
|||
|
Летрозол (Фемара 2,5 мг №30) |
313 236 |
0,7 |
447 480 |
|
Анастрозол (Аримидекс 1 мг №28) |
322 446 |
0,7 |
460 485 |
|
Переключение с продолжением терапии тамоксифеном |
|||
|
Анастрозол (Аримидекс 1 мг №28) |
339 612 |
0,7 |
485 160 |
|
Экземестан (Аромазин 25 мг №30) |
131 521 |
0,7 |
187 887 |
|
Примечание. DFS – Показатель безрецидивной выживаемости; CER – показатель эффективности затрат. |
Основные выводы
-
При анализе эффективности затрат инициальной адъювантной терапии при РМЖ наиболее экономически эффективным препаратом является летрозол.
-
При анализе эффективности затрат при переключении с продолжением терапии тамоксифеном при РМЖ наиболее экономически эффективным препаратом является экземестан.
-
Все три препарата: анастрозол, летрозол и экземестан более чем в 2 раза меньше установленного «порога готовности платить», поэтому могут быть рекомендованы для включения в список ЖНВЛП (кроме анастрозола, который уже присутствует там) и для применения в системе государственного возмещения.
-
Анализ чувствительности подтвердил полученные результаты.
Ограничения исследования
Проведённые нами фармакоэкономические анализы эффективности затрат сравниваемых препаратов для лечения рака молочной железы имеют ряд ограничений:
-
в расчётах были использованы данные клинических исследований оригинальных препаратов, что не позволяет перенести их на генерические – нет взаимозаменяемости результатов исследований, в том числе, доказать фармацевтическую и терапевтической эквивалентности;
-
не учитывались побочные эффекты сравниваемой гормональной терапии;
-
полученные результаты не отображают популяцию больных в «реальном мире».
Конфликт интересов
Данный фармакоэкономический анализ был профинансирован фармацевтической компанией «АстраЗенека», однако это не оказало влияние на результаты данного исследования.
Литература
