Глюкозамин: инструкция по применению
Зотина Наталья Игоревна
25 мая 2023

ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ. ВОЗМОЖНЫ ПОБОЧНЫЕ ЭФФЕКТЫ. НЕОБХОДИМА КОНСУЛЬТАЦИЯ СПЕЦИАЛИСТА.
Автор статьи
Профессия: провизор
Название вуза: Пермская государственная фармацевтическая академия (ПГФА)
Специальность: провизор- технолог. Интернатура на кафедре фармацевтическая технология лекарственных средств
Стаж работы: 8 лет
Диплом о фармацевтическом образовании: 105924 1197876, рег. номер 30353
Места работы: провизор в аптеке, провизор сервиса Мегаптека
Все авторы
Содержание
- Глюкозамин или Хондроитин: что лучше для суставов?
- Состав
- Побочные эффекты
- Коллаген или Хондроитин с Глюкозамином: что лучше?
- Краткое содержание
Остеоартроз (ОА) — это хроническое прогрессирующее заболевание суставов, разрушающее суставной хрящ и поражающее другие части сустава — синовиальную оболочку и связки. При заболевании идет постепенное замещение хрящевой ткани на соединительную и костную. К основным факторам риска развития остеоартроза (или остеоартита, как его еще называют) относят травмы, ожирение и возраст. Так, признаки ОА встречаются у 80% людей старше 75 лет.
Основными направлениями лечения являются устранение причин, способствующих прогрессированию заболевания, уменьшение боли и восстановление нарушенного метаболизма суставного хряща. В последнем случае применяются так называемые модифицирующие средства замедленного действия на основе глюкозамина, диацереина, хондроитина, гиалуроновой кислоты. Данные препараты объединены тем, что их терапевтический эффект проявляется более медленно по сравнению с обычными симптоматическими средствами и длится даже после окончания их применения.
Рассказываем в статье о хондропротекторах глюкозамине и хондроитине. Их часто комбинируют в препаратах для предупреждения деградации хряща.
Глюкозамин или Хондроитин: что лучше для суставов?
Любой сустав состоит из костей, покрытых хрящем, и суставной капсулы, заполненной синовиальной жидкостью. Сам хрящ состоит из воды, коллагена II типа, протеогликанов и клеток-хондроцитов. Синовиальная жидкость служит для смазки, амортизации и питания суставного хряща.
Глюкозамин — это аминосахарид. Он вырабатывается клетками-хондроцитами и является исходным «строительным» материалом для биосинтеза хондроитина и протеогликанов, а значит и хрящевой ткани. Также входит и в состав синовиальной жидкости. При ОА продукция собственного глюкозамина снижена, поэтому для предотвращения дистрофии хрящевой ткани необходимо восполнять его извне.
Хондроитин сульфат — высокомолекулярный мукополисахарид. Это тоже естественный компонент, который содержится в соединительной, хрящевой и костной ткани. В организме синтезируется из глюкозамина, входит в состав протеогликанов – основы матрикса хряща, и нужен для синтеза гиалуроновой кислоты. Он оказывает противовоспалительное действие, улучшает обмен кальция и фосфора, ускоряет восстановление хряща и поддерживает вязкость синовиальной жидкости.
И глюкозамин, и хондроитин участвуют в образовании соединительной ткани, стимулируют регенерацию хрящей и снижают активность ферментов, повреждающих хрящевую ткань. В качестве лекарственных средств целесообразно их сочетать и принимать вместе. Монопрепарат принимают в случае непереносимости либо хондроитина, либо глюкозамина.
Состав
Ассортимент препаратов, содержащих глюкозамин и хондроитин (вместе и по отдельности), очень большой. Они производятся в различных лекарственных формах, содержат разные дозы и представлены как в виде лекарственных средств, так и в виде БАДов. Вот примеры лекарств, содержащих только глюкозамин:
- Дона: порошок для приготовления раствора для приема внутрь (1500 мг), раствор для внутримышечного введения (200 мг/мл); таблетки, покрытые пленочной оболочкой (750 мг);
- Глюкозамин сульфат 750: таблетки, покрытые пленочной оболочкой (750 мг);
- Глюкозамин: порошок для приготовления раствора для приема внутрь (1500 мг);
- Сустагард артро: концентрат для приготовления раствора для внутримышечного введения (200 мг/мл);
- Сустилак: таблетки модифицированного высвобождения, покрытые пленочной оболочкой (1500 мг);
- Эльбона: порошок для приготовления раствора для приема внутрь (1500 мг), раствор для внутримышечного и внутрисуставного введения (200 мг/мл).
Обращаем внимание, что глюкозамин не выпускают в такой лекарственной форме, как мазь для наружного применения.
Лекарственные препараты, в которые входит глюкозамин-хондроитин комплекс:
- Артра: таблетки, покрытые пленочной оболочкой (глюкозамин/хондроитин 500 мг/500 мг);
- КОНДРОнова: капсулы (250 мг/200 мг);
- Терафлекс: капсулы (500 мг/400 мг);
- Хондроглюксид: гель для наружного применения (5 г/2,5 г).
БАДы, содержащие хондроитин с глюкозамином для лечения суставов, могут иметь в своем составе и другие компоненты (минералы, растительные экстракты, экстракт акульего хряща, метилсульфонилметан МСМ):
- Глюкозамин Максимум: таблетки;
- Глюкозамин Ультра MSM: саше;
- Глюкозамин Форте: капсулы;
- Глюкозамин Хондроитин МСМ с гиалуроновой кислотой и пиперином: таблетки;
- Артроцин: крем для наружного применения.
Врачи рекомендуют использовать именно лекарственные препараты глюкозамина и хондроитина, у которых фармацевтическое качество и доказательная база не вызывают сомнений.
Побочные эффекты
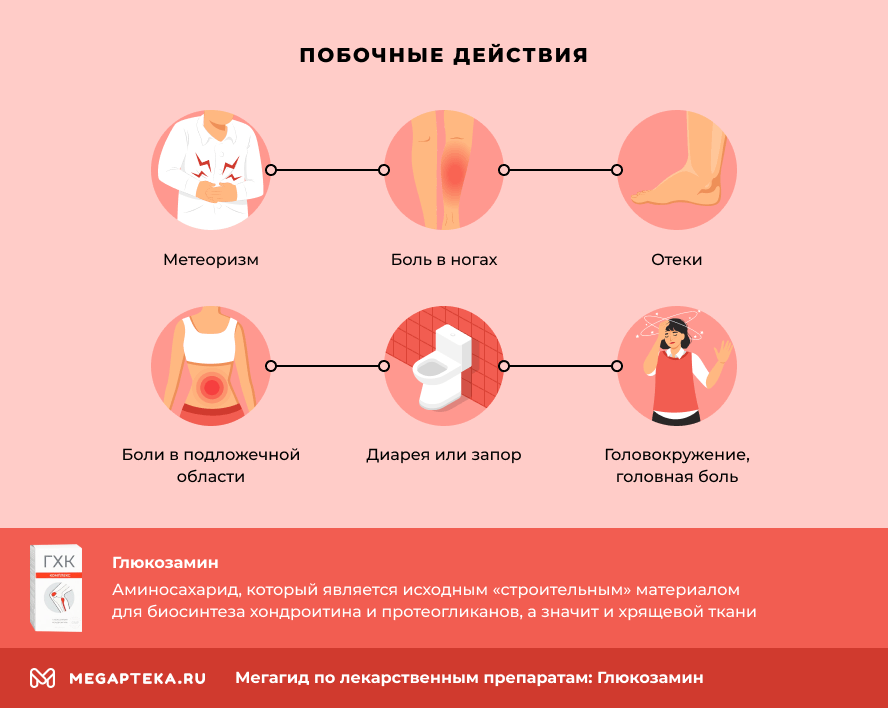
Как самое частое побочное действие хондропротекторов хондроитина и глюкозамина сульфата, инструкция указывает нарушение работы желудочно-кишечного тракта:
- боли в подложечной области;
- метеоризм;
- диарея или запор.
Также возможны:
- головокружение, головная боль;
- боль в ногах;
- отеки;
- сонливость или бессонница;
- учащенное сердцебиение;
- кожные аллергические реакции.
Коллаген или Хондроитин с Глюкозамином: что лучше?
Коллаген — это белок. Он отличается по своей структуре: I и III тип содержится в коже, сосудах и костях, II тип — в тканях хрящей и связок. Поэтому при остеоартрозе следует обращать внимание, какой коллаген содержится в препарате. Например, коллаген II типа и глюкозамин для суставов входят в состав БАДа Кветрель Артро. Два компонента усиливают действие друг друга и улучшают состояние хрящей суставов.
Глюкозамин является основной структурной единицей для биосинтеза хрящевого матрикса и синовиальной жидкости, он стимулирует работу хондроцитов, вместе с хондроитином нужен для синтеза гиалуроновой кислоты и защиты хряща от повреждений ферментами. Коллаген II типа – источник полипептидов для синтеза каркаса хряща.
В Федеральные клинические рекомендации по лечению остеоартрита включены препараты, содержащие только хондроитин и глюкозамин. Они рекомендуются при ОА для уменьшения боли и улучшения функции суставов. Хондроитин применяют по 500 мг 2 раза в сутки, длительно. Глюкозамин сульфат назначают по 1500 мг/сутки в течение 4–12 недель, курсы повторяют 2–3 раза в год.
Краткое содержание
- И глюкозамин, и хондроитин участвуют в образовании соединительной ткани, стимулируют регенерацию хрящей и снижают активность ферментов, повреждающих хрящевую ткань. В качестве лекарственных средств целесообразно их сочетать и принимать вместе.
- Препараты, содержащие глюкозамин и хондроитин (вместе и по отдельности), производятся в различных лекарственных формах, содержат разные дозы и представлены как в виде лекарственных средств, так и в виде БАДов.
- Как самое частое побочное действие хондропротекторов хондроитина и глюкозамина сульфата, инструкция указывает нарушение работы желудочно-кишечного тракта.
- В Федеральные клинические рекомендации по лечению остеоартрита включены препараты, содержащие только хондроитин и глюкозамин.
Задайте вопрос эксперту по теме статьи
Остались вопросы? Задайте их в комментариях ниже – наши эксперты ответят вам. Там же вы можете поделиться своим опытом с другими читателями Мегасоветов.
Хондропротекторы составляют важную часть лечения артроза и остеоартроза. Хондроитин способствует задержке в хрящевых тканях жидкости, а глюкозамин помогает хрящам восстанавливаться. Принимать их в виде биодобавок можно годами – курсами с определенным перерывом. Если вы выбрали для себя этот вариант, обратите внимание вот на что.
Глюкозамин получают из экзоскелетов моллюсков или из зерна пшеницы
1. При больших дозировках, которые превышают рекомендуемые 1500 мг в день в разы, наблюдается увеличение газообразования и «размягчение стула». У некоторых людей этот эффект бывает и при обычном приеме.
2. В составе биодобавок есть балластные загрязняющие вещества, от которых невозможно полностью избавиться с помощью современных технологий. Считается, что они могут вызывать аллергическую реакцию.
3. В составе сульфата глюкозамина, стабилизированного солью (хлоридом натрия), достаточно много пищевой соли. Поэтому при его приеме ее количество в пище необходимо намеренно сократить, например, перестать подсаливать еду во время приготовления. Иначе есть риск развития почечных патологий и проблем с артериальным давлением.
При патологиях почек сульфат глюкозамина с хлоридом натрия может быть опасен
4. Хондропротекторы нельзя принимать во время беременности и лактации, а также детям до 15 лет. Среди этих категорий пациентов исследования относительно воздействия глюкозамина и хондроитина на организм не проводились.
5. Хондроитин способен разжижать кровь. Поэтому люди, принимающие разжижающие препараты, должны быть особенно осторожны, чтобы избежать кровотечений.
Источник хондроитина – хрящи и трахеи рыб и крупного рогатого скота
6. Есть мнение, что доза глюкозамина, превышающая допустимую в 6-7 раз, может спровоцировать сахарный диабет, поскольку вещество является моносахаридом. Это мнение подкреплено исследованиями, которые проводились пока только на животных. Тем не менее, людям с сахарным диабетом или склонностью к нему, стоит проявлять предельную осторожность.
7. Хондроитин и глюкозамин – вовсе не панацея: для них характерна индивидуальная усваиваемость. Организм одного пациента усваивает моносахариды отлично, а у другого терапевтический эффект от лечения хондропротекторами напрочь отсутствует.
Эффективность хондроитина и глюкозамина не так однозначна, как утверждают многие ортопеды. Вот один из альтернативных взглядов на хондропротекторы с указанием их побочных эффектов:
Несмотря на определенные побочные эффекты, хондропротекторы все равно во много сотен раз безопаснее, чем длительный прием нестероидных противовоспалительных средств, которые часто назначают при лечении артроза.
Современной медицине известны еще более безопасные терапевтические методы, например внутрисуставные инъекции синтетического заменителя синовиальной жидкости «Нолтрекс». Препарат не содержит животного белка, поэтому не вызывает аллергии, кроме того, с осторожностью разрешен для приема людям с сахарным диабетом.
Какой бы вариант борьбы с остеоартрозом ни был выбран, лечение должно быть комплексным. Чтобы помочь организму восстановить вязкость и количество синовиальной жидкости, необходимо потреблять достаточно воды, придерживаться принципов здорового питания и жить активной жизнью.
Глюкозамин+хондроитин+мсм: инструкция по применению

Форма выпуска: Капсулы
Цены в аптеках: Минск
14,72 — 26,34 р.
Содержание
- Состав
- Назначение
- Рекомендации по применению
- Противопоказания
- Форма выпуска
- Условия хранения
- Срок годности
Состав
Глюкозамина сульфат, хондроитина сульфат, оболочка капсулы (желатин, красители (диоксид титана)), метилсульфонилметан, агент антислеживающий (магния стеарат).
Содержание биологически активных веществ в БАД:
|
Наименование активных компонентов |
Содержание в четырех капсулах (суточная доза), мг |
% от адекватного уровня суточного потребления в 4-х капсулах |
| Глюкозамин | 460 | 65,7 |
| Хондроитина сульфат | 1080 | 180* |
* — не превышает верхний допустимый уровень суточного потребления
Не обладает пищевой и энергетической ценностью.
Назначение
Рекомендуется в качестве дополнительного источника глюкозамина и хондроитина сульфата для поддержания функционального состояния суставов опорно-двигательного аппарата.
Рекомендации по применению
Лицам старше 18 лет по 2 капсулы 1-2 раза в день во время еды. Курс приема не менее 3-6 месяцев.
Перед применением рекомендуется проконсультироваться с врачом.
Цены в аптеках Минск
Глюкозамин+хондроитин+мсм, капсулы ×30
Биотерра, Беларусь • Без рецепта
Аналоги
Терафлекс, капсулы ×120
Байер Консьюмер Кэр, Швейцария • Без рецепта
Терафлекс, капсулы ×30
Байер Консьюмер Кэр, Швейцария • Без рецепта
Терафлекс ультра, капсулы ×120
Байер, Россия • Без рецепта
Терафлекс, капсулы ×60
Байер Консьюмер Кэр, Швейцария • Без рецепта
Терафлекс ультра, капсулы ×60
Байер, Россия • Без рецепта
Резюме
Введение. Остеоартрит является одним из наиболее распространенных хронических заболеваний опорно-двигательного аппарата во всем мире и частой причиной развития хронического болевого синдрома и инвалидности. Входящие в состав ряда фармаконутрицевтиков хорошо известные молекулы, такие как хондроитина сульфат, глюкозамина сульфат и неденатурированный коллаген II типа, обладают подтвержденными эффектами в отношении суставного хряща, субхондральной кости, синовии. Применение данных молекул позволяет влиять на основные звенья патогенеза остеоартрита и в конечном итоге может замедлять прогрессию заболевания, улучшать качество жизни пациентов. Перспективными молекулами для профилактики остеоартрита и ряда заболеваний опорно-двигательного аппарата, наряду с хондроитина сульфатом и глюкозамина сульфатом, являются витамины D3 и К2. Одна из важнейших функций витамина D (25(ОН)D) – поддержание должного уровня минерализации скелета. Снижение концентрации 25(ОН)D в сыворотке крови ниже оптимальных значений приводит к повышению риска переломов, особенно у пожилых. Витамин К2, являясь кофактором карбоксилирования остеокальцина, улучшает минеральную плотность костей и повышает их прочность. Хондроитина сульфат, глюкозамина сульфат и неденатурированый коллаген II типа блокируют активность провоспалительных цитокинов, стимулируют активность остеобластов и снижают избыточную активность остеокластов. Молекулы хондроитина сульфата и глюкозамина сульфата, витамины D3 и К2 имеют доказанную клиническую эффективность и безопасность в отношении остеоартрита.
Заключение. На сегодняшний день молекулы хондроитина сульфата, глюкозамина сульфата, неденатурированного коллагена II типа и витамин D3 могут быть отнесены к болезнь-модифицирующим остеоартрит препаратам (Disease Modifying Anti-Osteoarthritis Drug, DMOADs), которые обладают и симптом-модифицирующим, и структурно-модифицирующим действием. Хондроитина сульфат, глюкозамина сульфат, витамины D3 и К2 назначают для лечения и профилактики заболеваний опорно-двигательного аппарата. Они могут быть представлены как в форме лекарственных препаратов, так и в составе биологически активных добавок к пище. Применение этих компонентов может быть обосновано у пациентов с остеоартритом и сопутствующими заболеваниями (например, сердечно-сосудистой системы, сахарным диабетом 2-ого типа).
Конфликт интересов. Авторы статьи подтвердили отсутствие конфликта интересов, о котором необходимо сообщить.
Остеоартрит (ОА) является одним из наиболее распространенных хронических заболеваний опорно-двигательного аппарата (ОДА) во всем мире и частой причиной развития хронического болевого синдрома и инвалидности.
В основе патогенеза ОА лежит нарушение тонкого равновесия между анаболическими и катаболическими процессами внутри гиалинового хряща и субхондральной кости. При ОА для торможения остеодеструктивных процессов в субхондральной кости, непосредственно прилегающей к суставному хрящу, применяются хондропротекторы (ХП) как в форме лекарственных препаратов (ЛП), так и в форме фармаконутрицевтиков (нутриентов).
На сегодняшний день накоплена большая доказательная база эффективности и безопасности таких активных действующих веществ (АДВ), как хондроитина сульфат (ХС), глюкозамина сульфат (ГС), неденатурированный коллаген II типа (НК-II), витамин D3, витамин К2, гиалуроновая кислота (ГК) по отдельности и в комбинациях. Созданные на основе комбинаций АДВ фармаконутрицевтики применяются для нутритивной поддержки пациентов с заболеваниями суставов и позвоночника [1].
СОВРЕМЕННЫЙ ВЗГЛЯД НА БОЛЕЗНЬ-МОДИФИЦИРУЮЩИЕ ОСТЕОАРТРИТ ПРЕПАРАТЫ
В последние годы применяется новый подход к терапии любых заболеваний, когда предпочтение отдается болезнь-модифицирующим ЛП. Болезнь-модифицирующая фармакотерапия назначается пациентам с болезнью Альцгеймера или нейродегенеративными расстройствами, сердечно-сосудистыми заболеваниями (ССЗ) и др. Под болезнь-модифицирующими подразумевают ЛП, которые видоизменяют течение заболевания, препятствуя прогрессированию, и воздействуют непосредственно на его основную причину. Для лечения пациентов с заболеваниями ОДА применяют симптоматические лекарственные средства замедленного действия, для лечения ОА – SYSADOA (SYmptomatic Slow Acting Drugs for OsteoArthritis – симптоматические медленно действующие препараты для лечения ОА) и DMOADs (Disease-Modifying Osteoarthritis Drugs – болезнь-модифицирующие препараты для лечения ОА) [2, 3].
К группе SYSADOA относятся ХС, ГС, диацереин, неомыляемые соединения авокадо и сои (НСАС), ГК (для внутрисуставного введения – в/с). SYSADOA как аббревиатура, обозначающая данную группу ЛП, используется с 1995 г., однако в отдельную лекарственную группу препараты были выделены только в 2003 г. экспертами Европейской антиревматической лиги (EUropean League Against Rheumatism – EULAR) [4], которая в 2021 г. переименована в Европейский альянс ассоциаций ревматологов (EUropean Alliance of Associations for Rheumatology) с сохранением аббревиатуры EULAR.
SYSADOA обладают симптом-модифицирующим эффектом (т. е. способствуют уменьшению боли и улучшению функции) и структурно-/болезнь-модифицирующим эффектом (т. е. оказывают влияние на структуру хряща, субхондральную кость, синовий) [5]. Происходит постепенная замена аббревиатуры SYSADOA на DMOADs, что связано с вновь выявленными свойствами активно действующих молекул. Однако если в определении SYSADOA заложен смысл длительного назначения ЛП с симптом-модифицирующим действием, то DMOADs означает, что у ЛП этой группы обнаружен болезнь-модифицирующий (disease modifying) эффект [6]. В более ранних публикациях встречается обозначение группы ЛП как S/DMOAD (Structure/Disease Modifying Anti-Osteoarthritis Drug – Препарат против остеоартрита, модифицирующий структуру/заболевание) [7].
Исследования эффектов DMOADs ведутся с 1990-х гг., а в наши дни это направление приобрело еще большую актуальность и перспективность. К группе потенциальных DMOADs ранее относили далеко не все препараты, а только те, в отношении которых есть данные о влиянии на симптомы и структурные изменения при остеоартрите: ХС, ГС, диацереин, НСАС, ГК, гидролизат коллагена, ингибиторы матриксных металлопротеиназ (ММП), витамин Е, витамин D3, ингибиторы индуцируемой синтазы оксида азота (inducible nitric oxide synthase, iNOS), ранелат стронция, доксициклин, бисфосфонаты, кальцитонин, ликофелон, согласно проведенному систематическому метаанализу [8]. Группа ЛП DMOADs препятствуют прогрессированию и дальнейшему структурному повреждению сустава (структурно-модифицирующий эффект), приводя к уменьшению выраженности симптомов (симптом-модифицирующий эффект), таких как боль, улучшению функции сустава [2, 3]. Основной механизм действия потенциальных DMOADs – уменьшение активности провоспалительных цитокинов.
Сегодня наиболее изучены молекулы ХС, ГС, а также активно изучаются НК-II, ГК, витамин D3, которые рассматриваются как потенциальные DMOADs [6]. В 2021 г. для оценки сравнительной эффективности различных молекул из категории потенциальных DMOADs (ХС, ГС, витамин D3, и др.) проведено масштабное когортное исследование, включавшее анализ 28 рандомизированных контролируемых исследований (РКИ) при участии 11 890 пациентов с ОА коленного или тазобедренного суставов [8]. Одним из критериев включения в анализ была длительность терапии (не менее 12 мес; 6 мес для МРТ). Акцент делался на оценку положительной динамики структурных изменений в суставе (ширина суставной щели, объем хряща) и клинические симптомы (боль, функция) в течение длительного периода наблюдения. Показано, что из всех исследуемых препаратов только ХС и ГС обладают умеренно выраженным симптом- и структурно-модифицирующим действием (в дополнение к благоприятному профилю безопасности), а витамин D3 проявляет симптом-модифицирующее действие. Авторы отметили, что из исследуемых молекул убедительное долгосрочное выраженное структурно-модифицирующее действие выявлено только у ХС и ГС [8].
В 2021 г. эксперты EULAR провели анализ 24 систематических обзоров, 150 оригинальных статей, 83 исследований влияния различных диет и биологически активных добавок (БАД), предназначенных для улучшения качества жизни пациентов с заболеваниями ОДА [9]. Данный анализ отвечал всем требованиям доказательной медицины, так как был проведен по стандартной процедуре, в соответствии с принципами PRISMA (Preferred Reporting Items for Systematic Reviews and Meta-Analyses – Предпочтительные элементы отчетности для систематических обзоров и метаанализов), одобренными в рекомендациях EULAR.
Эксперты проанализировали диеты с использованием следующих активных действующих веществ: витамин Е, бромелайн, глюкозамин, экстракт коры ивы, хондроитин, экстракт полыни однолетней (Artemisia annua), экстракт новозеландской зеленогубой мидии (New Zealand green lipped mussel), метилсульфонилметан, НСАС, L-карнитин, куркумин, пикногенол, экстракт босвеллии пильчатой (Boswellia serrata), экстракт куркумы длинной (Curcuma longa), экстракт кожуры маракуйи, гидролизат коллагена, морские масла (полиненасыщенные жирные кислоты и полярные липиды), омега-3, пробиотики, витамин D3. В ходе проведенного метаанализа авторы заключили: умеренная доказательность эффекта достигнута только для таких веществ, как ХС, ГС, НСАС, рыбий жир [9].
В одном из аналитических обзоров за период с 1994 по 2023 гг. продемонстрирована значимость изменения рациона питания/приема БАД, в основе которых лежат омега-3 полиненасыщенные жирные кислоты (ПНЖК) – линолевая, α-линолевая, эйкозапентаеновая (ЭПК), докозагексаеновая (ДГК) и полярные липиды, как эффективной стратегии первичной профилактики ССЗ [10]. БАД с омега-3 ПНЖК, содержащие витамин D3, повышают эластичность и дилатацию артерий, снижают уровень провоспалительных цитокинов и С-реактивного белка (СРБ). Применение ЭПК и ДГК ведет к снижению уровня триглицеридов, частоты сердечных сокращений, артериального давления, агрегации тромбоцитов. Авторы пришли к выводу, что прием омега-3 ПНЖК и полярных липидов ведет к снижению риска ССЗ [10].
На основании анализа результатов ряда исследований сделан вывод, что только ХС, ГС, НК-II и витамин D3 обладают доказанным симптом- и структурно-модифицирующим действием и могут быть отнесены к категории потенциальных DMOADs. Однако ставить знак равенства между группами SYSADOA и потенциальных DMOADs некорректно, поскольку в последнюю включено гораздо большее число препаратов, в т. ч. и некоторые SYSADOA, перечень которых обозначен в рекомендациях Европейского общества по клиническим и экономическим аспектам остеопороза и остеоартрита (ESCEO) 2019 г. [11].
Применение фармаконутрицевтиков на основе действующих веществ с подтвержденными эффектами может способствовать влиянию на различные звенья патогенеза ОА и в конечном итоге замедлению прогрессирования ОА и улучшению качества жизни пациентов [6].
АНАЛИЗ РЕЗУЛЬТАТОВ ИССЛЕДОВАНИЙ ЭФФЕКТИВНОСТИ И БЕЗОПАСНОСТИ МОЛЕКУЛ ХОНДРОИТИНА СУЛЬФАТА, ГЛЮКОЗАМИНА СУЛЬФАТА, ВИТАМИНОВ D3 И К2
В проведенном в 2020 г. систематическом компьютерном анализе 21 300 публикаций оценивали противовоспалительные эффекты витамина D3 [12]. Установлено, что витамин D3, модулируя активность Т-лимфоцитов, тучных и антиген-презентирующих клеток, способствует ослаблению чрезмерного воспалительного ответа, повышая уровни противовоспалительного интерлейкина-10 (ИЛ), снижая уровни иммуноглобулина Е (IgE), цитокинов-аларминов, ИЛ-17, гистамина и лейкотриенов. Таким образом, витамин D3 важен для реализации противовоспалительного эффекта и компенсации хронических коморбидных патологий – цереброваскулярной, сахарного диабета (СД) 2-го типа, ССЗ, заболеваний почек, нарушений иммунитета, онкологических заболеваний и др., особенно у пожилых [12].
Витамин К2 является кофактором карбоксилирования остеокальцина (OК), который связывается с гидроксиапатитом – основой минеральной составляющей кости, повышая ее минеральную плотность и прочность. ОК – биомаркер костного метаболизма, гамма-карбоксильный глапротеин кости, представляет собой витамин К-зависимый белок, который синтезируется и секретируется остеобластами. ОК играет важную роль в регуляции метаболизма кальция в костях, но недокарбоксилированный ОК (н-OК) не имеет биологической функции, поскольку не может связываться с гидроксиапатитом и не способствует отложению кальция в кости. При помощи витамина К н-OК может превращаться в карбоксилированный ОК (к-OК), который имеет высокое сродство к кальцию и способствует образованию гидроксиапатита и минерализации костей [13].
В 2022 г. проведен метаанализ 16 РКИ, включавший 694 работы с 6425 участниками, чтобы уточнить влияние витамина K2 в качестве БАД на минерализацию костной ткани и частоту переломов у женщин в постменопаузе [13]. В данный метаанализ вошли результаты исследований, проведенных в Японии, Дании, Нидерландах, Норвегии, Китае и Индонезии. Авторы пришли к выводу [13], что витамин К2 по сравнению с контрольными группами:
1) эффективен в снижении частоты переломов по сравнению с группой контроля;
2) статистически значимо снижает уровни н-ОК в сыворотке крови;
3) повышает минеральную плотность костной ткани поясничного отдела позвоночника, бедра, шейки бедренной кости и предплечья;
4) низкие уровни витамина К2 в сыворотке и высокие уровни н-ОК рассматриваются как фактор риска перелома бедра у пожилых женщин.
Тест на общий эффект (метод синтеза результатов нескольких исследований) в данном метаанализе показал, что витамин K2 значительно снижает уровни н-ОК в сыворотке и соотношение н-ОК к к-ОК в ней же. В ходе исследования сделаны выводы [13]: витамин K2 может быть особенно эффективным в сочетании с другими средствами профилактики, такими как витамин D, кальций или алендронат (ингибитор костной резорбции, подавляющий активность остеокластов). Результаты метаанализа продемонстрировали способность витамина K2 значительно снижать уровень н-OК в сыворотке крови, под действием витамина K2 большее количество ОК подвергается γ-карбоксилированию и превращается в к-ОК, что способствует минерализации костей и увеличивает их прочность [13].
Витамин К2 влияет на обмен в костной ткани, не только участвуя в карбоксилировании ОК. Регулируя активность ядерного фактора NF-κB, витамин К2 способствует трансформации остеобластов в остеоциты [14]. Таким образом, замедление карбоксилирования ОК негативно сказывается на его способности связывать ионы кальция и снижает минерализацию костей, при недостатке витамина К образуются н-ОК, а при его выраженном дефиците часть ОК остается некарбоксилированной полностью.
В 2022 г. проведен компьютерный анализ 3926 публикаций, касающихся исследований ОА и нарушений метаболизма костной ткани методом топологической теории распознавания, выявивший [15], что такие ХП, как ХС, ГС, НК-II, блокируют активность провоспалительных цитокинов (каскады NF-κB и толл-рецепторов), стимулируют активность остеобластов (клетки, синтезирующие костную ткань) и снижают избыточную активность остеокластов (клетки, разрушающие костную ткань). Фармацевтически стандартизированные формы ХС и ГС, наряду с безопасными остеопротекторными средствами (витамин D3, кальций и др.), могут использоваться для нормализации костного метаболизма при ОА.
В 2023 г. проведен систематический компьютерный анализ 6176 публикаций о взаимосвязи ХС/ГС/НК-II и опухолевых заболеваний [16]. В крупномасштабных клинико-эпидемиологических исследованиях и метаанализах продемонстрировано онкопротективное действие (снижение риска развития рака толстой кишки и легких) при регулярном употребления ХС/ГС. Механизмы онкопротективного действия ХС/ГС оказались связаны с ингибированием каскада провоспалительных факторов и ряда цитокинов (фактор некроза опухоли альфа – ФНО-α, ядерный фактор каппа B – ЯФ-ϰB, фактор роста эндотелия сосудов и ММП, арахидоновая кислота, ИЛ-6, ИЛ-8, циклинзависимые киназы), а также инициацией апоптоза опухолевых клеток. Проведены первые постгеномные исследования онкопротективных эффектов ХС/ГС, а также исследования микробиома. Результаты анализа позволили сделать заключение о том, что потенциально онкопротективные эффекты ХС/ГС могут усиливаться противовоспалительным действием НК-II. Так, добавление в комплекс ХС/ГС молекулы НК-II позволяет снизить аутоиммунный ответ, участвующий в патогенезе ОА (первичного и вторичного) и ревматоидного артрита (РА) [16]. Авторы пришли к выводу, что совместное применение стандартизированных фармацевтических форм ХС, ГС и НК-II усиливает противовоспалительное и иммуномодулирующее действие их комбинации.
РОЛЬ ВИТАМИНА К2 В КОМПЛЕКСНОЙ ТЕРАПИИ И ПРОФИЛАКТИКЕ БОЛЕЗНЕЙ ОПОРНО-ДВИГАТЕЛЬНОГО АППАРАТА И АССОЦИИРОВАННЫХ С НИМ ЗАБОЛЕВАНИЙ
Жирорастворимый витамин К является кофактором карбоксилирования ОК и представлен в двух структурных вариантах: витамин К1 (филлохинон) и витамин К2 (менахинон) [14]. Дефицит витамина К2 связан с рядом патологических состояний, таких как ССЗ, хроническая болезнь почек (ХБП), ОА, РА, остеопороз, СД 2-го типа, рак, деменция, некоторые кожные заболевания [17].
В последние годы витамин К2 привлек внимание как вспомогательное средство для профилактики остеопороза [18]. Эпидемиологические исследования показали, что недостаток витамина К2 может привести к остеопорозу и ОА у пожилых людей. Кроме того, витамин К2 клинически используется для профилактики остеопороза и проявляет свое протективное действие, способствуя дифференцировке и минерализации остеобластов. Повышенный риск переломов у больных СД 2-го типа – диапороз, или диабетопороз, является одним из осложнений СД и может наблюдаться даже при нормальных показателях минеральной плотности кости (МПК) [19]. Витамин К2 рассматривается как потенциальное средство профилактики остеопоротических переломов [20]. При совместном применении с фибринолитиками и антитромобическими средствами он проявляет антиатеросклеротическое и гиполипидемическое действие [21]. Таким образом, использование витамина К2 в качестве добавки к пище позволит предотвратить процесс патологической минерализации мягких тканей при возраст-ассоциированных заболеваниях, таких как остеопороз, ОА, ХБП и ССЗ.
Витамин К-зависимые протеазы, а именно ОК, MGP (matrix Gla protein) – антикальцифицирующий матриксный белок и GRP (Gla-rich protein) – белок с достаточным содержанием Gla (γ-carboxyglutamate) – внепеченочные γ-карбоксиглутаматные белки, связаны патогенезом с OA [22]. Основные патофизиологические механизмы витамин К-зависимых белков в отношении заболеваний ОДА заключаются в следующем:
1) точками реализации механизмов действия MGP являются хондроциты и гладкомышечные клетки сосудов, основные эффекты – регуляция отложения кальция во внекостных тканях;
2) точки приложения GRP – хондроциты, хондробласты, остеобласты и остеоциты, основные эффекты – подавление патологической кальцификации в хрящевой и сосудистой тканях, противовоспалительное действие [23].
Физиологическая потребность в витамине К2 для взрослых составляет 120 мкг/сут, для детей разных возрастов – от 30 до 120 мкг/сут [23]. При остеопорозе терапевтическая доза витамина К2 п/о составляет 45-100 мг/сут [24, 25].
Оказывая множественное воздействие на суставной хрящ и субхондральную кость, витамин К2 может модулировать патогенез ОА. В одном из исследований показано распределение витамина К2 в биообразцах костей, взятых у пациентов с ОА при тотальном эндопротезировании коленного сустава [26]. В исследование вошли 53 пациента от 33 до 90 лет (средний возраст – 73 ± 8 года) с ОА коленного сустава (КС, всего 58 КС), которым было проведено его тотальное эндопротезирование. Концентрация витамина К2 в губчатых субхондральных областях бедренных и большеберцовых костей измерялась методом высокоэффективной жидкостной хроматографии с электрохимическим детектором. У пациентов с прогрессирующим ОА уровень витамина К2 в медиальных мыщелках бедренной и большеберцовой костей был статистически значимо ниже (р < 0,0001), тогда как в латеральных мыщелках с менее прогрессирующим ОА уровень витамина К2 был статистически значимо выше (р < 0,0001). Данное исследование продемонстрировало, что уровень витамина К2 в костях является значимым прогностическим показателем у пациентов с ОА. Авторы пришли к заключению о том, что витамин К2 влияет на регенерацию субхондральной кости при ОА коленного сустава [26].
РОЛЬ ВИТАМИНА D3 В КОМПЛЕКСНОЙ ТЕРАПИИ И ПРОФИЛАКТИКЕ БОЛЕЗНЕЙ ОПОРНО-ДВИГАТЕЛЬНОЙ СИСТЕМЫ И КОМОРБИДНЫХ С НИМИ ЗАБОЛЕВАНИЙ
Дефицит витамина D характеризуется снижением концентрации 25(ОН)D в сыворотке крови ниже оптимальных значений, что может потенциально приводить к снижению всасывания кальция в кишечнике, развитию вторичного гиперпаратиреоза и повышению риска переломов, особенно у пожилых [27].
Витамин D является гормоном, участвующим во многих физиологических процессах, его активная форма – 25(OH)D модулирует кальций-фосфатный гомеостаз сыворотки крови и гомеостаз скелета [28]. Витамин D3 проявляет ряд молекулярных эффектов: модуляция функции эндотелия, защита от повреждения подоцитов (висцеральные эпителиальные клетки почек, которые покрывают капилляры клубочков), регуляция ренин-ангиотензин-альдостероновой системы, противовоспалительное действие. Витамин D3 выступает в качестве ренопротектора, способствуя замедлению прогрессирования ХБП, в т. ч. диабетической болезни почек [28].
В клиническом исследовании у 200 амбулаторных пациентов с ОА (69,03 ± 2,34 года) изучалась взаимосвязь уровня витамина D3 с биохимическими показателями крови [29, 30]. У больных с ОА и дефицитом или недостаточностью витамина D3 наблюдались такие коморбидные заболевания, как ССЗ (гипертоническая болезнь); тогда как у пациентов с дефицитом витамина D3 по сравнению с группой с недостаточностью витамина D3 чаще отмечались такие коморбидные заболевания, как СД 2-го типа, онкологическая патология, хроническая обструктивная болезнь легких, острое нарушение кровообращения в анамнезе.
Из 200 наблюдаемых пациентов 100 были после тотального эндопротезирования суставов (ТЭС). У всех пациентов определяли уровни витамина D3, триглицеридов, тиреотропного гормона (ТТГ), общего холестерина, липопротеидов низкой и высокой плотности, глюкозы и кальция крови, мочевой кислоты, креатинина, общего белка. У пациентов, не подвергшихся ТЭС:
1) чаще наблюдался недостаток витамина D3 по сравнению с пациентами, которым уже было выполнено ТЭС;
2) выявлена статистически значимая взаимосвязь между концентрацией витамина D и глюкозы крови.
При этом в группе протезированных пациентов выявлена взаимосвязь между концентрацией витамина D3, альбумином и ТТГ.
Таким образом, дефицит витамина D3 является одним из факторов риска развития ряда полиморбидных ОА заболеваний. Пациенты с дефицитом витамина D3 имеют более прогрессивную рентгенологическую стадию ОА и выраженность нарушений функций суставов, по сравнению с теми, у которых уровень витамина D3 недостаточный [29, 30].
Одной из важнейших функций витамина D3 является поддержание должного уровня минерализации скелета. Обсервационные исследования продемонстрировали связь между низким уровнем витамина D (25-гидроксивитамина D [25(OH)D]) в сыворотке крови и наличием (развитием) и тяжестью заболеваний ОДА (ОА, РА, спондилоартропатии, системная красная волчанка) [31]. В ходе анализа обзорных исследований был сделан вывод, что пациенты с заболеваниями ОДА для предотвращения остеомаляции, вторичного остеопороза и переломов должны поддерживать уровень 25(OH)D в сыворотке крови на уровне не менее 30 нг/мл (75 нмоль/л), для укрепления иммунитета и общего состояния здоровья – 40-60 нг/мл (100-150 нмоль/л) [31].
В открытом проспективном контролируемом рандомизированном исследовании у 67 пациентов с посттравматическим фенотипом ОА КС (41-73 года) при увеличении концентрации остеокальцина и 25(ОН)D при выписке из стационара и через 3 месяца после ТЭС наблюдалось статистически значимое снижение уровня исследуемых биомаркеров воспаления в крови (ультрачувствительный СРБ, ММП, ИЛ-6, ФНО-ɑ и др.) [32]. Пациентов рандомизировали на две группы: основная (n = 32) получала нестероидные противовоспалительные препараты (НПВП) и в/м ХС за 2 мес до проведения ТЭС, контрольная (n = 35) – только НПВП. У пациентов основной группы на фоне ХС выявлено снижение концентрации биомаркеров воспаления при более значимом увеличении уровня ОК (витамин К-зависимый белок), что свидетельствует о структурно- и болезнь-модифицирующем эффекте ХС, различия в увеличении уровня 25(ОН)D (витамин D3) – о структурно- и болезнь-модифицирующем эффекте при посттравматическом и эндокринном фенотипах ОА КС [32].
В 2022 г. рабочая группа Европейского общества клинических и экономических аспектов остеопороза, остео-артрита и заболеваний опорно-двигательного аппарата (European Society of Clinical and Economical Aspects of Osteoporosis, Osteoarthritis and Musculoskeletal Diseases, ESCEO), проанализировав метаданные, РКИ влияния витамина D3 на риск переломов, падений или ОА КС, пришла к выводу, что пациентам с повышенным риском развития дефицита витамина D3 необходимо рекомендовать его профилактический прием в дозе 1000 МЕ в день [33]. Также эксперты отметили [33], что:
1) витамин D3 является ключевым компонентом кальциево-фосфатного гомеостаза;
2) основным источником витамина D3 в организме является его фотосинтез в коже;
3) ограниченное пребывание на солнце и недостаточное поступление витамина D3 с пищей требуют приема добавок витамина D3 в определенных возрастных группах;
4) рекомендуемые пожилым дозы витамина D3 варьируют от 200 до 2000 МЕ/сут для достижения уровня 25-гидроксивитамина D3 (кальцифедиола) не менее 50 нмоль/л.
В одном из продолжавшихся в течение 2 лет исследований влияния 2000-3000 МЕ/сут витамина D на симптомы заболевания у 500 пациентов с ОА было получено значительное улучшение параметров «боль» по Визуально-аналоговой шкале и «функция» по шкале WOMAC [34].
Согласно проекту Федеральных клинических рекомендаций по диагностике, лечению и профилактике дефицита витамина D3 (Россия, 2021 г.) [27] пересмотрена классификация уровней 25(ОН)D с конкретизацией целевого диапазона значений, разработаны рекомендации по скринингу заболеваний, ассоциированных с дефицитом витамина D3. Рекомендуется считать его дефицитом концентрацию 25(ОН)D < 20 нг/мл (< 50 нмоль/л), недостаточностью – уровень ≥ 20 и <3 0 нг/мл (≥ 50 и < 75 нмоль/л), адекватным уровнем – 30-100 нг/мл (75-250 нмоль/л), целевыми уровнями – 30-60 нг/мл (75-150 нмоль/л) (уровень убедительности рекомендаций В, уровень достоверности доказательств – 1).
Адекватный уровень концентрации 25(OH)D по версии Российской ассоциации эндокринологов составляет 30-100 нг/мл (75-250 нмоль/л). При профилактическом приеме у взрослых при невозможности лабораторного контроля уровня 25(OH)D и кальция во время длительного (более 6 мес) лечения рекомендуется придерживаться доз не выше 4000 МЕ в сутки у людей без факторов риска недостаточности витамина D3 и не более 10 000 МЕ в сутки у пациентов с риском дефицита витамина D [27].
Согласно обновленным Рекомендациям по профилактике и лечению дефицита витамина D3 [35] указаны диапазоны общей концентрации 25(ОН)D в сыворотке крови: < 20 нг/мл (< 50 нмоль/л) – дефицит витамина D, 20-30 нг/мл (50-75 нмоль/л) – неоптимальный статус, 30-50 нг/мл (75-125 нмоль/л) – оптимальная концентрация. Взрослым (19-65 лет) и пожилым (> 65-75 лет) рекомендуется принимать добавки на основе холекальциферола в дозе 1000-2000 МЕ/сут (25-50 г/сут) в течение всего года, исходя из массы тела и потребления витамина D3 с пищей. Пожилым (> 75-89 лет) и достигшим старческого возраста (90 лет и старше) рекомендуется принимать добавки на основе холекальциферола в дозе 2000-4000 МЕ/сут (50-100 г/сут) в течение всего года. Кальциферол во всех возрастных группах рекомендовано принимать в суточной дозе 10 мг (раствор для приема внутрь) в течение всего года и проводить контрольный анализ сыворотки на содержание 25(OH)D через 6-8 дней после начала приема добавок [35].
КОМПЛЕКС ВИТАМИНОВ К2 И D3 В ПРОФИЛАКТИКЕ ЗАБОЛЕВАНИЙ ОПОРНО-ДВИГАТЕЛЬНОГО АППАРАТА
Витамин К2 может быть целесообразно назначать совместно с другими нутриентами, участвующими в образовании костной ткани. Для профилактики остеопороза и риска переломов (особенно в период менопаузы) при дефиците витамина D3. рекомендован прием добавок с витамином D3 и кальцием; для профилактики скелетно-мышечных заболеваний и рисков переломов назначаются витамин К2 и магний [14]. Исследования показали, что витамин K2 может способствовать минерализации, индуцированной 25(OH)D в остеобластах человека, и что эффект приема витамина K2 в сочетании с витамином D3, или кальцием, или другими препаратами, препятствующими развитию остеопороза, на костную массу статистически значимо выше, чем при приеме одного только витамина K2 [14].
Систематический анализ научно-исследовательских материалов (систематические обзоры, метаанализы, РКИ, консенсусы мнений экспертов), размещенных в базах данных PubMed и Medline до марта 2020 г. включительно и сообщающих о влиянии добавок к пище (кальций, витамин D3, витамин К3, магний) на МПК, структуры костей, риск развития переломов, мышечную силу у взрослых [36], показал, что применение добавок с витамином D3 (отдельно или в сочетании с кальцием) является основополагающим для специфической терапии пациентов с более высоким риском переломов, связанных с метаболизмом костной ткани (остеопороз или дефицит витамина D3).
ОА и другие заболевания суставов коморбидны различной почечной патологии (гломерулонефрит, нефросклероз) и мочевыводящих путей (цистит, уролитиаз). В одном из исследований изучали влияние витамина К2 на прогрессирование атеросклероза и кальцификации сосудов у 42 пациентов с ХБП 3-5 стадии без диализа [37], которые наблюдались в течение 270 дней. Динамику состояния оценивали по результатам измерения толщины интимы общей сонной артерии, показателя кальцификации коронарных артерий, а также по биохимическим параметрам: MGP, дефосфори-лированный/некарбоксилированный MGP, ОК, остеопротегерин, фетуин А, фактор роста фибробластов-23. Сравнивали показатели в двух группах пациентов: первая принимала витамин К2 (менахинон, 90 мкг) в сочетании с витамином D (холекальциферол, 10 мкг), вторая – только витамином D (холекальциферол, 10 мкг). По результатам исследования сделан вывод [37]: у пациентов с ХБП длительный прием комплекса витаминов К2 + D уменьшает прогрессирование атеросклероза, подавляя риск кальцификации.
ЗАКЛЮЧЕНИЕ
По результатам проведенного анализа материалов исследований можно прийти к заключению, что перспективными молекулами для профилактики ОА и заболеваний ОДА наряду с ХС и ГС являются витамины D3 и К2.
Вклад авторов:
Концепция и дизайн — О. А. Шавловская; сбор и обработка данных источников литературы — О. А. Шавловская, статистический анализ данных источников литературы — О. А. Шавловская; написание текста — О. А. Шавловская; редактирование — И. Д. Романов, И. А. Бокова.
Contribution of authors:
Concept and design — O. A. Shavlovskaya; collection and processing of data from literature sources — O. A. Shavlovskaya, statistical analysis of data from literature sources — O. A. Shavlovskaya; text writing — O. A. Shavlovskaya; editing — I. D. Romanov, I. A. Bokova.
Литература/References
- Данилов Ал. Б., Лила А. М., Маджидова Ё. Н. и др. Новый фармаконутрицевтик Хондрогард®ТРИО для профилактики заболеваний опорно-двигательного аппарата и нутритивной поддержки пациентов с остеоартритом и неспецифической болью в спине: оценка клинических возможностей. Резолюция мультидисциплинарного экспертного совета. Неврология, нейропсихиатрия, психосоматика. 2023; 15 (2): 134-146. / Danilov Al. B., Lila A. M., Majidova Yo. N., et al. New pharmaconutraceutical Chondroguard®TRIO for the prevention of musculoskeletal diseases and nutritional support for patients with osteoarthritis and nonspecific back pain: an assessment of clinical options. Resolution of the Multidisciplinary Expert Council. Neurology, Neuropsychiatry, Psychosomatics. 2023; 15 (2): 134-146. (In Russ)]. DOI: 10.14412/2074-2711-2023-2-134-146.
- Oo W. M., Little C., Duong V., Hunter D. J. The development of disease-modifying therapies for osteoarthritis (DMOADS): the evidence to date. Drug Des Devel Ther. 2021; 15: 2921-2945. DOI: 10.2147/DDDT.S295224.
- Oo W. M., Hunter D. J. Repurposed and investigational disease-modifying drugs in osteoarthritis (DMOADs). Ther Adv Musculoskel Dis. 2022; 14: 1759720X221090297. DOI: 10.1177/1759720X221090297.
- Jordan K. M., Arden N. K., Doherty M., et al. EULAR Recommendations 2003: An evidence based approach to the management of knee osteoarthritis: Report of a Task Force of the Standing Committee for International Clinical Studies Including Therapeutic Trials (ESCISIT). Ann. Rheum. Dis. 2003; 62: 1145-1155. DOI: 10.1136/ard.2003.011742.
- Шавловская О. А., Громова О. А., Торшин И. Ю., Романов И. Д. От мисконцепций к обоснованной терапии пациентов с остеоартритом. ФАРМАКОЭКОНОМИКА. Современная фармакоэкономика и фармакоэпидемиология. 2023; 16 (2): 317-330. DOI: 10.17749/2070-4909/farmakoekonomika.2023.183. / Shavlovskaya O. A., Gromova О. А., Torshin I. Yu., Romanov I. D. From misconceptions to reasonable osteoarthritis patients therapy. FARMAKOEKONOMIKA. Modern Pharmacoeconomics and Pharmacoepidemiology. 2023; 16 (2): 317-330. (In Russ.) DOI: 10.17749/2070-4909/farmakoekonomika.2023.183.
- Шавловская О. А., Громова О. А., Кочиш А. Ю. и др. Болезнь-модифицирующие остеоартрит препараты (DMOADs) – новые тенденции в терапии пациентов с остеоартритом. ФАРМАКОЭКОНОМИКА. Современная фармакоэкономика и фармакоэпидемиология. 2023; 16 (3): 482-499. DOI: 10.17749/2070-4909/farmakoekonomika.2023.207. / Shavlovskaya O. A., Gromova О. А., Kochish A. Yu., et al. Disease-modifying osteoarthritis drugs (DMOADs): new trends in osteoarthritis therapy. FARMAKOEKONOMIKA. Modern Pharmacoeconomics and Pharmacoepidemiology. 2023; 16 (3): 482-499. (In Russ.) DOI: 10.17749/2070-4909/farmakoekonomika.2023.207.
- Verbruggen G., Goemaere S., Veys E. M. Chondroitin sulfate: S/DMOAD (structure/disease modifying anti-osteoarthritis drug) in the treatment of finger joint OA. Osteoarthritis Cartilage. 1998; Suppl.A: 37-38. DOI: 10.1016/s1063-4584 (98)80010-1.
- Yang W., Sun C., He S. Q., et al. The efficacy and safety of disease-modifying osteoarthritis drugs for knee and hip osteoarthritis – systematic review and network meta-analysis. J Gen Intern Med. 2021; 36 (7): 2085-93. DOI: 10.1007/s11606-021-06755-z.
- Gwinnutt J. M., Wieczorek M., Rodriguez-Carrio J., et al. Effects of diet on the outcomes of rheumatic and musculoskeletal diseases (RMDs): systematic review and meta-analyses informing the 2021 EULAR recommendations for lifestyle improvements in people with RMDs. RMD Open. 2022; 8 (2): e002167. DOI: 10.1136/rmdopen-2021-002167.
- Caffrey C., Leamy A., O’Sullivan E., et al. Cardiovascular diseases and marine oils: a focus on omega-3 polyunsaturated fatty acids and polar lipids. Mar. Drugs. 2023; 21: 549. DOI: 10.3390/md21110549.
- Bruyere O., Honvo G., Veronese N., et al. An updated algorithm recommendation for the management of knee osteoarthritis from the European Society for Clinical and Economic Aspects of Osteoporosis, Osteoarthritis and Musculoskeletal Diseases (ESCEO). Semin Arthritis Rheum. 2019; 49 (3): 337-350. DOI: 10.1016/j.semarthrit.2019.04.008.
- Громова О. А., Лила А. М., Торшин И. Ю., Рейер И. А. О перспективах применения хондропротекторов для торможения остеодеструктивных процессов в субхондральной кости при остеоартрите. ФАРМАКОЭКОНОМИКА. Современная фармакоэкономика и фармакоэпидемиология. 2022; 15 (1): 107-118. DOI: 10.17749/2070-4909/farmakoekonomika.2022.126. / Gromova О. А., Lila А. М., Torshin I. Yu., Reyer I. А. Application of chondroprotective agents to inhibit osteodestructive processes in the subchondral bone in patients with osteoarthritis. FARMAKOEKONOMIKA. Modern Pharmacoeconomics and Pharmacoepidemiology. 2022; 15 (1): 107-118. (In Russ.) DOI: 10.17749/2070-4909/farmakoekonomika.2022.126.
- Ma M.-L., Ma Z.-J., He Y.-L., et al. Efficacy of vitamin K2 in the prevention and treatment of postmenopausal osteoporosis: A systematic review and meta-analysis of randomized controlled trials. Front. Public Health. 2022; 10: 979649. DOI: 10.3389/fpubh.2022.979649.
- Bus K., Szterk A. Relationship between structure and biological activity of various vitamin K forms. Foods. 2021; 10 (12): 3136. DOI: 10.3390/foods10123136.
- Громова О. А., Торшин И. Ю., Габдулина Г. Х. Пандемия COVID-19: защитные роли витамина D. ФАРМАКОЭКОНОМИКА. Современная Фармакоэкономика и Фармакоэпидемиология. 2020; 13 (2): 132-145. DOI: 10.17749/2070-4909/farmakoekonomika.2020.044. / Gromova O. A., Torshin I. Yu., Gabdulina G. Kh. COVID-19 pandemic: protective role of vitamin D. FARMAKOEKONOMIKA. Modern Pharmacoeconomics and Pharmacoepidemiology. 2020; 13 (2): 132-145. (In Russ.) DOI: 10.17749/2070-4909/farmakoekonomika.2020.044.
- Торшин И. Ю., Чучалин А. Г., Громова О. А. Об онкопротективных эффектах хондропротекторов: глюкозамина, хондроитина сульфата и неденатурированного коллагена II типа. ФАРМАКОЭКОНОМИКА. Современная фармакоэкономика и фармакоэпидемиология. 2023; 16 (4): 681-698. DOI: 10.17749/2070-4909/farmakoekonomika.2023.182. / Torshin I. Yu., Chuchalin A. G., Gromova О. А. Oncoprotective effects of chondroprotectors: glucosamine, chondroitin sulfate and undenatured type II collagen. FARMAKOEKONOMIKA. Modern Pharmacoeconomics and Pharmacoepidemiology. 2023; 16 (4): 681-698. (In Russ.) DOI: 10.17749/2070-4909/farmakoekonomika.2023.182.
- Simes D. C., Viegas C. S. B., Araujo N., Marreiros C. Vitamin K as a diet supplement with impact in human health: current evidence in age-related diseases. Nutrients. 2020; 12 (1): 138. DOI: 10.3390/nu12010138.
- Palermo A., Tuccinardi D., D’Onofrio L., et al. Vitamin K and osteoporosis: Myth or reality? Metabolism. 2017; 70: 57-71. DOI: 10.1016/j.metabol.2017.01.032.
- Радугин Ф. М., Каронова Т. Л. Особенности костного ремоделирования у больных сахарным диабетом: фокус на витамин К2. Остеопороз и остеопатии. 2021; 24 (3): 11-18. DOI: 10.14341/osteo12929. / Radugin F. M., Karonova T. L. Bone metabolism in diabetes mellitus: focus on vitamin K2. Osteoporosis and Bone Diseases. 2021; 24 (3): 11-18. (In Russ.) DOI: 10.14341/osteo12929.
- Ших Е. В., Махова А. А. Витамин К2-менахинон: перспективы применения в комплексной терапии остеопороза с позиции доказательной медицины. Вопросы гинекологии, акушерства и перинатологии. 2019; 18 (2): 114-121. DOI: 10.20953/1726-1678-2019-2-114-121. Shikh E. V., Makhova A. A. Vitamin К2-menaquinone: the potential for usin g in complex therapy of osteoporosis from the positions of evidencebased medicine. Gynecology, Obstetrics and Perinatology. 2019; 18 (2): 114-121. (In Russ.) DOI: 10.20953/1726-1678-2019-2-114-121.
- Chen H., Chen J., Zhang F., et al. Effective management of atherosclerosis progress and hyperlipidemia with nattokinase: A clinical study with 1,062 participants. Front. Cardiovasc. Med. 2022; 9: 964977. DOI: 10.3389/fcvm.2022.964977.
- Ерусланова К. А., Онучина Ю. С., Иванникова Е. В., Дудинская Е. Н. Витамин К и возраст-ассоциированные заболевания. Российский журнал гериатрической медицины. 2022; 4 (12): 236-249. DOI: 10.37586/2686-8636-4-2022-236-249. / Eruslanova K. A., Onuchina Yu. S., Ivannikova E. V., Dudinskaya E. N. Vitamin K and age-related diseases. Russian Journal of Geriatric Medicine. 2022; 4 (12): 236-249. (In Russ.) DOI: 10.37586/2686-8636-4-2022-236-249.
- Никитина Е. А., Орлова С. В., Магомедова Х. А. и др. Витамин К2: известный и неизвестный. Современный взгляд: возможности и перспективы. Медицинский алфавит. 2022; 16: 102-108. DOI: 10.33667/2078-5631-2022-16-102-108. / Nikitina E. A., Orlova S. V., Magomedova Kh. A., et al. Vitamin K2: known and unknown. Modern view: opportunities and prospects. Medical alphabet. 2022; 16: 102-108. (In Russ.) DOI: 10.33667/2078-5631-2022-16-102-108.
- Palmer C. R., Blekkenhorst L. C., Lewis J. R., et al. Quantifying dietary vitamin K and its link to cardiovascular health: a narrative review. Food Funct. 2020; 11 (4): 2826-2837. DOI: 10.1039/c9fo02321f.
- Halder M., Petsophonsakul P., Akbulut A. S., et al. Vitamin K: double bonds beyond coagulation insights into differences between vitamin K1 and K2 in health and disease. Int J Mol Sci. 2019; 20 (4): 896. DOI: 10.3390/ijms20040896.
- Ishii Y., Noguchi H., Takeda M., et al. Distribution of vitamin K2 in subchondral bone in osteoarthritic knee joints. Knee Surg Sports Traumatol Arthrosc. 2013; 21: 1813-1818. DOI: 10.1007/s00167-012-2239-4.
- Дедов И. И., Мельниченко Г. А., Мокрышева Н. Г. и др. Проект федеральных клинических рекомендаций по диагностике, лечению и профилактике дефицита витамина D. Остеопороз и остеопатии. 2021; 24 (4): 4-26. DOI: https://DOI.org/10.14341/osteo12937. / Dedov I. I., Mel’nichenko G. A., Mokrysheva N. G., et al. Draft federal clinical practice guidelines for the diagnosis, treatment, and prevention of vitamin D deficiency. Osteoporosis and bone diseases. 2021; 24 (4): 4-26. (In Russ.) DOI: https://DOI.org/10.14341/osteo12937.
- Huang H.-Y., Lin T.-W., Hong Z.-X., Lim L.-M. Vitamin D and diabetic kidney disease. Int. J. Mol. Sci. 2023: 24: 3751. DOI: 10.3390/ijms24043751.
- Кашпанов М. Д., Новикова И. А., Харькова О. А. Особенности полиморбидной патологии у пациентов г. Мурманска с остеоартритом, имеющих различный уровень витамина D. Российские биомедицинские исследования. 2023; 8 (3): 18-25. DOI: 10.56871/RBR.2023.80.61.003. / Kashpanov M. D., Novikova I. A., Kharkova O. A. Polymorbid pathology in the city of Murmansk in patients with osteoarthritis having various vitamin D level. Russian biomedical research (St. Petersburg). 2023; 8 (3): 18-25. (In Russ.) DOI: 10.56871/RBR.2023.80.61.003.
- Кашпанов М. Д., Попов В. В., Новикова И. А., Харькова О. А. Взаимосвязь уровня витамина D и некоторых биохимических показателей крови у пациентов старше 60 лет с остеоартритом до оперативного лечения и после протезирования. Врач. 2023; 34 (4): 72-76. DOI: 10.29296/25877305-2023-04-15. / Kashpanov M., Popov V., Novikova I., Kharkova O. Relationship of vitamin D level with some biochemical indicators of blood in patients over 60 years of age with osteoarthritis before surgery and after prosthetics. Vrach. 2023; 34 (4): 72-76. (In Russ.) DOI: 10.29296/25877305-2023-04-15.
- Charoenngam N. Vitamin D and rheumatic diseases: a review of clinical evidence. Int. J. Mol. Sci. 2021; 22: 10659. DOI: 10.3390/ijms221910659.
- Минасов Т. Б., Лила А. М., Назаренко А. Г. и др. Стратификация декомпенсированной формы остеоартрита и современные возможности предоперационной терапии препаратом Хондрогард® на основе фено- и эндотипирования. РМЖ. Медицинское обозрение. 2023; 7 (3): 124-136. DOI: 10.32364/2587-6821-2023-7-3-124-136. / Minasov T. B., Lila A. M., Nazarenko A. G., et al. Stratification of decompensated osteoarthritis and modern options of the preoperative therapy using Chondroguard® based on pheno- and endotyping. Russian Medical Inquiry. 2023; 7 (3): 124-136 (In Russ.) DOI: 10.32364/2587-6821-2023-7-3-124-136.
- Chevalley T., Brandi M. L., Cashman K. D., et al. Role of vitamin D supplementation in the management of musculoskeletal diseases: update from an European Society of Clinical and Economical Aspects of Osteoporosis, Osteoarthritis and Musculoskeletal Diseases (ESCEO) working group. Aging Clin Exp Res. 2022; 34 (11): 2603-23. DOI: 10.1007/s40520-022-02279-6.
- Mathieu S., Soubrier M., Peirs C., et al. A meta-analysis of the impact of nutritional supplementation on osteoarthritis symptoms. Nutrient. 2022; 14 (8): 1607. DOI: 10.3390/nu14081607.
- Pludowski P., Kos-Kudła B., Walczak M., et al. Guidelines for preventing and treating vitamin D deficiency: A 2023 Update in Poland. Nutrients. 2023; 15: 695. DOI: 10.3390/nu15030695.
- Capozzi A., Scambia G., Lello S. Calcium, vitamin D, vitamin K2, and magnesium supplementation and skeletal health. Maturitas. 2020; 140: 55-63. DOI: 10.1016/j.maturitas.2020.05.020.
- Kurnatowska I., Grzelak P., Masajtis-Zagajewska A., et al. Effect of vitamin K2 on progression of atherosclerosis and vascular calcification in nondialyzed patients with chronic kidney disease stages 3-5. Pol Arch Med Wewn. 2015; 125 (9): 631-640. DOI: 10.20452/pamw.3041.
О. А. Шавловская1, shavlovskaya@1msmu.ru, https://orcid.org/0000-0003-3726-0730, WoS Researcher ID: V-4470-2018, Scopus Author ID: 15124744300,РИНЦ SPIN-код: 5300-4282
И. Д. Романов1, 2, https://orcid.org/0009-0003-0874-2834, Scopus Author ID: 57211891982; РИНЦ SPIN-код: 5960-1607
И. А. Бокова3, https://orcid.org/0000-0002-1640-1605, Scopus Author ID: 24773384800; РИНЦ SPIN-код: 6123-7160
1 Международный университет восстановительной медицины, Москва, Россия,
2 Сеть медицинских центров «МД Клиник», Москва, Россия
3 Первый Московский государственный медицинский университет имени И. М. Сеченова, Москва, Россия
Сведения об авторах:
Шавловская Ольга Александровна, д.м.н., профессор кафедры восстановительной медицины и медицинской реабилитации, Автономная некоммерческая организация высшего образования «Международный университет восстановительной медицины»; Россия, 105062, Москва, Фурманный переулок, 8/2; shavlovskaya@1msmu.ru
Романов Игорь Дмитриевич, невролог, руководитель по научной и консультативной неврологической помощи, Общество с ограниченной ответственностью «МД Клиник»; Россия, 111675, Москва, ул. Дмитриевского, 11; главный специалист отдела методического обеспечения программ дополнительного профессионального образования, Автономная некоммерческая организация высшего образования «Международный университет восстановительной медицины»; Россия, 105062, Москва, Фурманный переулок, 8/2
Бокова Ирина Анатольевна, к.м.н., доцент кафедры восстановительной медицины, реабилитации и курортологии, Федеральное государственное автономное образовательное учреждение высшего образования Первый Московский государственный медицинский университет имени И. М. Сеченова Министерства здравоохранения Российской Федерации; 119991, Россия, Москва, ул. Трубецкая, 8/2
Information about the authors:
Olga A. Shavlovskaya, Dr. of Sci. (Med.), Professor, Chair of Organization of Medical Rehabilitation and Sanatorium Treatment, Autonomous nonprofit organization of higher education International University of Restorative Medicine; 8/2 Furmanny Lane, Moscow, 105062, Russia; shavlovskaya@1msmu.ru
Igor D. Romanov, Neurologist, Head of Scientific and Advisory Neurological Care, MD Clinic Limited Liability Company; 11 Dmitrievsky str., Moscow, 111675, Russia; Chief specialist of the Department of methodological support of additional professional education programs, Autonomous nonprofit organization of higher education International University of Restorative Medicine; 8/2 Furmanny Lane, Moscow, 105062, Russia
Irina A. Bokova, Cand. of Sci. (Med.), Associate Professor, Chair of Restorative Medicine, Rehabilitation and Balneology, Federal State Autonomous Educational Institution of Higher Education I. M. Sechenov First Moscow State Medical University of the Ministry of Health of the Russian Federation; 8/2 Trubetskaya str., Moscow, 119991, Russia
Доказательная база фармаконутрицевтиков с хондропротективным действием/ О. А. Шавловская, И. Д. Романов, И. А. Бокова
Для цитирования: Шавловская О. А., Романов И. Д., Бокова И. А. Доказательная база фармаконутрицевтиков с хондропротективным действием. Лечащий Врач. 2024; 4 (27): 47-54. https://doi.org/10.51793/OS.2024.27.4.007
Теги: опорно-двигательный аппарат, болевой синдром, качество жизни
