Статьи
Опубликовано в журнале:
«ГИНЕКОЛОГИЯ»; ТОМ 12; № 2; стр. 1-12.
О.А.Громова1,2, И.Ю.Торшин1,2, О.А.Лиманова1,2, А.А.Никонов1,3
1Российский сотрудничающий центр «Нейробиология» Международного института микроэлементов ЮНЕСКО, 2ГОУ ВПО Ивановская государственная медицинская академия РФ (ректор — акад. РАЕН Р.Р.Шиляев), 3ГОУ ВПО Российский государственный медицинский университет РФ (ректор — акад. РАМН Н.Н.Володин)
Введение
Специфические вегетативно-сосудистые пароксизмы — так называемые «приливы» — наиболее частый вазомоторный симптомокомплекс перименопаузы. Субъективно «прилив» можно описать как внезапную волну интенсивного тепла и даже жара по телу, сопровождающуюся профузным потоотделением, тахикардией и, у многих пациенток, подъемом артериального давления. Пароксизмы приливов могут длиться от нескольких минут до получаса. Ощущение жара, как правило, начинается с лица, груди, затылка, задней части шеи, распространяясь далее по верхней части туловища, и у некоторых женщин доходит до периферии. Помимо субъективного ощущения тепла или жара поверхность кожи, особенно на лице и верхней части груди, кратковременно становится более горячей на ощупь. Прилив может происходить от нескольких раз в месяц до нескольких раз в сутки. Приливы ухудшают настроение, препятствуют концентрации внимания и снижают работоспособность. Особо частые и интенсивные приливы в ночное время могут вызвать бессонницу.
Обзор более 60 публикаций по эпидемиологии приливов в перименопаузе показал повсеместную их распространенность. Распространенность приливов среди населения варьирует в значительных пределах: в Европе и США приливы отмечаются у 70% женщин в менопаузе, а в Юго-Восточной Азии — у 5-18%. Распространенность в различных популяциях может быть обусловлена целым рядом факторов, включая диету, образ жизни и обусловленное культурой психологическое отношение к концу репродуктивного периода жизни [1].
Патофизиология приливов до сих пор не уточнена. Возможно, что недостаток эстрогенов в менопаузе так или иначе влияет на центр терморегуляции в головном мозге [2]. В репродуктивном возрасте женщины подавляющее количество эстрогенов синтезируется в яичниках, желтом теле и плаценте. Во время менопаузы уровни так называемых позитивных эстрогенов (например, 17-β-эстрадиола) постоянно падают, поэтому возрастает значение эстрогенов, синтезируемых в печени и надпочечниках. При наступлении менопаузы на фоне хронической надпочечниковой недостаточности появляются различные симптомы дезадаптации, в том числе и приливы. Применение синтетических эстрогенов может поддерживать уровни эстрогенов и в ряде случаев снижать интенсивность симптоматики приливов. В самом деле, метаанализ 24 исследований (более 3300 пациенток) указал на значительное уменьшение числа приливов и их интенсивности при использовании заместительной гормональной терапии (ЗГТ): относительный шанс (ОШ) 0,13; 95% доверительный интервал (ДИ) 0,07-0,23 [3]. Поэтому приливы являются наиболее распространенной причиной приема женщинами ЗГТ.
Хотя ЗГТ синтетическими эстрогенами приводит к уменьшению остроты и частоты приливов у 80-90% женщин, принимающих ЗГТ, некоторые пациентки не решаются на столь радикальное гормональное вмешательство [4]. Всем женщинам, страдающим раком молочной железы [5], яичников [6], матки [7], венозной тромбоэмболией [8] или имеющим семейную историю рака груди [5], следует категорически избегать применения эстрогеновых препаратов. Кроме того, не следует забывать, что эстроген-терапия имеет негативные последствия, такие как головная боль, избыточная задержка жидкости, болезненность молочных желез, маточные кровотечения [9].
Повышенный риск осложнений и серьезные побочные эффекты синтетических эстрогенов делают разработку альтернативных видов терапии приливов насущно необходимой [10]. Многочисленные исследования показывают возрастающую тенденцию не применять ЗГТ при умеренной симптоматике приливов. Все чаще используют эффективную модификацию диеты и образа жизни наряду с альтернативной фармакотерапией [11]. Шире применяют альтернативные фармакологические препараты: избирательные ингибиторы серотонина или норадреналина [12], габа-пентин (аналог ГАМК, используемый для лечения различных неврологических расстройств), вералиприд (антидопаминергик) [13] и клонидин (β-адреноблокатор). Некоторые нутриенты (токоферол [14]; омега-3-жирные кислоты [15], соевые изофлавоны/генистеин [16, 17]) также уменьшают симптоматику приливов. Альтернативные методы фармакотерапии, например селективные ингибиторы серотонина, снижают частоту и тяжесть приливов на 19-60% [18]. Габапентин показал снижение частоты и тяжести приливов на 20-30% по сравнению с плацебо [19].
Лечение приливов препаратом Клималанин производства компании «Бушара Рекордати» на основе β-аланина является альтернативным ЗГТ. Требованием времени остается поиск негормональных, но высокоэффективных фармакологических средств для патогенетического лечения приливов. Представляем систематический анализ [1] патофизиологии приливов [2] и молекулярных ролей препарата Клималанин, имеющих значение для терапии приливов.
Систематический анализ патофизиологии приливов и механизмов воздействия β-аланина
Наиболее разработанными являются три подхода к патофизиологическому объяснению приливов: вегетативный, абстинентный и гормонально-нейротрансмиттерный. Эти подходы отображают многообразие социальных, психологических и эндокринных факторов, вносящих свой вклад в этиологию приливов. Фармакологическое действие Клималанина невозможно напрямую объяснить, используя вегетативный и абстинентный подходы. Однако действие Клималанина на купирование вегетативной и так называемой абстинентной симптоматики все же объяснимо с точки зрения гормонально-нейротрансмиттерного подхода.
Вегетативная дисфункция
Климактерический период связан не только с проявлениями эндокринных расстройств, но и с нарушениями функционирования вегетативной нервной системы. Известно, что психологические факторы, в том числе беспокойство, стресс, страх и т.д., влияют на возникновение приливов [1, 20] и приводят к так называемым сердечно-сосудистым неврозам по Г.Ф.Лангу [21]. Сердечно-сосудистые неврозы встречаются у женщин гораздо чаще, особенно в менопаузе. Приливы характеризуются дисфункцией вегетативной нервной системы. Поэтому исключение факторов, провоцирующих вегетативную дисфункцию, наряду со специфически направленной тренировкой нервной системы может быть использовано в терапии приливов. Изменение образа жизни помогает смягчению симптоматики проявления приливов. Пациенткам следует отказаться от курения, алкоголя, избегать кофеина, острой пищи, горячих напитков. Гиподинамия — важный стрессовый фактор, также приводящий к дезадаптации и формированию хронической надпочечниковой недостаточности. Хорошо известно, что гиподинамия не только фактор риска так называемых болезней цивилизации (ожирение, сердечно-сосудистые и цереброваскулярные заболевания и т.д.). Малоподвижный образ жизни значительно повышает риск развития и вазомоторных пароксизмов в климактерии. Регулярные физические упражнения и аутотренинг уменьшают интенсивность проявления симптоматики приливов, способствуют установлению более адекватной реакции организма на стресс [22].
Приливы как разновидность абстинентного синдрома
Приливы могут быть рассмотрены как проявление своеобразной «абстиненции» эстроген-чувствительных нейрональных систем, находившихся долгое время в условиях высокого содержания эстрогенов [23]. В самом деле, существует определенная схожесть в симптоматике менопаузы и симптоматике, связанной с абстинентным синдромом в случае болезней зависимости (курение, алкоголизм, наркомания). Например, симптомами абстиненции в случае каннабиноидов являются беспокойство, раздражительность, депрессия, приливы, ночной пот, инсомния и тремор [24, 25]. Многие из этих симптомов также соответствуют и вегето-сосудистой дистонии, и менопаузальной симптоматике.
Не менее чем у 20% пациенток с приливами использование ЗГТ не эффективно и не приводит к уменьшению симптоматики приливов. В контексте абстинентного подхода к объяснению этиологии приливов ЗГТ не будет эффективна, если в составе используемого эстрогенового препарата отсутствует именно та форма эстрогена, которая и вызвала химическую зависимость [25]. Фактом, подтверждающим применимость абстинентного подхода, является провокация приливов при использовании ЗГТ у пациенток с первичной аменореей. Несмотря на крайне низкое содержание эстрогенов у пациенток с различными формами первичной аменореи, у них никогда не бывает приливов. Они появляются только после назначения и отмены гормональной терапии. Удаление яичника у пременопаузальных женщин вызывает быстрое наступление приливов, в то время как женщины с первичной аменореей (гонадальный дисгенез), имеющие низкий уровень эндогенных эстрогенов, не испытывают приливов. Если, однако, женщина с гонадальным дисгенезом пройдет курс ЗГТ в течение нескольких месяцев, а затем прием эстрогенов будет резко прекращен, то приливы появятся [26].
Рассмотрение приливов как разновидности абстинентного синдрома имеет ряд важных последствий для терапии. Во-первых, регулярное и длительное использование пероральных контрацептивов в репродуктивном периоде повышает уровни эстрогеновых производных в крови значительно выше биологически приемлемых норм. В последующем, при наступлении менопаузы, у этой категории женщин может развиваться крайне тяжелая абстиненция, выраженная приливами с симптоматикой, типичной для абстинентного синдрома у больных наркоманией (жар, профузный пот, тремор, чувство полного бессилия после приступа). Во-вторых, инициацию и окончание курса ЗГТ не следует проводить резко. Возможно использование общих принципов лечения химической зависимости, таких как постепенное сокращение дозировки и увеличение интервалов между приемами препаратов. Это также касается и применения других пероральных эстрогеновых препаратов, таких как синтетические контрацептивы.
Гормонально- нейротрансмиттерные механизмы развития приливов
Дисфункция терморегуляторного центра, вызванная изменениями в уровнях эстрогенов в период менопаузы, считается основой патофизиологии приливов. Когда происходит возрастное падение уровней эстрогенов в организме женщины, концентрация эстрогенов, достигающих гипоталамуса, также снижается. Расположенный в гипоталамусе центр регулирования температуры [27] лишается привычной эстрогеновой стимуляции. В результате дестабилизируется функционирование терморегуляторного центра и возникают приливы как следствие избыточной активации теплоотдачи за счет вазодилатации и потоотделения. Гипоталамус — вершина фундаментальной гормональной оси гипоталамус-гипофиз-кора надпочечников. Гипоталамус обеспечивает функционирование сложнейшего интерфейса между нервной и эндокринной системами. Эта область мозга реагирует на нейрональные сигналы от других систем организма (длительность светового дня, обонятельные рецепторы, стресс, температура), а также на многочисленные гормональные и другие стимулы, переносимые с кровью (стероиды, кортикостероиды, ангиотензин, инсулин, концентрация глюкозы и др.). В медиальной преоптической области гипоталамуса содержится терморегуляторное ядро, активирующее механизмы для поддержания температуры тела в нормальном диапазоне, называемом терморегуляторной зоной [26]. У женщин с приливами может иметь место сужение границ терморегуляторной зоны по сравнению с женщинами, которые не имеют приливов [28]. Сужение терморегуляторной зоны может быть обусловлено избытком норадреналина и недостатком серотонина (рис. 1).
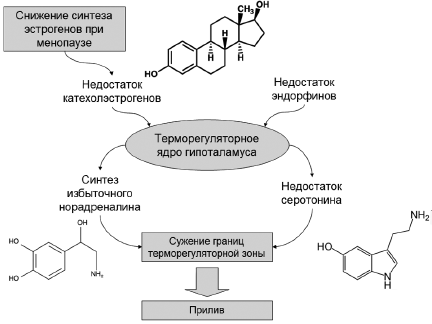
Рис. 1. Предполагаемые гормонально-нейрорегуляторные механизмы, задействованные в этиологии приливов.
Катехоламины и серотонин
Норадреналин считается основным нейротрансмиттером, ответственным за сужение терморегуляторной зоны гипоталамуса [27, 29]. Во время приливов резкий подъем уровней метаболитов норадреналина коррелирует с повышениями температуры тела и теплоотдачи [30]. Считается, что производство и секреция норадреналина в термо-регуляторном ядре гипоталамуса полностью ингибируются эндорфинами и катехол-эстрогенами [31]. Поэтому при недостатке последних будет происходить нарушение терморегуляции. Серотонин — еще один вероятный нейро-трансмиттер, участвующий в механизме приливов. Снижение уровней серотонина происходит параллельно со снижением уровней эстрогенов в менопаузе, а также у пациенток с аменореей и удаленными яичниками [32]. Было высказано предположение, что определенные типы рецепторов серотонина имеют отношение к нарушениям терморегуляции при приливах [33].
Патофизиология приливов и кальцитониноподобный пептид
Предположительные влияния катехоламинов и серотонина на ширину терморегуляторной зоны являются общеизвестными объяснениями влияния эстрогенов на этиологию приливов. В данном разделе мы предлагаем принципиально новую концепцию патогенеза приливов, основанную на систематическом анализе последних данных по молекулярной физиологии кальцитониноподобного пептида (англ. саlcitonin gene related peptide -CGRP).
Кальцитониноподобный пептид широко распространен в центральной и периферической нервной системе, обладает отчетливым вазодилатационным эффектом. Основным источником пептида является место ветвления тройничного нерва, который отвечает за иннервацию кожи и сосудов верхней, средней и нижней части лица. При приливах, как известно, наблюдается внезапное покраснение всего лица за счет расширения сосудов. Прием эстрогенов увеличивает уровни кальцитониноподобного пептида и метионин-энкефалина [34, 35] именно в преоптической зоне гипоталамуса [36, 37]. Преоптическая зона располагается вблизи двух анастомозов сосудистых сплетений гипоталамуса. Нормальной терморегуляции соответствует достаточный кровоток через эти сплетения; при нарушении терморегуляции кровоток снижен. Результаты исследования 13 женщин с приливами и 13 здоровых (контроль) показали, что суточная экскреция кальцитониноподобного пептида с мочой была значительно выше у женщин с приливами. Повышенная экскреция пептида с мочой позволяет предположить, что именно этот пептид может являться специфическим медиатором вазодилатации при приливах [38]. Это предположение напрямую подтверждается исследованием 8 женщин с вазомоторными синдромами, у которых проводили круглосуточное мониторирование биохимических параметров крови. Уровни кальцитониноподобного пептида и нейропептида Y повышаются во время прилива (на 73 и 34% соответственно) [39]. Прием эстрогенов может способствовать нормализации базальных уровней кальцитониноподобного пептида [40]. Особенно важно, что кальцитониноподобный пептид взаимосвязан с энергетическим метаболизмом. На энергетический метаболизм также влияет и Клималанин (см. далее). В исследовании 45 женщин в менопаузе уровни кальцитониноподобного пептида коррелировали с уровнями инсулина [41]. Низкие уровни пептида нарушают вазодилатационный эффект инсулина [42]. Пептид стимулирует базальную секрецию инсулина и глюкагона [43].
Механизмы воздействия препарата Клималанин
Рассматривая механизмы действия Клималанина, а точнее его действующего начала — β-аланина (C3H7NO2), следует начать с того, что это — β-аминокислота, синтезируемая в организме человека. В отличие от распространенного в белках α-аланина в β-аланине амидная группа присоединена не к атому Са, а к атому Сb (рис. 2). Подобная химическая структура β-аланина приводит к тому, что эта аминокислота не включается в состав белков. Тем не менее β-аланин весьма важен для метаболизма тканей и функционирования нервной системы.
Рис. 2. α-Аланин (слева) и β-аланин (справа).
β-Аланин используется для уменьшения мышечной утомляемости при повышенных физических нагрузках. При типичной разовой дозировке от 400 до 800 мг (или от 0,4-0,8 г) β-аланин в спортивной медицине принимают с интервалами до 8 ч в течение нескольких недель [44]. После 10-недельного приема β-аланина содержание дипептида карнозина увеличивается в среднем на 80% [45].
В организме β-аланин образуется в результате деградации дигидроурацила (метаболизм нуклеотидов) и карнозина. β-Аланин необходим для синтеза карнозина и пантотеновой кислоты. β-Аланин также является агонистом глициновых рецепторов головного мозга. Принятый непосредственно в момент приливов β-аланин противодействует резкому высвобождению гистамина и брадикинина из тучных клеток, способствующих быстрому расширению сосудов кожи и покраснению. При этом β-аланин не блокирует Н1-рецепторы к гистамину и не обладает эффектами, присущими Н1-гистаминоблокаторам, в том числе и побочными (сухость во рту, сонливость и т.д.). Противодействие высвобождению гистаминолибераторов происходит по пути прямого стабилизирующего действия β-аланина на мембраны тучных клеток.
Эти механизмы воздействия β-аланина рассматриваются более подробно ниже.
Карнозин — дипептид, состоящий из β-аланина и гистидина. Карнозин максимально концентрируется в головном мозге и мышечной ткани, регулирует уровень внутриклеточного кальция и силу мышечного сокращения [46]. Карнозин обладает ярко выраженными антиоксидантными свойствами [47, 48], проявляет иммуномодулирующий эффект, поддерживая заживление ран [49]. Прием β-аланина увеличивает уровень карнозина в мышцах, уменьшает утомляемость и увеличивает работоспособность мышц [45]. Возможно, что достаточная обеспеченность карнозином нормализует работу мышечного слоя сосудов и тем самым способствует нормализации терморегуляции организма.
β-Аланин необходим для синтеза пантотеновой кислоты (витамин В5). Пантотеновая кислота в свою очередь необходима для синтеза ацилкоэнзима А — центрального кофермента биохимических путей, вовлеченных в метаболизм жиров, белков и углеводов. Ацилкоэнзим А необходим для ферментов цикла карбоновых кислот (цикл Кребса) и, таким образом, жизненно необходим для синтеза основного субстрата энергетического метаболизма — АТФ [50]. Так как В5 стимулирует процесс переработки жиров, прием препаратов пантотеновой кислоты обладает гиполипидемическим эффектом [51]. Симптомы дефицита витамина В5 схожи с симптоматикой дефицитов других витаминов группы В и включают астению, раздражительность, утомляемость и апатию, дерматиты, сухость кожи. Так как дефицит пантотеновой кислоты приводит к снижению синтеза ацетилхолина, неврологическая симптоматика гиповитаминоза В5 также включает парестезии и спазмы мышц. β-Аланин увеличивает уровни пантотеновой кислоты и способствует стабилизации энергетического метаболизма, что важно для нормализации терморегуляции.
Стабилизация энергетического метаболизма способствует уменьшению симптоматики приливов. Подобно тому, как интенсивный приток газа и кислорода стабилизирует пламя горелки, так и стабильный энергетический метаболизм позволяет избежать «всполохов», проявляющихся как приливы. В частности, поддержка энергетического метаболизма янтарной кислотой (основным метаболитом цикла трикарбоновых кислот) способствует ослаблению симптоматики приливов [52]. Частота приливов заметно уменьшается после еды и увеличивается в перерывах между приемом пищи, когда падает уровень глюкозы в крови [53]. Диетологи отмечают, что дробное питание (6-8 раз в день, небольшими порциями), особенно у пациенток с ожирением, часто способствует устранению приливов. Такая практика питания традиционна для стран Полинезии и Тайланда, где не только существенно реже встречаются ожирение и сахарный диабет, но и приливы у женщин в климактерии. Одним из эффектов такого рода дробного питания несомненно является стабилизация уровня глюкозы в крови. Уровни глюкозы коррелируют со встречаемостью приливов. У женщин с уровнем глюкозы более 130 мг/дл приливы отмечены значительно реже (p=0,04) по сравнению с пациентками, имевшими низкий уровень глюкозы (менее 110 мг/дл). Внутривенное введение раствора глюкозы приводило к значительному уменьшению числа приливов [54]. Важно также отметить, что одним из эффектов более опасных (по сравнению с глюкозой) эстрогеновых препаратов является именно уменьшение дефицита глюкозы в головном мозге [55]. Клималанин, влияя на уровни карнозина, синтез пантотеновой кислоты и уровни коэнзима А, стабилизирует энергетический метаболизм у женщины и стабилизирует отчасти и уровни глюкозы. С точки зрения влияния β-аланина на терапию приливов следует отметить прямое воздействие β-аланина на глициновые рецепторы центральной нервной системы (ЦНС). Хотя воздействие β-аланина на глициновые рецепторы несколько слабее, чем воздействие самого глицина, из всех известных агонистов глициновых рецепторов именно β-аланин занимает 2-е место [56]. То, что β-аланин является агонистом глициновых рецепторов, позволяет сделать обоснованное предположение о воздействии β-аланина на них. Поэтому далее рассматриваются эффекты глициновых рецепторов и самого глицина, а также проводится их сравнение с воздействием β-аланина. С одной стороны, глицин — тормозный нейротрансмиттер. Глициновые рецепторы (гены GLRA1, GLRA2, GLRA3 и GLRB) представляют собой лигандоуправляемые ионные каналы (рис. 3), имеющие ГАМК-подобную активность и расположенные, как правило, на постсинаптических мембранах. С другой стороны, глицин связывается со специфическими сайтами NMDA-рецепторов и, таким образом, способствует передаче сигнала от возбуждающих нейротрансмиттеров глутамата и аспартата. В отличие от глицина β-аланин связывается только с глициновыми рецепторами типа управляемых ионных каналов; данных о взаимодействии β-аланина с NMDA-рецепторами не имеется.
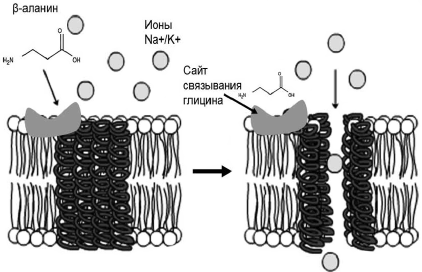
Рис. 3. Глициновые рецепторы действуют как лигандуправляемые ионные каналы. Связывание глицина (или β-аланина) рецептором увеличивает поток хлоридионов через плазматическую мембрану нейрона.
Большая плотность глициновых рецепторов обнаружена не только в структурах ствола, но и в коре больших полушарий, мозжечке, стриатуме, ядрах гипоталамуса. Основная масса глицина сосредоточена в спинном мозге, где аминокислота опосредует постсинаптическое торможение моторных нейронов. Поэтому глицин как препарат используется в неврологической практике для устранения повышенного мышечного тонуса и тремора. Генетически обусловленные дефекты глициновых рецепторов связаны с повышенным мышечным тонусом, акинезией и крайне обостренной реакцией на стимулы. С другой стороны, активация глициновых рецепторов оказывает седативное, транквилизирующее и антидепрессивное действие, усиливает действие противосудорожных препаратов, антидепрессантов, улучшает память и ассоциативные процессы. Особенно важно назначение глицина для смягчения абстинентного синдрома у алкоголиков, снятия симптоматики тремора. Представляет интерес тот факт, что глициновые рецепторы также взаимодействуют с генистеином, одним из активных компонентов соевых экстрактов. Как было отмечено ранее, соевые экстракты значительно способствуют ослаблению симптоматики приливов [16, 17].
Таким образом, следует отметить двойственную роль глицина в ЦНС -воздействие и на глициновые, и на глутаматные рецепторы. В то же время β-аланин воздействует, по всей видимости, только на глициновые рецепторы. Кроме того, глицин быстро метаболизируется, так как глицин как общераспространенная протеиногенная аминокислота включается в состав белков. Следовательно, для достижения заметных клинических эффектов необходимы высокие дозы глицина (граммы). β-Аланин, также являясь агонистом глициновых рецепторов, не включается в состав белков и метаболизируется в организме гораздо медленнее [57]. Как результат, значительно меньшие дозы β-аланина будут необходимы для достижения клинически наблюдаемых эффектов терапии. Следовательно, препарат Клималанин реализует свои клинические эффекты при приливах через участие в синтезе: 1) карнозина, 2) пантотеновой кислоты; 3) модуляции активности глициновых рецепторов. Предлагаемые механизмы терапевтического воздействия Клималанина при приливах отражены на рис. 4.
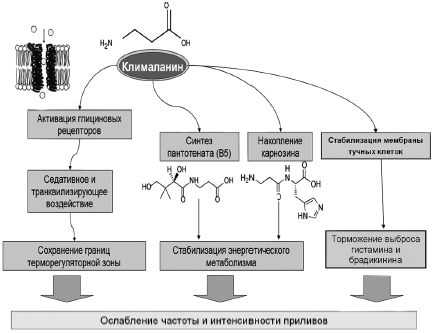
Рис. 4. Предлагаемые механизмы терапевтического воздействия препарата Клималанин при приливах.
«Препарат Клималанин выпускают в таблетках по 400 мг, применяют внутрь по 1-2 таблетки в сутки. Доза может быть увеличена до 3 таблеток в сутки (1200 мг β-аланина). Длительность лечения составляет 5-10 дней, до исчезновения «приливов». При возобновлении симптомов следует провести повторный курс лечения. Клималанин может реализовывать быстрый и медленный ответы на прием препарата у пациентов. Начало реализации быстрого ответа исчисляется от нескольких до 15-30 мин. Быстрый ответ Клималанина опосредован прямым взаимодействием β-аланина на глициновые рецепторы преоптической области гипоталамуса, что приведет к торможению избыточной активности терморегуляторного центра. За счет накопления карнозина и пантотеновой кислоты в клетках, постепенной стабилизации энергетического метаболизма при длительном приеме β-аланина не исключено развитие накопительного защитного эффекта, предотвращающего приливы. Этот аспект может быть очень перспективным в плане дальнейшего изучения действия препарата. Энергетическая стабильность способствует увеличению резервов адаптации организма женщины к пониженному уровню эстрогенов. Именно поэтому препарат Клималанин может быть рекомендован женщинам с приливами в период менопаузы в качестве монотерапии, а также в составе комплексной терапии с эстрогенами для уменьшения дозы последних. Особенно следует подчеркнуть, что применение Клималанина у пациенток с генетической предрасположенностью к приливам (нуклеотидные полиморфизмы генов CYP1B1, CYP19, ERbeta и Eralpha) является высокоэффективным средством из разряда так называемой персонализированной медицины [58].
Заключение
Приливы — одна из наиболее часто встречающихся жалоб при менопаузе. Вазомоторные пароксизмы — не что иное как проявления дезадаптационного синдрома на фоне снижения активности яичников в период менопаузы. Снижение уровня эстрогенов с наступлением менопаузы является нормой и отражает нормальный ход биологических часов. Поэтому борьба с вазомоторной симптоматикой при менопаузе посредством эстроген-терапии далеко не всегда оправданна. Более того, у 10-20% пациенток ЗГТ эстрогенами не имеет никакого эффекта, а у 20-30% пероральные эстрогены противопоказаны из-за резкого увеличения риска онкологических, сердечно-сосудистых и цереброваскулярных заболеваний. Недостатки эстрогеновой терапии (которые, к сожалению, зачастую замалчиваются) стимулируют поиск новых, альтернативных подходов к терапии приливов. Клималанин способствует стабилизации энергетического метаболизма через накопление карнозина, пантотеновой кислоты и оказывает седативное воздействие на вазомоторные пароксизмы посредством активации глициновых рецепторов. Представленный в настоящей работе новый взгляд на патофизиологию приливов и механизмы молекулярного воздействия β-аланина позволяет проанализировать фармакодинамические свойства препарата Клималанина в качестве достойной альтернативы терапии приливов. Особенно важно, что β-аланин способен проявлять быстрое действие на приливы, т.е. «гасить» возникновение приступов вегетососудистых пароксизмов и клинические проявления приливов в считанные минуты после применения.
Литература
1. Freeman EW, Sherif K. Prevalence of hot flushes and night sweats around the world: a systematic review. Climacteric 2007; 10 (3): 197-214.
2. Shanafelt TD, Barton DL, Adjei AA, Loprinzi CL Pathophysiology and treatment of hot flashes. Mayo Clin Proc 2002; 77 (11): 1207-18.
3. Maclennan AH, Broadbent JL, Lester S, Moore V. Oral oestrogen and combined oestrogen/progestogen therapy versus placebo for hot flushes. Cochrane Database Syst Rev 2004; 1052 (4): CD002978.
4. Rabin DS, Cipparrone N, Linn ES, Moen M. Why menopausal women do not want to take hormone replacement therapy. Menopause 1999; 6 (1): 61-7.
5. RossouwJE, Anderson GL, Prentice RL, LaCroix AZ, WHI Investigators. Risks and benefits of estrogen plus progestin in healthy postmenopausal women: Women’s Health Initiative randomized controlled trial. JAMA 2002; 288 (3): 321-33
6. Lacey JV, Mink PJ, Lubin JH et al. Menopausal hormone replacement therapy and risk of ovarian cancer. JAMA 2002; 288 (3): 334-41.
7. Coughlin SS, Giustozzi A, Smith SJ, Lee NC. A metaanalysis of estrogen replacement therapy and risk of epithelial ovarian cancer. J Clin Epidemiol 2000; 53 (4): 367-75.
8. Tanis BC, van den Bosch MA, Kemmeren JM et al. Oral contraceptives and the risk of myocardial infarction. N Engl J Med 2001; 345 (25): 1787-93
9. Reynolds RF, Obermeyer CM, Walker AM et al. Side effects and sociobehavioral factors associated with the discontinuation of hormone therapy in a Massachusetts health maintenance organization. Menopause 2001; 8 (3): 189-99.
10. Nelson HD, Vesco KK, Haney E et al. Nonhormonal therapies for menopausal hot flashes: systematic review and meta-analysis. JAMA 2006; 295 (17): 2057-71.
11. Nachtigall LE, Baber RJ, Barentsen R et al. Complementary and hormonal therapy for vasomotor symptom relief: a conservative clinical approach. J Obstet Gyn Can 2006; 28 (4): 279-89.
12. Shen W, Stearns V. Treatment strategies for hot flushes. Expert Opin Pharmacother 2009; 10 (7): 1133-44.
13. Melis GB, Gambacciani M, Cagnacci A et al. Effects of the dopamine antagonist veralipride on hot flushes and luteinizing hormone secretion in postmenopausal women. Obstet Gyn 1988; 72 (5): 688-92.
14. Barton DL, Loprinzi CL, Quella SK et al. Prospective evaluation of vitamin Efor hot flashes in breast cancer survivors. J Clin Oncol 1998; 16 (2): 495-500.
15. Bourre JM. Dietary omega-3 fatty acids for women. Biomed Pharmacother 2007; 61 (2-3): 105-12.
16. Kurzer MS. Soy consumption for reduction of menopausal symptoms. Inflammopharmacology 2008; 16 (5): 227-9.
17. Williamson-Hughes PS, Flickinger BD, Messina MJ, Empie MW. Isoflavone supplements containing predominantly genistein reduce hotflash symptoms: a critical review of published studies. Menopause 2006; 13 (5): 831-9.
18. Carroll D.G. Nonhormonal therapies for hot flashes in menopause. Am Fam Physician 2006; 73 (3): 457-64.
19. Toulis KA, Tzellos T, Kouvelas D, Goulis DG. Gabapentin for the treatment of hotflashes in women with natural or tamoxifen-induced menopause: atematic review and meta-analysis. Clin Ther 2009; 31 (2): 221-35.
20. Hunter M, Rendall M. Bio-psycho-socio-cultural perspectives on menopause. Best Pract Res Clin Obstet Gyn 2007; 21 (22): 261-74.
21. Ланг Г.Ф. Учебник внутренних болезней. Т. I, ч. 1. Л.: Медгиз, 1938.
22. Chattha R, Nagarathna R, Padmalatha V, Nagendra HR. Effect of yoga on cognitive functions in climacteric syndrome: a randomised control study. B]OG 2008; 115 (8):991-1000.
23. Сметник В.П. Приливы: загадка климактерия. Климактерий. 2009; 1.
24. Arendt M, Rosenberg R, Foldager L et al. Withdrawal symptoms do not predict relapse among subjects treated for cannabis dependence. Am J Addict 2007; 16 (6): 461-7.
25. Crawford SJ. Hot flushes and cold turkey. Br Med J 1977; 1 (6076): 1599.
26. Casper RF, Yen SS. Neuroendocrinology of menopausal flushes: an hypothesis offlush mechanism. Clin Endocrinol (Oxf) 1985; 22 (3): 293-312.
27.Andrikoula M, Prelevic G. Menopausal hot flushes revisited. Climacteric 2009; 12 (1): 3-15.
28. Freedman RR, Krell W. Reduced thermoregulatory null zone in postmenopausal women with hot flashes. Am J Obstet Gyn 1999; 181 (1): 66-70.
29. RosenbergJ, Larsen SH. Hypothesis: pathogenesis of postmenopausal hot flush. Med Hypotheses 1991; 35 (4): 349-50.
30. Freedman RR, Norton D, Woodward S, Cornelissen G. Core body temperature and circadian rhythm of hot flashes in menopausal women. Clin Endocrinol Metab 1995; 80 (8): 2354-8.
31. Schurz B, Wimmer-Greinecker G, Metka M et al. Beta-endorphin levels during the climacteric period. Maturitas 1988; 10 (1): 45-50.
32. Gonzales GF, Carrillo C. Blood serotonin levels in postmenopausal women: effects of age and serum oestradiol levels. Maturitas 1993; 17 (1): 23-9.
33. Berendsen HH. The role of serotonin in hotflushes. Maturitas 2000; 36 (3): 155-64.
34. Yuri K., Kawata M. Estrogen receptor-immunoreactive neuron contain calcitonin gene-related peptide, methionine-enkephalin or tyrosine hydroxylase in the female rat preoptic area. Neurosci Res 1994; 21 (2): 135-41.
35. Yuri K, Kawata M. Estrogen affects calcitonin gene-related peptide- and methionine-enkephalin-immunoreactive neuron in thefemale rat preoptic area. Neurosci Lett 1994; 169 (1-2): 5-8.
36. Yuri K, Kawata M. Time-course analysis of changes in calcitonin gene-related peptide-and methionine-enkephalin-immunoreactivity in thefemale rat preoptic area after estrogen treatment. Neuroscience 1993; 55 (4): 1067-74.
37. Yuri K, Kawata M. Semi-quantitative analysis of the effects of estrogen on CGRP-immunoreactivity in the periventricular preoptic nucleus and the medial preoptic area of female rats. Brain Res 1992; 578 (1-2): 282-8.
38. Wyon Y, Frisk J, Lundeberg T et al. Postmenopausal women with vasomotor symptoms have increased urinary excretion of calcitonin gene-related peptide. Maturitas 1998; 30 (3): 289-94.
39. Wyon YA, Spetz AC, Theodorsson GE, Hammar ML. Concentration of calcitonin gene-related peptide and neuropeptide Y in plasma increase during fluhes in postmenopausal women. Menopause 2000; 7 (1): 25-30.
40. Valentini A, Petraglia F, De Vita D et al. Changes of plasma calcitonin gene-related peptide levels in postmenopausal women. Am] Obstet Gyn 1996; 175 (3 Pt 1): 638-42.
41. Gupta P, Harte A, Sturdee DW et al. Effects of menopausal status on circulating calcitonin gene-related peptide and adipokines: implications for insulin resistance and cardiovascular risks. Climacteric 2008; 11 (5): 364-72.
42. Salem N, Dunbar JC. The insulin-mediated vascular and blood pressure responses are suppressed in CGRP-deficient normal and diabetic rats. Diabetes Metab Res Rev 2002; 18 (3): 238-44.
43. Pettersson M, Ahren B. Insulin and glucagon secretion in rats: effects of calcitonin gene-related peptide. Regul Pept 1988; 23 (1): 37-50.
44. Derave W, Ozdemir MS, Harris RC, PottierA. beta-Alanine supplementation augments muscle carnosine content and attenuates fatigue during repeated isoki-netic contraction bouts in trained sprinters. J Appl Physiol 2007; 103 (5): 1736-43.
45. Hill CA, Harris RC, Kim HJ et al. Influence of beta-alanine supplementation on skeletal muscle carnosine concentrations and high intensity cycling capacity. Amino Acids 2007; 32 (2): 225-33.
46. Zaloga GP, Roberts PR, Nelson TE. Carnosine: a novel peptide regulator of intracellular calcium and contractility in cardiac muscle. New Horiz 1996; 4 (1): 26-35.
47. Klebanov GI, Teselkin YuO, Babenkova IV et al. Effect of carnosine and its components on free-radical reactions. Membr Cell Biol 1998; 12 (1): 89-99.
48. Babizhayev MA, Seguin MC, Gueyne J et al. L-carno-sine act as natural antioxidants. Biochem J 1994; 304 (Pt 2) (8): 509-16.
49. Nagai K, Suda T. Realization of spontaneous healing function by carnosine. Methods Find Exp Clin Pharmacol 1988; 10 (8):497-507.
50. Voet D, VoetJG, Pratt CW. Fundamentals of Biochemistry: Life at the Molecular Level, 2nd ed. Hoboken, 2006 NJ:John Wiley & Sons, Inc.
51. Naruta E, Buko V. Hypolipidemic effect of pantothenic acid derivatives in mice with hypothalamic obesity induced by aurothioglucose. Exp Toxicol Pathol 2001; 53 (5): 393-8.
52. Peskov AB, Maevskii EI, Uchitel’ ML et al. Succinate-based preparation alleviates manifestations of the climacteric syndrome in women. Bull Exp Biol Med; 2005 Sep; 140(3):312-4.
53. Dormire S, Howharn C. The effect of dietary intake on hotflashes in menopausal women. J Obstet Gynecol Neonatal Nurs 2007;36 (3): 255-62.
54. Dormire SL, Reame NK. Menopausal hot flash frequency changes in response to experimental manipulation of blood glucose. Nurs Res 2003; 52 (5): 338-43.
55. Ratka A. Menopausal hot flashes and development of cognitive impairment. Ann N Y Acad Sci 2005; 1052 (3): 11-26.
56. HenleyJM. Encyclopedia of Life Sciences Amino Acid Neurotransmitters. 2001]ohn Wiley & Sons, Ltd.
57. Harris RC, Tallon MJ, Dunnett M et al. The absorption of orally supplied beta-alanine and its effect on muscle carnosine synthesis in human vastus lateralis. Ammo Acids 2006; 30 (3): 279-89.
58. Malacara JM, Perez-Luque EL, Martinez-Garza S, Sanchez-Marin FJ. The relationship of estrogen receptor-alpha polymorphism with symptoms and other characteristics in post-menopausal women. Maturitas 2004; 49 (2): 163-9.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Период менопаузы у женщины характеризуется понижением уровня в ее организме таких гормонов, как прогестерон и эстроген, а также перестройкой в работе всех внутренних органов на новый режим. Такая перестройка влияет на протяженность болезней, усиливает хронические заболевания и может вызывать осложнения.
Период климакса у женщины может иметь такие явления:
- Внезапные перепады настроения.
- Повышение потливости (см. как справиться с приливами при климаксе).
- Беспричинный жар.
Для правильной терапии, которая помогает справиться с вышеприведенными состояниями и ослабить их действие, назначается Бета-Аланин. Он прекрасно подходит для борьбы с негативными симптомами климакса и противостоит различным некомфортным проявлениям, которые вызываются нарушением работы центра терморегуляции в гипоталамусе. Кроме этого, он успешно может справиться с пониженным формированием специальных гормонов яичниками в нормальном количестве и качестве.
Что это за препарат?
В большинстве случаев при подборе подходящей схемы лечения климакса основное внимание уделяется эффективному устранению проявления приливов, иными словами, стабилизировать функциональность центра терморегуляции.
При таком лечении могут назначаться гормональные препараты, однако существует вариант, который прекрасно улучшает самочувствие и пополняет недостаток эстрогенов фитоэстрогенами – препарат Бета-аланин.
Бета-аланин является аминокислотой, которая в организме человека может самостоятельно вырабатываться. Проблема состоит в том, что в период климакса эта аминокислота образуется в малых количествах, а это приводит к нарушению терморегуляции организма. Поэтому пополнять запасы этой кислоты необходимо медикаментозным путем.
Бета-аланин при климаксе сдерживает внезапный выброс в огромном количестве гистамина, который оказывает негативное влияние на вегетативные процессы и расширяет периферические сосуды. Аминокислота, которая в достаточном количестве для организма находится в препарате, способна эффективно справляться с:
- чрезмерным потоотделением;
- сильными головными болями;
- приливами.
Такое воздействие происходит за счет насыщения периферических рецепторов нейротрансмиттеров.
Согласно исследованиям ученных было выявлено, что аминокислота Бета-аланина успешно снижает количество и тяжесть приливов, а это является настоящим спасением для большинства женщин в период климакса.
Кроме этого, Бета-аланин способствует выведению из организма молочной кислоты, которая застаивается в мышцах и увеличивает степень утомляемости.
Благодаря этому женщина при климаксе может:
- Быть более устойчивой к различным заболеваниям, так как повышается иммунитет.
- Успешно справляться с серьезными стрессовыми ситуациями.
- Эффективно заострять внимание на важных моментах.
- Плодотворно работать без лишнего недомогания.
ВАЖНО! Beta-Alanine (β-Alanine) выпускается в формах разных препаратов: «Клималанин», «Ци-клим аланин» (Эвалар) и т.п. Зачастую цена у этих препаратов завышена. В любом спортивном магазине можно купить «Beta Alanine» с этим же составом, но по значительно низкой цене. Попробуйте, если вам подходит данный препарат, как говорится, зачем платить больше.
Врачи отмечают, что применение бета-аланина при климаксе может иметь как положительные, так и отрицательные аспекты. С одной стороны, этот аминокислотный препарат может способствовать улучшению физической выносливости и снижению усталости, что особенно важно для женщин в период гормональных изменений. Некоторые исследования показывают, что бета-аланин может помочь в поддержании мышечной массы и улучшении общего самочувствия.
С другой стороны, специалисты предупреждают о возможных побочных эффектах, таких как покалывание и дискомфорт в коже, что может быть неприятно для некоторых пациентов. Кроме того, недостаток долгосрочных исследований о влиянии бета-аланина на здоровье женщин в период климакса вызывает опасения. Врачи рекомендуют подходить к его применению с осторожностью и обязательно консультироваться с медицинским специалистом перед началом приема.

#Климакс бета аланин приливы #эндокринолог
Полезные свойства
Бета-аланин обладает такими свойствами:
- Влияет на работу нервной системы. Во время приема препарата устраняются внезапные перепады в настроении, улучшается внимание, реакция.
- Влияет на защитные функции организма. В организме укрепляется иммунитет и устойчивость к инфекционным заболеваниям, а также повышается антиоксидантная функция.
- Увеличивается анаэробная сила. Благодаря этому женщина становиться более активной и энергичной.
- Увеличивается уровень карнозина, который отвечает за структуру тела и уровень рН в мышечной ткани. Нормализует обмен веществ, так что женщины во время менопаузы не набирают лишних килограммов.
Однако при всей полезности препарата принимать его следует согласно четким назначениям врача. Каждый организм индивидуален, поэтому дозу препарата следует приписывать в зависимости от тяжести симптоматики во время климакса.
Бета-аланин приписывают при средней степени симптомов по 2 таблетки в сутки, но при сильных приливах и эмоциональных расстройствах, препарат могут назначить три раза в сутки.
Начинать принимать Бета-аланин каждый может самостоятельно, однако грамотное назначение курса, который сможет вам действительно помочь, может приписать только квалифицированный гинеколог-терапевт.
Бета-аланин, как добавка, вызывает интерес у женщин, переживающих климакс. Многие отмечают его положительное влияние на уровень энергии и выносливость, что особенно важно в этот период, когда физическая активность может снижаться. Пользователи сообщают о снижении чувства усталости и улучшении настроения, что может быть связано с улучшением общего самочувствия.
Однако не все так однозначно. Некоторые женщины отмечают, что у них возникают побочные эффекты, такие как покалывание кожи, что может быть неприятным. Кроме того, недостаток исследований на тему влияния бета-аланина именно в период климакса вызывает опасения. Важно помнить, что перед началом применения любых добавок стоит проконсультироваться с врачом, чтобы избежать возможных негативных последствий и подобрать оптимальный подход к своему здоровью.
В чем смысл применения Бета-Аланина при климаксе у женщин?
Препарат способствует укреплению иммунной системы и уменьшает риск появления песка и иных образований в почках. Также Бета-аланин прекрасно подходит для смягчения протекания эпилептических приступов и лечения гипогликемии. Он является отличным источником жизненной энергии, которая помогает активно работать головному мозгу и центральной нервной системе.
Во время климакса Бета-аланин достаточно эффективно борется с вегетативными симптомами – приливами. Такие процессы обусловлены наступлением естественной или искусственной менопаузой, предменопаузой или постменопаузой.
Бета-аланин назначается женщинами при климаксе в том случае, когда применение гормональных препаратов запрещено. В некоторых случаях препарат назначают перед началом приема гормональных средств. Если Бета-аланин прекрасно справляется со всеми неприятными симптомами климакса, то гормональную терапию могут и не назначать.
Согласно клиническим исследованиям, Бета-аланин хорошо переносится большинством пациентов. Во время испытания не было выявлено негативного влияния на функционирование кроветворной системы, а также препарат не провоцирует развитие сердечных и сосудистых болезней. Кроме этого, на протяжении приема негормонального средства не было обнаружено отрицательного влияния на работу почек или печени.
Преимуществом Бета-аланина является его способность выводит излишнюю жидкость из организма и не накапливать ее в тканях. Если сравнивать с гормональной терапией, то женщина стремительно набирает вес, в первую очередь, за счет накопления ненужной жидкости в организме.
Длительный прием препарата не вызывает развитие сонливости и потерю концентрации внимания за счет отсутствия антигистаминных веществ в нем. В противоположность этому, если долго принимать Бета-аланин, то в клетках происходит накопление карнозина и пантотеновой кислоты, которые улучшают метаболические и энергетические процессы.
После окончания курса терапии Бета-аланином лечащий врач может снова его назначить, так как препарат не вызывает зависимости.

Бета-аланин от климакса
Вопрос-ответ
Как бета-аланин влияет на женский организм?
Аминокислота широко используется для лечения климакса. На этом этапе в теле женщины происходит спад уровня эстрогена, что может повлиять на ее общее состояние. Прием добавок с бета-аланином снижает негативные проявления менопаузы, такие как приливы, утомляемость, эмоциональные перепады.

Что будет если принимать Бета Аланин
Есть ли какие-либо негативные эффекты бета-аланина?
Одним из наиболее часто встречающихся побочных эффектов приема бета-аланина является парестезия — ощущение покалывания, часто описываемое как щекотание.
Можно ли пить бета-аланин при климаксе?
β-аланин показан женщинам для коррекции вазомоторных проявлений дефицита эстрогенов в период менопаузы в качестве монотерапии, а также в составе комплексной терапии (совместно с ЗГТ) для снижения дозы эстрогенов.
Какие могут быть побочки от бета-аланина?
Бета-аланин — побочные эффекты. Поскольку бета-аланин может активировать нервные рецепторы под кожей, иногда в результате приема более высокой порции препарата может наблюдаться парестезия, то есть ощущение покалывания или пощипывания, а также зуд кожи.
Советы
СОВЕТ №1
Перед началом приема Бета-Аланина обязательно проконсультируйтесь с врачом. Это поможет избежать возможных побочных эффектов и убедиться, что добавка подходит именно вам.
СОВЕТ №2
Обратите внимание на дозировку. Начните с низкой дозы и постепенно увеличивайте ее, чтобы организм смог адаптироваться и минимизировать риск неприятных ощущений, таких как покалывание.
СОВЕТ №3
Сочетайте прием Бета-Аланина с физической активностью. Это может помочь улучшить его эффективность и повысить общее состояние здоровья во время климакса.
СОВЕТ №4
Следите за своим самочувствием. Ведите дневник, в котором будете отмечать изменения в состоянии здоровья и настроении, чтобы оценить влияние Бета-Аланина на ваш организм.

Три варианта лечения климакса: какой выбрать?
Менопауза – естественный этап в жизни каждой женщины. Однажды ее репродуктивная функция вполне планово вступает в стадию угасания, яичники начинают вырабатывать меньше женских гормонов…
Климакс – не болезнь, а естественное явление. Это постепенное угасание репродуктивной функции женского организма. Начинается менопауза со снижения выработки половых гормонов в яичнике. Поэтому «вылечить» климакс, конечно же, нельзя.
Однако 70 % женщин мучаются от неприятных проявлений, которые едва ли можно назвать естественными:
- «приливы», напоминающие подъем температуры, которой реально нет;
- сильная потливость,
- учащенное сердцебиение,
- беспричинный страх, особенно по ночам,
- перепады настроения, раздражительность,
- неприятные ощущения сухости в половых органах;
- ухудшение состояния кожи, волос и ногтей.
Эти признаки климакса вызваны гормональной перестройкой. К несчастью, климактерический период может длиться до десяти лет. Это огромный срок, на который раньше женщина фактически «вычеркивалась» из жизни. Но сегодня ситуация изменилась. Медицина предлагает женщинам доступные способы борьбы с симптомами климакса.
Первый вариант. Гормональная терапия
Заместительная гормональная терапия (ЗГТ) направлена именно на устранение причины неприятных симптомов климакса. Не хватает эстрогенов и прогестерона? Получите синтетические гормоны извне. Казалось бы, решение идеальное! Ведь проявления климакса полностью исчезают или сводятся к минимуму.
Важно помнить: гормоны применяют в малых дозировках, но ежедневно. Препараты подбираются гинекологом-эндокринологом индивидуально, на основании анализов. А каждые полгода доза должна корректироваться врачом после сдачи анализов.
Но у каждой медали две стороны. Гормоны нельзя принимать всю жизнь. Через несколько лет постоянного приема или по достижении шестидесятилетнего возраста их придется отменить, чтобы избежать онкологических заболеваний и когнитивных расстройств.
У приема гормонов много противопоказаний:
- сахарный диабет,
- сердечно-сосудистые заболевания,
- гипертония,
- нарушение свертываемости крови,
- тромбофлебит,
- заболевания желчного пузыря,
- новообразования, в том числе миома матки,
- мастопатия,
- тяжелые болезни печени и почек,
- эпилепсия,
- тяжелое течение варикоза,
- эндометриоз.
Кроме того, не все женщины имеют возможность раз в полгода посещать врача и сдавать анализы. Многие гормональные препараты не относятся к категории дешевых. Тем более, что неизвестно, как долго организм будет требовать гормональной поддержки. Нередко женщины пытаются найти более бюджетные варианты гормонов или без консультации врача принимают те, что посоветовала подруга или родственница. Результатом такой «гормональной поддержки» могут стать психоэмоциональные расстройства, снижение интеллекта, отеки, доброкачественные опухоли, инсульты… Вот почему самолечение и неграмотное «лечение» гормонами недопустимо!
Прием гормонов стоит рассматривать как подходящий вариант в следующих случаях:
- Ранний климакс, начавшийся до 40 лет.
- Тяжелое течение климакса: сильные нарушения самочувствия во время приливов, более 20 приливов в сутки.
- Гипертоническая болезнь, атеросклероз, остеопороз, возникшие вследствие климакса или быстро прогрессирующие.
При невозможности или нежелании принимать гормоны есть негормональные средства, которые тоже помогают справиться с проявлениями менопаузы. Негормональные средства применяют при климаксе среднего (до 20 приливов в день) и легкого (до 10) течения.
Второй вариант. Негормональные препараты: бета-аланин или фитоэстрогены
Долгое время у гормонов было всего две альтернативы. Женщине предлагали или бета-аланин, или фитоэстрогены. Каждое из этих веществ приносит пользу при климаксе.
Бета-аланин – естественная аминокислота. В период менопаузы она помогает справиться с приливами. Чувство жара возникает, когда сосуды «гонят» кровь к коже, так как организм «считает», что он перегрелся и следует «отвести» лишнее тепло через кожу. Бета-аланин регулирует тонус сосудов. В результате прилив останавливается в самом начале. «Быстрое» действие бета-аланина наступает через полчаса после приема, что позволяет его применять для профилактики приливов во время важных и ответственных событий, встреч и т.д.
Второе, «медленное» действие бета-аланина заключается в том, что, накапливаясь, он стабилизирует центр терморегуляции. При нехватке бета-аланина границы этого участка в мозге размываются, и в результате организм не может отличить нормальную температуру от повышенной.
Недостаток бета-аланина: он «работает» только с приливами, мало влияя на другие проявления климакса, и не предотвращает связанные с ним нежелательные изменения.
Самые распространенные препараты бета-аланина: Ци-Клим Аланин, Клималанин.
Вторая группа негормональных «помощников» – фитоэстрогены. Эти вещества получают из сои, красного клевера и некоторых других растений. Они действуют на те же рецепторы в организме, что и «собственные» гормоны, но несколько слабее. Когда «своих» гормонов не хватает, фитоэстрогены частично восполняют их недостаток. Так ослабляются проявления климакса, уменьшается риск развития сопутствующих заболеваний.
Фитоэстрогены действуют в нескольких направлениях:
- Снижают частоту и выраженность приливов легкой и средней тяжести.
- Улучшают состояние слизистых, также уменьшают дискомфорт в мочеполовых органах.
- Снижают риск развития остеопороза и сердечно-сосудистых заболеваний.
В Европе фитоэстрогены нередко назначают женщинам с 35 лет в профилактических целях.
Однако у фитоэстрогенов есть существенный недостаток. По сравнению с гормонами они действуют слабее, не могут быстро, в течение нескольких минут, купировать приливы. Препараты с фитоэстрогенами: Ци-Клим, Эстровэл, Ледис Формула.
Третий вариант. Комплекс фитоэстрогенов и бета-аланина
Логично, что ученые пришли к естественному решению и объединили оба вида негормональных средств борьбы с климаксом, чтобы лишить их недостатков.
В России сейчас только один такой препарат: Менсе – негормональный комплекс для женщин в период менопаузы.
Благодаря входящим в состав Менсе бета-аланину и фитоэстрогенам сои достигается двойной эффект:
1. Приливы быстро купируются.
2. Уменьшатся частота и выраженность приливов в будущем.
В составе Менсе содержатся другие вещества (витамины-антиоксиданты), витамины группы В и 5-гидрокситриптофан. Из-за комплексного состава Менсе влияет на большинство проявлений климакса:
- Уменьшаются периоды сердцебиений.
- Улучшается сон и эмоциональный фон, снижается тревожность и подавленность.
- Уменьшаются неприятные ощущения в половых органах.
- Нормализуется аппетит, пропадает тяга к сладкому, благодаря чему прекращается набор веса.
- Снижается вероятность сопутствующих климаксу заболеваний, в том числе остеопороза.
Практика показывает, что действие Менсе становится более выраженным по мере увеличения длительности его приема. А ограничений по курсу приема у Менсе нет, ведь в составе отсутствуют гормоны и другие вещества, которые нельзя принимать постоянно.

Помните, что правильно выбранный препарат сглаживает неприятные проявления менопаузы, возвращая женщине привычное качество жизни.
ПРОЙДИТЕ ТЕСТ для определения тяжести течения климактерического синдрома и получите ПЕРСОНАЛЬНЫЕ РЕКОМЕНДАЦИИ в период менопаузы на сайте mense.ru!
Пройти тест
НЕ ЯВЛЯЕТСЯ РЕКЛАМОЙ. МАТЕРИАЛ ПОДГОТОВЛЕН ПРИ УЧАСТИИ ЭКСПЕРТОВ.
«Быстрый эффект» клималанина (бета-аланина)
при приливах: сравнительное исследование
взаимодействий бета-аланина, таурина и глицина
с глициновыми рецепторами
Торшин И.Ю., Громова О.А., Лиманова О.А.,
Российский сателлитный центр института микроэлементов ЮНЕСКО, Москва
Кафедра фармакологии и клинической фармакологии ГБОУ ВПО Ивановская государственная медицинская академия Минздравсоцразвития РФ
- →
Абстракт
Бета-аланин – неканоническая аминокислота, содержащаяся в препарате клималанин, использующаяся в терапии «приливов» и позволяющая быстро, в течение считанных минут, купировать возникающий сосудистый пароксизм. В настоящей работе впервые проведено сравнительное биофизическое моделирование взаимодействий бета-аланина с пространственной структурой глициновых рецепторов. Показано, что энергия связывания рецептором бета-аланина превышает энергию связывания самого глицина, что соответствует пролонгированному (по сравнению с глицином) воздействию препаратов бета-аланина на глициновые рецепторы, оказывая нормализующее действие на терморегуляцию и вазомоторику.
Ключевые слова: приливы, бета-аланин, «быстрый эффект», глициновые рецепторы, терморегуляция, клималанин.
Rapid effect of beta-alanine in the therapy of hot flashes: a comparative biophysical modeling of interactions beta-alanine, taurine and glycine with the glycine receptors
Torshin I.Y., Gromova O.A., Limanova O.A.
Abstract
Beta-alanine is a noncanonical amino acid used in the treatment of hot flashes. In this paper we present the results of biophysical modeling of the interactions of ligands with glycine receptors. It is shown that the binding energy of the receptor beta-alanine greater than the binding energy of the glycine, which corresponds to the prolonged (compared with glycine) effects of beta-alanine on glycine receptors.
Key words: hot flashes, beta-alanine, rapid effects, glycine receptors, thermoregulation, klimalanin.
Cпецифические вегетативно-сосудистые пароксизмы – так называемые приливы – быстро развивающийся вазомоторный симптомокомплекс в перименопаузе. Субъективно «прилив» можно описать как внезапную волну интенсивного тепла и даже жара по телу, сопровождающуюся профузным потоотделением, тахикардией и у многих пациенток подъемом артериального давления.
Препараты для «быстрого» купирования возникающих пароксизом практически неизвестны. Наиболее часто в терапии приливов используется заместительная гормональная терапия (ЗГТ) препаратами эстрогенов. Эффекты синтетических эстрогенов развиваются постепенно, в течение недель и месяцев [1, 2]. Кроме того, пероральная ЗГТ может приводить к головной боли и повышает риск рака молочной железы, яичников, матки, венозной тромбоэмболии [3–6], что простимулировало проведение многочисленных исследований альтернативных видов терапии приливов [7].
Накапливающиеся клинические данные позволяют утверждать, что бета-аланин может купировать приливы в течение нескольких минут. Молекулярно физиологический механизм развития столь «быстрого» эффекта бетааланина не вполне ясен. Фармакологическое действие бетааланина объяснимо с точки зрения гормональнонейротрансмиттерного подхода [8] через воздействие на терморегуляторное ядро в преоптической области гипоталамуса. В терморегуляторном ядре содержатся многочисленные типы рецепторов, которые могут влиять на терморегуляцию: рецепторы гаммааминомасляной кислоты (ГАМК) [9], гистаминовые [10], альфаадренергические [11], допаминовые [12], простагландиновые [13, 14], глутаматные, холинергические [15] и глициновые рецепторы [16].
В настоящей работе рассматриваются молекулярнобиофизические механизмы глициновых рецепторов. Интерес к глициновым рецепторам обусловлен тем, что среди вышеперечисленных рецепторов взаимодействие бетааланина было достоверно доказано только для глициновых рецепторов [8]. Взаимодействуя с глициновыми рецепторами, бета-аланин может способствовать «быстрой» нормализации активности терморегуляторной зоны гипоталамуса, а через синтез пантотената (витамин В5) и накопление карнозина бета-аланин способствует стабилизации энергетического метаболизма, что также соответствует ослаблению симптоматики приливов (рис. 1).
Заметим, что «медленные» эффекты бета-аланина (дни-недели), обусловленные воздействием на энергетический метаболизм (синтез карнозина и пантотената), не менее важны, чем «быстрые» эффекты бета-аланина (минуты), обусловленные взаимодействиями с глициновыми рецепторами (и, возможно, с рецепторами других типов). Стабилизация энергетического метаболизма способствует уменьшению симптоматики приливов [16–19].
Прием бета-аланина постепенно увеличивает уровни карнозина в мышцах, уменьшает утомляемость женщины во время приливов и увеличивает ресурс мышечной системы [20]. В конечном итоге долговременная обеспеченность карнозином нормализует работу гладкой мускулатуры сосудов и тем самым способствует нормализации терморегуляции организма.
Взаимодействие бета-аланина с глициновыми рецепторами является одним из наиболее вероятных объяснений «быстрого» эффекта клималанина. Активированные глициновые рецепторы (глицинуправляемые хлоридные каналы) опосредуют процессы торможения в стволе головного мозга и в спинном мозге. Связываясь с рецептором, нейротрансмиттер глицин и бета-аланин открывают канал рецептора, который пропускает внутрь постсинаптических нейронов ионы хлора. Активация глициновых рецепторов оказывает нормализующее (в случае повышенного нервного возбуждения) действие[21]. В частности, глициновые рецепторы воздействуют на терморегуляторное ядро гипоталамуса [22], активирующее механизмы для поддержания температуры тела в нормальном диапазоне, называемом терморегуляторной зоной. Как известно, у женщин с приливами имеет место сужение границ терморегуляторной зоны [23, 24].
В настоящей работе было проведено сравнительное биофизическое моделирование взаимодействия бета-аланина, таурина и глицина с глициновыми рецепторами. На основе полученных моделей глициновых рецепторов оценивалось сродство (энергия связывания) глицина, бета-аланина и таурина с рецепторами.
Материал и методы
Модели пространственной структуры глициновых рецепторов человека были приготовлены по методике, описанной в работе [25]. Затем были исследованы возможности размещения молекул лигандов в связывающих карманах рецепторов. Для этого проводилась минимизация энергии при различных начальных расположениях молекулы относительно кармана рецептора [26]; для анализа данных расчетов использовался метод молекулярных энергетических профилей [25], позволяющий анализировать энергетический вклад (dGост) каждого аминокислотного остатка белка.
Результаты и обсуждение
В ходе настоящего исследования были получены различные пространственные структуры глицинового рецептора и рассчитаны значения энергий связывания (отражающих степень сродства к рецептору) рецепторов с глицином, бетааланином, таурином. Полученные данные были сравнены с имеющимися литературными данными по структурефункции глициновых рецепторов.
Модель пространственной структуры глицинового рецептора
Рецептор глицина является трансмембранным белком, состоящим из пяти белковых субъединиц (рис. 2), образующих центральный канал для селективного проведения ионов хлора [27, 28]. Каждая субъединица состоит из трансмембранного домена (который, собственно, и образует хлоридный канал) и лигандсвязывающего домена (опосредует взаимодействия рецептора с агонистами: глицином, бетааланином, таурином). К настоящему времени известны 5 типов субъединиц глициновых рецепторов – 4 субъединицы типа альфа (a1, a2, a3, a4) и одна b-субъединица, так что молекула глицинового рецептора может быть образована различными комбинациями этих 5 типов субъединиц.
Расчет энергий связывания бета-аланина с глициновыми рецепторами
Отметим, что вследствие существования пяти взаимозаменяемых субъединиц (a1, a2, a3, a4 и b), может существовать множество (тысячи) разновидностей глициновых каналов, различающихся как по количественному набору субъединиц (например, 3a1 и 2b и т.д.), так и по порядку включения субъединиц в состав канала (например, a1a2a3a4b, a1a1a2a3b, a1a2a1bb и десятки других) [28]. Состав субъединиц весьма важен, так как участки связывания глицина и других агонистов расположены в контактах между субъединицами [29], что делает необходимым оценку энергий связывания для разных сочетаний субъединиц (a1a1, a1a2, a2a2 и др.). Так как субъединицы a1 и a2 обнаруживаются наиболее часто [30], в настоящей работе расчет энергий связывания агонистов с глициновыми рецепторами проводился для трех сочетаний субъединиц – a1a1, a1a2 и a2a2 (рис. 3).
Приведенные на рис. 3 значения энергии связывания
DDG = DG — DG (DG – энергия образования комплеккомп своб комп
са лигандрецептор, DG – энергия образования рецептосвоб
ра, не связанного с лигандом) отражают так называемый выигрыш в энергии при образовании комплекса рецептора с глицином, бета-аланином и другими лигандами. Чем более отрицательно значение DDG, тем более прочен комплекс исследуемого лиганда с рецептором (т.е. выше сродство лиганда к рецептору). Как видно из рис. 3, сродство бетааланина к глициновым рецептором было сравнимо (а в случае a1a2 и a2a2 – даже выше) со сродством самого глицина.
Молекулярные детерминанты ионной селективности глициновых рецепторов
Аминокислоты агонисты глициновых рецепторов образуют следующий порядок по степени активации каналов глициновых рецепторов: глицин>бета-аланин>таурин>ГАМК [31–33]. Следует отметить, что определяемая в биохимических экспериментах «степень активации каналов» не отражает «сродства» (т.е. степени связывания) агониста к каналам. Бол́ьшая энергия связывания (бол́ ьшее сродство) агониста к каналам, даже при более низкой активации, обеспечивает более пролонгированное воздействие агониста на рецептор. Это имеет прямое отношение к результату, полученному в настоящей работе: рассчитанная энергия связывания бета-аланина с глициновым рецептором выше, чем энергия связывания самого глицина с рецептором (или, по крайней мере, сравнима с энергией связывания глицина).
Поэтому клималанин может характеризоваться более продолжительным эффектом воздействия на глициновые рецепторы, чем сам глицин. Подобно глицину бетааланин в составе клималанина активирует глициновые рецепторы и в коре больших полушарий головного мозга, что в той или иной мере может положительно влиять на когнитивные функции (память и концентрацию внимания). Это открывает еще одну очень интересную перспективу изучения препарата клималанин на когнитивные возможности, как правило, подавленные при патологическом течении периклимактерического периода. Более пролонгированное воздействие бета-аланина на глициновый рецептор при приливах соответствует более продолжительному воздействию препаратов на основе бета-аланина на процессы нормализации работы терморегуляторного ядра. Этот вывод представляется важным для понимания фармакологических эффектов препарата клималанин. Иначе говоря, клималанин может способствовать продолжительной стабилизации функционирования терморегуляторного ядра гипоталамуса. Нами была уточнена структура участка связывания глицина и бета-аланина глициновым рецептором. По данным биохимических исследований, остатки N102, G160, L200, Y202 и T204 (нумерация по последовательности a1 субъединицы) образуют участок связывания агонистов и определяют чувствительность рецептора [34]; лейцин-200 (L200), тирозин-202 (Y202) и треонин-204 (T204) играют особую роль в чувствительности рецептора к глицину [35]. В соответствии с полученными данными, амино- кислоты L200, Y202 и T204 поддерживают структуру всего глицинсвязывающего участка (рис. 4). В то же время остатки фенилаланина F159 и тирозина Y161, специфически влияющие на чувствительность к агонистам, расположены в непосредственной близости с молекулами глицина и бета-аланина. Замены аминокислот F159Y и Y161F приводили к увеличению чувствительности к глицину в 12 раз, а чувствительности к бета-аланину – в 120 раз (!) [35].
Следует отметить, что полученные модели комплексов позволяют подробно рассмотреть молекулярные механизмы воздействия ионов цинка и кислотности среды (рН) на активность глициновых рецепторов. Модуляция активности глициновых рецепторов посредством связывания ионов цинка весьма важна для активности рецептора. Как известно, ионы Zn2+ концентрируются в прозрачных пресинаптических пузырьках и секретируются в синаптическую щель одновременно с секрецией соответствующего нейротрансмиттера. Цинк повышает сродство глицина к рецептору, но повышенные концентрации цинка (более 10 мкмоль/л) способствуют снижению сродства [36].
Участок связывания цинка образован аминокислотными остатками H107 и H109, расположенными в лигандсвязывающем домене рецептора (рис. 6). Связывание данными остатками цинка стабилизирует структуру агонистсвязывающего участка, образованного F159 и другими остатками, что и способствует повышению сродства рецептора к агонистам. Избыточные уровни цинка соответствуют связыванию второго иона цинка непосредственно в участке связывания агониста, что и будет приводить к снижению сродства рецептора к глицину и бета-аланину.
Отметим, что у 80–90% женщин в климактерическом периоде развивается дефицит цинка, связанный со снижением кислотности желудка, сокращением микробиоты кишечника и диетарным дефицитом (в частности, вследствие углеводного типа питания). Дефицит цинка является диетарным фактором риска развития инсулинорезистентности, глюкозотолерантности, метаболического синдрома и сахарного диабета [37]. Поэтому эффективность терапии приливов бета-аланином может повышаться при нормальной обеспеченности пациентки цинком. При этом не следует превышать физиологических суточных потребностей в цинке (10–15 мг/сут). Отметим, что в климактерическом периоде дефицит цинка встречается в сотни раз чаще, чем избыточное потребление цинка.
Эффекты кислотности (рН) внеклеточной среды на активность рецепторов обусловлены взаимодействиями протонов с регуляторным цинк связывающим участком рецептора, образованным остатками гистидина H107 и H109 (рис. 6). Чувствительность рецепторов к глицину значительно уменьшается по мере понижения рН спинномозговой жидкости [38].
С клинической точки зрения, более низкие уровни рН соответствуют метаболическому ацидозу. Нарушения углеводного обмена способствуют формированию метаболического ацидоза и чаще сопровождаются симптоматикой приливов. Так как при снижении рН сродство лигандов к глициновым рецепторам снижается, для повышения эффективности терапии бета-аланином следует также принять комплекс мер по снижению метаболического ацидоза (снижение потребления углеводов, прием пищевых продуктов, способствующих ощелачиванию крови и др.).

Заключение
Требованием времени является поиск негормональных, но высокоэффективных фармакологических средств для патогенетического лечения приливов. Терапия приливов препаратом клималанин характеризуется «быстрым» эффектом. Одним из наиболее вероятных механизмов «быстрого» воздействия бета-аланина на купирование приливов является активация глициновых рецепторов.
Проведенное в настоящей работе сравнительное моделирование взаимодействий клималанина и глицина с пространственной структурой глициновых рецепторов показало, что энергия связывания рецептором бета-аланина превышает энергию связывания самого глицина. Последнее соответствует пролонгированному воздействию препаратов бета-аланина на глициновые рецепторы, что позволяет предположить, что при применении препарата клималанин возможно улучшение когнитивных функций. Анализ молекулярных детерминант селективности глициновых рецепторов показал, что при планировании терапии приливов бетааланином целесообразно оценивать наличие у пациентки дефицита цинка и метаболического ацидоза.
Следует подчеркнуть, что способ приема препарата клималанин может оказывать существенное влияние на то, какой эффект будет более выражен – «быстрый» или «медленный». Так, рассасывание таблетки под языком будет способствовать быстрому поступлению бета-аланина в относительно высоких концентрациях непосредственно в кровь со слизистой подъязычного пространства, оказывая воздействие на головной мозг (терморегуляторная зона гипоаламуса) через связывание с глициновыми рецепторами и приводя к «быстрому эффекту» воздействия на терморегуляторное ядро гипоталамуса.
ЛИТЕРАТУРА
1. Maclennan AH, Broadbent JL, Lester S, Moore V. Oral oestrogen and combined oestrogen/progestogen therapy versus placebo for hot flushes. Cochrane Database Syst Rev 2004; 4: CD002978.
2. Reynolds RF, Obermeyer CM, Walker AM, Guilbert D. Side effects and sociobehavioral factors associated with the discontinuation of hormone therapy in a Massachusetts health maintenance organization. Menopause 2001; 8 (3): 189–99.
3. Rossouw JE, Anderson GL, Prentice RL et al. Risks and benefits of estrogen plus progestin in healthy postmenopausal women: principal results From the Women’s Health Initiative randomized controlled trial. JAMA 2002; 288 (3): 321–33.
4. Lacey JV Jr, Mink PJ, Lubin JH et al. Menopausal hormone replacement therapy and risk of ovarian cancer. JAMA 2002; 288 (3): 334–41.
5. Coughlin SS, Giustozzi A, Smith SJ, Lee NC. A meta-analysis of estrogen replacement therapy and risk of epithelial ovarian cancer. J Clin Epidemiol 2000; 53 (4): 367–75.
6. Tanis BC, van den Bosch MA, Kemmeren JM et al. Oral contraceptives and the risk of myocardial infarction. N Engl J Med 2001; 345 (25): 1787–93. 7. Nelson HD, Vesco KK, Haney E et al. Nonhormonal therapies for menopausal hot flashes: systematic review and meta-analysis. JAMA 2006; 295 (17): 2057–71.
8. Громова О.А., Торшин И.Ю., Лиманова О.А. Патофизиология вегетативно-сосудистых пароксизмов (приливов) в период менопаузы у женщин и механизмы воздействия бета-аланина. Новая клинико- фармакологическая концепция. Вопросы акушерства, гинекологии и перинатологии. 2011; 1.
9. Alo R, Avolio E, Di Vito A et al. Distinct alpha subunit variations of the hypothalamic GABAA receptor triplets (alphabetagamma) are linked to hibernating state in hamsters. BMC Neurosci 2010; 11: 111.
10. Lundius EG, Sanchez-Alavez M, Ghochani Y et al. Histamine influences body temperature by acting at H1 and H3 receptors on distinct populations of preoptic neurons. J Neurosci 2010; 30 (12): 4369–81.
11. Frontini A, Giordano A. Leptin sensitive neurons in mouse preoptic area express alpha 1A- and alpha 2A-adrenergic receptor isoforms. Neurosci Lett 2010; 471 (2): 83–8.
12. Lee TF, Mora F, Myers RD. Dopamine and thermoregulation: an evaluation with special reference to dopaminergic pathways. Neurosci Biobehav Rev 1985; 9 (4): 589–98.
13. Nakamura Y, Nakamura K, Morrison SF. Different populations of prostaglandin EP3 receptor-expressing preoptic neurons project to two fever-mediating sympathoexcitatory brain regions. Neuroscience 2009; 161 (2): 614–20.
14. Nakamura Y, Nakamura K, Matsumura K et al. Direct pyrogenic input from prostaglandin EP3 receptor-expressing preoptic neurons to the dorsomedial hypothalamus. Eur J Neurosci 2005; 22 (12): 3137–46.
15. Takahashi A, Ishimaru H, Ikarashi Y et al. Hypothalamic cholinergic regulation of body temperature and water intake in rats. Auton Neurosci 2001; 94 (1–2): 74–83.
16. Karlsson U, Haage D, Johansson S. Currents evoked by GABA and glycine in acutely dissociated neurons from the rat medial preoptic nucleus. Brain Res 1997; 770 (1–2): 256–60.
17. Peskov AB, Maevskii EI, Uchitel’ ML et al. Succinate-based preparation alleviates manifestations of the climacteric syndrome in women. Bull Exp Biol Med 2005; 140 (3): 312–4.
18. Dormire S, Howharn C. The effect of dietary intake on hot flashes in menopausal women. J Obstet Gynecol Neonatal Nurs 2007; 36 (3): 255–62. 19. Dormire SL, Reame NK. Menopausal hot flash frequency changes in response to experimental manipulation of blood glucose. Nurs Res 2003; 52 (5): 338–43.
20. Hill CA, Harris RC, Kim HJ et al. Influence of beta-alanine supplementation on skeletal muscle carnosine concentrations and high intensity cycling capacity. Amino Acids 2007; 32 (2): 225–33.
21. Lynch JW. Native glycine receptor subtypes and their physiological roles. Neuropharmacology 2009; 56 (1): 303–9.
22. Casper RF, Yen SS. Neuroendocrinology of menopausal flushes: an hypothesis of flush mechanism. Clin Endocrinol (Oxf) 1985; 22 (3): 293–312. 23. Freedman RR, Krell W. Reduced thermoregulatory null zone in postmenopausal women with hot flashes. Am J Obstet Gynecol 1999; 181 (1): 66–70.
24. Harris RC, Tallon MJ, Dunnett M et al. The absorption of orally supplied beta-alanine and its effect on muscle carnosine synthesis in human vastus lateralis. Amino Acids 2006; 30 (3): 279–89.
25. Torshin IY. Bioinformatics in the Post-Genomic Era: The Role of Biophysics 2006 Nova Biomedical Books, NY, ISBN: 1-60021-048, p. 96–108.
26. Торшин И.Ю., Громова О.А., Рудаков К.В. Сравнительный анализ дидрогестерона и других прогестагенов: расчет энергий связывания со стероидными рецепторами. Вопросы гинекологии, акушерства и перинатологии. 2011; 2 (10): 68–80.
27. Lynch JW. Molecular structure and function of the glycine receptor chloride channel. Physiol Rev 2004; 84 (4): 1051–95.
28. Langosch D, Thomas L. Conserved quaternary structure of ligand-gated ion channels: the postsynaptic glycine receptor is a pentamer. Proc Natl Acad Sci USA1988; 85: 7394–8.
29. Corringer PJ, Le Novere N, Changeux JP. Nicotinic receptors at the amino acid level. Annu Rev Pharmacol Toxicol 2000; 40: 431–58.
30. Mohammadi B, Krampfl K, Cetinkaya C et al. Kinetic analysis of recombinant mammalian -1 and -1 -glycine receptor channels. Eur Biophys J 2003; 32: 529–36.
31. Lester HA. The permeation pathway of neurotransmitter-gated ion channels. Annu Rev Biophys Biomol Struct 21: 267–292, 1992.
32. Bormann J, Rundstrom N, Betz H. Residues within transmembrane segment M2 determine chloride conductance of glycine receptor homo and hetero-oligomers. EMBO J 1993; 12: 3729–37.
33. Lynch JW, Rajendra S, Pierce KD et al. Identification of intracellular and extracellular domains mediating signal transduction in the inhibitory glycine receptor chloride channel. EMBO J 1997; 16: 110–20.
34. Han NL, Haddrill JL, Lynch JW. Characterization of a glycine receptor domain that controls the binding and gating mechanisms of the в-amino acid agonist, taurine. J Neurochem 2001; 79: 636–47.
35. Rajendra S, Vandenberg RJ, Pierce KD et al. The unique extracellular disulfide loop of the glycine receptor is a principal ligand binding element. EMBO J 1995; 14: 2987–98.
36. Laube B, Kuhse J, Rundstrom N et al. Modulation by zinc ions of native rat and recombinant human inhibitory glycine receptors. J Physiol 1995; 483: 613–9.
37. Ребров ВГ, Громова ОА. Витамины, макро и микроэлементы, ГЭОТАР-МЕД. 2008; с. 647.
38. Chen Z, Dillon GH, Huang R. Molecular determinants of proton modulation of glycine receptors. J Biol Chem 2004; 279: 876–83.
ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ. ПЕРЕД ПРИМЕНЕНИЕМ ОЗНАКОМЬТЕСЬ С ИНСТРУКЦИЕЙ.
ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ.
ПЕРЕД ПРИМЕНЕНИЕМ ОЗНАКОМЬТЕСЬ С ИНСТРУКЦИЕЙ.

ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ. ВОЗМОЖНЫ ПОБОЧНЫЕ ЭФФЕКТЫ. НЕОБХОДИМА КОНСУЛЬТАЦИЯ СПЕЦИАЛИСТА.
Автор статьи
Подойницына Алёна Андреевна
,
Профессия: провизор
Название вуза: Пермская государственная фармацевтическая академия (ПГФА)
Специальность: фармация
Стаж работы: 5 лет
Диплом о фармацевтическом образовании: 105924 3510722 рег. номер 31917
Места работы: провизор в аптеке, преподаватель ПГФА на кафедре Управления и экономики фармации, провизор сервиса Мегаптека
Все авторы
Содержание
- Состав препарата
- Для чего препарат?
- Противопоказания
- Побочные эффекты
- Клималанин или Ци-Клим?
- Климадинон или Клималанин: что лучше?
- Клималанин или Менсе: что лучше?
- Клималанин или Эстровэл: что лучше?
- Краткое содержание
К сожалению, в жизни любой женщины наступает период менопаузы. В организме постепенно снижается выработка половых гормонов — эстрогенов, что отражается на многих функциях организма. Пресловутые симптомы — приливы, раздражительность, потливость, проблемы со сном, головные боли — изматывают женщин и нарушают качество жизни. Они проявляются у женщин в разной степени, но часто пугают их уже «заранее» до наступления климакса.
Но не стоит их бояться. Большинства симптомов можно избежать или существенно уменьшить их выраженность. Прежде всего необходимо обратиться к врачу, пройти обследования и сдать анализы. В дальнейшем доктор подберет медикаментозную терапию и даст рекомендации по образу жизни. Возможно, он предложит по показаниям ЗГТ — заместительную гормональную терапию — или другие, более «легкие» варианты. Например, Клималанин.
Рассказываем в статье о составе, показаниях к применению, противопоказаниях и побочных действиях препарата. Сравниваем с другими противоклимактерическими средствами: Климадинон, Менсе, Эстровэл и Ци-Клим.
Состав препарата
Клималанин — это зарегистрированное лекарственное средство в таблетках. Производитель — французская фармацевтическая компания Лаборатории Бушара-Рекордати. При его назначении пациентки, как правило, спрашивают: «Клималанин — это гормональный препарат или нет?». Клималанин — лекарство, которое согласно РЛС (Регистру лекарственных средств) содержит аминокислоту бета-аланин в количестве 400 мг в одной таблетке. Других активных веществ, включая гормоны и фитоэстрогены, в составе нет.
Для чего препарат?
В официальной инструкции по медицинскому применению Клималанина указано одно показание: приливы в период менопаузы. Аминокислота бета-аланин блокирует высвобождение гистамина, который вызывает расширение сосудов в коже и возникновение приливов. Таким образом препарат Клималанин купирует приступы, связанные с внезапным ощущением жара, головной болью и потливостью, уменьшает их частоту, улучшает переносимость.
Клималанин сколько можно принимать по времени?
Организм постепенно «привыкает» к недостатку эстрогенов. Поэтому, как и другие противоклимактерические лекарства, Клималанин таблетки рекомендуют принимать курсами не менее 5-10 дней и до исчезновения приливов. При длительном курсовом приеме (3 месяца) препарат дополнительно улучшает сон, память, концентрацию внимания и уменьшают утомляемость. При возобновлении симптомов лечение можно повторить. Клималанин не вызывает привыкания, его можно принимать на протяжении всего времени, пока возникают приливы.
Клималанин как принимать: до еды или после?
В инструкции нет указаний о времени приема таблеток. В таком случае, следуя общим правилам назначения, Клималанин принимают внутрь или за 30 минут до еды, или через 1–2 часа после еды. В день можно принять до 3 таблеток.
Противопоказания
Клималанин нельзя принимать только при гиперчувствительности к активным и вспомогательным компонентам лекарства. А также при непереносимости глютена из-за наличия пшеничного крахмала в составе таблеток.
Побочные эффекты
Еще один частый вопрос пациенток: «Какой может быть вред от Клималанина?». Препарат лишь в редких случаях вызывает аллергические реакции в виде зуда или сыпи, а также ощущения покалывания или «мурашек» в конечностях.
Клималанин или Ци-Клим?
В отечественную линейку препаратов Ци-Клим входят два лекарственных средства: Ци-Клим Аланин и Ци-Клим.
Первый препарат идентичен по составу Клималанину. Он также выпускается в таблетках, которые содержат 400 мг бета-аланина. Показания и противопоказания у них одинаковые. Разница только в том, где производится субстанция аминокислоты: для Клималанина в Японии, для Ци-Клима — в России. Клималанин и Ци-Клим Аланин взаимозаменяемы.
Ци-клим содержит другое активное вещество — сухой экстракт цимицифуги даурской. Гликозиды, содержащиеся в растении, обладают эстрогеноподобными действиями. Их называют фитоэстрогенами и часто используют в средствах «от климакса». Показания у Ци-клима схожи с таковыми для Клималанина, но у препаратов разный механизм действия и есть другие отличия:
- формы выпуска: Ци-клим представлен в виде таблеток и капель для приема внутрь;
- противопоказания: у Ци-клима больше (эстроген-зависимые опухоли, бронхиальная астма);
- дополнительный эффект: Ци-Клим оказывает седативное действие и предотвращает старение кожи в менопаузе;
- продолжительность лечения:как правило, курс лечения Ци-Климом дольше, первый эффект проявляется через 2-4 недели.
Прежде чем начать терапию, рекомендуем проконсультироваться с врачом. чтобы выбрать наиболее эффективный препарат в конкретном случае.
Климадинон или Клималанин: что лучше?
Климадинон также относится к зарегистрированным противоклимактерическим лекарственным средствам. Выпускается немецкой компанией Бионорика СЕ в таблетках и каплях для приема внутрь. Жидкая лекарственная форма будет преимуществом для пациентов, которые имеют проблемы с глотанием таблеток или просто предпочитают капли.
У Климадинона действующим веществом является экстракт корней и корневищ растения Цимицифуга кистевидная, который помогает облегчить такие симптомы в период менопаузы, как приливы и повышенная потливость. Климадинон не следует принимать больше 6 месяцев без назначения врача.
Однозначно сказать, какой препарат эффективнее, нельзя. Реакция каждого организма индивидуальна, одним женщинам больше помогает бета-аланин (Клималанин), другим — фитоэстрогены (Климадинон).
Клималанин или Менсе: что лучше?
Менсе — средство, которое уменьшает симптомы климактерического синдрома. Производится в России, зарегистрировано как БАД. Имеет многокомпонентный состав:
- тоже содержит бета-аланин, влияющий на приливы, но в меньшей дозировке — 200 мг:
- экстракт изофлавонов сои и фолиевая кислота восполняют недостаток гормонов, восстанавливают гормональный баланс;
- 5-гидрокситриптофан (экстракт гриффонии) и витамины группы В устраняют тревожность, раздражительность, улучшают сон и жизненный тонус;
- витамины С и Е оказывают антиоксидантное действие.
Преимущества Менсе: содержит и фитоэстрогены, и бета-аланин, и комплекс других активных веществ, влияющих на все симптомы менопаузы, а не только на приливы. Но в то же время «богатый» состав повышает риски аллергических реакций.
Клималанин или Эстровэл: что лучше?
Эстровэл — еще один российский БАД растительного происхождения. Это негормональный комплекс фитоэстрогенов, витаминов и микроэлементов не только для уменьшения симптомов климактерического синдрома, но и предменструального (ПМС).
В его состав входят
- изофлавоны сои — снижают частоту приливов, потливость, головные боли, восстанавливают гормональный баланс при ПМС, укрепляют кости;
- экстракт ямса китайского содержит вещества-предшественники прогестерона и других гормонов, нормализует дисбаланс гормонов при ПМС и в климактерическом периоде;
- экстракт плодов витекса священного нормализует уровень прогестерона, уменьшает симптомы ПМС: раздражительность, нервозность, болезненность молочных желез;
- индол-З-карбинол нормализует метаболизм эстрогенов, снижает риск возникновения опухолей;
- 5-гидрокситриптофан и витамины группы В снижают тревожность и улучшают сон и настроение;
- витамин К1 обладает кровоостанавливающим эффектом и играет важную роль в формировании костей и профилактике остеопороза;
- микроэлемент бор усиливает действие фитоэстрогенов;
- витамин Е оказывает антиоксидантное действие.
Бета-аланин в состав Эстровэла не входит, но зато он, в отличие от Клималанина, содержит несколько фитоэстрогенов, имитирующих действие естественных половых гормонов женщины. Преимущество Эстровэла — комбинированный состав. Он включает фитоэстрогены ямса и сои, а также дополнительные элементы, которые стабилизируют психоэмоциональный фон. Но если пациентку больше всего беспокоят жар и приливы, то предпочтение лучше отдать не БАДу, а лекарственному средству Клималанин.
Краткое содержание
- Клималанин содержит аминокислоту бета-аланин в количестве 400 мг в одной таблетке. Других активных веществ, включая гормоны и фитоэстрогены, в составе нет.
- В официальной инструкции по медицинскому применению Клималанина указано одно показание: приливы в период менопаузы.
- Клималанин нельзя принимать только при гиперчувствительности к активным и вспомогательным компонентам лекарства и при непереносимости глютена из-за наличия пшеничного крахмала в составе таблеток.
- Препарат редко вызывает аллергические реакции в виде зуда или сыпи, а также ощущения покалывания или «мурашек» в конечностях.
- Ци-Клим Аланин выпускается в таблетках, которые содержат 400 мг бета-аланина. Показания и противопоказания одинаковые с Клималанином.
- У Климадинона действующим веществом является экстракт корней и корневищ растения Цимицифуга кистевидная, который содержит фитоэстрогены. Однозначно сказать, какой препарат эффективнее, нельзя. Реакция каждого организма индивидуальна, одним женщинам больше помогает бета-аланин (Клималанин), другим — фитоэстрогены (Климадинон).
- Преимущества Менсе: содержит и фитоэстрогены, и бета-аланин, и комплекс других активных веществ, влияющих на все симптомы менопаузы, а не только на приливы. Но в то же время «богатый» состав повышает риски аллергических реакций.
- Эстровэл (БАД) — негормональный комплекс фитоэстрогенов, витаминов и микроэлементов не только для уменьшения симптомов климактерического синдрома, но и предменструального (ПМС). Если пациентку больше всего беспокоят жар и приливы, то предпочтение лучше отдать не БАДу, а лекарственному средству Клималанин.
Задайте вопрос эксперту по теме статьи
Остались вопросы? Задайте их в комментариях ниже – наши эксперты ответят вам. Там же вы можете поделиться своим опытом с другими читателями Мегасоветов.
от 788,30 ₽
от 666,50 ₽
от 640 ₽
