Авторы описывают результаты исследования эффективности терапии препаратом Аллокин-альфа (аллоферон) в сравнении с Ацикловиром у 60 пациентов с генитальной формой хронической рецидивирующей герпесвирусной инфекции (ХРГВИ). Исследование показало, что у пациентов с высокой частотой рецидивов простого герпеса противовирусная терапия Аллокином-альфа более эффективна, чем стандартная терапия.
Лечение Аллокином-альфа приводило к уменьшению клинических проявлений ХРГВИ в фазе обострения, сокращению продолжительности рецидивов и заметному снижению их частоты в отдаленном периоде. На основании результатов исследования предложен алгоритм обследования и лечения больных рецидивирующим простым герпесом.
Таблица 1. Клиническая эффективность стандартной и альтернативной терапии больных простым герпесом
Рис. 1. Динамика NK-активности при лечении пациентов с простым герпесом
Таблица 2. Показатели интерферонового статуса при лечении простого герпеса Аллокином-альфа и Ацикловиром
Рис. 2. Частота выявления цитокинов до и после лечения Ацикловиром (n = 30)
Рис. 3. Частота выявления цитокинов до и после лечения Аллокином-альфа (n = 30)
Рис. 4. Изменения интерлейкинового профиля после лечения Аллокином-альфа
Рис. 5. Алгоритм обследования и терапии пациентов с частыми (более 6 раз в год) обострениями простого герпеса
Герпесвирусная инфекция широко распространена в человеческой популяции, поскольку вирусы этой группы пантропны и способны поражать многие системы и органы человека. Восприимчивость человека к вирусам герпеса высока. Около 90% всего населения планеты инфицированы одним или несколькими серотипами семейства герпесвирусов. По данным разных исследователей, от 12 до 25% носителей страдают рецидивирующими формами герпесвирусной инфекции, у 30% из них обнаруживается атипичная или бессимптомная форма заболевания [1, 2, 3].
Анализ ежегодной заболеваемости в России показал: 15% населения страдают герпетическим поражением кожи и слизистых, при этом у 10% встречается генитальная форма заболевания. Герпетические инфекции как этиологический фактор выявляются в 60–65% при поражении роговицы глаза, в 10% случаев – при заболеваниях нервной системы (менингиты, энцефалиты). По данным некоторых исследователей, в России ежегодно различными формами герпесвирусной инфекции заболевают около 20 млн человек [4, 5].
Одной из распространенных форм простого герпеса является генитальный герпес, частота которого достигает 6–10% среди взрослого населения [1, 6], а в целом по России – до 20% [4]. Показатель заболеваемости генитальным герпесом в Москве увеличился в 6 раз, в Московской области – в 2 раза (по сравнению с 2000 г.). Эти данные являются приблизительными, поскольку отсутствует обязательная регистрация случаев заболеваемости простым герпесом.
Исследование патогенеза простого герпеса показало, что инфекция включает острый или субклинический первый эпизод, установление латентного состояния вируса и последующую реактивацию. Вирус простого герпеса (ВПГ) попадает в организм через кожу или слизистые оболочки путем прямого контакта с биологическими жидкостями или поверхностью слизистой оболочки зараженного человека. Показано, что заражение может происходить от инфицированного пациента как при наличии симптомов заболевания, так и при их отсутствии. Вирус простого герпеса распространяется в тканях из-за способности заражать соседние клетки напрямую через клеточные контакты [7], что позволяет ему избежать воздействия внеклеточных факторов, включающих антитела и систему комплемента. Такой способ инфицирования, характерный для эпителиальных тканей, предполагает наличие гликопротеинов gE и gI [8]. Во время рецидива герпесвирусной инфекции в материале из очагов поражения находят зрелые вирионы с дополнительными мембранными слоями, а у больных со спокойным клиническим течением заболевания чаще всего выявляются незрелые формы (капсиды и нуклеокапсиды).
Взаимодействие между вирусом и организмом человека является решающим этапом в развитии герпесвирусной инфекции. Для подавления иммунной защиты вирус использует различные механизмы. Первой линией защиты являются факторы естественного иммунного ответа (клетки моноцитарно-макрофагального ряда, естественные киллеры). Эта система защиты вступает в действие с первых дней контакта с вирусными антигенами. Естественные киллеры (NK-клетки) относятся к важным факторам естественной врожденной резистентности. Для реализации цитотоксической реакции NK-клеткам не требуется распознавать специфические антигены. Это одно из преимуществ быстрого цитолиза, осуществляемого NK-клетками по отношению к ВПГ-инфицированным мишеням. Кроме того, продукция альфа- и бета-интерферонов приводит чувствительные клетки в состояние резистентности к ВПГ, под их влиянием усиливается функция макрофагов и естественных киллеров, в результате разрушаются вирус-инфицированные клетки. В ходе эволюции вирус выработал различные механизмы модуляции активности NK-клеток: блокирование лигандов (NKG2D) для активирующих рецепторов, синтез гомологов цитокинов человека, взаимодействие вирусных белков с ингибирующими рецепторами NK-клеток [9, 10, 11].
Лечение пациентов с рецидивирующим простым герпесом представляет определенные трудности из-за способности вируса простого герпеса к длительному персистированию, часто рецидивирующему течению, что приводит к снижению противовирусной иммунной защиты. Исследование механизмов репликации вируса простого герпеса, изучение взаимодействия вируса с клетками-мишенями позволило за последние 30 лет создать целый ряд химиотерапевтических препаратов, обладающих противогерпетической активностью [3, 12, 13, 14].
Клинический опыт их применения показал, что они способны быстро и эффективно купировать острые проявления простого герпеса, но не предотвращают развитие рецидивов хронической герпесвирусной инфекции и не снижают их частоту [15]. Именно поэтому актуальной задачей остается изучение механизмов функционирования иммунной и цитокиновой системы при рецидивирующей герпесвирусной инфекции и поиск новых препаратов с противовирусной и иммуномодулирующей активностью для лечения этого заболевания.
Целью настоящего исследования стало определение клинической эффективности стандартной и альтернативной противовирусной терапии пациентов с хронической рецидивирующей герпесвирусной инфекцией (ХРГВИ).
Материалы и методы
Исследование проводилось открытым методом у 60 пациентов с ХРГВИ. В состав исследуемых включались пациенты (возрастной интервал от 18 до 65 лет) мужского и женского пола с установленным диагнозом «ХРГВИ, генитальная форма». Все пациенты, включенные в исследование, находились в периоде продрома или обострения не более 48 часов от момента появления высыпаний. К исследованию не допускались пациенты с некомпенсированными заболеваниями сердечно-сосудистой, эндокринной, желудочно-кишечной, нервной систем, которые могли повлиять на результаты исследований, беременные и кормящие женщины. Условием включения для женщин детородного возраста было соблюдение полноценной контрацепции. Пациенты, вошедшие в изучаемые группы, отбирались методом произвольной выборки при поступлении на амбулаторное лечение. На предварительном этапе были сформированы две группы пациентов по 30 человек. Клиническими проявлениями простого герпеса у пациентов были пузырьковые или эрозивные высыпания в области гениталий, субъективные симптомы – болезненность, зуд, жжение. Верификация ВПГ 1, 2 типа проводилась методом ПЦР мазка из области высыпаний, положительный результат был получен в 95% случаев.
Дозировка и схемы введения
В основной группе (n = 30) терапия проводилась препаратом Аллокин-альфа по следующей схеме: 3 подкожные инъекции препарата в дозе 1 мг с интервалом 48 часов. Курсовая доза составляла соответственно 3 мг. Аллокин-альфа – коммерческое название лекарственной формы аллоферона – синтетического линейного олигополипептида, который относится к индукторам синтеза интерферона и активаторам системы натуральных киллеров, обладает противовирусной активностью в экспериментальных моделях различных инфекций, в частности вызванных вирусом простого герпеса. Важной характеристикой данного препарата является способность селективно стимулировать активность факторов естественного иммунитета. Препарат действует только в очаге вирусной инфекции, не активируя весь каскад иммунологических реакций организма.
Дополнительно все пациенты получали стандартную противовирусную терапию: Ацикловир 0,2 г 5 раз в день в течение 7 дней.
В контрольной группе пациентов (n = 30) проводилось лечение только ациклическими нуклеозидами: Ацикловир 0,2 г 5 раз в день в течение 7 дней.
Обследование проводилось до приема препарата (0-й день), на 7-й день от начала приема препарата и через 6 месяцев после окончания приема препарата. Обследование включало общеклиническое, объективное исследование области высыпаний и иммунологическое исследование крови. Перед началом приема препарата собирался подробный анамнез пациента.
При оценке клинической эффективности проведенного лечения использовали 3 основных критерия.
- Снижение частоты рецидивов простого герпеса.
- Уменьшение продолжительности рецидивов.
- Уменьшение степени тяжести клинического течения рецидивов.
Оценка влияния терапии на иммунопатогенез герпесвирусной инфекции проводилась по следующим критериям:
- цитотоксическая активность натуральных киллеров;
- вариабельность цитокинового звена.
Метод определения функциональной активности NK-клеток основан на их способности лизировать как чужеродные в антигенном отношении (опухолевые и неопухолевые клетки), так и нормальные клетки человека и животных при нарушении их дифференцировки без предварительной сенсибилизации.
Цитокиновый профиль оценивали методом ОТ-ПЦР (определение активности мРНК цитокинов в мононуклеарах периферической крови методом обратной транскрипции и полимеразной цепной реакции).
Результаты и обсуждение
Основные критерии оценки клинической эффективности стандартной (Ацикловир) и альтернативной (Аллокин-альфа) противовирусной терапии больных простым герпесом отражены в таблице 1. Это частота, длительность и степень тяжести рецидивов.
Все клинические показатели достоверно улучшились только у пациентов, леченных препаратом Аллокин-альфа. Так, частота рецидивов простого герпеса в течение полугода в первой группе сократилась с 6,3 до 2,8 случаев, во второй – с 6,0 до 5,6, при этом длительность рецидивов на фоне терапии Аллокином-альфа уменьшилась практически в 2 раза. Положительные изменения на фоне лечения Ацикловиром оказались статистически незначимыми.
Наше исследование показало, что до терапии ни в одной из групп не наблюдалось корреляционной связи между частотой, длительностью и тяжестью течения рецидивов. У пациентов, получавших комбинацию Аллокина-альфа с Ацикловиром, после лечения была выявлена прямая связь между частотой и длительностью рецидивов, между длительностью и тяжестью течения рецидивов, а также между частотой и тяжестью течения рецидивов. В первой группе отмечено достоверное снижение тяжести рецидивов. У пациентов, которым проведена монотерапия Ацикловиром, аналогичных взаимосвязей не отмечено.
Изучение динамики NK-активности при лечении Аллокином-альфа показало, что на 3-и и 7-е сутки рецидива простого герпеса наблюдался плавный рост NK-активности с 39% до 52% и 57% соответственно (рис. 1). Аналогичных изменений при лечении Ацикловиром отмечено не было.
Выявлена прямая корреляция между изменениями показателей NK-активности до и после лечения Аллокином-альфа и тяжестью течения рецидивов, то есть более глубокий уровень снижения показателей NK-активности во время лечения сопровождался более тяжелым течением рецидива заболевания.
Полученные нами данные сопоставимы с результатами других исследователей [4, 10]. В первой фазе иммунного ответа наблюдается продукция интерферона и активация натуральных киллеров. NK-клетки выполняют роль первого барьера инфекции и вырабатываются в первые 24 часа после антигенной стимуляции до момента образования специфических антител и цитотоксических лимфоцитов. Помимо высокой цитотоксической активности NK-клетки обладают способностью продуцировать лимфокины (интерферон-гамма) и цитокины (фактор некроза опухоли) и таким образом контролировать дифференцировку клеток. У больных с рецидивирующим простым герпесом активность NK-клеток снижается во время рецидива и восстанавливается в период ремиссии. При низкой цитотоксической активности NK-клеток организм более чувствителен к ВПГ [8].
Содержание NK-клеток в периферической крови здоровых людей составляет в среднем 15%. При этом важное значение имеет не только количественное содержание, но и функциональная активность натуральных киллеров. В исследованиях обнаружено снижение цитотоксической активности NK-клеток примерно у 60% больных с манифестными формами простого герпеса и показана тенденция к снижению цитотоксичности в среднем за 7 дней до очередного рецидива и последующее ее повышение в острый период герпетической инфекции [1, 8]. Учитывая многообразие функций противовирусной защиты NK-клеток, мы считаем, что снижение функциональной активности NK-клеток, с одной стороны, является следствием неполноценности клеточного иммунитета, с другой – характеризует недостаточность функций самих лимфоцитов и может служить причиной вторичного иммунодефицита, лежащего в основе реактивации вируса простого герпеса.
Изучению системы интерферонов при герпесвирусной инфекции посвящено большое количество работ, которые показали, что роль интерферонов в формировании противогерпетического иммунитета не ограничивается подавлением репродукции вируса или санацией организма от его активных форм, но и проявляется в регуляции защитных реакций, в частности, усиления цитотоксичности NK-клеток [9, 10, 12]. Определение уровня альфа- и гамма-интерферона дает информацию о потенциальной активности интерфероновой системы.
В нашем исследовании до начала лечения показатели интерферонового статуса у всех больных простым герпесом были снижены, в основном за счет индуцированной альфа- и гамма-фракции интерферона. При этом уровень сывороточного интерферона был повышен, что свидетельствует об активности воспалительного процесса.
После лечения у больных, принимавших Аллокин-альфа, достоверно повысился уровень индуцированного альфа- и гамма-интерферона. Положительная разница показателей составила при лечении Аллокином-альфа 122,7 и 52,3 Ед/мл соответственно. При монотерапии Ацикловиром разница показателей была минимальной и недостоверной – 29,3 и 2,1 Ед/мл соответственно (табл. 2). Полученные данные позволяют считать, что высокая частота рецидивов простого герпеса способствует истощению синтеза эндогенного интерферона. Соответственно, таким пациентам следует рекомендовать прием препаратов, индуцирующих выработку интерферона.
Согласно полученным данным, у больных с синдромом интерферонового дефицита отсутствует индукция противовирусного ответа клеток и достоверно снижен синтез альфа- и гамма-интерферона. У больных с рецидивирующим простым герпесом резко снижена активность NК-клеток и продукция интерферона-гамма, особенно в стадии ремиссии. По всей вероятности, рецидив генитального герпеса связан с истощением выработки интерферона-альфа, что создает благоприятные условия для персистенции вируса. При дефиците интерферона организм не может адекватно контролировать распространение вирусной инфекции. Инверсия синтеза интерферона у больных рецидивирующей ВПГ-инфекцией может быть также связана с наличием антител в сыворотке крови, ингибирующих продукцию интерферона.
Цитокиновый профиль составляет основу специфических иммунных реакций и оказывает непосредственное влияние на механизмы иммунорезистентности при герпесвирусной инфекции [5]. К сожалению, до настоящего времени не существует единого подхода к определению интерлейкинового профиля больных герпесвирусной инфекцией. Именно поэтому все проводимые исследования представляют собой сравнительный анализ изменений уровня цитокинов до и после противовирусного лечения или в период рецидива и ремиссии заболевания.
Как показало наше исследование цитокинового профиля, у больных простым герпесом с высокой частотой рецидивов в период обострения до начала противовирусной терапии превалирует экспрессия мРНК интерферона-альфа и ИЛ-18, кроме того, в целом отмечена тенденция к повышению экспрессии мРНК ИЛ-4, ИЛ-6, ИЛ-8, ИЛ-10 (рис. 2–3). Все это свидетельствует об активации Тh-2-лимфоцитов.
Наше исследование выявило определенные тенденции к изменению активности мРНК интерлейкинов в зависимости от вида противовирусной терапии. Как видно на рисунке 3, после лечения Аллокином-альфа наблюдалась тенденция к повышению экспрессии мРНК ИФН-α, ИФН-γ, ИЛ-2, ИЛ-12, ФНО-α и понижению ИЛ-4, ИЛ-10 и ИЛ-8, что свидетельствует о переключении цитокинового ответа с Тh-2 на Тh-1. При стандартной терапии ациклическими нуклеозидами, в частности Ацикловиром, аналогичных изменений интерлейкинового профиля не отмечено.
Полученные данные позволяют предположить, что во время лечения Аллокином-альфа происходит активация макрофагально-моноцитарного звена иммунитета. На это указывает наличие ИЛ-1β и ИФН-γ, ИЛ-12 и ФНО-α. Кроме этого, снижение частоты выявляемости ИЛ-4 и ИЛ-6 свидетельствует об угнетении гуморального иммунного ответа. Наличие отрицательного баланса ИЛ-10, с одной стороны, может быть вызвано положительным балансом ФНО-α и ИФН-γ, с другой – эти изменения могут свидетельствовать о завершающем этапе воспалительной реакции (рис. 4).
Известно, что нормальное функционирование иммунной системы обеспечивают Thl- и Тh2-лимфоциты при равноценной продукции их регуляторных цитокинов [10]. Однако некоторые авторы [8] отрицают строгое разделение цитокинов на Thl- и Тh2-типы, так как считают, что один цитокин не способен влиять на степень выраженности иммунологического эффекта. Наряду с функциональным антагонизмом цитокинов существует их ингибирующее влияние друг на друга, обусловленное конкуренцией за связывание клеточных рецепторов.
Суммируя все вышеизложенное, нам хотелось бы выделить ряд ключевых моментов развития герпесвирусной инфекции.
1. Все звенья иммунной системы, так или иначе участвующие в формировании противогерпетического иммунитета, можно разделить на две основные группы. К первой относятся факторы, которые прямо или косвенно активируются только при репликации ВПГ и развитии клинических проявлений заболевания. Они являются основой стадии острого воспаления и фазы специфического иммунного воздействия. Это все факторы гуморального иммунитета, макрофаги, NK-клетки, альфа-интерферон, ИЛ-6, ИЛ-8 и фактор некроза опухоли. Их основной функцией является подавление рецидива герпесвирусной инфекции за счет прямых или опосредованных лизисно-киллерных воздействий непосредственно на вирус или инфицированные им клетки. Важной характеристикой функциональной активности всех вышеуказанных показателей является скорость купирования рецидива.
Ко второй группе относят CD8+-цитотоксические лимфоциты, ИФН-γ, ИЛ-4 и ИЛ-2. Их основная функция – контроль за репродукцией ВПГ и предотвращение его активации, что обеспечивает латентную персистенцию вируса и блокирует его репродукцию в ганглиях. При нарушениях в указанных звеньях иммунной системы ВПГ вновь активируется, что приводит к развитию клинических форм заболевания.
2. При рецидивах герпесвирусной инфекции все факторы иммунитета прямо или опосредованно активируются даже в тех случаях, когда имеется функциональный дефект одного из звеньев иммунитета, поэтому необходимо изучение этих показателей в динамике вирусного процесса.
Все звенья противовирусного иммунитета тесно взаимосвязаны, и нарушения в одном из них приводят к дисбалансу всей иммунной системы по принципу цепной реакции. При рецидивирующем герпесе это осложняет оценку исходных параметров иммунитета в целом и затрудняет выявление нарушений в отдельных звеньях иммунной системы, контролирующих репликацию ВПГ (иммунорегуляторный индекс СD4+/CD8+, количество NK-клеток, их функциональная активность, уровень альфа- и гамма-интерферонов и цитокинов, переключающих иммунный ответ).
Итогом нашего исследования стала разработка алгоритма обследования и лечения больных рецидивирующим простым герпесом.
Для оценки активности вирусного процесса и адекватности противовирусного иммунного ответа мы выбрали наиболее информативный и доступный для широкой клинической практики тест определения уровня специфических антител к вирусу простого герпеса IgM и IgG. Важно отметить особенности интерпретации данного теста. У ряда пациентов без клинических проявлений простого герпеса встречается повышение только специфических IgG. Среди практических врачей распространено мнение, что это свидетельствует о репликации вируса, и для снижения активности инфекционного процесса часто проводится противовирусная и иммуномодулирующая терапия. Мы считаем такую тактику неверной, поскольку следует лечить больного, а не его анализы.
Как видно на рисунке 5, у больных с высокой частотой рецидивов простого герпеса (более 6 раз в год) в период обострения заболевания необходимо оценить показатели гуморального иммунитета (уровень специфических IgM и IgG).
Рассмотрим возможные варианты иммунного ответа.
1. Повышение уровня специфических IgM и IgG более чем в 4 раза у больных с клиническими проявлениями простого герпеса и высокой частотой рецидивов свидетельствует об усиленном иммунном ответе и не требует дальнейшего изучения противовирусного иммунитета. Таким пациентам рекомендуется пролонгированная противовирусная терапия согласно следующим схемам:
- Ацикловир 400 мг 2 раза в сутки в течение 2–12 месяцев или
- Валтрекс 500 мг 1 раз в сутки в течение 2–12 месяцев или
- Фамвир 250 мг 2 раза в сутки в течение 2–12 месяцев.
Продолжительность лечения строго индивидуальна.
2. При низком уровне специфических IgM и IgG, свидетельствующем о слабо выраженном иммунном ответе, больным с клиническими проявлениями простого герпеса и высокой частотой рецидивов необходимы дополнительные исследования, в частности, иммунограмма с оценкой NK-активности и уровня сывороточного альфа- и гамма- интерферонов. При индексе цитотоксичности ниже 40% и низком уровне индуцированного альфа- и гамма-интерферона показана пролонгированная противовирусная терапия в комбинации с другими противовирусными и иммунотропными препаратами. Приведем пример схемы терапии:
Аллокин-альфа 1 мг подкожно через день, № 3 плюс
- Ацикловир 400 мг 2 раза в сутки в течение 2 месяцев или
- Валтрекс 500 мг 1 раз в сутки в течение 2 месяцев или
- Фамвир 250 мг 2 раза в сутки в течение 2 месяцев.
Таким образом, противовирусная терапия препаратом Аллокин-альфа у пациентов с высокой частотой рецидивов простого герпеса является эффективным способом уменьшения клинических проявлений в фазе обострения, сокращения продолжительности рецидивов и заметного снижения их частоты в отдаленном периоде.
Аллокин-альфа – коммерческое название лекарственной формы аллоферона – синтетического линейного олигополипептида, который относится к индукторам синтеза интерферона и активаторам системы натуральных киллеров, обладает противовирусной активностью в экспериментальных моделях различных инфекций, в частности вызванных вирусом простого герпеса. Важной характеристикой данного препарата является способность селективно стимулировать активность факторов естественного иммунитета. Препарат действует только в очаге вирусной инфекции, не активируя весь каскад иммунологических реакций организма.
Представлены результаты обследования и лечения 67 пациентов в возрасте от 18 до 45 лет. Больные страдали хроническим простатитом, хроническим простатовезикулитом, хроническим уретропростатитом, осложненной экскреторно-токсической формой бесплодия. У всех пациентов были выявлены возбудители заболевания, в том числе инфекций, передаваемых половым путем (ИППП). Больные контрольной группы получали традиционную терапию (этиотропные препараты, α-адреноблокаторы, энзимотерапия). В основной группе пациенты дополнительно получали аллокин-альфа. Включение аллокина-альфа способствовало более быстрой и полной эрадикации возбудителей ИППП, нормализации показателей спермограммы. Результаты данного исследования позволяют рекомендовать аллокин-альфа для комбинированного лечения больных инфекционно-воспалительными заболеваниями мочеполовой системы, осложненными экскреторно-токсической формой бесплодия.
Введение. Частота бесплодия в браке в мире, по данным ВОЗ, составляет 15%. В структуре причин
бесплодного брака на долю мужского фактора приходиться примерно 40% и предполагается, что она
будет увеличиваться [1]. Основными причинами мужского бесплодия являются инфекционно-возпалительные заболевания гениталий (22,1%), варикоцеле (14,9%), эндокринопатии (14,8%), идиопатическая патозооспермия (22,8%); на долю других факторов приходится 25,4% [2]. Из года в год наблюдается рост заболеваемости инфекционно воспалительными болезнями мочеполовой системы среди населения детородного возраста, что безусловно отрицательно сказывается на репродуктивной функции. Экскреторно-токсическая форма бесплодия чаще связана с заболеваниями мочеиспускательного канала и придаточных половых желез. У мужчин инфекционный процесс и его осложнения могут изолированно или последовательно влиять на различные органы мочеполовой системы: предстательную железу, семенные пузырьки, семявыносящие протоки, яички и их придатки. Нарушения физико-химических свойств семенной плазмы – среды обитания сперматозоидов – закономерно приводят к патозооспермии, чаще всего в виде астенозооспермии или индукции образования “ложных” антиспермальных антител, ассоциированных с инфекциями [1]. Роль инфекционного фактора в нарушении оплодотворяющей способности сперматозоидов неоднозначна. Несмотря на то что во многих работах показано наличие возбудителей в половых путях мужчин при бесплодии, выводы относительно роли, которую они играют в возникновении бесплодия, весьма противоречивы. Прежде всего это объясня-ется тем, что данные инфекционные заболевания часто выявляются как у фертильных, так и у бесплодных пар [2]. Условно-патогенные микробы и возбудители инфекций, передаваемых половым путем (ИППП), при этом характеризуются устойчивостью
к антибиотикам. Возбудители инфекционных заболеваний могут проникать в половые органы через
кровь (например, вирус эпидемического паротита, M. tuberculosis, M. leprae) или восходящим путем из
уретры.
Среди возможных последствий инфекционного поражения половых путей мужчин выделяют следу-
ющие [3]:
• инфицирование женщины, которое может приводить к развитию у нее различных заболеваний, в
том числе бесплодия и патологии беременности;
• изменение половых клеток, клеток Сертоли, клеток Лейдига, что приводит к мужскому бесплодию
(стерильность);
• лейкоцитарная инфильтрация половых путей с возможным развитием аутоиммунного бесплодия;
• снижение образования тестостерона и как следствие – мужское бесплодие;
• встраивание вирусного генома в геном половой клетки с риском передачи последующим поколениям.
Инфекционно-воспалительные заболевания органов репродуктивного тракта – одна из нередких и
потенциально исправимых причин мужского бесплодия [4]. Комплексные схемы лечения инфекционно-воспалительных заболеваний гениталий при бесплодии предусматривают назначение этиологической, патогенетической, иммунологической, общеукрепляющей терапии. При выявлении инфекционно-воспалительного заболевания, передаваемого половым путем, лечение проводится обязательно обоим супругам независимо от того, у кого выявлена инфекция, при этом практикуются защищенные половые контакты в связи с возможностью реинфекции партнеров. Этиологическое лечение направлено на эрадикацию возбудителя. С этой целью чаще всего назначают антибиотики широкого спектра действия. В комплексной терапии инфекционных заболеваний наиболее целесообразно применение иммуномодуляторов. Одной из основных причин роста числа заболеваний является снижение факторов местной защиты слизистых оболочек и иммунологической резистентности организма, позволяющее проявлять маловирулентным возбудителям свои патогенные свойства. Такие формы воспалительных заболеваний наиболее опасны с точки зрения возникновения бесплодия, так как с момента инфицирования до обращения к врачу по поводу отсутствия детей в семье проходят годы, в течение
которых инфекция не диагностируется и не лечится. Возникающие у мужчин уретриты, эпидидимиты,
простатиты, везикулиты и другие заболевания трудно поддаются лечению антибактериальными препаратами. Возникает необходимость в управляемой иммунокоррекции с помощью иммунотропных препаратов.
Отечественный препарат аллокин-альфа является одним из новых иммунотропных средств для
повышения эффективности лечения инфекций, связанных с внутриклеточным паразитированием. Это
первый представитель новой группы иммуномодуляторов природного происхождения, основным
действующим веществом которого является аллоферон [5]. Аллокин-альфа разработан международным коллективом ученых, запатентован в России и за рубежом. Это олигопептид, способствующий повышению продукции интерлейкина-18, кроме того, является индуктором естественного синтеза всего пула эндогенных интерферонов-α, -ß и -γ, активатором системы естественных клеток-киллеров [6]. Действие аллокина-альфа направлено на усиление распознавания вирусных антигенов и инфицированных клеток (связывается с наружными рецепторами) естественными киллерами, нейтрофилами и другими эффекторными звеньями системы естественного иммунитета, ответственными за элиминацию возбудителя. Такой механизм действия актуален при лечении не только герпес-вирусных инфекций, но и заболеваний, обусловленных другими патогенами с внутриклеточным паразитированием.
Применение аллокина-альфа улучшает распознавание пораженных клеток и позволяет подавлять
очаги репликации патогенов. Аллокин-альфа усиливает продукцию интерферона (ИФН)-γ естественными киллерами в ответ на стимуляцию интерлейкином-18, выступает в качестве кофактора, позволяя продуцирующим ИФН-α лейкоцитам эффективно реагировать на вирусный антиген [8, 9]. В результате этого иммунокомпетентные клетки активируются, возрастает их цитотоксическая активность, что способствует элиминации возбудителя. Действие аллоферона направлено как на усиление распознавания вирусных антигенов иммунокомпетентными клетками, так и на уничтожение очагов вирусной инфекции [7].
Показана безопасность и клиническая эффективность трехкратного подкожного введения аллокинаальфа (дозы 10, 1 и 0,1 мг) при лечении больных рецидивирующим генитальным герпесом. Наблюдалось достоверное уменьшение продолжительности и тяжести текущего и последующего рецидивов, увеличение продолжительности ремиссии, уменьшение частоты последующих рецидивов. Терапия аллокином-альфа вызывала значимое повышение функциональной активности естественных киллеров, способствовала нормализации титров циркулирующего и спонтанно вырабатываемого ИФН, ИФН-ингибирующей активности сыворотки крови больных. При этом клиническая эффективность курса
лечения подобных инъекций аллокином-альфа была сопоставимой с таковой терапии ацикловиром в
течение 7 или 30 дней [8]. В ходе наблюдения за пациентами с папиломавирусной инфекцией, получавшими аллокин-альфа в течение 1, 3 мес., установлено, что у 98 (89,9%) больных наступала ремиссия заболевания, подтвержденная результатами методов амплификации нуклеиновых кислот (полимеразной цепной реакции – ПЦР), цитологического и кольпоскопического исследований [10]. Отсутствие маркеров ИППП после лечения свидетельствует о том, что использование аллокина-альфа в комбинации с этиотропной антибиотикотерапией способствует полной элиминации хламидий, мико-, уреаплазм [11].
Цель настоящего исследования – совершенствование терапии инфекционно-воспалительных заболеваний мочеполовых органов, осложненных экскреторно-токсической формой бесплодия у мужчин репродуктивного возраста.
Материалы и методы. В основу настоящего исследования положены результаты обследования и лечения 67 пациентов, которые обратились в клинику репродуктивного здоровья ООО “Деметра” Волгограда. Это были мужчины в возрасте от 18 до 45 лет с хроническим уретропростатитом (n=35), хроническим простатитом (n=9), хроническим простатовезикулитом (n=23), для которых заболевание осложнилось экскреторно-токсической формой бесплодия.
В основную группу вошел 41 (61,2%) пациент, в контрольную – 26 (38,8%). При этом хронический
уретропростатит диагностирован у 23 (56,1%) больных основной группы и у 12 (46,1%) – контрольной,
хронический простатовезикулит – у 15 (36,6%) и 8 (30,8%), хронический простатит у 3 7,3%) и 6 (23,1%) соответственно.
Обследование пациентов включало изучение жалоб, данных анамнеза заболевания и результатов
лабораторных исследований. Всем больным выполнили микроскопию секрета простаты и мазков из
уретры, спермограмму, биохимический анализ семенной плазмы, бактериологическое исследование эякулята, ультразвуковое исследование мочеполовых органов. Обследование включило морфологическое исследование соскоба из уретры посредством световой микроскопии и с помощью ПЦР на ИППП (Ureaplasma urealyticum, Mycoplasma genitalium, Chlamydia trachomatis, Mycoplasma hominis, Candida albicans, Trichomonas vaginalis, Papillomavirus hominis, Herpes simplex virus, Cytomegalovirus). Критерии включения пациентов в исследование: выявление различных инфекций репродуктивного тракта и патологических отклонений в спермограмме (pH более 7,8, разжижение более 60 мин, агглютинация и снижение подвижности сперматозоидов). Показателями, указывающими на наличие инфекций гениталий, в данном исследовании считались количество лейкоцитов в спермограмме более 1 млн в 1 мл; концентрация микробных тел более 103 КОЕ /мл по данным микробиологического исследования спермы; наличие 10 и более лейкоцитов в мазках из уретры или анализе секрета простаты, а также выявление ИППП.
Все больные обследованы и на неспецифические заболевания инфекционной природы. По результатам обследования выявлены: Ureaplasma urealyticum у 13 (19,4%) больных, Mycoplasma genitalium — у
10 (14,9%), Chlamydia trachomatis – у 6 (8,96%), Mycoplasma hominis — у 5 (7,5%), Candida albicans – у
2 (2,99%), Trichomonas vaginalis — у 1 (1,49%), ассоциации различных микроорганизмов — у 30 (44,76%). Следует отметить, что Papillomavirus hominis выявлена у 5 (7,5%) больных, Herpes simplex virus – у 8 (11,94%), Cytomegalovirus – у 2 (2,99%), но все они встречались только в ассоциациях и вошли в основную группу. Наиболее часто встречаемыми ассоциациями микроорганизмов были уреаплазмы и грибы, микоплазмы и вирусы герпеса, папилломавирусы и уреаплазмы. При обследовании у 41 больного была выявлена бактериоспермия более 103 КОЕ/мл. У остальных больных бактерии в эякуляте выявились не в диагностическом титре или отсутствовали. Среди условно-патогенных возбудителей наиболее часто встречались Enterobacter spp.– 36%; E. сoli – 24%; Staphylococcus spp.– 18%; Enterococcus spp. – 13%. На остальные бактериальные агенты приходилось 8%.
До и после лечения проведен ПЦР-скрининг на присутствие выявленных ранее патогенов. Для контрольных исследований с целью выявления Ureaplasma urealiticum, Mycoplasma hominis,
Papillomavirus hominis в уретре использован количественный способ. Результаты лечения оценивались через 2 и 3 мес. после начала курса терапии: через 2 мес. проводилось обследование на ИППП
и условно-патогенную флору в эякуляте, через 3 мес. после начала лечения – контроль спермограммы. Общепринято выполнять контрольную спермограмму не менее 3 мес. после окончания лечения, но
в нашем исследовании мы хотели получить предварительные результаты лечения и выполнили спермограмму через 3 мес. после начала лечения. В зависимости от проводимого лечения пациенты
были разделены на две группы. Больные контрольной группы (n=26) получали только традиционную
терапию. В основной группе (n=41) наряду с традиционным лечением пациенты получали аллокинальфа.
Базовая (этиотропная) терапия при наличии ИППП и неспецифической микробной флоре проводилась антибиотиками широкого спектра действия в течение 28 дней. При трихомонадной этиологии заболевания одному больному назначили метронидазол 7 дней, при грибковой – 2 (2,99%), флюконазол по 0,15 мг 3 дня подряд, далее 1 раз в неделю в течение 3 нед.
В схеме лечения применяли биологически активную добавку (БАД) спермактин по 1 саше 2 раза в
день в течение 90 дней. Терапевтическая эффективность спермактина обусловлена входящими в его
состав ингредиентами. L-карнитина фумарат способствует нормальному созреванию и увеличению
подвижности сперматозоидов, усиливает естественные обменные процессы, в том числе энергетические, в половых клетках. Ацетил-L-карнитин является важнейшим компонентом сперматозоидов, обеспечивает созревание и подвижность половых клеток, стабилизирует мембраны сперматозоидов и обеспечивает их функционирование. Фруктоза является основным источником энергии для эякулированных сперматозоидов и биохимическим маркером функции семенных пузырьков, по ее концентрации оценивают секреторную функцию семенных пузырьков; она улучшает фертильные свойства эякулята. Лимонная кислота является биохимическим маркером функции простаты, обеспечивает разжижение семенной жидкости и активацию гиалуронидазы, способствующей проникновению сперматозоидов в яйцеклетку. Использование лекарственного комплекса спермактин содействует улучшению качества спермы у мужчин с различной патозооспермией [12, 13].
В схему лечения входил α-адреноблокатор тамсулозин (омник окас) в дозе 0,4 мг 1 раз в день в течение 90 дней, являющийся высокоселективным блокатором α-адренорецепторов, обеспечивающим постоянную доставку лекарственного вещества без пикового повышения концентрации [14]. При возникновении ретроградной эякуляции больному назначали вместо тамсулозина доксазозин (артезин) 2 мг на ночь. Доксазозин по сравнению с тамсулозином обладает схожим порогом безопасности и не вызывает такого нежелательного эффекта, как ретроградная эякуляция, которую связывают с расширением суженных участков семявыносящих канальцев [15]. Альфа-адреноблокаторы способтвуют увеличению объема эякулята и рекомендованы к применению при патологических изменениях
семенной плазмы [4].
Для энзимотерапии использовали БАД протеаза плюс по 1 капсуле 3 раза в день в течение 90 дней.
Протеолитические ферменты успешно применяются в комплексной терапии различных заболеваний уже несколько десятилетий, что позволяет сокращать сроки лечения. Высокая эффективность обусловлена противовоспалительным, иммуномодулирующим, фибринолитическим действиями, а
также способностью улучшать региональную микроциркуляцию и ускорять регенеративные процессы.
В состав комплекса протеаза плюс входит не только высокоактивный фермент протеаза, но и микроминеральный комплекс, полученный из растительных источников. Данный препарат эффективен при хроническом воспалении и рекомендован к назначению при появлении в спермограмме агглютинации сперматозоидов [16].
Аллокин-альфа вводили подкожно по 1 мг через день на курс 6 инъекций. Первые 3 инъекции осуществлены до начала этиотропной терапии, остальные 3 инъекции — начиная со 2–3-го дня от начала базового лечения.
Клинико-диагностические критерии восстановления репродуктивной функции мужчин при изученных инфекционно-воспалительных заболеваниях урогенитального тракта [2]: элиминация ИППП; нормализация показателей количества лейкоцитов в сперме и/или секрете предстательной железы;
отсутствие микробной флоры или наличие условно-патогенных микроорганизмов в титре менее 103 КОЕ/мл в сперме и/или секрете предстательной железы; отсутствие симптомов заболевания; восстановление фертильности спермы; наступление беременности в отсутствие других причин бесплодия. Статистическую обработку полученных данных проводили по методу Стьюдента. Различия между показателями считали статистически достоверными при р<0,05.
Результаты и обсуждение. Спустя 2 месяца лечения в основной группе элиминация ИППП зафиксирована у 37 (90,2%) больных, у остальных наблюдалось снижение количества возбудителей. В контрольной группе элиминации возбудителя удалось достичь 16 (61,54%) пациентам (табл. 1). Больным с выявленными при контрольном обследовании инфекциями проведен повторный курс лечения с включением таких методик, как массаж простаты и физиотерапия. После окончания лечения в основной группе жалобы от 73,6% пациентов полностью отсутствовали, у 8,1% отмечено уменьшение выраженности клинических симптомов. Для остальных пациентов заболевание урогенитального тракта протекало бессимптомно. В контрольной группе у трети больных хроническим уретропростатитом, простатовезикулитом и простатитом сохранялись субъективные симптомы разной степени выраженности.
Таблица 1. Результаты обследования больных через 2 мес. после начала лечения.
Следует, кроме того, отметить, что у всех больных основной группы, получавших лечение аллокиномальфа, у которых в ассоциациях с другими микроорганизмами встречались вирусы, отмечено также их исчезновение в контрольных анализах, несмотря на то что противовирусные препараты им не назначались. Мы связываем этот эффект с непосредственным действием аллокина-альфа.
Изменения в спермограмме (отсутствие агглютинации, нормализация количества лейкоцитов, разжижение менее 60 мин) с большей положительной динамикой через 2 мес. после начала лечения было у пациентов, где использовалось комплексное лечение с применением аллокина-альфа.
В результате проведенного исследования было установлено, что применение схемы лечения с использованием аллокина-альфа пациентами с инфекционно-воспалительными заболеваниями
мочеполовой сферы, которые осложнились экскреторно-токсической формой бесплодия через 3 мес.
приводит к увеличению количества сперматозоидов на 31,6%, подвижности на 43,4%, количества
морфологически нормальных форм на 54,2%. В основной группе беременность наступила в шести
наблюдениях, в контрольной – только в одном (табл. 2)
Таблица 2. Результаты исследования эякулята через 3 мес. после начала лечения.
Использование аллокина-альфа в данном исследовании преследовало две цели. Первая — усилить
действие основных этиотропных средств базовой терапии. Антибактериальные препараты понижают
функциональную активность микроба, а иммуномодулятор повышает функциональную активность
фагоцитарных клеток, за счет чего достигается более эффективная элиминация возбудителя из
организма. Вторая – непосредственно иммуномодулирующая. Эффективность аллокина-альфа при
инфекционных заболеваниях различной локализации, вызванных микоплазмами, уреаплазмами, хламидиями, высока, так как при его использовании реализуется механизм киллерной защиты в отношении внутриклеточных инфекций. Действие аллокина-альфа направлено на активацию компонентов иммунной системы, облегчающих распознавание вирусных антигенов и других патогенов с внутриклеточным паразитированием и их дальнейшую элиминацию. В результате повышается функциональная активность клеток фагоцитарной системы, усиливается их способность поглощать и убивать возбудителя, повышается функциональная активность макрофагов, NK-клеток и Т-лимфоцитов, усиливается их способность разрушать клетки, инфицированные внутриклеточными возбудителя-
ми, в том числе вирусами.
Заключение. Воспалительные заболевания гениталий, включая вызванные ИППП, у пациентов репродуктивного возраста играют важную роль в нарушениях фертильности. Проведение полного обследования на различные инфекции является частью мер, направленных на успешное решение проблем бесплодного брака. Без коррекции иммунного ответа с помощью иммунотропных лекарственных средств справиться с описанными инфекционными процессами довольно сложно. Становится очевидным, что лечение хронических инфекционно-воспалительных процессов гениталий должно быть комплексным и состоять из этиотропных препаратов, направленных на элиминацию возбудителя, и иммуномодулирующих средств, направленных на оптимизацию функциональной активности иммунной системы больного человека. Результаты настоящего исследования позволяют рекомендовать аллокин-альфа для комбинированного лечения больных инфекционно-воспалительными заболеваниями урогенитального тракта, в том числе осложненных экскреторно-токсической формой бесплодия.
1. Калинченко С.Ю., Тюзиков И.А. Практическая андрология. М.: Практическая медицина. 2009. С. 147, 151.
2. Тер-Аванесов Г.В. Проблемы репродуктивного здоровья мужчин. М., 2004. С. 26–31, 69–75.
3. Шилла В.Б., Комхаира Ф., Харгрива Т. Клиническая андрология. М.: ГЭОТАР-Медиа, 2011. С. 178–183.
4. Сухих Г.Т., Божедомов В.А. Мужское бесплодие. М.: Эксмо, 2009. С. 43, 152–153, 165.
5. Федеральное руководство по использованию лекарственных средств. Вып. 5. М., 2004. Разд. 20.1.2.2.3.2.
6. Черныш С.И. Аллокины (цитокиноподобные пептиды насекомых) как модуляторы иммунного ответа человека и других млекопитающих. Rus. J. Immunol. 2004;9(S. 1):36.
7. Серебряная Н.Б. Иммунные дисфункции при герпесвирусной инфекции: новые подходы к терапии. Медицинская иммунология. 2005;7(2–3):321–322.
8. Ершов Ф.И., Кубанова А.А., Пинегин Б.В. и др. Влияние терапии ”аллокином альфа” на течение рецидивов хронического генитального герпеса. Materia Medica. 2003;4:103–111.
9. Исаков В.А., Архипова Е.И., Азовцева О.В. и др. Аллокин-альфа в комплексной терапии герпетической инфекции. Terra Medica. 2006;3:14–17.
10. Ершов Ф.И., Ковчур П.И., Бахлаев И.Е. Применение Аллокинальфа в комплексной терапии папилломавирусной инфекции шейки матки. Акушерство и гинекология. 2009;2.
11. Ткаченко Е., Духовлинов И. Применение аллокина-альфа в лечении мужчин с инфекциями, передаваемыми половым путем. Врач. 2009;11:93–94.
12. Божедомов В.А. и соавт. Эффективность лекарственного комплекса, включающего карнитины, при лечении различных нарушений качества спермы. Эффективная фармакотерапия в урологии. 2009;3.
13. Виноградов И.В. Опыт применения карнитина у больных идеопатической патоспермией. Проблема репродукции. 2009;1.
14. Djavan B. et al. Eur Urol 2005;4(Suppl.):61–68.
15. Перепанова Т.С., Хазан П.Л. Отчет о проведении клинических испытаний препарата Артезин для лечения пациентов с доброкачественной гиперплазией предстательной железы. Артезин 5 лет на рынке. Сборник статей и исследований. 2008. С. 8–14.
16. Бавильский В.Ф., Матыгин А.С. Репродуктивное здоровье мужчин. Ч. 2. 2010. С. 32.
О. В. Акимов, e-mail: ol.akimov2009@yаndex.ru
Вся информация размещенная на данном информационном ресурсе предназначена исключительно для практикующих специалистов и не может использоваться посетителями сайта для самостоятельной постановки диагноза и назначения лечения.

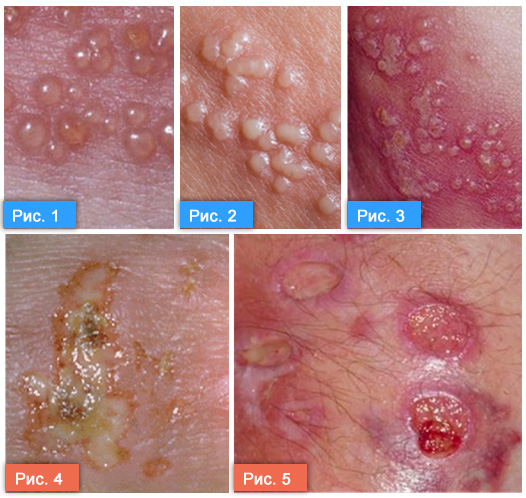
Генитальный герпес (в обиходе иногда встречается выражение — половой герпес) – это инфекция, передающаяся преимущественно половым путем. Характерными признаками являются высыпания в виде пузырьков размером 1-2 мм (рис. 1, 2, 3), на месте которых после вскрытия образуются болезненные язвочки (рис. 4, 5). Высыпания чаще всего локализуются в области гениталий (иногда на внутренней поверхности бедра или на ягодицах) и сопровождаются зудом, жжением и болью, что может повлечь за собой раздражительность, угнетенность, депрессию и более серьезные психические расстройства, ведущие за собой скандалы в семье, на работе, в общественном транспорте и т.д.
Так же существуют проявления генитального герпеса без характерных признаков, описанных выше. Тогда на первое место выходят такие проявления, как покраснение и отек кожи, слизистых, трещины и выделения из половых путей. Которые, в свою очередь, так же могут сопровождаться болью, зудом и жжением.
Возбудителем генитального герпеса в 80% случаев является вирус простого герпеса 2 типа (hsv 2). Реже причиной генитального герпеса становится так называемый «лабиальный» герпес (вирус герпеса 1 типа). (Лабиальные герпес-высыпания обычно локализуются в области рта). Это связано с широким распространением практики орогенитальных контактов между половыми партнерами. Иногда в развитии генитального герпеса могут участвовать сразу два типа вируса герпеса: 1-й и 2-й соответственно.
Более чем 90% населения планеты являются носителями вируса простого герпеса 1 и 2 типа. У взрослых антитела к вирусу простого герпеса 1 типа определяются в 99% случаев, а к вирусу 2 типа в 73%.
По оценкам Всемирной организации здравоохранения 10% женщин регулярно страдают от рецидивов генитального герпеса (чаще всего рецидив бывает один раз в месяц и связан с менструальным циклом).
Как передается герпес?
Передача вируса происходит во время незащищённых половых контактов с инфицированным партнером. Входными воротами для инфекции являются слизистые половых органов, микротрещины и регулярные микротравмы кожи, то есть нарушения целостности кожи в месте контакта.
Вероятность заражения даже при однократном контакте достигает 80%.
После заражения вирус герпеса по периферическим нервам перемещается от места проникновения в ганглии спинного мозга и там переходит в латентную стадию (стадию затишья). К сожалению, после попадания в организм вирус навсегда остается в нем.
Проявления генитального герпеса
Генитальный герпес проявляется в виде различных высыпаний: пузырьков, расположенных на нормальной или покрасневшей коже, язвочек, а иногда трещин слизистой оболочки. Вначале содержимое пузырьков прозрачное (рис 1), далее, через 1-3 дня, содержимое мутнеет (рис 2, 3). На 3-4 день на месте вскрывшихся пузырьков образуются болезненные язвочки (рис 4,5), часто покрытые медово-желтыми корочками. Высыпания обычно локализуются на гениталиях и анальной области.
У женщин сыпь локализуется в промежности, на лобке, половых губах и во влагалище. Для генитального герпеса у мужчин характерны высыпания в паху, на мошонке, на головке полового члена, крайней плоти.
Пораженные участки вызывают чувство жжения, зуд, доставляют сильную боль при ходьбе, особенно при занятиях спортом. Во время рецидивов герпеса женщины и мужчины вынуждены полностью отказаться от половых отношений. Высыпания неприглядны, а их повреждение во время полового акта вызывает сильные болезненные ощущения.
У пациентов с продолжительными и частыми рецидивами развиваются комплексы, нередко они впадают в депрессивные состояния, которые могут привести, как к проблемам в семье, так и на работе. Зачастую такие пациентки вынуждены обращаться за помощью к психотерапевту.
Почему герпес рецидивирует?
Вирус герпеса надежно укрывается от иммунного ответа организма в нервных клетках спинного мозга. Из 100% всех людей с генитальным герпесом рецидивирующей формой страдает около 80%. У оставшихся 20%, инфицированных вирусом простого герпеса 2 типа, заболевание протекает бессимптомно, и люди даже не подозревают, что являются носителями вируса.
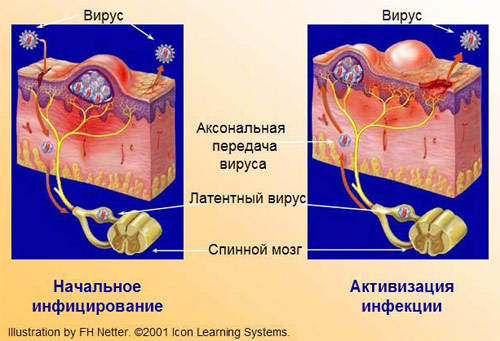
Механизм развития генитального герпеса (герпесвирусной инфекции)
Обострение обычно возникает на фоне снижения иммунной защиты, которое происходит из-за множества факторов:
- простуда
- стресс
- нервное переутомление
- хирургические вмешательства
- резкая смена климата
- длительное пребывание на солнце
- цикличные колебания гормонального фона (менструальный цикл)
На этом фоне вирус начинает размножаться и из нервных клеток спинного мозга, своего места обитания, по нервным волокнам перемещаться к коже и слизистым, где вызывает типичные проявление герпеса. (см. описание выше).
Генитальный герпес – фактор риска для женщин, которые хотят иметь детей. Если на этапе планирования беременности женщина с генитальным герпесом не позаботится об эффективном лечении, то это заболевание может стать проблемой на пути к материнству.
Носительство вируса герпеса является одной из причин нарушения репродуктивной функции: развитие хронического эндометрита, невынашивание беременности, внутриутробное инфицирование плода и преждевременные роды.
Если женщина впервые заразилась герпесом во время беременности, особенно в первом триместре, то герпес может передаться плоду. При внутриутробном заражении до 80 % детей погибают или становятся инвалидами, так как в первую очередь страдает нервная система. Развивается энцефалопатия, тугоухость, поражения печени и селезенки. К счастью, это встречается редко.
Диагностика генитального герпеса
Диагностика генитального герпеса довольно проста. Если человек обнаружил у себя внешние признаки генитального герпеса, ему следует обязательно как можно скорее обратится к врачу дерматовенерологу, урологу или гинекологу!
В первую очередь доктор проводит внешний осмотр высыпаний. В большинстве случаев этого достаточно для постановки диагноза, так как генитальный герпес имеет характерную клиническую картину.
Если проявления герпеса не вкладываются в классическую картину, у врача появляются сомнения, то проводят лабораторные исследования на герпес:
- ПЦР-тестирование на ДНК вируса герпеса 1 и 2 типов. (HHV-1,2, ПЦР) Тест показывает наличие вируса герпеса в организме, а также определяет его количество.
- Тест на антитела к вирусу простого герпеса. Положительный результат анализа на антитела М (IgM) говорит о том, что вероятнее всего человек впервые заразился герпесом. Наличие антител G (IgG) (anti – HSV (1 и 2 типа) IgG) показывает, что человек уже давно инфицирован, а увеличение количества антител G говорит о реактивации вируса – рецидиве.
Лечение герпеса
Если вы заметили первые проявления инфекции, необходимо начать лечение, которое должен назначать врач (гинеколог, дерматовенеролог или уролог). К сожалению, полностью избавиться от вируса герпеса невозможно. Тем не менее терапия убирает неприятные симптомы и существенно снижает риск рецидивов.
Существуют несколько подходов к лечению генитального герпеса. Пациентам, впервые заболевшим генитальным герпесом, назначают противогерпетические препараты (таблетки и мази) на 7-10 дней. После лечения вирус переходит в латентную фазу (затихает и прячется в нервной системе). Для пациента наступает стадия ремиссии.
Во время последующих рецидивов генитального герпеса, если обострения становятся более частыми (не менее 6 раз в год) и длительными, протекают с выраженными болевыми симптомами и оказывают сильное влияние на психоэмоциональное состояние, врач может назначить супрессивную терапию. В этом случае противовирусные препараты приходится принимать длительное время — в течение месяца или более длительного срока. Такая терапия обычно помогает сократить длительность рецидива и уменьшить выраженность симптомов. Однако лечение не всегда влияет на частоту и тяжесть развития рецидивов в последующем.
Применение при лечении генитального герпеса современных противовирусных препаратов с иммуномодулирующим действием показало преимущество перед монотерапией противогерпетическимим препаратами.
Применение инновационного препарата Аллокина-альфа способствует сокращению длительности рецидива генитального герпеса и снижению его тяжести в 2 раза. Длительное наблюдение за больными показало, что частота обострений в течение года снизилась более чем в 2 раза* (при рецидивах 4-6 раз в год было отмечено снижение обострений до 2 раз в год).
При лечении Аллокином-альфа уже в течение первых 2-х часов после подкожной инъекции проходят боль, жжение и зуд. А период заживления сокращается примерно на 30%.**
Терапия Аллокином-альфа значительно улучшает качество жизни больных генитальным герпесом.
Запомните: Генитальный герпес необходимо лечить, даже если обострения редкие и не вызывают сильного дискомфорта. Потому что без лечения количество вируса в организме будет увеличиваться, что приводит к серьезным осложнениям и заболеваниям. Вирус простого герпеса, особенно вирус герпеса 2 типа, в ассоциации с вирусами папилломы человека, цитомегаловирусом, хламидиями и микоплазмами способствует развитию неопластических процессов у человека, в частности, рака шейки матки и рака предстательной железы.
*«Клиническая эффективность и механизм действия Аллокина-альфа у больных рецидивирующим генитальным герпесом»
Авторы: Ф.И.Ершов, А.А Кубанова, А.Е. Шульженко, Б.В.Пинегин, Г.П.Беккер, С.И. Черныш, Л.В.Бугаев
Новое поколение противовирусной терапии при рецидивирующем простом герпесе
Авторы: д.м.н., проф. А.Е. Шульженко, И.Н. Зуйкова
**«Аллокин-альфа в комплексной терапии рецидивирующей герпетической инфекции»
Авторы: В.А. Исаков, Е.И. Архипова, О.В. Азовцева, С.И. Черныш, Ф.Р. Кутуева, А.Е. Семенов
Структура заболеваемости ИППП в РФ за 2005–2016 гг.
| Заболевание\год | 2005 | 2006 | 2007 | 2008 | 2009 | 2010 | 2011 | 2012 | 2013 | 2014 | 2015 | 2016 | ср. темп прироста / убыли, % |
| Герпес урогенитальный | 4,3% | 4,9% | 4,8% | 5,3% | 5,5% | 5,8% | 6,1% | 6,3% | 6,6% | 7,0% | 7,5% |
7,9% |
+5,0 |
| Аногенитальные бородавки | 6,3% | 6,9% | 7,4% | 8,0% | 9,1% | 9,7% | 9,7% | 9,7% | 10,2% | 10,7% | 11,7% |
12,9% |
+5,6 |
| Сифилис | 13,6% | 13,5% | 13,8% | 13,9% | 14,0% | 13,3% | 12,5% | 12,4% | 12,4% | 12,5% | 13,0% |
13,3% |
-0,8 |
| Гонорея | 14,2% | 13,2% | 13,3% | 13,1% | 12,6% | 12,6% | 12,7% | 13,6% | 12,8% | 11,7% | 10,2% |
9,0% |
-2,6 |
| Трихомоноз | 42,6% | 41,3% | 40,7% | 38,9% | 37,9% | 37,5% | 37,1% | 35,1% | 35,2% | 35,0% | 34,8% |
34,7% |
-2,0 |
| Хламидиоз | 19,0% | 20,1% | 19,9% | 20,8% | 21,0% | 21,0% | 21,9% | 22,9% | 22,8% | 23,0% | 22,8% |
22,1% |
+1,6 |
Смотрите также:
Спросите у своего гинеколога, есть ли у него (неё) опыт лечения папилломавирусной инфекции до полного удаления вируса папилломы человека из организма?
Аллокин-Альфа: инструкция по применению
Асанова Наталья Геннадьевна
11 августа 2023

ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ. ВОЗМОЖНЫ ПОБОЧНЫЕ ЭФФЕКТЫ. НЕОБХОДИМА КОНСУЛЬТАЦИЯ СПЕЦИАЛИСТА.
Автор статьи
Асанова Наталья Геннадьевна
,
Профессия: провизор
Название вуза: Иркутский государственный медицинский университет
Специальность: фармация
Стаж работы: 30 лет
Диплом о фармацевтическом образовании: 587802
Места работы: контрольно-аналитическая лаборатория, фарминспектор аптек и ЛПУ, компания «ПРОТЕК», провизор сервиса Мегаптека
Все авторы
Содержание
- Аллокин-альфа: РЛС
- Аллокин-альфа: состав
- Аллокин-альфа: как разводить?
- Аллокин-альфа: противопоказания
- Аллокин-альфа: побочные эффекты
- Аллокин-альфа: как хранить?
- Краткое содержание
По оценке ВОЗ (Всемирной организации здравоохранения) 67% людей до 50 лет инфицированы вирусом простого герпеса первого типа (ВПГ-1), вызывающим лабиальный герпес. Носителей вирусов ВПГ-2 — причины генитального герпеса — 13% населения планеты.
Наряду с противовирусными препаратами прямого действия для терапии герпесвирусных заболеваний часто применяют иммуномодуляторы. Например, препарат Аллокин-альфа, о котором рассказываем в этой статье. Узнаем, что является действующим веществом лекарства, как его применять и хранить, какие есть побочные эффекты и противопоказания.
Аллокин-альфа: РЛС
Согласно Регистру лекарственных средств РФ, Аллокин-альфа представляет собой препарат в виде лиофилизата для приготовления раствора для подкожного введения. Легкая пористая масса в количестве 1 мг помещена в стерильные флаконы. Относится к группе противовирусных и иммуномодулирующих средств. Из аптек отпускается по рецепту врача.
Аллокин-альфа: состав
Действующим веществом препарата является олигопептид с длинным МНН: гистидил-глицил-валил-серил-глицил-гистидил-глицил-глутаминил-гистидил-глицил-валил-гистидил-глицин. Он обладает действием, подобным действию интерферона-альфа: стимулирует синтез собственных интерферонов в организме и активирует клетки-естественные киллеры — лимфоциты.
В экспериментах была доказана эффективность Аллокин-альфа против вирусов гриппа А и В, простого герпеса 1 и 2 типа, гепатита В и С, вируса папилломы человека. При каких показаниях согласно инструкции назначают Аллокин-альфа инъекции:
- хроническая инфекция, вызванная онкогенными вирусами папилломы человека (препарат входит в Клинические рекомендации Минздрава для лечения ВПЧ);
- хронический рецидивирующий лабиальный и генитальный герпес, вызванный ВПГ-1 и ВПГ-2;
- среднетяжелая форма острого гепатита В (комплексное лечение).
Аллокин-альфа: как разводить?
При приобретении Аллокин-альфа в аптеке пациенты задают вопросы: «Чем развести порошок, как колоть и кто может сделать уколы?». Отвечаем по порядку:
- Лиофилизат разводят стерильным 0,9% раствором хлорида натрия (физиологическим раствором). Во флакон с 1 мг порошка добавляют 1 мл растворителя.
- Аллокин-альфа вводится подкожно. При внутримышечном введении он слишком быстро выводится, его действие не будет достаточно эффективным в борьбе с вирусом.
- Введение препарата лучше доверить профессионалам и обратиться в процедурный кабинет. Медсестры проведут процедуру правильно и проконтролируют ваше состояние после инъекции.
Аллокин-альфа: противопоказания
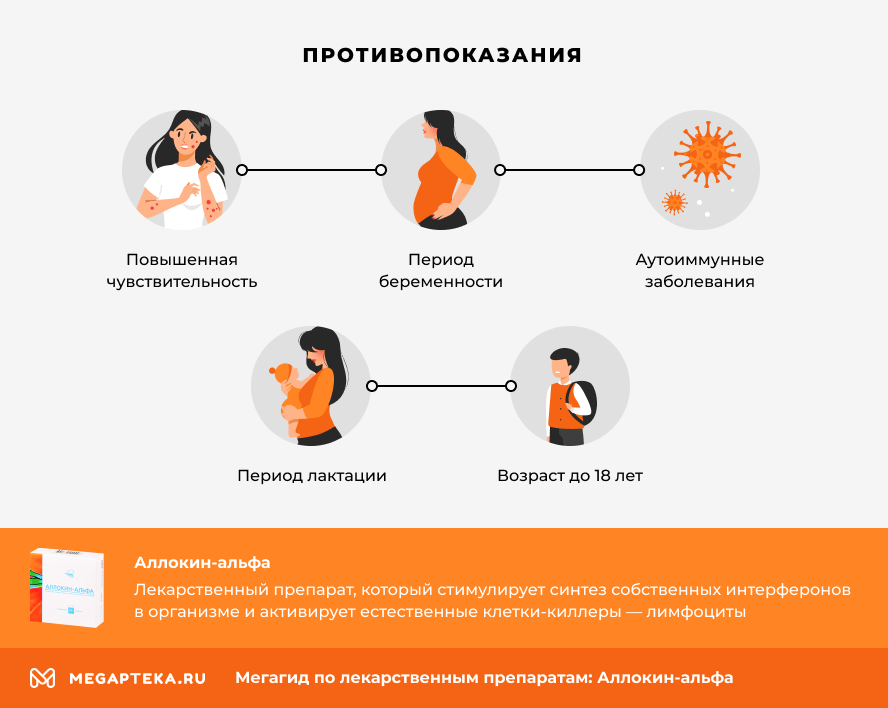
Аллокин-альфа, несмотря на высокий профиль безопасности, нельзя применять, если у пациента:
- повышенная чувствительность к препарату;
- период беременности;
- период лактации (на время лечения грудное вскармливание отменяют);
- аутоиммунные заболевания;
- возраст до 18 лет.
Аллокин-альфа: побочные эффекты
Препарат не оказывает токсического, аллергенного, мутагенного, канцерогенного и эмбриотоксического действия, а также не влияет на детородную функцию. В отдельных случаях пациент может испытывать слабость, головокружение, при герпесе возможно появление новых высыпаний.
Аллокин-альфа: как хранить?
У препарата Аллокин-альфа хранение в домашних условиях должно быть организовано в холодильнике при температуре от 2 до 8 °С. Флаконы следует держать в заводской упаковке. Приготовленный раствор используют немедленно.
Краткое содержание
- Согласно Регистру лекарственных средств РФ, Аллокин-альфа представляет собой препарат в виде лиофилизата для приготовления раствора для подкожного введения. Относится к группе противовирусных и иммуномодулирующих средств.
- Действующим веществом препарата является олигопептид, который обладает действием, подобным действию интерферона-альфа: стимулирует синтез собственных интерферонов в организме и активирует клетки-естественные киллеры — лимфоциты.
- Лиофилизат разводят стерильным 0,9% раствором хлорида натрия (физиологическим раствором). Во флакон с 1 мг порошка добавляют 1 мл растворителя.
- Аллокин-альфа нельзя применять, если у пациента: повышенная чувствительность к препарату; период беременности; период лактации (на время лечения грудное вскармливание отменяют); аутоиммунные заболевания; возраст до 18 лет.
- При лечении Аллокином-альфа в отдельных случаях пациент может испытывать слабость, головокружение, при герпесе возможно появление новых высыпаний.
- У препарата Аллокин-альфа хранение в домашних условиях должно быть организовано в холодильнике при температуре от 2 до 8 °С.
Задайте вопрос эксперту по теме статьи
Остались вопросы? Задайте их в комментариях ниже – наши эксперты ответят вам. Там же вы можете поделиться своим опытом с другими читателями Мегасоветов.
Гость
Анонимный пользователь
Войти
Частые рецидивы генитального герпеса
Мудрость форума:
Женское здоровье
12 ответов
Последний —
Перейти
К иммунологу нужно идти, назначать терапию иммуностимуляторами
Ацикловир заменить на валцикловир или фамцикловир. И не конские дозировки, а наоборот малодозированно но длительно принимать. Но это врач должен схему приёма расписать
Я болею ВПГ-2 -генитальным герпесом 6 лет. После заражения у меня проявились и другие типы этого вируса: ВПГ-1 , вирус Эпштейна-Барр — тип 4, цитомегаловирус — тип 5. Очень долго лечилась. Постоянно проявлялись между ягодицами по линии стрингов красные прыщи, которые исчезали на следующий день после приема ацикловира. Это случалось от холода . Невозможно было присесть зимой в транспорте на сиденье . Начиналось нытье нервов в копчике , затем высыпание поверхностных язв. Этот процесс не совсем был похож на реактивацию генитального герпеса, когда он начинает активизироваться в половом нерве. Я точно знаю место входа вируса в мой организм и его локализацию на коже интимной зоны . У герпесвирусных больных очень активны бактериальные инфекции. Решила пролечиться в этом направлении. Купить мазь Пантенол (декспантенол 5 % репарация тканей , стимулятор) , потому что кожа под копчиком была травмирована ( стерта) от физических упражнений на пресс и Синтомицин (хлорамфеникол 10 %) антибактериальное средство. После применения мазей прекратились высыпания. Ощущения покалывания может быть от того, что вирусом поражены нервы. К , сожалению , многие женщин в дальнейшем страдают от хронических тазовых болей ( жжение слизистой, покалывание , блуждающие боли, возбуждение нервов в половой зоне и т. д. )
И еще цистит при хороших анализах . Начинает ползти герпес по паховому нерву , учащаются позывы в туалет и ноет мочевой пузырь.
#5
тоже самое . ничего не помогает. все испробовал. потратил 500,000 руб, только супрессивная валациловир на постяонной остнвое
Я почти все препараты из Вашего списка пробовала, схемы были схожие. Честно говоря, мне только аллокин альфа помогает. Мази свечи, другие уколы имеют крайне слабый эффект. Увы. Кроме аллокина сильнее средства не пробовала.
#7
Странно, я лично колю аллокин уже года 4 и горя не знаю. Ремиссии по году с лишним и с каждым разом, как будто, дольше. Я бы могла рекомендовать аллокин при герпесе смело.
#8
При беременности были частые рецидивы, раз в месяц точно( отошли воды внезапно на 7 месяце. Были высыпания на тот момент, из-за этого сделали кесарево. Самой рожать если есть высыпания нельзя. Малыш родился здоровым. Удачи вам и здоровья)
#9
Я живу в Германии, сдесь врачи от гг приписывают только мази, других лекарств они даже не знают! При рецидиве только кесарево( естественным путем рожать нельзя, чтобы не заразить малыша. Ну а пока малыш в животике, он защищён. Не переживайте, беременейте. Никаких таблеток принимать не нужно во время беременности точно) на фоне стресса могут быть частые рецидивы, поменьше думайте о герпесе.
#10
Сразу при любых намеках на герпес колю аллокин альфа. Помогает всегда безотказно. Доверяю только ему. Многим помогает, многие хвалят.
Я бы на Вашем месте попробовала аллокин альфа. Я его колю периодически, своей коллеге рекомендовала, ей тоже подошло. Да и отзывы хорошие, попробуйте его.
Внимание
Администрация сайта Woman.ru не дает оценку рекомендациям и отзывам о лечении, препаратах и специалистах, о которых идет речь в этой ветке. Помните, что дискуссия ведется не только врачами, но и обычными читателями, поэтому некоторые советы могут быть не безопасны для вашего здоровья. Перед любым лечением или приемом лекарственных средств рекомендуем обратиться к специалистам!
Ну вообще аллокин альфа лечит герпес. Я только его и использую, хотя раньше использовала учу разных других средств, не помогали.
На информационном ресурсе применяются cookie-файлы. Оставаясь на сайте, вы подтверждаете свое согласие на их использование.
